Воздействие LGG на иммунную систему
СтатьиПредыдущая глава | Оглавление | Следующая глава
2. Воздействие LGG® на иммунную систему
Инфекционные заболевания, включая заболевания, которые поражают полость рта, дыхательные пути и желудочно-кишечный тракт, являются значительной проблемой даже среди относительно здорового, по иным показателям, населения.
Они создают большую нагрузку на пациентов и на их семьи и ложатся огромным экономическим грузом на общество: консультации врачей, прямые затраты на оплату лечения и косвенные убытки из-за пропущенных рабочих дней.
По разным оценкам, среди населения, относительно здорового по другим показателям, дети страдают от респираторных инфекций от 5 до 10 раз в год, в то время как взрослые, в среднем, от 1 до 5 раз соответственно. У детей острые респираторные заболевания и наиболее часто встречающееся осложнение - воспаление среднего уха (отит), диагностируются в 80% случаев всех инфекционных заболеваний. На втором месте по частоте диагнозов находится вирусный гастроэнтерит. Известно также, что большим фактором риска для детей является посещение общественных мест (детские сады, школы и т. д.). Среди пожилого населения на респираторные инфекции приходится приблизительно половина инфекционных заболеваний, тогда как на гастроэнтерит -одна треть соответственно. Поверхности слизистой оболочки эпителия покрывают значительную часть желудочно-кишечного тракта и дыхательных путей, служа при этом воротами для инфекционных агентов. В желудочно-кишечном тракте организм защищен от вредных микробов физическим и химическими барьерами, создаваемыми кишечным эпителием. Кишечный эпителий здорового человека с нормальной микрофлорой создает барьер против патогенов, известный как защита от колонизации. Нормальная микрофлора усиливает сопротивляемость организма в целом, конкурируя за питательные вещества и места прикрепления на поверхности слизистой оболочки, а также выделяя продукты метаболизма. Прикрепление бактерий к поверхности слизистой оболочки является главным пусковым механизмом в развитии заболевания, а снижая вероятность этого события, таким образом, можно снизить риск заражения организма. Симбиотические бактерии, как правило, происходят от видов, принадлежащих нормальной микрофлоре кишечника. Они адаптируются, таким образом, будучи частью нормальной микрофлоры. Прикрепление пробиотических бактерий к поверхности слизистой является одним из важнейших свойств, помогающих предотвратить прикрепление патогенов. Кроме того, также задействуются механизмы усиления иммунной реакции, укрепления барьера слизистой оболочки и подавления кишечного воспаления.
Специальная Комиссия Международного Биологического Института в Европе по Питанию и Иммунитету Человека (The ILSI Europe Nutrition and Immunity Task Force) опубликовала свои работы по показателям, идентифицирующим иммуномодулирующий эффект принимаемых внутрь продуктов/препаратов. (Albers et al., 2005).
L. rhamnosus GG- самый изученный в мире штамм пробиотических бактерий.
Отчет описывает несколько показателей и методов для измерения иммунной реакции. Кроме того, в работе отмечается, что у здорового взрослого человека отклонения одних отдельно взятых показателей могут не иметь медицинского значения. Отчет также вводит градацию показателей иммунной функции по их применимости.
Наиболее подходящими показателями были признаны:
1) выделение вакциноспецифических антител;
2) аллергическая реакция отложенного типа после местного применения антигена для измерения общей иммунной функции организма.
В случае идентификации иммунных функций слизистой оболочки, в особенности при описании кишечной (кишечно-ассоциированной) иммунной функции, наиболее высокие оценки были отданы вакциноспецифическому секреторному иммуноглобулину А — IgA и неспецифическому IgA слюны и стула (кала). В заключении отчета отмечается, что истинным тестом эффективности пищевого продукта или пищевого элемента, которому приписывается улучшение иммунной функции, является изменение частоты эпизодов заболеваний, а также тяжести и длительности симптомов инфекции, так как это является конечным результатом, имеющим наибольшую медицинскую значимость.
Когда показатель не поддается подтверждению, отслеживание изменений в одном или нескольких аспектах иммунной функции может предоставить информацию о наиболее вероятном механизме воздействия пищевого продукта. Lactobacillus rhamnosus GG (АТСС 5353103, LGG®) является самым изученным пробиотиком в мире. Широкие исследования в различных областях применения проводились как среди добровольцев, так и с использованием лабораторных животных.
L. rhamnosus GG был впервые выделен в организме человека в 1983 г. и применяется в продуктах питания с 1990 г.
Штамм имеет наибольшее количество характеристик и свойств, рекомендованных для оптимального пробиотика, включая прекрасную выживаемость и транзиторную колонизацию в желудочно-кишечном тракте, которая основана на способности прикрепляться к кишечному слою слизистой оболочки и эпителиальным клеткам. Успешное выделение штамма LGG® в образцах стула позволило провести исследования зависимости реакции от дозы препарата и, таким образом, найти оптимальную дозировку для использования. Кроме того, в результате проведенных исследований было обнаружено, что L.rhamnosus GG оказывает очень много других положительных эффектов на здоровье человека.
2.1. LGG® поддерживает иммунитет. LGG®снижает заболеваемость кишечными инфекциями
Наибольшее количество исследований пробиотиков посвящено проблематике предотвращения желудочно-кишечных инфекционных заболеваний, таких как диарея.
Большинство исследований проводились с участием детей и результаты показали статистически значимый положительный эффект, выраженный в снижении длительности течения диареи при использовании таких штаммов, как L. rhamnosus GG.
В исследовании, проводившемся в Польше с участием детей, находившихся в стационаре не по причине желудочно-кишечных инфекций, рандомизированные группы пациентов получали L. rhamnosus GG (109 КОЕ, два раза в день) и плацебо на протяжении своего пребывания в госпитале (Szajewska et al., 2001). Медсестры записывали частоту случаев диареи, а также тип стула. Во время периода диареи стул анализировался на наличие антигенов ротавируса. Прием L. rhamnosus GG снизил частоту эпизодов острой диареи (33.3% против 6.7%, плацебо и L. rhamnosus GG соответственно, р=0.0002). Несмотря на то, что статистически достоверной разницы выявления ротавируса в обеих группах не было (27,8% против 20%, плацебо и L. rhamnosus GG соответственно), среди детей из группы, принимавшей L. rhamnosus GG, случаи гастроэнтерита, вызванные ротавирусом, встречались гораздо реже (16,7 % в группе плацебо по сравнению с 2,2% в группе L. rhamnosus GG, р=0.02) (рисунок 2).
Рисунок 2. Эффективность L rhamnosus GG (109 КОЕ/день) в предотвращении нозокомиальной диареи среди новорожденных (Szajewska et аl., 2001). 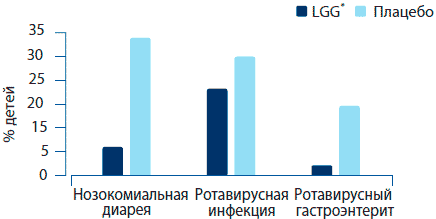
Другое исследование проводилось в Перу, также с участием детей (Oberhelman et al.,1999). В данном случае L. rhamnosus GG (3.7х1010 КОЕ в день) и плацебо назначались в капсулах. Препараты доставлялись на дом испытуемым детям шесть дней в неделю. Заболеваемость острой диареей в группе L. rhamnosus GG была ниже, чем в группе, принимавшей плацебо (5.21 против 6.2 эпизодов/ ребенка/год, р=0.028). Более того, в группе L. rhamnosus GG эпизодов аденовирусной инфекции было меньше в сравнении с группой, принимавшей плацебо (8 против 19, р=0.03). Продолжительность приема препарата равнялась 15 месяцам, что также указывает: длительное употребление L. rhamnosus GG не уменьшает положительный эффект.
В исследовании, проводившемся в Индии, дети, страдающие диареей, были рандомизированы в две группы, которые получали либо раствор для регидратации (oral rehydration solution, ORS) (ORS, n-185), либо ORS с добавлением L. rhamnosus GG в форме порошка, содержащего 1010 КОЕ (п=188), либо 0RS с добавлением L. rhamnosus GG в форме порошка, содержащего 1012 КОЕ (п=186) два раза в день, с минимальным курсом приема от 7 дней или до момента остановки диареи вместе с восполнением недостатка воды (Basu et al., 2009). Обе дозировки L. rhamnosus GG показали одинаковую эффективность в снижении частоты и длительности диареи, а также уменьшение срока пребывания в стационаре пациентов с острой диареей.
В аналогичном исследовании, также проводившемся в Индии, были задействованы 684 ребенка с диагнозом «острая диарея», где пациенты получали L. rhamnosus GG в в меньшей дозе, 107 КОЕ, которая не оказала никакого влияния на длительность пребывания в стационаре и частоту эпизодов диареи (Basu et al., 2007) (рисунок 3). В случаях же устойчивых эпизодов диареи у 235 детей L. rhamnosus GG (107 КОЕ) смог существенно снизить частоту стула и длительность течения заболевания (Basu et al., 2007).
Рисунок 3. Воздействие L. rhamnosus GG на длительность острой диареи и время нахождения в стационаре среди детей (Basu et al. 2007 and 2009).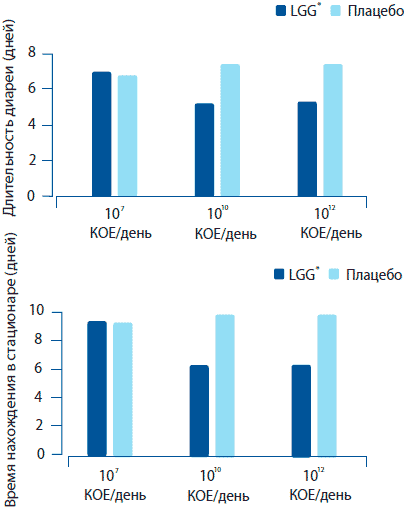
Дети в возрасте от 3 до 36 месяцев (п=571), посещавшие семейного педиатра в связи с острой диареей, были разделены на две группы случайным образом. Одна из них получала раствор для регидратации (контрольная группа), другая — аналогичный раствор, но с добавлением L. rhamnosus GG (109 КОЕ); Saccharomyces boulardii (109 КОЕ); Bacillus clausei (109 КОЕ), смесь L. delbrueckii var bulgaricus (109 КОЕ), Streptococcus thermophilus (109 КОЕ), L. acidophilus (109 КОЕ) и Bifidobacterium bifidum (108 КОЕ); или Enterococcus faecium SF68 (107 КОЕ) (Canani et al., 2007). Средняя продолжительность заболевания была существенно меньше (р<0.001) среди детей, получавших L. rhamnosus GG (78.5 часов) и смесь из четырех бактериальных культур (70.0 часов), чем у детей из контрольной группы, получавших только раствор для регидратации (115.0 часов). Через один день после первого приема пробиотиков частота стула существенно снизилась (р<0.001) среди детей, принимавших L. rhamnosus GG, и тех, кто принимал смесь пробиотических культур, в сравнении с другими группами. Остальные препараты не повлияли на первичные результаты.
Исследование, проводившееся в Италии (Guarino et al.,1997), а также европейское мультицентровое исследование (european multicenter study) (Guandailini et al.,2000) продемонстрировали значительное положительное влияние L. rhamnosus GG как в лечении ротавирусной инфекции, так и в случаях, когда причина диареи была неизвестна.
Прием L. rhamnosus GG способен существенно снизить длительность острой диареи.
Аналогичное исследование, проведенное в Петровской больнице (Россия), также показало существенную разницу в пользу L. rhamnosus GG, несмотря на то, что только у 27% пациентов причиной диареи был ротавирус. У примерно пятой части диарея была вызвана известной бактерией, и в половине случаев этиология была неизвестна (Шорникова и др., 1997). Таким образом можно заключить, что L. rhamnosus GG эффективен не только при лечении ротавирусной диареи, но также и в случаях, когда этиология остается неизвестной.
Результаты исследований по снижению риска острой диареи также коррелируют с результатами культурно-специфичного мета-анализа снижения длительности острой диареи среди детей при использовании L. rhamnosus GG (Szajewska et al., 2007). Было проведено восемь смешанных контрольных исследований (RCT, randomized controlled studies) с участием 988 человек, преимущественно детей, помещенных в дневной стационар в связи с обезвоживанием. Прием L. rhamnosus GG существенно снизил длительность острой диареи в сравнении с плацебо (семь RCT, 876 детей, разница в среднем взвешенном -1.1 дней (95% доверительный интервал, ДИ -1.9 до -0.3), особенно в случаях, когда диарея была вызвана ротавирусом (разница в среднем взвешенном -2.1 дней, 95% ДИ -3.6 до -0.6), риск диареи >7 дней (одно RTC, п=287, относительный риск 0.25, 95% ДИ 0.09-0.75). Исследования с использованием ферментированных молочных продуктов с добавлением L. rhamnosus GG были исключены из публикации. Авторы, тем не менее, отметили, что исследования на ферментированных молочных продуктах подтверждают данные мета-анализа.
Также существует два исследования, оценивающих влияние приема L. rhamnosus GG на заболеваемость острой диареей среди взрослых путешественников. В первом исследовании перед поездкой в регионы с высоким риском заболеваемости острой диареей 820 туристам выдавались L. rhamnosus GG (2х109 КОЕ/день) или плацебо (Oksanen et al., 1990). В месте назначения присутствовал доктор, также участвовавший в проведении исследования, а данные собирались в виде опросника и отсылались обратно по возвращении. Прием пробиотика показал снижение эпизодов острой диареи только в одном из двух мест назначения (24% против 40%, р=0.04 для недельной поездки), что отличается от суммарных результатов всех участников (41% против 46%, не уточнено). В месте назначения, где наблюдались несущественные результаты, распределение групп по возрасту было неравномерно: возраст в группе, принимавшей плацебо, был выше, что потенциально могло повлиять на результаты.
В другом исследовании заболеваемости диареей среди туристов риск заболеваемости отличался в зависимости от места назначения путешествия (Hilton et al., 1997). Смешанные группы взрослых (п=245) получали либо L. rhamnosus GG (2х109 КОЕ/день), либо плацебо. Заболеваемость острой диареей в группе, принимавшей L. rhamnosus GG, была ниже, чем в группе, принимавшей плацебо (3.9% против 7.4%, р=0.05).
В заключение
Результаты многочисленных исследований доказывают, что L. rhamnosus GG снижает риск заболевания острой диареей среди детей. Исследования также показывают, что прием L. rhamnosus GG способен снизить длительность течения острой диареи.
2.2. LGG® снижает заболеваемость респираторными инфекциями
Продолжающиеся исследования показывают, что пробиотические культуры могут помочь в защите от респираторных инфекций и простуды. Влияние L. rhamnosus GG на снижение заболеваемости респираторными инфекциями изучалось в трех исследованиях с участием детей и одним - с участием взрослых спортсменов, готовившихся к марафону. Кроме того, было проведено пять клинических испытаний, исследующих влияние L. rhamnosus GG, принимаемого в комплексе с другими пробиотиками. Первое исследование было проведено с участием здоровых детей, посещающих дошкольные образовательные учреждения (Hatakka et al., 2001). Всего в исследованиях принимали участие 513 детей из 18 учреждений г. Хельсинки, Финляндия, где они были разделены случайным образом на две группы, одна из которых получала L. rhamnosus GG, а другая - плацебо. Одна группа употребляла молоко, обогащенное L. rhamnosus GG (108 КОЕ/день), или обычное молоко в дневном рационе питания, пять дней в неделю в течение семи месяцев. Случайное разделение было проведено отдельно для детей младше 3 лет и детей от 3 лет и старше. Статистически значимой разницы в возрасте среди детей в группах выявлено не было, но при проведении сравнения внутри возрастных групп (со ступенью в один год) в группе, принимавшей L. rhamnosus GG, оказалось больше детей старшего возраста. Таким образом, результаты были проанализированы с коррекцией по возрасту. Несмотря на то, что число дней отсутствия по болезни, сообщенное родителями, не было статистически достоверно ниже в группе L. rhamnosus GG, частота отсутствия в связи с прочими заболеваниями в этой группе была ниже (4.9 против 5.8 дней/ребенок, р=0.03; корректировка по возрасту р=0.09) (рисунок 4).
Рисунок 4 . Воздействие молока с добавлением L. rhamnosus GG на инфекции, острое воспаление среднего уха, а также лечение антибио -тиками среди детей, находящихся в дошкольных учреждениях (Hatakka et al., 2001).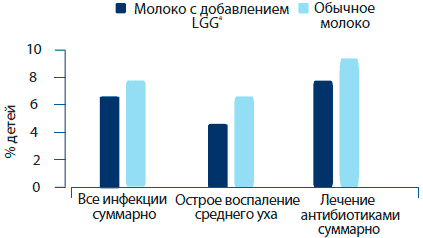
У детей, которые получали молочные продукты с L. rhamnosus GG, инфекционные заболевания встречались реже.
Кроме того, дети в группе L. rhamnosus GG не были подвержены симптомам респираторных заболеваний дольше на одну неделю от начала исследований (4 нед. против 5 нед., р=0.03). Несмотря на то, что разницы между симптомами респираторных заболеваний, сообщенными родителями, не было, в группе L. rhamnosus GG, согласно диагнозам терапевтов, наблюдалось меньше эпизодов осложнений (например, воспаления среднего уха) (относительная разница между группами — 17%), и для лечения инфекций дыхательных путей антибиотики применялись реже (относительное снижение —19%).
В другом двойном-слепом, рандомизированном, плацебо-кон-тролируемом исследовании в дошкольном учреждении в Хорватии среди детей, принимавших 100 мл ферментированного молочного продукта с добавлением L. rhamnosus GG (109 КОЕ) (п=139), инфекционные заболевания респираторного тракта встречались реже, чем в группе, принимавшей плацебо (п=142) (43% против 67.6%, р<0.001) (рисунок 5) (Hojsak 2009а). У детей из группы, принимавшей плацебо, чаще наблюдались эпизоды желудочно-кишечной инфекции, однако разница не была статистически значима (22.5% против 14.4%, р=0.079). Разница также не была выявлена и в отсутствии детей в учреждении по случаю болезни (р=0.069).
Рисунок 5. Воздействие молока с добавлением L. rhamnosus GG на инфекции среди детей, находящихся в дошкольных учреждениях (Hojsak et al., 2009а).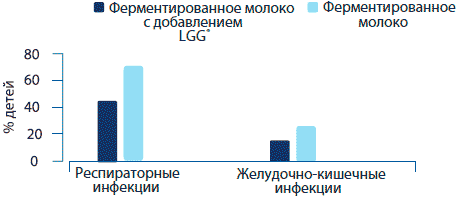
В детской больнице было проведено исследование воздействия L. rhamnosus GG на предотвращение нозокомиальной инфекции (Hojsak, 2009b). В рандомизированном, двойном-слепом, плацебо-котролиру-емом исследовании 742 ребенка были случайным образом разделены на две группы, одна из которых получала 100 мл ферментированного молока, содержащего L. rhamnosus GG (109 КОЕ), а другая тот же продукт, но без добавления бактерии. В группе L. rhamnosus GG наблюдалось существенное снижение риска заболевания желудочно-кишечными инфекциями (относительный риск [0Р] 0.4,95%, доверительный интервал [ДИ] 0.25-0.7, число больных, требующих лечения (number needed to treat (NNT)) 15,95% ДИ 9-34) и больных респираторными инфекциями (0Р 0.38695% ДИ 0.18-0.85, NNT 30,95% ДИ 16-159) по сравнению с группой, принимавшей плацебо (рисунок 6).
Рисунок 6. Воздействие молока с добавлением L. rhamnosus GG на инфекции среди детей, находящихся в стационаре (Hojsak et al., 2009b).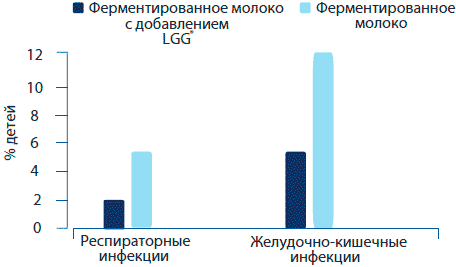
В еще одном исследовании, проведенном среди здоровых взрослых (п=119), тренировавшихся на летний марафонский забег (Кеккоnеn et al., 2007), участники были разделены на две группы, одна из которых получала молочный напиток, обогащенный L. rhamnosus GG (4х1010 КОЕ/ день), а другая получала тот же напиток, однако без добавления пробиотика. Обе группы получали препараты в период тренировки (3 месяца) и в течение 4 недель после забега. В группе L. rhamnosus GG в двухнедельный период после забега длительность расстройств желудочно-кишечного тракта была меньше (1 против 2.3 дней, р=0.046). Влияние на заболеваемость респираторными инфекциями комбинаций пробиотиков, содержащих L. rhamnosus GG, изучалась в нескольких исследованиях. В рандомизированном, двойном-слепом, плацебо-контроли-руемом исследовании с применением плацебо изучалась способность пробиотиков снизить риск заболевания среди детей грудного возраста (Rautava et al., 2009). Исследование проводилось среди детей в возрасте до двух месяцев, посещавших детские консультации и питающихся молочной смесью. До достижения возраста 12 месяцев исследуемые ежедневно получали молочную смесь с добавлением пробиотических культур L. rhamnosus GG и Bifidobacterium lactis Bb-12 (n=32) или плацебо (n=40). В течение первых семи месяцев жизни у 22% детей, принимавших пробиотики, и у 50% детей, принимавших плацебо, наблюдались эпизоды острого воспаления среднего уха (соотношение риска (СР) 0.44 (95% ДИ 0.21, 0.90); р=0.014), после чего 31% детей, принимавших пробиотики, и 60% детей, принимавших плацебо, были прописаны антибиотики (СР 0.52 (95% ДИ 0.29,0.92); р=0.015). В течение первого года жизни у 28% детей, принимавших пробиотики, и у 55% детей, принимавших плацебо, наблюдались хронические заболевания дыхательных путей (СР 0.51 (95% ДИ 0.27,0.95); р=0.022).
Детям младше трех лет, посещающим дошкольные образовательные центры, давали молочный продукт, содержащий L. rhamnosus GG, Bifidobacterium lactis ssp animalis ВЬ 12 и Lactobacillus acidophilus La-5 или плацебо в течение семи месяцев (Smerud, 2008). Эпизоды желудочно-кишечных инфекций в группе, принимавшей комбинации пробиотиков, наблюдались реже, чем в группе, принимавшей плацебо (1.7 против 3.0 дней с симптомами, p=0.02) (Smerud, 2008).
Также исследовалось влияние комбинации пробиотиков, содержащей L. rhamnosus GG, Lactobacillus rhamnosus LC705, Bifidobacterium breve 99 и Propionibacterium shermanii ssp. Freudenreichii JS на детей, склонных к заболеванию отитом, детей грудного возраста, склонных к аллергии, а также пожилых людей, находящихся в специализированных учреждениях по уходу. Среди детей, склонных к заболеванию отитом (п=309), данная комбинация не смогла предотвратить как воспаление среднего уха, так и инфицирование носоглотки, однако наблюдалась тенденция снижения частоты хронических респираторных заболеваний (Hatakka et al, 2007b). Среди грудных детей (п=925), склонных к аллергии, в течение двухгодичного периода исследований было выяснено, что прием данной комбинации пробиотиков с добавлением 0.8 г фруктоолигосаха-ридов снижает частоту заболеваемости респираторными инфекциями в сравнении с группой, принимающей плацебо (среднее геометрическое: 3.7 против 4.2 эпизодов инфекции) (Kukkonen et al., 2008). Кроме того, в течение 6-месячного периода исследования антибиотики прописывались реже в симбиотической группе в сравнении с группой плацебо (23% против 28%).
Суммируя приведенную выше информацию
Среди детей, принимавших L. rhamnosus GG, показал эффективность в снижении частоты заболеваемости респираторными инфекциями, однако среди взрослых исследования предоставляют недостаточные данные, чтобы дать однозначное заключение. У детей L. rhamnosus GG эффективен в снижении частоты заболеваемости респираторными инфекциями, достоверно снижает % осложнений респираторных инфекций, таких как отит и др., а также значительно уменьшает % случаев заболеваний, при которых необходимо назначение антибиотиков.
2.3. LGG® повышает выработку антител при заболевании вирусной инфекцией
Положительное влияние L. rhamnosus GG на выработку антител при попадании обычной инфекции исследовалось на примере вызванной ротавирусом диареи (Kaila et al., 1995;Kaila et al., 1992: Majamaa et al., 1995). Данные исследования проводились среди детей, помещенных в стационар в связи с острой диареей или обезвоживанием. На время пребывания они были разделены на две группы, одна из которых получала L. rhamnosus GG, а другая плацебо. Препараты давались после регидратации в виде ферментированного молочного напитка с добавлением L. rhamnosus GG или без него (Kaila et al., 1992), а также в виде лиофилизи-рованного порошка (Kaila et al.,1995; Majamaa et al., 1995). Анализы крови брались в начале исследования, спустя восемь дней после этого, а также спустя 3-4 недели после госпитализации. Длительность диареи во время пребывания в госпитале была существенно меньше в группе, принимавшей L. rhamnosus GG, а также наблюдался существенный рост общего числа иммуноглобулино-секретирующих клеток в острой фазе инфекции во всех классах lg, причем аналогичный результат показали все исследования. В анализах крови детей из группы, принимавшей L. rhamnosus GG, было выявлено существенно более высокое содержание В-лимфоцитов, вырабатывающих lgA-антитела против ротавируса, чем в анализах группы, принимавшей плацебо. Увеличение антиген-специфичных клеток, вырабатывающих IgA, было выявлено спустя три недели после инфицирования, чего, однако, не наблюдалось во время острой фазы, что указывает на необходимость присутствия определенного периода времени, требуемого для созревания лимфоцитов. В двух исследованиях также было выявлено увеличение ротавирус-специфичного IgA ответа и в сыворотках (Kaila et al., 1995; Majamaa et al., 1995). Результаты указывают на то, что антиген-специфичный ответ «слишком медленен», чтобы быть в состоянии помочь в случае острой диареи, вызванной ротавирусом, однако неспецифический иммуноглобулиновый ответ может быть важным механизмом, участвующим в снижении риска симптомов заболевания. Данное утверждение было показано в исследовании 2001 года Szajewska et al. В данном исследовании среди детей из группы L. rhamnosus GG и детей, принимавших плацебо, наблюдалось одинаковое количество эпизодов ротавирусной инфекции, однако случаи гастроэнтерита, вызванного ротавирусом, встречались значительно реже в группе L. rhamnosus GG (16.7% против 2.2%, р=0.02). Кроме того, улучшенный антиген-специфичный ответ способен увеличить защиту от повторного заболевания. Существуют указания на то, что L. rhamnosus GG способен увеличить выработку вакцино-специфичных антител после вакцинации. Первое исследование проводилось с участием детей грудного возраста, которым давали L. rhamnosus GG или плацебо в форме порошка в течение пяти дней вместе с пероральной ротавирусной вакциной (Isolauri et al.,1995). В группе L. rhamnosus GG существенно более часто наблюдался рост ротавирус-специфичных клеток, вырабатывающих антитела класса IgM в сравнении с плацебо (79% против 29%, р=0.02), и более высокий уровень вакцино-специфичных клеток, вырабатывающих IgM в группе L. rhamnosus GG в сравнении с плацебо (р=0.02). Сероконверсия в IgA классе встречалась чаще в группе L. rhamnosus GG, чем в группе плацебо (р=0.05), а также была выявлена тенденция к повышению уровня IgA и IgG антител в сыворотках среди участников, которым также давали L. rhamnosus GG при вакцинации (р=0.10).
Увеличение выработки антител в ответ на введение пероральной вакцины было также выявлено и среди взрослых, которым давали либо обычное молоко, либо молоко с добавлением L. rhamnosus GG до и во время полиовирусной вакцинации (de Vrese et al., 2005). L.rhamnosus GG существенно повышает титры антител, нейтрализующих полиовирус (серотип полиомиелита-1 р=0.048, серотип-2 р=0.014, серотип-3 р=н.у.), а также формирование полиовирусно-специфичного IgA в сыворотке (серотип полиомиелита-1 р=0.36, и серотип-2 р=0.02, серотип-3, р=0.076). Кроме того, была выявлена тенденция к увеличению образования IgG в сыворотке (серотип-1 р=0.083, серотип-2 р=0.291, серотип-3, р=0.211). Результаты данного исследования показывают: усиливающее влияние L. rhamnosus GG не ограничивается образованием антител на инфекции, локализующиеся исключительно в желудочно-кишечном тракте, но также распространяется и на весь организм.
2.4. LGG® улучшает выработку вакциноспецифичных антител после вакцинации
Третье исследование с использованием вакцины было проведено с участием взрослых добровольцев (Не et al., 2000). Участники были разделены случайным образом на две группы, одна из которых получала плацебо, а другая L. rhamnosus GG в форме порошка в течение семи дней с целью оценить усиливающий эффект на введение вакцины Salmonella typhi. Все участники исследования нормально реагировали на вакцину, однако существенной разницы в числе IgA-, IgG- и IgM - секретирующих клеток между группами выявлено не было. Среди большого числа участников из группы L. rhamnosus GG наблюдалась тенденция к проявлению высокого количества вакцино-специфичных клеток, производящих антитела в классе IgA. Гуморальный ответ не измерялся.
В другом исследовании беременные женщины в течение четырех недель перед родами принимали смесь из L. rhamnosus GG, Lactobacillus rhamnosus LC705, Bifidobacterium breve 99, Propioni bacterium sher-manii ssp. freudenreichii JS, а также фруктоолигосахариды или плацебо (Kukkonen et al., 2006). После рождения подверженные аллергии дети получали аналогичный комплекс препаратов в течение шести месяцев. Грудным детям были сделаны прививки против дифтерии, столбняка и коклюша в возрасте 3,4 и 5 месяцев, а также коньюгат полисахарида Hib (Haemophilis influenzae type b polysaccharide conjugate). Уровень антител против дифтерии, столбняка и Hib IgG в сыворотке измерялся в возрасте 6 месяцев. В группе, принимавшей пробиотики, защитная концентрация антител к Hib (1 рг/мл) наблюдалась чаще, 16 из 32 (50%) против шести из 29 (21%) (р=0.020), и геометрическое среднее (интерквартильный размах) концентрации Hib IgG имело тенденцию к увеличению 0.75 (0.15-2.71) рг/мл в сравнении с группой плацебо, 0.40 (0.15-0.92) рг/мл (р=0.064). Исследования показали, что пробиотики не влияют на выработку антител на введение вакцин против дифтерии, столбняка и Hib и способны улучшить ответ на иммунизацию Hib.
2.5. Влияние на проницаемость слизистой оболочки желудочно-кишечного тракта
Длительный прием нестероидных противовоспалительных средств повреждает слизистую оболочку желудочно-кишечного тракта и ведет к образованию язв. Проводились различные исследования защитного влияния кисломолочных напитков на вызванные индометацином изменения проницаемости слизистой оболочки. В кисломолочные продукты были добавлены живые или дезактивированные высокой температурой культуры L. rhamnosus GG, L helveticus и L. acidophilus (>107 КОЕ/г каждой) (Gotteland et al., 2001). Среди 16 взрослых пациентов в случайном порядке было проведено четыре теста на проницаемость слизистой оболочки:
1) базовый;
2) после приема индометацина;
3) после приема индометацина и после употребления кисломолочного напитка с живыми культурами в течение пяти дней;
4) после приема индометацина и после употребления кисломолочного напитка с дезактивированными культурами в течение пяти дней.
Желудочная проницаемость определялась путем измерения сахара в моче, а кишечная — путем измерения выделения лактулозы/ маннитола. Индометацин значительно повышал как желудочную, так и кишечную проницаемость. Кисломолочный напиток с живыми культурами L. rhamnosus GG существенно снизил аномальную проницаемость слизистой желудка, однако в слизистой кишечника аналогичный эффект не наблюдался. Напиток, содержавший дезактивированные культуры, не оказал никакого влияния.
Среди малавийских детей в возрасте от 3 до 5 лет (п=164) проводились исследования показателей функционирования кишечника, а также проницаемости его слизистой оболочки (Gaalprin et al., 2005). Прием L. rhamnosus GG не показал никакого влияния на показатели функционирования или целостность, измеренную концентрацией сахара в моче, а также измерением лактулозы/маннитола (Sentongo et al., 2008). Однако исследование, проводившееся среди пациентов, страдающих болезнью Крона (п=4), в котором как участники, так и исследователи знали, какая группа принимает препарат, выявило, что ежедневное употребление L. rhamnosus GG в течение шести месяцев существенно снизило кишечную проницаемость (Gupta et al., 2000).
2.6. Модуляция прочих показателей иммунной системы
Согласно анализам биопсии слизистой оболочки двенадцатиперстной кишки взрослых пациентов, L. rhamnosus GG, как правило, влиял на гены, задействованные в иммунной реакции и процессе воспаления (TBF-p, также группа TNF, цитокины, синтаза оксида азота 1, дефенсин альфа 1), апоптоза, клеточного роста и деления (циклины, каспазы, онкогены), клеточного сообщения (белки ICAM и интегрины), клеточного соединения (кадгерины), транскрипции и преобразования сообщений, что говорит о способности регулировать иммунную реакцию слизистой оболочки кишечника (Di Caro et al., 2005). Прием L. rhamnosus GG также сопровождался системными изменениями в функционировании иммунитета. Среди взрослых субъектов наблюдалось противовоспалительное действие L. rhamnosus GG, выраженное в снижении воспалительных факторов: сенсибилизированного СРБ, воспалительных цитокинов, а также воспалительных факторов, производных от липидов, в особенности лизофосфатидилхолин и сфингомиелин (Kekkonen et al., 2008b, Kekkonen et al., 2008c). Кроме того, согласно результатам другого исследования, также среди взрослых субъектов, L. rhamnosus GG снизил выделение воспалительных цитокинов через РВМС ex vivo (Schultz et al., 2003), что также наблюдалось среди пациентов с болезнью Крона (Braat et al., 2004). При введении внутрь L. rhamnosus GG существенно улучшил выработку фагоцитарных рецепторов CR1, CR3, FcgRIII и FcgR в нейтрофильных лейкоцитах среди здоровых взрослых людей (Pelto et al., 1998).
Среди детей, склонных к аллергии, L. rhamnosus GG, вероятнее всего, по-другому влияет на иммунную реакцию. Среди них было доказано профилактическое действие L. rhamnosus GG в отношении развития атопических заболеваний, благодаря выявленному механизму возбуждения иммунного ответа типа Th1 и снижения воспалительной реакции, измеряемое сенсибилизированным СРБ в сыворотке (Marschan et al., 2008; Viljanen et al., 2005b). В дополнение к этому эффекту у детей, склонных к аллергии, L. rhamnosus GG снижает интенсивность воспалительной реакции в кишечнике и увеличивает содержание Ig A (Viljanen et al., 2005). Также отмечается, что комбинация L. rhamnosus GG и В. animalis subsp. Lactis Bb12 способна ускорить созревание иммунитета слизистой оболочки среди детей грудного возраста, питающихся молочной смесью во время добавления в диету ребенка коровьего молока, что выражается в увеличении количества IgA-секретирующих клеток, а также увеличении растворимых врожденных микробных рецепторов sCD14 (Rautava et al., 2006).
Суммируя приведенную выше информацию
L. rhamnosus GG увеличивает как выработку антител в целом, так и вакциноспецифичных после вакцинации. L. rhamnosus GG также способен нормализовать кишечную проницаемость. L. rhamnosus GG модулирует и усиливает иммунный ответ слизистой оболочки кишечника, что отражается в системных изменениях иммунной функции, таких как снижение количества медиаторов воспаления.
Предыдущая глава | Оглавление | Следующая глава
Комментарии
ПРАКТИКА ПЕДИАТРА
