akvion.ru
akvion.ru

Комплексное влияние
на основные проявления
климактерического синдрома:
• снижает частоту и выраженность приливов;
• нормализует гормональный баланс;
• улучшает психоэмоциональный фон.
Больше информации на сайте:
mense.ru
Рациональная дотация микронутриентов как способ повышения качества жизни у пациенток с климактерическим синдромом
СтатьиОпубликовано в журнале:
Медицинский совет • №13, 2017
Е.В. Ших1, д.м.н., профессор, Л.Ю. Гребенщикова2, к.м.н.
1 Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава России
2 Областной клинический перинатальный центр им. Е.М. Бакуниной, Тверь
Эффективная модификация диеты в виде применения рационально составленных биологически активных добавок (БАД) открывает перспективы улучшения качества жизни пациенток при умеренной симптоматике приливов. Дотация микронутриентов приводит к комплексному воздействию на организм женщины: стимулирует собственные резервы по поддержанию гормонального баланса и нормализации психоэмоционального состояния, что клинически выражается в снижении частоты приливов и улучшении качества жизни пациенток. Проанализирован опыт применения БАД МЕНСЕ у пациенток с вегетососудистыми нарушениями и психоэмоциональными расстройствами в период менопаузы. За период наблюдения выявлено снижение индекса Купермана в 1,7 раза в среднем по всей группе пациенток. В группе пациенток с изначально средней тяжестью течения климактерического синдрома по шкале Вихляевой отмечено снижение количества приливов более, чем в 1,5 раза; в группе пациенток с изначально легким течением климактерического синдрома – более, чем в 2 раза.
Ключевые слова: климактерический синдром, менопауза, приливы, индекс Купермана, шкала Вихляевой, МЕНСЕ.
A rational grant of micronutrients as a way to improve quality of life of climacteric syndrome patients
E. Shikh1, MD, Prof., L.Y. Grebenshhikova2, PhD in medicine
1 Sechenov First Moscow State University of the Ministry of Health of Russia
2 Bakunina Regional Clinical Perinatal Centre, Tver
Effective dietary modification in the form of use of rationally designed biologically active additives (BUD) offers prospects for improving quality of life of patients with moderate symptoms of hot flashes. The micronutrients introduction results in a complex impact on the woman's body: it stimulates own body reserves to maintain the hormonal balance and to normalize the psychoemotional state, which is clinically reflected in the lowering of the hot flashes frequency and the improvement of the quality of life of the patients. The authors analyzed the experience of use of the biologically active additive MENSE in patients with vegetovascular disorders and psychoemotional disorders during the menopause. During the observation period, the observed decrease in the Kupperman index amounted to 1.7 times on average for the entire group of patients. In the group of patients with an initially average gravity the climacteric syndrome by Vikhlaeva scale, the number of hot flashes was reduced by more than 1.5 times; in the of patients with an initially slight menopause syndrome – by more than 2 times.
Keywords: menopause syndrome, menopause, hot flashes, Kupperman index, Vikhlyaeva scale, MENSE.
Введение
Возникающий с возрастом дефицит эстрогенов приводит к ряду характерных изменений в организме женщины: со стороны обмена веществ (резорбция костей, мышечные боли), со стороны функционирования вазомоторной системы (приливы, сосудистые заболевания), со стороны психоэмоциональной сферы (депрессии, психозы), урогенитальной и др. Степень выраженности этих изменений лежит в основе клинических проявлений течения климактерического периода и, соответственно, в основе выбора врачебной тактики: проведение дотации микронутриентов и/или фармакологической поддержки.
Существует в настоящее время два основных стратегических направления – нормализация уровня эстрогенов путем применения гормональных лекарственных средств (традиционная гормональная терапия) либо купирование симптомов фармакологическими средствами (антидепрессанты, транквилизаторы, сердечно-сосудистые средства, препараты кальция, магния). Гормональная терапия эффективно облегчает менопаузальные симптомы, но существует ряд противопоказаний к ее назначению: рак молочной железы, яичников, матки, венозная тромбоэмболия. Такие побочные эффекты, как задержка жидкости в организме, масталгия, головная боль, также ограничивают применение гормональных средств [1, 2].
Приливы (специфические вегетативно-сосудистые пароксизмы) – наиболее частый вазомоторный симптомокомплекс, который доминирует в жалобах пациенток, значимо снижает качество жизни и является одним из ведущих симптомов для определения тяжести течения. Многочисленные исследования показывают возрастающую тенденцию не применять менопаузальную гормональную терапию при умеренной симптоматике приливов. Все чаще используют эффективную модификацию диеты и образа жизни наряду с альтернативной фармакотерапией [3].
Клинико-фармакологические аспекты влияния микронутриентов на частоту возникновения и выраженность приливов
Первые публикации об эстрогенной активности растений появились в начале 1950 г. В 1951 г. австралийские химики Bradbury и White, изучая причину эпидемии бесплодия у овец, установили, что таковой является изофлавон генистейн, содержащийся в клевере (Trifolium subterranium). Позднее генистейн и другие соединения с эстрогенной активностью были найдены в люцерне, сое, хмеле и других лекарственных растениях. Они получили название фитоэстрогены.
Следующим этапом в изучении фитоэстрогенов стали исследования, посвященные течению климактерического периода у азиатских женщин. Так, у японских женщин в перименопаузальный период выявили очень низкую распространенность приливов – всего 5%. Сравнительный анализ климактерических симптомов у американских, канадских и японских женщин показал, что наиболее низкая распространенность приливов и депрессии, а также наименее частое употребление лекарственных средств против этих симптомов были выявлены у японских женщин. Более того, в японском языке нет термина для обозначения приливов. Такое течение климактерического периода у азиатских женщин объясняется особенностями их питания – преобладанием растительной пищи (прежде всего, продуктов из сои) [4, 5].
Фитоэстрогены не являются стероидами, однако способны проявлять свойства эстрогенов, что обусловлено их структурой, которая позволяет им связываться с эстрогеновыми рецепторами. Хотя сила такого связывания у фитопрепаратов ниже, чем у эстрадиола, тем не менее в количествах, обнаруживаемых в некоторых продуктах (пиво из хмеля, соевые продукты) или биологически активных добавках, фитоэстрогены могут индуцировать биологические эффекты.
Фитоэстрогены действуют как селективные модуляторы эстрогеновых рецепторов, обеспечивая в зависимости от эстрогенной насыщенности слабое антиандрогенное или эстрогенное воздействие.
Соя, соевые продукты и препараты, созданные на основе соевых бобов, нашли широкое применение в связи с высоким содержанием в них фитоэстрогенов. Изофлавоны сои классифицируют как фитоэстрогены, поскольку они связываются с рецепторами эстрогенов и оказывают влияние, подобное эстрогенам. Гормональная активность сои установлена как в экспериментах на животных, так и в клинических исследованиях. Клинические исследования продемонстрировали, что изофлавоны сои отличаются наилучшим профилем эффективность/безопасность среди всех фитоэстрогенов. Эффективность экстрактов сои по редукции частоты приливов составляет 20,6%, а тяжести приливов – 26,2%. Регулярное потребление изофлавонов сои смягчает проявление негативных эффектов менопаузы, маскируя отсутствие эндогенных эстрогенов [6].
Фитоэстрогены сохраняют безопасность в отношении пролиферативных процессов репродуктивной системы, что связано с разным сродством к двум типам эстрогеновых рецепторов. Широко обсуждается вопрос о возможном влиянии фитоэстрогенов на костную ткань и факторы риска развития сердечно-сосудистых заболеваний. Доклинические и клинические исследования показали, что фитоэстрогены могут улучшать липидный профиль плазмы крови, а также влиять на процессы костного ремоделирования [4, 6].
Аминокислота бета-аланин посредством активации глициновых рецепторов способствует сохранению границ терморегуляторной зоны; оказывает седативный эффект, антигистаминное действие, стабилизирует энергетический метаболизм. Данные клинических и экспериментальных исследований демонстрируют, что бета-аланин реализует быстрый и медленный эффекты купирования приливов. Быстрый эффект происходит за счет блокады Н3-гистаминового рецептора в терморегуляторном ядре гипоталамуса. Обогащенная β-аланином кровь поступает в мозг и оказывает воздействие на терморегуляторное ядро гипоталамуса путем связывания с Н3-рецепторами к гистамину и с глициновыми рецепторами, обеспечивая быстрый эффект. Обладая более продолжительным эффектом воздействия на глициновые рецепторы, чем сам глицин, β-аланин оказывает нормализующее действие на терморегуляцию, вазомоторику, улучшение памяти, концентрацию внимания. Медленный эффект связан с метаболизмом β-аланина в ЖКТ и с последующим накоплением карнозина и пантотеновой кислоты в организме, что стабилизирует энергетический метаболизм, снижая вероятность приливов и оказывая долговременный защитный эффект [7, 8].
5-гидрокситриптофан представляет собой одну из форм натуральной аминокислоты триптофана, которая эффективно снимает проявления депрессии, нейтрализует стресс и улучшает сон. 5-гидрокситриптофан представляет собой прекурсор нейромедиаторов, обладает серотонинергическим действием. Результаты метаанализа 108 клинических исследований по изучению антидепрессивного действия 5-гидрокситриптофана показали, что в 95% случаях назначение давало положительный результат, фиксируемый на основании формализованных опросников. Предполагается, что дополнительный прием 5-гидрокситриптофана может формировать преждевременное ощущение сытости и снижать, таким образом, количество потребляемой пищи [9].
Витамин С участвует в синтезе стероидных гормонов, в частности эстрогенов. Улучшает способность организма усваивать кальций, фолиевую кислоту. Обладает противовоспалительными свойствами и уменьшает риск развития инфекций мочеполовой системы. В сочетании с витамином Е повышает переносимость физических нагрузок и снижает тревожность.
Витамин Е способствует улучшению капиллярного кровообращения в области гипофиза, а также выполняет коферментные функции, стимулирующие синтез холестерина и стероидных гормонов.
Дополнительное поступление в организм фолиевой и пантотеновой кислот способствует поддержанию более высокого уровня эстрогенов во время менопаузы.
Витамины В6 и В12 улучшают состояние нервной системы, нормализуют сон и снижают утомляемость [10].
Вышеперечисленные компоненты входят в состав биологически активной добавки (БАД) МЕНСЕ, которая предназначена для микронутриентной поддержки женщин во время менопаузы. Рациональный состав компонентов позволяет рассматривать комплекс как вариант эффективной модификации диеты и/или эффективный компонент альтернативной терапии у пациенток с легкой и средней тяжестью течения климактерического синдрома.
Опыт применения БАД МЕНСЕ у женщин в климактерическом периоде
Целью научно-исследовательской работы является анализ опыта применения БАД МЕНСЕ (ЗАО «АКВИОН», Россия) у пациенток с вегетососудистыми нарушениями и психоэмоциональными расстройствами в период менопаузы. Проанализирован опыт применения МЕНСЕ у женщин в период менопаузы (отсутствие месячных в течение 6 мес.) с клинически верифицированным климактерическим синдромом слабой и умеренной степени тяжести течения (по шкалам Купермана и/или Вихляевой). В исследовании не принимали участие женщины с эстрогензависимыми опухолями; миомой матки; опухолями гипоталамо-гипофизарной системы; при наличии сопутствующих декомпенсированных заболеваний или острых состояний, наличие которых могло бы повлиять на результаты исследования. Пациентки принимали МЕНСЕ по 1 капсуле 2 раза в день на протяжении 3 месяцев, а также получали терапию, постоянно используемую для лечения имеющихся сопутствующих заболеваний. Не применялись седативные и снотворные средства; антидепрессанты; транквилизаторы; средства, стимулирующие центральную нервную сиситему; анальгетики; β-адреноблокаторы; валокордин.
Проанализирован опыт применения МЕНСЕ у 30 женщин в возрасте от 45 до 58 лет с климактерическим синдромом в период менопаузы. Средний возраст пациенток, включенных в исследование, составил 50,8±5,6 года. У всех женщин верифицирован климактерический синдром слабой и умеренной степени тяжести течения (по шкалам Купермана и/или Вихляевой). Легкая степень тяжести климактерического синдрома была диагностирована у 12 пациенток (40% от общего количества пациенток; средний балл по шкале Купермана составил 32,5±1,3; среднее количество приливов по шкале Вихляевой – 8,2±0,7). Средняя степень тяжести была диагностирована у 18 пациенток (60% от общего количества пациенток, средний балл по шкале Купермана составил 42,06±4,05 балла; среднее количество приливов по шкале Вихляевой – 12,4±1,8).
Длительность климактерического синдрома колебалась от 1,5 до 7 лет: у 7 пациенток (23,3%) длительность составила менее 3 лет; у 10 пациенток (33,3%) – от 3 до 5 лет; у 11 пациенток (36,6%) – от 5 до 7 лет.
В качестве критерия оценки эффективности применения БАД МЕНСЕ использовалась динамика индекса Купермана (модифицированного менопаузального индекса) и оценка состояния женщин по шкале Вихляевой.
На первом визите (до начала приема МЕНСЕ;) тяжесть течения климактерического синдрома у женщин, включенных в исследование, как средняя была расценена у 18 женщин (60%), как легкая – у 12 женщин (40%). Среднее значение индекса Купермана по группе составило 38,33±5,31 балла. На втором визите (через 1 месяц приема МЕНСЕ) средняя тяжесть течения, согласно рассчитанному индексу, имела место у 16 пациенток (53,3%), легкая – у 14 (46,7%), среднее по группе рассчитанное значение индекса Купермана составило 37,06±4,75 балла. На третьем визите (после 2 месяцев приема МЕНСЕ) средняя тяжесть течения была диагностирована у 12 пациенток (40%), легкая – у 18 (60%) пациенток, среднее по группе значение индекса Купермана1 составило 32,96±4,44 балла. В конце периода наблюдения (после 3 месяцев приема МЕНСЕ) средняя тяжесть течения определялась у 6 пациенток (20%); легкая – у 24 пациенток (80%), среднее по группе значение индекса Купермана составило 29,73±3,94 балла (табл. 1).
Таблица 1. Динамика индекса Купермана (модифицированного менопаузального индекса) у пациенток на фоне приема МЕНСЕ
| №п/п | ВИЗИТ 1 Исходные значения | ВИЗИТ 2 1 месяц приема МЕНСЕ | ВИЗИТ 3 2 месяца приема МЕНСЕ | ВИЗИТ 4 3 месяца приема МЕНСЕ | Динамика значения индекса Δ% |
| 1 | 40 | 38 | 32 | 28 | 30,0 |
| 2 | 39 | 37 | 33 | 30 | 23,07 |
| 3 | 44 | 42 | 37 | 33 | 25,0 |
| 4 | 34 | 34 | 30 | 26 | 23,52 |
| 5 | 45 | 44 | 40 | 35 | 22,22 |
| 6 | 34 | 34 | 30 | 25 | 26,47 |
| 7 | 48 | 46 | 40 | 35 | 27,08 |
| 8 | 34 | 34 | 33 | 28 | 17,64 |
| 9 | 32 | 34 | 28 | 26 | 18,75 |
| 10 | 44 | 42 | 37 | 33 | 25,0 |
| 11 | 40 | 37 | 34 | 30 | 25,0 |
| 12 | 42 | 40 | 35 | 31 | 26,19 |
| 13 | 30 | 30 | 28 | 25 | 16,66 |
| 14 | 40 | 42 | 37 | 31 | 22,5 |
| 15 | 32 | 33 | 30 | 27 | 15,62 |
| 16 | 39 | 33 | 30 | 27 | 30,76 |
| 17 | 34 | 32 | 29 | 27 | 20,58 |
| 18 | 38 | 36 | 32 | 30 | 21,05 |
| 19 | 34 | 30 | 25 | 24 | 29,41 |
| 20 | 42 | 42 | 37 | 33 | 21,42 |
| 21 | 34 | 30 | 30 | 26 | 23,52 |
| 22 | 42 | 40 | 35 | 29 | 30,95 |
| 23 | 32 | 33 | 29 | 27 | 15,62 |
| 24 | 34 | 34 | 30 | 28 | 17,64 |
| 25 | 48 | 45 | 40 | 37 | 22,91 |
| 26 | 40 | 38 | 35 | 35 | 12,5 |
| 27 | 46 | 44 | 40 | 36 | 21,73 |
| 28 | 38 | 34 | 30 | 27 | 28,94 |
| 29 | 42 | 40 | 38 | 37 | 11,9 |
| 30 | 33 | 30 | 25 | 24 | 27,27 |
| M±m | 38,33±5,31 | 37,06±4,75 | 32,96±4,44 | 29,73±3,94 | 22,7±5,21 |
| Max | 48 | 46 | 40 | 37 | 30,95 |
| Min | 30 | 30 | 25 | 24 | 11,9 |
| Mediana | 39 | 36,5 | 32,5 | 28,5 | 22,99 |
Итоговое изменение индекса Купермана в дельта-процентах колебалось от 12 до 31 Δ%. Клинически значимое изменение индекса Купермана – 14,0 Δ% отмечено на третьем визите, после двух месяцев применения МЕНСЕ.
Динамика индекса Купермана в дельта-процентах по визитам в среднем по всей группе наблюдаемых пациенток представлена на рисунке 1.
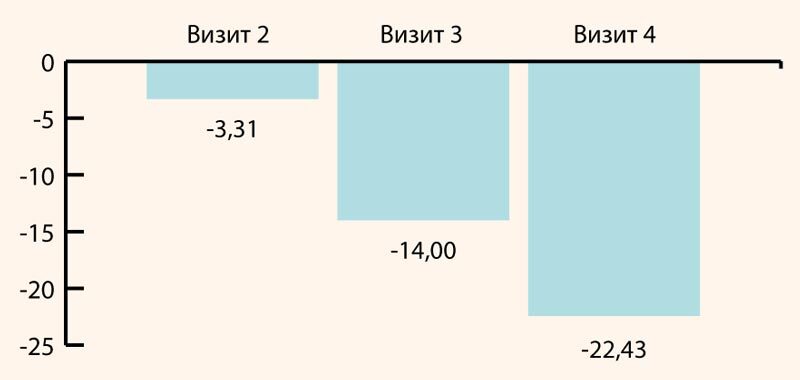
Рисунок 1. Динамика индекса Купермана в дельтапроцентах в среднем по группе наблюдаемых пациенток на фоне приема МЕНСЕ
На фоне курсового применения МЕНСЕ в группе наблюдаемых пациенток отмечена четкая тенденция к снижению степени тяжести течения климактерического синдрома по мере увеличения длительности применения препарата: до начала приема препарата средняя степень тяжести течения по шкале Вихляевой определялась у 18 пациенток (60%), легкая – у 12 пациенток (40%); на втором визите средняя – у 16 (53,3%), легкая – у 14 (46,7%); на третьем визите средняя тяжесть течения была диагностирована у 12 пациенток (40%), легкая – у 18 (60%) пациенток; в конце периода наблюдения средняя тяжесть течения определялась у 6 пациенток (20%); легкая – у 24 пациенток (80%).
Результаты оценки тяжести течения климактерического синдрома у пациенток по шкале Вихляевой были идентичными оценке тяжести течения, проведенной по шкале Купермана. Таким образом, в результате курсового использования МЕНСЕ тяжесть течения климактерического синдрома у 12 (40%) пациенток перешла из средней (10-20 приливов в сутки с выраженным нарушением общего состояния и трудоспособности) в легкую (до 10 приливов в сутки с нерезко выраженным нарушением общего состояния и трудоспособности) (табл. 2, рис. 2). В группе пациенток с изначально средней тяжестью течения климактерического синдрома за период наблюдения отмечено снижение количества приливов с 16,1±2,4 до 9,8±3,2 (в 1,64 раза, на 39,12 Δ%), которое не явилось статистически значимым (р>0,05). В группе пациенток с изначально легким течением климактерического синдрома за период наблюдения отмечено статистически значимое снижение количества приливов с 7,8±1,2 до 3,5±1,1 (более чем в 2 раза, на 55,12 Δ%), которое явилось статистически значимым (р<0,05).
Таблица 2. Динамика состояния пациенток, принимавших МЕНСЕ, по шкале Вихляевой
| ВИЗИТ 1 до начала приема МЕНСЕ | ВИЗИТ 2 1 месяц приема МЕНСЕ | ВИЗИТ 3 2 месяца приема МЕНСЕ | ВИЗИТ 4 3 месяца приема МЕНСЕ | |
| ЛЕГКОЕ ТЕЧЕНИЕ до 10 приливов в сутки с нерезко выраженным нарушением общего состояния и трудоспособности | ||||
| Количество пациенток (%) | 12 (40%) | 14 (46,7%) | 18 (60%) | 24 (80%) |
| СРЕДНЯЯ ТЯЖЕСТЬ ТЕЧЕНИЯ 10-20 приливов в сутки с выраженным нарушением общего состояния и трудоспособности | ||||
| Количество пациенток (%) | 18 (60%) | 16 (53,3%) | 12 (40%) | 6 (20%) |
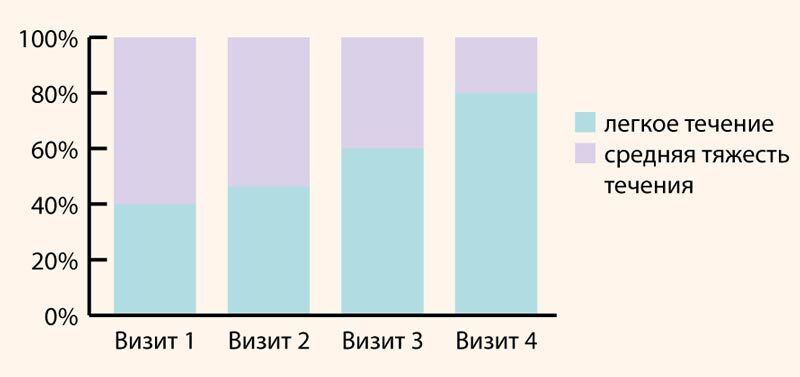
Рисунок 2. Динамика изменения степени тяжести течения климактерического синдрома на фоне применения МЕНСЕ
Для качества жизни пациенток с климактерическим синдромом важное значение имеет состояние психоэмоционального статуса, оценка которого проводилась с применением нейропсихологического теста Спилберга (табл. 3).
Таблица 3. Динамика состояния пациенток на фоне приема МЕНСЕ по нейропсихологическому тесту Спилберга
| Методики Тест Спилберга | ВИЗИТ 1 Исх. значения, баллы | ВИЗИТ 2 Через 1 мес., баллы | ВИЗИТ 3 Через 2 мес., баллы | ВИЗИТ 4 Через 3 мес., баллы |
| Личностная тревожность | 52,6 ± 5,6 | 27,2 ± 6,3 * | 26,8 ± 5,9* | 26,1 ± 6,2* |
| Ситуационная тревожность | 45,4 ± 5,7 | 25 ± 5,3* | 25,6 ± 5,4* | 24,9 ± 5,8* |
| Общий балл | 101,4 ± 5,7 | 51,0 ± 5,9 |
* р<0,05.
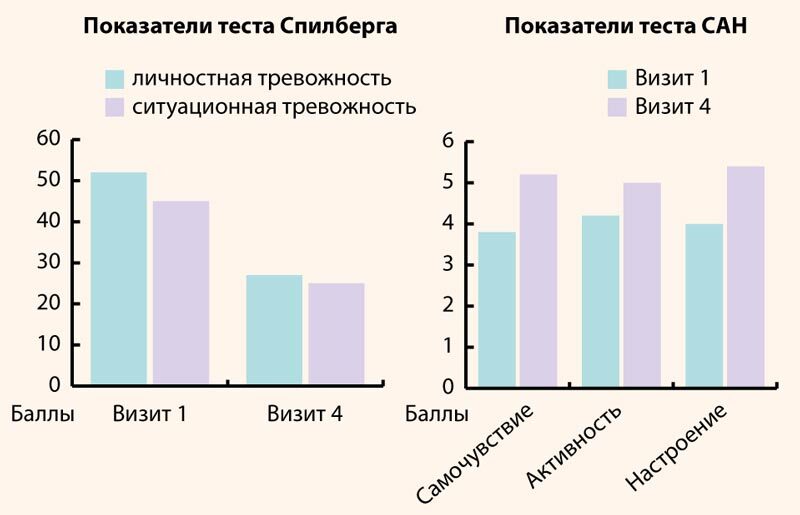
Рисунок 3. Динамика показателей нейропсихологического теста Спилберга у наблюдаемых пациенток на фоне приема БАД МЕНСЕ
При анализе результатов теста Спилберга (табл. 3, рис. 3) выявлено, что исходные параметры личностной тревожности, характеризующие устойчивую склонность личности воспринимать большой круг ситуаций как угрожающие, реагировать на такие ситуации состоянием тревоги, а также свидетельствующие о наличии невротического конфликта, эмоциональных и невротических срывов, составили у пациенток исследуемой группы 52,6±5,6 балла. Подобные уровни показателей трактуются как высокий уровень тревожности. После первого цикла приема МЕНСЕ (1 месяц) этот показатель статистически достоверно уменьшился по сравнению с исходным на 48,3 Δ% и составил 27,2±6,3 (р<0,05), что говорит о переходе уровня личностной тревожности из категории «высокая тревожность» (более 50 баллов) в категорию низкого уровня личностной тревожности (менее 30 баллов), который и сохранялся у пациенток в течение дальнейшего периода наблюдения. После второго цикла приема (2 месяца) показатель практически не изменился (уменьшение по сравнению с исходным значением составило 49,04 Δ%), после третьего цикла (3 месяца) также не отмечено дальнейших значимых изменений (уменьшение по сравнению с исходным значением составило 50,4 Δ%).
У пациенток наблюдаемой группы исходные показатели ситуационной тревожности (реактивной тревожности как состояния), свидетельствующие о наличии напряжения, беспокойства, нервозности, нарушении внимания, тонкой координации, соответствовали категории «средний уровень тревожности» (от 30 до 50 баллов). Динамика показателей ситуационной тревожности на фоне приема МЕНСЕ в целом соответствовала динамике показателей личностной тревожности (табл. 3). После первого цикла приема МЕНСЕ (1 месяц) этот показатель статистически достоверно уменьшился по сравнению с исходным на 44,71 Δ% и составил 25,1±5,3 балла (р<0,05). Динамика балльной оценки состояния ситуационной тревожности говорит о переходе уровня личностной тревожности из категории «средняя тревожность» (от 30 до 50 баллов) в категорию низкого уровня ситуационной тревожности (менее 30 баллов), которая и сохранялась у пациенток в течение дальнейшего периода наблюдения (табл. 3). По итогам приема МЕНСЕ при проведении субъективной оценки пациентками результатов приема получены следующие результаты: более половины пациенток – 17 (56,6%) отметили значительное улучшение; 12 (40%) пациенток отметили некоторое улучшение; отсутствие улучшения отметила 1 (3,3%) пациентка. Ухудшение не было отмечено ни одной из пациенток.
Заключение
Проведенный анализ опыта применения у пациенток выявил эффективность МЕНСЕ производства ЗАО «АКВИОН» и позволил сделать заключение о положительном влиянии на выраженность и частоту проявлений вегетососудистых нарушений и психоэмоциональных расстройств у женщин в менопаузе с климактерическим синдромом легкой и средней степени тяжести.
Индекс Купермана является интегральным показателем степени выраженности симптомов менопаузы. Полученная в ходе исследования динамика индекса Купермана – снижение индекса в 1,7 раза в среднем по всей группе пациенток – является показателем, реально отражающим улучшение качества жизни женщин с климактерическим синдромом на фоне применения МЕНСЕ. В результате курсового использования МЕНСЕ тяжесть течения климактерического синдрома у 12 пациенток перешла из средней (10-20 приливов в сутки с выраженным нарушением общего состояния и трудоспособности) в легкую (до 10 приливов в сутки с нерезко выраженкым нарушением общего состояния и трудоспособности).
В группе пациенток с изначально средней тяжестью течения климактерического синдрома по шкале Вихляевой за период наблюдения отмечено снижение количества приливов более, чем в 1,5 раза; в группе пациенток с изначально легким течением климактерического синдрома за период наблюдения отмечено уменьшение количества приливов более, чем в 2 раза.
Несмотря на то что клинически значимая динамика индексов Купермана и Вихляевой определялась только после второго месяца приема МЕНСЕ, при субъективной оценке динамики состояния значительное улучшение состояния на втором визите (после 1 мес. применения) отметили 12 (40%) пациенток, что, вероятнее всего, объясняется более быстрой положительной динамикой состояния по нейропсихологической шкале Спилберга. Статистически значимое снижение уровня личностной и ситуационной тревожности по тесту Спилберга и переход в категорию низкого уровня тревожности отмечены уже на втором визите.
Прослеживается тенденция к повышению эффективности по мере увеличения длительности приема МЕНСЕ. Регистрационный статус БАД не ограничивает МЕНСЕ по длительности применения и позволяет использовать в качестве источника микронутриентов при проведении лекарственной терапии климактерического синдрома.
В результате дотации микронутриентов комплексное воздействие МЕНСЕ на организм женщины заключается в стимуляции собственных резервов организма по поддержанию гормонального баланса и нормализации психоэмоционального состояния, что клинически выражается в снижении частоты приливов и улучшении качества жизни пациенток.
Литература
- BeraL V. Breast cancer and hormone-replacement therapy in the Million Women Study. Lancet 2003; 362: 419-27.
- Tsai SA, Stefanick ML, Stafford RS. Trends in menopausal hormone therapy use of US office-based physicians, 2000-2009, Menopause 2011; 18: 385-92.
- Nachtigall LE, Baber RJ, Barentsen R et al. Complementary and hormonal therapy for vasomotor symptom relief: a conservative clinical approach. J Obstet Gyn Can 2006; 28 (4): 279-89.
- Булаев В.М., Ших Е.В., Сычев Д.А. Современная фитотерапия. М.: МЕДПРЕСС-информ, 2011. 144 С.
- Зайдиева Я.З. Альтернативная терапия менопаузальных расстройств у женщин в климактерии. РМЖ. 2017. 12. 873-878.
- Jenks BH, Iwashita S, Nakagawa Y, Ragland K, Lee J, Carson WH, Ueno T, Uchiyama S. A pilot study on the effects of S-equol compared to soy isoflavones on menopausal hot flash frequency. J Womens Health (Larchmt). 2012 Jun; 21(6): 674-82.
- Громова О.А., Торшин И.Ю., Лиманова О.А., Никонов А.А. Патофизиология вегетативно-сосудистых пароксизмов (приливы) у женщин в период менопаузы и механизм действия β-аланина. Новая клиникофармакологическая концепция. Гинекология. 2010 2. 29-36.
- Торшин И.Ю., Громова О.А., Лиманова О.А. Быстрый эффект клималанина (β-аланина) при приливах: сравнительное исследование взаимодействий бета-аланина, таурина и глицина с глициновыми рецепторами. Гинекология. 2012. 2. 25-29.
- Смирнова Т.Н. Опыт применения 5-гидрокситриптофана в комплексном лечении депрессивных расстройств. Материалы YII научнопрактической конференции с международным участием по нутрициологии «Питание и здоровье. XXI век».
- Ших Е.В., Махова А.А. Витамины в клинической практике. М.: Практическая медицина, 2014. 367.