Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
Без антибиотиков здесь не обойтись. Инфекционные осложнения при искусственном прерывании беременности — вызов современной медицине
СтатьиОпубликовано в :
Status Praesens. Гинекология, акушерство, бесплодный брак / №5 [16]
Галина Борисовна Дикке, докт. мед. наук,
проф. кафедры акушерства, гинекологии и репродуктивной медицины ФПК МР РУДН (Москва)
В последние годы достигнуто значительное снижение количества абортов1, хотя в целом нежелательная беременность, безусловно, остаётся нерешённой проблемой российского общества. Теперь пришло время обратить более пристальное внимание на вопрос качества медицинской помощи при нежелательной беременности. На фоне достижений мирового сообщества в вопросах обеспечения безопасности пациенток при аборте этот вопрос обострился как никогда.
Подходы к оценке медицинских последствии аборта в российской и зарубежной литературе имеют существенные различия. За рубежом на основе методов доказательной медицины пришли к выводу об отсутствии влияния на репродуктивное здоровье женщины современных технологий прерывания беременности2. В России же в средствах массовой информации тиражируются сведения о «калечащих» последствиях любого аборта 3-5 независимо от метода его проведения. А ведь именно метод - ключевой вопрос, поскольку 70% искусственных прерываний беременности выполняют в нашей стране методом дилатации и кюретажа (ДиК)1,6,7, т.е. классического «выскабливания» (называемого у нас хирургическим абортом), от которого развитые страны отказались ещё в 60-х годах прошлого столетия.
Как бы то ни было, возвращаясь к вопросам качества даже безопасного прерывания беременности, наиболее актуальной проблемой на современном этапе признана профилактика инфекционных осложнений, поскольку предсуществующие инфекции гениталий существенно повышают риск неблагоприятных исходов аборта3,8,9. Поскольку единые подходы к профилактике инфекционных осложнений после искусственного прерывания беременности не разработаны, стандарты медицинской помощи женщинам при нежелательной беременности и аборте отсутствуют, практикующим врачам будет полезен обзор данных по этому вопросу, соответствующих строгим рамкам доказательной медицины.
Несмотря на то что в критическом осознании научной ценности любой информации исследователи придерживаются правила 5-летнего «разбега» литературных источников, в представленном обзоре глубина поиска составила 10 лет для оригинальных исследований, 3 года - для метаанализов (обзоры) и клинических рекомендаций (Clinical Guidelines). Это та самая осознанная необходимость, которая позволила авторам настоящего обзора, опираясь на весьма авторитетные источники, предоставить читателям журнала наиболее полную и корректную информацию о рациональных подходах к профилактике инфекций после аборта.
Поиск осуществляли в базах данных Cochrane Collaboration, PubMed, Medline, на сайтах Всемирной организации здравоохранения, Королевского и Американского обществ акушеров-гинекологов (RCOG, Великобритания, и ACOG, США), Национальной федерации абортов (NAF, США), Управления по контролю качества пищевых продуктов и лекарственных препаратов (FDA) и Института Гуттмахера (США)11-15 по ключевым словам «инфекция», «антибиотики», «профилактика», «осложнения» в ассоциации со словами «аборт», «легальные аборты» и «медицинский аборт». Уровни доказательности рекомендаций приведены в соответствие с требованиями, оформленными по классификации RCOG16.
Оцифрованная опасность
Для прояснения масштаба проблемы инфекционных постабортных осложнений обратимся к статистике собственно абортов. По данным ВОЗ, в 2008 году показатель абортов в мире составил 28 на 1000 женщин фертильного возраста (15-45 лет)17. При этом разброс между развитыми и развивающимися странами был невелик - от 24 до 29 соответственно (например, в США прерывают нежелательную беременность 16 из 1000 женщин18). В 2010 году в России было проведено 28 абортов на 1000 женщин фертильного возраста (15-49 лет вместе с самопроизвольными и другими видами абортов)1, а в 2011 - 26,7, что вполне сопоставимо с мировыми показателями. И это действительно новость, поскольку до сих пор было распространено мнение о чрезмерно большом количестве абортов в нашей стране. Правда, говорим мы сейчас только об официальной статистике.
На этом фоне общая частота инфекций после легального аборта в I триместре в целом невелика, но колеблется в определённом диапазоне в зависимости от выбранных критериев, которые отличаются в разных странах. Так, в США независимо от используемого метода регистрируют менее 1% инфекционных осложнений абортов, а в Великобритании - на порядок выше17. Когда в качестве объективного критерия используют, например, температуру тела 38°C и более, уровень частоту инфекционных осложнений оценивают в диапазоне 0,01-2,44%9.
Данные обзора 65 исследований по медикаментозному аборту с участием 46 421 женщины, полученные исследователями из Колумбийского университета С. Шеннон и соавт. (Shanon C. et al.), показали частоту инфекционных осложнений 0,92% после его проведения в сроке до 26 нед гестации19. В сравнении показателя частоты инфекционных осложнений после искусственного прерывания гестации хирургическим и медикаментозным путём в I триместре именно фармаборт имеет больше преимуществ. На протяжении четырёх лет экспертам авторитетнейшей организации - FDA - удалось выявить 607 неблагоприятных исходов медикаментозного аборта20. Серьёзные или опасные для жизни инфекции возникли у 46 женщин (7,6% от числа всех зарегистрированных осложнений).
Другое ретроспективное исследование, изучавшее 95 163 выполненных медикаментозных аборта, продемонстрировало 206 случаев осложнений, требующих госпитализации пациенток, из них 19 были инфекционными (0,02%; 95% ДИ от 0,01-0,03%)21.
Другой хирургический При поиске необходимой информации в зарубежных источниках русскоязычная аудитория может столкнуться с неожиданной сложностью. Термин «surgical abortion» по сей день очень часто можно встретить в публикациях на PubMed.com, причём вполне серьёзно и доказательно обсуждаются в том числе преимущества этого метода в сравнении с медикаментозным прерыванием беременности. Например, публикация 2013 года10 позволяет сделать такой вывод: хирургический аборт, выполненный в сроке до 7 нед беременности, несёт в себе гораздо меньший вред для организма женщины, чем аборты более позднего срока. Что это - ренессанс хирургического аборта? А как же тогда современные и бесспорно прогрессивные представления о необходимости отказа от выскабливания? А всё оказывается очень просто! Дело в том, что термин «surgical abortion» сегодня в англоязычной литературе применяют для обозначения вакуумной аспирации, а не традиционных для нашего понимания дилятации и кюретажа. Сбить с толку может также «elective abortion - surgical» или «therapeutic abortion - surgical», достаточно помнить, что под этими терминами за границей понимают искусственное прерывание нежелательной беременности с применением специального вакуумного отсоса. |
АБОРТЫ В МИРЕ И В РОССИИ (НА 1000 ЖЕНЩИН ФЕРТИЛЬНОГО ВОЗРАСТА) 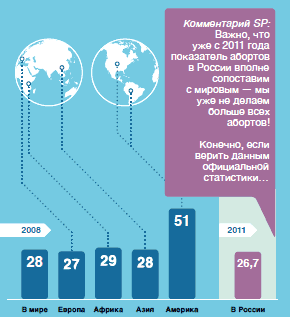 |
Prognosis pessima: летальность
В США в 2008 году зафиксировано относительно небольшое число смертей, связанных с легальным абортом, - 0,7 случая на 100 000 прерываний гестации17, однако из них примерно 30% связаны с инфекционными осложнениями22.
По данным Американской федерации планирования семьи, исходный риск тяжёлых случаев послеабортных инфекционных осложнений (сепсис или смерть) составляет 9,3 на 10 000 медицинских абортов (0,09%)15. Сепсис, обусловленный Clostridium sordellii, стал причиной восьми случаев материнской смертности от инфекций после всех медикаментозных абортов в США, выполненных к 2010 году23. Кстати, этот микроорганизм вызывает осложнения не только после медикаментозного аборта: женщины также умирали из-за инфицирования им после родов, выкидышей, хирургического аборта и лечения заболеваний шейки матки у небеременных24. Тем не менее связи между септическим шоком и приёмом мифепристона или мизопростола не установлено25.
Данные о материнской смертности в России приведены в общей совокупности абортов, включая самопроизвольные: в 2003-2009 годах в среднем по этой причине ежегодно умирали около 100 женщин (125 - в 2003-м, 76 - в 2006-м, 93 - в 2009 году), что в структуре материнской смертности составило 25,5; 19,6 и 20,3% соответственно. При этом доля умерших женщин от медицинского (легального) аборта в среднем за этот период - 4%, а за 2008-2009 годы - 1,1% (по одному случаю в год), причём в 2009 году причиной гибели женщины стал эпилептический статус26. Основное количество материнских смертей наблюдают при выполнении аборта в поздних сроках.
Резюмируя, важно отметить, что уровень летальности при безопасных абортах (выполненных в медицинских учреждениях) существенно ниже, чем при небезопасных (внебольничных и криминальных). Даже при самом низком уровне небезопасных абортов (Восточная Европа) материнская смертность после аборта составляет 30 случаев, что в 40 раз выше, чем в США.
Кроме того, эксперты отмечают, что при увеличении срока беременности на каждые 2 нед риск материнской смертности увеличивается в 2 раза независимо от метода и достигает максимума при сроках выше 20 нед17. Основная причина материнской заболеваемости и смертности - внебольничный аборт. Квалифицированно выполненный искусственный аборт очень редко вызывает тяжёлые осложнения11,17, хотя это и не снимает необходимости активных профилактических мероприятий.
При увеличении срока беременности на каждые 2 нед риск материнской смертности увеличивается в 2 раза независимо от метода. |
ИНФЕКЦИОННОЕ ОСЛОЖНЕНИЕ АБОРТА 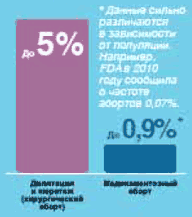 |
Засланные агенты
Наиболее значимыми в развитии инфекционных осложнений после искусственного прерывания беременности считают хламидии и гонококки (А*)27. Отмечено, что распространённость обеих инфекций выше среди молодых и бедных женщин, женщин с определёнными факторами риска (большое количество половых партнёров, ранний сексуальный дебют, выявленная (острая или хроническая) гонорейная или хламидийная инфекция в течение последних 12 мес)16. К слову, в нашей стране в 2009 году заболеваемость хламидийной инфекцией составила 80,3 на 100 000 населения28, однако данные по её распространённости весьма дискуссионны ввиду высокой доли бессимптомного «носительства».
* Здесь и далее уровни доказательности приведены по классификации RCOG16.
Особую роль играет C. trachomatis как фактор персистирующего длительно текущего патологического процесса в развитии хронического эндометрита29. И вот что интересно: практически любые внутриматочные вмешательства и роды сопровождает манифестация клинической картины эндометрита, и после аборта нередко её расценивают как «осложнение, возникающее вследствие травмы эндометрия», однако именно последнее утверждение неверно по сути. Так, изучение 1032 женщин, которые подверглись хирургическому аборту в I триместре без антибиотикопрофилактики, показало, что наличие C. trachomatis до аборта повышает риск лапароскопически подтверждённых сальпингитов в 30 раз (ОР 30; 95% ДИ 11-85) и эндометрита (без сальпингита) - в 4 раза (ОР 4,1; 95% ДИ 2,5-6,7). В целом в присутствии C. trachomatis опасность ВЗОМТ возрастает в 9 раз9.
Табл. Лихорадка при медикаментозном аборте: дифдиагноз
| Симптомы | Побочное действие мизопростола | Инфекция |
| Время возникновения | В течение первых часов после приёма |
Через 8 ч и более после приёма мизопростола |
| Продолжительность | 2-3 ч | Постоянная на протяжении нескольких дней |
| Степень гипертермии | Субфебрильная (37,0-37,8°С) | 38°С и выше |
| Купирование | Самостоятельно без использования лекарственных препаратов |
|
| Необходимы медикаменты | Частота 4-37% | 0,09-0,5% |
Этиологически менее значимы микоплазмы, анаэробы и вирусы, а о роли условно-патогенных микроорганизмов в литературе сведений практически нет. Тем не менее очевидно, что при процедурах с доступом в полость матки через шейку бактериальное обсеменение неизбежно9, тогда как медикаментозный аборт этот риск практически исключает - скорее всего именно поэтому инфекции гораздо реже осложняют медикаментозный аборт по сравнению с хирургическим.
Участие бактериального вагиноза в развитии инфекционных осложнений искусственного прерывания беременности до сих пор признаётся не всеми специалистами. Эксперты RCOG считают его одним из ведущих факторов риска послеабортной инфекции (С) наряду с хламидиями и гонококками16, а например, о значительном снижении риска ВЗОМТ после аборта при назначении профилактики9 найдено лишь одно сообщение. Высокую вероятность послеабортного эндометрита в условиях инфицирования беременных возбудителями ИППП и наличия сочетанных инфекций подтверждают и отечественные исследователи3.
Вопросу взаимосвязи вагинальной микроэкологии, ВЗОМТ и различных внутриматочных вмешательств посвящено достаточное количество исследований. Мнения экспертов единодушны: аборт сам по себе не служит причиной отдалённых последствий в виде невынашивания беременности, предлежания плаценты, низкой массы тела новорождённых, причём они происходят с той же частотой, что и у женщин, перенёсших ВЗОМ, вне связи с процедурой прерывания беременности. Перечисленные осложнения становятся результатом именно инфицирования матки ещё до наступления беременности и её прерывания (В)5,17,30. Так, обследование женщин, которые перенесли инфекцию в послеабортный период9, демонстрирует, что в этой группе пациенток вторичное бесплодие, диспареуния, тазовые боли и спонтанные аборты при последующей беременности более вероятны.
В свою очередь риск восходящей инфекции патогенными микроорганизмами непосредственно во время аборта, выполненного в лечебном учреждении, ничтожно мал. Все случаи тяжёлых инфекционных осложнений признаны результатом внебольничных вмешательств, что наиболее актуально для стран с высоким уровнем небезопасных абортов17.
Таким образом, можно сделать вывод о том, что перед осуществлением аборта крайне важно диагностировать уже имеющуюся инфекцию и провести соответствующие профилактические мероприятия.
Умерла от сепсиса после медаборта В официальной структуре материнской смертности о летальных исходах после медикаментозного прерывания беременности сообщений нет1. И всё же один клинический случай, наступивший в подобных условиях, известен (в статистике отнесён на счёт сепсиса). 31 августа 2011 года пациентка Ш., 36 лет, обратилась в частную медицинскую клинику для прерывания беременности в сроке 5 нед. Наличие маточной беременности и её срок были подтверждены данными УЗИ. В плановом порядке выполнены анализы на RW, HBs и ВИЧ. В этот же день пациентка в присутствии врача приняла мифепристон в дозе 600 мг, а 2 сентября - мизопростол в дозе 400 мкг. Контрольное УЗИ назначили на 12 сентября. Однако именно в этот день пациентка в тяжёлом состоянии поступила в гинекологическое отделение и 13 сентября скончалась в связи с развитием послеабортного панметрита, сальпингита, пельвиоперитонита, сепсиса, септического шока III степени, септицемии. Из цервикального канала в значительном количестве высеяли стафилококк и гемолитический стрептококк. Ретроспективно было выяснено, что в период между днём приёма мизопростола и поступлением в стационар больная отмечала наличие субфебрильной температуры тела, слабости, недомогания и связывала это состояние с ОРВИ, которым она «заразилась» от своего ребёнка. Дальнейший анализ документации показал, что развитие септического состояния у пациентки Ш. могло произойти вследствие гематогенного инфицирования из очагов хронической инфекции (хронический пиелонефрит, хронический тонзиллит), вызванной стафилококком и гемолитическим стрептококком, на фоне сниженного иммунитета и общих защитных сил организма (указание на наличие аллергической реакции и, возможно, влияние вирусной инфекции от контакта с больным ребёнком). Скорее всего данный случай следует рассматривать как трагическое стечение обстоятельств: совокупности клинических особенностей соматического статуса пациентки (наличие очагов хронической инфекции и снижение защитных сил организма) и внешних факторов, приведших к инфицированию матки и дальнейшему прогрессированию инфекционного процесса, имеющего молниеносный характер течения. Однако видны и ошибки. В частности, лечащий врач не назначил пациентке антибиотикопрофилактику, хотя анамнез требовал особого внимания к этому вопросу. Кроме того, женщина не была информирована о необходимости срочного обращения к врачу при появлении «тревожных» симптомов, свидетельствующих о развитии инфекционного процесса. |
Подводные камни диагностики
Инфекционные осложнения после аборта, выполненного любым методом, обычно диагностируют на основании клинической картины. Среди симптомов выделяют следующие: боль в области малого таза, кровотечение, лихорадку, болезненную матку (пальпаторно нормальную или мягковатую), влагалищные выделения с запахом. По данным УЗИ полость матки может быть свободна от тканей гестации или определяют наличие остатков.
В связи с тем, что мизопростол, используемый для медикаментозного аборта, повышает температуру тела, необходимо дифференцировать лихорадку, связанную с действием простагландинов, от лихорадки, вызванной инфицированием матки.
Эксперты FDA рекомендуют обращать внимание на следующие симптомы: слабость, тошноту, рвоту, диарею с наличием или без боли в животе, с гипертермией или без неё, а также другие клинические данные, указывающие на инфекцию, за исключением случаев тахикардии, если эти признаки появились спустя 24 ч после аборта. Особенно важен анализ крови - значительный лейкоцитоз со сдвигом формулы влево и гемоконцентрация могут быть признаками сепсиса. Результаты анализа крови показательны и для дифдиагностики c обычными реакциями на медикаментозный аборт, вызванными приёмом мизопростола24,31.
При первых же признаках пациентку следует госпитализировать в стационар и провести полный комплекс лечения, включающий антибактериальную, трансфузионную и другие виды терапии в соответствии с принципами лечения тазовых инфекций. При инфицировании на фоне остатков тканей гестации показана вакуумная аспирация.
Подумать заранее
| Сегодня уже не вызывает сомнений постулат, что антибиотики, рекомендуемые женщине параллельно с процедурой аборта, способны предотвратить инфекционные осложнения (А). На основе анализа данных 19 рандомизированных клинических исследований, включённых в метаанализ, риск инфекционных осложнений у женщин, получающих антибиотики, был ниже на 58% (ОР 0,58; 95% ДИ 0,47-0,71) в отличие от пациенток, которые получали плацебо. Причём защитный эффект антибиотиков был очевиден независимо от того, к каким подгруппам были отнесены обследуемые женщины: с историей воспалительных заболеваний (ОР 0,56; 95% ДИ 0,37-0,84), с выявленной хламидийной инфекцией во время процедуры (ОР 0,38; 95% ДИ 0,15-0,92), к группе низкого риска (ОР 0,65; 95% ДИ 0,47-0,90) и группе без хламидий (ОР 0,63; 95% ДИ 0,42-0,97)9,32. На основании указанного систематического обзора была предложена универсальная стратегия профилактики путём назначения антибиотиков в периоперационный период при хирургическом аборте16,17. Ряд исследований показал, что профилактические меры более экономически эффективны, даже когда применяли азитромицин, который намного дороже, чем доксициклин9,27 (сравнивали, что дешевле - лечить всех профилактически или сначала найти ИППП и лечить только инфицированных). Предпочтение скрининга перед антибиотикопрофилактикой было определено только для регионов, испытывающих дефицит антибиотиков9,14. До последнего времени вопрос о необходимости профилактического назначения антибиотиков при медикаментозном аборте практически не изучали. Однако в одном недавнем исследовании15 была показана реальная возможность снизить риск серьёзной инфекции при медикаментозном аборте с 0,093 до 0,025% посредством перехода с вагинального на буккальный путь введения мизопростола. И, наконец, самое важное - исследование позволило доказать сокращение инфекционного риска до 0,006% при рутинной антибиотико-профилактике. Таким образом, сегодня можно с высокой долей уверенности утверждать, что применение антибиотиков должно войти в стандарты оказания медицинской помощи при нежелательной беременности независимо от выбранного метода её прерывания. |
 |
Что, когда, кому и сколько?
Наиболее обсуждаемые препараты выбора - нитроимидазолы (метронидазол и тинидазол), доксициклин, азитромицин и цефтриаксон. Их высокая эффективность продемонстрирована во многих исследованиях: для нитроимидазолов снижение риска на 51% (ОР 0,49; 95% ДИ 0,31-0,80) (В), для доксициклина - на 88% (ОР 0,12; 95% ДИ 0,02-0,94) (А) с аналогичным показателем для азитромицина. Несмотря на довольно высокий - 76% - показатель снижения риска инфекционных постабортных осложнений, характерный для цефтриаксона (ОР 0,24; 95% ДИ 0,06-0,93)9, этот антибиотик всё же не должен применяться, поскольку неэффективен в отношении хламидий.
Табл. Профилактика инфекционных осложнений при прерывании беременности, RCOG (2011)16
| Для женщин, не обследованных на ИППП |
| Азитромицин 1 г внутрь в день аборта, а также метронидазол 1 г ректально или 800 мг внутрь до или во время аборта или |
| Доксициклин 100 мг перорально 2 раза в день в течение 7 дней начиная со дня аборта, а также метронидазол 1 г ректально или 800 мг перорально до или во время аборта |
| Для женщин, у которых не выявлено хламидийной инфекции |
| Метронидазол 1 г ректально или 800 мг внутрь до или во время аборта |
Относительно времени назначения антибиотиков показано, что слишком ранний приём лишь увеличивает риск побочных эффектов и может способствовать формированию резистентности микроорганизмов, в то время как задержка приёма препарата даже на 3 ч после хирургического аборта может привести к полному отсутствию эффекта профилактики33. Рекомендации, разработанные на основе исследований с использованием доксициклина, свидетельствуют об эффективности и безопасности этого препарата для целей периоперационной профилактики инфекций (А). Его следует назначить в день операции до её начала (возможно, накануне вечером после ужина, но не ранее 12 ч до манипуляции для снижения побочных эффектов [А]) коротким курсом (для минимизации риска резистентности) - достаточно одной дозы (А) - либо коротким периоперационным курсом. Назначение антибиотиков после аборта профилактического эффекта не даёт (С).
Современные рекомендации таковы: все женщины при искусственном прерывании беременности должны получать антибиотики против хламидий, гонококков и анаэробов, чтобы уменьшить риск послеабортной инфекции34 - как при хирургическом (А), так и при медикаментозном аборте (С)33. В руководстве RCOG (2011)16 рекомендованы схемы, представленные в таблице.
В опубликованных в 2010 году Рекомендациях по лечению ИППП35 и Европейском руководстве по ведению пациентов с инфекцией, вызванной C. trachomatis29, основными препаратами названы азитромицин (1 г внутрь однократно) и доксициклин (7-дневным курсом по 100 мг 2 раза в сутки)5.
Последние тенденции, описывающие появление суперустойчивых бактерий, в попытке оптимизировать антибиотико-терапию заставляют искать пути местного применения противомикробных средств. Местное использование антисептических растворов для санации считают обычной практикой в попытке уменьшить риск инфекции при хирургическом аборте, предполагая, что влагалищные процедуры эффективны. Тем не менее доказательных данных, подтверждающих этот вывод, недостаточно. Количество высеваемых видов бактерий во влагалище снижается с 5,6 до 0,1 на одну пациентку, но число видов в канале шейки матки уменьшается с 3,9 лишь до 1,79. Таким образом, угнетение вагинальных видов бактерий не коррелировало с изменением количества бактерий внутри шейки матки. Сравнивали также эффективность повидон-йода с хлоргексидином в пользу последнего (рост вагинальных культур условно-патогенной микрофлоры после обработки влагалища наблюдали соответственно в 62 и 22%)9, однако при этом риск инфекций не уменьшался (В).
Важный вопрос, нередко возникающий перед практикующим врачом при прерывании беременности, - лечение клинически выраженных инфекций, вызванных анаэробами. В этом случае также предпочтительны схемы с введением метронидазола в дозе 500 мг 2 раза в день на протяжении 7 дней по сравнению с однократной дозой 2 г внутрь (эффективность 82 против 62%)34. Существует мало доказательств пользы от продления терапии более 7 дней. При этом не следует забывать о необходимости восстановления нормальной микроэкологии влагалища с помощью любого из доступных для этого средств.
При баквагинозе, независимо от наличия клинической картины, следует провести санацию, отдавая предпочтение местным антибактериальным средствам. |
Роль бессимптомного бактериального вагиноза в развитии инфекционных осложнений после инвазивных вмешательств бесспорно доказана. Тем не менее вопрос роли местной терапии этого состояния требует переосмысления. Устранение бактериального вагиноза снижает долю инфекционных осложнений искусственного прерывания беременности на 10-75%36. Добавление к интравагинальному метронидазолу миконазола увеличивает эффективность терапии и предотвращает вагинальный кандидоз, который нередко развивается после монотерапии метронидазолом37. Весьма удачный вариант - «Метромикон-Нео», в состав которого входят 500 мг метронидазола в сочетании со 100 мг миконазола нитрата. Восстановление нормальной лактофлоры после завершения курса терапии сегодня следует считать непреложным правилом.
При всей очевидной остроте проблемы аборта важно осознать: гораздо больший потенциал опасности несут в себе именно его осложнения, в том числе инфекционные. Женщины умирают не от аборта - они гибнут от его осложнений. Именно поэтому использование антибиотиков для профилактики инфекционных осложнений в программах прерывания нежелательной беременности следует признать обязательной, возведя в ранг рутинной.
Библиографию см. StatusPraesens на с. 94-95.
Список литературы
1. Основные показатели здоровья матери и ребенка, деятельность службы охраны
детства и родовспоможения в Российской Федерации. М., 2012.
2. Tang O.S., Chan C.C., Ng E.H., Lee S.W., Ho P.C. A prospective, randomized, placebo-
controlled trial on the use of mifepristone with sublingual or vaginal misoprostol for
medical abortions of less than 9 weeks gestation // Human Reproduction. 2003. Vol. 18
(11). HP. 2315-2318.
3. Ранние сроки беременности. Изд. 2-е, испр. и доп. / под ред. В.Е. Радзинского,
А.А. Оразмурадова. М.: Медиабюро «Статус презенс», 2009.
4. Хамошина М.Б., Лебедева М.Г., Руднева О.Д., Архипова М.П., Зулумян Т.Н.
Послеабортная реабилитация: возможности комбинированных оральных
контрацептивов // Гинекология. 2010. №2. С. 25-28.
5. Хрянин А.А., Стецюк О.У., Андреева И.В. Хламидийная инфекция в гинекологии и
акушерстве: тактика ведения пациенток Нв соответствии с современными
зарубежными и российскими рекомендациями // Гинекология. 2012. №3.
6. Дикке Г.Б., Яроцкая Е.Л., Ерофеева Л.В. Стратегическая оценка политики, программ
и услуг в сфере непланируемой беременности, абортов и контрацепции в
Российской Федерации. Совместное исследование МЗ и СР РФ и ВОЗ // Проблемы
репродукции. 2010. №3. С. 92-108.
7. Тихомиров А.Л., Батаева А.Е. Лучше поздно, чем никогда // Русский медицинский
журнал. 2013. №1. С. 1-4.
8. Infection and ectopic pregnancy in medical abortion. Unpublished data. The Population
Council. 2001.
9. Prevention of infection after induced abortion. Clinical Guidelines. Release date October
2010.
10. Lichtenberg E.S., Paul M. Surgical abortion prior to 7 weeks of gestation //
Contraception. 2013. Jul. Vol. 88 (1). P. 7-17.
11. Осложнения при аборте. Руководство по техническим и управленческим
аспектам предупреждения и лечения. Всемирная организация здравоохранения,
1995. 183 с.
12. Сухих Г.Т., Яроцкая Е.Л. Стратегический подход к решению проблемы
непланированной беременности в России // Современные медицинские технологии.
2010. №5. Декабрь. С. 96-99.
13. Bartlett L.A., Berg C.J., Shulman H.B. et al. Risk factors for legal induced abortion-related
mortality in the United States // Obstet. Gynecol. 2004. Vol. 103. P. 729-737.
14. Finer L.B., Henshaw S.K. Abortion incidence and services in the United States in 2000 //
Perspect. Sex Reprod. Health. 2003. Vol. 35. P. 6-15.
15. Fjerstad M., Trussell J., Sivin I. et al. Rates of serious infection after changes in regimens
for medical abortion // N. Engl. J. Med. 2009. Vol. 361. P. 145-151.
16. Royal College of Obstetricians and Gynaecologists (RCOG). The care of women
requesting induced abortion. London (England) //HRCOG. 2011. Nov. 130 p. (Evidence-
based Clinical Guideline; no. 7). — URL: rcog.org.uk.
17. Safe abortion: technical and policy guidance for health systems. Second edition. World
Health Organization, Department of Reproductive Health and Research. 2012.
18. World Abortion Policies 2011. United Nations, 2012. — URL: un.org.
19. Shannon C., Brothers L.P., Philip N.M., Winikoff B. Infection after medical abortion: a
review of the literature // Contraception. 2004. Vol. 70 (3). P. 183-190.
20. Gary M.M., Harrison D.J. Analysis of Severe Adverse Events Related to the Use of
Mifepristone as an Abortifacient // Ann Pharmacother. 2006. Vol. 40 (2). P. 191-197.
21. Henderson J.T., Hwang A.C., Harper C.C. et al. Safety of mifepristone abortions in clinical
use // Contraception. 2005. Vol. 72. P. 175-178.
22. Achilles S., Reeves M. Prevention of infection after induced abortion // Contraception.
2011. Vol. 83. P. 295-309.
23. Spitz I.M., Grunberg S.M., Chabbert-Buffet N., Lindenberg T., Gelber H., Sitruc-Ware R.
Management of patient reseivening long-term treatment with mifepristone // Fertil Steril.
2005. Vol. 84 (6). P. 1719-1726.
24. Zane S., Guarner J. Gynecologic Clostridial Toxic Shock in Women of Reproductive Age
//ECurrent Infectious Disease Reports. 2011. Vol. 13 (6). P. 561-570.
25. Fisher M., Bhatnagar J., Guamer J., Reagan S., Hacker L.K. et al. Fatal toxic shock
syndrome associated with Clostridium sordellii after medical abortion // New Engl. J. Med.
2005. Vol. 353. P. 2352-2360.
26. О материнской смертности в Российской Федерации в 2009 году. Методическое
письмо. Письмо МЗ и СР РФ от 21 февраля 2011 г. №15-4/10/2-1694.
27. Chen S., Li J., Hoek A. van den. Universal screening or prophylactic treatment for
Chlamydia trachomatis infection among women seeking induced abortions: which strategy
is more cost-effective? // Sex Transm. Dis. 2007. Vol. 34. P. 230-236.
28. Российское общество дерматовенерологов. Инфекции, передаваемые половым
путем. Клинические рекомендации. Дерматовенерология / под ред. А.А. Кубановой.
М.: ДЭКС-Пресс, 2010. С. 413-425.
29. Lamy C., Malartic C.M. de, Perdriolle E., Gauchotte E., Villeroy-de-Galhau S.,
Delaporte M.-O., Morel O., Judlin P. Prise en charge des infections du post-abortum // J. de
Gynecol. Obstet. et Biol. de la Reproduction. 2012. Vol. 41 (8). P. 904-912.
30. Mullick S., Watson-Jones D., Beksinska M. et al. Sexually transmitted infections in
pregnancy: prevalence, impact on pregnancy outcomes, and approach to treatment in
developing countries // Sex. Trans. Infect. 2005. Vol. 81. P. 294-302.
31. Dempsey A. Serious Infection Associated With Induced Abortion in the United States
//EClinical Obstetrics and Gynecology. 2012. Vol. 55. №4. P. 888-892.
32. Russo J.A., Achilles S., DePineres T., Gil L. Controversies in family planning: postabortal
pelvic inflammatory disease // Contraception. 2012. Vol. 87 (4). P. 497-503.
33. Patel A., Rashid S., Godfrey E.M. et al. Prevalence of Chlamydia trachomatis and
Neisseria gonorrhoeae genital infections in a publicly funded pregnancy termination clinic:
empiric vs. indicated treatment? // Contraception. 2008. Vol. 78. P. 328-331.
34. Van Eyk N., Schalkwyk J. van. Infectious Diseases Committee. Antibiotic prophylaxis in
gynaecologic procedures // J. Obstet. Gynaecol. Can. 2012. Vol. 34 (4). P. 382-391.
35. Workowski K.A., Berman S. Centers for Disease Control and Prevention (CDC). Sexually
Transmitted Diseases Treatment Guidelines, 2010 // MMWR Recomm. Rep. 2010. Vol. 59
(RR-12). P. 1-10.
36. Sobel J.D. Bacterial vaginosis. Literature review current through. Jul 2013. — URL:
uptodate.com/contents/bacterial-vaginosis.
37. Фрипту В.Г. Сравнительная оценка эффективности вагинальных суппозиториев
метромикон-нео и нео-пенотран при лечении вагинитов смешанной этиологии //
Фармаприм. 2008. №2 (29). С. 55-59.
