Оценка клинической эффективности современного стероида алклометазона дипропионата (Афлодерма) в наружной терапии атопического дерматита у детей
СтатьиН.Г. Короткий, А.А.Тихомиров, Б.Н. Гамаюнов
Российский государственный медицинский университет, Российская детская клиническая больница Росздрава
Опубликовано в "Клиническая дерматология и венерология", №6, 2007, с.24-31
За последние годы предложено немало новых средств и методов лечения хронических воспалительных заболеваний кожи. При этом неотъемлемой частью комплексной терапии дерматозов у детей, не редко занимающей в ней ведущее место, является наружная терапия. Повышение эффективности местного лечения требует дифференцированного подхода и рационального использования наружных лекарственных средств и их различных форм с целью обеспечения положительного влияния на течение патологического кожного процесса. Одним из наиболее распространенных хронических рецидивирующих заболеваний кожи у детей является атопический дерматит (АД). Особенности анатомо-морфологического и функционального состояния кожи у детей с АД, относительно низкое соотношение площади кожи к массе тела у пациентов раннего возраста всегда требует от врача тщательного выбора лекарственных форм при назначении наружной терапии [1].
Лекарственные препараты при наружном применении оказывают не только местное, но и общее воздействие на организм в результате кожного всасывания. Исчезновение или уменьшение под влиянием наружной терапии клинических, в том числе субъективных проявлений кожного заболевания благоприятно сказывается на общем и психоэмоциональном состоянии ребенка. Традиционно для наружной терапии применяются такие лекарственные формы как примочки, взбалтываемые смеси, пасты, кремы, мази, компрессы, которые назначаются с учетом соответствующих стадий АД и переносимости их больными. Вышеперечисленные лекарственные формы, оказывая терапевтическое воздействие благодаря своим физическим свойствам, могут содержать различные действующие субстанции - антисептические или вяжущие средства (борная кислота, дерматол), кератопластические (осажденная сера, нафталан, метилурацил), редуцирующие (деготь, ихтиол), зудоуспокаивающие средства (ментол, димедрол) и т.д. [2-4].
При отсутствии эффекта от применения данных средств, а также при тяжелых формах АД возникает необходимость использования местных глюкокортикостероидов (ГКС). В настоящее время наружные ГКС занимают лидирующие позиции, благодаря их выраженному противовоспалительному, пpoтивoаллepгичecкoму, противозудному, антипролиферативному и другим положительным эффектам по сравнению с традиционными средствами наружной терапии [3,4].
Отношение к наружному использованию ГКС при лечении хронических дерматозов у детей всегда было неоднозначным. С одной стороны, применение галогенизированных, особенно фторированных кортикостероидных препаратов, нередко приводит к развитию нежелательных местных явлений, в частности, атрофии кожи и подкожно-жировой клетчатки, развитию телеангиэктазий, застойной гиперемии, стероидным акне, появлению участков растяжения кожи (стрий) и гипертрихозу, а также появлению системных эффектов. Перечисленные осложнения являются противопоказанием к широкому и длительному применению ряда кортикостероидных мазей в детской практике, и нередко приводит к возникновению «кортикофобии», как со стороны врача, так и со стороны пациентов.
С другой стороны, как показывает практика, применяемые в детской дерматологии наружные стероиды высокоэффективны и нередко занимают лидирующие позиции при выборе средств наружной терапии большинства дерматозов детского возраста. В этой связи, одной из главных задач ученых является достижение максимально низкого риска возникновения побочных эффектов при назначении наружных ГКС одновременно с повышением их терапевтической эффективности [3].
Суммируя многочисленные данные литературы можно выделить следующие основные механизмы действия наружных кортикостероидных препаратов [1,3,4]:
- повышение связывания гистамина и серотонина в очагах воспаления, активизация гистаминазы, что приводит к снижению зуда и экссудации;
- снижение чувствительности нервных окончаний к гистамину;
- ингибирующее влияние на процессы местной иммунной защиты;
- блокада фосфолипазы A2 и, как следствие, снижение синтеза лейкотриенов (противовоспалительный эффект);
- торможение синтеза нуклеиновых кислот, прежде всего ДНК;
- торможение пролиферации фибробластов и синтеза коллагена (развитие дермальной атрофии);
- задержка эпидермального митоза и стабилизация лизосом;
- снижение активности гиалуронидазы, что уменьшает проницаемость сосудистой стенки, нормализует тонус капилляров и снимает воспалительный отек;
- уменьшение количества растворимого и нерастворимого коллагена и мукополисахаридных фракций с воздействием на керотиноциты и фибробласты;
- выраженный ангиоспазм.
Введение в дерматологическую практику местных кортикостероидов относится к началу 50 годов прошлого столетия. Это время можно назвать революцией в лечении воспалительных заболеваний кожи. Первые препараты содержали естественный стероид - гидрокортизон, который широко используется в медицинской практике до настоящего времени. Однако гидрокортизон обладает слишком низкой силой для эффективного лечения тяжелых воспалительных поражений и требует длительного применения. Эти недостатки в некоторой степени компенсируются высокой безопасностью гидрокортизона. Именно поэтому во многих странах лекарственные средства, содержащие 1% или менее гидрокортизона, могут быть приобретены без рецепта врача.
Тот факт, что естественный гидрокортизон оказывал благоприятное лечебное действие на целый ряд заболеваний кожи, явилось стимулом для фармацевтических компаний для разработки синтетических дериватов естественной молекулы, которые обладали бы большей эффективностью. Для достижения этой цели молекула гидрокортизона видоизменялась самыми разнообразными способами. Вскоре было выяснено, что только три модификации молекулы существенно повышали эффективность подобных препаратов:
— добавление двойной связи между атомами углерода C1 и С2;
— эстерификация по С17 и/или по C21;
— галогенизация (особенно посредством добавления атомов хлора или фтора) к С6 и/или С9.
Последний путь приводил к наиболее существенному повышению эффективности лекарственных препаратов: некоторые вещества, полученные синтетическим путем, обладали на несколько порядков большей силой, чем естественный гидрокортизон. Однако вскоре стало известно, что галогенизация, придавая более выраженный противовоспалительный эффект, вызывает больший риск возникновения нежелательных побочных эффектов [1,3,4]. Фармакологические эффекты стероидов в коже обусловлены их взаимодействием со стероидными рецепторами, находящимися в цитоплазме клеток кожи. Выраженность этих эффектов определяется степенью связывания молекулы стероида с соответствующим рецептором, которая может повышаться посредством:
• эстерификации по С2, что приводит к увеличению растворимости молекулы стероида в жирах;
• галогенизации.
В результате связывания молекулы стероида рецепторами клеток кожи отмечаются следующие два основных эффекта:
• противовоспалительный эффект в результате торможения воспалительного каскада, и, как следствие, сужение сосудов кожи;
• антимитотический эффект вследствие торможения синтеза белков, приводящий к уменьшению пролиферации и торможению синтеза коллагена фибробластами.
Эти фармакологические эффекты неотделимы друг от друга. Стероиды, обладающие наиболее сильным противовоспалительным эффектом, являются также наиболее сильными ингибиторами синтеза белков. Таким образом, вопросы безопасности применения препаратов должны всегда стоять на первом месте, особенно если состояние больных требует продолжительного лечения. Идеальный наружный ГКС должен обладать сильным противовоспалительным действием, низкой системной биодоступностью, быстрым началом действия и минимальными местными побочными эффектами, другими словами иметь улучшенный индекс “риск-безопасность”.
На фармацевтическом рынке России представлен широкий спектр наружных ГКС, в связи с чем, выбор наиболее оптимального препарата подчас является сложной задачей. Однако определенный уровень знаний позволяет выбрать наиболее эффективные ГКС с минимальным риском развития побочных эффектов, которые в зависимости от формы выпуска препарата могут использоваться для лечения АД различной локализации с учетом стадии, периода и тяжести кожного патологического процесса. Всем этим требованиям в полной мере соответствует современный наружный ГКС препарат афлодерм (0,05% алклометазона дипропионат), выпускаемый фармацевтической компанией БЕЛУПО (Хорватия) [3-5].
Афлодерм - 0,05% алклометазона дипропионат, уникальный нефторированный наружный кортикостероид последнего поколения, не имеющий аналогов на фармацевтическом рынке России. Афлодерм не содержит атомов фтора (от присутствия которых зависит степень выраженности побочных эффектов местных кортикостероидных препаратов) и может применяться у детей, начиная с 6-месячного возраста. Алклометазона дипропионат - единственный наружный кортикостероид, содержащий один атом хлора в положении С7, а не в С6 или С9, что делает его более безопасным в сравнении с существующими кортикостероидами, которые имеют в своем составе атомы хлора [4].
Хотя афлодерм и относится к группе умеренно активных кортикостероидов, по эффективности он сопоставим с сильными кортикостероидами, а по безопасности применения - со слабыми кортикостероидами (гидрокортизоном). По активности он в 60 раз превосходит гидрокортизон, при том, что вероятность развития местных побочных эффектов у афлодерма в 10 раз меньше, чем у клобетазола пропионата, в 5 раз меньше, чем у триамцинолона ацетонида и в 4 раза меньше, чем у бетаметазона валерата.
При аппликации на интактную кожу в системный кровоток в течение 8 ч абсорбируется менее 3% алклометазона дипропионата. В открытом исследовании у 10 здоровых добровольцев, в течение 21 дня, каждое утро и вечером 30 г крема алклометазона дипропионата наносилось на 80% поверхности тела под окклюзионную повязку на 12 часов. Уровень кортизола плазмы, свободный кортизол и 17-гидроксистероид в моче в период исследования оставались в пределах нормы, т.е. не было отмечено угнетающего действия афлодерма на гипоталамо-гипофизарно-надпочечниковую систему, что убедительно свидетельствует о его высочайшей системной и местной безопасности [6].
Препарат обладает выраженным противовоспалительным, противозудным, иммуносупрессивным, сосудосуживающим и антипролиферативным действиями. Уменьшает проницаемость и изменяет структуру тканевых и клеточных мембран, уменьшает миграцию макрофагов и лимфоцитов в очаг воспаления, тормозит все фазы воспаления, блокирует высвобождение из сенсибилизированных тучных клеток и базофилов гистамина и других биологически активных веществ.
Противовоспалительное действие афлодерма является результатом снижения образования, высвобождения и активности медиаторов воспаления (кинины, гистамин, лизосомальные ферменты, простагландины и лейкотриены), инициирующих воспалительный процесс. Алклометазона дипропионат стимулирует стероидные рецепторы, индуцирует образование липокортинов, ингибирующих активность фосфолипазы A2, тормозит синтез арахидоновой кислоты. Обладая сосудосуживающим действием, афлодерм препятствует расширению кровеносных сосудов, их росту и пролиферации, а также уменьшает их проницаемость, что тормозит доступ экссудата в ткани, охваченные воспалительным процессом, и, тем самым, уменьшает отек и боль. Антипролиферативный эффект проявляется в уменьшении поверхности гиперплазированных тканей. Избирательное связывание активного вещества афлодерма с кортикостероидными рецепторами обеспечивает высокую местную эффективность, минимальное системное воздействие и возможность длительного применения данного препарата [5,7,8]. Афлодерм выпускается в двух лекарственных формах – в виде крема и мази в тубах по 20 и 40 грамм.
В 2002-2004 гг Duchkova и Haskova (госпиталь Мазарюк, Чешская республика) провели клиническое исследование, оценивающее влияние крема афлодерм на гидратацию кожи. В исследовании участвовали здоровые добровольцы (22 человека), пациенты с АД (23) и псориазом (25). Все они были пролечены кремом афлодерм, который наносился 2 раза в день в течение 4-х недель. Степень гидратации кожи измерялась путем корнеометрии 1 раз в неделю, всегда по утрам на протяжении всего периода лечения. Первое измерение было выполнено до первой аппликации крема афлодерм. Результаты этого исследования убедительно продемонстрировали выраженный увлажняющий эффект крема афлодерм. Так степень гидратации кожи у здоровых добровольцев увеличилась по сравнению с исходными величинами на 21%, у пациентов с АД на 35% и у больных псориазом на 53%.
Таким образом, крем афлодерм помимо выраженного противовоспалительного действия характеризуется прекрасными увлажняющими свойствами, что чрезвычайно важно для наружного лечения хронических воспалительных заболеваний, нередко сопровождающихся сухостью кожных покровов, и является препаратом первого выбора в арсенале врачей и пациентов.
Все вышеизложенное дало нам основание применить препарат афлодерм для наружного лечения более 100 детей с АД различной степени тяжести в возрасте от 1 года до 16 лет. Афлодерм крем использовали при остро воспалительном и подостровоспалительном процессах, нередко с явлениями сухости кожных покровов; мазь афлодерм - при хроническом воспалительном процессе с выраженной инфильтрацией, лихенизацией и сухостью кожи. Препарат наносили 2 раза в сутки, утром и вечером и в зависимости от степени тяжести заболевания применяли в течение 7-21 дней. Системная и местная терапия другими ГКС не проводилась. Все больные получали седатив-ную микстуру, внутрь 10% р-р сульфата магния, препараты кальция, антигистаминные средства, витаминотерапию.
Клиническая картина АД у больных с легкой степенью тяжести течения заболевания характеризовалась ограниченной площадью поражения кожных покровов. Патологический процесс локализовался в локтевых сгибах, подколенных ямках, периоральной области и был представлен слабо выраженной эритемой, единичными мелко папулезными элементами, экскориациями, серозными корками, умеренно выраженной сухостью кожи и мелко пластинчатым шелушением. Кроме этого отмечался незначительный зуд кожи и лихенификация в очагах поражения.
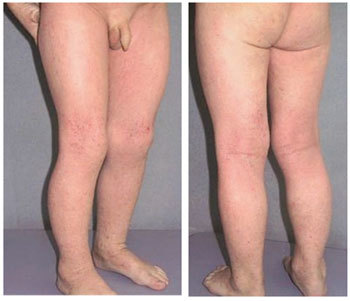
Рис.1-2. - Больной с АД, островоспалительный процесс с выраженной сухостью и шелушением кожи до применения крема Афлодерм
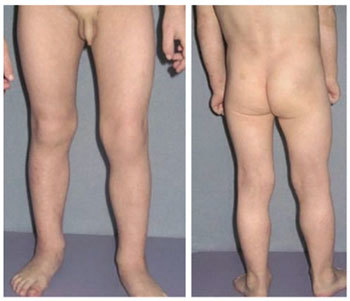
Рис.3-4. - Тот же больной после применения крема афлодерм
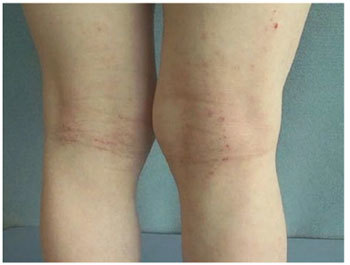
Рис. 5. - Больной с АД, подостро-воспалительный процесс с умеренно выраженной сухостью и шелушением кожи
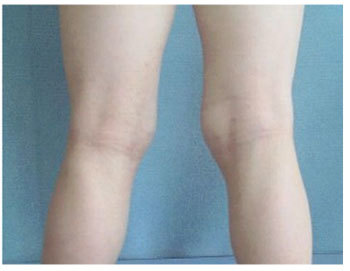
Рис.6. - Тот же больной после применения крема афлодерм
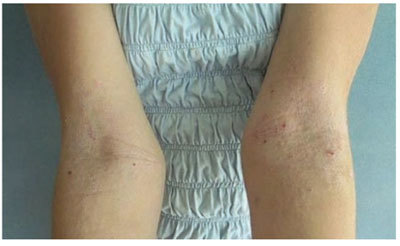
Рис.7. - Больная с АД, хронический воспалительный процесс с выраженной сухостью и шелушением кожи до применения мази афлодерм
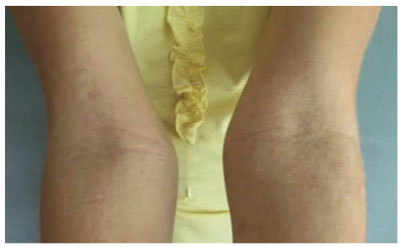
Рис.8. - Та же больная после применения мази Афлодерм
Среди преобладающих симптомов у пациентов со средней степенью тяжести заболевания мы выделили более интенсивный зуд кожи по сравнению с предыдущей группой больных, в ряде случаев сопровождающийся нарушением сна. Кожный процесс носил распространенный характер и локализовался на коже лица (периорбитальная и периоральная области), передней поверхности шеи, сгибательной и разгибательной поверхностях лучезапястных суставов, в локтевых сгибах и подколенных ямках. Отмечалась более выраженная острота воспалительной реакции: умеренно выраженные эритема и отек, папулезные элементы ярко - красного цвета, серозно-геморрагические корки, экскориации, трещины на фоне очагов лихенификации, выраженной сухости кожи и значительного шелушения, как в очагах АД, так и на не пораженной коже.
У больных с тяжелым течением заболевания патологический процесс локализовался на коже лица, передне - и заднебоковых поверхностей шеи, туловище, верхних и нижних конечностей, где на фоне значительно выраженной отечной эритемы отмечались многочисленные папулезные элементы, серозно-геморрагические корки, экскориации, трещины, выраженная лихенификация кожи. Практически все больные жаловались на интенсивный зуд кожи, сопровождающийся нарушением сна.
В процессе использования афлодерма у всех пациентов оценивали динамику основных клинических (эритема, отек, папулы/лихенификация) и субъективных симптомов заболевания (зуд, жжение, сухость) и других оценочных критериев.
Таблица. Клиническая эффективность применения препарата афлодерм в терапии детей с атопическим дерматитом
| Результат лечения | Степень тяжести заболевания | Всего детей | ||
|---|---|---|---|---|
| Легкая | Cредняя | Тяжелая | ||
| Клиническая ремиссия | 25 | 16 | 11 | 52 |
| Значительное улучшение | 4 | 19 | 17 | 40 |
| Улучшение | 2 | 7 | 9 | 18 |
| Без изменений | - | - | - | - |
| Ухудшение | - | - | - | - |
| Всего детей | 31 | 42 | 37 | 110 |
У большинства детей с АД зуд значительно уменьшался к 5-7-му дню терапии и полностью исчезал к 13-15 дням лечения при тяжелом течении заболевания. При легкой и средней степени тяжести течения АД, зуд значительно уменьшался или исчезал к 3 - 5 дням терапии. Эритема при легком течении АД исчезала или значительно уменьшалась к 3-5 дням, при среднетяжелом течении к 7-10, при тяжелом течении заболевания к 10-15 дням терапии. Шелушение исчезало при легком течении АД к 5-7 дням от начала терапии. У больных со среднетяжелым и тяжелым течением АД значительное уменьшение шелушения на фоне применения афлодерма отмечали к 10-му дню, которое полностью исчезало к 15-17 дням от начала терапии. Папулезная инфильтрация разрешалась при легком течении АД, к 7-10 дням, при сред-нетяжелом течении - к 12-14, при тяжелом течении АД к 16-21 дням терапии.
Таким образом, на динамику основных клинических проявлений АД у детей в первую неделю лечения повлияло значительное уменьшение или исчезновение эритемы и зуда. Разрешение папулезной инфильтрации, сухости кожных покровов и распространенности кожного процесса наблюдалось с первой по третью неделю терапии в зависимости от тяжести течения заболевания. Эффективность проведенной терапии оценивалась следующим образом:
• клиническая ремиссия - исчезновение всех клинических в т.ч. субъективных симптомов, по сравнению с исходным состоянием, и даже остаточных проявлений, таких как легкая эритема;
• значительное улучшение - разрешение большей части клинических симптомов по сравнению с исходным состоянием, с сохранением остаточных проявлений, таких как легкая эритема, отсутствие субъективных симптомов;
• улучшение - уменьшение большей части клинических симптомов по сравнению с исходным состоянием, сохраняются легкая эритема или единичные папулы, незначительная лихенификация, субъективных симптомов нет;
• без изменений - клинические симптомы не изменились по сравнению с исходным состоянием;
• ухудшение - ухудшение клинических симптомов по сравнению с исходным состоянием.
Результаты оценки клинической эффективности использования препарата афлодерм у детей с различной степенью тяжести АД представлены в таблице.
Обобщая результаты применения препарата афлодерм в терапии детей с АД различной степени тяжести, мы отметили клиническую ремиссию у 52 (47,3%), значительное улучшение у 40(36,4%), улучшение у 18 (16,3%) детей. Случаев отсутствия эффекта или ухудшения со стороны кожного процесса у пациентов с АД мы не наблюдали.
Семилетний опыт применения препарата аф-лодерм в наружной терапии АД более чем у 100 детей, дает основания утверждать, что наряду с выраженным антиаллергическим и противовоспалительным действием, афлодерм обладает прекрасным увлажняющим свойством (рис.1-8), он характеризуется отличной переносимостью, отсутствием осложнений и нежелательных побочных реакций, в связи с чем обоснованно и заслуженно пользуется популярностью как среди врачей, так и среди пациентов.
Таким образом, препарат афлодерм отвечает основным требованиям, предъявляемым к современным наружным стероидам – получение быстрого и выраженного терапевтического эффекта при минимуме побочных реакций и осложнений - что позволяет с успехом использовать его в наружной терапии АД у детей разных возрастных групп с различной степенью тяжести заболевания, Благодаря наличию различных лекарственных форм выпуска (крем, мазь), афлодерм может с успехом применяться при любой стадии болезни.
1.Короткий НГ, Таганов АВ.. Атопический дерматит у детей: принципы наружной терапии:Метод. пос. для педиатp. Сер.: аллерг. бол. М.: 2000; 51.
2.Короткий НГ, Таганов АВ. Лечение атопического дерматита у детей традиционными наружными средствами. Мед. сестра. 2001; 3: 27-30.
3.Короткий НГ, Таганов АВ, Тихомиров АА.. Современная наружная терапия дерматозов (с элементами физиотерапии). Тверь,2001; 528.
4.Короткий НГ, Тихомиров АА, Таганов АВ, Моисеенко АВ. Атопический дерматит у детей. Тверь, 2003; 238.
5.Макарова ИВ, Гайдук ИМ, Жиглинская ОВ. и др. Применение 0,05% крема алклометазона дипропионата в терапии атопического дерматита у детей раннего возраста. Вопр. совр. педиатр. 2004; 3:4: 20-22.
6.Thornfeldt C, Cornel R, Stoughton R. The effect of alclometasone dipropionate cream 0,05% on the hypothalamic-pituitary-adrenal axis of normal volunteers. J. Int. Med. Res. 1985; 13: 276-280.
7.Торопова НП, Черкасова ЛА, Платонова ИН. и др. Опыт применения препарата «Афло-дерм» (алклометазона дипропионат) в детской дерматологической практике. Росс. журн. кож. вен. бол. 2003;3: 39-40.
8.Курдина МИ. Опыт применения Афлодер-ма на лице у больных различными дерматозами. Там же; 41-44.
