Нефропротекция при сахарном диабете 2 типа: Уроки исследования ADVANCE
СтатьиОпубликовано в журнале:
Фарматека № 14 — 2011
С.В. Недогода
Кафедра терапии и эндокринологии ФУВ, Волгоградский государственный медицинский университет, Волгоград На базе результатов исследования ADVANCE рассматриваются вопросы медикаментозной нефропротекции у больных сахарным диабетом 2 типа (СД2), включая пациентов с неконтролируемой артериальной гипертензией. Обсуждаются возможности применения с этой целью фиксированной комбинации периндоприл + индапамид (Нолипрел А/Нолипрел А форте/Нолипрел А Би-форте), оказывающей лечебный эффект на всех этапах ренального континуума. Установлено, что улучшение контроля над артериальным давлением с помощью Нолипрела у больных СД2 приводит к реальному снижению смертности.
Ключевые слова: сахарный диабет 2 типа, диабетическая нефропатия, артериальная гипертензия, периндоприл, индапамид, Нолипрел
Based on the results of the ADVANCE study, the article considers the issues of medication nephroprotection in patients with type 2 diabetes mellitus (DM 2), including patients with uncontrolled arterial hypertension. Potentials for use of fixed combination of perindopril + indapmide (Noliprel A / Noliprel A Forte/ Noliprel A BI-Forte), which provides therapeutic effect at all stages of renal continuum, are discussed. It is established that improved control of blood pressure by Noliprel leads to a significant decrease in mortality in DM 2 patients.
Key words: type 2 diabetes mellitus, diabetic nephropathy, arterial hypertension, perindopril, indapamide, Noliprel
Тесная связь между контролем артериальной гипертензии (АГ), поражением органов мишеней и состоянием функции почек хорошо известна, равно как и взаимосвязь между сахарным диабетом (СД), почками и риском развития сердечно-сосудистых осложнений. Фактически наличие АГ и СД обусловливает до двух третей всех новых случаев терминальной почечной недостаточности.
Показано, что раннее выявление поражения почек при СД 2 типа (СД2) и проведение адекватной фармакологической нефропротекции как минимум отдаляют момент развития необратимых изменений почечной ткани и последующей почечной недостаточности, но в последнее время указывается на способность такой терапии улучшать прогноз за счет снижения частоты сердечно-сосудистых осложнений и смертности.
Еще одним важным аспектом рассматриваемой проблемы является осознание того факта, что препараты, используемые для нефропротекции при СД должны быть эффективными не только на начальном этапе кардиоренального континуума, когда имеются функциональные изменения без серьезного органического поражения, но и при наличии сформировавшихся выраженных органических изменений. В этом случае “идеальная” нефропротекция должна не только замедлять и приостанавливать патологический процесс в почках, но хотя бы у части пациентов способствовать его обратному развитию.
Всемирная организация здравоохранения рассматривает микроальбуминурию (МАУ) как один из компонентов метаболического синдрома (1999). Она является доказанным маркером развития системной эндотелиальной дисфункции, и на фоне МАУ, как правило, наблюдается более выраженное поражение органовмишеней (рис. 1). Кроме того, МАУ часто сопутствует таким факторам риска сердечно-сосудистых осложнений, как ожирение по центральному типу, инсулинорезистентность, повышение уровня С-реактивного белка, гиперурикемия, курение, дислипидемия, пожилой возраст.
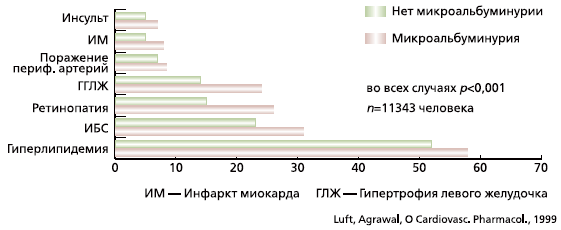
Рис. 1. Частота выявления сопутствующей патологии при АГ в зависимости от наличия микроальбуминурии
Считается, что МАУ имеет место приблизительно среди 30–40 % всех больных АГ. Причем это минимальное значение частоты ее встречаемости, т. к. в крупном международном исследовании i-SEARCH с участием около 22 тыс. пациентов МАУ отмечена среди 53–71 % больных, особенно часто наблюдаясь при неконтролируемой и резистентной АГ [9].
По данным различных исследований, МАУ встречается среди 10–40 % больных СД 1 типа и среди 15–40 % – СД2. Результаты эпидемиологических исследований [3, 9] показали, что в целом частота МАУ СД составляет около 33 %, незначительно возрастая на фоне сопутствующей АГ (до 35 %) и при наличии макро- и/или микрососудистых осложнений (до 38–39 %). По данным исследования UKPDS, при СД риск МАУ прогрессивно возрастает с увеличением длительности заболевания – приблизительно на 1–2 % в год. При сочетании различных факторов риска вероятность нарушения функции почек еще больше возрастает.
В последнее время активно обсуждается прогностическая значимость МАУ. Не вдаваясь в полемику по данному вопросу, необходимо констатировать, что результаты многочисленных клинических и эпидемиологических исследований доказывают значение МАУ как одного из важнейших независимых факторов риска сердечно-сосудистых и цереброваскулярных осложнений, а также смерти от них [1, 5]. Для подтверждения достаточно привести результаты ряда крупных исследований: LIFE – повышение в моче соотношения альбумин/креатинин прямо коррелировало с возрастанием риска развития серьезных сердечнососудистых событий (кардиоваскулярная смерть, нефатальные инсульт и инфаркт миокарда), а также выраженностью гипертрофии левого желудочка;
HOPE – у пациентов с АГ из группы высокого риска повышение соотношения альбумин/креатинин в моче на каждые 0,4 мг/ммоль выше нормы увеличивало риск серьезных сердечнососудистых событий на 5,9 %;
DIABHYCAR (the type 2 DIABetes, HYpertension, microalbuminuria or proteinuria, CArdiovascular events and Ramipril study) – при наличии МАУ повышался риск развития сердечной недостаточности;
EPIC-Norfolk (European Prospective Investigation into Cancer in Norfolk study) – при наличии МАУ достоверно повышался риск инсульта;
Copenhagen City Heart-3 – риск ишемической болезни сердца и сердечно-сосудистой смерти достоверно повышался при уровне альбуминурии > 4,8 мкг/мин (общепринятый нижний порог для верификации МАУ – 20 мкг/мин).
Для снижения МАУ и эффективной нефропротекции в первую очередь необходимо достижение целевых значений артериального давления (АД; рис. 2). Интересно, что на фоне уменьшения МАУ может иметь место дополнительное снижение систолического АД [6]. При этом необходимо особо отметить, что для нефропротекции ключевое значение имеют антигипертензивные препараты, подавляющие активность ренин-ангиотензинальдостероновой системы (ингибиторы АПФ, блокаторы рецепторов ангиотензина II). Доказано что их нефропротективный эффект обусловлен не только снижением АД, но и другими, в т. ч. плейотропными, эффектами этих препаратов [2, 8, 10]. В последние годы стало очевидным, что для эффективпациентов с СД2, требуется использование комбинации антигипертензивных препаратов. Во-первых, как известно, именно комбинированная антигипертензивная терапия позволяет достигать целевого АД у подавляющего большинства пациентов; во-вторых, комбинация антигипертензивных препаратов способна обеспечивать более выраженное защитное действие в отношении почек и сердца.
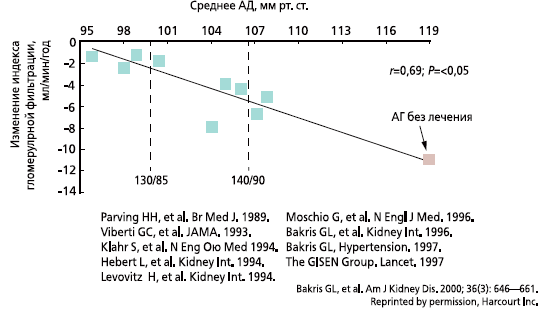
Рис. 2. Мета-анализ: зависимость между средним АД и ухудшением фукнции почек у больных с диабетической и недиабетической нефропатией
Сегодня серьезная доказательная база существует лишь в отношении некоторых фиксированных комбинаций антигипертензивных средств. Это, в частности, комбинации периндоприл + индапамид (препарат Нолипрел; исследования ADVANCE и PREMIER) и трандалоприл + верапамил SR (исследование BENEDICT). При этом необходимо подчеркнуть, что комбинация периндоприл + индапамид является единственной эффективной на всех этапах ренального континуума (табл. 1). Это объясняется тем, что она практически полностью устраняет дисбаланс между повышением афферентного и эфферентного давления в почке при АГ и СД.
Таблица 1. Нефропротективное действие комбинации периндоприл + индапамид (Нолипрел А форте) при СД
| Прогрессирование повреждения почек | Уменьшение риска на фоне лечения Нолипрелом А форте | ||||||||||||||||||||||||||||||||||||||||||
| Все почечные осложнения | -21 % (р | Прогрессирование альбуминурии на 1-й стадии и более | -22 % (p | Новые случаи МАУ | -21 % (р | Новые случаи макроальбуминурии | -31 % (р | Обратное развитие нефропатии | Улучшение прогноза на фоне лечения Нолипрелом А форте | ||||||||||||||||||||||||||||||||||
| Уменьшение альбуминурии на 1-й стадии и более | +16 % (р | Восстановление почечной функции | +15 % (р Сегодня благодаря исследованию ADVANCE применение больными СД2 фиксированной комбинации периндоприла с индапамидом стало единственным вариантом лечения, который не только оказывает нефропротективное действие, но и снижает смертность при этой патологии (табл. 2). В это исследование были включены 11 140 больных СД2 с высоким риском осложнений. В ходе длительного наблюдения риск главных макро- и микрососудистых событий снизился на 9 %. Таблица 2. Влияние различных вариантов лечения почечные осложнения и смертность пациентов с СД
Лечение Нолипрелом уменьшило среди больных СД2 риск смерти от всех причин на 14 %, а сердечнососудистой смерти – на 18 %. В группе активного лечения риск развития коронарных осложнений снизился на 14 %, а почечных осложнений – на 21 %. Итак, улучшение контроля над АД с помощью Нолипрела у больных СД2 приводит к реальному снижению смертности. В дальнейшем были проанализированы результаты воздействия Нолипрела на АД у больных СД2 в исследовании ADVANCE на риск развития почечных осложнений. Терапия Нолипрелом обеспечивала нефропротекцию у всех больных СД2, даже у пациентов с исходным АД меньше 120/70 мм рт. ст. В 2010 г. были представлены новые данные по оценке влияния комбинации периндоприл/индапамид на риск развития сердечно-сосудистых и почечных осложнений у больных СД2 и хроническим почечным заболеванием. Из 10 640 пациентов, включенных в ADVANCE, у 6125 не было нарушений почечной функции, у 2482 были I–II стадии и у 2033 – III стадия ХПЗ. Польза от присоединения Нолипрела к лечению больных СД2 в виде снижения риска сердечнососудистых, почечных осложнений и смертности отмечена у всех пациентов независимо от исходного состояния почечной функции. Наиболее последовательно преимущества комбинации периндоприл + индапамид как средства нефропротекции отстаивали L. Ruilope и J. Segura [7]. На ежегодном конгрессе Европейского общества по АГ в июне 2010 г. ими был представлен доклад, в котором анализировались результаты наиболее крупных клинических исследований по изучению влияния препаратов, воздействующих на активность ренин-ангиотензиновой системы, на почечные исходы у больных СД2. Было показано (табл. 2), что только фиксированная комбинация периндоприл + индапамид (исследование ADVANCE) не только снизила риск прогрессирования почечной недостаточности, но и улучшила выживаемость больных. Дальнейший анализ результатов исследования ADVANCE выявил ряд интересных тенденций. Так, через 3 месяца лечения практически все пациенты перешли с комбинации периндоприл 2 мг + индапамид 0,625 мг на комбинацию периндоприл 4 мг + индапамид 1,25 мг, а к концу периода наблюдения к этой терапии 74 % больных были добавлены другие антигипертензивные препараты (β-адреноблокаторы – 31 %, антагонисты кальция – 32 %, антагонисты рецепторов ангиотензина II – 10 %, другие антигипертензивные средства – 27 %). То есть большинство пациентов либо получали “тройную” терапию, либо доза периндоприла была “двойной”. Несколько позже появились результаты анализа [4] исследований PIXEL и PREMIER (PREterax in albuMInuria rEgRession), которые показали необходимость использования комбинации периндоприл + индапамид в максимальной терапевтической дозе практически у трети пациентов. В связи c этим появление препарата Нолипрел А Би-форте, представляющего собой фиксированную комбинацию периндоприла 10,0 мг и индапамида 2,5 мг, упрощает достижение эффективной нефропротекции в условиях реальной клинической практики у пациентов с СД2 при неконтролируемой АГ. Это осуществляется путем замены 2 таблеток Нолипрела А форте на 1 таблетку Нолипрела А Би-форте. Литература
Информация об авторе: |
