Применение препарата пидотимод при острой респираторной инфекции у часто болеющих детей
Статьи Опубликовано в издании:Вопросы современной педиатрии, 2009, Том 8, N2 Харламова Ф.С., Учайкин В.Ф., Кладова О.В., Бевза С.Л.
Российский государственный медицинский университет, Москва. В исследовании изучалась эффективность и безопасность добавления препарата пидотимод (Имунорикс) к комплексной терапии детей с острой респираторной инфекцией (ОРИ). Показано, что в результате 2.недельной терапии в группе пидотимода (n = 30) была отмечена меньшая, по сравнению с группой контроля (n = 30), продолжительность лихорадки и симптомов интоксикации, а также симптомов ларинготрахеобронхита. Кроме того, у детей этой группы трансформация сухого кашля во влажный, а также уменьшение выраженности последнего, происходили быстрее. Указанные изменения у детей, получавших пидотимод, сопровождались положительной динамикой показателей высеваемости патогенетически значимых микроорганизмов. Эффективность терапии препаратом пидотимод 73% врачей оценили как "хорошая" (67% в группе контроля). При этом не было зафиксировано ни одного случая побочного эффекта, связанного с назначением препарата. Через 6 мес после окончания терапии в группе пидотимода частота повторных случаев ОРИ была втрое ниже, чем в группе контроля. Все случаи ОРИ при этом протекали в легкой форме без рецидива стеноза гортани. Ключевые слова: часто болеющие дети, острые респираторные инфекции, лечение, профилактика, пидотимод. Острые респираторные инфекции (ОРИ) являются наиболее распространенными в детском возрасте. Их доля с учетом случаев гриппа составляет около 90% в структуре всей заболеваемости у детей, около 70% этих инфекций поражают верхние дыхательные пути, область среднего уха, придаточные пазухи носа, лимфоэпителиальное кольцо. В результате ОРИ формируется гиперсенсибилизация, часто развиваются аллергические заболевания. У детей с предрасположенностью к атопии ОРИ нередко сопровождаются обструкцией дыхательных путей (крупом, обструктивным бронхитом). Более того, около 20-30% случаев ОРИ осложняются пневмонией либо обострением хронических заболеваний легких, сердечно-сосудистой системы, почек. Часто болеющие дети подвергаются повторному заражению дыхательных путей 6-8 раз в год и более или в эпидемический период (октябрь-март) - чаще одного раза в месяц, в то время как нормой в детском возрасте считается 4-6 эпизодов инфицирования дыхательных путей в год. В отечественной педиатрии разработаны и применяются четкие критерии, позволяющие включить ребенка в диспансерную группу часто болеющих детей [1]. Доля таких детей в детской популяции колеблется в широком диапазоне: от 15 до 75%, оставаясь все последние годы без изменений. Эти дети часто страдают наследственными, врожденными или хроническими заболеваниями, способствующими рецидивирующему течению респираторных инфекций. Частые и особенно тяжело протекающие ОРИ снижают функциональную активность иммунной системы, важной составляющей которой является фагоцитарная система. Кроме того, причины частой заболеваемости детей респираторными инфекциями в значительной степени обусловлены изменением иммунного реагирования организма на фоне неблагоприятных анте. и перинатальных факторов; предрасположенностью к Th2-типу иммунного ответа - аллергии; большим числом контактов в начале посещения детских дошкольных учреждений; широкими контактами внутри семьи и семьи с окружающими; низкой санитарной культурой и дефектами ухода за детьми; плохими социально-бытовыми условиями [2]. Высокий риск развития и тяжелого течения ОРИ часто связывают с физиологической незрелостью иммунной системы ребенка, которая может проявляться различными вариантами временного иммунодефицита - такими как:
- количественный и функциональный дефицит Т лимфоцитов;
- дефицит цитокинов;
- временный дефицит иммуноглобулинов (Ig) классов А, М и G;
- нарушение хемотаксиса иммунокомпетентных клеток и др.
Пациенты и методы В исследовании участвовали 60 детей в возрасте от 3 до 14 лет с острым (или рецидивирующим) обструктивным ларинготрахеобронхитом, развившемся на фоне ОРИ. Критерием включения часто болеющих детей в исследование было наличие симптомов ОРИ в среднетяжелой и тяжелой формах при отсутствии в схемах терапии детей в течение 3 мес иммуномодулирующих препаратов. Пациенты были рандомизированы в группы по 30 человек в каждой. Часто болеющие дети основной группы получали в составе комплексной терапии респираторной инфекции пидотимод (Имунорикс, Солвей Фарма, Франция) в растворе по 7 мл (400 мг) внутрь вне приема пищи 2 раза в день ежедневно в течение 15 дней с последующей оценкой профилактического эффекта. Больные контрольной группы получали только средства рекомендованной комплексной терапии.
В основной группе у 20 (67%) больных на фоне ОРИ развился стенозирующий ларинготрахеит (бронхит), из них у 13 отмечалась I степень стеноза гортани, у 7 - II степень; рецидивирующий круп был зафиксирован в 6 случаях. Пидотимод в сочетании с антибиотикотерапией получали 6 больных. В группе контроля стенозирующий ларинготрахеит (бронхит) был диагностирован у 23 (77%) больных, из них у 14 была установлена I степень, у 9 - II степень стеноза гортани; рецидивы крупа возникали у 8 детей. Антибиотикотерапию получали 6 больных. Обе группы больных были сопоставимы по полу, возрасту и основным клиническим проявлениям заболевания. Из сопутствующей патологии у детей основной группы хронический тонзиллит был диагностирован у 10 (у 8 - в группе контроля); острый средний отит - у 5 (7); гайморит - у 3 (3); инфекция мочевых путей - у 2 (3); аденоиды - у 7 (5); персистирующая герпесвирусная инфекция - у 5 (3) детей соответственно. В обеих группах было по 1 больному (всего 4 в каждой), страдавших атопическим дерматитом, дисбиозом кишечника, панкреатопатией и тимомегалией. Эффективность лечения в обеих группах оценивалась в баллах и определялась в соответствии с динамикой таких критериев, как: скорость исчезновения/уменьшения лихорадки, интоксикации, катаральных явлений в ротоглотке, симптомов ринита, ларингита, стеноза гортани, сухого кашля и появления продукции мокроты; длительность приема антибиотика, нормализация лабораторных показателей периферической крови и мочевого осадка, а также нормализация микробиоценоза ротоглотки. Эффективность оценивали как "хорошую" при значительном клиническом улучшении общего состояния, исчезновении симптомов интоксикации и катаральных явлений в течение 2-3 дней лечения с последующим полным исчезновением признаков и симптомов инфекции, "удовлетворительную" - при улучшении общего состояния и исчезновении симптомов респираторного заболевания в течение первых 3.х дней с неполным исчезновением признаков инфекции в течение периода последующего наблюдения, но без необходимости дополнительного лечения антибиотиками. Отсутствие эффекта "неудовлетворительный результат" - определяли при усилении симптомов инфекции спустя как минимум 72 ч лечения. Контроль лабораторных показателей, клинические анализы крови и мочи, исследование биоценоза ротоглотки проводились до и после (спустя 15 дней) назначения препарата пидотимод и в те же сроки в группе контроля. По показаниям проводились рентгенологическое исследование органов грудной клетки и отоскопия. Профилактическая эффективность препарата пидотимод оценивалась после его отмены в течение последующих 6 мес (с июля по декабрь 2008 г.), катамнестического амбулаторного наблюдения за пациентами основной и контрольной групп. Учитывались эпизоды повторных ОРИ и случаи рецидива крупа. Статистический анализ результатов исследования проведен с помощью пакета программ, интегрированных в Microsoft Excel 2003. Количественные признаки представлены в виде среднего арифметического значения ± стандартное отклонение, дискретные признаки - в виде частот (процент наблюдений к общему числу обследованных). Сравнение количественных признаков осуществлялось с помощью t-критерия Стьюдента для независимых выборок, дискретных признаков - критерия Пирсона χ2. Полученные результаты рассматривали как статистически значимые при pРезультаты исследования и их обсуждение Больные поступали в первые 2 сут от начала заболевания (большинство с симптомами стеноза гортани), с лихорадкой, интоксикацией (умеренной или выраженной), все с выраженной гиперемией и отеком миндалин. Дети старшего возраста жаловались на боль в горле при глотании и/или в ухе при наличии острого среднего отита. У всех детей отмечался сухой грубый кашель без (или со слабой) продукции мокроты. Продолжительность основных симптомов заболевания представлена в табл. 1. Показано, что в группе детей, получавших пидотимод, статистически значимо уменьшилась продолжительность лихорадки и симптомов интоксикации, отмечавшихся к 5-м суткам терапии еще у 14% детей группы контроля (ни у одного ребенка основной группы) (рис. 1).
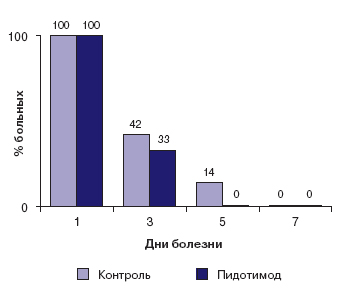
Рис. 1. Динамика симптомов лихорадки и интоксикации при ОРИ на фоне терапии
Таблица 1. Продолжительность симптомов ОРИ у детей, включенных в исследование
| Возраст | Продолжительность, дни | |
| Группа контроля, n = 30 |
Основная группа, n = 30 |
|
| Лихорадка и интоксикация | 2,4 ± 0,1 | 1,6 ± 0,2* |
| Катаральные явления в ротоглотке | 3,7 ± 0,1 | 3,1 ± 0,3 |
| Ларинготрахеобронхит | 4,7 ± 0,4 | 2,9 ± 0,2* |
| Стеноз гортани | 1,7 ± 0,1 | 1,5 ± 0,4 |
| Начало продукции мокроты (дни от начала терапии) | 2,6 ± 0,3 | 2,4 ± 0,1 |
| Признаки ринита | 3,8 ± 0,2 | 3,2 ± 0,1 |
р
В группе детей, получавших пидотимод, отмечено также и сокращение продолжительности симптомов ларинготрахеобронхита при том, что к 3 суткам признаки стеноза гортани сохранялись у 13% детей этой группы (17% в группе контроля; рис. 2). Полностью купировать симптомы стеноза гортани у всех детей удалось к 4 суткам в основной группе и к 5 сутам терапии - в контрольной группе. Катаральные явления в ротоглотке у детей основной группы были менее продолжительными, к концу лечения (к 7.м суткам) они отмечались лишь у каждого третьего пациента этой группы и у половины больных группы контроля (рис. 3). Динамика кашля представлена на рисунке 4. Очевидно, что в основной группе трансформация сухого кашля во влажный, а также уменьшение выраженности последнего происходила быстрее.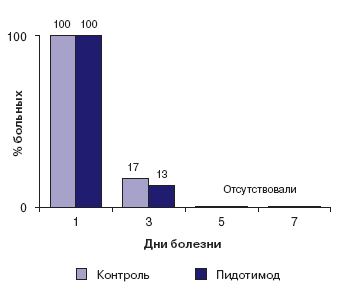
Рис. 2. Динамика симптомов стеноза гортани при ОРИ со стенозирующим ларинготрахеобронхитом на фоне терапии
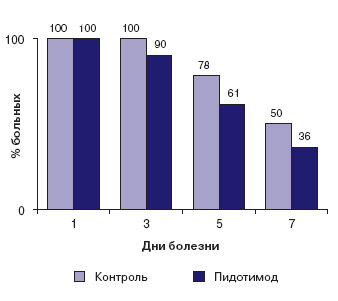
Рис. 3. Динамика признаков катарального воспаления слизистой оболочки ротоглотки при ОРИ на фоне терапии
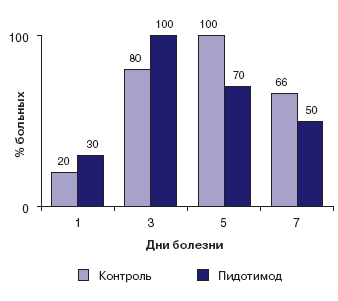
Рис. 4. Динамика кашля с продукцией мокроты при ОРИ со стенозирующим ларинготрахеобронхитом на фоне терапии
| Симптомы | Продолжительность, дни | |
| Группа контроля, n = 6 |
Основная группа, n = 6 |
|
| Лихорадка и интоксикация | 4,3 ± 0,9 | 4,1 ± 0,2 |
| Катаральные явления в ротоглотке | 5,2 ± 0,4 | 4,3 ± 0,6 |
| Ларинготрахеобронхит | 6,8 ± 0,5 | 5,6 ± 0,3* |
| Стеноз гортани | 2,2 ± 0,4 | 2,0 ± 0,7 |
| Начало продукции мокроты (дни от начала терапии) | 5,2 ± 0,4 | 2,4 ± 0,1** |
| Признаки ринита | 5,5 ± 0,8 | 4,8 ± 0,8 |
* р ** р
У детей основной и контрольной групп на фоне терапии не было выявлено достоверных различий в показателях периферической крови и клинического анализа мочи, что говорит о безопасности иммуномодулятора. Результаты исследования свидетельствовали об исходном дисбиозе ротоглотки у больных обеих групп. Дисбиоз был обусловлен колонизацией слизистой ротоглотки преимущественно золотистым стафилококком - у 29 (48%) детей, β-гемолитическим стрептококком - у 22 (37%), лактозонегативной Escherichia coli - у 11 (18%), Klebsiella pneumoniae - у 5 (8%), Enterococcus - у 3 (5%), Candida albicans - у 20 (33%) больных, включенных в исследование (табл. 3). Таблица 3. Высеваемость микрофлоры в посевах слизи из ротоглотки детей, включенных в исследование| Микроорганизмы | Норма, КОЕ/мл | До лечения, КОЕ/мл | Группа контроля, абс. | Основная группа, абс. | ||
| до лечения | после лечения | до лечения | после лечения | |||
| S. aureus | 2 | 8 | 12 | 12 | 17 | 11 |
| S. haemolyticus | 3-104 | 8 | 10 | 9 | 12 | 3 |
| E. coli | 2 | 8 | 5 | 7 | 6 | 2 |
| P. aeruginosa | 2 | 6 | - | - | 2 | 1 |
| K. pneumoniae | 2 | 7 | 3 | 2 | 2 | 1 |
| C. albicans | 2 | 8 | 10 | 10 | 10 | 4 |
| Enterococcus | 2 | 8 | 1 | 5 | 2 | 1 |
| Микроорганизмы | Норма, КОЕ/мл | До лечения, КОЕ/мл | Группа контроля, абс. | Основная группа, абс. | ||
| до лечения | после лечения | до лечения | после лечения | |||
| S. aureus | 2 | 8 | 5 | 3 | 3 | 2 |
| S. haemolyticus | 3-104 | 8 | 5 | 3 | 6 | 1 |
| E. coli | 2 | 8 | 1 | 2 | 3 | - |
| P. aeruginosa | 2 | 6 | - | - | - | - |
| K. pneumoniae | 2 | 7 | 1 | 1 | - | - |
| C. albicans | 2 | 8 | 3 | 3 | 4 | 1 |
| Enterococcus | 2 | 8 | - | - | - | - |
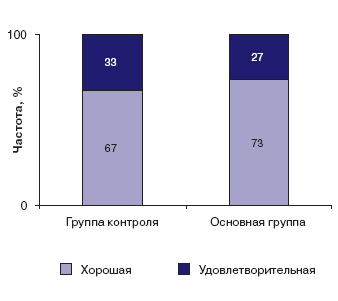
Рис. 5. Клиническая оценка эффективности терапии в сравниваемых группах

Рис. 6. Заболеваемость ОРИ и случаи возникновения стеноза гортани в сравниваемых группах через 6 мес после проведенного лечения
Список литературы
- Острые респираторные заболевания у детей: лечение и профилактика: Научно-практическая программа Союза педиатров России, 2002. - С. 73.
- Альбицкий В.Ю., Баранов А.А. Часто болеющие дети. Клинико-социальные аспекты. Пути оздоровления. - Саратов, 1986. - С. 45.
- Кладова О.В., Харламова Ф.С., Легкова Т.П. и др. Клинико-патогенетическое обоснование применения ИРС 19 у детей с бронхолегочными заболеваниями // Вопросы совр педиатрии. - 2002. - Т. 1, N 3. - С. 36-39.
- Careddu P., Mei V., Venturoli V., Corsini A. Pidotimod in the treatment of recurrent respiratory infections in paediatric patients // Arzneimittelforschung. - 1994. - V. 44, N 12. - Р. 1485-1489.
- Illeni M.T., Bombelli G., Poli A., Pattarino P.L. NK cell cytotoxic activity induced by a synthetic immunostimulant (pidotimod): an in vitro study // J. Chemother. - 1991. - V. 3 (Supl. 3). - Р. 157-159.
- Сенцова Т.Б., Ревякина В.А. Современные иммуномодуляторы в практике педиатра. - М.: Materia medica, 2006. - С. 41-43.
- Burgio G.R., Marseglia G.L., Severi F. et al. Immunoactivation by pidotimod in children with recurrent respiratory infections // Arzneimittelforschung. - 1994. - V. 44, N 12. - Р. 1525-1529.
- Pugliese A. et al. Evaluation of the effect of pidotimod on the in vitro production of interferons // Int. J. Immunotherapy. - 1995. - N 11. - Р. 71-76.
- Pugliese A. et al. Evaluation of the effect of pidotimod on the immune system // Int. J. Immunotherapy. - 1992. - V. 3. - Р. 212-219.
- Caramia G., Clemente E., Solli R. et al. Efficacy and safety of pidotimod in the treatment of recurrent respiratory infections in children // Arzneimittelforschung. - 1994. - V. 44, N 12. - P. 1480-1484.
- De Martino P. and the multicentre study group. Pidotimod: efficacy and tolerability profile in the prophylaxis of RRI // 3rd International Conference on Pediatric Otorhinolaryngology. - 1993 (Abstracts).


