Синдром удлиненного интервала QT и псевдогипопаратиреоз. клинический случай
СтатьиОпубликовано в журнале: «ПРАКТИКА ПЕДИАТРА»; июнь; 2016; стр. 40-48.
Е.В. Тозлиян, педиатр-эндокринолог, генетик, к. м. н.; В.В. Березницкая, врач - детский кардиолог, к. м. н.; А.Ю. Якшина, врач - детский кардиолог
Обособленное структурное подразделение «Научно-исследовательский клинический институт педиатрии» ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
Ключевые слова: дети, синдром удлиненного интервала QT, псевдогипопаратиреоз, наследственная остеодистрофия Олбрайта, гипокальциемия, диагностика, резистентность к паратиреоидному гормону.
Keywords: children, syndrome long QT interval, pseudohypoparathyroidism, Albright hereditary osteodystrophy, hypocalcemia, diagnostics, parathyroid hormone resistance.
В течение последних двух десятилетий значительный прогресс в понимании электрофизиологических основ внезапной аритмической смерти во многом был обусловлен интенсивными исследованиями синдрома удлиненного интервала QT (СУИQT), при котором имеется высокий риск внезапной сердечной смерти (ВСС) вследствие развития жизнеугрожающих желудочковых аритмий. Для клиницистов, помимо выявления синдрома удлиненного интервала QT, чрезвычайно важным является установить первичную или вторичную его формы. От этого полностью зависит выбор тактики лечения и прогноз.
Синдром удлиненного интервала QT (СУИQT) встречается в виде первичного (наследственные синдромы Романо-Уорда, Джервелла-Ланге-Нильсена и спорадические формы, обусловленные специфическими генными мутациями) и вторичного вариантов. Наследственный СУИQT является заболеванием с высоким риском внезапной сердечной смерти, относится к генетически детерминированным первичным электрическим заболеваниям сердца и характеризуется удлинением интервала QT на электрокардиограмме (ЭКГ) покоя, приступами потери сознания вследствие развития тахикардии типа «пируэт» и фибрилляции желудочков. С момента открытия синдрома до настоящего времени это заболевание служит уникальной моделью для изучения патофизиологии, электрокардиографических проявлений, молекулярногенетических механизмов, а также факторов риска внезапной аритмической смерти [1, 2].
Синдром удлиненного интервала QT выявляется в европейской и американской популяциях с частотой до 1:2500-1:7000 при пенетрантности 90%. При этом распространенность молекулярно-генетических вариантов синдрома Романо-Уорда различна. Описаны семьи со спорадическими случаями СУИQT и очень низкой пенетрантностью, составляющие около 25% (LQT4-LQT12). Большинство пациентов с установленным молекулярно-генетическим диагнозом относятся к первым трем вариантам синдрома, соответственно, LQT1 выявляется в 50-55% случаев, LQT2 - в 35-45%, LQT3 - в 5-15% [2, 3].
В патогенезе СУИQT ведущая роль принадлежит генам, кодирующим трансмембранные ион-селективные каналы. При СУИQT мутации найдены в генах, кодирующих калиевые, натриевые и кальциевые каналы, мембранные переносчики, а также некоторые структурные белки, локализованные на 3, 4, 7, 11, 12, 17, 20 и 21-й хромосомах. Большинство идентифицированных генетических дефектов при СУИQT относится к мутациям, нарушающим структуру кодируемого белка [3, 4]. Молекулярно-генетические варианты синдрома и характер мутаций определяют электрофизиологические особенности и клиническую картину заболевания. В то же время, несмотря на различия, все варианты СУИQT объединяются общими фенотипическими проявлениями. Клиническая диагностика синдрома основана на критериях, впервые предложенных в 1985 г. P. Schwartz и уточненных автором в 1993 г. [5]. Диагноз складывается из: 1) анализа предшествующей истории обмороков («синкопальных эпизодов»); 2) семейного анамнеза, включающего случаи ВСС в возрасте моложе 40 лет; 3) оценки специфических изменений ЭКГ [6, 7, 8].
Для клиницистов, помимо выявления синдрома удлиненного интервала QT, чрезвычайно важным является установить первичную или вторичную его формы. От этого полностью зависит выбор тактики лечения и прогноз.
Вторичный синдром удлиненного интервала QT провоцируется приемом лекарственных препаратов, может развиваться на фоне низкокалорийной диеты, при психогенных заболеваниях, заболеваниях ЦНС, при нарушениях метаболизма, вегетативной дисфункции, вследствие нарушения функции паращитовидных желез, электролитных нарушениях, токсического действия лекарственных препаратов [8].
Лечение больных с синкопальной формой СУИQT заключается в исключении специфических для каждого пациента факторов, которые запускают угрожающие жизни аритмии, исключении препаратов, способных удлинять интервал QT, а также в обязательном длительном (пожизненном) приеме антиаритмических препаратов. Препаратами первого ряда являются бета-адреноблокаторы -пропранолол, атенолол, метопролол или надолол [8].
В представленной статье нами описано клиническое наблюдение вторичного синдрома удлиненного интервала QT вследствие гипокальциемии как проявление наследственного синдрома - псевдогипопаратиреоза (наследственной остеодистрофии Олбрайта). В литературе описаны клинические случаи синкопальных состояний вследствие синдрома удлиненного интервала QT на фоне гипокальциемии. В основе патогенеза - асинхронность реполяризации различных участков миокарда желудочков и, как следствие, увеличение ее общей продолжительности. Электрокардиографическим признаком асинхронной реполяризации миокарда (на фоне гипокальциемии) является удлинение интервала QT [9, 10, 11, 12].
Нормальное протекание всех жизненно важных процессов в организме обеспечивается за счет поддержания кальция в плазме крови в очень узких пределах, контролируемых паратгормоном (ПГТ) и метаболитами витамина D. Мишенями этих гормонов являются: костная ткань, почки и тонкая кишка. Концентрации кальция и фосфора во внеклеточной жидкости взаимосвязаны: любые изменения одного из ионов приводят к обратному изменению концентрации другого. Регуляция фосфорно-кальциевого обмена и эффекты паратиреоидного гормона представлены на схеме 1. Клинические проявления гипокальциемии:
Схема 1
Регуляция фосфорно-кальциевого обмена (эффекты паратиреоидного гормона)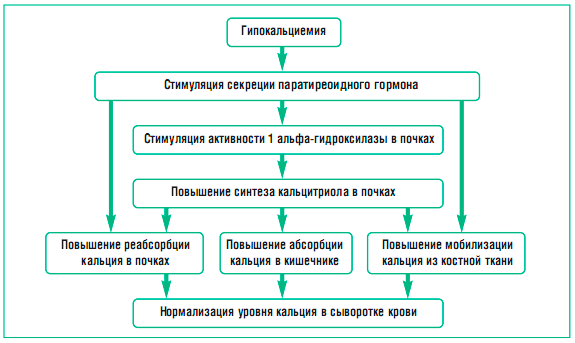
Одним из редких генетических синдромов, при котором гипокальциемия - патогномоничный симптом, является псевдогипопаратиреоз.
Псевдогипопаратиреоз (ПГПТ) (греч. pseudes ложный + гипопаратиреоз; синоним: наследственная остеодистрофия Олбрайта; OMIM 103580) - редкий наследственный синдром, имитирующий гипопаратиреоз и характеризующийся тканевой резистентностью к ПГТ, нарушением обмена кальция и фосфора; увеличением функции околощитовидных желез; низкорослостью и скелетными аномалиями.
Заболевание описано впервые швейцарским терапевтом Eric Martin с соавторами в 1940 г. и американским врачом-эндокринологом Fuller Albright с соавторами в 1942 г. Характеризуется аутосомно-доминантным типом наследования [13].
Частота заболевания 1:100 000-1 000 000. В литературе описано около 300 наблюдений. Соотношение женщин/мужчин - 2:1. Заболевание диагностируется чаще в возрасте 5-10 лет. Клинические формы: тип 1А, тип 1В, тип 1С, тип 2.
Известен ген, ответственный за развитие заболевания. Ген GNAS1 (Guanine Nucleotide-binding protein, Alpha-Stimulating activity polypeptide 1) локализован на хромосоме 20 в регионе 20q13, содержит 13 экзонов; кодирует стимулирующую aльфа-субъединицу G-белка (Gsa). Патогенез: белок Gs-альфа является посредником между рецепторами гормонов на поверхности клеток-мишеней и аденилатциклазой, которая катализирует синтез циклического аденозинмонофосфата, запуская реакцию клеток на воздействие гормонов. Мутантные белки Gs-альфа не активируют аденилатциклазу либо их активность сильно снижена. У больных ПГПТ типа 1А активность Gs-aльфа в 2 раза ниже, чем у здоровых людей, поэтому реакция клеток-мишеней на ПГТ ослаблена [14, 15].
Дифференциальная диагностика различных типов ПГПТ представлена в табл. 1.
Таблица 1
Биохимический анализ крови - гипокальциемия, гиперфосфатемия
| 28 01 2016 | 02 02 2016 | норма | |
| Кальций общий | 1,51 | 1,66 | 2,02-2,60 мМоль/л |
| Са2+ (ионизированный) | 0,66 | 0,74 | 1,13-1,32 мМоль/л |
| Фосфор неорганический | 3,21 | 3,23 | 1,30-2,26 мМоль/л |
Псевдогипопаратиреоз, критерии диагноза:
Лечение при псевдогипопаратиреозе:
Прогноз и профилактика при ПГПТ:
Клиническое наблюдение
Софья Т., 10 лет, поступила в научно-исследовательский клинический институт педиатрии, детский научно-практический центр нарушений сердечного ритма с диагнозом: синдром удлиненного интервала QT, синкопальные состояния.
Жалобы при поступлении на эпизоды потери сознания на фоне физической нагрузки, тонического напряжения рук при сильном волнении.
Анамнез семейный: родители - мать пробанда - русская, отец - родом из Афганистана; со слов - не имеющие профессиональных вредностей. В родословной по линии матери отмечаются случаи внезапной смерти (ВС) родственников, пароксизмальных состояний неясной этиологии, психических заболеваний, синдрома Фара (кальцинаты в веществе головного мозга). Сибс, брат 3 лет, со слов - здоров.
Анамнез жизни и заболевания: девочка от IV беременности (I-III беременности у матери - выкидыши на ранних сроках), от I срочных плановых оперативных родов, масса тела при рождении 3900 г, длина тела при рождении 52 см. На первом году жизни отмечались избыточные прибавки в весе (паратрофия).
Дебют заболевания с 10 лет, манифестация синкопальных состояний (4 эпизода) на фоне физической нагрузки (бег на улице во время уроков физкультуры), тоническое напряжение рук при сильном волнении (по типу «руки акушера»).
Данные объективного исследования:
Рост 132,5 см (< 25 %о), вес 24 кг (< 10%о).
Физическое развитие ниже среднего, гармоничное, телосложение пропорциональное. Sds роста соответствует -1 отклонению от нормы (норма -2+2). Особенности фенотипа: круглое лицо, короткая шея, низко расположенные ушные раковины, широкие межзубные промежутки, сандалевидная щель. Фото 1. По внутренним органам - без особенностей. Щитовидная железа не увеличена, клинически - эутиреоз. Половое развитие - Tanner I (что соответствует возрасту).
Фото 1
Особенности фенотипа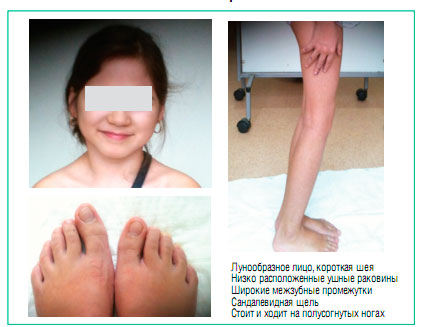
Данные лабораторных и функциональных исследований:
Клинический анализ крови и мочи - норма.
Электрокардиограмма покоя (рис. 1) -удлинение корригированного интервала QT (QTc) до 460мс N<440мс) на фоне синусовой тахикардии.
Рисунок 1
ЭКГ покоя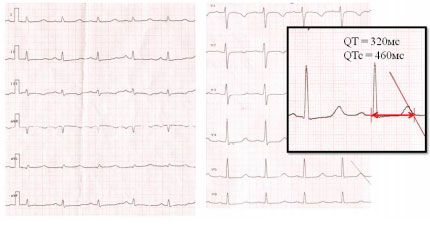
Электрокардиограмма после физической нагрузки (рис. 2) - удлинение интервала QTc до 510 мс (N<440мс) на фоне синусовой тахикардии.
Рисунок 2
ЭКГ после физической нагрузки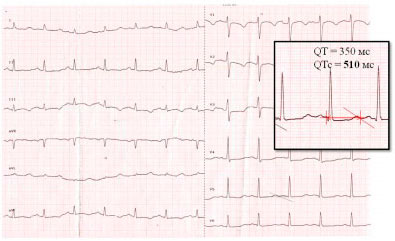
По данным холтеровского мониторирования (рис. 3) имеет место незначительная тахикардия в течение суток; отмечено удлинение интервала QT в течение всего времени исследования; QTmax = 475 мс, meanQTс = 525, maxQTc = 580 мс.
Рисунок 3
Холтеровское мониторирование ЭКГ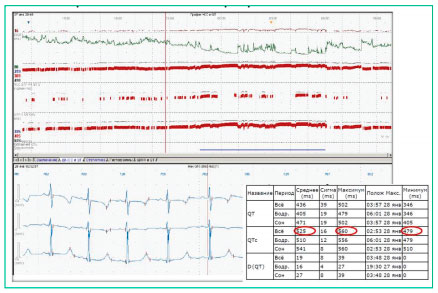
По данным ЭХО-КГ структурной патологии не выявлено; имеет место тенденция к снижению систолической функции левого желудочка; обращает внимание отсутствие ускоренного электромеханического проведения и удлинение ВИР, типичных для первичного синдрома удлиненного интервала QT
По данным тредмил-теста функциональная способность снижена, ответ ЧСС на нагрузку снижен; отмечено удлинение интервала QTc в исходе QTc = 466-475 мс без динамики продолжительности интервала QTc на нагрузке, нарушений ритма и проводимости в течение времени исследования не зарегистрировано.
Биохимический анализ крови - гипокальциемия, гиперфосфатемия (табл. 2).
Таблица 2
Дифференциальная диагностика различных типов псевдогипопаратиреоза
| Типы ПГПТ | Гипокальциемия Гиперфосфатемия |
Паратгормон крови | Дефицит субъединицы альфа Gбелка | Экскреция цАМФ с мочой (тест Элсворса-Говарда) | Резистентность к другим гормонам (кроме ПТГ) |
| IA | + | ↑ | + | ↓ | + |
| IB | + | ↑ | - | ↓ | - |
| IC | - | N | + | N | + |
| II | + | ↑ | - | N | - |
Биохимический анализ мочи - кальций в моче суточный 0,16 ммоль/сут (1,50-4,00), фосфор в моче суточный 3,4 мМоль/л (16,032,0), в расчете на креатинин: Са/Сr = 0,1 (норма 0,04-0,7), P/Cr = 0,5 (норма 1,2-3,6). Таким образом, почечная экскреция фосфатов снижена.
Паратиреоидный гормон крови - 1738 пг/мл (норма 16-62 пг/мл).
Тиреоидный профиль - тиреотропный гормон (ТТГ) - 7,48 мкМЕ/мл (норма 0,36-5,57), Т4 свободный - 9,04 пмоль/л (норма 9,0414,37).
УЗИ щитовидной железы без патологии.
Электроэнцефалография - выявляется умеренная дисфункция диэнцефальных структур мозга. Очаговых изменений и эпилептиформной активности не отмечено.
УЗИ брюшной полости - реактивные изменения печени, поджелудочной железы. Аномалия формы, увеличение желчного пузыря.
УЗИ почек - диффузные изменения паренхимы почек.
Компьютерная томография головного мозга - КТ-картина множественных кальцинатов в веществе мозга (синдром Фара) (рис. 4).
Рисунок 4
Множественные кальцинаты в веществе головного мозга (желтые стрелки). 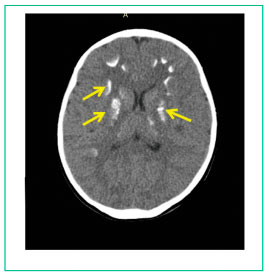
Денситометрия - снижение минеральной плотности костной ткани (рис. 5).
Рисунок 5
Денситометрия (снижение минеральной плотности костной ткани).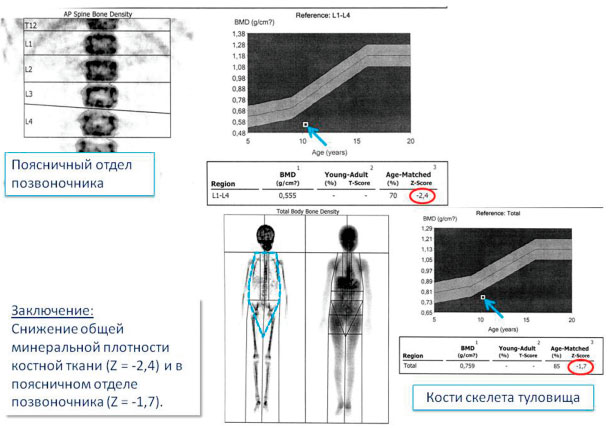
Консультации специалистов:
Генетик - необходимость исключения гипопаратиреоза с аутосомно-доминантным типом наследования; дифференциальный диагноз с велокардиофациальным синдромом и ПГПТ.
Невролог - данных за эпилептический генез синкопальных состояний нет. Логоневроз. Синдром Фара. Рекомендовано проведение ноотропной терапии.
Эндокринолог - ПГПТ (наследственная остеодистрофия Олбрайта). Первичный гипотиреоз. Начало пубертата.
Молекулярно-генетическое исследование -поиск мутации в гене GNAS1 - в работе.
Проведено комплексное обследование родственников пробанда. У матери и бабушки по линии матери выявлены аналогичные изменения: гипокальциемия, гиперфосфатемия, гиперпаратиреоз, синдром удлиненного интервала QT. Родословная после уточнения диагноза представлена на рис. 6.
Рисунок 6
Фрагмент родословной Софьи Т., 10 лет (после обследования родственников и уточнения диагноза)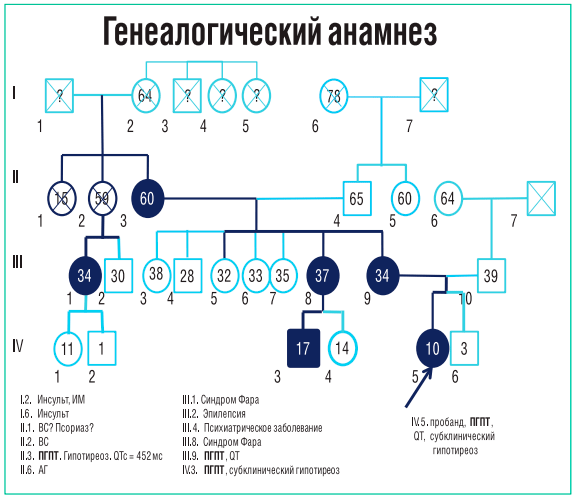
Сходство ряда клинических и биохимических признаков, которые имелись у пробанда, обуславливали необходимость проведения дифференциального диагноза с рядом патологических состояний, сопровождающихся гипокальциемией:
1. Гипопаратиреоз (с которым в первую очередь проводился дифференциальный диагноз) был исключен в связи с высоким уровнем ПГТ у нашей пациентки (при гипопаратиреозе уровень ПТГ снижен).
2. Рахитоподобные заболевания (РПЗ) (при которых часто отмечается гипокальциемия) были исключены, ввиду отсутствия у пробанда типичных для РПЗ рахитических деформаций скелета и характерных лабораторных и рентгенологических изменений.
На основании совокупности критериев:
ребенку выставлен основной диагноз: псевдогипопаратиреоз (МКБ X: Е20.1). Первичный гипотиреоз. Осложнение основного диагноза: синдром удлиненного интервала QT, синкопальная форма (МКБ X: 145.8)
Лечение. Ребенку рекомендован прием активного метаболита витамина D - альфа-кальцидола (альфаДЗ, Тева) 1 мкг х 1 раз в день, карбоната кальция (Кальций Сандоз) 500 мг х 3 раза в день, бета-блокатора (Атенолол) в дозе 1 мг/кг/сут., левотироксина (L-тироксин) 25 мкг х 1 раз в день. Контроль показателей фосфорно-кальциевого обмена, уровня ПГТ.
Заключение: представленное клиническое наблюдение демонстрирует сложности дифференциально-диагностического поиска, важность своевременного исследования простых биохимических параметров (при синдроме удлиненного интервала QT, эпилепсии, выявлении эктопических кальцинатов обязателен скрининг показателей фосфорно-кальциевого обмена); необходимость интегрировать отдельные признаки в общий фенотип патологического состояния для целенаправленной своевременной диагностики наследственных заболеваний. Своевременная и ранняя диагностика позволяет найти оптимальный подход к лечению, профилактике осложнений и предупреждению повторного возникновения заболевания в семье (медико-генетическое консультирование). Это диктует необходимость врачам различных специальностей четко ориентироваться в потоке наследственно обусловленной патологии.
Комментарии
ПРАКТИКА ПЕДИАТРА

