Современная системная фармакотерапия младенческих гемангиом
СтатьиН.П. Котлукова1,2, д-р мед. наук, профессор, Н.К. Константинова1,2, И.И. Трунина1,2, д-р мед. наук, профессор, Н.Д. Тележникова2, Е.В. Полетаева1
1 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
2 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
Ключевые слова: инфантильная гемангиома, пропранолол, лечение, β-блокатор, Гемангиол®
Keywords: infantile hemangioma, propranolol, treatment, β-blocker, Hemangiol®
Резюме. Данная публикация продолжает освещать современные подходы к ведению пациентов с инфантильными гемангиомами. Начало этому положено в статье «Современная стратегия и тактика ведения детей с младенческими гемангиомами» тех же авторов, вышедшей в № 4 журнала «Практика педиатра» за 2020 г. Цель настоящей работы – описать первый опыт системной терапии инфантильных гемангиом пероральным раствором пропранолола. Этот препарат зарегистрирован в России 10 ноября 2015 г. под торговым наименованием Гемангиол® («Пьер Фабр Медикамент», Франция). Гемангиол® (раствор для перорального применения) является первым и единственным официально зарегистрированным, в том числе в России, лекарственным средством для лечения детей с данной патологией.
В отделении кардиологии Детской городской клинической больницы им. З.А. Башляевой Департамента здравоохранения г. Москвы с декабря 2019 г. лечение препаратом Гемангиол® прошли 55 пациентов с инфантильными гемангиомами. В статье представлены результаты применения препарата Гемангиол® у данного контингента пациентов.
Summary. This publication continues to highlight the problem of modern management tactics for patients with infant hemangiomas. This problem was discussed in an article published in the journal «Practice of Pediatrics» No. 4, 2020. «Modern strategy and tactics of management of children with infant hemangiomas». In this article, the same team of authors introduces readers to the first experience of modern systemic pharmacotherapy of infant hemangiomas with Hemangiol® (Pierre Fabre Medicament, France). Hemangiol® (propranolol for oral use) is the first and only officially registered drug, including in Russia, created for the treatment of children with this pathology. Since December 2019, 55 patients with infantile hemangiomas have been treated with Hemangiol® in the Department of Cardiology of the Bashlyaeva State Clinical Hospital in Moscow. The article presents data on the results of the use of Hemangiol® in this cohort of patients.
Введение
12 июня 2008 г. статья в New England Journal of Medicine изменила взгляды педиатров всего мира на лечение одной из самых распространенных патологий детей раннего возраста – инфантильных гемангиом (ИГ). Доктор медицины C. Leaute-Labreze с коллегами из Детского госпиталя Бордо (Франция) опубликовали результаты терапии ИГ неселективным β-адреноблокатором пропранололом. Ранее неизвестный эффект пропранолола был обнаружен случайно: у ребенка с ИГ лица на фоне стандартного лечения кортикостероидами развилось характерное осложнение – обструктивная гипертрофическая кардиомиопатия, и пропранолол был назначен с целью коррекции данного состояния. Уже на следующий день после начала терапии цвет ИГ изменился с интенсивного красного до фиолетового, ИГ стала более мягкой на ощупь. За 10 мес лечения пропранололом ИГ практически полностью исчезла. Повторное подобное наблюдение заставило группу французских докторов провести пилотное исследование эффективности пропранолола как медикаментозного средства лечения ИГ. В результате назначения пропранолола во всех 9 случаях было констатировано явное уменьшение сосудистого образования уже через 24 ч с дальнейшим регрессом в течение нескольких месяцев [2, 3].
Таким образом, фармакотерапия ИГ – новое направление педиатрии. В России медикаментозное лечение сосудистых гиперплазий неселективным β-адреноблокатором пропранололом впервые было начато авторами настоящей публикации в отделении кардиологии Перинатального кардиологического центра Городской клинической больницы № 67 г. Москвы. В течение 10 лет (2010-2020 гг.) прошли лечение пропранололом более 500 пациентов с различной локализацией, распространенностью ИГ и глубиной поражения.
В статье «Современная стратегия и тактика ведения детей с младенческими гемангиомами», опубликованной в № 4 журнала «Практика педиатра» за 2020 г., мы оценили эффективность и безопасность данного способа лечения ИГ и представили разработанный нами протокол ведения пациентов с ИГ различной локализации на всех этапах наблюдения [1].
Цель настоящей работы – описать первый в России опыт применения для лечения детей с ИГ официально зарегистрированного препарата Гемангиол® (МНН – пропранолол, форма выпуска – раствор для перорального приема) («Пьер Фабр Медикамент», Франция). Лечение проводилось в отделении кардиологии детской городской клинической больницы (ДГКБ) им. З.А. Башляевой г. Москвы.
Пропранолол хорошо известен кардиологам, в том числе детским. Он с успехом применяется при тахиаритмиях, артериальной гипертензии, тиреотоксикозе, дилатационной и гипертрофической кардиомиопатии (идиопатическом гипертрофическом субаортальном стенозе), сердечной недостаточности, врожденных пороках сердца с подклапанным стенозом легочной артерии. Терапевтические эффекты пропранолола – снижение артериального давления, уменьшение частоты сердечных сокращений, купирование тахикардии. При тетраде Фалло пропранолол назначают для купирования и профилактики критических состояний – одышечно-цианотических приступов. В то же время известен и отрицательный инотропный эффект пропранолола, заключающийся в угнетении сократительной функции миокарда и снижении потребности миокарда в кислороде. Доза препарата для лечения вышеуказанных состояний колеблется от 1 до 8 мг/кг/сут.
Механизм действия пропранолола
Пропранолол относится к неселективным β-адреноблокаторам. Он конкурентно блокирует как β1-адренорецепторы, находящиеся в миокарде, так и β2-адренорецепторы, которые преимущественно локализуются в бронхах и периферических сосудах.
Эффект пропранолола при лечении ИГ основан в первую очередь на способности препарата вызывать периферическую вазоконстрикцию, в том числе и в сосудах ИГ, благодаря снижению образования и высвобождения оксида азота (NO). В результате вазоконстрикции уменьшается скорость кровотока в ИГ, цвет сосудистого образования меняется с насыщенного багрово-фиолетового на более бледный, снижается напряженность ИГ и местная температура. Данные изменения появляются уже на 1-2-е сутки от начала приема препарата.
Во-вторых, пропранолол ингибирует процессы ангиогенеза, снижая экспрессию васкулоэндотелиального фактора роста сосудов (VEGF) и фактора роста фибробластов (FGF). VEGF и FGF участвуют в процессах ангиогенеза, как и матриксные металлопротеиназы (ММР-2 и ММР-9), уровень которых повышается в фазе пролиферации ИГ. Их деятельность регулируется β-адренорецепторами. Пропранолол ингибирует активность ММР-2 и ММР-9, снижая тем самым интенсивность ангиогенеза.
В-третьих, установлено, что пропранолол запускает процессы апоптоза (запрограммированной клеточной гибели) эндотелиальных клеток.
Подытоживая вышеизложенное, следует подчеркнуть, что случайно обнаруженное положительное влияние пропранолола на сосудистые гиперплазии обусловлено его периферическим сосудосуживающим действием, торможением роста новых сосудов и активацией апоптоза. Эти эффекты соответствуют ранней (побледнение поверхности), промежуточной (прекращение роста), и долгосрочной (регресс) фазам обратного развития ИГ [4, 5].
До недавнего времени терапия ИГ пропранололом рассматривалась как off-label, т. е. считалась отступлением от инструкции по применению препарата, в связи с чем проведение данного вида лечения было возможным только после получения разрешения от этических комитетов соответствующих медицинских учреждений и информированного согласия родителей.
В настоящее время доступна специальная форма пропранолола для перорального применения в детском возрасте. Такой формой является препарат Гемангиол® в форме раствора. Гемангиол® рассматривается как новый стандарт терапии и зарегистрирован как препарат для лечения детей со следующими показаниями к применению [8, 9]:
- пролиферирующая ИГ, требующая системной терапии (ИГ, представляющая угрозу для жизни или оказывающая отрицательное влияние на функционирование систем организма;
- язвенная ИГ, характеризующаяся болью и/или отсутствием реакции на предшествующие мероприятия по лечению изъязвления;
- ИГ с потенциальным риском возникновения стойких рубцов или деформаций).
В международном интервенционном рандомизированном двойном слепом контролируемом исследовании, проведенном в 65 медицинских центрах 16 стран была доказана его эффективность и безопасность.
Препарат выпускается во флаконах, где 1 мл раствора содержит 3,75 мг пропранолола. Рекомендуемая терапевтическая доза 3 мг/кг/сут. Применение препарата Гемангиол® обеспечило положительную динамику к 5-й неделе лечения у 88% пациентов с ИГ. Динамика сохранялась в течение всего периода лечения, а к 24-й неделе полное или почти полное исчезновение ИГ наблюдалось у 60% больных. После получения этих доказательств эффективности и безопасности препарат был включен в европейские и американские международные рекомендации по лечению ИГ, став первым и единственным на сегодняшний день педиатрическим препаратом, одобренным для лечения данной патологии [6, 7].
Применение других β-блокаторов, попытки назначения которых также имеют место как в России, так и за рубежом, относятся к терапии off-label. Кроме того, следует отметить, что β-блокатор атенолол обладает большей кардиоселективностью, чем пропранолол, следовательно, имеет большее влияние на сердечно-сосудистую систему.
Материалы и методы
В отделении кардиологии ДГКБ им. З.А. Башляевой с декабря 2019 г. лечение препаратом Гемангиол® прошли 55 детей с ИГ. Препарат назначался согласно инструкции по применению. Возраст 30 (54,5%) из 55 пациентов при поступлении составил <6 мес, 17 (31,0%) – от 6 до 12 мес, 8 (14,5%) были старше 1 года1. Анализируя возрастной состав детей, следует отметить, что половина из них поступила с ИГ в стадии пролиферации, когда своевременное назначение лечения способно дать хороший результат. При этом вторая половина пациентов была старше 6 мес, а в этом возрасте в сосудистом образовании начинаются фиброзные изменения, что снижает эффективность системной фармакотерапии. Девочек среди пациентов было значительно больше (36 (65,4%) из 55), чем мальчиков (19 (34,5%) из 55), что совпадает с данными мировых популяционных исследований. Известно, что ИГ чаще наблюдаются у недоношенных детей, рожденных с массой тела <1 кг (22%), чем у доношенных (3-5%). [1]. Анализ гестационного возраста обследованных показал, что больше половины из них (65,4%) были недоношенными. Очаговые сосудистые гиперплазии (32 (58,2%) случая) незначительно преобладали над множественными (23 (41,8%) случая). Поверхностные ИГ имели место у 12 (21,8%) детей, глубокие – 10 (18,2%), смешанные, содержащие как наружный, так и внутренний компонент, были наиболее частыми и наблюдались у 33 (60,0%).
1 Согласно инструкции по медицинскому применению Гемангиол® предназначен для применения у младенцев в возрасте от 5 нед до 5 мес.
Весьма позитивным моментом следует считать тот факт, что большинство детей (48 (87,3%) из 55) были первичными пациентами, т. е. ничем не лечились до поступления в стационар. При этом меньшая часть (7 (12,7%) из 55) имели в анамнезе неудачные попытки применения различных методов лечения (табл. 1).
Таблица 1. Обобщенные данные пациентов (n = 55)
| Параметр | Число пациентов, абс. (%) |
| Возраст пациентов при поступлении | |
| <6 мес | 30 (54,5) |
| от 6 до 12 мес | 17 (31,0) |
| >1 года | 8 (14,5) |
| Пол | |
| женский | 36 (65,4) |
| мужской | 19 (34,5) |
| Гестационный возраст | |
| доношенные | 19 (34,5) |
| недоношенные | 36 (65,4) |
| Распространенность | |
| очаговые сосудистые гиперплазии | 32 (58,2) |
| множественные сосудистые гиперплазии | 23 (41,8) |
| Глубина поражения | |
| поверхностные | 12 (21,8) |
| глубокие | 10 (18,2) |
| смешанные | 33 (60,0) |
| Предшествующая терапия | |
| ранее не проходили лечения | 48 (87,3) |
| ранее прошли лечение | 7 (12,7) |
Комплексное обследование включало общий и биохимический анализ крови, электрокардиографию (ЭКГ), измерение артериального давления, суточное мониторирование ЭКГ по Холтеру, эхокардиографию, ультразвуковое исследование (УЗИ) ИГ по специально составленному нами протоколу с оценкой толщины образования, количества сосудов в нем, линейной скорости кровотока (ЛСК) в сосудах ИГ разного диаметра, степени резистентности сосудов, а также УЗИ печени и щитовидной железы с определением параметров тиреоидного статуса. При отсутствии противопоказаний к лечению назначали Гемангиол® по определенной схеме с постепенным повышением дозы до терапевтической. Фотодокументация до старта терапии была обязательной.
Исходно при УЗИ выявлены типичные эхографические признаки ИГ: наличие расширенных сосудов с пульсирующим кровотоком различной скорости. При толщине тканей в области ИГ от 2 до 41 мм у 30 (54,54%) пациентов в режиме цветового доплеровского картирования (ЦДК) определялось значительное количество сосудов (>10 в 1 ультразвуковом срезе); у 7 (12,73%) пациентов визуализировано от 5 до 10 сосудов, у 18 (32,73%) количество сосудов было незначительным (<5). ЛСК в питающих (приносящих) сосудах варьировала от 12 до 170 см/с. В крупных интрапаренхиматозных сосудах ИГ ЛСК была высокой и колебалась от 20 до 108 см/с, в артериях среднего калибра ЛСК также была высокой – 12-57 см/с, а в мелких артериях в толще гемангиомы она составляла 8-19 см/с. Исходно низкой ЛСК (4-7 см/с) не было ни у одного ребенка. О значительной вазодилатации в ИГ свидетельствовало снижение индекса резистентности до 0,43-0,55 (в норме он должен превышать 0,8-0,9). Таким образом, результаты исходного УЗИ, наряду с клиническими данными, служили объективным критерием, позволяющим принять о необходимости системной фармакотерапии ИГ. Последующее регулярное проведение данного исследования (1 раз в 3 мес) с динамическим определением вышепредставленных параметров служило объективным методом оценки эффективности лечения.
В течение 1-й недели лечения препаратом Гемангиол® оценивали переносимость препарата, контролировали появление возможных нежелательных симптомов. Ежедневным был контроль артериального давления и частоты сердечных сокращений. Через 1 нед осуществлялся контрольный забор крови (с определением уровня глюкозы, трансаминаз, мочевины и креатинина), а также ЭКГ и эхокардиография.
Результаты
В 46 (83,6%) из 55 случаев препарат Гемангиол® оказал быстрый положительный клинический эффект. Признаки обратного развития ИГ появились уже на 2-3-и сутки от начала терапии, что также отметили родители, осуществляя фотодокументацию. Весьма отрадным был тот факт, что положительный эффект наблюдался в том числе у детей, у которых предшествующее лечение альтернативными методами было безуспешным (6 из 7 пациентов). Клинический эффект зависел от локализации ИГ и заключался в изменении цвета ИГ, которая становилась менее яркой, а также в уменьшении плотности, напряженности ИГ и снижении местной температуры. У 9 (16,4%) пациентов за этот период отчетливого положительного эффекта не наблюдалось. У 4 из этих детей имелся мультифокальный гемангиоматоз печени, и контрольное УЗИ печени, проведенное через 1 нед от начала лечения, еще не выявило признаков снижения интенсивности кровотока, уменьшения количества и размеров сосудистых образований.
Нежелательные явления транзиторного характера были зарегистрированы у 9 (16,4%) из 55 детей. К таким явлениям мы отнесли повышенную возбудимость, трудности с засыпанием, периферический вазоспазм (похолодение ног и рук), срыгивания; у 1 ребенка с аллергическим фоном отмечены симптомы бронхообструкции. В последнем случае препарат был отменен по медицинским показаниям (табл. 2).
Таблица 2. Оценка эффективности и безопасности терапии инфантильных гемангиом препаратом Гемангиол® (n = 55)
| Параметр | Значение |
| Время начала развития ответа на терапию | 2-3-и сутки |
| Число пациентов с быстрым положительным клиническим эффектом, абс. (%) | 46 (83,6) |
| Число случаев нежелательных явлений, абс. (%) | 9 (16,4) |
| Число случаев отмены терапии, абс. (%) | 1 (1,8) |
Ниже мы приводим клинический пример лечения осложненного течения смешанной ИГ в области мягких тканей левой щеки.
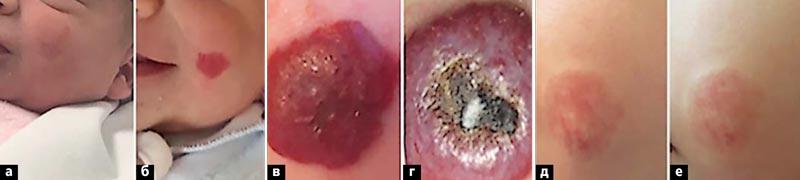 Лечение препаратом Гемангиол® смешанной инфантильной гемангиомы, осложненной язвенным дефектом, в области мягких тканей левой щеки: а – розовое пятно на левой щеке (первые дни жизни); б – начало пролиферации инфантильной гемангиомы на 14 день жизни; в – стадия выраженной пролиферации (2 мес); г – язвенный дефект в 2,5 мес; д – стадия выраженной инволюции. Отмена терапии в 2 года; е – резидуальные изменения
Лечение препаратом Гемангиол® смешанной инфантильной гемангиомы, осложненной язвенным дефектом, в области мягких тканей левой щеки: а – розовое пятно на левой щеке (первые дни жизни); б – начало пролиферации инфантильной гемангиомы на 14 день жизни; в – стадия выраженной пролиферации (2 мес); г – язвенный дефект в 2,5 мес; д – стадия выраженной инволюции. Отмена терапии в 2 года; е – резидуальные изменения Клинический пример
Девочка С. впервые поступила в отделение кардиологии ДГКБ им. З.А. Башляевой в возрасте 2 мес жизни с сосудистым образованием в области левой щеки. Из анамнеза известно, что ребенок родился от матери 25 лет с отягощенным соматическим анамнезом (наследственная тромбофилия), от 1-й беременности, наступившей в результате 3-й попытки экстракорпорального оплодотворения и протекавшей на фоне угрозы прерывания в 8-9 нед постменструального возраста, повышения артериального давления в I триместре, анемии и отеков в III триместре. Во время беременности мать принимала дюфастон, клексан (по поводу повышения D-димера). Роды первые, своевременные, путем кесарева сечения (показания: тазовое предлежание плода, плевистое прикрепление пуповины к плаценте. Девочка родилась с массой тела 3310 г, длиной 51 см, оценкой по шкале Апгар 8/9 баллов.
После рождения у ребенка обнаружено светло-розовое сосудистое пятно в области левой щеки. Со 2-й недели жизни цвет пятна стал изменяться в сторону ярко-красного, начался бурный рост образования с формированием «кратерообразного» язвенного дефекта. В возрасте 2 мес жизни развилось кровотечение из данного дефекта.
При осмотре в стационаре у девочки была диагностирована смешанная ИГ мягких тканей в области левой щеки с большим внутреннем компонентом, диаметром до 3 см, осложненная язвенным дефектом в центре, с выраженной капиллярной сетью по краям. В связи с наличием язвенного дефекта было принято решение начать терапию препаратом Гемангиол® без проведения исходного УЗИ ИГ. По данным предварительного обследования противопоказаний со стороны сердечно-сосудистой системы выявлено не было, и девочке был назначен Гемангиол®. На фоне терапии отмечена выраженная положительная динамика: объем образования уменьшился, исчезла капиллярная сеть. В начале лечения появились срыгивания после приема препарата, которые постепенно прекратились. Через 2 нед после назначения терапии язвенный дефект эпителизировался. В ходе регулярного динамического наблюдения (1 раз в 3 мес) с проведением фотодокументации констатирован стойкий положительный эффект лечения. ИГ становилась все более светлой и мягкой при пальпации.
По данным УЗИ ИГ, проведенного в возрасте 8 мес, толщина образования составляла 12 мм. При ЦДК визуализировано до 10 сосудов в 1 ультразвуковом срезе с максимальной скоростью кровотока 55 см/с в питающей артерии и 19 см/с в интрапаренхиматозных сосудах среднего калибра.
В возрасте 1 года 4 мес по данным УЗИ скорость кровотока в питающей артерии составила 43 см/с, в интрапаренхиматозных сосудах (внутри образования) максимальная ЛСК – 13 см/с. В дальнейшем в ходе динамического обследования наблюдалась медленная инволюция ИГ, что подтверждалось уменьшением ЛСК, толщины тканей и количества сосудов. Появлялись небольшие фиброзно-жировые участки внутри ИГ, свидетельствующие об обратном развитии. В возрасте 2 лет количество сосудов, выявляемых в режиме ЦДК, стало минимальным (4-5 в 1 ультразвуковом срезе), и препарат был отменен.
После завершения терапии и отмены препарата проведено последнее УЗИ, при котором в области левой щеки определялась дополнительная ткань в виде фиброзно-жировых участков (резидуальные изменения). В режиме цветокодированных методик выявлено минимальное количество (3-5) мелких сосудов в 1 ультразвуковом срезе. Максимальная скорость кровотока составляла 8-9 см/с. В месте язвенного дефекта сформировался небольшой рубец.
Девочка регулярно проходила кардиологическое обследование, включавшее эхокардиографию и мониторирование ЭКГ по Холтеру, измерение артериального давления, оценку гемограммы, уровня аланин- и аспартатаминотрансферазы, глюкозы. Кардиальных и экстракардиальных нежелательных эффектов на фоне терапии препаратом Гемангиол® после ее завершения не было.
Данный клинический случай демонстрирует результат успешного лечения препаратом Гемангиол® смешанной ИГ мягких тканей левой щеки, осложненной язвенным дефектом. Особенностью данного случая является то, что язвенный дефект сформировался у ребенка достаточно рано, в возрасте 2 мес. В связи с этим, а также с учетом осложненного течения ИГ, медленного регресса сосудистого образования (о чем свидетельствовали данные УЗИ), высокого риска синдрома отмены было принято решение, пролонгировать курс терапии препаратом Гемангиол®, что дало хороший результат.
Заключение
Результаты применения препарата Гемангиол® в качестве современного средства системной терапии ИГ в отделении кардиологии ДГКБ им. З.А. Башляевой г. Москвы продемонстрировали его высокую эффективность и безопасность. Препарат был эффективен в 83,6% случаев. Только у 1 ребенка с отягощенным аллергическим анамнезом наблюдались нежелательные явления, повлекшие отмену препарата. Лечение препаратом Гемангиол® не относится к терапии off-label, поскольку он является единственным лекарственным средством, созданным специально для лечения ИГ. Гемангиол® зарегистрирован в более чем 40 странах, включая Российскую Федерацию, как препарат для лечения данной патологии.
Литература
- Котлукова Н.П., Константинова Н.К., Трунина И.И. и др. Современная стратегия и тактика ведения детей с младенческими гемангиомами // Практика педиатра. 2020. № 4. С. 4-12.
- Leaute-Labreze C., Dumas de la Roque E., Hubiche T. et al. Propranolol for severe haemangiomas of infancy // New England Journal of Medicine. 2008. Vol. 358. No. 24. P. 2649-2651. DOI: 10.1056/NEJMc0708819.
- Leaute-Labreze C., Hoeger P., Mazereeuw-Hautier J. et al. A randomized, controlled trial of oral propranolol in infantile hemangioma // New England Journal of Medicine. 2015. Vol. 372. P. 735-746. DOI: 10.1056/NEJMoa1404710.
- Lamy S., Lachambre M.P., Lord-Dufor S., Beliveau R. Propranolol suppresses angiogenesis in vitro: inhibicion of proliferacion, migration, and differentiation of endothelial cells // Vascular Pharmacology. 2010. Vol. 53. No. 5-6. P. 200-208. DOI: 10.1016/j.vph.2010.08.002.
- Tu J.B., Ma R.Z., Dong Q. et al. Induction of apoptosis in infantile hemangioma endothelial cells by propranolol // Experimental and Therapeutic Medicine. 2013. Vol. 6. No. 2. P. 574-578. DOI: 10.3892/etm.2013.1159.
- Hoeger P.H., Harper J.I., Baselga E. et al. Treatment of infantile haemangiomas: recommendations of a European expert group // European Journal of Pediatrics. 2015. Vol. 174. No. 7. Р. 855-865. DOI: 10.1007/s00431-015-2570-0.
- Krowchuk D.P., Frieden I.J., Mancini A.J. et al. Clinical practice guideline for the management of infantile hemangiomas // Pediatrics. 2019. Vol. 143. No. 1. DOI: 10.1542/peds.2018-3475.
- Инструкция по медицинскому применению препарата Гемангиол®
- grls.rosminzdrav.ru

