Энтеровирусная инфекция у детей: современное состояние проблемы
СтатьиОпубликовано в журнале:
«Практика педиатра» №4, 2020
О.Н. Солодовникова, канд. мед. наук, Л.А. Харитонова, д-р мед. наук, профессор, кафедра педиатрии с инфекционными болезнями у детей факультета дополнительного профессионального образования ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
Ключевые слова: энтеровирусная инфекция, энтеровирусы, вирусоносительство, бессимптомные формы, полиомиелитоподобные формы, серозный менингит, энерготропная терапия, L-карнитин, Элькар®
Keywords: enterovirus infection, enteroviruses, carriage of viruses, asymptomatic forms, poliomyelitis-like forms, serous meningitis, energotropic therapy, L-carnitine, Elkar®
Резюме. Энтеровирусы являются одними из наиболее распространенных патогенов человека. Во всем мире они ежегодно вызывают почти миллиард инфекций у людей. Энтеровирусная инфекция (ЭВИ) в основном протекает бессимптомно или с неспецифическими симптомами, но может иметь и тяжелое течение со смертельным исходом. Клинический полиморфизм, распространенность бессимптомных форм ЭВИ, на долю которых приходится до 75% всех случаев заболевания, а также высокая контагиозность позволяют отнести данное заболевание к группе «высокого риска». Повсеместная распространенность ЭВИ и отсутствие специфических средств ее лечения и профилактики постоянно поддерживают высокий уровень инфицированности населения во всем мире.
В Российской Федерации, помимо программы Всемирной организации здравоохранения, направленной на ликвидацию полиомиелита, осуществляется постоянный эпидемиологический надзор за циркуляцией энтеровирусов и заболеваемостью энтеровирусными инфекциями. Высокая восприимчивость людей к ЭВИ с возможностью длительного вирусоносительства при отсутствии видимых проявлений ведет к формированию механизмов аутоиммунных процессов, что является стимулом для разработки рекомендаций по реабилитации пациентов.
Summary. Enteroviruses are one of the most common human pathogens. Worldwide, they cause almost a billion infections in people every year. Enterovirus infection (EVI) is mostly asymptomatic and is limited to viral symptoms, but can also cause severe diseases with fatal outcomes. Clinical polymorphism, the prevalence of asymptomatic forms of EVI, accounting for up to 75% of all cases of the disease, and high contagiousness are factors that make it possible to classify this disease as a "high risk" group. The ubiquity of EVI and the lack of specific treatment and prevention tools constantly maintain a high level of infection in the world's population.
In the Russian Federation, in addition to the World Health Organization programmes, there is ongoing epidemiological surveillance of the circulation of enteroviruses and the incidence of enterovirus infections. High susceptibility of people to EVI with the possibility of long-term viral transmission in the absence of visible manifestations contributes to the formation of mechanisms of autoimmune processes, which is a trigger for the development of recommendations for its rehabilitation.
Введение
Актуальность энтеровирусной инфекции (ЭВИ) связана с ее клиническим полиморфизмом, повсеместной распространенностью, широтой и массовостью поражения энтеровирусами (ЭВ) населения, склонностью к вспышечному характеру заболевания.
Особенностью ЭВИ является поражение центральной нервной системы (ЦНС) с развитием полиомиелитоподобных форм. Установлено, что от 18 до 31% случаев поражения ЦНС у детей раннего возраста связано с внутриутробным инфицированием ЭВ [1]. Способность ЭВ к персистенции с формированием аутоиммунного процесса может приводить к гибели плода, самопроизвольным выкидышам и заболеваниям новорожденных.
Для ЭВИ характерна высокая генетическая изменчивость с образованием новых высокопатогенных штаммов и отсутствием стойкого иммунитета. Не менее важным фактором считается способность ЭВ запускать аутоиммунные механизмы с поражением паренхиматозных органов, что зачастую приводит к хронизации процесса [2, 3].
Отсутствие этиотропной терапии ЭВИ и вакцинопрофилактики этой инфекции побуждает к поискам методов патогенетической терапии и ее обоснованию.
Эпидемиология
Энтеровирусы являются одними из самых распространенных патогенов человека. Во всем мире они ежегодно вызывают почти миллиард инфекций у людей [1]. В то же время продолжают появляться все новые серотипы ЭВ, некоторые из которых, как полагают ученые, получены людьми от других приматов [4]. Вследствие высокой генетической изменчивости ЭВ в последние годы обнаружены их новые высокопатогенные штаммы (А71 и D68) [4, 5], вызываемая ими инфекция протекает с респираторными и неврологическими симптомами и характеризуется тенденцией к вспышкам и высокой летальности [1, 4, 6].
С 2006 г. в Российской Федерации была реализована Программа эпидемиологического надзора и профилактики энтеровирусной (неполио) инфекции. В рамках этой Программы проведено множество организационных и практических мероприятий и научно-исследовательских работ, разработан ряд нормативных и методических документов, в том числе СП 3.1.2950-1 «Профилактика энтеровирусной (неполио) инфекции», и значительно укреплена материально-техническая база тех лабораторий, которые осуществляют исследования на наличие ЭВ в биологических образцах людей и объектах окружающей среды [5].
По данным литературы, заболеваемость ЭВ типа A71 связана со вспышками hand, foot and mouth disease и редкими поражениями ЦНС в виде энцефалита с поражением ствола мозга. Данные вспышки регистрировались главным образом в Азиатско-Тихоокеанском регионе. В странах Азии также наблюдалась значительная распространенность ЭВ, а именно Коксаки А16 [7]. Выявление ЭВ серотипа D68 связано с развитием респираторных проявлений и дебютом острых вялых параличей в Северной Америке, Европе и Азии в последние 5 лет [8, 9]. В последние годы тяжелые формы заболеваний, вызванных ЭВ типов A71 и D68, регистрировались и в ряде европейских стран [10].
Высока заболеваемость ЭВИ и в Российской Федерации. По данным литературы, выявление циркуляции возбудителей ЭВИ на территории РФ значительно улучшилось в рамках реализации Программы «Эпидемиологический надзор и профилактика энтеровирусной (неполио) инфекции на 2015-2017 гг.», но при росте заболеваемости ЭВИ и выявлении новых клинических форм болезни практически отсутствуют данные о профилактике ЭВИ и патогенетической терапии.
На рисунке представлены данные о заболеваемости детей ЭВИ в целом и заболеваемости серозным менингитом как одной из форм ЭВИ у детей в РФ. Согласно этим данным рост заболеваемости детей ЭВИ не имеет тенденции к снижению. Наоборот, за последние годы, а именно с 2015 по 2019 г., заболеваемость ЭВИ увеличилась почти в 2 раза. Заболеваемость серозным менингитом энтеровирусной этиологии также остается на стабильно высоком уровне.
По эпидемиологическим данным, ЭВИ имеет летне-осеннюю сезонность, хотя спорадические случаи в отдельных регионах России встречаются круглогодично, а максимальная заболеваемость данной инфекцией чаще регистрируется в августе-сентябре [2].
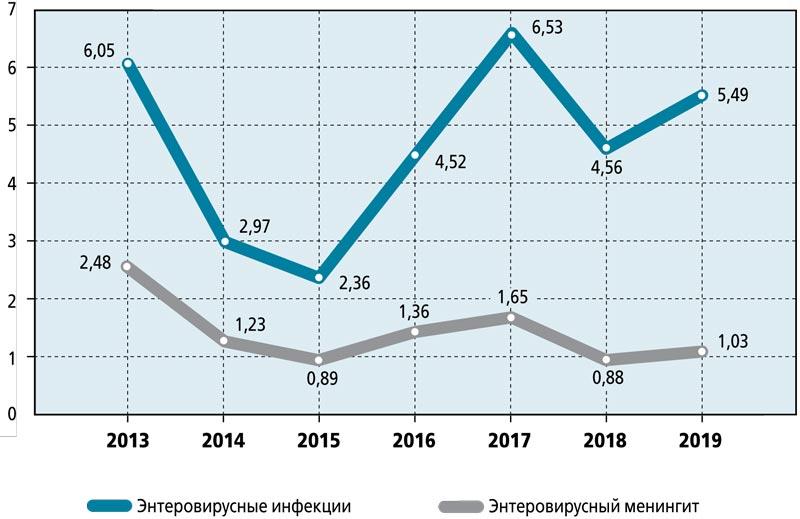 Показатели заболеваемости энтеровирусной (неполио) инфекцией за 2013-2019 гг. по РФ (на 100 тыс. населения)
Показатели заболеваемости энтеровирусной (неполио) инфекцией за 2013-2019 гг. по РФ (на 100 тыс. населения)
Этиологическая характеристика энтеровирусов
ЭВ представляют собой род вирусов из семейства пикорнавирусов (Picornaviridae), порядок Picornavirales.
Согласно современной таксономии, основанной на геномных и биологических свойствах вирусов, ЭВ делятся на 15 видов, из которых ЭВ видов А-D и риновирусы видов A-C заражают человека [3, 5]. Это одна из самых многочисленных групп вирусов, включающая полиовирус, неполиомиелитные энтеровирусы, вирус гепатита А и риновирусы A, B, C.
Семейство характеризуется икосаэдрической симметрией капсида и одноцепочечной + РНК как носителя наследственной информации [1, 5]. Название ЭВ связано с их репродукцией в желудочно-кишечном тракте, однако энтерит они вызывают редко.
Клиническая картина
В классификации ЭВИ выделяют типичные и атипичные формы. Клиническая классификация представлена в таблице.
Клиническая классификация форм энтеровирусной инфекции
| Типичные формы | Атипичные формы |
| Герпангина | Инапарантная форма (субклиническая) |
| Эпидемическая миалгия, или болезнь Борнхольма (плевродиния) | Катаральная форма |
| Бостонская лихорадка (экзантема) | Энцефалитическая форма |
| Асептический серозный менингит | «Летний грипп», или трехдневная лихорадка |
| Мезаденит | Энцефаломиокардит новорожденных |
| Гастроэнтерит | Полиомиелитоподобная форма |
| Миокардит, перикардит | Эпидемический геморрагический конъюнктивит (болезнь АНС, болезнь «Аполло-11») |
| Геморрагический конъюнктивит | |
| Увеит | |
| Нефрит | |
| Гепатит | |
| Панкреатит |
Клиническая картина ЭВИ характеризуется полиморфизмом симптомов – от 3- и 5-дневной лихорадки, респираторных поражений дыхательной системы, экзантемных форм до более грозных проявлений, паралитических полиомиелитоподобных форм. Инкубационный период длится от 2 до 35 дней, в среднем 7-10 дней.
ЭВИ может протекать в виде поражения дыхательной системы – герпангины, ринита, фарингита, бронхита, бронхиолита, пневмонии, вплоть до отека легких. Эти клинические формы составляют до 30% всех случаев ЭВИ у детей [4]. Экзантемные формы, варианты с формированием серозного менингита и паралитические полиомиелитоподобные формы ЭВИ встречаются значительно реже.
Тем не менее дети младше 5 лет подвержены тяжелым формам с развитием неврологических осложнений, таких как асептический мозжечковый менингит, мозжечковый энцефалит, острый вялый паралич. Развитие данных неврологических и респираторных форм чаще вызвано ЭВ типа A71 и D68.
Одна из форм ЭВИ – серозно-вирусный менингит. В большинстве случаев асептический серозный менингит протекает классически и характеризуется острым началом, выраженной головной болью, рвотой и симптомами интоксикации. Менингеальный синдром носит непостоянный характер и отличается диссоциацией менингеальных симптомов.
Лихорадка держится 3-4 дня, реже до 6 дней, в 25% случаев температурная кривая имеет «двухволновый» характер. Гипертензионно-гидроцефальный синдром является ведущим в патогенезе серозного менингита. Может наблюдаться также полиорганность поражения: экзантема, герпангина, миалгия, желудочно-кишечные расстройства, абдоминальный синдром, полиаденопатия, гепатомегалия, реже спленомегалия.
У новорожденных и детей грудного возраста асептический серозный менингит развивается как составляющая тяжелого системного поражения, включающего некроз печени, миокардит, некротизирующий энтероколит, внутрисосудистую коагуляцию. Менингеальные симптомы могут быть стертыми. Летальный исход у детей этого возраста является не следствием поражения ЦНС, а результатом острой печеночной недостаточности (вирусы ЕСНО) или миокардита (вирусы Коксаки).
После воспалительных форм ЦНС формируются резидуальные явления. Данные изменения наблюдаются в подростковом периоде и характеризуются проявлением таких форм, как цереброастенический синдром, неврозоподобные расстройства, гипертензионный синдром.
Клинический полиморфизм, распространенность бессимптомных форм ЭВИ, которые составляют до 75% всех случаев заболевания, высокая контагиозность позволяют отнести данное заболевание к группе «высокого риска» [9].
В отечественной литературе практически отсутствуют сведения о редких проявлениях ЭВИ, поражении ЭВ сердечно-сосудистой системы, желчного пузыря и почек.
В 50% случаев выявлена взаимосвязь с тропностью ЭВ к кардиомиоцитам и развитием дилатационной кардиомиопатии у детей [8]. Данная инфекция способствуют развитию кардиомиопатии двумя различными способами. При первом типе поражения ЭВ могут непосредственно инфицировать и индуцировать гибель клеток кардиомиоцитов. Во втором же случае ЭВ вызывают аутоиммунный ответ, при котором собственная иммунная система хозяина разрушает кардиомиоциты (стадия апоптоза) и приводит к формированию кардиомиопатии.
Изучая данные литературы, мы также обнаружили связь ЭВ Коксаки B4 с развитием сахарного диабета I типа. Вирус Коксаки В4 выступает триггером в развитии патологического процесса в поджелудочной железе [4, 8], вызывая апоптоз ^-клеток и гипогликемию в экспериментальных исследованиях. Таким образом, подтверждается тот факт, что ЭВ могут вызывать поражение поджелудочной железы с последующим развитием гипо- или гипергликемии.
Вопросы диагностики и терапии
Лабораторная диагностика ЭВИ осложняется большим количеством серотипов возбудителей, поэтому наряду с классическими вирусологическими методами в диагностике используют молекулярно-биологические методы, позволяющие секвенировать геном возбудителя и определить филогенетические связи между различными штаммами ЭВ [2]. Тип ЭВ может быть определен с использованием молекулярного типирования (генотипирования), которое основано на определении нуклеотидной последовательности области генома, кодирующей капсидный белок VP1. Полипептид VP1 содержит аминокислотные последовательности, определяющие серотип вируса, и является главным рецепторным локусом вириона. Определение типа ЭВ проводят путем секвенирования фрагментов области генома, кодирующей белки капсида VP3 и VP1. Молекулярное типирование ЭВ с использованием амплификации и секвенирования нуклеотидных последовательностей региона VP1 является прямым методом идентификации, обладает высокими показателями специфичности [11].
Диагноз ЭВИ и ее форм базируется в основном на клинической симптоматике и эпидемиологических данных.
Этиотропной терапии ЭВИ в настоящее время в России не существует. Препараты плеконарил (США) и вапендавир (США), действующие непосредственно на вирусный капсид и тем самым ингибирующие инфекцию, вызванную только ЭВ типа A71 и D68, в России пока не зарегистрированы.
Патогенетическая и симптоматическая терапия ЭВИ проводится с учетом клинической формы и основана на восстановлении метаболизма и энергетического потенциала поврежденных клеток. На этом фоне при развитии неврологической симптоматики в периоде реконвалесценции, особенно после серозно-вирусного менингита, может быть рекомендована метаболическая терапия [12], коррекция вегетативных расстройств, ассоциированных с синдромом вегетативной дистонии.
В основе патогенеза синдрома вегетативной дистонии лежит дезинтеграция высших вегетативных центров, нарушение равновесия между симпатическим и парасимпатическими отделами, расстройство взаимодействия различных органов и систем организма, метаболических процессов, что отражается на развитии адаптационно-компенсаторных реакций, формировании энергетического обмена [13].
В многочисленных исследованиях было показано, что нарушения энергетического обмена выявлены у детей с перинатальной патологией, урологическими и нефрологическими заболеваниями, острыми респираторными инфекциями [12, 14-17]. При всех отмеченных патологических состояниях целесообразно применение энерготропных препаратов.
В современной литературе имеются данные об использовании препаратов L-карнитина у детей и подростков при вегетативных расстройствах [13] и при всех указанных выше патологических состояниях и заболеваниях.
Таким препаратом L-карнитина с выраженным метаболическим действием является Элькар® (левокарнитин) отечественной компании «ПИК-ФАРМА». Фармакологическое действие L-карнитина обусловлено его участием в процессах обмена веществ в качестве переносчика длинноцепочечных жирных кислот (пальмитиновой и др.) из цитоплазмы в митохондрии, где эти кислоты подвергаются процессу β-окисления с образованием аденозинтрифосфорной кислоты и ацетил-КоА.
Карнитин улучшает белковый и жировой обмен, повышает секрецию и ферментативную активность желудочного и кишечного соков, способствует усвоению пищи, снижает избыточную массу тела. Участвует в транспорте ксенобиотиков и органических кислот из клетки, усиливает процесс детоксикации, позволяя устранить последствия интоксикации организма.
Элькар® улучшает обмен веществ, непосредственно влияет на обеспечение клеток организма энергией, тем самым способствуя нормализации клеточного энергообмена, коррекции метаболических нарушений.
Важным направлением реабилитации детей после перенесенных вирусных инфекций является назначение препаратов на основе L-карнитина в связи с уникальностью его воздействия на клеточный метаболизм [18, 19]. Необходимость включения Элькара в патогенетическую терапию при инфекционных заболеваниях у детей отмечена в исследовании Т.А. Руженцовой [17]: вирусные агенты, в том числе и ЭВ [8], способны не только длительно персистировать в организме, находясь в латентном состоянии, и активизироваться на фоне ослабления иммунитета при присоединении интеркуррентной инфекции, но и вызывать поражение миокарда, что зачастую бывает сложно связать с первоначальным этиологическим фактором [17].
В работах О.В. Гончаровой показано, что включение в реабилитацию детей с острыми респираторными инфекциями препарата Элькар® в возрастных дозах курсами длительностью 1-1,5 мес предупреждает развитие повторных эпизодов острых респираторных инфекций у детей и сокращает длительность их течения, восстанавливая активность иммунных клеток [14]. Кроме того, в литературе представлены данные об эффективности применения Элькара в дозе 30-50 мг/кг/сут в 2-3 приема курсами 1-1,5 мес при гипоксических состояниях у детей с перинатальной патологией [12]. Такая коррекция патологических процессов возможна и в периоде реконвалесценции серозных менингитов. Курсы необходимо повторять 2 раза в год в течение 3 лет.
Изучая отечественную литературу, мы нашли сообщения о том, что лечение левокарнитином позволяет существенно улучшить состояние здоровья детей с вегетативными дисфункциями, нормализуя механизмы вегетативной регуляции, стабилизируя клеточный энергообмен, что, в свою очередь, способствует возрастанию физической активности детей и повышению иммунитета [16]. Эти изменения крайне необходимы и в реабилитационной терапии как ЭВИ в целом, так и ее неврологических форм.
Элькар® незаменим для восстановления детей после болезни. Он улучшает энергообеспечение органов и тканей, повышает аппетит и усвоение белков, помогает организму работать на полную мощность, являясь естественным эндогенным метаболитом живого организма, принимая участие во всех видах обмена веществ, в регуляции энергетических и пластических процессов.
Элькар® эффективно восполняет потребность организма в L-карнитине, когда организму необходима энергетическая поддержка.
Заключение
Значительный полиморфизм клинических проявлений ЭВИ с отсутствием четкой зависимости от серологического типа возбудителя, большая частота бессимптомных форм, длительное вирусоносительство, отсутствие специфических методов профилактики делают ЭВИ неуправляемой болезнью. Глубокое знание клинической симптоматики, своевременность постановки диагноза, а также принятые меры профилактики способствуют снижению частоты осложненных и тяжелых форм ЭВИ.
Энтеровирусы ассоциируются со многими заболеваниями, этиология которых ранее не связывалась с инфекционными факторами, – это кардиомиопатии, нефриты, сахарный диабет, васкулиты, бесплодие.
Трудности проведения диагностики требуют разработки новых высокоэффективных, в том числе «экспресс», методов диагностики для раннего выявления инфекции, а обоснование применения патогенетических метаболических препаратов (Элькар®) позволит эффективно корректировать патологические состояния, вызываемые ЭВ. При изучении катамнеза ЭВИ возрастает необходимость в разработке рекомендаций по реабилитации детей, перенесших тяжелые формы ЭВИ.
Таким образом, хотя большинство энтеровирусных инфекций и являются бессимптомными (90% случаев), эти энтеровирусы ответственны за различные инфекционные синдромы. Прогноз их развития зависит от инфекционной дозы, органа-мишени, возраста, пола, иммунного статуса пациента, проводимой патогенетической терапии и реабилитации.
Литература
- Домашенко О.Н., Гридасов В.А. Энтеровирусная инфекция: новая классификация вирусов, клинические формы, перспективы исследования // Университетская клиника. 2018. № 2(27). С. 75-81.
- Протасеня, И.И. Энтеровирусная инфекция у детей. LAP Lambert Akademic Publishing, 2015. 274 с.
- Toczylowski K., Wieczorek M., Bojkiewicz E. et al. Children's enterovirus infections of the central nervous system in Bialystok, Poland: epidemiology, viral types and seasonal factors // Viruses. 2020. Vol. 12. No. 8. P. 893.
- Zell R., Delwart E., Gorbalenya A.E. et al. ICTV Virus taxonomy profile: Picornaviridae // The Journal of General Virology. 2017. Vol. 98. No. 10. P. 2421-2422.
- Программа «Эпидемиологический надзор и профилактика энтеровирусной (неполио) инфекции на 2015-2017 гг.». rospotrebnadzor.ru/deyatelnost/epidemiological-sur…
- Messacar K., Asturias E.J, Hixon A.M et al. Enterovirus D68 and acute flaccid myelitis-evaluating the evidence for causality // The Lancet. Infectious Diseases. 2018. Vol. 18. No. 8. P. 239-247.
- Hassel С., Mirand А., Farkas А. et al. Phylogeography of coxsackievirus A16 reveals global transmission pathways and recent emergence and spread of a recombinant genogroup // Journal of Virology. 2017. Vol. 91. No. 18.
- Midgley C.M., Watson J.T., Nix W.A. et al. Severe respiratory illness associated with a nationwide outbreak of enterovirus D68 in the USA (2014): a descriptive epidemiological investigation // The Lancet. Respiratory Medicine. 2015. Vol. 3. No. 11. P. 879-887.
- Dyrdak R., Grabbe M., Hammas В. Outbreak of enterovirus D68 of the new B3 lineage in Stockholm, Sweden, August to September 2016 // Euro Surveillance. 2016. Vol. 21. No. 46. P. 30403.
- Enteroviruses detections with severe neurological symptoms among children and adults in European countries // Communicable disease threats report CDTR Week 46, 13-19 November 2016.
- Молекулярно-генетические исследования при мониторинге энтеровирусной инфекции. Методические рекомендации МР 4.4.0136-18. М., 2019.
- Неудахин Е.В. Роль левокарнитина в реабилитации детей с перинатальной патологией // Consilium Medicum. 2019. № 3. С. 115-121.
- Неудахин Е.В. О целесообразности использования препаратов карнитина при лечении синдрома вегетативной дистонии у детей // Практика педиатра. 2017. № 1. С. 52-59.
- Гончарова О.В. Реабилитация детей с острыми респираторными инфекциями // Вопросы практической педиатрии. 2018. Т. 13. № 5. С. 84-90.
- Османов И.М., Бекмурзаева Г.Б., Мумладзе Э.Б., Тамбиева Е.В. Место энерготропной терапии в лечении инфекции мочевой системы // Практика педиатра. 2019. № 2. С. 42-48.
- Морозов С.Л. Часто болеющие дети. Современный взгляд педиатра // РМЖ. Медицинское обозрение. 2019. № 8. С. 7-9.
- Руженцова Т.А., Горелов А.В., Смирнова Т.В., Счастных Л.А. Диагностика и лечение инфекционных поражений миокарда у детей // Детская больница. 2012. № 2. С. 62-66.
- Хорошилов И.Е. Карнитин: Роль в организме человека и возможности терапевтического применения при различных заболеваниях. Врач. 2017. № 3. С. 2-6.
- Брин И.Л., Дунайкин М.Л., Лисицина С.В. Проблемы дозирования препаратов карнитина в детском возрасте // Российский вестник перинатологии и педиатрии. 2014. Т. 59. № 4. С. 16-22.

