Простой герпес (ПГ) у взрослых. Клинические рекомендации.
Статьи
Простой герпес (ПГ) у взрослых
- Международная ассоциация специалистов в области инфекций (МАСОИ)
Оглавление
- Список сокращений
- Термины и определения
- 1. Краткая информация
- 2. Диагностика
- 3. Лечение
- 4. Реабилитация
- 5. Профилактика и диспансерное наблюдение
- 6. Дополнительная информация, влияющая на течение и исход заболевания
- Критерии оценки качества медицинской помощи
- Список литературы
- Приложение А1. Состав рабочей группы
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение А3. Связанные документы
- Приложение Б. Алгоритмы ведения пациента
- Приложение В. Информация для пациентов
Список сокращений
АГ– антиген
АлАТ – аланинаминотрансфераза
АсАТ – аспартатаминотрансфераза
АТ– антитела
В/м – внутримышечно
ВИЧ – вирус иммунодефицита человека
ВОЗ – Всемирная организация здравоохранения
ВПГ – вирус простого герпеса
ВПГ-1– вирус простого герпеса первого типа
ВПГ- 2– вирус простого герпеса второго типа
ГГТП – гаммаглюмамилтраспептидаза
Д.м.н. – доктор медицинских наук
ДНК – дезоксирибонуклеиновая кислота
ЖКТ – желудочно-кишечный тракт
ИППП – инфекции, передающиеся половым путем
ИФА – иммуноферментный анализ
К.м.н. – кандидат медицинских наук
КТ – компьютерная томография
Мг – миллиграмм
Мл – миллилитр
МЗ РФ – Министерство здравоохранения Российской Федерации
МКБ-10 – Международная классификация болезней, травм, и состояний, влияющих на здоровье 10-го пересмотра
МРТ – магнитно-резонансная томография
ПВТ – противовирусная терапия
ПГ – простой герпес
ПЦР – полимеразная цепная реакция
РАН – Российская академия наук
РКИ – рандомизированное контролируемое исследование
РФ – Российская Федерация
ФЗ – федеральный закон
ЦИК – циркулирующие иммунные комплексы
ЦНС – центральная нервная система
ЩФ – щелочная фосфатаза
IgА – иммуноглобулины класса А
IgМ – иммуноглобулины класса М
IgG – иммуноглобулины класса G
Термины и определения
Афта – небольшое изъязвление (единичное или множественное) слизистой оболочки в виде эрозии, круглой или овальной формы, имеющее серый, белый, иногда красноватый оттенок.
Везикула (пузырек) – элемент сыпи, представляющий собой полушаровидное слегка возвышающееся над уровнем кожи, полостное образование величиной от мелкой булавочной головки (микровезикула) до небольшой горошины, располагающееся внутри эпидермиса. Полость содержит прозрачный или мутноватый серозный экссудат, изредка – серозно-геморрагический.
Качество медицинской помощи – совокупность характеристик, отражающих своевременность оказания медицинской помощи, правильность выбора методов профилактики, диагностики, лечения и реабилитации при оказании медицинской помощи, степень достижения запланированного результата.
Клинические рекомендации – документ, основанный на доказанном клиническом опыте, описывающий действия врача по диагностике, лечению, реабилитации и профилактике заболеваний, помогающий ему принимать правильные клинические решения.
Супрессивная терапия – длительный, иногда многолетний, постоянный прием низких доз противовирусных препаратов из группы синтетических ациклических нуклеозидов вне рецидива заболевания.
Эпизодическая терапия – прием противовирусных препаратов из группы синтетических ациклических нуклеозидов в момент рецидива в терапевтических дозах при соблюдении кратности и длительности лечения.
1. Краткая информация
1.1 Определение
Простой герпес (ПГ) – заболевание, возникающее в результате инфицирования вирусами простого герпеса (ВПГ) 1 или 2 антигенных типов, характеризующееся появлением одиночных или сгруппированных везикулярных высыпаний величиной 1 – 4 мм на коже и/или слизистых оболочках на отечно-эритематозном основании, протекающие с возможным поражением внутренних органов, полиморфизмом клинических проявлений и хроническим течением с тенденцией к рецидивированию.
1.2 Этиология и патогенез
Вирус простого герпеса (Herpes simplex virus;) – вирус семейства Herpesviridae подсемейства Alphaherpesvirinae, содержащий дезоксирибонуклеиновую кислоту (ДНК). ВПГ первого (ВПГ-1) и второго (ВПГ-2) типа имеют общее свойство – постоянное персистирование в организме после инфицирования [1, 2, 3, 4, 5].
Вирион состоит из следующих основных компонентов: 1) нуклеоида, располагающегося в центральной части; 2) капсида, покрывающего нуклеоид и составленного из капсомеров, 3) суперкапсидной оболочки, 4) оболочки вириона, заключающей эти структуры. Нуклеоид включает вирусный геном, состоящий из линейной двуспиральной ДНК [1, 4, 5].
При комнатной температуре и нормальной влажности ВПГ сохраняется в течение суток, при температуре 50 – 52?С инактивируется через 30 мин., а при низких температурах (-70?С) вирус способен сохранять жизнеспособность в течение 5 суток. На металлических поверхностях (монеты, дверные ручки, водопроводные краны) вирус выживает в течение 2 часов, на влажной стерильной медицинской вате и марле – в течение всего времени их высыхания (до 6 часов) [1, 4].
ВПГ неустойчив к действию физических и химических факторов, разрушается органическими растворителями, детергентами, протеолитическими ферментами [1, 4].
Уникальными биологическими свойствами ВПГ является тканевой тропизм, способность к персистенции и латенции в организме инфицированного человека [1, 4, 5].
Персистенция представляет собой способность вируса непрерывно или циклично размножаться (реплицироваться) в инфицированных клетках тропных тканей, что создает постоянную угрозу развития инфекционного процесса [1, 2, 3, 4, 5].
Основными звеньями патогенеза герпетической инфекции являются [1, 4, 6]:
-
тропизм ВПГ к эпителиальным и нервным клеткам, обусловливающий полиморфизм клинических проявлений герпетической инфекции;
-
инфицирование сенсорных ганглиев вегетативной нервной системы;
-
пожизненная персистенция ВПГ.
Первый этап патогенеза приобретенной герпетической инфекции – абсорбция и размножение вируса в месте инокуляции (у входных ворот инфекции): на слизистых оболочках полости рта, красной кайме губ, верхних дыхательных путей, конъюнктивы, половых органов, где появляются типичные пузырьковые высыпания. С током лимфы и крови ВПГ заносится в лимфатические узлы, различные внутренние органы [4, 6].
Второй этап – проникновение ВПГ неврогенным путем в сенсорные (симпатические) регионарные нервные ганглии, где он пожизненно сохраняется в латентном состоянии. Инфицирование сенсорных ганглиев – один из важных этапов патогенеза герпетической инфекции. Скорость распространения ВПГ по ходу нервных волокон достаточно высокая: через 3 часа после заражения вирус проникает в ближайшие нервные ганглии. Локализация ВПГ-1 и ВПГ-2 в ганглиях тех или иных нервов зависит от места (уровня) внедрения вируса в организм человека. ВПГ-1, вызывающий, как правило, поражение слизистой ротовой полости, носоглотки, губ, сохраняется в чувствительных ганглиях тройничного нерва (в Гассеровом узле) и других черепно-мозговых нервов. ВПГ-2, вызывающий преимущественно поражение гениталий, промежности, анальной области, нижних конечностей, ягодиц, персистирует в ганглиях пояснично-крестцового отдела позвоночника. Распространение ВПГ в центробежном направлении во время рецидива определяет анатомическое постоянство очагов поражения при рецидивах герпеса [1, 4, 6].
Распространение ВПГ-1 возможно также по зрительному нерву при офтальмогерпесе и обонятельному нерву при поражении носоглотки с последующим проникновением в центральную нервную систему (ЦНС), реже гематогенным путем [1, 4].
Диссеминация ВПГ-2 идет преимущественно гематогенным путем и в меньшей степени по ходу нервных волокон. Гематогенное распространение вируса и его занос в отдаленные нервные ганглии, в частности, крестцовых и поясничных нервов, обуславливают возможность развития герпетических поражений гениталий при неполовом заражении через слизистую ротовой полости. Именно этой особенностью патогенеза герпетической инфекции обусловлена возможность развития генитального герпеса у взрослых, не живущих половой жизнью [1, 4].
В нервных ганглиях вирус не доступен действию факторов гуморального и клеточного иммунитета – вируснейтрализующих антител и Т-киллеров. Вирус обладает способностью распространяться из инфицированной клетки в соседнюю неинфицированную клетку по межклеточным мостикам и контактам, минуя межклеточное пространство. ВПГ вызывает также слияние клеток. Тем самым вирус избегает контакта с нейтрализующими противовирусными антителами, которые в клетку не проникают. Именно указанными особенностями герпетической инфекции обусловлено явление «иммунного ускользания» ВПГ [7, 8, 9].
Возможно персистирование ВПГ в эпидермоцитах кожи, эпителии слизистых оболочек. Размножение герпеса в клетках эпителия кожи и слизистых оболочек приводит к развитию дистрофии и гибели клеток [1, 4].
Размножение вируса в региональных лимфатических узлах приводит к развитию лимфаденита, развивается внутриклеточная и внеклеточная вирусемия и последующая гематогенная диссеминация вируса во внутренние органы, мозг, отдаленные лимфоузлы и нервные ганглии [1, 4, 7].
Регистрируют адсорбцию вируса как на лейкоцитах, так и на эритроцитах. Особенность биологической аффинности (цитотропизма) вируса проявляется в инфицировании клеток мононуклеарно-макрофагальной системы, полиморфноядерных нейтрофилов, лимфоцитов. Репликация ВПГ в нейтрофилах и лимфоцитах сопровождается деструкцией последних. Что касается макрофагов, то эти клетки рассматриваются как микромодель резистентности или чувствительности макроорганизма к герпетической инфекции. Пермиссивность макрофагов для ВПГ и активная репродукция вируса в этих клетках, являются одним из патогенетических механизмом, детерминирующих чувствительность макроорганизма к герпетической инфекции и развитию клинических проявлений. Непермисивность макрофагов и развитие абортивной герпетической инфекции не способствует клинической реализации герпеса. У таких индивидуумов возможно развитие субклинических форм инфекции [10].
Герпетическая инфекция сопровождается развитием специфического гуморального и клеточного иммунитета. Особенности противогерпетического иммунитета: нестерильный (вирус не элиминируется из организма), типоспецифический (преимущественно против соответствующего типа вируса), частично перекрестный [8, 9, 11, 12, 13, 14].
Неэффективность противогерпетического иммунитета обусловлена тем, что вирус в ганглиях сохраняется не в виде интактных частиц, а в форме субвирусных структур – ДНК-белкового комплекса. О неэффективности гуморального иммунитета свидетельствуют рецидивы герпеса на фоне высоких титров противогерпетических антител. Противовирусные антитела не защищают от заражения тем же вирусом в другое место (аутоинокуляция), либо серологически родственным штаммом вируса в то же место (суперинфекция). После рецидива герпеса регистрируют недостоверное повышение титров антител к ВПГ, у меньшей части больных титры антител не меняются. В тоже время, высокий уровень гуморальных антител может обеспечить защиту плода от внутриутробного инфицирования [8, 9, 11].
Клеточный иммунитет, опосредованный Т-киллерами, естественными киллерами, макрофагами играет важную роль в предупреждении рецидива герпеса [13].
Важную роль играет местный иммунитет (мукозальный) при рецидивирующем герпесе. Обострение герпеса регистрируют на фоне снижения местного иммунитета при травмах, хирургических вмешательствах, половом контакте с травматизацией слизистых оболочек, местном применении кортикостероидов, обработке лица жидким азотом для омоложения кожи и др. [1, 4, 8].
Репродукция вируса в лимфоцитах, нейтрофилах, моноцитах-макрофагах лежит в основе иммунодефицита по Т-клеточному типу, который выявляется при герпетической инфекции. Механизмы иммунодепрессивного действия обусловлены подавлением хемотаксиса и снижением активности процесса фагоцитоза, угнетением функции естественных киллеров, реакции бласттрансформации лимфоцитов, возможной прямой стимуляции Т-супрессоров. Кроме того, регистрируют 50% снижение уровней иммуноглобулинов класса IgG2, авидности иммуноглобулинов класса IgМ. Регистрируют образование циркулирующих иммунных комплексов (ЦИК), их имуннопатологическое действие [9, 10, 13].
Существенную роль в патогенезе герпеса играет интерферонодефицит. Регистрируют подавление интерфероновой реакции лейкоцитов, их способности синтезировать in vitro альфа-интерферон при обработке (стимуляции) индукторами интерферона – интерфероногенами. Снижена способность лимфоцитов синтезировать гамма-интерферон, фибробластов – бета-интерферон. Уровни альфа-, бета- и гамма-интерферонов у больных рецидивирующей герпетической инфекцией снижены в 10 – 20 раз по сравнению с контрольной группой. Регистрируют также местное подавление образования интерферона в очагах герпетических поражений [8, 9, 11, 12, 14].
Важным патогенетическим компонентов герпетической болезни является сенсибилизация макроорганизма антигеном ВПГ. Развивается реакция гиперчувствительности замедленного типа с инфильтрацией клеточных элементов на месте образующихся высыпаний, которые клинически регистрируются в виде покраснения, отечности, зуда в очаге герпетического поражения. С другой стороны наблюдают более тяжелое клиническое течение герпеса у аллергиков [1, 4].
1.3 Эпидемиология
Источник инфекции – больные люди и вирусоносители [1, 2, 3, 4, 6].
Пути и механизмы заражения ВПГ многочисленны и разнообразны, определяют особенности патогенеза герпетической инфекции.
ВПГ может присутствовать в различных биологических жидкостях организма: в слюне, моче, сперме, секретах из шейки матки, уретры, влагалища, отделяемом из носоглотки, слезной жидкости, в крови, в ликворе, в везикулярной жидкости высыпаний и др. [1, 4, 15, 16, 17, 18].
Входными воротами для вируса являются слизистые губ, ротовой полости, носоглотки, гениталий, конъюнктивы глаз, а так же кожа. Уровень риска заражения герпесом повышается при травматизации слизистых, например, при заболеваниях урогенитального тракта, сопровождающихся нарушением интактности слизистых и развитием язв, эрозий и трещин [1, 4, 16].
Инфицирование происходит при попадании вируссодержащих биологических жидкостей на слизистые при интимных контактах: половым путем (генито-генитальные, генито-анальные, орогенитальные контакты), при поцелуях. Возможна аутоинокуляция – механический перенос вируса из герпетического очага в другие места, например, занос руками вируса из полости рта при герпетическом стоматите на конъюнктиву глаза, в области гениталий, на любые участки тела через микроповреждения кожи [1, 4, 19, 20].
Присутствие вируса в слюне обеспечивает возможность его передачи воздушно-капельным путем, хотя этот путь заражения к ведущим не относится [1, 4, 16].
К горизонтальным путям передачи следует отнести ятрогенные: гемотрансфузионный, трансплантционный (при пересадке органов и тканей) [1, 4].
Вертикальный механизм заражения включает внутриутробное инфицирование плода через материнскую кровь, а также восходящим путем (из инфицированной шейки матки в полость матки беременной). Высокий риск заражения регистрируется при преждевременном разрыве оболочек плодного яйца. Наиболее часто заражение плода ВПГ происходит во время родов при прохождении плода через инфицированный родовой канал. Риск инфицирования плода может достигнуть 50% при развитии первичного генитального герпеса у беременной до 6 недель перед родами, при рецидиве генитального герпеса риск инфицирования плода оценивается в 3 – 5% [21, 22].
По оценкам экспертов, во всем мире ВПГ-1 инфицированы около 3,7 миллиарда человек в возрасте до 50 лет (67% населения), а ВПГ-2 инфицировано около 417 млн. человек в возрасте от 15 до 49 лет (11%) [23, 24].
Согласно данным Всемирной организации здравоохранения (ВОЗ), смертность от герпетических энцефалитов и диссеминированных форм болезни (15,8%) занимает второе место после гриппа (35,8%) в общей структуре инфекционных заболеваний. [24, 25].
В России общее число пациентов с хроническими формами офтальмогерпеса, кожными и генитальными формами заболевания, герпетическими стоматитами в настоящее время приближается к 20 млн. человек [18, 26, 27].
По данным сероэпидемиологических исследований показатель выявления антител к ВПГ-1 и ВПГ-2 составляет от 70 до 90% и более. Инфицированность населения зависит от социально-экономического уровня жизни, бытовых традиций различных этнических групп населения. При герпетической инфекции манифестные клинические формы заболевания развиваются в 10 – 15% случаев, малосимптомные формы – в 10%, бессимптомная секреция вируса регистрируется – в 5%. Лица без эпизодов герпеса в анамнезе составляют 70% [16, 18, 25].
Генитальный герпес занимает второе место среди вирусных инфекций, передающихся половым путем (ИППП) после папилломавирусной инфекции. Всего пациентов с генитальным герпесом в России – около 8 млн. Около трети женщин детородного возраста инфицированы ВПГ-2 [19].
Частота регистрации неонатального герпеса за последние 30 лет возросла в 4 раза. При первичном генитальном герпесе во время беременности 50% детей, а при рецидивах герпеса только 5% детей рождаются с признаками очагового или генерализованного герпеса. Частота неонатального герпеса, по разным данным, составляет от 1:2500 до 1:60 000 [21, 26].
1.4 Кодирование по МКБ-10
1.4.1 Инфекции, вызванные вирусом герпеса [herpes simplex] (B00):
B00.0 Герпетическая экзема
B00.1 Герпетический везикулярный дерматит
В00.2 Герпетический гингивостоматит и фаринготонзиллит
В00.3+ Герпетический менингит (G02.0*)
В00.4+ Герпетический энцефалит (G05.1*)
В00.5+ Герпетическая болезнь глаз
В00.7 Диссеминированная герпетическая болезнь
В00.8 Другие формы герпетических инфекций
В00.9 Герпетическая инфекция неуточненная
1.4.2 Аногенитальная герпетическая вирусная инфекция [herpes simplex] (A60):
А60.0 Герпетические инфекции половых органов и мочеполового тракта
А60.1 Герпетические инфекции перианальных кожных покровов и прямой кишки
А60.9 Аногенитальная герпетическая инфекция неуточненная
1.5 Классификация
1.5.1 По механизму инфицирования:
-
приобретенная:
-
первичная;
-
рецидивирующая;
-
врожденная.
1.5.2 По форме инфекционного процесса:
-
латентная (бессимптомное носительство);
-
локализованная (один очаг поражения);
-
распространенная (два и более очага поражения);
-
генерализованная (висцеральная, диссеменированная).
1.5.3 По длительности присутствия вируса в организме:
-
острая;
-
хроническая;
-
медленная.
1.5.4 По клиническим проявлениям и локализации:
-
типичные формы:
-
поражения слизистых оболочек желудочно-кишечного тракта: стоматит, гингивит, фарингит, эзофагит и др.;
-
поражения глаз (офтальмогерпес): конъюктивит, кератит, иридоциклит, неврит зрительного нерва, оптикомиелит и др.;
-
поражения кожи: герпес губ, герпес крыльев носа, лица, рук, ягодиц и т.д.;
-
поражения половых органов (генитальный герпес): поражение слизистых оболочек полового члена, вульвы, влагалища, цервикального канала и т.д.;
-
поражения нервной системы: менингит, энцефалит, менингоэнцефалит, неврит, менингоэнцефалорадикулит, поражения бульбарных нервов и др.;
-
поражение внутренних органов: трахеобронхит, пневмония, гепатит, панкреатит и др.)
-
генерализованный ПГ: висцеральная форма (пневмония, гепатит, эзофагит и др.) и диссеминированная форма (сепсиса).
-
атипичные формы:
-
абортивная;
-
отечная;
-
зостериформный простой герпес;
-
герпетиформная экзема Капоши (варицеллеформный пустулез Капоши);
-
язвенно-некротическая;
-
геморрагическая;
-
эрозивно-язвенная;
-
диссеминированная;
-
рупиоидная;
-
мигрирующая.
1.5.5 По наличию осложнений:
-
без осложнений;
-
с наличием осложнений.
1.5.6 По периоду заболевания:
-
продромальный период;
-
катаральный период;
-
период высыпаний;
-
период регресса.
- .5.7По степени тяжести:
-
легкая;
-
средней тяжести;
-
тяжелая.
1.5.8 По стадии:
-
активная:
-
с клиническими проявлениями (рецидив);
-
бессимптомная;
-
неактивная.
1.5.9 По форме инфекции:
-
первичная инфекция:
Развивается после заражения вирусом неинфицированного ранее лица. В крови
пациентов антитела к ВПГ до развития герпетической инфекции не выявляются.
Инфекция сопровождается появлением противовирусных антител
(сероконверсией), 4-кратным нарастанием концентрации иммуноглобулинов
класса G.
-
первичная клиническая инфекция;
-
первичная субклиническая инфекция (характеризуется бессимптомной секрецией вируса);
-
первичная инфекция с одиночным местом внедрения вируса (например, через слизистую гениталий или ротовой полости);
-
первичная инфекция с множественными входными воротами инфекции (слизистая гениталий, ротовой полости, сосков молочных желез, кожные покровы промежности, ягодиц, внутренней поверхности бедер, перианальной области и т.д.).
-
аутоинокуляция (механический перенос вируса у инфицированного с одного участка на другие участки тела (например, из ротовой полости на гениталии).
-
латентная инфекция (неактивная стадия инфекции; вирус не обнаруживается в биологических материалах (слюне, моче, секретах гениталий), но сохраняется в виде ДНК-белкового комплекса в нервных ганглиях).
-
первый эпизод герпеса (впервые выявленные клинические проявления герпеса у ранее инфицированных лиц).
-
рецидив герпеса (повторно регистрируемые клинические проявления герпеса).
-
коинфекция (субклиническая и клиническая; инфицирование одновременно двумя вирусами).
-
суперинфекция (субклиническая и клиническая; наслоение одной инфекции на другую – например, заражение ВПГ-2 половым путем лица, страдающим герпетическим стоматитом, вызванным ВПГ-1).
2. Диагностика
Скрининговое обследование на ВПГ рекомендовано следующим группам населения [1, 4, 6, 16, 17, 18, 19, 20, 24, 28, 29]:
-
Планирование беременности;
-
Женщины, имеющие в анамнезе либо на момент обращения типичные герпетические высыпания любой локализации, в т. ч. рецидивирующий генитальный герпес, или наличие пузырьковых и/или эрозивных высыпаний на коже, ягодицах, бедрах, слизисто–гнойные выделения из влагалища;
-
Наличие полового контакта с партнером, имеющим генитальный герпес;
-
Атипичная форма заболевания: отсутствие зуда или жжения, отсутствие везикул, веррукозные узелки; обширные кожные поражения (до 10% случаев предполагаемого опоясывающего герпеса обусловлено не вирусом varicella zoster, а ВПГ);
-
Женщины с отягощенным акушерским анамнезом (перинатальные потери, рождение ребенка с врожденными пороками развития);
-
Беременные женщины (в первую очередь имеющие ультразвуковые признаки внутриутробной инфекции, лимфоаденопатии, лихорадку, гепатит и гепатоспленомегалию неясного генеза);
-
Пациенты с сепсисом, гепатитами, менингоэнцефалитом, пневмонией, поражением глаз (увеит, кератит, ретинит, ретинальный некроз), поражением желудочно-кишечного тракта;
-
Лица, относящиеся к группам риска по заражению ВПГ (потребители инъекционных наркотиков и их половые партнеры; лица, оказывающие услуги сексуального характера, и их половые партнеры; мужчины, практикующие секс с мужчинами; лица с большим количеством случайных половых партнеров);
-
Пациенты с иммунодефицитом (пациенты с ВИЧ-инфекцией, онкологическими заболеваниями, пациенты на гемодиализе, пациенты на лечении иммунодепрессантами и др.).
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1а).
-
При сборе анамнеза рекомендовано обратить внимание на факт контакта с больным ПГ, эпизоды ПГ в анамнезе с характерной повторяющейся локализацией высыпаний для каждого пациента («locus minoris») [1, 4, 17].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b).
-
При сборе анамнеза рекомендовано обратить внимание на периодические подъемы температуры (лихорадку), симптомы интоксикации (немотивированную усталость, слабость, снижение работоспособности, раздражительность) [1, 4].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
2.2 Физикальное обследование
На этапах постановки диагноза, обследования после завершения противовирусной терапии (ПВТ), диспансерного наблюдения:
-
Рекомендовано начать с общего осмотра кожных покровов и видимых слизистых оболочек ЛОР-органов и половых органов, органа зрения с выявлением характерных высыпаний [1, 4, 17, 19, 20].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Комментарий: с использованием шпателя (зонда) определяют состояние надгортанника, оценивают текстуру и плотность поверхности, обращают внимание на наличие пятен и характер дефектов слизистой полости рта. При осмотре обращают внимание на локализацию, величину, глубину патологических изменений (везикулы, афты), болезненность или отсутствие чувствительности при исследовании.
-
Рекомендовано проведение осмотра и пальпации лимфатических узлов с определением их болезненности и размеров [1, 4].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Комментарий: исследование лимфатических узлов проводится бимануально и билатерально, сравнивая правую и левую области исследования. Осмотр лимфатических узлов позволяет получить информацию о наличие воспалительного, инфекционного и онкологического процессов.
На этапе постановки диагноза:
-
Рекомендовано провести клинический анализ крови с исследованием лейкоцитарной формулы; общий анализ мочи; биохимический анализ крови: общий билирубин и его фракции, аланинаминотрансфераза (АлАТ), аспартатаминотрансфераза (АсАТ), гамма-глютамилтранспептидаза (ГГТП), щелочная фосфатаза (ЩФ), глюкоза, мочевина, креатинин [1, 4].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Комментарии. Выполняется для определения увеличения активности АлАТ, АсАТ, ЩФ, ГГТП, что позволяет оценить наличие и активность синдромов цитолиза и холестаза.
-
Рекомендовано проведение серологического исследования сыворотки крови, содержимого везикулезных или пустулезных высыпаний и других локусов (носоглотки, конъюнктивы, уретры, влагалища, цервикального канала) с определением антигена (АГ) ВПГ методом иммуноферментного анализа (ИФА) [1, 4, 29, 30, 31, 32, 33, 34].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1а).
Комментарий: При использовании метода ИФА чувствительность исследования составляет 95% и более, специфичность при манифестном герпесе варьирует от 62 до 100%. Однако большинство наборов реагентов для выявления АГ ВПГ методом ИФА не позволяют провести дифференцирование серотипов вируса.
-
Рекомендовано проведение серологического исследования сыворотки крови с определением антител (АТ) к ВПГ разных классов (IgА, IgM, IgG), суммарных к АГ ВПГ обоих типов или типоспецифичных, а так же авидности АТ ВПГ IgG методом ИФА [1, 4 29, 30, 31, 32, 33, 34, 35, 36].
Уровень убедительности рекомендаций А (уровень достоверности доказательств –1а ).
Комментарий: Наибольшее диагностическое значение имеет детекция АТ ВПГ IgM как показателя активности процесса – их выявление свидетельствует об остром заболевании, реинфекции, суперинфекции или реактивации. Однако в клинически выраженных случаях, в т. ч. при типичном течении генитального или неонатального герпеса, специфические АТ ВПГ IgM выявляются редко (в 3 – 6% случаев). Определение авидности АТ ВПГ IgG несет низкую информационную нагрузку: реактивация при клинически выраженных случаях сопровождалась наличием высокоавидных АТ. Тест на выявление АТ ВПГ IgА является методом выбора наряду с определением ДНК либо АГ ВПГ при определении активности инфекционного процесса.
-
Рекомендовано проведение молекулярно-биологического исследования различного биологического материала для обнаружения ДНК ВПГ-1 и/или ВПГ-2 (качественный тест, количественный тест) [1, 4, 29, 32, 33, 37, 38, 39, 40, 41, 42].
Уровень убедительности рекомендаций A (уровень достоверности доказательств –1а).
Комментарий: Выявление ВПГ в соскобах со слизистых оболочек полости рта, урогенитального тракта, в отделяемом пузырьковых высыпаний (везикул) и эрозивно-язвенных поражений кожи с помощью полимеразной цепной реакции (ПЦР) является методом выбора. Несомненную ценность имеет определение количества ДНК ВПГ методом ПЦР в режиме реального времени, результаты исследования можно использовать как с диагностической целью, так и для оценки эффективности лечения. Особое значение имеет при асимптомном герпесе, когда заболевание не имеет явной клинической картины, но патологические процессы присутствуют, и больные, выделяя вирус при контактах, инфицируют партнеров. Обследованию методом ПЦР в обязательном порядке должны подвергаться беременные, поскольку нахождение вируса герпеса в половых путях даже у серопозитивных, имеющих иммунитет к вирусу герпеса, резко повышает риск инфицирования плода. ПЦР-исследование может использоваться также для дифференциальной диагностики ВПГ-1 и ВПГ-2.
-
Рекомендовано выявление телец Арагао в окрашенных серебрением по Морозову в мазках жидкости везикул при обычной или электронной микроскопии, выявление клеток Цанка.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
-
Рекомендовано выполнение люмбальной пункции (при наличии общемозговой или очаговой неврологической симптоматики).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Диагностическая люмбальная пункция выполняется при наличии менингеальных или очаговых симптомов, подозрении на поражение головного мозга с исследованием уровня общего белка и фракций в ликворе, микроскопическим исследованием ликвора, подсчетом клеток в счетной камере (определение цитоза), исследованием ликвора на наличие ДНК ВПГ и ДНК иных возбудителей менингоэнцефалита и энцефалита у пациентов с поражением ЦНС.
-
Рекомендовано исследование ликвора при наличии клинических признаков поражения ЦНС [1, 4, 29].
Уровень убедительности рекомендаций B (уровень достоверности доказательств –2).
Комментарий: Исследование ликвора позволяет определить содержание белка, глюкозы, цитоз, а также выявить маркеры ВПГ, определить индекс отношения АТ в сыворотке крови к титру АТ в ликворе (300:1 и более).
На этапе обследования после завершения ПВТ:
-
Рекомендовано проведение контрольного клинического анализа крови с исследованием лейкоцитарной формулы; общий анализ мочи; биохимический анализ крови: общий билирубин и его фракции, АлАТ, АсАТ, креатинин [1, 4].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
-
Рекомендовано проведение контрольного молекулярно-биологического исследования различного биологического материала для обнаружения ДНК ВПГ-1 и/или ВПГ-2 (качественный тест, количественный тест) [1, 4, 29, 32, 33, 37, 38, 39, 40, 41, 42].
Уровень убедительности рекомендаций A (уровень достоверности доказательств –1b).
-
Рекомендовано проведение контрольного исследования ликвора при наличии клинических признаков поражения ЦНС [1, 4, 29].
Уровень убедительности рекомендаций B (уровень достоверности доказательств –2).
На этапе диспансерного наблюдения:
-
Рекомендовано провести клинический анализ крови с исследованием лейкоцитарной формулы; общий анализ мочи; биохимический анализ крови: общий билирубин и его фракции, АлАТ, АсАТ, креатинин. [1, 4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
-
Рекомендовано проведение серологического исследования сыворотки крови с определением АТ к ВПГ разных классов (IgА, IgM, IgG), суммарных к АГ ВПГ обоих типов или типоспецифичных, а так же авидности АТ ВПГ IgG методом ИФА [1, 4 29, 30, 31, 32, 33, 34, 35, 36].
Уровень убедительности рекомендаций B (уровень достоверности доказательств –3).
-
Рекомендовано проведение контрольного молекулярно-биологического исследования различного биологического материала для обнаружения ДНК ВПГ-1 и/или ВПГ-2 (качественный тест, количественный тест) [1, 4, 29, 32, 33, 37, 38, 39, 40, 41, 42].
Уровень убедительности рекомендаций A (уровень достоверности доказательств –1b).
2.4 Инструментальная диагностика
На этапе постановки диагноза:
-
Рекомендовано выполнение ультразвукового исследования (УЗИ) органов брюшной полости и забрюшинного пространства [1, 4, 17, 32].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарий: УЗИ органов брюшной полости и забрюшинного пространства проводится для диагностики увеличения и изменения структуры печени и селезенки, лимфатических узлов, исключения сопутствующей патологии желудочно-кишечного тракта, что в некоторых случаях может иметь решающее значение в определении тактики лечения
-
Рекомендовано проведение компьютерной томографии (КТ) или магнитно-резонансная томография (МРТ) головного мозга (при наличии общемозговой или очаговой неврологической симптоматики) [1, 4, 32, 43].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарии: Дифференциальная диагностика в продромальном периоде, когда отсутствуют пузырьковые высыпания, но имеются симптомы интоксикации, лихорадка с менингоэнцефалитом, опухолями мозга, сосудистыми изменениями и т.д. Наличие очагов некроза в мозге, чаще в лобно-височной области мозга (с 5 – 7-го дня заболевания). При герпетическом энцефалите регистрируют уменьшение плотности ткани в височных долях, расширение желудочков, смещение центральных структур головного мозга в сторону большего поражения.
-
Рекомендовано проведение нейросонографии (при наличии общемозговой или очаговой неврологической симптоматики) [1, 4, 32].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарии: Выполняется с дифференциально-диагностической целью при наличии очаговой неврологической симптоматики, судорог, признаков внутричерепной гипертензии.
На этапе диспансерного наблюдения
-
Рекомендовано выполнение УЗИ органов брюшной полости и забрюшинного пространства (при наличии показаний) [1, 4, 17, 32].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
-
Рекомендовано проведение КТ или МРТ головного мозга (при наличии общемозговой или очаговой неврологической симптоматики) [1, 4, 32, 43].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
2.5 Иная диагностика
-
При наличии показаний рекомендовано проведение консультаций смежных специалистов – врача-офтальмолога, врача-дерматовенеролога, врача-невропатолога.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
2.6 Дифференциальная диагностика
Наибольшую трудность для диагностики представляют случаи, при которых отсутствуют характерные эпидемиологические данные, а клиническая симптоматика ограничивается общеинтоксикационными симптомами.
Диагностические трудности возникают в продромальном периоде болезни, когда отсутствуют пузырьковые высыпания, но имеются симптомы интоксикации, лихорадка и др., а также при генерализованных формах инфекции (поражении внутренних органов, нервной системы) в отсутствии характерных высыпаний. В подобных случаях ранние проявления ПГ следует дифференцировать со стенокардией, инфарктом, инсультом, плевритом, холециститом, панкреатитом и др. При данных состояниях необходима консультация терапевта, кардиолога, хирурга, проведение электрокардиографии, рентгенграфии, УЗИ органов желудочно-кишечного тракта и др.
В период клинических проявлений болезни при появлении сыпи дифференциацию проводят с высыпаниями при опоясывающем герпесе, роже, дерматите; в случае с генерализованной формой ПГ – с ветряной оспой. В отличие от ПГ рожа характеризуется более яркой гиперемией, большей отграниченностью отека от окружающей здоровой кожи, валикообразными, неровными краями. При этом очаги поражения сплошные, кожа более плотная. Клинически малоотличимые зостериформный ПГ и опоясывающий герпес различают по результатам вирусологического обследования.
Причинами развития язвенного поражения слизистой полости рта могут быть:
-
хронические заболевания желудочно-кишечного тракта (ЖКТ): гастрит, гастродуоденит, панкреатит и др.;
-
различные инфекции: ВИЧ-инфекция, вирус Эпштейна – Барр, цитомегаловирус, 6-й тип герпесвируса человека;
-
аутоиммунные и иммунодефицитные заболевания: болезнь Бехчета, болезнь или синдром Рейтера, системная красная волчанка, синдром Стивенса –Джонсона, циклическая нейтропения, периодическая болезнь;
-
заболевания неясной этиологии: болезнь Крона, синдром PFAPA («Periodic Fever, Aphtous stomatitis, Pharyngitis and Adenitis») и др.
|
Заболевание |
Генитальные язвы |
Примечание |
|
Сифилис |
В первичном периоде может сопровождаться образованием множественных первичных аффектов – твердых шанкров, во вторичном периоде – эрозивных папул |
Положительные серологические исследования на сифилис, обнаружение T.pallidum при микроскопии в темном поле |
|
Мягкий шанкр |
В начальной стадии образуются эрозии и язвы, сопровождающиеся болезненностью |
Образуются округлые, а не полициклические эрозивно-язвенные элементы, отсутствует их сгруппированность. Реакция паховых лимфатических узлов ярко выражена. При микроскопии отделяемого язв обнаруживается возбудитель мягкого шанкра – Haemophilus ducreyi |
|
Паховая гранулема |
Начинается с образования узелка, пустулы, которые быстро изъязвляются, формируя первичный аффект – язву. По периферии часто возникают дочерние язвы-сателлиты |
Характерен выраженный распад тканей, края язв отечны, гиперемированы, несколько приподняты. При микробиологическом исследовании обнаруживают возбудитель – тельца Донована (Calyimmatobacterium granulomatis) |
|
Чесотка |
Может протекать с эрозивными поражениями половых органов, возникающими вследствие расчесов и мацерации кожи серозным отделяемым |
Наличие зудящих высыпаний в межпальцевых промежутках, на запястье, в локтевых ямках и в других типичных для чесотки местах. Обнаружение чесоточного зудня при микроскопии |
|
Фиксированная эритема |
Возникает в ответ на прием различных медикаментов – сульфаниламидных препаратов, снотворных средств и др. Может сопровождаться образованием эрозивных элементов как на половых органах, так и в ротовой полости и на других участках кожи |
Характерен симптом «бычьего глаза»: эрозия образуется в центральной части пятна, интенсивность окраски которого убывает от центра к периферии. Тщательно собранный анамнез помогает установить правильный диагноз |
|
Эритроплазия Кейра |
Характеризуется образованием розовато-красной бархатистой бляшки, которая иногда изъязвляется с появлением серозного отделяемого |
Возникает после 50 лет. Установить диагноз помогают клиническая картина и гистологическое исследование |
|
Болезнь Бехчета |
Сопровождается появлением афтозных болезненных высыпаний на половых органах |
Высыпания имеются также в ротовой полости – афтозный стоматит. Характерны поражения глаз. Диагноз устанавливают на основании клинических признаков |
|
Болезнь Крона |
Терминальный илеит может протекать с образованием язв, расположенных как на половых органах, так и в перианальной области |
Характерны абдоминальные боли, рубцы вследствие ранее перенесенной аппендэктомии, астеничное телосложение больных |
|
Контактный дерматит, травма |
Появляются вследствие аппликации на половые органы различных антисептиков, мазей и других средств. Встречаются аллергические реакции на латекс и смазку презервативов. Могут сопровождаться появлением эрозий на половом члене |
Установить диагноз помогает тщательно собранный анамнез |
|
Пузырные дерматозы |
Могут манифестировать образованием пузырных, а затем эрозивно-язвенных элементов, в том числе и на половых органах |
Имеются высыпания также и на других участках кожи, в ротовой полости. При дифференциальной диагностике используют цитологическое исследование, прямую иммунофлюоресценцию. |
|
Стрептококковое импетиго, шанкриформная пиодермия |
Гнойничковые заболевания, которые могут протекать с образованием эрозивно-язвенных элементов |
В отличие от герпетических поражений в отделяемом эрозий и язв обнаруживают стрептококки и стафилококки |
|
Баланопостит |
Может сопровождаться образованием болезненных эрозий на головке и внутреннем листке крайней плоти |
Часто возникает при сопутствующем течении уретрита вследствие мацераций уретральным отделяемым. Нередко выявляют снижение толерантности глюкозы. Диагноз устанавливают путем исключения других заболеваний |
|
Плазмоклеточный баланит Зуна |
Протекает с образованием эритематозных эрозивных безболезненных, четко очерченных бляшек с блестящей поверхностью на коже головки полового члена |
Гистологическое исследование участка пораженной кожи выявляет плазмоцитарный инфильтрат |
Таблица 1. Дифференциальная диагностика генитального герпеса
Дифференциальная диагностика простого герпеса, сопровождающего поражением нервной системы проводится с бактериальными менингитами, абсцессом головного мозга, туберкулёом, болезнью кошачьих царапин, пятнистой лихорадкой Скалистых Гор, эрлихиозом, сифилисом, болезнью Лайма, лептоспирозом, амёбным энцефалитом (вызванные видами Naegleria и Acanthamoeba), токсоплазмозом, инсультом, субарахноидальным кровоизлиянием, опухолями ЦНС, травмой головного мозга, системной красной волчанкой, отравлением, гипогликемией.
3. Лечение
На выбор тактики лечения оказывают влияние следующие факторы [1, 4,17, 32, 44]:
-
период болезни;
-
клиническая форма болезни;
-
тяжесть заболевания;
-
возраст больного;
-
наличие и характер осложнений;
-
доступность и возможность выполнения лечения в соответствии с необходимым видом оказания медицинской помощи.
Информация, касающаяся доз, показаний к применению и способов применения лекарственных средств, содержащаяся в данных рекомендациях, может отличаться от информации, указанной в инструкции по их медицинскому применению. Для получения полной информации о применении того или иного препарата следует внимательно ознакомиться с вложенной в упаковку аннотацией, составленной производителем.
Персональная ответственность за интерпретацию и использование настоящих рекомендаций лежит на лечащем враче.
3.1 Консервативное лечение
Цели лечения:
-
подавление репликации вируса;
-
снижение тяжести и продолжительности болезни;
-
предотвращение развития осложнений.
Пациенты с первичным эпизодом болезни или рецидивом требуют назначения противовирусного лечения для минимизации осложнений и сокращения сроков заболевания/рецидива, а так же рецидивов в дальнейшем [1, 4, 17, 32, 44, 45].
-
Противовирусная терапия химиопрепаратами из группы синтетических ациклических нуклеозидов рекомендована в качестве метода выбора всем пациентам, инфицированным ВПГ-1 и ВПГ-2 с первичным эпизодом заболевания или с рецидивом, независимо от локализации и степени тяжести заболевания [46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b).
Комментарии: синтетические ациклические нуклеозиды:
-
ацикловир**: по 1 таблетке (0,2 г) 5 раз в день, продолжительность курса обычно 5 дней. Возможно внутривенное введение препарата по 5 мг/кг 3 раза в день (каждые 8 часов). Для внутривенного введения содержимое 1 ампулы с ацикловиром (250 мг) разводят в 10 мл изотонического раствора натрия хлорида или специального растворителя. Раствор можно вводить в виде инъекции медленно (в течение часа) или применять капельно, для чего полученный раствор (25 мг в 1 мл) разводят дополнительно в 50 мл растворителя, или содержимое 2 ампул (500 мг) ацикловира разводят в 100 мл растворителя.
-
валацикловир: рекомендуемая доза составляет 500 мг 2 раза в сутки. В случае первичного герпеса, тяжелая форма, лечение следует начинать как можно раньше, а его продолжительность должна быть увеличена с 5 до 10 дней. Валацикловир является ацикловиром второго поколения, за счет увеличения биодоступности позволяет уменьшить дозу до 3г в сутки. На фоне использования эпителизация и регресс высыпаний наступает на 3 – 4 дня раньше, чем при использовании ацикловира. Препарат может быть использован у ВИЧ-положительных пациентов.
-
фамцикловир назначают по 0,25 г 3 раза в день (или по 0,75 г 1 раз в сутки) в течение 7 дней. При генитальном герпесе – в той же дозе в течение 5 дней. При рецидивирующем генитальном герпесе по 0,25 г 2 раза в день. Механизм действия фамцикловира идентичен ацикловиру.
-
пенцикловир рекомендуется для местного применения взрослым: небольшой объем крема наносят на пораженный участок каждые 2 часа (примерно 8 раз в день). Крем также можно наносить при помощи ватного тампона или одноразового аппликатора (для упаковок, содержащих аппликаторы). Курс терапии проводят в течение 4 дней.
-
Консервативная терапия препаратами из группы интерферонов рекомендована пациентам, инфицированным ВПГ-1 и ВПГ-2, независимо от локализации и степени тяжести заболевания [1, 4, 17, 32, 44, 45, 51, 52, 60, 61, 62, 63, 64, 65, 66, 67].
Уровень убедительности рекомендаций А (уровень достоверности
доказательств – 1b).
Комментарии: Возможны различные пути введения: в/м, наружно, ректально, вагинально.
Препараты из группы интерферонов:
-
интерферон альфа 2b человеческий рекомбинантный** вводится в/м в дозе 10 000 000 ЕД ежедневно в течение 5 суток, приводит к уменьшению и прекращению боли в первые 3 дня.
-
человеческий рекомбинантный интерферон-aльфа-2b + ?-токоферол ацетат + аскорбиновая кислота. Суппозитории для ректального применения (содержание интерферона 1 000 000 МЕ) по 1 суппозиторию 2 раза в сутки через 12 часов ежедневно в течение 10 суток и более при рецидивирующей инфекции; по клиническим показаниям терапия может быть продолжена. Мазь для местного и наружного применения (содержание интерферона 40 000 МЕ) наносят тонким слоем на очаги поражения 3 – 4 раза в сутки и осторожно втирают. Продолжительность терапии – 5 – 7 дней. Гель для местного и наружного применения (содержание интерферона 36 000 МЕ) 0,5 см наносят при помощи шпателя или ватного тампона/ватной палочки на предварительно подсушенную пораженную поверхность 3 – 5 раз в день в течение 5 – 6 дней, при необходимости продолжительность курса увеличивают до исчезновения клинических проявлений. Вне зависимости от формы выпуска рекомендуется начинать терапию при появлении первых признаков поражений кожи и слизистых оболочек (зуд, жжение, покраснение). При лечении рецидивирующего герпеса желательно начинать лечение в продромальном периоде или в самом начале появления признаков рецидива
-
интерферон альфа-2b + натрия гиалуронат – комбинированный препарат, выпускаемый в свечах, в состав которого входят рекомбинантный интерферон-альфа-2 человека (500 000 МЕ в одной свече) и гиалуронат натрия в терапевтических дозировках. Вводят по 2 свечи ежедневно с 12-часовым интервалом в течение 10 дней. Курсовая доза составляет 20 свечей. Входящая в состав препарата гиалуроновая кислота, являясь основным структурным элементом соединительной ткани человека, обеспечивает равномерное и пролонгированное поступление интерферона в кровь и усиливает противовирусную активность препарата. Препарат применяется в комплексной терапии ПГ, а также при смешанной инфекции, обусловленной уреаплазмой, микоплазмой, хламидиями, гарднереллой.
-
Консервативная терапия химиопрепаратами из группы синтетических индукторов интерферона рекомендована пациентам, инфицированным ВПГ-1 и ВПГ-2, независимо от локализации простого герпеса и степени тяжести заболевания [1, 4, 17, 32, 44, 45, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1b).
Комментарии: При тяжелом течении ПГ рекомендуется комбинированная терапия индукторами интерферонов в сочетании с синтетическими ациклическими нуклеозидами. При присоединении гнойной бактериальной флоры высокоэффективна комбинация индукторов интерферона и антибиотиков
Химиопрепараты из группы синтетических индукторов интерферона:
-
Оксодигидроакридинилацетат натрия фармакотерапевтическая группа иммуностимулирующее средство. Многочисленные исследования доказали следующие эффекты применения: противовирусный (в отношении ДНК и РНК-геномных вирусов), иммуномодулирующий, противоопухолевый, антипротозойный, антибактериальный. Препарат применяется в/м, по 250 мг (4 – 6 мг/кг), курс лечения 5 – 7 инъекций в течение 10 – 15 дней с интервалом 48 часов; при необходимости в разовой дозе до 500 мг с интервалом 18 – 36 часов (курсовая доза зависит от характера заболевания).
-
Меглюмина акридонацетат** применяется по схеме: 3 инъекции с интервалом в 24 часа и далее еще 3 инъекции с интервалом в 48 часов. В период ремиссии рекомендуется одна инъекция в неделю 250 мг препарата с целью профилактики рецидивов. После месячного курса лечения следует сделать перерыв на 4 – 5 недель.
-
Пациентам с частыми рецидивами (более 6 раз в год) или при монотонном типе заболевания, а также неэффективности эпизодической терапии рекомендовано применение супрессивной терапии с целью подавления репродукции инфекционного агента в период обострения, формирования адекватного иммунного ответа и его длительного сохранение для блокирования реактивации вируса герпеса в очагах персистенции [1, 4, 44, 51, 52, 79].
- Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1
Комментарии: Перед проведением супрессивной терапии необходимо ПЦР-подтверждение ВПГ-инфекции. Терапия проводится с использованием химиопрепаратов из группы синтетических ациклических нуклеозидов – ацикловира**, фамцикловира или валацикловира. Для эффективности проведения супрессивной терапии крайне важно своевременное назначение и выбор оптимальной схемы с позиций эффективности и переносимости. Следует учитывать возможности и желания пациента проводить лечение в соответствии с назначенной схемой. Необходимо тщательно следить и учитывать какие-либо нарушения, допускаемые пациентом при приеме препаратов.
3.1.2 Патогенетическая терапия
-
Всем пациентам не зависимо от тяжести течения заболевания рекомендован рациональный режим (запрещается прием ванн, душа, кожу вокруг очагов протирают 2% салициловым спиртом) [1, 4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
-
Всем пациентам не зависимо от тяжести течения заболевания рекомендовано обязательное проведение десенсибилизирующей терапии с использование антигистаминных препаратов [1, 4].
Уровень убедительности рекомендаций B (уровень достоверности доказательств –3).
-
Рекомендовано проведение дезинтоксикационной, метаболической, антиоксидантной терапии [1, 4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарии: Дезинтоксикационная терапия направлена на купирование синдрома интоксикации, ее объем зависит от степени тяжести пациента.
Метаболическая терапия влияет на обмен веществ в организме. Схема назначения адеметионина**: первые две недели в/в струйно в дозе 800–1600 мг ежедневно с последующим переходом на таблетированную форму по 2 – 4 таблетки в день. При проведении антиоксидантной терапии необходимо сочетать жирорастворимые и водорастворимые препараты. В качестве жирорастворимого антиоксидантного средства применяют альфа-токоферола ацетат по 0,1г в сутки в течение 1 – 2 месяцев, который можно сочетать с препаратами селена.
3.1.3 Симптоматическая терапия
Основными задачами симптоматических средств является купирование воспалительных и токсических проявлений заболевания, предупреждение развития осложнений.
-
При повышении температуры более 38,0?С рекомендовано назначение жаропонижающих средств, которые не влияют на эффективность терапии.
Уровень убедительности рекомендаций С (уровень достоверности
доказательств –4).
Комментарии: могут быть назначены производные пропионовой кислоты, анилиды, производные уксусной кислоты и родственные соединения.
-
Рекомендовано местное применение водных и спиртовых растворов анилиновых красителей (бриллиантовый зеленый, жидкость Кастеллани)
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
4. Реабилитация
4.1 Реабилитация
-
Реабилитационные мероприятия рекомендовано начинать уже в периоде разгара или в периоде ранней реконвалесценции
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
-
Рекомендовано соблюдать последовательность и преемственность проводимых мероприятий, обеспечивающих непрерывность на различных этапах реабилитации и диспансеризации.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
-
Рекомендован комплексный характер восстановительных мероприятий с участием различных специалистов и с применением разнообразных методов воздействия.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
-
Рекомендована адекватность реабилитационно-восстановительных мероприятий и воздействий адаптационным и резервным возможностям реконвалесцента.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Важны постепенность возрастания дозированных физических и умственных нагрузок, а также дифференцированное применение различных методов воздействия
-
Рекомендован постоянный контроль эффективности проводимых мероприятий. При этом учитываются скорость и степень восстановления функционального состояния и профессионально-значимых функций переболевших (косвенными и прямыми методами)
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
4.2 Диспансерное ведение
-
За лицами, перенесшими неосложненные формы ПГ, диспансерное наблюдение не устанавливается.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-
Реконвалесценты, перенесшие осложненные формы ПГ подлежат обязательному диспансерному наблюдению у врача-инфекциониста по месту жительства или в территориальном специализированном центре.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: диспансеризация в течение 1 года (с контрольными клинико?лабораторными обследованиями через 3 (легкая форма), 6 (среднетяжелая форма) и 12 месяцев (тяжелая форма) после выздоровления.
-
Реконвалесценты, перенесшие вирусно-бактериальную пневмонию подлежат обязательному диспансерному наблюдению у врача-пульмонолога по месту жительства в течение 12 месяцев.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: периодичность обследования составляет врачом-инфекционистом поликлиники 3, 6 и 12 месяцев, врачом-пульмонологом – 3,6 и 12 месяцев.
-
Реконвалесценты, перенесшие поражение нервной системы (менингит, энцефалит, менингоэнцефалит) подлежат обязательному диспансерному наблюдению у врача-невролога по месту жительства в течение 3-х лет.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: наблюдение включает контрольные клинико?лабораторные обследования с частотой 1 раз в 3 месяца в течение первого года, затем 1 раз в 6 месяцев.
-
Реконвалесцентам, перенесшим поражение глаз (офтальмогерпес – кератоконъюнктивит, ретинит, отслойка сетчатки и др.) рекомендовано обязательное диспансерное наблюдение у врача-инфекциониста и врача-офтальмолога в медицинской организации по месту жительства или в территориальном офтальмологическом центре в течение 6 – 12 месяцев.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: наблюдение включает контрольные клинико-лабораторное обследование через 1 месяц, затем 1 раз в 6 месяцев; контроль зрения 1 раз в 6 месяцев.
5. Профилактика и диспансерное наблюдение
-
Первичная профилактика – предотвращение заражения ВПГ [1, 4, 6, 7, 18].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1а).
Комментарии: санитарно-просветительская работа в рамках полового воспитания и гигиенического образования в школах, в процессе работы с подростками в подростковых центрах, при обращении девушек-подростков и молодых женщин в женские консультации, при работе с молодыми супругами, а также при любом обращении пациентов за дерматовенерологической помощью; исключение случайных сексуальных контактов; использование презервативов и средств индивидуальной профилактики во время сексуальных контактов с непостоянными партнерами; виду особой опасности заражения ВПГ во время беременности в течение всего ее срока обязательно использование барьерных методов контрацепции при всех видах сексуальных отношений; отказ от сексуальных отношений во время рецидива герпетической инфекции, если кто-либо из половых партнеров не инфицирован ВПГ.
-
Первичная профилактика у беременных – предотвращение передачи ВПГ от матери к ребенку [1, 4, 21, 45, 80].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1b).
Комментарии: выявление беременных высокого риска: а) тщательный сбор анамнеза с целью выявления эпизодов генитального герпеса; б) тщательное клиническое обследование родовых путей, промежности и вульвы в процессе наблюдения в женских консультациях и перед началом родов; в) вирусологическое подтверждение герпесподобных генитальных поражений у всех женщин, планирующих беременность.
-
Вторичная профилактика направлена на замедление или предотвращение развития заболевания [1, 4, 6, 45, 51].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2а).
Комментарии: полное специфическое лечение первичного эпизода генитального герпеса; адекватно пролеченный первичный эпизод менее склонен к рецидивированию генитального герпеса; использование супрессивной терапии с целью предупреждения рецидивов генитального герпеса; контроль факторов, провоцирующих заболевание; коррекция недостаточности различных звеньев иммунитета; санация очагов инфекции; коррекция гормонального статуса и т.д.
6. Дополнительная информация, влияющая на течение и исход заболевания
Отрицательно влияют на исход лечения:
-
Отказ от проведения адекватной терапии, назначенной специалистом в зависимости от тяжести заболевания и периода ВПГ-инфекции;
-
Назначение противовирусных средств вне периода разгара или рецидива заболевания;
-
Присутствие факторов, оказывающих влияние на угнетение иммунной системы организма пациента;
-
Воздействие факторов, вызывающих реактивацию ВПГ-1 и ВПГ-2 (психоэмоциональное напряжение, резкая смена климата, ультрафиолетовое облучение, менструации, прием алкоголя).
-
Присоединения инфекционных осложнений.
Критерии оценки качества медицинской помощи
Список литературы
-
Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека. Руководство для врачей. СПб.: Спецлит, 2006: 302 с.
-
Кускова Т. К., Белова Е. Г. Семейство герпес-вирусов на современном этапе. Лечащий врач. 2004; 5: С. 5 – 9.
-
Покровская М.С. Герпес-вирусные инфекции – краткий обзор литературы [Электронный ресурс]. Режим доступа: http://lages-lab.ru/article_4.htm
-
Баринский И.Ф., Махмудов Ф.Р. Герпес. Баку: Victory, 2013:352 с.
-
Куханова М.К., Коровина А.Н., Кочетков С.Н. Вирус простого герпеса человека: жизненный цикл и поиск ингибитора Успехи биологической химии. 2014;54: С. 457 – 494.
-
Халдин А.А., Игнатьев Д.В., Васильев А.Н. Простой герпес: этиология, патогенез, диагностика, лечение. Дерматология. Приложение к журналу Consilium Medicum. 2009; 1: С. 35 – 39.
-
Mettenleiter T.C. Herpesvirus assembly and egress. J. Virol. 2002; 76 (4): P. 1537 – 1547.
-
Chan T., Barra N.G., Lee A.J., Ashkar A.A. Innate and adaptive immunity against herpes simplex virus type 2 in the genital mucosa. J. Reprod. Immunol. 2011; 88 (2): P. 210 – 218.
-
Злотникова М.В., Новикова И.А. Механизмы естественного и адаптивного иммунитета при инфекциях, вызванных вирусами простого герпеса 1 и 2 типа. Проблемы здоровья и экологии. 2014; 1 (39): С. 7 – 14.
-
Камбачокова З.А. Функциональная активность фагоцитов у больных простым герпесом. Вестник новых медицинских технологий. 2011; 18 (3): С. 106 – 108.
-
Мельниченко А.В., Мезенцева М.В., Шаповал И.М. и др. Сравнительная оценка показателей интерферонового, иммунного и цитокинового статуса при комплексном исследовании больных с герпесвирусными инфекциями. Вопр. вирусол. 2011;6: С.11 – 33.
-
Желязникова Г.Ф. Воздействие вирусов на систему цитокинов хозяина. Вопр. вирусол. 2002;4: С.6 – 8.
-
Gill N., Chenoweth M.J., Verdu E.F., Ashkar A.A. NK cells require type I IFN receptor for antiviral responses during genital HSV-2 infection. Cell. Immunol. 2011; 269 (1): P. 29 – 37.
-
Lieberman L.A., Hunter C.A. Regulatory pathways involved in the infection-induced production of IFN-gamma by NK cells. Microbes. Infect. 2002; 4 (15): P. 1531 – 1538.
-
Lowhagen G.B., Tunback P., Bergstrom T. Proportion of herpes simplex virus (HSV) type 1 and type 2 among genital and extragenital HSV isolates. Acta Derm Venereol. 2002;82(2): P. 118 – 120.
-
Семенова Т.Б. Простой герпес. Клинико-эпидемиологические особенности, диагностика, лечение. Лечащий врач. 2003;7: С. 23-26.
-
Patel R., Alderson S., Geretti A. et al. IUSTI/WHO Europe. European guideline for the management of genital herpes. Int. J. STD AIDS. 2011; 22 (1): P. 1 – 10.
-
Халдин А.А., Баскакова Д.В. Эпидемиологические аспекты заболеваний, вызываемых вирусом простого герпеса (обзор литературы). Consilium medicum. 2007; 9 (1): C. 27 – 30.
-
Gupta R., Warren T., Wald A. Genital herpes. Lancet. 2007; 370 (9605): P. 2127 – 2137.
-
Beauman J.G. Genital herpes: a review. Am Fam Physician 2005; 72: 1527 – 1534.
-
Anzivino E., Fioriti D., Mischitelli M. et al. Herpes simplex virus infection in pregnancy and in neonate: status of art of epidemology, diagnosis, therapy and prevention. Virol J, 2009; 6: P.6 –40.
-
Wald A., Zeh J., Selke S. et al. Reactivation of genital herpes simplex virus type 2 infection in asymptomatic seropositive persons. N Engl J Med. 2000;342:Р. 844 – 850.
-
Looker K.J., Garnett G.P., Schmid G.P. An estimate of the global prevalence and incidence of herpes simplex virus type 2 infection. Bull World Health Organ. 2008; 86: P.805 – 812.
-
Всемирная организация здравоохранения. Вирус простого герпеса. Информационный бюллетень N?400. Январь 2016г. [Электронный ресурс]. Режим доступа: http://www.who.int/mediacentre/factsheets/fs400/ru/
-
Kupila L. Etiology of aseptic meningitis and encephalitis in an adult population. Neurology. 2006; 66: Р.75 – 80.
-
Хрянин А.А. Герпес под подушкой. Распространённость вируса простого герпеса в российской популяции: многолетний мониторинг. «StatusPraesens». 2014; 6: С. 67 – 74.
-
Шульженко А.Е. Герпетические инфекции человека: перспективы диагностики и противовирусной терапии. Цитокины и воспаление. 2005; 3: C. 76-81.
-
Wald A. Testing for genital herpes: how, who, and why. Curr Clin Top Infect Dis. 2002;22:р. 166 – 180.
-
Domeika M., Bashmakova M., Savicheva A. et al. Guidelines for the laboratory diagnosis of genital herpes in eastern European countries. Euro Surveill. 2010;15 (44): Р. 1 – 7.
-
Scoular A. Using the evidence base on genital herpes: optimising the use of diagnostic tests and information provision. Sex Transm Infect 2002; 78: P. 160 – 165.
-
Алгоритмы диагностики и лечения наиболее распространенных инфекций, передающихся половым путем. Трудный пациент. 2004; 2 (5): С.3 – 8.
-
Кудин А.П., Германенко И.Г., Астапов А.А. Роль Herpes simplex в патологии человека. Ч. 3. Лабораторная диагностика, лечение и профилактика герпетической инфекции. Мед. новости. 2004;9: С. 3 – 10.
-
Ковтонюк Г. В., Ганова Л. А., Шепелин К. А. Иммуноферментная тест-система для серодиагностики герпеса 2-го типа. Мед. алфавит. Современная лаборатория. 2013; 3: С. 58 – 60.
-
Ashley-Morrow R., Nollkamper J., Robinson N.J. et al. Performance of focus ELISA tests for herpes simplex virus type 1 (HSV-1) and HSV-2 antibodies among women in ten diverse geographical locations. Clin Microbiol Infect 2004; 10:Р.530.
-
Ashley-Morrow R. Genital herpes. Type-specific antibodies for diagnosis and management. Dermatol Clin. 1998;16(4):Р. 789 – 793.
-
Slomka M.J., Emery L., Munday P.E. et al. A comparison of PCR with virus isolation and direct antigen detection for diagnosis and typing of genital herpes. J Med Virol.1998;55(2):Р.177 – 183.
-
Wald A., Huang M.-L., Carrell D. et al. Polymerase chain reaction for detection of herpes simplex virus (HSV) DNA on mucosal surfaces: comparison with HSV isolation in cell culture. J Infect Dis 2003; 188: P. 1345 – 3151.
-
Burrows J., Nitsche A., Bayly B. et al. Detection and subtyping of Herpes simplex virus in clinical samples by LightCycler PCR, enzyme immunoassay and cell culture. BMC Microbiol. 2002;2:Р.12.
-
Ramaswamy M., McDonald C., Smith M. et al. Diagnosis of genital herpes by real time PCR in routine clinical practice. Sex Transm Infect 2004; 80: Р.406 – 410.
-
Geretti A.M. Brown D.W. National survey of diagnostic services for genital herpes. Sex Transm Infect 2005; 81: Р.316 – 317.
-
Scoular A. Using the evidence base on genital herpes: optimising the use of diagnostic tests and information provision. Sex Transm Infect 2002; 78: Р.160 – 165.
-
Григорьева О.О., Шейх Ж.В., Кармазановский Г.Г. и др. Компьютерная и магнитно-резонансная томография в диагностике герпетического энцефалита (клиническое наблюдение). Медицинская визуализация. 2015; 4: С. 31-38.
-
Баринский И.Ф., Алимбарова Л.М. Препараты для лечения герпетической инфекции. Российские аптеки. 2005; 71 (1): С. 30 – 33.
-
Crumpacker C.S. Use of antiviral drugs to prevent herpesvirus transmission.N. Engl. J. Med. 2004;350 (1): P. 67 – 68.
-
Elion G.B. Acyclovir: discovery, mechanism of action, and selectivity. Journal of medical virology. 1993; Suppl 1: Р. 2 – 6.
-
Vere Hodge R.A., Field H.J. Antiviral agents for herpes simplex virus. Advances in pharmacology. 2013; 67: Р. 1 – 38.
-
Coen D.M., Schaffer P.A. Antiherpesvirus drugs: a promising spectrum of new drugs and drug targets. Nature reviews Drug discovery. 2003;2: Р. 278 – 288.
-
Pula J.H., Macdonald C.J. Current options for the treatment of optic neuritis. Clin. Ophthalmol. 2012;6:Р.1211 – 1223.
-
Sen P., Barton S.E. Genital herpes and its management. BMJ. 2007; 334:Р.1048.
-
Халдин А.А., Самгин М.А., Львов А.Н Алгоритм ведения больных рецидивирующим простым герпесом: от науки к практике. Российский журнал кожных и венерических болезней.2008;S1:С.21 – 25.
-
Ершов Ф.И. Антивирус,ные препараты. М.: Гэотар-Медиа, 2006: 312 с.
-
Mindel A., Kinghorn G., Allason-Jones E. et al. Treatment of ?rst-attack genital herpes — acyclovir versus inosine pranobex. Lancet. 1987; 1(8543): Р.1171–1173.
-
De Clercq E., Field H.J. Antiviral prodrugs – the development of successful prodrug strategies for antiviral chemotherapy, British journal of pharmacology . 2006; 147: Р.1–11.
-
Karpenko I.L., Jasko M.V., Andronova V.L. et al. Synthesis and antiherpetic activity of acyclovir phosphonates. Nucleosides, nucleotides & nucleic acids.2003; 22: Р. 319 – 328.
-
Skoblov Y.S., Karpenko I.L., Jasko M.V. et al. Cell metabolism of acyclovir phosphonate derivatives and antiherpesvirus activity of their combinations with alpha2- interferon. Chemical biology & drug design. 2007; 69: Р. 429 – 434.
-
Field H.J., Biswas S. Antiviral drug resistance and helicase-primase inhibitors of herpes simplex virus. Drug Resist. Updat. 2011; 14 (1): P. 45 – 51.
-
Thust R., Tomicic M., Klocking R. et al. Comparison of the genotoxic and apoptosis-inducing properties of ganciclovir and penciclovir in Chinese hamster ovary cells transfected with the thymidine kinase gene of herpes simplex virus-1: implications for gene therapeutic approaches. Cancer gene therapy. 2000; 7: Р. 107 – 117.
-
Thackray A.M., Field H.J. Famciclovir and valaciclovir differ in the prevention of herpes simplex virus type 1 latency in mice: a quantitative study. Antimicrobial agents and chemotherapy.1998; 42: Р. 1555 – 1562.
-
Alecu M., Ghyka G.R., C?lug?ru A. et al. Interferon e?ciency in the treatment of herpetic dermatites. I. A double-blind placebo controlled study. Med. Interne. 1989; 27(2): Р.127 – 135.
-
Borrego L., Castro I., Franc?s A. et al. Treatment of acyclovir-resistant perianal herpetic ulceration with intramuscular interferon alfa. Arch. Dermatol. 1996; 132(10): Р. 1157 – 1158.
-
Cabrera-G-mez J.A., L-pez-Saura P. Recent advances in the treatment the nervous system disorders with interferon-alpha. Rev. Neurol. 1999; 29(12):Р. 1225 – 1235.
-
Cardamakis E., Relakis K., Kotoulas I.G. et al. Treatment of recurrent genital herpes with interferon alpha-2alpha. Gynecol. Obstet. Invest. 1998; 46(1): Р. 54 – 57.
-
Crespi H., de Mora E., Pueyo S. et al. Therapeutic use of human leukocyte interferon in dermatologic disorders caused by herpes simplex virus. Multicenter study. Med. Cutan. Ibero Lat. Am. 1988; 16(6): Р.459 – 465.
-
Granados Loarca E.A., Estrada Barrondo E.A. Treatment of genital herpes with alfa2b interferon. Actas. Urol. Esp. 2000; 24(5): Р. 388 – 392.
-
L-pez Garc"a F., Enr"quez Ascarza R., Rodr"guez Mart"nez J.C. et al. Interferon therapy for herpes simplex virus infection in a 70 years old patient. An. Med. Interna. 2002; 19(11):Р. 600 – 601.
-
Деленян Н.В., Ариненко Р.Ю., Мешкова Е.Н. Виферон. Комплексный противовирусный и иммуномодулирующий препарат для детей и взрослых. Руководство для врачей. М.: ИНКО-ТНК, 2002: 52 с.
-
Шперлинг И.А., Венгеровский А.И., Шперлинг Н.В. Фармакологическая коррекция индукторами интерферона цитокиновых нарушений при рецидивирующем генитальном герпесе. Эксперим. и клин. Фармакология. 2010; 73(8):С. 39 – 42.
-
Ломоносов К.М., Иванов О.Л., Кладова А.Ю. Неовир в практике дерматовенеролога. Российский журнал кожных и венерических болезней. 2003; 2: С. 30 – 32.
-
Копаенко А.И., Жабоедов Г.Д., Иванова Н.В. Особенности клиники и лечения больных передними эндогенными увеитами вирусной этиологии. Офтальмология Восточная Европа. 2013; 1 (16): С. 41 – 48.
-
Алиева Э.Ш., Ширяева А.А., Копаенко А.И. Эффективность применения неовира в комплексном лечении передних увеитов вирусной этиологии. Украинский научно-медицинский молодежный журнал. 2012; 1: С. 17 – 18.
-
Зуйкова И.Н., Шульженко А.Е., Щубелко Р.В. Коррекция цитокиновых нарушений у пациентов с хронической рецидивирующей герпесвирусной инфекцией. Фарматека. 2014;10 (283): С. 48 – 54.
-
Хрянин А.А., Решетников О.В. Индукторы интерферона в терапии генитального герпеса у женщин. Акушерство и гинекология. 2015; 7: С. 88 – 93.
-
Змушко Е.И., Шувалова Е.Е., Кацалуха В.В., Старенченко В.В. Сравнительная оценка эффективности индукторов интерферона при экспериментальной генерализованной герпетической инфекции. Инфекционные болезни. 2014; 12(2): С. 59 – 63.
-
Баткаев Э.А. Генитальный герпес. Вестник последипломного медицинского образования. 2013; 3: С. 20 – 24.
-
Рахматулина М.Р. Комбинированная терапия больных рецидивирующей аногенитальной герпетической инфекцией. Антибиотики и химиотерапия. 2011; 56 (11-12): С. 25 – 29.
-
Исаков В.А., Исаков Д.В. Иммуномодуляторы в терапии и профилактике герпесвирусных инфекций. Клиническая медицина. 2015; 93(4): С. 16 – 24.
-
Сологуб Т.В., Романцов М.Г., Рыбалкина Т.С., Рыбалкин С.Б., Смагина А.Н., Исаков В.А., Коваленко А.Л. Модифицированная терапия герпетической инфекции. Клиническая медицина. 2011; 89 (3): С. 54 – 57.
-
Горячкина М.В., Белоусова Т.А. Эпизодическая и супрессивная терапия простого герпеса ациклическими нуклеозидами. Клиническая дерматология и венерология. 2014; 12 (4): С. 68 – 74.
-
Протоколы диагностики, лечения и профилактики внутриутробных инфекций у новорожденных детей. Под ред. Н.Н. Володина. М.: ГОУ ВУНМЦ МЗ РФ, 2002: 100с.
Приложение А1. Состав рабочей группы
-
Алимбалова Л.М., к.м.н., Институт вирусологии им. Д.И.Ивановского
ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава России; -
Баринский И.Ф., д.м.н., профессор, Институт вирусологии им. Д.И.Ивановского
ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава России; -
Шестакова И.В., д.м.н., профессор кафедры инфекционных болезней и эпидемиологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России;
-
Эсауленко Е.В., д.м.н. профессор, заведующая кафедрой инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО СПбГПМУ Минздрава России;
-
Сухорук А.А., к.м.н., ассистент кафедры инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО СПбГПМУ Минздрава России.
Все члены рабочей группы являются членами некоммерческой корпоративной организации «Международная ассоциация специалистов в области инфекций» («МАСОИ»).
Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория клинических рекомендаций:
-
Врачи-инфекционисты;
-
Студенты медицинских ВУЗов, ординаторы, аспиранты.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица П1 - Уровни достоверности доказательности
|
Уровень достоверности |
Тип данных |
|
1а |
Мета анализ рандомизированных контролируемых исследований (РКИ) |
|
1b |
Хотя бы одно РКИ |
|
2а |
Хотя бы одно хорошо выполненное контролируемое исследование без рандомизации |
|
2b |
Хотя бы одно хорошо выполненное квазиэкспериментальное исследование |
|
3 |
Хорошо выполненные не экспериментальные исследования: сравнительные, корреляционные или «случай-контроль» |
|
4 |
Экспертное консенсусное мнение либо клинический опыт признанного авторитета |
Таблица П1 - Уровни убедительности рекомендаций
|
Уровень убедительности |
Основание рекомендации |
|
А |
Основана на клинических исследованиях хорошего качества, по своей тематике непосредственно применимых к данной специфической рекомендации, включающих по меньшей мере одно РКИ |
|
В |
Основана на результатах клинических исследований хорошего дизайна, но без рандомизации |
|
С |
Составлена при отсутствии клинических исследований хорошего качества, непосредственно применимых к данной рекомендации |
Порядок обновления клинических рекомендаций
Клинические рекомендации обновляются каждые 3 года.
Форма помощи
Медицинская помощь оказывается в форме:
-
экстренной медицинской помощи;
-
неотложной медицинской помощи;
-
плановой медицинской помощи.
Условия оказания медицинских услуг
Медицинская помощь оказывается в виде:
-
первичной медико-санитарной помощи;
-
скорой, в том числе скорой специализированной, медицинской помощи;
-
специализированной, в том числе высокотехнологичной, медицинской помощи.
Медицинская помощь больным ПГ может оказываться в следующих условиях:
-
амбулаторно (в условиях, не предусматривающих круглосуточное медицинское наблюдение и лечение);
-
в дневном стационаре (в условиях, предусматривающих медицинское наблюдение и лечение в дневное время, не требующих круглосуточного медицинского наблюдения и лечения);
-
стационарно (в условиях, обеспечивающих круглосуточное медицинское наблюдение и лечение).
Первичная медико-санитарная помощь предусматривает:
-
первичную врачебную медико-санитарную помощь;
-
первичную специализированную медико-санитарную помощь.
Первичная медико-санитарная помощь оказывается в амбулаторных условиях и в условиях дневного стационара.
Первичная медико-санитарная помощь в амбулаторных условиях осуществляется в медицинских кабинетах учреждений.
При подозрении или выявлении у пациента ПГ, не требующего лечения в условиях стационара, врач-терапевт участковый (врачи общей практики (семейные врачи), средние медицинские работники медицинских организаций при наличии медицинских показаний направляет на консультацию в кабинет инфекционных заболеваний медицинской организации для оказания ему первичной специализированной медико-санитарной помощи.
Первичная специализированная медико-санитарная помощь осуществляется врачом-инфекционистом медицинской организации, оказывающим медицинскую помощь в амбулаторных условиях (поликлиника).
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается в условиях стационара врачами-инфекционистами и другими врачами-специалистами и включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских технологий, а также медицинскую реабилитацию.
Лечение осуществляется в условиях стационара по направлению врача-терапевта участкового, врача общей практики (семейного врача), врача-инфекциониста, других специалистов, выявивших ПГ.
Приложение А3. Связанные документы
Связанные документы
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
-
Федеральный закон Российской Федерации от 29 ноября 2010г. №326-ФЗ «Об обязательном медицинском страховании в Российской Федерации».
-
Федеральный закон от 21 ноября 2011г. №323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации».
-
Приказ Минздравсоцразвития России от 9 августа 2005г. №494 «О порядке применения лекарственных средств у больных по жизненным показаниям».
-
Приказ Минздравсоцразвития России от 27 декабря 2011г. №1664н «Об утверждении номенклатуры медицинских услуг».
-
Приказ Минздравсоцразвития России от 31 января 2012г. № 69н «Об утверждении Порядка оказания медицинской помощи взрослым больным при инфекционных заболеваниях».
-
Приказ Минздрава России от 20 декабря 2012г. №1183н «Об утверждении Номенклатуры должностей медицинских работников и фармацевтических работников»
-
Приказ Минздрава России от 07 октября 2015г. №700н «О номенклатуре специальностей специалистов, имеющих высшее медицинское и фармацевтическое образование».
-
Приказ Минздрава России от 17 декабря 2015г. № 1024н «О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы».
-
Санитарно-эпидемиологические правила СП 3.1/3.2.3146-13 «Общие требования по профилактике инфекционных и паразитарных болезней» (утверждены Постановлением Главного государственного санитарного врача Российской Федерации от 16 декабря 2013 года №65).
Приложение Б. Алгоритмы ведения пациента
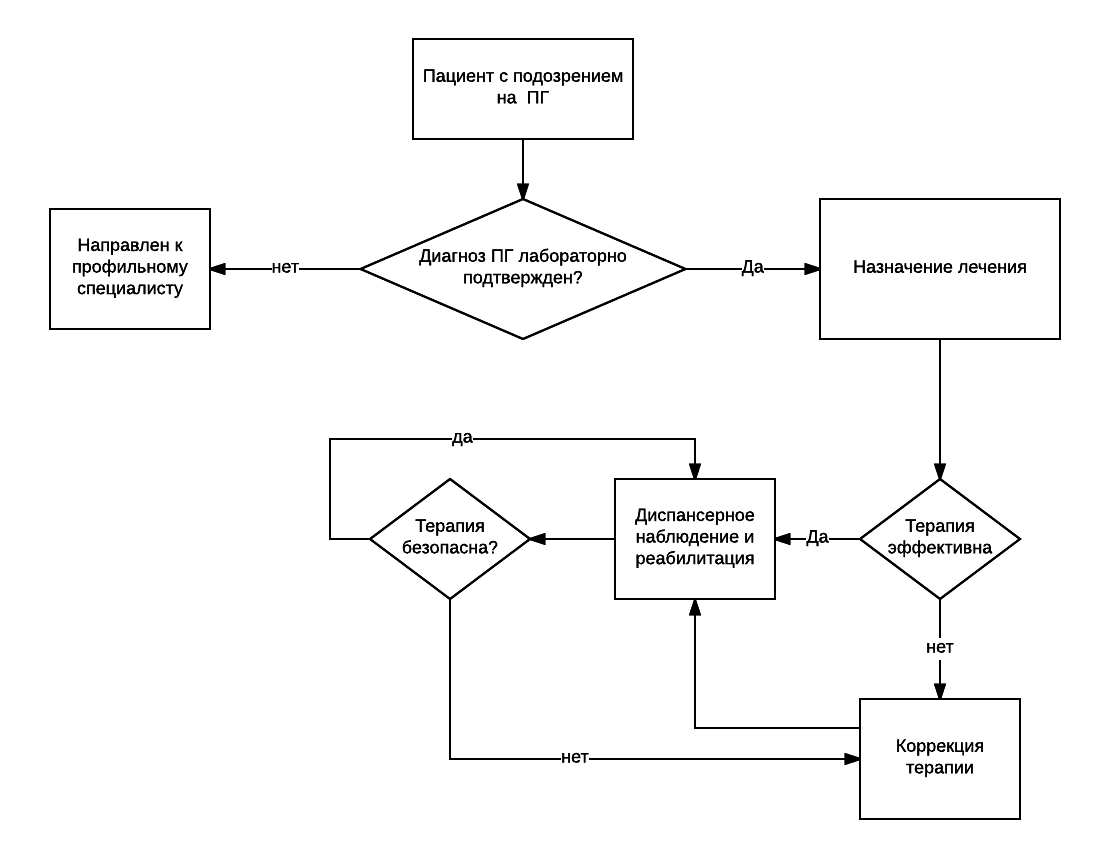
Приложение В. Информация для пациентов
Стоматит – поражение слизистой оболочки полости рта.
Меры профилактики возникновения стоматита:
-
Полноценная санация ротовой полости;
-
Объективная систематическая оценка состояния слизистой оболочки полости рта.
Признаки стоматита: «пощипывание», покраснение слизистой оболочки полости рта, обильное выделение слюны, болезненность при пережевывании пищи. Могут появиться пузырьки, отечность языка, жжение, дискомфорт.
При возникновении стоматита назначается терапия, направленная на уменьшение воспаления:
-
диета с включением в рацион мягкой, теплой, не раздражающей, термически обработанной пищи;
-
очищающие средства: 3% раствор перекиси водорода, слабый раствор калия перманганата, раствор натрия бикарбоната, орошение 0,12% раствором хлоргексидина;
-
заживляющие/обволакивающие средства: яичный белок, разведенный в одном стакане воды, антиоксидант витамин Е, аппликации 2% раствором метилурацила, дерината;
-
местные анальгетики: 1-2% раствор лидокаина, раствор анастезина, новокаина;
-
к другим местным воздействиям можно отнести обработку полости рта маслом шиповника, облепихи, раствором прополиса, витамином В12.
Ниже приводим несколько советов, как справиться со стоматитом:
-
Чистите зубы в период бодрствования каждые 4 часа зубной щеткой с мягкой щетиной;
-
Мы советуем полоскать рот по 3-5 мин каждые 2-3 часа не менее 8 раз в день. Между полосканиями, используйте для смазывания слизистой оболочек и язвочек облепиховым маслом, солкосерилом, актовегином;
-
Полощите рот раствором соды (1 чайная ложка на 1,5-2 стакана воды) или комбинацией: 1 чайная ложка соды + 1 чайная ложка соли на 1000 мл воды. Дежурными средствами для полосканий давно стали теплые отвары ромашки, шалфея, коры дуба, зверобоя, а также белковый раствор (один белок куриного яйца на 0,5 литра воды);
-
Можно использовать готовые лекарства для полоскания, содержащие смеси экстрактов ромашки, календулы и тысячелистника и обладающие противовоспалительным действием, кровоостанавливающими свойствами и способствует восстановлению поврежденной слизистой оболочки;
-
При язвенных стоматитах возможно лечение по следующей схеме: полоскание полости рта раствором перикиси водорода (1 столовая ложка на стакан воды), затем слабым (бледно-розовым) раствором марганцовки, далее использование различных полосканий и аэрозолей и на завершающем этапе – смазывание язвенных участков облепиховым маслом, соком колонхое или более современными препаратами: солкосерилом (гель, желе), актовегином (гель, желе). Солкосерил или актовегин способствуют быстрейшему заживлению язв и восстановлению поврежденной слизистой, Один сантиметр одного из гелей наносят чистым пальцем 3-4 раза в день перед едой, слегка массируя больное место;
-
При сильных болях полощите рот обезболивающими средствами.
Диетические рекомендации при стоматитах:
Продукты, которые помогут Вам в лечении стоматита – готовые смеси для детей (мясные, овощные и фруктовые), различные виды творога, йогурты, некислые желе, мягкие неострые сыры, взбитые сливки.
Включайте в рацион следующие блюда и напитки: овсяная каша, процеженный молочный суп, яйца всмятку, картофельное пюре, суп-пюре, творожный пудинг (можно размять с молоком), крем из яиц и молока и другую не раздражающую пищу. Не рекомендуется употреблять кислые фрукты и цитрусовые, так как они могут усилить раздражение слизистой оболочки полости рта. Используйте мягкую пищу, когда утихнут острых явлений стоматита. Готовьте тушеные, вареные, мятые блюда (мясо на пару, салаты с провернутым мясом и птицей, запеканки, суфле, пудинги, супы и бульоны с минимальным количеством соли и, естественно, без перца). Помидоры употребляйте с осторожностью, т.к. они обладают способностью усиливать раздражение слизистой оболочки полости рта. Многим помогает варенье из лепестков роз. Настоятельно рекомендуется при стоматитах сливочное и молочное мороженое без каких-либо добавок.
В тех случаях, когда у Вас появляется сухость или дискомфорт в полости рта или горле, когда пережевывание и глотание пищи затрудненно, попробуйте пить больше жидкости (до 2-х литров в день). Арбуз и дыня должны регулярно появляться на Вашем столе. Держите недолго во рту кусочки льда или не содержащие сахара леденцы и жевательные резинки.
Роль психологической поддержки при герпесвирусной инфекции, вызванной ВПГ-1 и ВПГ-2
Герпесвирусная инфекция меняет образ жизни и характер человека. Эти психические нарушения нельзя назвать приятными, но Вы можете справиться с большинством из них, настраиваясь на собственное оптимистическое отношение к ним и правильное поведение.
Не стесняйтесь задавать вопросы по поводу того, что происходит. Помните, что Ваше эмоциональное благополучие так же важно, как и физическое здоровье.
Очень помогает отвлечение внимания. Каждый человек нуждается в психологической поддержке в трудные времена.
