Спирива - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер: П №014410/01 от 19.11.2007
Торговое (патентованное) название: Спирива®
Международное непатентованное название: тиотропия бромид
Лекарственная форма:
капсулы с порошком для ингаляцийСостав
1 капсула содержит активного вещества: тиотропия бромида моногидрат 0,0225 мг эквивалент тиотропия 0,0180 мг
вспомогательные вещества: лактоза моногидрат, 200 М 5,2025 мг; лактоза моногидрат микронизированный 0,2750 мг.
Состав капсулы (мг/капсула): макрогол 2,4000 мг, индигокармин (Е132) 0,0120 мг, титана диоксид (Е171) 1,0240 мг, железа оксид желтый (Е172) 0,0120 мг, желатин 44,5160 мг
Описание
Твердые желатиновые капсулы, размер 3, светло-зеленовато-голубого цвета, непрозрачные, с надпечаткой символа компании и ТI01 черными чернилами Содержимое капсул - белый порошок.
Фармакотерапевтическая группа: М-холиноблокатор.
Код ATC: RO3BB04Фармакологические свойства
Тиотропия бромид - антимускариновый препарат продолжительного действия м-холиноблокатор, в клинической практике часто называемый антихолинергическим средством. Он обладает одинаковым сродством к различным подтипам мускариновых рецепторов от М1 до М5. Результатом ингибирования М3-рецепторов в дыхательных путях является расслабление гладкой мускулатуры. Бронходилатирующий эффект зависит от дозы и сохраняется не менее 24 часов. Значительная продолжительность действия связана, вероятно, с очень медленной диссоциацией от М3-рецепторов, по сравнению с ипратропия бромидом. При ингаляционном способе введения тиотропия бромид как N-четвертичное антихолинергическое средство оказывает местный избирательный эффект, при этом в терапевтических дозах не вызывает системных м-холиноблокирующих побочных эффектов. Диссоциация от М2-рецепторов происходит быстрее, чем от М3. Высокое сродство к рецепторам и медленная диссоциация обуславливают выраженный и продолжительный бронходилатирующий эффект у пациентов с хронической обструктивной болезнью легких.
Бронходилятация после ингаляции тиотропия бромида является следствием местного, а не системного эффекта.
Было показано, что СПИРИВА значительно увеличивает функцию легких (объем форсированного выдоха в 1 секунду ОФВ1, форсированную жизненную емкость легких ФЖЕЛ) спустя 30 минут после однократной дозы на протяжении 24 часов. Фармакодинамическое равновесие достигалось в течение первой недели, а выраженный бронходилятирующий эффект наблюдался на 3 день. СПИРИВА значительно увеличивает утреннюю и вечернюю пиковую потоковую скорость выдоха, измеряемую больными. Бронходилятирующий эффект СПИРИВЫ, оцениваемый на протяжении года, не выявил проявлений толерантности.
СПИРИВА значительно уменьшает одышку на протяжении всего периода лечения. В двух рандомизированных двойных слепых плацебо-контролируемых исследованиях было доказано, что СПИРИВА значительно улучшала переносимость физической нагрузки по сравнению с плацебо.
СПИРИВА значительно снижает число обострений ХОБЛ, и увеличивает период до момента первого обострения по сравнению с плацебо.
СПИРИВА значительно улучшает качество жизни. Это улучшение наблюдается на протяжении всего периода лечения.
Было показано, что СПИРИВА значительно снижает количество случаев госпитализации, связанной с обострением ХОБЛ, и увеличивает время до момента первой госпитализации. Также было показано, что СПИРИВА приводит к стойкому улучшению ОФВ1 после применения в течение 4-х лет без изменения темпов ежегодного снижения ОФВ1. Во время лечения наблюдается снижение риска смерти на 16%.
По сравнению с приемом сальметерола, применение СПИРИВЫ увеличивает время до первого обострения (187 дней против 145), со снижением риска развития обострений на 17 % (отношение рисков 0,83; 95 % доверительный интервал [ДИ], ОТ 0,77 до 0,90; Р< 0,001). Также прием Спиривы® увеличивает время наступления первого тяжелого (требующего госпитализации) обострения (отношение рисков 0,72; 95 % ДИ от 0,61 до 0,85; Р< 0,001) снижает ежегодное число средних или тяжелых (требующих госпитализации) обострений (0,64 против 0,72; отношение рисков 0,89; 95 % ДИ от 0,83 до 0,96; Р= 0,002), снижает ежегодное число тяжелых (требующих госпитализации) обострений (0,09 против 0,13; отношение рисков 0,73; 95 % ДИ от 0,66 до 0,82; Р< 0,001)
Фармакокинетика
Тиотропий- четвертичное аммониевое соединение умеренно растворимое в воде. Всасывание: При ингаляционном способе введения абсолютная биодоступность тиотропия составляет 19,5 %, свидетельствуя о том, что фракция препарата, достигающая легкие, высоко биодоступна. Тиотропий в растворе при приеме внутрь имеет абсолютную биодоступность равную 2-3 %. Прием пищи не влияет на всасывание тиотропия. Максимальная концентрация тиотропия в плазме (Cmax) после ингаляции достигается через 5-7 минут. На стадии динамического равновесия пиковая концентрация тиотропия в плазме крови у пациентов с ХОБЛ составляет 12,9 пг/мл и быстро снижается. Это указывает на мультикомпартментный тип распределения препарата. На стадии динамического равновесия базальная концентрация тиотропия в плазме крови составляет 1,71 пг/мл
Распределение. 72 % от принятой дозы препарата связывается с белками плазмы и объем распределения равен 32 л/кг. Исследования показали, что тиотропий не проникает через гематоэнцефалический барьер.
Биотрансформация: Степень биотрансформации незначительна. Это подтверждается тем, что после внутривенного введения препарата здоровым молодым добровольцам, в моче обнаруживается 74 % неизменной субстанции. Тиотропий расщепляется неферментным способом до алкоголь N-метилскопина и дитиенилгликоливой кислоты, которые не связываются с мускариновыми рецепторами.
При исследованиях показано, что препарат (< 20 % от дозы после внутривенного применения) метаболизируется цитохромом P450, этот процесс зависит от оксидации и последующей коньюгации с глютатионом с образованием различных метаболитов. Нарушение метаболизма может иметь место при использовании ингибиторов CYP 450 2D6 и 3А4 (хинидина, кетоконазола и гестодена). Таким образом, CYP 450 2D6 и 3А4 включаются в метаболизм препарата. Тиотропий даже в сверхтерапевтических концентрациях не ингибирует цитохром Р450, 1A1, 1A2, 2B6, 2C9, 2C19, 2D6, 2E1, или 3А в микросомах печени человека.
Выведение: Период полувыведения тиотропия после ингаляции варьирует от 27 до 45 часов. Общий клиренс при внутривенном введении здоровым молодым добровольцам составляет 880 мл/мин. Тиотропий после внутривенного введения в основном выводится почками в неизменном виде (74 %). После ингаляции сухого порошка на стадии динамического равновесия почечная экскреция составляет 7 % в сутки от дозы, оставшаяся не всосавшаяся часть, выводится через кишечник. Почечный клиренс тиотропия превышает клиренс креатинина, что свидетельствует о канальцевой секреции препарата. После длительного приема препарата однократно в сутки пациентами с ХОБЛ, фармакокинетическое равновесие достигается на 7 день, при этом не наблюдается аккумуляции в дальнейшем.
Тиотропий имеет линейную фармакокинетику в терапевтических пределах независимо от лекарственной формы препарата. Пожилые больные:
У пожилых больных наблюдается снижение почечного клиренса тиотропия (365 мл/мин у пациентов с ХОБЛ младше 65 лет, до 271 мл/мин у пациентов с ХОБЛ старше 65 лет). Эти изменения не приводили к соответствующему увеличению значений площади под кривой «концентрация/время» (AUCo-6) или Cmax. Пациенты с нарушенной функцией почек:
У пациентов с ХОБЛ и легкими нарушениями функции почек(клиренс креатинина 50-80 мл/мин) ингаляционное применение тиотропия один раз в сутки на стадии динамического равновесия приводило к повышению значения AUC0-6 на 1,8 - 30 %. Значение Cmaxсохранялось таким же, как у пациентов с нормальной функцией почек (клиренс креатинина > 80 мл/мин). У пациентов с ХОБЛ и средними или тяжелыми нарушениями функции почек (клиренс креатинина < 50 мл/мин) внутривенное введение тиотропия приводило к двукратному увеличению концентрации препарата в плазме (значение AUC0-4чувеличивалось на 82 % а значение Cmax увеличивалось на 52 %) по сравнению с пациентами с ХОБЛ и нормальной функцией почек. Аналогичное повышение концентрации тиотропия в плазме отмечалось и после ингаляции сухого порошка.
Пациенты с нарушенной функцией печени: Предполагается, что печеночная недостаточность не будет оказывать значительного влияния на фармакокинетику тиотропия, так как тиотропий в основном выводится почками, и с помощью не ферментативного расщепления эфирных связей, с образованием метаболитов, которые не связываются с мускариновыми рецепторами.
Показания
Спирива показана в качестве поддерживающей терапии у пациентов с ХОБЛ, включая хронический бронхит и эмфизему (поддерживающая терапия при сохраняющейся одышке и для предупреждения обострений).
Противопоказания
Повышенная чувствительность к атропину или его производным (например, ипратропию или окситропию) или к компонентам данного препарата (в частности, к лактозы моногидрату, который содержит молочный белок, вследствие дефицита лактазы, непереносимости лактозы, глюкозо-галактозная мальабсорбция); I триместр беременности; дети до 18 лет.
С осторожностью
Закрытоугольная глаукома, гиперплазия предстательной железы, обструкция шейки мочевого пузыря.
Беременность и лактация
Данные об использовании тиотропия при беременности у человека ограничены. В исследованиях на животных не получено указаний на прямые или опосредованные неблагоприятные влияния на беременность, развитие эмбриона/плода, процесс родов или постнатальное развитие.
В качестве меры предосторожности предпочтительнее воздержаться от применения препарата СПИРИВА во время беременности.
Клинических данных о применении тиотропия у женщин, кормящих грудью, не имеется. В доклинических исследованиях были получены данные что, небольшое количество тиотропия экскретируется в грудное молоко.
СПИРИВА не должна применяться у беременных или кормящих грудью женщин, если только ожидаемая польза не превышает возможный риск для плода или ребенка.
Способ применения и дозы
Ингаляционно.
При использовании Спиривы в виде ингаляций с помощью прибора ХандиХалер® рекомендуется применять одну капсулу в сутки в одно и тоже время.
Препарат не нужно глотать.
Пожилые больные должны принимать Спириву в рекомендуемых дозах. Пациенты с нарушенной функцией почек могут использовать Спириву в рекомендуемых дозах. Однако необходимо тщательное наблюдение за больными с умеренной или тяжелой почечной недостаточностью получающими Спириву (как и в случае с другими препаратами, эскретирующимися в основном почками). Пациенты с печеночной недостаточностью могут принимать Спириву в рекомендуемых дозах.
Инструкция по применению прибора ХандиХалер®
Прибор ХандиХалер® был специально разработан для Спиривы. Он не должен использоваться для приема других медикаментов. Вы можете использовать Ваш ХандиХалер® в течение одного года.
Прибор ХандиХалер® включает в себя:
- пылезащитный колпачок;
- мундштук;
- основание;
- прокалывающую кнопку;
- центральную камеру.
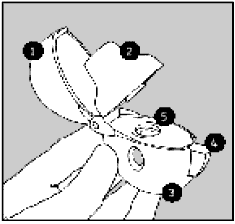
Использование прибора ХандиХалер
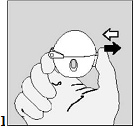
Откройте пылезащитный колпачок, нажав на прокалывающую кнопку полностью и затем отпустив
Полностью откройте пылезащитный колпачок, подняв его вверх. Затем откройте мундштук, подняв его вверх.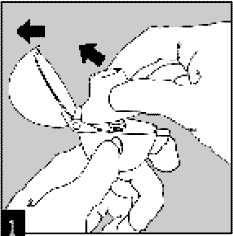
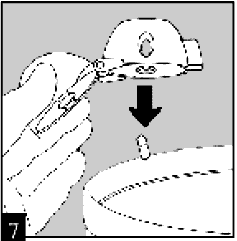
Достать капсулу Спиривы из блистера (непосредственно перед использованием) и положить ее в центральную камеру, как показано на рисунке. Не имеет значение, какой стороной капсула помещается в камеру.
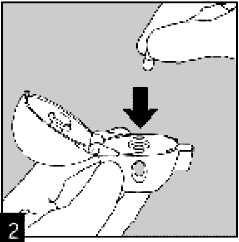
Плотно закрыть мундштук до момента щелчка, пылезащитный колпачок оставить открытым.
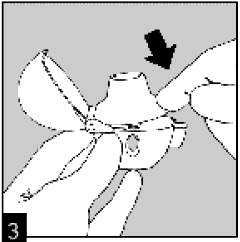
Держа ХандиХалер® мундштуком вверх, нажать прокалывающую кнопку один раз до конца и затем отпустить.
Таким образом, образуется отверстие, через которое препарат высвобождается из капсулы во время вдоха.
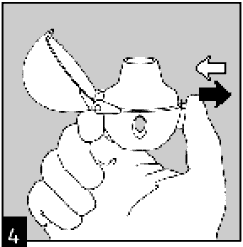
Полностью выдохните.
Внимание: никогда не выдыхайте в мундштук.
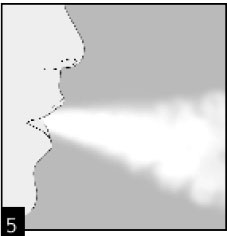
Возьмите ХандиХалер® в рот и плотно сожмите губы вокруг мундштука. Держа голову прямо, вдыхайте медленно и глубоко, но в тоже время с достаточной силой, чтобы услышать вибрацию капсулы. Делайте вдох до полного заполнения легких; затем задержите дыхание до ощущения дискомфорта, одновременно вынимая ХандиХалер® изо рта. Снова продолжайте дышать спокойно. Повторите процедуры 6 и 7, для полного опустошения капсулы.
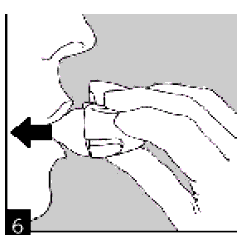
Снова откройте мундштук. Достаньте и выбросите использованную капсулу. Закройте мундштук и пылезащитный колпачок для хранения Вашего прибора ХандиХалер.
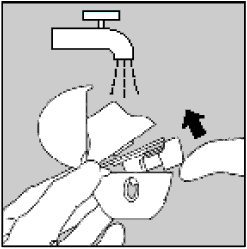
Чистку ХандиХалера® проводите раз в месяц.
Откройте мундштук и пылезащитный колпачок. Затем откройте основание прибора, подняв прокалывающую кнопку. Тщательно промойте ингалятор в теплой воде до полного удаления порошка. ХандиХалер® оботрите бумажным полотенцем и с открытыми мундштуком, основанием и пылезащитным колпачком оставьте сохнуть на воздухе в течение 24 часов. После чистки прибора согласно инструкции, он будет готов к следующему использованию. В случае необходимости наружная поверхность мундштука может быть очищена с помощью влажной, но не мокрой ткани.
Вскрытие блистера
Отделите полоску блистера вдоль перфорированной линии. 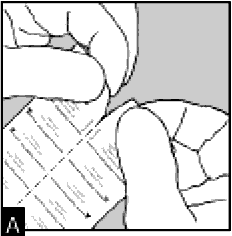
Вскройте полоску блистера непосредственно перед использованием так, чтобы одна капсула была полностью видна. В случае, если вторая капсула случайно была вскрыта (подверглась действию воздуха) не следует ее использовать.
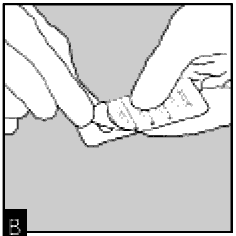
Достаньте капсулу.
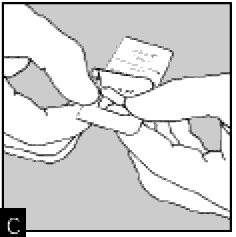
Ни в приборе, ни в блистере капсулы не должны подвергаться воздействию высоких температур, т.е. действию солнечных лучей и др. В капсуле содержится небольшое количество порошка - поэтому капсула заполнена не полностью.
Побочные эффекты
Побочные реакции препарата были выявлены на основании данных, полученных при проведении клинических исследований и отдельных сообщений в течение пострегистрационного использования препарата.
Нарушения со стороны обмена веществ и питания
дегидратация*
Нарушения со стороны желудочно-кишечного тракта
часто (≥1% и < 10 %) - сухость во рту, обычно легкой степени выраженности;
нечасто (≥0,1% и < 1 %) - стоматиты; запор, гастроэзофагеальный рефлюкс;
редко (≥0,01% и < 0,1 %) - кандидоз ротоглотки, гингивиты, глосситы; кишечная
непроходимость, включая паралитический илеус, дисфагия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
нечасто (≥0.1% и < 1 %) - дисфония, кашель, фарингиты;
редко (≥0,01% и < 0,1 %) - пародоксальный бронхоспазм, ларингиты, синуситы, носовое кровотечение.
Нарушения со стороны сердечно-сосудистой системы
нечасто (≥0,1% и < 1 %) - мерцательная аритмия;
редко (≥0,01% и < 0,1 %) - тахикардия (включая суправентрикулярную тахикардию), ощущение сердцебиения.
Нарушения со стороны почек и мочевыводящих путей
нечасто (≥0,1% и < 1 %) - затрудненное мочеиспускание и задержка мочеиспускания (у мужчин с предрасполагающими факторами); дизурия;
редко (≥0,01% и < 0,1 %) - инфекции мочевыводящих путей.
Аллергические реакции
нечасто (≥0,1% и < 1 %) - сыпь;
редко (≥0,01% и < 0,1 %) - крапивница, зуд, реакции повышенной чувствительности,
включая реакции немедленного типа. Ангионевротический отек*.
Нарушения со стороны кожных покровов
кожные инфекции и язвы на коже, сухость кожи*.
Костно-мышечная система и связанные с ней заболевания соединительной ткани
припухание суставов*.
Нарушения со стороны нервной системы
нечасто (≥0,1% и < 1 %) - головокружение;
редко (≥0,01% и < 0,1 %) - бессонница.
Нарушения со стороны органа зрения нечасто
(≥0,1% и < 1 %) - нечеткое зрение;
редко (≥0,01% и < 0,1 %) - повышение внутриглазного давления, глаукома.
* в объединенной базе клинических исследований данные побочные реакции не были выявлены; отмечены лишь единичные сообщения о данных побочных реакциях при широком применении препарата, однако связь с м-холиноблокирующим действием СПИРИВЫ не доказана; частоту этих редких явлений трудно оценить.
Передозировка
При применении высоких доз возможны проявления антихолинергического действия. Однако системные антихолинергические побочные эффекты не выявлялись после однократной ингаляционной дозы до 282 мкг тиотропия при приеме здоровыми добровольцами.
Билатеральный конъюнктивит в сочетании с сухостью во рту наблюдались у здоровых добровольцев после повторного приема однократной суточной дозы 141 мкг, которые исчезали при продолжении лечения. При исследовании, в котором изучался эффект многократных доз тиотропия у пациентов с ХОБЛ, получавших максимально 36 мкг препарата более 4 недель, сухость во рту была единственным побочным эффектом.
Острая интоксикация, связанная со случайным приемом капсул внутрь, маловероятна в связи с низкой биодоступностью препарата.
Взаимодействие с другими лекарственными средствами
Возможно применение тиотропия в комбинации с другими препаратами, обычно использующимися для лечения ХОБЛ: симпатомиметиками, метилксантинами, пероральными и ингаляционными глюкокортикостероидами. Совместное применение с длительнодействующими бета2-агонистами, ингаляционными глюкокортикостероидами и их комбинациями не влияет на действие тиотропия.
Ограниченная информация о совместном применении с антихолинергическими препаратами получила из 2-х клинических исследований: разовое назначение одной дозы ипратропия бромиде на фоне постоянного приема Спиривы у пациентов с ХОБЛ (64 пациента) и у здоровых добровольцев (20 человек) не приводила к уменьшению побочных реакций, изменению жизненных параметров и электрокардиограммы. Однако постоянное сочетанное применение антихолинергических препаратов и Спиривы не изучалось, и, следовательно, не рекомендуется.
Особые указания
Спирива - как бронходилятатор, применяемый раз в сутки для поддерживающего лечения, не должна использоваться в качестве начальной терапии при острых приступах бронхоспазма, т.е. в неотложных случаях.
После ингаляции порошка Спиривы могут развиваться немедленные реакции повышенной чувствительности.
Ингаляция препарата может привести к бронхоспазму.
Больных с умеренной или выраженной почечной недостаточностью (клиренс креатинина креатинина < 50мл/мин) при приеме СПИРИВЫ следует тщательно наблюдать, как это необходимо и в других случаях назначения лекарств, экскретирующихся преимущественно почками.
Пациенты должны быть ознакомлены с правилами использования капсул Спиривы . Не следует допускать попадания порошка в глаза. Боль в глазе или дискомфорт, нечеткое зрение, зрительные ореолы в сочетании с покраснением глаз, конъюнктивальным застоем и отеком роговицы могут свидетельствовать об остром приступе закрытоугольной глаукомы. При развитии любой комбинации этих симптомов следует немедленно обратиться к специалисту. Применение препаратов, вызывающих миоз, не является эффективным способом лечения в данном случае.
Спириву не следует применять чаще, чем раз в день.
Капсулы Спиривы должны применяться только с прибором ХандиХалер®.
В одной дозе/капсуле содержится 5,5 мг лактозы моногидрата.
Влияние на способность водить машину или работать с механизмами.
Не проводилось исследований по изучению такого влияния. Случаи головокружения и нечеткости зрения при приеме препарата могут оказывать такое влияние.
Форма выпуска
Капсулы с порошком для ингаляций 18 мкг.
По 10 капсул в блистер из ПВХ/алюминиевой фольги. 1,3 или 6 блистеров в комплекте с ингалятором ХандиХалер (HandiHaler), или без ингалятора, с инструкцией по применению помещены в картонную пачку.
Условия хранения
При температуре не выше 25°С. Не подвергать замораживанию. Хранить в недоступном для детей месте!
Срок годности
24 месяца.
Не использовать после истечения срока годности указанного на упаковке.
После вскрытия блистер использовать в течение 9 дней.
Условия отпуска из аптек
По рецепту врача.
Производитель
«Берингер Ингельхайм Фарма ГмбХ и Ко.КГ», Германия Бингер штрассе 173 55216 Ингельхайм-на-Рейне, Германия
Получить дополнительную информацию о препарате, а также направить свои претензии и информацию о нежелательных явлениях можно по следующему адресу в России
ООО «Берингер Ингельхайм» 125171, Москва, Ленинградское шоссе, 16А стр.3
Комментарии
ПРАКТИКА ПЕДИАТРА
