Окревус - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер
ЛП-004503
Торговое наименование
Окревус®
Международное непатентованное или группировочное наименование
Окрелизумаб
Лекарственная форма
Концентрат для приготовления раствора для инфузий
Состав
1 флакон содержит:
действующее вещество: окрелизумаб – 300 мг;
вспомогательные вещества: натрия ацетата тригидрат – 21.4 мг, уксусная кислота ледяная – 2.5 мг, α,α-трегалозы дигидрат – 400.0 мг, полисорбат 20 – 2.0 мг, вода для инъекций до 10 мл.
1 мл концентрата содержит 30 мг окрелизумаба.
Описание
Прозрачная или слегка опалесцирующая жидкость от бесцветного до слегка коричневатого цвета.
Фармакотерапевтическая группа
Иммунодепрессанты, селективные иммунодепрессанты.
Код АТХ
L04AA36
Фармакологические свойства
Фармакодинамика
Механизм действия
Окрелизумаб – рекомбинантное гуманизированное моноклональное антитело, селективно воздействующее на В-клетки, экспрессирующие CD20.
CD20 представляет собой поверхностный антиген, расположенный на пре-В-клетках, зрелых В-клетках и В-клетках памяти. CD20 не экспрессируется на стволовых лимфоидных клетках и плазматических клетках.
Точный механизм, посредством которого достигается терапевтический клинический эффект окрелизумаба при рассеянном склерозе (РС), полностью не установлен. Предполагается, что данный механизм включает процесс иммуномодуляции путем уменьшения количества и подавления функции В-клеток, экспрессирующих CD20. После связывания на поверхности В-клеток, экспрессирующих CD20, окрелизумаб селективно уменьшает их количество посредством антителозависимого клеточного фагоцитоза, антителозависимой клеточной цитотоксичности, комплементзависимой цитотоксичности и апоптоза. Способность к восстановлению В-клеток и существующий гуморальный иммунитет сохраняются. Кроме того, окрелизумаб не влияет на врожденный иммунитет и общее количество Т-клеток.
Фармакодинамические эффекты
К 14 дню терапии (первая точка оценки) окрелизумабом наблюдалось быстрое истощение пула CD19+ В-клеток в крови, которое сохранялось в течение всего периода лечения и являлось ожидаемым фармакологическим эффектом. Для подсчета количества В-клеток используется именно CD19, так как окрелизумаб препятствует распознаванию CD20 при проведении анализа.
В исследованиях III фазы в периодах между введениями окрелизумаба наблюдалось восстановление пула В-клеток (до исходного значения или выше нижней границы нормы (НГН)), как минимум, однократно приблизительно у 5% пациентов.
Степень и длительность истощения пула В-клеток в исследованиях при первично-прогрессирующем рассеянном склерозе (ППРС) и рецидивирующих формах РС были сходными.
По результатам наиболее длительного периода наблюдения с момента последней инфузии окрелизумаба (исследование II фазы, WA21493, N=51) медиана периода восстановления пула В-клеток (возвращение к НГН или к исходному значению, если оно меньше НГН) составила 72 недели (27-175 недель). У 90% пациентов пул В-клеток восстановился до значений НГН или исходного значения приблизительно через два с половиной года после последней инфузии препарата.
Клиническая эффективность и безопасность
Клинические исследования при рецидивирующих формах РС
Профиль эффективности и безопасности окрелизумаба оценивали у пациентов с рецидивирующими формами РС (согласно диагностическим критериям МакДональда 2010) и с признаками активности заболевания (определяемыми клиническими или визуализирующими признаками) в течение предыдущих 2 лет в двух рандомизированных, двойных слепых клинических исследованиях (WA21092, WA21093) с идентичным дизайном, с двойной имитацией и с использованием активного препарата сравнения (интерферон бета-1а). Дизайн исследования и исходные характеристики исследуемой популяции представлены в таблице 1.
Демографические и исходные характеристики были сбалансированы в обеих группах терапии. Пациенты группы А получали окрелизумаб 600 мг каждые 6 месяцев (доза 1 в виде 2 внутривенных (в/в) инфузий по 300 мг с интервалом в 2 недели), последующие дозы вводились в виде однократной в/в инфузии 600 мг. Пациенты группы B получали интерферон бета-1а 44 мкг 3 раза в неделю подкожно.
Таблица 1. Дизайн исследований, демографические и исходные характеристики
| Название исследования | Исследование 1 | Исследование 2 | ||
| WA21092 (OPERA I) (n = 821) |
WA21093 (OPERA II) (n = 835) |
|||
| Дизайн исследования | ||||
| Исследуемая популяция | Пациенты с рецидивирующими формами РС | |||
| История болезни при скрининге | Как минимум два рецидива в течение предшествующих двух лет или один рецидив в течение предшествующего года; оценка по шкале EDSS* от 0 до 5.5 балла включительно | |||
| Продолжительность исследования | 2 года | |||
| Группы лечения | Группа А: окрелизумаб, 600 мг Группа В: интерферон бета-1а, 44 мкг, подкожно |
|||
| Исходные характеристики | Окрелизумаб, 600 мг (n = 410) |
Интерферон бета-1а, 44 мкг (n = 411) |
Окрелизумаб, 600 мг (n = 417) |
Интерферон бета-1а, 44 мкг (n = 418) |
| Средний возраст (лет) | 37.1 | 36.9 | 37.2 | 37.4 |
| Возрастной диапазон (лет) при включении | 18-56 | 18-55 | 18-55 | 18-55 |
| Распределение по полу (%, мужчины/%, женщины) | 34.1/65.9 | 33.8/66.2 | 35.0/65.0 | 33.0/67.0 |
| Среднее значение/медиана продолжительности заболевания с момента постановки диагноза (лет) | 3.82/1.53 | 3.71/1.57 | 4.15/2.10 | 4.13/1.84 |
| Пациенты, ранее не получавшие болезнь-модифицирующие препараты (БМП) (%)** | 73.4 | 71.0 | 72.7 | 74.9 |
| Среднее количество рецидивов за прошедший год | 1.31 | 1.33 | 1.32 | 1.34 |
| Доля пациентов с очагами, накапливающими гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях | 42.5 | 38.1 | 39.0 | 41.4 |
| Средняя оценка по шкале EDSS* | 2.82 | 2.71 | 2.73 | 2.79 |
* EDSS – расширенная шкала оценки степени инвалидизации (Expanded Disability Status Scale)
** Пациенты, не получавшие БМП в течение 2 лет до рандомизации
Основные клинические результаты и результаты магнитно-резонансной томографии (МРТ) для оценки эффективности представлены в таблице 2 и на рисунке 1.
Результаты этих исследований показывают, что окрелизумаб значительно подавлял рецидивы, субклиническую активность заболевания, определяемую с помощью МРТ, и прогрессирование заболевания по сравнению с интерфероном бета-1а в дозе 44 мкг подкожно.
Таблица 2. Основные клинические конечные точки и конечные точки по данным МРТ в исследованиях WA21092 и WA21093 (рецидивирующие формы РС)
| Конечные точки | Исследование 1: WA21092 (OPERA I) |
Исследование 2: WA21093 (OPERA II) |
||
| Окрелизумаб 600 мг (n = 410) | Интерферон бета-1а, 44 мкг (n = 411) | Окрелизумаб 600 мг (n = 417) | Интерферон бета-1а, 44 мкг (n = 418) | |
| Клинические конечные точки | ||||
| Годовая частота развития рецидивов (первичная конечная точка)8 | 0.156 | 0.292 | 0.155 | 0.290 |
| Относительное сокращение | 46% (p<0.0001) |
47% (p<0.0001) |
||
| Доля пациентов с подтвержденным прогрессированием инвалидизации в течение 12 недель3 | 9.8% в группе окрелизумаба по сравнению с 15.2% в группе интерферона бета-1а | |||
| Снижение риска (объединенный анализ1) | 40% (p = 0.0006)7 |
|||
| Снижение риска (отдельные исследования2) | 43% (p = 0.0139)7 |
37% (p = 0.0169)7 |
||
| Доля пациентов с подтвержденным прогрессированием инвалидизации в течение 24 недель3 | 7.6% в группе окрелизумаба по сравнению с 12.0% в группе интерферона бета-1а | |||
| Снижение риска (объединенный анализ1) | 40% (p = 0.0025)7 |
|||
| Снижение риска (отдельные исследования2) | 43% (p = 0.0278)7 |
37% (p = 0.0370)7 |
||
| Доля пациентов с подтвержденным уменьшением степени инвалидизации в течение как минимум 12 недель4 (объединенный анализ) | 20.7% в группе окрелизумаба по сравнению с 15.6% в группе интерферона бета-1а | |||
| Относительное улучшение (объединенный анализ1) | 33% (p = 0.0194) | |||
| Относительное улучшение (отдельные исследования2) | 61% (p = 0.0106) |
14% (p = 0.4019) |
||
| Доля пациентов без рецидивов через 96 недель2 | 80.4% | 66.7% | 78.9% | 64.3% |
| (p <0.0001) | (p <0.0001) | |||
| Доля пациентов с отсутствием признаков активности заболевания (No Evidence of Disease Activity – NEDA)5 | 48% | 29% | 48% | 25% |
| Относительное улучшение2 | 64% (p<0.0001) | 89% (p<0.0001) | ||
| Конечные точки по данным МРТ | ||||
| Среднее число очагов, накапливающих гадолиний-содержащее контрастное вещество, на Т-1 взвешенных изображениях на МРТ | 0.016 | 0.286 | 0.021 | 0.416 |
| Относительное уменьшение | 94% (p <0.0001) | 95% (p <0.0001) | ||
| Среднее количество новых и/или увеличение существующих гиперинтенсивных очагов на Т-2 взвешенных изображениях на МРТ | 0.323 | 1.413 | 0.325 | 1.904 |
| Относительное уменьшение | 77% (p <0.0001) | 83% (p <0.0001) | ||
| Процентное изменение объема головного мозга с недели 24 по неделю 96 | -0.572 | -0.741 | -0.638 | -0.750 |
| Относительное снижение потери объема головного мозга | 22.8% (p = 0.0042)6 |
14.9% (p = 0.0900) |
||
1 Проспективно объединены данные из исследований 1 и 2.
2 Неподтвержденный p-критерий; не является частью предварительно определенной иерархии тестирования
3 Определяется как увеличение на ≥1.0 балла по сравнению с исходной оценкой по шкале EDSS у пациентов с исходной оценкой ≤5.5 балла или увеличение на ≥0.5 балла при исходной оценке >5.5 балла, оценка Каплана-Мейера на неделе 96.
4 Определяется как уменьшение на ≥1.0 балла по сравнению с исходной оценкой по шкале EDSS у пациентов с исходным баллом по шкале EDSS ≥2 и ≤5.5 или уменьшение на ≥0.5 балла при исходной оценке >5.5 балла. В анализ не были включены пациенты с исходной оценкой <2 баллов.
5 Статус NEDA определяется как отсутствие определенных в протоколе рецидивов, подтвержденного прогрессирования инвалидизации (ППИ) и любой активности заболевания по результатам МРТ (очаги, накапливающие гадолиний-содержащий контраст, на Т1-взвешенных изображениях, либо появление новых или увеличение существующих очагов на Т2-взвешенных изображениях) в течение всего 96-недельного периода лечения. Результаты поискового анализа получены для всей ITT-популяции.
6 Неподтвержденный р-критерий; процедура иерархического исследования прекращена до достижения конечной точки.
7 Лог-ранговый критерий
8 Подтвержденный рецидив (сопровождающийся клинически значимым изменением в соответствии со шкалой EDSS)
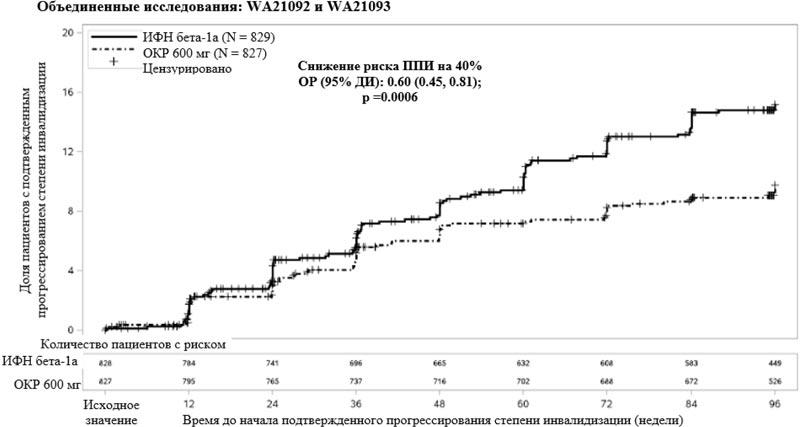 Рисунок 1. Кривая Каплана-Мейера – время до ППИ, сохраняющегося в течение по меньшей мере 12 недель, от эпизода неврологического ухудшения, случившегося в период двойной слепой фазы (объединенная популяция в соответствии с назначенным лечением (ITT-популяция), исследования WA21092 и WA21093)*
Рисунок 1. Кривая Каплана-Мейера – время до ППИ, сохраняющегося в течение по меньшей мере 12 недель, от эпизода неврологического ухудшения, случившегося в период двойной слепой фазы (объединенная популяция в соответствии с назначенным лечением (ITT-популяция), исследования WA21092 и WA21093)*
Результаты предварительно заданного объединенного анализа времени до ППИ, сохраняющегося в течение по крайней мере 12 недель (снижение риска на 40% при применении окрелизумаба по сравнению с интерфероном бета-1а, p = 0.0006), в значительной степени сопоставимы с результатами применения в течение, как минимум, 24 недель (снижение риска на 40% при применении окрелизумаба по сравнению с интерфероном бета-1а, р = 0.0025).
В исследования включали пациентов с активным заболеванием, к ним относились как пациенты, ранее не получавшие активного лечения, так и пациенты с недостаточным ответом на лечение, что определялось по клиническим данным или результатам визуализирующих тестов.
Анализ популяций пациентов с различными исходными уровнями активности заболевания, включая активное и высокоактивное заболевание, показал, что эффективность окрелизумаба в снижении годовой частоты развития рецидивов и ППИ в течение 12 недель соответствовала таковой в общей популяции.
Клинические исследования при ППРС
Профиль эффективности и безопасности окрелизумаба оценивали в ходе рандомизированного, двойного слепого, плацебо-контролируемого клинического исследования при участии пациентов с ППРС (WA25046) на ранней стадии заболевания согласно основным критериям включения: возраст 18-55 лет включительно; оценка по шкале EDSS при скрининге от 3.0 до 6.5 баллов; длительность заболевания от появления симптомов РС менее 10 лет у пациентов с оценкой по шкале EDSS при скрининге ≤5.0 баллов или менее 15 лет у пациентов с оценкой по шкале EDSS при скрининге >5.0 баллов. Что касается активности заболевания, признаки, характерные для воспалительной активности, даже при прогрессирующем РС, могут быть связаны с результатами визуализирующих тестов (т. е. очаги, накапливающие гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях и/или активные (новые или увеличивающиеся) очаги на Т2-взвешенных изображениях). Данные МРТ необходимо использовать для подтверждения воспалительной активности у всех пациентов. Пациентов старше 55 лет не включали в исследование. Дизайн исследования и исходные характеристики исследуемой популяции представлены в таблице 3.
Демографические признаки и исходные характеристики были хорошо сбалансированы в обеих группах терапии. МРТ головного мозга показала признаки, характерные для воспалительной активности, в очагах, накапливающих гадолиний-содержащее контрастное вещество на Т1 – или Т2-взвешенных изображениях.
Во время исследования III фазы пациенты с ППРС получали окрелизумаб в дозе 600 мг каждые 6 месяцев в виде двух инфузий по 300 мг с интервалом в две недели, в течение всего периода лечения. Однократная инфузия 600 мг среди популяции пациентов с рецидивирующими формами РС и 2 инфузии по 300 мг каждая у пациентов с ППРС показали сходные фармакокинетические и фармакодинамические профили.
Профили инфузионных реакций были также сходными независимо от того, вводился ли окрелизумаб в виде однократной в/в инфузии в дозе 600 мг или в виде двух отдельных инфузий по 300 мг каждая с интервалом в 2 недели (см. подраздел «Фармакокинетика» и раздел «Побочное действие»); поскольку суммарное количество инфузий было больше при введении доз по 300 мг с интервалом в 2 недели, то в этой группе общее количество инфузионных реакций было выше.
Таким образом, после введения первой дозы, в последующем рекомендуется применять 600 мг окрелизумаба в виде однократной инфузии (см. раздел «Способ применения и дозы»), чтобы снизить общее количество инфузий (при одновременной профилактической премедикации метилпреднизолоном и антигистаминным препаратом) и связанных с ними инфузионных реакций.
Таблица 3. Дизайн исследования, демографические и исходные характеристики исследования WA25046
| Название исследования | Исследование WA25046 ORATORIO (n=732) | |
| Дизайн исследования | ||
| Популяция исследования | Пациенты с ППРС | |
| Длительность исследования | Определяется на основе наступления событий (минимум 120 недель и 253 подтвержденных случая прогрессирования инвалидизации) Среднее время последующего наблюдения: окрелизумаб 3.0 года, плацебо 2.8 года |
|
| Анамнез заболевания при скрининге | Возраст 18-55 лет Оценка по шкале EDSS: 3.0-6.5 |
|
| Группы лечения | Группа А: окрелизумаб, 600 мг Группа В: плацебо, рандомизация 2:1 |
|
| Исходные характеристики | Окрелизумаб, 600 мг (n=488) | Плацебо (n=244) |
| Средний возраст (годы) | 44.7 | 44.4 |
| Возрастной диапазон (годы) при включении в исследование | 20-56 | 18-56 |
| Распределение по полу (% мужчины/% женщины) | 51.4/48.6 | 49.2/50.8 |
| Средняя/ медианная длительность с момента постановки диагноза ППРС (годы) | 2.9/1.6 | 2.8/1.3 |
| Среднее значение оценки по шкале EDSS | 4.7 | 4.7 |
Клинические конечные точки и конечные точки по данным МРТ приведены в таблице 4 и на рисунке 2.
Результаты данного исследования показали, что окрелизумаб значимо замедляет прогрессирование заболевания и снижает ухудшение показателей скорости ходьбы в сравнении с плацебо.
Таблица 4. Клинические конечные точки и конечные точки по данным МРТ в исследовании WA25046 (ППРС)
| Конечные точки | Исследование 3 | |
| WA25046 (ORATORIO) | ||
| Окрелизумаб, 600 мг (n=488) |
Плацебо (n=244) |
|
| Клинические конечные точки | ||
| Первичная конечная точка эффективности
Доля пациентов с 12-недельным подтвержденным прогрессированием инвалидизации1 (первичная конечная точка) |
30.2% | 34.0% |
| Снижение риска | 24% (p=0.0321) |
|
| Доля пациентов с 24-недельным подтвержденным прогрессированием инвалидизации1 | 28.3% | 32.7% |
| Снижение риска | 25% (p=0.0365) |
|
| Процентное изменение измеренного времени ходьбы на расстояние 25 футов с начала исследования до 120 недели | 38.9 | 55.1 |
| Относительное снижение скорости увеличения времени ходьбы | 29.4% (p=0.0404) |
|
| Конечные точки по данным МРТ | ||
| Процентное изменение объема гиперинтенсивных очагов на Т2-взвешенных изображениях с начала исследования до 120 недели | -3.4 | 7.4 |
| (p<0.0001) | ||
| Процентное изменение объема мозга с 24-й по 120-ю неделю | -0.902 | -1.093 |
| Темп относительного снижения потери объема мозга | 17.5% (p=0.0206) | |
1 Определено как увеличение на ≥1.0 пункт по шкале EDSS для пациентов с исходным уровнем 5.5 или меньше, или увеличение на ≥0.5, если исходный уровень шкалы >5.5, оценка Каплана-Майера была зафиксирована на 120 неделе.
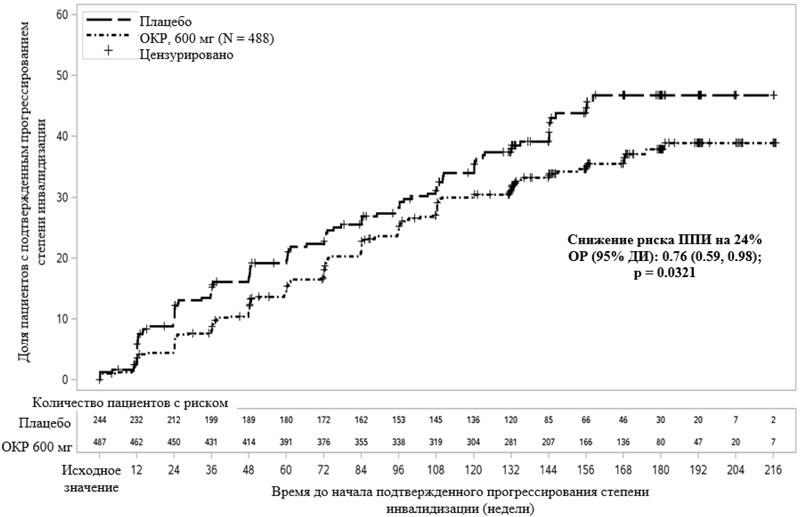 Рисунок 2. Кривая Каплана-Майера времени до начала подтвержденного прогрессирования, сохраняющегося как минимум 12 недель от эпизода неврологического ухудшения, который возник в период двойной слепой фазы исследования (WA25046, ITT-популяция)* * Продолжительность последующего наблюдения для всех пациентов, включенных в данный анализ, составляла как минимум 120 недель. В первичный анализ включены все возникшие явления.
Рисунок 2. Кривая Каплана-Майера времени до начала подтвержденного прогрессирования, сохраняющегося как минимум 12 недель от эпизода неврологического ухудшения, который возник в период двойной слепой фазы исследования (WA25046, ITT-популяция)* * Продолжительность последующего наблюдения для всех пациентов, включенных в данный анализ, составляла как минимум 120 недель. В первичный анализ включены все возникшие явления.
Предварительно определенный анализ первичной конечной точки в подгруппах без заданной статистической мощности позволяет предположить, что более молодые пациенты или пациенты с очагами, изначально накапливающими гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях, получают большую пользу от лечения, чем более взрослые пациенты или пациенты без очагов, накапливающими гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях (≤45 лет: ОР = 0.64 [0.45; 0.92], >45 лет: ОР = 0.88 [0.62; 1.26]; с очагами, изначально накапливающими гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях: ОР = 0.65 [0.40; 1.06]; без очагов, изначально накапливающих гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях: ОР = 0.84 [0.62; 1.13]).
Кроме того, ретроспективные анализы показали, что у более молодых пациентов с очагами, изначально накапливающими гадолиний-содержащее контрастное вещество на Т1-взвешенных изображениях, терапия более эффективна (≤45 лет: ОР = 0.52 [0.27; 1.00]; ≤46 лет [медиана возраста участников исследования WA25046]: ОР = 0.48 [0.25; 0.92]; <51 года: ОР = 0.53 [0.31; 0.89]).
Был проведен ретроспективный анализ в рамках расширенного контролируемого периода исследования, который включал в себя этап применения препарата в двойном слепом режиме и приблизительно 9 месяцев последующего контролируемого наблюдения до перехода пациентов в открытый расширенный период исследования или до завершения применения препарата в исследовании. Доля пациентов с оценкой ППИ в течение 24 недель по шкале EDSS ≥7.0 балла (24Н-ППИ EDSS ≥7.0 балла, время до начала использования инвалидного кресла) составила 9.1% в группе плацебо по сравнению с 4.8% в группе окрелизумаба на неделе 144. Таким образом, снижение риска в отношении времени до начала использования инвалидного кресла в расширенном контролируемом периоде исследования составило 47% (ОР 0.53 [0.31; 0.92]). Данные результаты носили исследовательский характер и включали данные после расслепления, поэтому их следует интерпретировать с осторожностью.
Дополнительное исследование коротких инфузий
Профиль безопасности короткой (2 часа) инфузии окрелизумаба оценивали у пациентов с рецидивирующими формами РС, не получающих БМП в проспективном многоцентровом рандомизированном, двойном слепом контролируемом дополнительном исследовании с параллельными группами MA30143 (Ensemble). Первую дозу препарата вводили в виде двух инфузий по 300 мг (всего 600 мг) с интервалом 14 дней. Пациенты были рандомизированы после получения второй дозы препарата (со 2-й по 6-ю дозу) в соотношении 1:1 в группу стандартной инфузии окрелизумаба продолжительностью приблизительно 3.5 часа каждые 24 недели или в группу короткой инфузии окрелизумаба продолжительностью приблизительно 2 часа каждые 24 недели. Рандомизация была стратифицирована по региону и дозе препарата, которую пациенты получали после первой рандомизации.
Первичной конечной точкой была доля пациентов с инфузионными реакциями, возникшими в течение 24 часов после получения первой инфузии в соответствии с рандомизацией. Первичный анализ был проведен после рандомизации 580 пациентов. Соотношение пациентов с инфузионными реакциями, развившимися во время инфузии или в течение 24 часов после первой рандомизированной инфузии составило 24.6% в группе короткой инфузии и 23.1% в группе стандартной инфузии. Разница в стратифицированных группах была сопоставимой. Во всех рандомизированных дозах большинство инфузионных реакций было легкой или средней степени тяжести, отмечалось только 2 инфузионные реакции тяжелой степени тяжести, по одной в каждой группе. Не отмечалось жизнеугрожающих, летальных или серьезных инфузионных реакций.
Иммуногенность
У пациентов, участвующих в исследованиях РС (WA21092, WA21093 и WA25046), проводили тестирование на наличие антитерапевтических антител (АТА) в нескольких временных точках (перед первым введением и каждые 6 месяцев в течение всего исследования). Из 1311 пациентов, получавших лечение окрелизумабом, положительный результат анализа на АТА отмечался у 12 пациентов (~1%), из которых у 2 пациентов положительный результат анализа отмечался на нейтрализующие антитела. Оценить влияние возникших во время лечения АТА на профиль безопасности и эффективности терапии не представляется возможным из-за низкой частоты встречаемости АТА к окрелизумабу.
Иммунизация
В рандомизированном открытом исследовании у пациентов с рецидивирующими формами РС (N = 102) доля пациентов с положительным ответом на вакцину от столбняка через 8 недель после вакцинации составляла 23.9% в группе окрелизумаба по сравнению с 54.5% в контрольной группе (без применения БМП, кроме интерферона-бета). Средние геометрические значения титров специфических антител к столбнячному анатоксину через 8 недель составляли 3.74 и 9.81 МЕ/мл, соответственно. Положительный ответ на ≥5 серотипов 23-валентной пневмококковой полисахаридной вакцины (23-PPV) через 4 недели после вакцинации составил 71.6% в группе окрелизумаба и 100% в контрольной группе. У пациентов, получавших окрелизумаб, бустерная 13-валентная пневмококковая конъюгированная вакцина (13-PCV), введенная через 4 недели после введения 23-PPV, не привела к заметному усилению ответа на 12 серотипов, общих с 23-PPV. Доля пациентов с серопротективными титрами в отношении пяти штаммов гриппа в группе окрелизумаба находилась в пределах 20.0-60.0% до вакцинации и 55.6-80.0% через 4 недели после вакцинации; в контрольной группе – 16.7-43.8% до вакцинации и 75.0-97.0% через 4 недели после вакцинации. См. разделы «Взаимодействие с другими лекарственными средствами» и «Особые указания».
Данные доклинической безопасности
Данные доклинической безопасности не выявили потенциального риска для человека на основании результатов фармакологических исследований безопасности, токсичности при многократном введении и эмбриофетального развития. Исследования канцерогенности и мутагенности окрелизумаба не проводили.
В двух исследованиях пре- и постнатального развития у яванских макак введение окрелизумаба с 20-го дня беременности, как минимум, до родов было связано с гломерулопатией, образованием лимфоидных фолликулов в костном мозге, лимфоплазмоцитарным воспалением почек и снижением массы яичек у потомства. Дозы, которые вводились беременным самкам, в данных исследованиях приводили к максимальным средним концентрациям в сыворотке (Cmax), которые были в 4.5-21 раз выше ожидаемых в клинических условиях.
Было зарегистрировано пять случаев смерти новорожденных, одна из которых была связана со слабостью из-за преждевременных родов, сопровождавшихся оппортунистической бактериальной инфекцией, другая – вследствие инфекционного менингоэнцефалита с поражением мозжечка новорожденного от матери с активной бактериальной инфекцией (мастит). В трех случаях новорожденные имели признаки желтухи и поражения печени с подозрением на вирусную этиологию, возможно, полиомавирус. Течение данных 5 подтвержденных или подозреваемых инфекций могло быть потенциально вызвано истощением В-клеток. Отмечено, что у новорожденного потомства самок, которым вводили окрелизумаб в постнатальном периоде наблюдалось истощение пула В-клеток. Измеряемый уровень окрелизумаба был обнаружен в грудном молоке (приблизительно 0.2% от уровня в сыворотке в равновесном состоянии) в течение периода лактации.
Фармакокинетика
Фармакокинетические (ФК) свойства окрелизумаба в исследованиях при РС описаны с помощью двухкамерной модели с зависимым от времени клиренсом и с использованием ФК параметров, характерных для моноклонального антитела класса IgG1.
Суммарные значения площади под кривой «концентрация-время» (AUC) в течение 24-недельных интервалов дозирования были идентичными при двукратном введении 300 мг у пациентов с ППРС и при однократном введении 600 мг препарата в исследованиях у пациентов с рецидивирующими формами РС. Значение площади под кривой «концентрация-время» за период дозирования (AUCτ) после 4-го введения окрелизумаба в дозе 600 мг составило 3510 мкг/мл·сут. Средняя максимальная концентрация (Cmax) составляла 212 мкг/мл при рецидивирующих формах РС (инфузия 600 мг) и 141 мкг/мл при ППРС (инфузия 300 мг).
Абсорбция
Окрелизумаб вводится в/в. Другие пути введения препарата не изучались.
Распределение
Согласно данным популяционной фармакокинетики рассчитанное значение центрального объема распределения составило 2.78 л. Рассчитанные значения периферического объема распределения и межкамерного клиренса составили 2.68 л и 0.294 л/сут, соответственно.
Биотрансформация
Отдельных исследований метаболизма окрелизумаба не проводилось. Как и другие антитела, окрелизумаб преимущественно подвергается катаболизму (т.е. распаду на пептиды и аминокислоты).
Элиминация
Рассчитанный показатель постоянного клиренса составил 0.17 л/сут. Первоначальный зависимый от времени клиренс составил 0.0489 л/сут с дальнейшим уменьшением при периоде полувыведения 33 недели. Терминальный период полувыведения составил 26 дней.
Фармакокинетика у особых групп пациентов
Дети
Исследований фармакокинетики окрелизумаба у детей и подростков в возрасте <18 лет не проводилось.
Лица пожилого возраста
Специальные исследования фармакокинетики окрелизумаба у пациентов ≥55 лет отсутствуют из-за ограниченного клинического опыта применения препарата в данной популяции (см. раздел «Способ применения и дозы»).
Почечная недостаточность
Отдельных исследований фармакокинетики не проводилось. Пациенты с нарушением функции почек легкой степени тяжести были включены в программу клинических исследований. Изменений фармакокинетических параметров окрелизумаба у таких пациентов не наблюдалось. Доступная информация о фармакокинетике у пациентов с нарушением функции почек средней и тяжелой степени тяжести отсутствует.
Печеночная недостаточность
Отдельных исследований фармакокинетики не проводилось. Пациенты с нарушением функции печени легкой степени тяжести были включены в клинические исследования. Изменений ФК параметров окрелизумаба у таких пациентов не наблюдалось. Доступная информация о фармакокинетике у пациентов с нарушением функции печени средней и тяжелой степени тяжести отсутствует.
Показания к применению
Препарат Окревус® показан к применению у взрослых пациентов с рецидивирующими формами рассеянного склероза с активным заболеванием, определяемым клиническими или визуализирующими признаками (см. раздел «Фармакологические свойства»).
Препарат Окревус® показан к применению у взрослых пациентов с ранним первично-прогрессирующим рассеянным склерозом в зависимости от продолжительности заболевания и уровня инвалидизации, а также с признаками воспалительной активности по данным визуализирующих исследований (см. раздел «Фармакологические свойства»).
Противопоказания
Гиперчувствительность к окрелизумабу или любому из вспомогательных веществ.
Активная инфекция (см. раздел «Особые указания»).
Тяжелый иммунодефицит (см. раздел «Особые указания»).
Установленные активные злокачественные новообразования (см. раздел «Особые указания»).
С осторожностью
Применение других БМП для лечения РС.
Применение во время беременности и в период грудного вскармливания
Женщины с детородным потенциалом
Женщины с детородным потенциалом должны использовать эффективные методы контрацепции в период лечения окрелизумабом и в течение 12 месяцев после последней инфузии препарата.
Беременность
Данные по применению окрелизумаба у беременных женщин ограничены.
Окрелизумаб предположительно проникает через плацентарный барьер, так как относится к иммуноглобулинам подтипа G1.
Следует отложить вакцинацию живыми или живыми ослабленными вакцинами у новорожденных и детей, матери которых получали окрелизумаб в ходе беременности.
Изменение числа В-клеток у новорожденных и детей, матери которых получали окрелизумаб, не изучалось в клинических исследованиях. Длительность потенциального истощения пула В-клеток у новорожденных и детей неизвестна (см. раздел «Особые указания»).
У некоторых новорожденных, матери которых получали другие антитела к CD20 во время беременности, наблюдались временное истощение пула периферических В-клеток и лимфоцитопения.
Исследования у животных (эмбриофетальная токсичность) не выявили тератогенных эффектов. Однако отмечалось истощение пула В-клеток во время внутриутробного развития. В ходе пре- и постнатальных исследований развития отмечалась репродуктивная токсичность (см. раздел «Фармакологические свойства», подраздел «Данные доклинической безопасности)».
Следует избегать применения окрелизумаба во время беременности, за исключением случаев, когда потенциальная польза для матери превышает возможный риска для плода.
Лактация
Неизвестно, выводятся ли окрелизумаб/его метаболиты с грудным молоком.
Согласно доступным данным по фармакодинамике/токсикологии, полученным у животных, окрелизумаб проникает в молоко (см. раздел «Фармакологические свойства», подраздел «Данные доклинической безопасности).
Риск для новорожденных и младенцев не может быть исключен.
Женщинам следует рекомендовать прекратить грудное вскармливание во время терапии окрелизумабом.
Фертильность
Согласно доклиническим данным, полученным в результате изучения фертильности у самцов и самок яванских макак, особых рисков для человека не выявлено.
Способ применения и дозы
Лечение следует начинать и проводить под контролем врача-специалиста, имеющего опыт в диагностике и лечении неврологических заболеваний и при наличии доступа к медицинским средствам для купирования тяжелых реакций, таких как серьезные инфузионные реакции.
Премедикация для профилактики инфузионных реакций
Перед каждым введением окрелизумаба с целью снижения частоты и тяжести инфузионных реакций следует проводить следующую двухкомпонентную премедикацию (см. раздел «Особые указания» по дополнительным шагам для снижения частоты и тяжести инфузионных реакций):
- метилпреднизолон (или эквивалентный лекарственный препарат) в дозе 100 мг в/в приблизительно за 30 минут до каждой инфузии;
- антигистаминный препарат приблизительно за 30-60 минут до каждой инфузии.
В дополнение следует рассмотреть премедикацию антипиретиком (например, парацетамолом) приблизительно за 30-60 минут до начала каждой инфузии.
Режим дозирования
Начальная доза
Начальную дозу 600 мг следует вводить в виде двух отдельных в/в инфузий: с первой инфузией вводят 300 мг препарата, затем через 2 недели вводят еще 300 мг препарата (см. таблицу 5).
Последующие дозы
Все последующие дозы окрелизумаба в дальнейшем вводятся в виде однократной в/в инфузии в дозе 600 мг каждые 6 месяцев (см. таблицу 5). Первую из последующих доз 600 мг следует проводить через 6 месяцев после 1-ой инфузии начальной дозы.
Минимальный интервал между каждым введением окрелизумаба должен составлять 5 месяцев.
Коррекция дозы при инфузионных реакциях
Жизнеугрожающие инфузионные реакции
Если во время инфузии возникли симптомы жизнеугрожающих или инвалидизирующих инфузионных реакций, такие как острая гиперчувствительность или острый респираторный дистресс-синдром, инфузию следует немедленно прекратить. Пациент должен получить соответствующее поддерживающее лечение. У таких пациентов применение окрелизумаба следует отменить и не возобновлять в дальнейшем (см. раздел «Противопоказания»).
Тяжелые инфузионные реакции
При развитии тяжелой инфузионной реакции (например, одышки) или при одновременном появлении приливов, лихорадки и боли в горле, инфузию следует немедленно прекратить. Пациенту необходимо провести симптоматическое лечение. Инфузию можно возобновить только после разрешения всех симптомов. Начальная скорость при возобновлении инфузии должна быть в два раза ниже, чем скорость инфузии на момент начала развития реакции. Для последующих инфузий коррекция дозы не требуется, за исключением случаев, когда у пациента разовьется инфузионная реакция.
Инфузионные реакции легкой или средней степени тяжести
При развитии инфузионной реакции легкой или средней степени тяжести (например, головной боли) скорость инфузии следует снизить до половины скорости на момент начала явления. Следует продолжать введение с данной сниженной скоростью в течение минимум 30 минут. В случае хорошей переносимости инфузии, скорость введения можно увеличить в соответствии с изначальным графиком. Для последующих инфузий коррекция дозы не требуется, за исключением случаев, когда у пациента разовьется инфузионная реакция.
Коррекция дозы в ходе терапии
Приведенные выше примеры прерывания инфузии или снижения ее скорости (в случае инфузионных реакций легкой/средней и тяжелой степени тяжести) приведут к изменению скорости инфузии и увеличению общей продолжительности инфузии, но не дозы. Снижение дозы окрелизумаба не рекомендуется.
Задержка или пропуск дозы
При пропуске в плановом введении окрелизумаба необходимо в кратчайшие сроки ввести препарат в рекомендуемой дозе, не дожидаясь следующего запланированного введения.
График введений окрелизумаба должен быть скорректирован с целью поддержания 6-ти месячного (минимум 5-ти месячного) интервала между введениями (см. таблицу 5).
Особые указания по дозированию
Пациенты старше 55 лет и пожилого возраста
Согласно имеющимся ограниченным данным (см. раздел «Фармакологические свойства»), у пациентов >55 лет коррекция дозы не требуется. Пациенты, включенные в текущие клинические исследования, продолжают получать окрелизумаб в дозе 600 мг каждые 6 месяцев после того, как им исполнится 55 лет.
Пациенты с нарушением функции почек
Безопасность и эффективность применения окрелизумаба у пациентов с нарушением функции почек отдельно не изучались. В клинические исследования были включены пациенты с нарушением функции почек легкой степени тяжести. Опыт применения препарата у пациентов с нарушением функции почек средней или тяжелой степени тяжести отсутствует. Так как окрелизумаб представляет собой моноклональное антитело, которое выводится путем катаболизма (распада на пептиды и аминокислоты), предполагается, что у пациентов с нарушением функции почек изменения дозы не требуется (см. раздел «Фармакологические свойства»).
Пациенты с нарушением функции печени
Безопасность и эффективность применения окрелизумаба у пациентов с нарушением функции печени отдельно не изучались. В клинические исследования были включены пациенты с нарушением функции печени легкой степени тяжести. Опыт применения препарата у пациентов с нарушением функции печени средней или тяжелой степени тяжести отсутствует. Так как окрелизумаб представляет собой моноклональное тело, которое выводится путем катаболизма (а не печеночного метаболизма), предполагается, что изменение дозы у пациентов с нарушением функции печени не требуется (см. раздел «Фармакологические свойства»).
Дети
Безопасность и эффективность окрелизумаба у детей в возрасте от 0 до 18 лет не установлены. Данные отсутствуют.
Способ применения
После разведения, препарат вводят путем в/в инфузии через отдельную инфузионную систему. Вводить препарат в/в струйно или болюсно нельзя.
Если в течение всех предыдущих инфузий окрелизумаба у пациента не отмечалось серьезных инфузионных реакций, последующие дозы препарата можно вводить более короткими (2 часа) инфузиями (см. таблицу 5, вариант 2).
Таблица 5. Схема дозирования
| Количество окрелизумаба, подлежащее введению | Инструкции по проведению инфузии | ||
| Начальная доза (600 мг), разделенная на 2 инфузии | 1-ая инфузия | 300 мг в 250 мл | - Начать инфузию со скоростью 30 мл/ч в течение 30 минут. - Затем скорость можно увеличивать с шагом 30 мл/ч каждые 30 минут до максимальной скорости 180 мл/ч. - Каждую инфузию следует проводить в течение приблизительно 2. 5 часов. |
| 2-ая инфузия (через 2 недели после первой) | 300 мг в 250 мл | ||
| Последующие дозы (600 мг) Однократная инфузия каждые 6 месяцев |
Вариант 1 Длительность приблизительно 3.5 часа |
600 мг в 500 мл | - Начать инфузию со скоростью 40 мл/ч в течение 30 минут. - Затем скорость можно увеличивать с шагом 40 мл/ч каждые 30 минут до максимальной скорости 200 мл/ч. - Каждую инфузию следует проводить в течение приблизительно 3.5 часов. |
| или | |||
| Вариант 2 Длительность приблизительно 2 часа |
600 мг в 500 мл | - Начать инфузию со скоростью 100 мл/ч в течение первых 15 минут. - Увеличить скорость до 200 мл/ч в течение следующих 15 минут. - Увеличить скорость до 250 мл/ч в течение следующих 30 минут. - Увеличить скорость до 300 мл/ч в течение оставшихся 60 минут. - Каждую инфузию следует проводить в течение приблизительно 2 часов. |
|
За пациентами необходимо наблюдать во время инфузии и, как минимум, в течение одного часа после завершения инфузии на предмет возникновения симптомов инфузионных реакций.
Правила приготовления и хранения раствора для инфузий
Подготовка препарата к введению должна проводиться медицинским специалистом в асептических условиях.
Не встряхивать.
Следует использовать стерильную иглу и шприц для приготовления раствора для инфузий окрелизумаба.
Препарат предназначен только для однократного использования.
Концентрат нельзя использовать при изменении окраски или при наличии дискретных посторонних включений.
Лекарственный препарат следует развести перед применением. Чтобы приготовить раствор для в/в введения, концентрат препарата Окревус® следует развести в инфузионном пакете, содержащем 0.9% раствор натрия хлорида в соотношениях 300 мг/250 мл или 600 мг/500 мл. Концентрация готового раствора должна составлять примерно 1.2 мг/мл.
Введение раствора должно проводиться с использованием инфузионной системы со встроенным фильтром с диаметром пор 0.2 или 0.22 микрон.
Непосредственно перед инфузией содержимое инфузионного пакета должно иметь комнатную температуру.
Была показана химическая и физическая стабильность в ходе использования в течение 24 часов при температуре 2-8 °C и далее 8 часов при комнатной температуре.
С точки зрения микробиологической чистоты раствор для инфузии следует использовать сразу после приготовления. Если готовый раствор не был использован сразу после приготовления, то он может храниться не более 24 часов при температуре 2-8 °С и далее 8 часов при комнатной температуре при условии, что разведение проводилось в валидированных асептических условиях.
Если инфузию не удается завершить в указанный период, оставшийся в инфузионном пакете раствор следует уничтожить.
Утилизация
Весь оставшийся лекарственный препарат и отходы следует уничтожить в соответствии с установленными национальным законодательством требованиями.
Совместимость
Не было обнаружено признаков несовместимости с инфузионными пакетами из поливинилхлорида или полиолефина и системами для в/в введения.
Для разведения препарата Окревус® следует использовать только 0.9% раствор натрия хлорида. Разводить препарат в других растворителях нельзя.
Побочное действие
Резюме профиля безопасности
Наиболее важными и частыми нежелательными реакциями (НР) были инфузионные реакции (34.3% при рецидивирующих формах РС и 40.1% при ППРС) и инфекции (58.5% при рецидивирующих формах РС и 72.2% при ППРС) (см. раздел «Особые указания»).
Табличное резюме нежелательных реакций
В Таблице 6 представлены данные о НР, которые наблюдались в клинических исследованиях окрелизумаба, а также были получены из спонтанных сообщений. НР сгруппированы в соответствии с системно-органной классификацией медицинского словаря для нормативно-правовой деятельности MedDRA и категорией частоты. Для описания частоты НР используется следующая классификация: очень часто (≥1/10), часто (≥1/100, но <1/10), нечасто (≥1/1000, но <1/100), редко (≥1/10000, но <1/1000), очень редко (<1/10000) и частота неизвестна (на основании имеющихся данных оценить невозможно). Внутри каждого системно-органного класса НР представлены в порядке уменьшения частоты возникновения.
Таблица 6. Нежелательные реакции
| Системно-органный класс по MedDRA | Очень часто | Часто | Частота неизвестна2 |
| Инфекции и инвазии | Инфекции верхних дыхательных путей, назофарингит, грипп | Синусит, бронхит, герпес полости рта, гастроэнтерит, инфекции дыхательных путей, вирусные инфекции, опоясывающий лишай (Herpes zoster), конъюнктивит, воспаление подкожно-жировой клетчатки | |
| Нарушения со стороны крови и лимфатической системы | Нейтропения | Отсроченная нейтропения2 | |
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Кашель, катаральные явления | ||
| Лабораторные и инструментальные данные | Снижение уровня иммуноглобулина М | Снижение уровня иммуноглобулина G | |
| Травмы, интоксикации и осложнения процедур | Инфузионные реакции1 |
1 См. подраздел «Описание отдельных нежелательных реакций»
2 Зарегистрировано в пострегистрационном периоде, на основании имеющихся данных частоту оценить невозможно
Описание отдельных нежелательных реакций
Инфузионные реакции
В исследованиях при рецидивирующих формах РС и ППРС наблюдались следующие симптомы, связанные с инфузионными реакциями, включая, но не ограничиваясь: зуд, сыпь, крапивница, эритема, приливы, понижение артериального давления, пирексия, повышенная утомляемость, головная боль, головокружение, раздражение горла, боль в ротоглотке, одышка, отек глотки или гортани, тошнота, тахикардия. В контролируемых клинических исследованиях случаев летальных инфузионных реакций не было. Кроме того, симптомы инфузионных реакций в пострегистрационном периоде включали анафилаксию.
В клинических исследованиях, контролируемых активным препаратом, при рецидивирующих формах РС, инфузионные реакции были самыми частыми нежелательными реакциями на фоне терапии окрелизумабом. Общие частоты инфузионных реакций составили 34.3% и 9.9% на фоне лечения окрелизумабом и интерфероном бета-1а, соответственно. Частота инфузионных реакций была максимальной во время 1-ой инфузии 1-ой дозы окрелизумаба (27.5%) и снижалась со временем до <10% во время введения 4-ой дозы. Большинство инфузионных реакций в обеих группах лечения были легкой или средней степени тяжести. У 21.7% и 10.1% пациентов, получавших окрелизумаб, наблюдались инфузионные реакции легкой и средней степени тяжести, соответственно; у 2.4% – инфузионные реакции тяжелой степени тяжести и у 0.1% – жизнеугрожающие.
В плацебо-контролируемом клиническом исследовании при ППРС инфузионные реакции были самыми частыми нежелательными реакциями на фоне терапии окрелизумабом с общей частотой 40.1% по сравнению с частотой 25.5% в группе плацебо. Частота инфузионных реакций была максимальной во время 1-ой инфузии 1-ой дозы окрелизумаба (27.4%) и снижалась при введении последующих доз до <10% во время введения 4-ой дозы. У большинства пациентов в обеих группах инфузионные реакции чаще развивались во время первой инфузии каждой дозы по сравнению со второй инфузией этой дозы. Большинство инфузионных реакций были легкой или средней степени тяжести. У 26.7% и 11.9% пациентов, получавших окрелизумаб, наблюдались инфузионные реакции легкой и средней степени тяжести, соответственно; у 1.4% – инфузионные реакции тяжелой степени тяжести. Жизнеугрожающих инфузионных реакций отмечено не было. См. раздел «Особые указания».
Альтернативные короткие инфузии последующих доз
В ходе исследования (MA30143 под-исследование коротких инфузий), которое было разработано для оценки профиля безопасности при проведении коротких (2 часа) инфузий окрелизумаба у пациентов с рецидивирующими формами РС частота, тяжесть и характер симптомов инфузионных реакций были сопоставимы с таковыми при проведении инфузий в течение 3.5 часов (см. раздел «Фармакологические свойства»). Общее количество необходимых вмешательств было низким в обеих группах, однако в группе коротких инфузий (2 часа) потребовалось больше вмешательств (снижение скорости или приостановка инфузии) для контроля инфузионных реакций по сравнению с группой с инфузией длительностью 3.5 часа (8.7% и 4.8%, соответственно).
Инфекции
В клинических исследованиях, контролируемых активным препаратом, инфекции наблюдались у 58.5% пациентов, получавших окрелизумаб, по сравнению с 52.5% пациентов, получавших интерферон бета-1а. Частота серьезных инфекций составила 1.3% и 2.9% у пациентов, получавших окрелизумаб и интерферон бета-1а, соответственно. В плацебо-контролируемом исследовании у пациентов с ППРС инфекции были зарегистрированы у 72.2% пациентов, получавших окрелизумаб, и у 69.9% пациентов, получавших плацебо. Частота серьезных инфекций составила 6.2% и 6.7% у пациентов, получавших окрелизумаб и плацебо, соответственно. Всех пациентов перевели на терапию окрелизумабом в открытом периоде исследований при рецидивирующих формах РС и ППРС. Увеличение числа серьезных инфекций наблюдалось у пациентов с рецидивирующими формами РС между 2 и 3 годами наблюдения, но не в последующие годы. У пациентов с ППРС увеличения не наблюдалось.
Инфекции дыхательных путей
Доля инфекций дыхательных путей была выше у пациентов, получавших окрелизумаб, по сравнению с интерфероном бета-1а и плацебо.
В клинических исследованиях при рецидивирующих формах РС инфекции верхних дыхательных путей наблюдались у 39.9% пациентов, получавших окрелизумаб, и у 33.2% пациентов, получавших интерферон бета-1a; инфекции нижних дыхательных путей – у 7.5% пациентов, получавших окрелизумаб, и 5.2% пациентов, получавших интерферон бета-1а.
В клиническом исследовании при ППРС инфекции верхних дыхательных путей наблюдались у 48.8% пациентов, получавших окрелизумаб, и у 42.7% пациентов, получавших плацебо; инфекции нижних дыхательных путей – у 9.9% пациентов, получавших окрелизумаб, и у 9.2% пациентов, получавших плацебо.
Инфекции дыхательных путей, которые отмечались у пациентов, получавших окрелизумаб, были в основном легкой и средней степени тяжести (80-90%).
Герпес
В клинических исследованиях, контролируемых активным препаратом, у пациентов с рецидивирующими формами РС частота герпетической инфекции была выше на фоне терапии окрелизумабом по сравнению с терапией интерфероном бета-1а. В группах окрелизумаба и интерферона бета-1а частоты следующих нежелательных реакций составляли: опоясывающий лишай (Herpes Zoster) 2.1% и 1.0%, простой герпес 0.7% и 0.1%, герпес полости рта 3.0% и 2.2%, генитальный герпес 0.1% и 0% и герпес-вирусная инфекция 0.1% и 0%, соответственно.
Все инфекции были преимущественно легкой и средней степеней тяжести (за исключением одного явления 3 степени тяжести), и пациенты выздоравливали после стандартного лечения.
В плацебо-контролируемом клиническом исследовании у пациентов с ППРС герпес полости рта возникал с частотой 2.7% и 0.8% на фоне лечения окрелизумабом и в группе плацебо, соответственно.
Изменения лабораторных показателей
Иммуноглобулины
Во время лечения окрелизумабом отмечалось снижение общей концентрации иммуноглобулинов, в основном за счет снижения уровня иммуноглобулина М (IgM). Данные клинических исследований показали очевидную связь между снижением уровня иммуноглобулинов IgG (и в меньшей степени иммуноглобулинов IgA или IgM) и развитием серьезных инфекций.
Лимфоциты
При рецидивирующих формах РС уменьшение числа лимфоцитов ниже НГН наблюдалось у 20.7% пациентов, получавших окрелизумаб, по сравнению с 32.6% пациентов, получавших интерферон бета-1а. При ППРС уменьшение числа лимфоцитов ниже НГН наблюдалось у 26.3% пациентов, получавших окрелизумаб, по сравнению с 11.7% пациентов, получавших плацебо.
Большинство изменений, зарегистрированных у пациентов, получавших окрелизумаб, были 1-й (<НГН – 800 клеток/мм³) и 2-й (500-800 клеток/мм³) степеней тяжести.
Приблизительно у 1% пациентов в группе окрелизумаба была лимфопения 3-й степени тяжести (200-500 клеток/мм³). Ни у одного из пациентов не была зарегистрирована лимфопения 4-й степени тяжести (<200 клеток/мм³).
Повышенная частота серьезных инфекций наблюдалась во время подтвержденного снижения числа лимфоцитов у пациентов, получавших окрелизумаб. Количество серьезных инфекций было недостаточным для установления причинно-следственной связи.
Нейтрофилы
В клинических исследованиях, контролируемых активным препаратом, у пациентов с рецидивирующими формами РС, получавших окрелизумаб, уменьшение числа нейтрофилов <НГН наблюдалось реже (14.7%), по сравнению с пациентами, получавшими интерферон бета-1а (40.9%). В плацебо-контролируемом клиническом исследовании у пациентов с ППРС, получавших лечение окрелизумабом, уменьшение числа нейтрофилов наблюдалось несколько чаще (12.9%), по сравнению с пациентами, получавшими плацебо (10.0%); у большего количества пациентов (4.3%), получавших окрелизумаб, нейтропения была ≥2 степени тяжести по сравнению с 1.3% пациентов, получавших плацебо. Примерно у 1% пациентов, получавших окрелизумаб, была нейтропения 4-й степени тяжести по сравнению с 0% в группе, получавшей плацебо.
В большинстве случаев уменьшение числа нейтрофилов на фоне терапии окрелизумабом было транзиторным, отмечалось однократно в ходе терапии и имело 1-ую (<НГН – 1500 клеток/мм³) или 2-ую степень тяжести (1000-1500 клеток/мм³). Нейтропения 3-ей или 4-ой степени тяжести наблюдалась приблизительно у 1% пациентов. Одному пациенту с нейтропенией 3-й степени тяжести (500-1000 клеток/мм³) и одному пациенту с нейтропенией 4-й степени тяжести (<500 клеток/мм³) потребовалась специфическая терапия гранулоцитарным колониестимулирующим фактором; после данного эпизода пациенты продолжили получать окрелизумаб. Нейтропения может развиваться спустя несколько месяцев после завершения терапии (см. раздел «Особые указания»).
Прочее
Сообщалось об одном летальном исходе вследствие развития синдрома системного воспалительного ответа (SIRS) неизвестной этиологии у пациента, получившего окрелизумаб в дозе 2000 мг. SIRS развился через 12 недель после последней инфузии окрелизумаба, после проведения МРТ с использованием гадолиний-содержащего контрастного вещества, анафилактоидная реакция на которое могла способствовать развитию SIRS.
Передозировка
Опыт превышения рекомендованной дозы окрелизумаба в клинических исследованиях ограничен. Максимальная изученная доза на данный момент составляет 2000 мг в виде двух в/в инфузий по 1000 мг с интервалом в 2 недели (исследование II фазы по подбору доз при рецидивирующих формах РС), при этом наблюдавшиеся нежелательные реакции соответствовали установленному профилю безопасности окрелизумаба в опорных клинических исследованиях.
Специфического антидота в случае передозировки не существует; необходимо немедленно прекратить инфузию и наблюдать за пациентом на предмет развития инфузионных реакций (см. раздел «Особые указания»).
Взаимодействие с другими лекарственными средствами
Исследований взаимодействия с другими лекарственными средствами не проводилось, поскольку взаимодействий, связанных с активностью изоферментов цитохрома Р450 и других метаболизирующих ферментов или транспортеров, не ожидается.
Вакцинация
Безопасность иммунизации живыми или живыми ослабленными вирусными вакцинами после терапии окрелизумабом не изучали.
Имеются данные об эффектах столбнячного анатоксина, 23-валентного пневмококкового полисахарида, KLH-неоантигену (keyhole limpet hemocyanin, KLH) и сезонных вакцин против гриппа у пациентов, получающих окрелизумаб (см. разделы «Особые указания» и «Фармакологические свойства»).
После терапии окрелизумабом в течение 2 лет доля пациентов с положительными титрами антител к S. pneumoniae, возбудителям эпидемического паротита, краснухи и ветряной оспы была в целом сходна с таковой на исходном уровне.
Иммунодепрессанты
Не рекомендуется одновременное применение других иммунодепрессантов, за исключением глюкокортикостероидов для симптоматического лечения рецидивов РС (см. раздел «Особые указания»).
Особые указания
Прослеживаемость
Для улучшения прослеживаемости биологических лекарственных препаратов следует фиксировать наименование препарата и номер серии.
Инфузионные реакции
Развитие инфузионных реакций у пациентов, получающих окрелизумаб, может быть связано с высвобождением цитокинов и/или других химических медиаторов.
Симптомы инфузионных реакций могут развиться во время любой инфузии, но наиболее часто они отмечались во время первого введения окрелизумаба.
Инфузионные реакции также могут развиться в течение 24 часов после инфузии (см. раздел «Побочное действие»).
Симптомами инфузионных реакций могут быть зуд, сыпь, крапивница, эритема, раздражение горла, боль в ротоглотке, одышка, отек глотки или гортани, приливы, понижение артериального давления, пирексия, повышенная утомляемость, головная боль, головокружение, тошнота, тахикардия и анафилаксия.
Перед инфузией
Контроль тяжелых реакций
Введение препарата проводится при наличии доступа к средствам для оказания экстренной помощи в случае возникновения тяжелых реакций, таких как серьезные инфузионные реакции, реакции гиперчувствительности и/или анафилактические реакции.
Понижение артериального давления
Во время инфузий окрелизумаба возможно понижение артериального давления как симптома инфузионных реакций. В связи с этим следует рассмотреть возможность приостановки лечения антигипертензивными препаратами в течение 12 часов до начала и на протяжении каждой инфузии. У пациентов с застойной сердечной недостаточностью (класс III и IV по классификации Нью-Йоркской Ассоциации по изучению заболеваний сердца) в анамнезе применение окрелизумаба не изучалось.
Премедикация
Рекомендации по премедикации для снижения частоты и тяжести инфузионных реакций приведены в разделе «Способ применения и дозы». Во время инфузии
При развитии тяжелых симптомов со стороны дыхательной системы (таких как бронхоспазм или эпизод обострения бронхиальной астмы):
- инфузия должна быть немедленно прекращена; продолжать терапию в дальнейшем нельзя;
- необходимо провести симптоматическое лечение;
- пациент должен находиться под наблюдением до полного разрешения симптомов со стороны дыхательной системы, поскольку за первоначальным улучшением клинических симптомов может последовать их ухудшение.
Реакции гиперчувствительности может быть сложно отличить от инфузионных реакций с точки зрения симптомов. При подозрении на развитие реакции гиперчувствительности во время инфузии необходимо немедленно прекратить инфузию и не возобновлять в дальнейшем (см. подраздел «Реакции гиперчувствительности» ниже).
После инфузии
За пациентами необходимо тщательно наблюдать на предмет возникновения симптомов инфузионных реакций, как минимум, в течение одного часа после завершения инфузии. Врач должен предупредить пациента о том, что развитие инфузионных реакций возможно в течение 24 часов после инфузии.
Рекомендации по коррекции инфузии препарата пациентам, у которых развились инфузионные реакции, приведены в разделе «Способ применения и дозы».
Реакции гиперчувствительности
Также возможно развитие реакции гиперчувствительности (острая аллергическая реакция на препарат). Реакции острой гиперчувствительности 1-го типа (опосредованных IgE) могут быть клинически неотличимы от симптомов инфузионных реакций.
Реакции гиперчувствительности могут возникнуть во время любой инфузии, однако, как правило, они отсутствуют во время первой инфузии. Если в ходе последующих инфузий усугубляются ранее наблюдавшиеся симптомы или возникают новые тяжелые симптомы, необходимо немедленно рассмотреть вероятность развития реакции гиперчувствительности. Пациентам с установленной IgE-опосредованной гиперчувствительностью к окрелизумабу противопоказана терапия данным препаратом (см. раздел «Противопоказания»).
Инфекции
У пациентов с активной инфекцией применение окрелизумаба следует отложить до купирования инфекции.
Перед применением препарата рекомендуется проверить иммунный статус пациента, так как препарат не следует применять у пациентов с тяжелым иммунодефицитом (например, при лимфопении, нейтропении, гипогаммаглобулинемии) (см. разделы «Противопоказания» и «Побочное действие»).
Общая доля пациентов, перенесших серьезную инфекцию, была сопоставима с таковой в группе сравнения (см. раздел «Побочное действие»). Частота инфекций 4-й (жизнеугрожающей) степени тяжести и 5-й (летальной) степени тяжести была низкой во всех группах лечения, но у пациентов с ППРС она была выше при применении окрелизумаба по сравнению с плацебо: жизнеугрожающие инфекции (1.6% в сравнении с 0.4%) и летальные инфекции (0.6% в сравнении с 0%). Все жизнеугрожающие инфекции разрешились без прекращения применения окрелизумаба.
Пациенты с ППРС, имеющие трудности с глотанием, подвержены повышенному риску развития аспирационной пневмонии. Лечение окрелизумабом может увеличить риск развития тяжелой пневмонии у таких пациентов. Врачи должны предпринимать незамедлительные меры для пациентов с пневмонией.
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ)
JC-ассоциированная ПМЛ очень редко наблюдалась у пациентов, получавших терапию антителами к CD20, включая окрелизумаб. Развитие JC-ассоциированной ПМЛ в большинстве случаев было связано с различными факторами риска (популяция пациентов, например, наличие лимфопении, пожилой возраст, терапия несколькими иммунодепрессантами).
Необходимо наблюдать за пациентами на предмет развития ранних признаков и симптомов ПМЛ, которые могут быть сходны с проявлениями РС и могут включать в себя появление любых новых или ухудшение уже имеющихся неврологических признаков и симптомов.
При подозрении на ПМЛ следует приостановить терапию окрелизумабом. Необходимо рассмотреть вопрос о проведении диагностики ПМЛ, в том числе МРТ, предпочтительно с использованием контрастного вещества (сравнить с результатом МРТ, выполненной до лечения), определение ДНК вируса JC в спинномозговой жидкости и повторные осмотры невролога.
При подтверждении диагноза ПМЛ следует полностью прекратить лечение.
Реактивация гепатита B
У пациентов, получавших лечение антителами к CD20, сообщалось о реактивации вируса гепатита В, в некоторых случаях приводившей к развитию фульминантного гепатита, печеночной недостаточности, летальному исходу.
Перед назначением окрелизумаба всем пациентам следует пройти скрининг на вирус гепатита B в соответствии с локальными руководствами. Окрелизумаб не следует применять пациентам с активным вирусом гепатита B (активная инфекция должна быть подтверждена положительными результатами определения поверхностного антигена (HBsAg) и антител к антигенам вируса гепатита B (HBcAb)) (см. раздел «Противопоказания»).
Пациентам с положительными серологическими маркерами гепатита B (отрицательный результат анализа на HBsAg и положительный результат на HBcAb), а также носителям вируса гепатита B (положительный результат на HBsAg), следует проконсультироваться с гепатологом перед назначением окрелизумаба.
В отношении таких пациентов необходимо проводить соответствующий мониторинг и принимать меры по профилактике реактивации вируса гепатита B в соответствии с локальными стандартами.
Отсроченная нейтропения
Сообщалось о случаях отсроченной нейтропении, как минимум, через 4 недели после последней инфузии окрелизумаба (см. раздел «Побочное действие»). Хотя в некоторых случаях развивалась нейтропения 3-ей или 4-й степени тяжести, в большинстве случаев наблюдалась 1-ая или 2-ая степень тяжести. У пациентов с признаками и симптомами инфекции рекомендуется провести анализ числа нейтрофилов в крови (см. раздел «Побочное действие»).
Малигнизация
В клинических исследованиях наблюдалось увеличение числа злокачественных новообразований (включая рак молочной железы) у пациентов, получавших окрелизумаб, по сравнению с контрольными группами. Заболеваемость была в пределах фонового уровня, ожидаемого для популяции пациентов с РС. Пациентам с установленным активным злокачественным образованием не следует проводить лечение окрелизумабом (см. раздел «Противопоказания»). У пациентов с известными факторами риска злокачественных новообразований и у пациентов, которые находятся под активным контролем на предмет рецидивов злокачественных новообразований, следует проводить индивидуальную оценку соотношения пользы и риска. Пациенты должны следовать стандартным рекомендациям по скринингу рака молочной железы.
В контролируемом периоде клинических исследований частота немеланомного рака кожи была низкой, и между группами лечения не было дисбаланса по этому показателю. Увеличение заболеваемости наблюдалось между 3 и 4 годами лечения за счет базальноклеточного рака, без дисбаланса между группами в последующие годы. Частота новых случаев была в пределах фонового уровня, ожидаемого в популяции пациентов с РС.
Лечение пациентов с тяжелым иммунодефицитом
Пациенты с тяжелым иммунодефицитом не должны получать терапию до тех пор, пока их состояние не разрешится (см. раздел «Противопоказания»).
При других аутоиммунных состояниях применение окрелизумаба одновременно с иммунодепрессантами (например, глюкокортикостероидами в течение длительного периода, болезнь-модифицирующими антиревматическими препаратами небиологического и биологического происхождения, микофенолата мофетилом, циклофосфамидом, азатиоприном) приводило к увеличению числа серьезных инфекций, включая оппортунистические. Инфекции включали, помимо прочих, атипичную и пневмоцистную пневмонию, ветряночную пневмонию, туберкулез и гистоплазмоз. В редких случаях некоторые из этих инфекций приводили к летальному исходу. Поисковый анализ выявил следующие факторы, связанные с риском серьезных инфекций: более высокие дозы окрелизумаба, чем рекомендовано для РС, другие сопутствующие заболевания и длительное применение иммунодепрессантов/глюкокортикостероидов.
Не рекомендуется применять другие иммунодепрессанты одновременно с окрелизумабом, за исключением глюкокортикостероидов для симптоматического лечения рецидивов РС. Данные о связи одновременного применения стероидов для симптоматического лечения рецидивов с повышенным риском инфекций в клинической практике ограничены. В опорных исследованиях окрелизумаба при РС назначение глюкокортикостероидов для лечения рецидивов не было связано с повышением риска серьезной инфекции.
Назначать терапию окрелизумабом после иммунодепрессивной терапии или иммунодепрессивную терапию после терапии окрелизумабом следует с учетом того, что возможно перекрывание их фармакодинамических эффектов (см. раздел «Фармакологические свойства»).
При назначении окрелизумаба следует соблюдать осторожность, принимая во внимание фармакодинамику других БМП для лечения РС.
Вакцинация
Безопасность иммунизации живыми или живыми ослабленными вакцинами после терапии окрелизумабом не изучалась.
Во время терапии окрелизумабом, а также до восстановления пула В-клеток проводить вакцинацию живыми или живыми ослабленными вакцинами не рекомендуется. В клинических исследованиях медиана времени восстановления В-клеток в клинических исследованиях составила 72 недели (см. раздел «Фармакологические свойства»).
В ходе рандомизированного открытого исследования у пациентов с рецидивирующими формами РС, получающих окрелизумаб, отмечался пониженный гуморальный иммунный ответ к столбнячному анатоксину, 23-валентному пневмококковому полисахариду с бустерной вакциной или без таковой, KLH-неоантигену и сезонной вакцине против гриппа (см. разделы ««Фармакологические свойства» и «Взаимодействие с другими лекарственными средствами»). Тем не менее, пациентам, получающим окрелизумаб, рекомендуется проводить сезонную вакцинацию против гриппа инактивированной вакциной.
Перед назначением окрелизумаба врач должен изучить статус иммунизации пациента. В случае проведения вакцинации ее необходимо завершить, по меньшей мере, за 6 недель до начала лечения окрелизумабом.
Внутриутробная экспозиция окрелизумаба и вакцинация новорожденных и детей живыми и живыми ослабленными вакцинами
Из-за потенциального истощения пула В-клеток у новорожденных и детей, матери которых получали окрелизумаб во время беременности, рекомендуется рассмотреть возможность отсрочки вакцинации живыми или живыми ослабленными вакцинами до восстановления пула В-клеток; перед проведением вакцинации новорожденных и детей рекомендуется измерять уровень CD19+ В-клеток.
Все вакцинации, за исключением вакцинации живыми и живыми ослабленными вакцинами, рекомендуется проводить согласно национальному графику иммунизации. Измерение титра антител после вакцинации позволяет проверить способность пациента развить защитный иммунный ответ, так как эффективность вакцинации может быть снижена.
Безопасность и сроки проведения вакцинации следует обсудить с педиатром (см. раздел «Применение во время беременности и в период грудного вскармливания»).
Натрий
Данный препарат содержит менее 1 ммоль (или 23 мг) натрия на дозу препарата, то есть по сути не содержит натрия.
Влияние на способность управлять транспортными средствами и механизмами
Препарат Окревус® не оказывает или оказывает несущественное влияние на способность управлять автомобилем и работать с механизмами.
Форма выпуска
Концентрат для приготовления раствора для инфузий 30 мг/мл
По 10 мл (300 мг/10 мл) препарата во флакон бесцветного стекла (гидролитический класс 1 ЕФ), укупоренный пробкой из бутилкаучука, ламинированного фторполимером, обжатый алюминиевым колпачком и закрытый пластмассовой крышкой.
1 флакон с препаратом вместе с инструкцией по применению помещают в картонную пачку. С целью контроля первого вскрытия на пачку наносится защитная голографическая наклейка.
В случае упаковки на АО «ОРТАТ»: с целью контроля первого вскрытия на пачку наклеивают самоклеящиеся стикеры с логотипом АО «ОРТАТ».
Срок годности
2 года.
Не применять по истечении срока годности.
Условия хранения
Хранить при температуре 2-8 °С в картонной пачке для защиты от света.
Хранить в недоступном для детей месте.
Условия отпуска
По рецепту.
Владелец Регистрационного удостоверения
Ф. Хоффманн-Ля Рош Лтд., Швейцария
F. Hoffmann-La Roche Ltd, Grenzacherstrasse 124, 4070 Basel, Switzerland
Производитель
Рош Диагностикс ГмбХ, Германия
Roche Diagnostics GmbH, Sandhofer Strasse 116, 68305 Mannheim, Germany
Ф. Хоффманн-Ля Рош Лтд., Швейцария
F. Hoffmann-La Roche Ltd, Wurmisweg, 4303 Kaiseraugst, Switzerland
Фасовщик (первичная упаковка)
Рош Диагностикс ГмбХ, Германия
Roche Diagnostics GmbH, Sandhofer Strasse 116, 68305 Mannheim, Germany
Ф. Хоффманн-Ля Рош Лтд., Швейцария
F. Hoffmann-La Roche Ltd, Wurmisweg, 4303 Kaiseraugst, Switzerland
Упаковщик (вторичная/потребительская упаковка)
Ф. Хоффманн-Ля Рош Лтд., Швейцария
F. Hoffmann-La Roche Ltd, Wurmisweg, 4303 Kaiseraugst, Switzerland
АО «ОРТАТ», Россия
157092, Россия, Костромская обл., Сусанинский район, с. Северное, мкр. Харитоново
Выпускающий контроль качества
Ф. Хоффманн-Ля Рош Лтд., Швейцария
F. Hoffmann-La Roche Ltd, Wurmisweg, 4303 Kaiseraugst, Switzerland
АО «ОРТАТ», Россия
157092, Россия, Костромская обл., Сусанинский район, с. Северное, мкр. Харитоново
Организация, уполномоченная на принятие претензий от потребителя
Претензии потребителей направлять в компанию АО «Рош-Москва» по адресу:
107031, Россия, г. Москва, Трубная площадь, д. 2, помещение 1, этаж 1, комната 42 или через форму обратной связи на сайте: www.roche.ru
В случае упаковки на АО «ОРТАТ» претензии потребителей направлять по адресу:
157092, Россия, Костромская обл., Сусанинский район, с. Северное, мкр. Харитоново
Комментарии
ПРАКТИКА ПЕДИАТРА
