НИОХ-14 - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
| Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях стационарной медицинской помощи. |
Регистрационный номер:
ЛП-008597
Торговое наименования:
НИОХ-14
Международное непатентованное наименование или группировочное наименование:
7-[N-(4-трифторметилбензоил)-гидразинокарбонил]-трицикло-[3.2.2.02,4]нон-8-ен-6-карбоновая кислота
Лекарственная форма:
Капсулы 200 мг
Состав
1 капсула содержит:
Действующее вещество:
7-[N-(4-трифторметилбензоил)-гидразинокарбонил]-трицикло-[3.2.2.02,4]нон-8-ен-6-карбоновая кислота (НИОХ-14) – 200 мг
Вспомогательные вещества:
Микрокристаллическая целлюлоза – 96 мг;
Лактозы моногидрат – 48 мг;
Магния стеарат – 2 мг;
Кремния диоксид коллоидный (аэросил) – 2 мг;
Крахмал картофельный – 9 мг;
Натрия хлорид – 35 мг;
Вода очищенная – 8 мг;
Капсулы твердые желатиновые – 100 мг.
Масса содержимого капсул: 400 мг.
Состав желатиновой капсулы:
Корпус:
Титана диоксид Е 171 – 2%.
Желатин медицинский – до 100%.
Крышка:
Азорубин Е 122 – 0,19%.
Желтый хинолиновый Е 104 – 0,37%.
Титана диоксид Е 171 – 1%.
Желатин медицинский – до 100%.
Описание:
Твердые желатиновые капсулы № 0 с корпусом белого цвета и крышечкой красного цвета. Содержимое капсул – порошок белого цвета.
Фармакотерапевтическая группа:
противовирусное средство системного действия
Код АТХ:
J05AX
Фармакологические свойства
Фармакодинамика
Механизм действия
Лекарственный препарат НИОХ-14 является пролекарством, активным метаболитом которого является ST-246 (Тековиримат), обладающий активностью в отношении ортопоксвирусов, в том числе вируса натуральной оспы, in vitro и in vivo. Тековиримат является ингибитором высококонсервативного оболочечного белка р37 ортопоксвирусов, присутствующего у всех представителей ортопоксвирусов. Таким образом, мишенью ST-246, является белок р37 – высоко консервативный продукт гомологичных генов ортопоксвирусов. Препарат НИОХ-14 в виде своего активного метаболита ST-246 блокирует взаимодействие р37 с клеточными ГТФазой Rab9 и TIP47 и тем самым предотвращает образование и выход из клетки заключенных в оболочку вирионов, благодаря которым вирус распространяется в культуре клеток и в организме.
Резистентность к препарату НИОХ-14
При изучении противовирусной активности препарата НИОХ-14 в отношении штаммов ортопоксвирусов (вирусов осповакцины, оспы коров, оспы мышей, оспы обезьян и натуральной оспы) из Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора не было выявлено штаммов, резистентных к этому препарату в культуре клеток и в экспериментах на животных.
Резистентность к препарату Тековиримат
При исследовании противовирусной активности препарата Тековиримат не было выявлено встречающихся в природе ортопоксвирусов, устойчивых к нему, хотя в условиях культивирования in vitro в присутствии препарата были получены штаммы вирусов осповакцины и оспы коров, обладающие резистентностью к Тековиримату. При длительном применении препарата возможно развитие устойчивости ортопоксвирусов к Тековиримату, связанное с заменами аминокислот в вирусном белке р37. Возможность резистентности вируса к препарату НИОХ-14, так же как и к Тековиримату, следует учитывать у пациентов, которые либо не реагируют на терапию, либо у которых развивается рецидив заболевания.
Специфическая активность препарата НИОХ-14
В экспериментах на культуре клеток препарат НИОХ-14 проявляет активность в отношении вирусов осповакцины, оспы коров, оспы мышей, оспы обезьян и натуральной оспы при величине 50%-й эффективной (вирус-ингибирующей) концентрации (ЕС50) в диапазоне 0,01-0,05 мкМ. При пероральном введении лабораторным животным препарат НИОХ-14 оказывает защитное действие против ортопоксвирусных инфекций. При этом противовирусное действие препаратов НИОХ-14 и ST-246 (Тековиримата) было одинаковым в отношении вируса натуральной оспы и других ортопоксвирусов в экспериментах in vitro и in vivo.
Специфическая активность препарата Тековиримат
В экспериментах на культуре клеток эффективные концентрации Тековиримата, приводящие к 50%-ному снижению индуцированного вирусом цитопатического эффекта (ЕС50) составляли 0,016-0,067 мкМ, 0,014-0,039 мкМ, 0,015 мкМ и 0,009 мкМ для вирусов натуральной оспы, оспы обезьян, оспы кроликов и осповакцины, соответственно. Также показано, что Тековиримат проявляет противовирусную эффективность при инфицировании мышей вирусом оспы мышей, кроликов – вирусом оспы кроликов, луговых собачек – вирусом оспы обезьян, обезьян – вирусами оспы обезьян и натуральной оспы.
Фармакокинетика
Всасывание и биодоступность
В клиническом исследовании при однократном пероральном применении препарата НИОХ-14 в дозе 200 мг максимальная концентрация активного метаболита ST-246 в плазме крови (Сmax) достигала 215 нг/мл через 6 ч (Тmax), время полувыведения (Т1/2) составило 17,8 ч; однократно в дозе 600 мг: Сmax = 375 нг/мл, Тmax = 6 ч, T1/2 = 19,8 ч; однократно в дозе 1200 мг: Сmax = 1212 нг/мл, Тmax = 6 ч, Т1/2 = 29 ч. При использовании НИОХ-14 в течение 6 суток по 200 мг в день были следующие фармакокинетические параметры активного метаболита ST-246 в плазме крови: Cmax = 189 нг/мл, Тmax = 6 ч, Т1/2 = 26 ч; в течение 6 суток по 600 мг в день: Сmax = 740 нг/мл, Тmax = 6 ч, T1/2 = 29 ч; в течение 6 суток по 1200 мг в день: Сmax = 607 нг/мл, Тmax = 96 ч, T1/2 = 18 ч.
После однократного перорального применения препарата Тековиримат в дозе 600 мг фармакокинетические параметры в плазме крови людей были следующими: Сmax = 1070 нг/мл, Тmax = 4 ч, Т1/2 = 24,4 ч. Кроме того, через 1 сут после его применения в дозе 250 мг Сmax в крови была 985 (±346) нг/мл, а после применения в течение 6 сут Сmax достигала 1212 (±350) нг/мл. При этом через 1 сут после применения Тековиримата в дозе 400 мг Сmax была 1392 (±411) нг/мл, а увеличение времени приема его в этой дозе до 6 сут не сопровождалось увеличением Сmax и составляло 1298 (±277) нг/мл.
Фармакокинетические показатели препарата НИОХ-14, полученные в экспериментах на мышах, свидетельствуют о его высокой биодоступности. После однократного перорального введения в дозе 50 мкг/г массы мыши тканевая доступность (fт) препарата НИОХ-14, рассчитанная на основе показателей его активного метаболита ST-246, для легких была 7,2%, для печени – 9,8%, для селезенки – 3,2%, а абсолютная биодоступность (Fabs) препарата НИОХ-14 составляла 61,1%.
Абсолютная биодоступность препарата Тековиримат при пероральном введении в дозах от 30 до 2000 мг/кг была равна 4-45% у мышей, 8-29% у кроликов и 28-50% у обезьян. Кроме того, в экспериментах на мышах показано, что Тековиримат распространялся в организме в пределах 4 ч, достигая наиболее высоких концентраций в крови, печени, легких и костном мозге.
Тековиримат достигает максимальных концентраций в плазме крови через 4 – 6 ч после перорального приема с пищей. Прием Тековиримата с пищей умеренного содержания жиров и калорий (~600 ккал и ~25 граммов жира), по сравнению с Тековириматом, принимаемым в натощак, увеличивал лекарственное воздействие (AUC) на 39%.
Распределение
В клинических исследованиях было установлено, что кажущийся объем распределения препарата НИОХ-14, т.е. гипотетический объем жидкости, в котором могло бы распределиться общее количество введенного вещества для создания его концентрации, такой как в крови, при однократном пероральном введении в дозах 200, 600 и 1200 мг был равен 950, 1400 и 1760 л соответственно.
При однократном пероральном применении препарата Тековиримат у здоровых добровольцев в дозах 200 и 600 мг его объем распределения составлял 986 и 1356 л соответственно.
Тековиримат на 77,3-82,2% связывается с белками плазмы крови человека. После однократного приема 600 мг дозы [14С]-тековиримата у здоровых субъектов концентрации общей радиоактивности во всех временных точках были ниже в цельной крови по сравнению с плазмой, причем во всех временных точках отношение цельной крови к плазме варьировалось от 0,62-0,90. Тековиримат имеет большой объем распределения (1356 л).
Биотрансформация (Метаболизм)
При проведении доклинических исследований препарата НИОХ-14 было установлено, что в растворителях, используемых для масс-спектрометрии, в организме, сыворотке крови и гомогенатах органов животных НИОХ-14 превращается в активный метаболит ST-246 (4-трифторметил-N-(3,За,4,4а,5,5а,6,6а-октагидро-1,3-диоксо-4,6-етеноциклопроп[f]изоиндол-2(1Н)-ил)-бензамид) и неактивный метаболит К (4-трифторметилбензойная кислота).
Основываясь на исследованиях на людях, Тековиримат метаболизируется с образованием метаболитов М4 (N-{3,5-диоксо-4-азатетрацикло[5.3.2.0{2,6}.0{8,10}]додек-11-ен-4-ил}амин), М5 (3,5-диоксо-4-аминотетрацикло[5.3.2.0{2,6}.0{8,10}]додек-11-ен) и TFMBA (4-трифторметил бензойная кислота). Ни один из метаболитов не является фармакологически активным. Тековиримат является субстратом UGT1A1 и UGT1A4. В моче первичный глюкуронидный конъюгат тековиримата и конъюгат глюкуронида М4 были наиболее распространенными компонентами, составляющими средние 24,4% и 30,3% дозы соответственно. Однако ни один из глюкуронидных конъюгатов не был обнаружен в качестве основного метаболита в плазме.
Выведение
Собственных исследований выделения препарата НИОХ-14 с мочой и калом не проводилось. После перорального применения препарата НИОХ-14 в дозе 200 время полувыведения его активного метаболита ST-246 из крови составило 17,8 часов.
После однократного приема Тековиримата примерно у 95% здоровых субъектов изотоп [14С] был обнаружен в моче и кале в течение 192-часового периода после введения дозы. При этом примерно у 73% изотоп [14С] был обнаружен в моче, а у 23% обнаруживался в кале, что указывает на то, что почечный путь является основным путем выведения. Почечная экскреция исходного соединения была минимальной и составляла менее 0,02%. Большая часть препарата, выводимого почками, находится в глюкуронизированной форме. С калом выделялся в основном неизмененный Тековиримат. Конечный период полувыведения Тековиримата составлял 19,3 часа.
Особые группы населения
Собственных исследований фармакокинетики препарата НИОХ-14 в зависимости от возраста, пола или расы не проводилось.
У здоровых людей не наблюдалось клинически значимых различий в фармакокинетике Тековиримата в зависимости от возраста, пола или расы.
Нарушение функции почек
Собственных исследований препарата НИОХ-14 у пациентов с нарушением функции почек не проводилось.
Согласно имеющимся данным о применении Тековиримата у пациентов с нарушением функции почек (на основе расчетной СКФ) не наблюдалось клинически значимых различий в его фармакокинетике.
Нарушение функции печени
Собственных исследований фармакокинетики препарата НИОХ-14 у пациентов с нарушением функции печени не проводилось.
Согласно имеющимся данным о препарате Тековиримат у пациентов с легкой, умеренной или тяжелой печеночной недостаточностью (на основании баллов Чайлд-Пью А, В или С) не наблюдалось клинически значимых различий в его фармакокинетике. Однако возможно, что у пациентов с тяжелой печеночной недостаточностью могут быть более высокие уровни несвязанного лекарственного средства и метаболитов.
Педиатрические пациенты
Фармакокинетика препарата НИОХ-14 у детей не оценивалась.
Фармакокинетика Тековиримата у детей не оценивалась. Ожидается, что рекомендуемый режим дозирования у детей для пациентов с массой тела не менее 13 кг приведет к воздействию Тековиримата, сопоставимому с таковым у взрослых пациентов в возрасте от 18 до 50 лет.
Показания к применению
Препарат показан к применению у взрослых пациентов от 18 лет для лечения инфекций, вызванных:
- вирусом натуральной оспы;
- вирусом оспы обезьян;
- вирусом коровьей оспы.
Противопоказания
- Гиперчувствительность к компонентам препарата (НИОХ-14 и другим);
- Непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция;
- Беременность и период грудного вскармливания (в связи с отсутствием данных об эффективности и безопасности);
- Дети до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Применение при беременности и в период грудного вскармливания
Препарат НИОХ-14 противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Препарат Тековиримат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались. При проведении исследований на животных было продемонстрировано, что Тековиримат передается потомству через молоко. Исследований на животных относительно репродуктивной токсичности Тековиримата недостаточно. Риск для новорожденных не может быть исключен. Потенциальный риск для человека неизвестен.
Влияние на фертильность
Не проводилось исследований влияния препарата НИОХ-14 на фертильность человека.
Введение препарата НИОХ-14 до спаривания не приводило к снижению показателей фертильности самцов и самок, не отражалось на длительности беременности, показателях пред- и постимплантационной смертности, количестве крысят в помете при рождении. Препарат не оказывал существенного влияния на выживаемость и прирост массы тела в ранний постнатальный период потомков самок, получавших препарат многократно. Длительное введение препарата до спаривания самцам приводило к снижению выживаемости их потомков.
Нет данных о влиянии Тековиримата на фертильность человека. У самцов мышей при приеме дозы 1000 мг/кг/день наблюдалось снижение фертильности из-за тестикулярной токсичности (увеличение процента аномальных сперматозоидов и снижение подвижности сперматозоидов).
Исследования репродуктивной токсичности Тековиримата были проведены на мышах и кроликах. Самая высокая доза, выбранная для исследования, у кролика составляла 100 мг/кг, а у мышей – 1000 мг /кг. У кроликов при введении препарата Тековиримат в дозе до 100 мг/кг/сут, а у мышей – в дозе до 1000 мг/кг/сут не наблюдалось токсичности для эмбрионов и плода. Токсическое воздействие на беременных самок было обнаружено у кроликов при введении Тековиримата дозе 100 мг/кг/сут, что проявлялось в виде снижения массы тела и смертности.
Имеющиеся токсикологические данные о безопасности у животных показали экскрецию Тековиремата в молоко. При пероральном введении Тековиримата в дозах до 1000 мг/кг/сут кормящим мышам на 10-11 день лактации среднее соотношение Тековиримата в молоке и плазме крови через 6 и 24 часа после приема препарата составляло примерно 0,8.
Способ применения и дозы
Препарат НИОХ-14 принимают внутрь, в течение 30 минут после еды (пища богатая жирами, молочные продукты).
Применение препарата НИОХ-14 возможно только в условиях стационарной медицинской помощи.
Рекомендуемая доза препарата составляет 600 мг (3 капсулы препарата по 200 мг) 2 раза в сутки (каждые 12 часов). Максимальная суточная доза – 1200 мг.
Длительность лечения 14 дней.
Корректировка дозы у пожилых пациентов, пациентов с нарушением функции печени или почек не требуется.
Побочное действие
Безопасность препарата НИОХ-14 не была изучена у больных оспой или другими ортопоксвирусными инфекциями.
В собственном клиническом исследовании препарата НИОХ-14 у 1 пациента наблюдались нежелательные явления со стороны пищеварительной системы – боли в животе (7%).
Частота развития нежелательных реакций приведена в соответствии с классификацией ВОЗ: «очень часто» ≥1/10, «часто» ≥1/100, но <1/10, «нечасто» ≥1/1000, но <1/100, «редко» ≥1/10000, но <1/1000 и «очень редко» <1/10000, включая отдельные сообщения.
Резюме профиля безопасности препарата Тековиримат
Побочные действия, о которых наиболее часто сообщают, были головная боль (12,3%) и тошнота (4,5%).
Резюме побочных реакций препарата Тековиримат
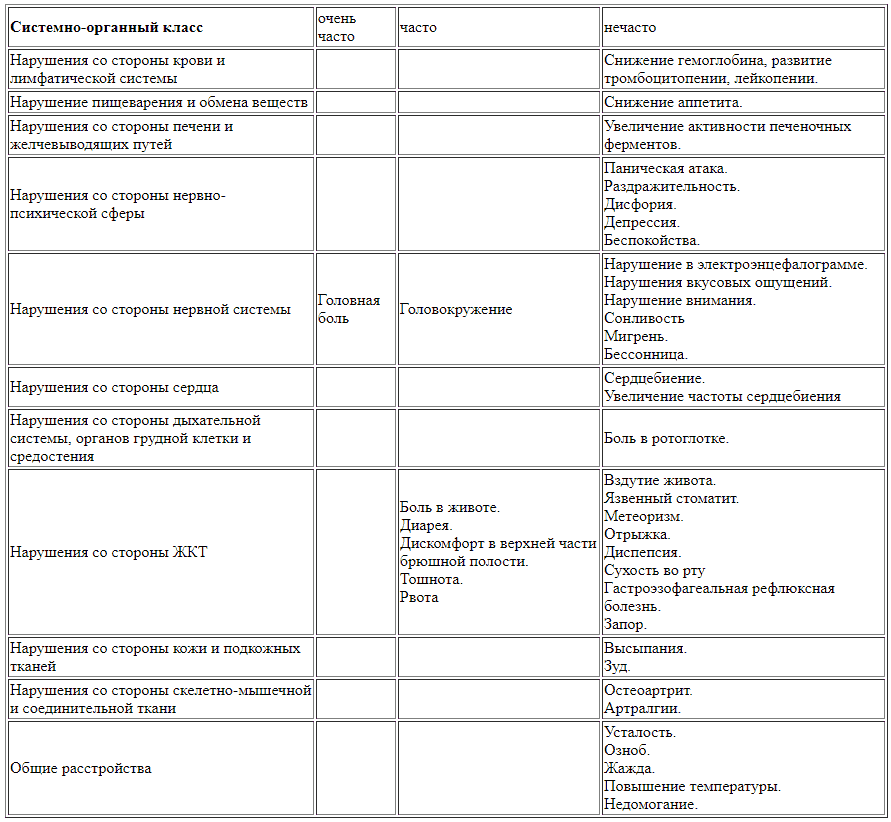
Передозировка.
Нет данных о побочных явлениях, связанных с передозировкой препарата НИОХ-14.
Нет данных о передозировке Тековиримата. При передозировке необходимо обратиться за медицинской помощью.
Взаимодействие с другими лекарственными средствами
Исследований взаимодействия препарата НИОХ-14 с другими лекарственными препаратами не проводилось.
Тековиримат и его метаболиты являются индукторами цитохрома Р450 (CYP) ЗА, CYP2B6 и CYP3A4, а также слабым ингибитором CYP2C8 и CYP2C19. Совместное назначение Тековиримата с другими препаратами может привести к изменению эффектов назначенных препаратов. Рекомендуется контроль во время совместного назначения Тековиримата с CYP2C8 и субстратами CYP2C19, имеющими узкие терапевтические окна.
Следует с осторожностью назначать одновременно с Тековириматом такие препараты как Вориконазол, Рилпивирин, Маравирок, Аторвастатин, Такролимус, Метадон, Силденафил, Тадалафил, Варденафил, Дарунавир, Рабепразол, Лансопразол. Данные лекарственные взаимодействия не были изучены. Совместно применение Тековиримата с Мидазоламом, Омепразолом, Бупропионом может повлиять на эффективность последних. Сочетание данных препаратов требует осторожности.
Совместное применение Репаглинида и Тековиримата может привести к гипогликемии. Рекомендован контроль глюкозы крови.
Взаимодействия с вакцинами
Исследования взаимодействия препарата НИОХ-14 с вакцинами на людях и животных не проводилось.
Исследования взаимодействия Тековиримата с вакцинами на людях не проводились. Некоторые исследования на животных показали, что при одновременном применении Тековиримата и живой вакцины против оспы может привести к снижению иммунного ответа на вакцину. Клиническое влияние этого взаимодействия на эффективность вакцины неизвестно.
Особые указания
Применение препарата НИОХ-14 возможно только в условиях стационарной медицинской помощи.
Препарат содержит краситель азорубин Е122, который может вызвать аллергические реакции.
Следует соблюдать осторожность при назначении препарата в пожилом возрасте. Препарат не изучался у данной группы пациентов.
У пациентов с нарушением функции почек и (или) печени НИОХ-14 должен использоваться с осторожностью, поскольку клинические данные отсутствуют.
Безопасность и эффективность препарата НИОХ-14 не была оценена в людях с ослабленным иммунитетом.
При развитии побочного действия препарата НИОХ-14 необходимо сообщать об этом в установленном порядке для осуществления мероприятий по фармаконадзору.
Препарат Тековиримат подлежит дополнительному мониторингу, который способствует быстрому выявлению новых сведений о безопасности. Это позволит в короткий срок выявить новую информацию о безопасности препарата. Работники здравоохранения просят сообщить о любых подозреваемых нежелательных реакциях.
Влияние на способность управлять транспортными средствами и механизмами
Исследования по изучению влияния препарата НИОХ-14 на способность к управлению автомобилями и другими механизмами не проводились.
Тековиримат оказывает незначительное влияние на способность управлять транспортными средствами и механизмами. Пациентам нужно сообщить о возможном возникновении головокружения и о необходимо соблюдать в период лечения осторожность при управлении транспортными средствами и занятиях потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, нужно предостеречь о вождении или операционных машинах.
Форма выпуска
Капсулы 200 мг.
По 45 капсул в банки полимерные из полипропилена с навинчиваемой крышкой из полипропилена и мембраны из фольги алюминиевой. По 1 банке вместе с инструкцией по медицинскому применению в пачку из картона коробочного.
Срок годности
3 года 8 месяцев.
Препарат с истекшим сроком годности применению не подлежит.
Условия хранения
Хранить в сухом, защищенном от света месте при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Условия отпуска
Отпускают по рецепту.
Производитель
Акционерное общество «Сибирский центр фармакологии и биотехнологии» (АО «СЦФБ»), 630056, г. Новосибирск, ул. Софийская, 20, офис 10 (все стадии производства и выпускающий контроль качества).
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
Федеральное бюджетное учреждение науки «Государственный научный центр вирусологии и биотехнологии «Вектор» Федеральной службы по надзору в сфере защиты прав и благополучия человека (ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора), 630559, Новосибирская область, р. п. Кольцово.
Комментарии
ПРАКТИКА ПЕДИАТРА
