Луцентис - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер:
ЛСР-004567/08
Торговое наименование:
Луцентис®
Международное непатентованное наименование (МНН):
ранибизумаб
Лекарственная форма:
раствор для внутриглазного введения
Состав:
1 мл раствора для внутриглазного введения/флакон/предварительно заполненный шприц содержит:
действующее вещество: ранибизумаб - 10/2,3/1,65 мг;
вспомогательные вещества: а,а-трегалозы дигидрат 100/23/16,5 мг, гистидина гидрохлорида моногидрат 1,662/0,382/0,274 мг, гистидин 0,321/0,074/0,053 мг, полисорбат 20 0,1/0,023/0,0165 мг, вода для инъекций до 1 мл/до 0,23/до 0,165 мл.
Описание:
прозрачный или слегка опалесцирующий, бесцветный или очень слабо окрашенный раствор.
Фармакотерапевтическая группа:
средства, препятствующие новообразованию сосудов.
Код ATX:
S01LA04
Фармакологические свойства
Механизм действия
Ранибизумаб является фрагментом гуманизированного антитела к эндотелиальному фактору роста сосудов A (VEGF-A) и экспрессируется рекомбинантным штаммом Escherichia coli. Он избирательно связывается с VEGF-A (VEGF110, VEGF121, VEGF165) и предотвращает его взаимодействие с рецепторами на поверхности клеток эндотелия (VEGFR1 и VEGFR2), что приводит к подавлению неоваскуляризации и пролиферации эндотелиальных клеток.
Фармакодинамика
Подавляя пролиферацию эндотелиальных клеток, рост новообразованных сосудов хориоидеи и экссудацию из них, ранибизумаб останавливает прогрессирование неоваскулярной (влажной) формы возрастной макулярной дегенерации (нВМД), развитие хориоидальной неоваскуляризации (ХНВ), включая ХНВ вследствие патологической миопии (ПМ), и уменьшает макулярный отек (МО) вследствие диабетической ретинопатии (ДР) или окклюзии (тромбоза) вен сетчатки (ОВС), сопровождающийся снижением остроты зрения (03).
Неоваскулярная (влажная) форма возрастной макулярной дегенерации
Безопасность и эффективность применения ранибизумаба при нВМД оценивалась в трех исследованиях: MARINA, PIER и ANCHOR.
Ключевые данные оценки эффективности отображены в таблице 1 и рисунке 1.
Таблица 1.
Обобщенные ключевые результаты к 12 и 24 месяцам исследований MARINA и ANCHOR (ар <0,01)
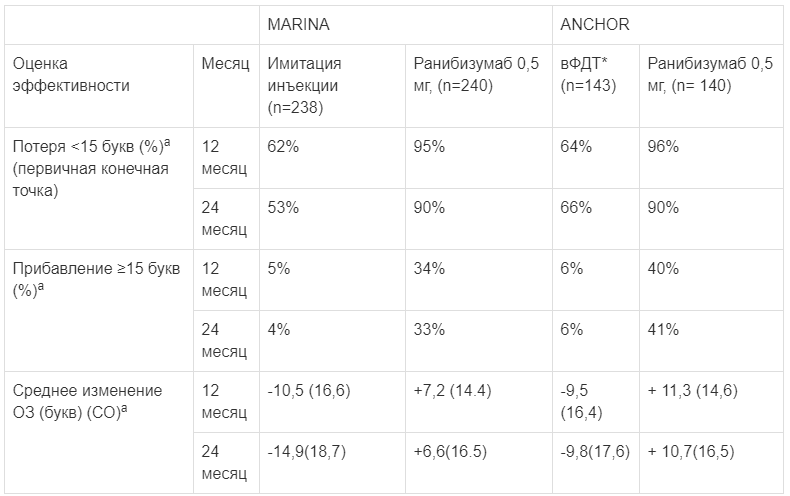 * вФДТ - фотодинамическая терапия с вертепорфином
* вФДТ - фотодинамическая терапия с вертепорфином
Рисунок 1. Среднее изменение 03 к 24 месяцу в исследованиях MARINA и ANCHOR.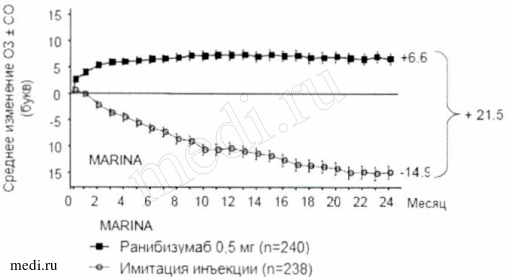
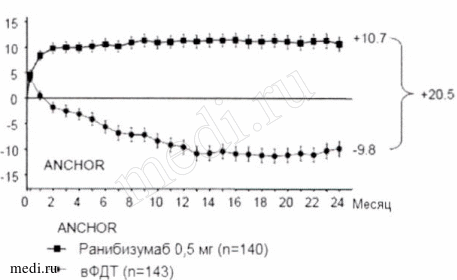
По данным обоих исследований продолжение терапии ранибизумабом оказывало положительный эффект у пациентов с потерей ≥15 букв от максимальной корригированной остроты зрения (МКОЗ) на протяжении первого года лечения.
В исследовании PIER в среднем пациентам было проведено по 10 инъекций.
После изначального повышения 03 на фоне ежемесячного введения ранибизумаба, на фоне применения препарата 1 раз в 3 месяца 03 снижалась вплоть до первоначального уровня к 12 месяцу терапии. Ограниченные данные применения ранибизумаба у пациентов, которым изначально проводили имитацию инъекции, предположительно указывают на то, что раннее начало лечения обеспечивает лучший результат по 03.
Снижение остроты зрения, связанное с диабетическим макулярным отеком
Безопасность и эффективность применения ранибизумаба при ДМО оценивалась в трех исследованиях (RESTORE, RESTORE Extension и RETAIN).
Ключевые данные оценки эффективности в исследованиях RESTORE и RESTORE Extension отображены в таблице 2 и рисунке 2.
Таблица 2.
Оценка эффективности к 12 месяцу (RESTORE) и к 36 месяцу (RESTORE Extension). ар<0,0001
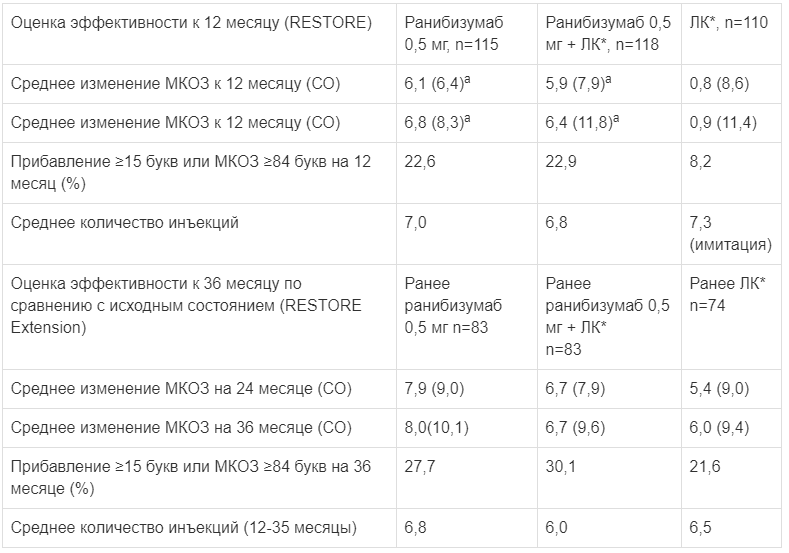 *ЛК - лазерная коагуляция
*ЛК - лазерная коагуляция
Рисунок 2. Среднее изменение 03 в исследовании RESTORE.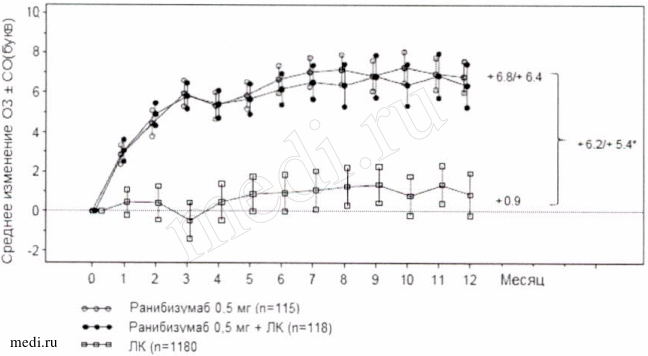
Ключевые данные оценки эффективности в исследовании RETAIN отображены в таблице 3.
Таблица 3.
Оценка эффективности в исследовании RETAIN.а р<0,0001
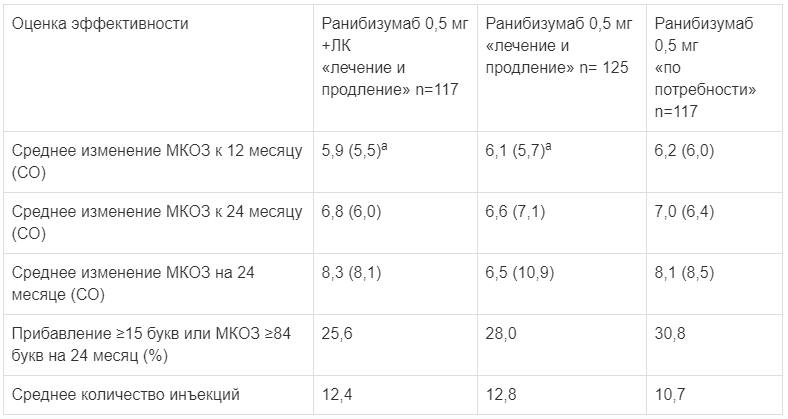
Снижение остроты зрения, вызванного макулярным отеком вследствие окклюзии вен сетчатки
Безопасность и эффективность применения ранибизумаба при МО вследствие ОВС оценивалась в исследованиях BRAVO (МО при окклюзии ветви центральной вены сетчатки, ОВЦВС), и CRUISE (МО при окклюзии центральной вены сетчатки, ОЦВС).
Ключевые данные оценки эффективности в исследованиях BRAVO и CRUISE отображены в таблице 4 и рисунках За, 3б.
Таблица 4.
Оценка эффективности на 6 и 12 месяцах (BRAVO и CRUISE).а р<0,0001
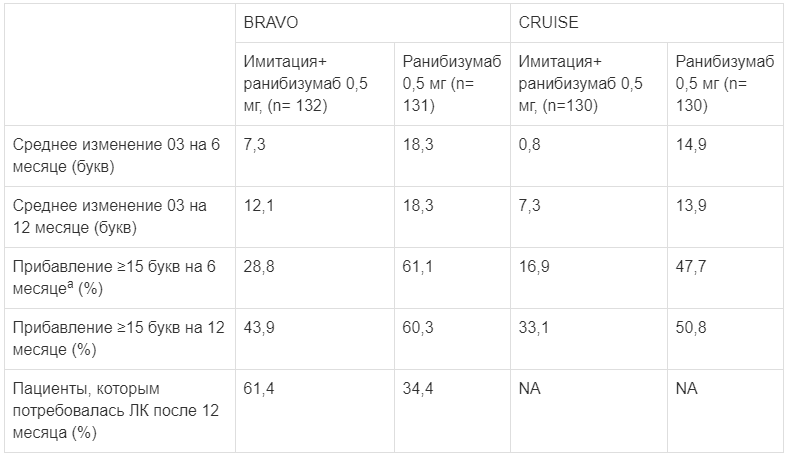
Рисунок За. Среднее изменение МКОЗ в исследовании BRAVO.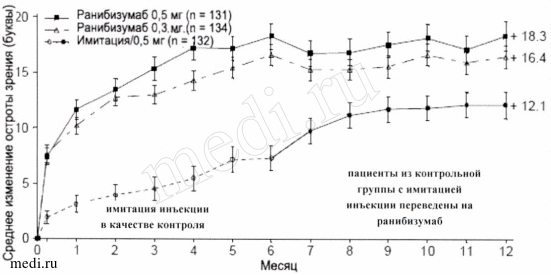
Рисунок 3б. Среднее изменение МКОЗ в исследовании CRUISE.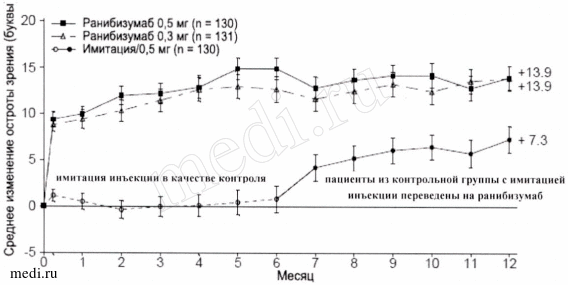
Отдаленные результаты безопасности и эффективности применения ранибизумаба оценивались в исследованиях BRIGHTER (МО при ОВЦВС) и CRYSTAL (МО при ОЦВС).
Ключевые данные оценки эффективности в исследованиях BRIGHTER и CRYSTAL отображены в таблице 5.
Таблица 5.
Оценка эффективности к 6 и 24 месяцам (BRIGHTER и CRYSTAL).а р<0,0001
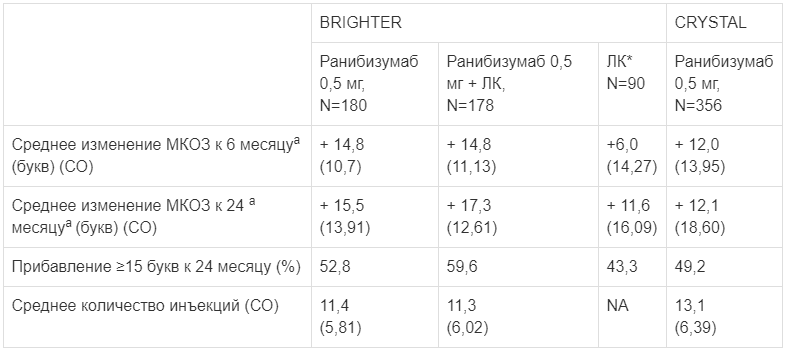 * Начиная с 6 месяца допускалось введение 0,5 мг ранибизумаба (24 пациентам проводилась только ЛК)
* Начиная с 6 месяца допускалось введение 0,5 мг ранибизумаба (24 пациентам проводилась только ЛК)Снижение остроты зрения, вызванное хориоидальной неоваскуляризацией
Безопасность и эффективность применения ранибизумаба при ХНВ, не обусловленной вВМД и/или ПМ, оценивалась в исследовании MINERVA.
Ключевые данные оценки эффективности в исследовании MINERVA отображены в таблицах 6, 7 и рисунке 4.
Таблица 6.
Оценка эффективности на 2 месяце (MINERVA).а р<0,001
|
Ранибизумаб 0,5 мг |
Имитация инъекции |
|
|
Среднее изменение МКОЗ ко 2 месяцу (букв) (предел среднего)a |
+9,5 |
-0,4 |
|
Прибавление ≥10 букв или МКОЗ ≥84 букв (%) |
42,4% |
14,0% |
|
Отсутствие потери ≥ 10 букв ко 2 месяцу (%) |
99,2% |
91,2% |
|
Уменьшение толщины центральной зоны сетчатки ко 2 месяцу (предел среднего)a |
77 мкм |
-9,8 мкм |
Таблица 7.
Общий эффект терапии и эффект терапии в зависимости от этиологии ко 2 месяцу (MINERVA).
|
Эффект лечения по сравнению с плацебо (букв) |
Количество пациентов (в обеих группах сравнения) |
|
|
Все подгруппы |
9,9 |
175* |
|
Ангиоидные полосы |
14,6 |
27 |
|
Поствоспалительная хориоретинопатия |
6,5 |
27 |
|
Центральная серозная хориоретинопатия |
5,0 |
23 |
|
Идиопатическая хориоретинопатия |
11,4 |
62 |
|
Другие патологии |
10,6 |
36 |
Рисунок 4. Среднее изменение МКОЗ за 12 месяцев (MINERVA).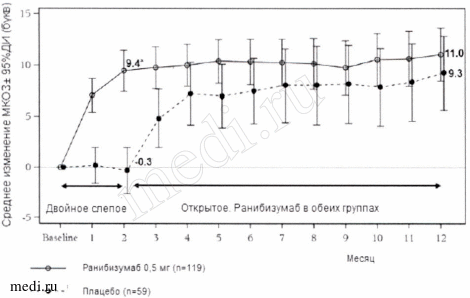
Имеются ограниченные данные по безопасности применения препарата у подростков 12-17 лет со снижением зрения, вызванным ХНВ. В исследовании применения ранибизумаба в дозе 0,5 мг по индивидуальной схеме, основанной на оценке активности заболевания (снижение ОЗ, наличие интра-/суб-ретинальной жидкости, геморрагия или экссудация), у 5 пациентов в возрасте от 12 до 17 лет со снижением 03 вследствие ХНВ улучшение МКОЗ составило от 5 до 38 букв (в среднем 16,6 букв) по таблице ETDRS. Улучшение зрения сопровождалось стабилизацией или уменьшением толщины центральной зоны сетчатки на протяжении 12 месяцев. В среднем за время исследования потребовалось проведение 3 интравитреальных инъекций в каждый глаз.
Снижение остроты зрения, вызванное хориоидальной неоваскуляризацией, обусловленной патологической миопией
Безопасность и эффективность применения ранибизумаба при ХНВ вследствие ПМ оценивалась в исследовании RADIANCE.
Ключевые данные оценки эффективности исследовании RADIANCE отображены в таблице 8 и на рисунке 5.
Таблица 8.
Оценка эффективности за 3 и 12 месяцев (RADIANCE). а р<0,00001 по сравнению с группой 3.
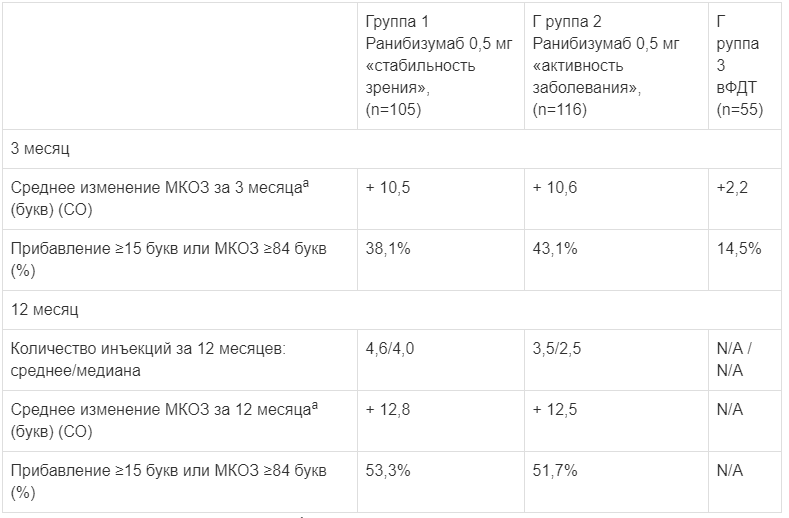
Рисунок 5. Среднее изменение МКОЗ за 12 месяцев (RADIANCE).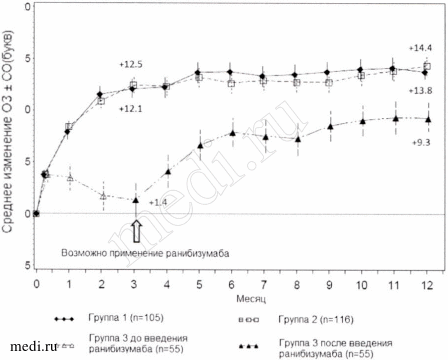
Фармакокинетика
Всасывание
При интравитреальном введении препарата (1 раз в месяц) у пациентов с нВМД максимальная концентрация ранибизумаба (Cmax) в плазме крови была низкой и недостаточной для ингибирования биологической активности VEGF-A (т.е. на 50% ниже необходимой, 11-27нг/мл по данным исследований клеточной пролиферации in vitro). При интравитреальном введении ранибизумаба в диапазоне доз от 0,05 мг до 1,0 мг Cmax в плазме крови была пропорциональна дозе. Ожидается, что при интравитреальном введении 1 раз в месяц Сmахранибизумаба, которая достигается через сутки после введения, будет в основном находиться в диапазоне 0.79-2,90 нг/мл, минимальная концентрация - в диапазоне 0,07-0,49 нг/мл. Сывороточная концентрация ранибизумаба у пациентов с ДМО и ОВС схожа с таковой у пациентов с нВМД.
Распределение и выведение
Но данным фармакокинетического анализа и, учитывая выведение ранибизумаба из плазмы крови, средний период полувыведения (доза 0.5 мг) из стекловидного тела в среднем составлял около 9 дней.
Концентрация ранибизумаба в плазме крови приблизительно в 90000 раз ниже таковой в стекловидном теле.
Особые группы пациентов
Пациенты с нарушением функции почек
У пациентов с нарушением функции почек специальные фармакокинетические исследования применения ранибизумаба не проводились. У 68% (136/200) пациентов с нВМД. включенных в фармакокинетический анализ, имелись нарушения функции почек (46,5% - легкой степени тяжести, 20% - средней степени тяжести и 1,5% - тяжелой степени). У 48,2% (253/525) пациентов с ОВС имелись нарушения функции почек (36,4% - легкой степени тяжести, 9,5% - средней степени тяжести и 2,3% - тяжелой степени). На фоне лечения препаратом у пациентов с нарушением функции почек отмечалось минимальное снижение клиренса ранибизумаба, не имеющее клинического значения.
Пациенты с нарушением функции печени
У пациентов с нарушением функции печени специальные фармакокинетические исследования применения ранибизумаба не проводились.
Показания к применению
- Лечение неоваскулярной (влажной) формы возрастной макулярной дегенерации (нВМД).
- Лечение снижения остроты зрения, вызванного хориоидальной неоваскуляризацией (ХНВ).
- Лечение снижения остроты зрения, связанного с диабетическим макулярным отеком (ДМО).
- Лечение снижения остроты зрения, вызванного макулярным отеком (МО) вследствие окклюзии вен сетчатки (ОВС, центральной вены сетчатки или ее ветвей).
Противопоказания
- Повышенная чувствительность к ранибизумабу или любому другому компоненту препарата.
- Подтвержденные или предполагаемые инфекции глаза или инфекционные процессы периокулярной локализации.
- Активный интраокулярный воспалительный процесс.
- Детский возраст до 18 лет (эффективность и безопасность применения препарата у данной категории пациентов не изучены).
- Беременность и период грудного вскармливания.
С осторожностью:
- при наличии в анамнезе инсульта или преходящей ишемии головного мозга в связи с риском развития тромбоэмболических явлений;
- у пациентов с гиперчувствительностью в анамнезе;
- у пациентов с нВМД и выявленной обширной и/или высокой отслойкой пигментного эпителия сетчатки;
- у пациентов с риском развития регматогенной отслойки сетчатки.
Применение при беременности и в период грудного вскармливания
Применение при беременности и в период грудного вскармливания противопоказано. Системное воздействие ранибизумаба после его интраокулярного введения низкое, но, принимая во внимание механизм действия препарата, ранибизумаб должен рассматриваться как потенциально тератогенное и эмбрио-/фетотоксичное лекарственное средство. Женщинам детородного возраста при применении ранибизумаба следует применять надежные методы контрацепции. Интервал между окончанием лечения и зачатием должен быть не менее 3 месяцев.
Не известно выделяется ли ранибизумаб в грудное молоко у человека. Применение ранибизумаба в период грудного вскармливания противопоказано.
Способ применения и дозы
Вводить препарат должен только офтальмолог, имеющий опыт выполнения интравитреальных инъекций, с соблюдением правил асептики.
Рекомендуемая доза препарата Луцентис® составляет 0,5 мг, что соответствует 0,05 мл раствора, в виде интравитреальной инъекции. Между введениями препарата в один глаз следует соблюдать интервал не менее 4 недель.
Лечение нВМД; снижения остроты зрения, связанного с ДМО; снижения остроты зрения, вызванного МО вследствие ОВС; снижения остроты зрения, вызванного ХНВ
Лечение препаратом Луцентис® начинают с одной инъекции в месяц и продолжают до достижения максимальной 03 или до исчезновения признаков активности заболевания, т.е. отсутствия изменения 03 и других признаков и симптомов активности заболевания на фоне продолжающегося лечения. Стабилизация заболевания определяется как отсутствие улучшения 03 и/или анатомических параметров сетчатки в течение одного месяца после последней ежемесячной инъекции.
У пациентов с нВМД, снижением 03, связанным с ДМО и снижением 03, вызванным МО вследствие ОВС изначально может потребоваться 3 или более последовательные ежемесячные инъекции препарата Луцентис®.
После достижения стабилизации заболевания на фоне ежемесячного введения препарата периодичность контрольных осмотров и временной интервал между инъекциями устанавливает врач в зависимости от активности заболевания, оцениваемой по 03 или анатомическим параметрам.
В случае если, по мнению врача, основанном на оценке 03 и анатомических параметров сетчатки, нет улучшения от проводимого лечения, терапию препаратом Луцентис® следует прекратить. При лечении нВМД и ПМ предупреждение снижения 03 даже при отсутствии ее улучшения следует считать положительной динамикой, по сравнению с естественным течением заболевания.
Контроль активности заболевания осуществляется путем оценки клинических данных, данных функциональных тестов, а также специальных методов визуализации (оптической когерентной томографии (ОКТ) или флуоресцентной ангиографии (ФАГ)). Оценка эффективности лечения может основываться на показателях 03 или анатомических параметрах (активность заболевания определяется как снижение 03 и/или ухудшение анатомических параметров сетчатки; отсутствие активности заболевания определяется как отсутствие изменения 03 или анатомических параметров сетчатки в течение одного месяца после последней инъекции).
При использовании режима «лечение и продление» после достижения максимальной 03 и/или при отсутствии признаков активности заболевания возможно поэтапное увеличение интервалов между введением препарата до повторного снижения 03 или возникновения признаков активности заболевания. Каждый интервал между инъекциями следует увеличивать не более чем на 2 недели при лечении нВМД и не более чем на 1 месяц при лечении снижения 03, связанного с ДМО. При лечении снижения 03, вызванного МО вследствие ОВС (центральной вены сетчатки или ее ветвей) возможно поэтапное увеличение интервалов, однако на данный момент недостаточно данных для определения величины интервалов. При реактивации заболевания интервалы следует укорачивать соответственно.
Режим лечения при снижении 03, вызванном ХНВ подбирают индивидуально для каждого пациента, основываясь на активности заболевания. Некоторым пациентам может потребоваться только одна инъекция в течение первого года лечения, другим же могут потребоваться более частые инъекции, вплоть до ежемесячных.
Для лечения снижения 03, вызванного ХНВ, обусловленной ПМ, многим пациентам может понадобиться одна или две инъекции в течение первого года лечения.
Терапия препаратом Луцентис® в сочетании с ЛК сетчатки при ДМО и ОВЦВС
В клинических исследованиях терапия препаратом Луцентис® сочеталась с применением ЛК у пациентов с ДМО и пациентов с ОВЦВС (в том числе у пациентов с предшествующей ЛК). При применении обоих методов терапии в течение одного дня, препарат Луцентис® следует вводить спустя как минимум 30 минут после ЛК.
Нет опыта одновременного применения препарата Луцентис® с вертепорфином.
Особые группы пациентов
Пациенты с нарушением функции печени
Применение препарата у пациентов с нарушением функции печени не изучалось. Учитывая незначительную концентрацию ранибизумаба в плазме крови, изменения режима дозирования препарата не требуется.
Пациенты с нарушением функции почек
Пациентам с нарушением функции почек не требуется коррекции дозы препарата.
Пациенты младше 18 лет
Применение препарата Луцентис® у пациентов младше 18 лет противопоказано в связи с недостаточностью данных по безопасности у пациентов данной группы. Имеющиеся данные для подростков в возрасте от 12 до 17 лет со снижением 03, вызванным ХНВ. представлены в разделе «Фармакодинамика».
Пациенты в возрасте 65 лет и старше
Пациентам в возрасте 65 лет и старше не требуется коррекции дозы препарата.
Способ применения
Флакон и предварительно заполненный шприц предназначены для однократного применения.
Поскольку объем раствора во флаконе (0,23 мл) превышает рекомендованную дозу (0,05 мл), часть раствора, содержащегося во флаконе, следует утилизировать до проведения инъекции. Проведение более одной инъекции с использованием одного флакона может привести к контаминации раствора и последующему развитию внутриглазной инфекции.
Препарат Луцентис® применяют только в виде интравитреальных инъекций.
Перед введением препарата Луцентис® следует проконтролировать качество растворения и цвет раствора. Препарат нельзя применять при изменении цвета раствора и появлении нерастворившихся видимых частиц.
Интравитреальную инъекцию препарата следует проводить в асептических условиях, включающих хирургическую обработку рук медицинских работников, использование стерильных перчаток, простыней, векорасширителя (или его аналога). В качестве меры предосторожности следует подготовить стерильный набор инструментов для парацентеза. Перед проведением процедуры следует обязательно провести сбор аллергологического анамнеза. Перед проведением интравитреальной инъекции необходимо обеспечить адекватную анестезию, провести дезинфекцию кожи век. области вокруг глаз и глазной поверхности с использованием местных бактерицидных средств широкого спектра действия.
Препарат Луцентис® следует вводить в стекловидную камеру глаза на 3,5-4 мм кзади от лимба, избегая горизонтального меридиана и направляя иглу к центру глазного яблока. Объем инъекции составляет 0,05 мл. Следующую инъекцию препарата следует производить в другой участок склеры.
За одну процедуру введение препарата Луцентис® проводят только в один глаз.
Контроль состояния пациента в период до и после проведения процедуры должен включать следующие этапы:
- перед проведением процедуры и в течение 30 минут после инъекции препарата Луцентис® следует контролировать внутриглазное давление (ВГД);
- непосредственно после проведения инъекции следует оценить перфузию диска зрительного нерва;
- на 2-7 день после проведения инъекции следует провести биомикроскопию и офтальмоскопию с целью раннего выявления возможного инфекционного процесса.
Побочное действие
Сводная характеристика безопасности препарата
Большинство нежелательных реакций (HP), отмеченных при применении препарата, связаны с процедурой интравитреальной инъекции.
Наиболее часто после введения препарата отмечались: боль в глазу, покраснение глаза, повышение ВГД, воспаление стекловидного тела, отслойка стекловидного тела, ретинальное кровоизлияние, зрительные нарушения, помутнение стекловидного тела, конъюнктивальное кровоизлияние, раздражение глаза, чувство «инородного тела» в глазу, слезотечение, блефарит, синдром «сухого» глаза, чувство зуда в глазу. Наиболее частыми HP, не связанными с органом зрения, являются: головная боль, назофарингит и артралгия. Более серьезными, но менее частыми являются: эндофтальмит, слепота, отслойка сетчатки, разрыв сетчатки и ятрогенная травматическая катаракта.
К HP отнесены нежелательные явления, которые встречались чаще (как минимум на 2%) в группе применения ранибизумаба по сравнению с группой контроля (имитация инъекции или применение вФДТ). HP, отмеченные в клинических исследованиях, сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов HP перечислены в порядке уменьшения частоты встречаемости. В пределах каждой группы частоты встречаемости HP указаны в порядке уменьшения их тяжести.
Для оценки частоты использованы следующие критерии: очень часто (≥1/10); часто (≥1/100; <1/10); нечасто (≥1/1000; <1/100); редко (≥1/10000; <1/1000); очень редко (<1/10000).
Инфекционные и паразитарные заболевания: очень часто - назофарингит; часто - грипп, инфекции мочевыводящих путей*.
Нарушения со стороны крови и лимфатической системы: часто - анемия.
Нарушения со стороны иммунной системы: часто - реакция гиперчувствительности.
Нарушения психики: часто - тревога.
Нарушения со стороны нервной системы: очень часто - головная боль; нечасто -инсульт.
Нарушения со стороны органа зрения: очень часто - интраокулярное воспаление, воспаление стекловидного тела. отслойка стекловидного тела, ретинальное кровоизлияние, зрительные нарушения, боль в глазу, помутнение стекловидного тела, конъюнктивальное кровоизлияние, раздражение глаза, чувство «инородного тела» в глазу, слезотечение, блефарит, синдром «сухого» глаза, покраснение глаза, чувство зуда в глазу; часто - дегенеративные изменения сетчатки, поражение сетчатки, отслойка сетчатки, разрыв сетчатки, отслойка пигментного эпителия сетчатки, разрыв пигментного эпителия сетчатки, снижение 03, кровоизлияние в стекловидное тело, поражение стекловидного тела, увеит, ирит, иридоциклит, катаракта, субкапсулярная катаракта, помутнение задней капсулы хрусталика, точечный кератит, эрозия роговицы, клеточная опалесценция в передней камере глаза, нечеткость зрения, кровоизлияние в месте инъекции, кровоизлияние в глаз, конъюнктивит, аллергический конъюнктивит, выделения из глаза, фотопсия, светобоязнь, чувство дискомфорта в глазу, отек века, болезненность века, гиперемия конъюнктивы; нечасто - слепота, эндофтальмит, гипопион, гифема, кератопатия, синехии радужки, отложения в роговице, отек роговицы, стрии роговицы, боль в месте инъекции, раздражение в месте инъекции, атипичные ощущения в глазу, раздражение век.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: часто - кашель.
Нарушения со стороны желудочно-кишечного тракта: часто - тошнота.
Нарушения со стороны кожи и подкожных тканей: часто - аллергические реакции (сыпь, крапивница, зуд, эритема).
Нарушения со стороны скелетно-мышечной и соединительной ткани: очень часто артралгия.
Лабораторные показатели: очень часто - повышение внутриглазного давления.
* - наблюдались только у пациентов с ДМО.
Нарушения со стороны сердечно-сосудистой системы
В исследованиях у пациентов с нВМД общая частота неофтальмологических кровоизлияний (нежелательного явления, которое может быть связано с системным подавлением активности VEGF) у пациентов, получавших ранибизумаб, была несколько повышена. Однако какой-либо четкой прослеживающейся закономерности кровоизлияний разного типа выявить не удалось.
По данным рабочей группы исследователей антитромбоцитарных препаратов (1994 г) существует связь между развитием артериальных тромбоэмболических осложнений (в т.ч. смертельные исходы в связи с сосудистыми причинами, инфаркт миокарда без летального исхода, геморрагический или ишемический инсульт без летального исхода) и системной биодоступностью высокоактивных ингибиторов VEGF. Частота развития тромбоэмболических осложнений в течение первого года лечения в группе пациентов, получавших препарат Луцентис® в дозах 0,3 мг и 0,5 мг, составила 2,3% по сравнению с 1,3% в контрольной группе. В одном из исследований данный показатель составил 3,0% по сравнению с 3,2% в контрольной группе в течение второго года лечения препаратом.
Иммуногенность
Как и при применении других терапевтических препаратов белкового происхождения у пациентов, получающих лечение препаратом Луцентис®, существует риск развития иммунных реакций. Данные, отражающие количество пациентов, у которых с использованием различных иммунологических диагностических тестов выявлены антитела к ранибизумабу, существенно зависят от специфичности и чувствительности указанных тестов.
В исследованиях лечения нВМД у взрослых частота развития иммунных реакций на введение препарата Луцентис® на этапе предварительного лечения составляла 0-3% во всех группах. После ежемесячного введения препарата на протяжении 12-24 месяцев антитела к ранибизумабу были обнаружены примерно у 1-8% пациентов с нВМД.
В исследованиях лечения снижения 03, связанного с ДМО, частота развития иммунных реакций на введение препарата Луцентис® на этапе предварительного лечения составляла 0-2% во всех группах. После ежемесячного введения препарата на протяжении 12 месяцев антитела к ранибизумабу были обнаружены примерно у 2-4% пациентов с ДМО. В исследованиях лечения снижения 03, вызванного МО вследствие ОВС, частота развития иммунных реакций на введение препарата Луцентис® на этапе предварительного лечения составляла 2-3% во всех группах. После ежемесячного введения препарата на протяжении 12 месяцев антитела к ранибизумабу были обнаружены примерно у 4-5% всех пациентов с МО вследствие ОВС.
Клиническая значимость иммунореактивности к препарату на данный момент остается невыясненной.
Мета-анализ совокупных данных по безопасности выявил, что при применении ранибизумаба в дозе 0,5 мг у пациентов с ДМО, частота случаев инфицирования/воспаления неглазных ран, не относящихся к серьезным, была выше, чем в группе контроля (1.85/100 пациенто/лет против 0,27/100 пациенто/лет). Взаимосвязь с ранибизумабом неясна.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты не указанные в инструкции, сообщите об этом врачу.
Передозировка
В клинических исследованиях и при применении препарата в клинической практике отмечались случаи непреднамеренной передозировки препаратом (введение большей дозы, чем рекомендованной - 0,05 мл). В указанных случаях при передозировке ранибизумабом наиболее часто отмечались повышение внутриглазного давления, преходящая слепота, снижение 03, отек роговицы, боль в роговице и боль в глазу. В случае передозировки препаратом следует обязательно контролировать ВГД; при необходимости пациент должен находиться под наблюдением врача.
В клинических исследованиях доза ранибизумаба у пациентов с нВМД и снижением 03, связанным с ДМО, достигала 2 мг в виде интравитреальной инъекции объемом 0,05 мл и 0,10 мл. Частота возникновения и характер местных и системных побочных эффектов соответствовали таковым при применении 0,5 мг ранибизумаба в виде интравитреальной инъекции объемом 0,05 мл.
Взаимодействие с другими лекарственными средствами
Взаимодействие препарата Луцентис® с другими лекарственными препаратами не изучалось.
В клинических исследованиях одновременное применение ранибизумаба для лечения снижения 03, связанного с ДМО, с производными тиазолидиндиона не оказывало влияния на результат лечения в отношении 03 и толщины центральной зоны сетчатки.
Препарат не следует смешивать с какими-либо другими лекарственными препаратами или растворителями.
Отсутствуют данные по применению ранибизумаба одновременно с вФДТ у пациентов со снижением 03, вызванным ХНВ при ПМ.
Особые указания
Проводить лечение препаратом должен только офтальмолог, имеющий опыт выполнения интравитреальных инъекций.
Реакции, связанные с интравитреальной инъекцией
При проведении интравитреальных инъекций возможно развитие эндофтальмита, внутриглазного воспаления, регматогенной отслойки сетчатки, разрыва сетчатки и ятрогенной травматической катаракты. Введение препарата Луцентис® следует всегда проводить в асептических условиях. Кроме того, в течение 1 недели после инъекции препарата необходимо наблюдать пациента с целью раннего выявления возможного местного инфекционного процесса и проведения своевременной терапии. Следует информировать пациента о необходимости незамедлительно сообщать врачу обо всех симптомах, которые могут свидетельствовать о развитии эндофтальмита, или любых вышеперечисленных явлениях.
Артериальная тромбоэмболия
При интравитреальной инъекции ингибиторов VEGF-A возможно развитие артериальных тромбоэмболических осложнений. В клиническом исследовании у пациентов с нВМД частота артериальной тромбоэмболии при применении ранибизумаба была сопоставима с контрольной группой.
Частота инсультов была выше в группе применения ранибизумаба в дозе 0,5 мг, по сравнению с таковой в группе применения ранибизумаба 0,3 мг или группе плацебо, однако это различие статистически не значимо. Риск развития инсульта может быть выше при наличии факторов риска, включая перенесенный ранее инсульт или транзиторные нарушения мозгового кровообращения в анамнезе. Лечащему врачу следует тщательно оценить соотношение польза/риск у пациентов данной группы.
Иммуногенность
Препарат обладает иммуногенными свойствами. Так как у пациентов с ДМО существует более высокий риск системного воздействия препарата, необходимо помнить и о более высоком риске развития реакций гиперчувствительности у пациентов данной категории. Следует предупредить пациента о необходимости сообщать врачу о признаках, свидетельствующих о развитии интраокулярного воспаления, что может указывать на интраокулярное формирование антител к препарату.
Одновременное применение препарата Луцентис® с другими лекарственными препаратами, оказывающими ингибирующее влияние на VEGF (для местного или системного применения)
Одновременное применение препарата Луцентис® с другими лекарственными препаратами, оказывающими ингибирующее влияние на VEGF (для местного или системного применения), недопустимо.
Приостановление терапии препаратом Луцентис®
Очередную инъекцию препарата Луцентис® следует отменить и не производить до следующей инъекции по расписанию в следующих случаях:
- снижение МКОЗ на ≥30 букв по сравнению с последним определением;
- ВГД ≥30 мм рт. ст.;
- разрыв сетчатки;
- субретинальные кровоизлияния, затрагивающие центральную часть фовеа, или площадь кровоизлияния составляет ≥50% площади поражения;
- в течение 28 дней до или после интраокулярного хирургического вмешательства.
Разрыв пигментного эпителия сетчатки
Следует соблюдать осторожность при применении препарата у пациентов с нВМД и выявленной обширной и/или высокой отслойкой пигментного эпителия сетчатки, так как у пациентов данной категории повышен риск развития разрывов пигментного эпителия.
Регматогенная отслойка сетчатки или макулярное отверстие
Препарат следует применять с осторожностью у пациентов с риском развития регматогенной отслойки сетчатки. У пациентов с регматогенной отслойкой сетчатки или макулярным отверстием 3, 4 стадии лечение препаратом Луцентис® должно быть прекращено.
Повышение внутриглазного давления
У пациентов после введения препарата Луцентис® отмечалось временное (в течение 60 мин после инъекции) повышение ВГД. Также отмечались случаи устойчивого повышения ВГД. На фоне применения препарата Луцентис® рекомендуется контролировать ВГД и перфузию диска зрительного нерва и при необходимости проводить надлежащее лечение.
Билатеральное применение
Из ограниченных данных по инъекциям препарата Луцентис® в оба глаза (включая инъекции в один день) не следует, что риск системных нежелательных явлений при этом выше, чем в случае инъекций в один глаз.
Лазерная коагуляция сетчатки
Возможно применение препарата Луцентис® как в монотерапии, так и в сочетании с предшествующей ЛК. При применении обоих методов терапии в течение одного дня, препарат Луцентис® следует вводить спустя как минимум 30 минут после ЛК.
Ограниченные данные
Опыт применения препарата Луцентис® ограничен у пациентов с ДМО вследствие сахарного диабета (СД) 1 типа; у пациентов, ранее получавших лечение препаратами для интраокулярного введения; у пациентов с активными системными инфекциями; с пролиферативной ДР; у пациентов с сопутствующими неинфекционными заболеваниями глаз, такими как отслойка сетчатки или макулярное отверстие. Отсутствует опыт применения препарата Луцентис® у пациентов с СД с концентрацией гликированного гемоглобина (HbAlc) более 12% и неконтролируемой артериальной гипертензией.
Опыт применения препарата Луцентис® ограничен у пациентов с ИМ, ранее безуспешно подвергавшихся вФДТ. Несмотря на то, что у пациентов с субфовеальной и юкстафовеальной локализацией поражения отмечался сходный эффект, недостаточно данных для выводов относительно эффективности применения препарата Луцентис® у пациентов с ПМ с экстрафовеальной локализацией поражения.
Женщины с сохраненным репродуктивным потенциалом
При проведении терапии препаратом Луцентис® женщинам с сохраненным репродуктивным потенциалом следует применять надежные методы контрацепции.
Влияние на способность управлять транспортными средствами и механизмами
На фоне применения ранибизумаба возможно развитие временных нарушений зрения, отрицательно влияющих на способность управлять транспортными средствами и механизмами. При возникновении таких симптомов пациентам не следует управлять транспортными средствами или механизмами до снижения выраженности временных зрительных нарушений.
Форма выпуска
Раствор для внутриглазного введения, 10 мг/мл.
I. По 0,23 мл во флакон из бесцветного стекла, укупоренный резиновой пробкой, обкатанной алюминиевым колпачком с отщелкивающейся крышкой.
По одному флакону вместе с инструкцией по медицинскому применению в картонную пачку или по одному флакону в комплекте с иглой, снабженной фильтром, для извлечения препарата из флакона, вместе с инструкцией по медицинскому применению в картонную пачку или по одному флакону в комплекте с иглой, снабженной фильтром, для извлечения препарата из флакона, шприцем, иглой для инъекций вместе с инструкцией по медицинскому применению в картонную пачку.
II. По 0,165 мл препарата в предварительно заполненном шприце из стекла, укупоренном резиновой пробкой с белой полипропиленовой крышкой контроля первого вскрытия.
По одному предварительно заполненному шприцу в блистере, снабженном этикеткой, вместе с инструкцией по медицинскому применению в картонную пачку.
Условия хранения
В защищенном от света месте при температуре от 2 до 8°С. Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять после истечения срока годности.
Условия отпуска
Отпускают по рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
Новартис Фарма АГ, Лихтштрассе 35, 4056 Базель, Швейцария / Novartis Pharma AG, Lichtstrasse 35, 4056 Basel, Switzerland.
Производитель
Производство готовой лекарственной формы и первичная упаковка
Флаконы:
Новартис Фарма Штейн АГ, Шаффхаузерштрассе, 4332 Штейн, Швейцария/ Novartis Pharma Stein AG, Schaffhauserstrasse, 4332 Stein, Switzerland.
Предварительно заполненные шприцы:
Веттер Фарма- Фертигунг ГмбХ & Ко., Айзенбанштр. 2-4, 88085 Лангенарген, Германия/
Vetter Pharma-Fertigung GmbH & Со. KG, Eisenbahnstr. 2-4, 88085 Langenargen. Germany.
Вторичная/потребительская упаковка и выпускающий контроль качества
Новартис Фарма Штейн АГ, Шаффхаузерштрассе, 4332 Штейн, Швейцария/ Novartis Pharma Stein AG, Schaffhauserstrasse, 4332 Stein, Switzerland.
Получить дополнительную информацию о препарате, а также направить претензии и информацию о нежелательных явлениях можно по следующему адресу в России
ООО «Новартис Фарма»
125315, г. Москва, Ленинградский проспект, дом 72, корпус 3.
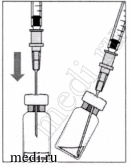
Указания по применению
Флакон
Невскрытый флакон можно хранить при температуре 25°С не более 24 часов.
Флакон предназначен для однократного применения. После проведения инъекции неиспользованный препарат следует утилизировать в соответствии с принятыми нормами. Флакон стерилен. Не использовать флакон при повреждении упаковки. Стерильность флакона не может быть гарантирована в случае, если упаковка повреждена. Не использовать флакон, если изменен цвет раствора, если раствор мутный или содержит нерастворенные частицы.
Для подготовки к интравитреальной инъекции потребуются следующие одноразовые медицинские изделия:
- игла, снабженная фильтром 18G (размер пор 5 мкм),
- шприц вместимостью 1 мл,
- игла для инъекций 30G х 1,2.
Перечисленные медицинские изделия не входят в состав упаковки, содержащей только флакон.
В комплект упаковки, содержащей флакон и иглу, снабженную фильтром, для извлечения содержимого из флакона, не входит стерильный шприц, вместимостью 1 мл и инъекционная игла.
Приготовление раствора препарата для интравитреальной инъекции следует проводить следующим образом:
|
A. |
1. Перед вскрытием флакона с препаратом поверхность резиновой пробки следует продезинфицировать. |
|
Б. |
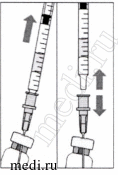
4. После извлечения препарата из флакона поршень шприца следует отодвинуть назад (до отметки 0,8-0,9 мл) для полного перехода раствора из иглы, снабженной фильтром, в шприц. |
B. |
6. В асептических условиях шприц плотно соединяют с иглой для инъекции (30G х 1,2). |
Г.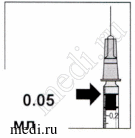 |
8. Аккуратно удаляют воздух из шприца и устанавливают поршень на отметке 0,05 мл. Только после этого можно вводить препарат в стекловидную камеру глаза. |
Инъекционная игла вводится в стекловидную камеру глаза на 3,5-4 мм кзади от лимба, избегая горизонтального меридиана и направляя иглу к центру глазного яблока. Объем инъекции составляет 0,05 мл, следующая инъекция выполняется в другой участок склеры.
Предварительно заполненный шприц
Невскрытую упаковку с предварительно заполненным шприцом можно хранить при температуре 25°С не более 24 часов.
Предварительно заполненный шприц предназначен для одноразового применения.
Предварительно заполненный шприц стерилен. Не использовать предварительно заполненный шприц при повреждении упаковки. Стерильность гарантирована только при отсутствии повреждений блистера. Не применять в случае изменения цвета, помутнения раствора или появления включений/осадка.
Приготовление раствора препарата для интравитреальной инъекции следует проводить следующим образом:
| Внимательно прочитайте эту инструкцию перед тем, как начать применение препарата. Необходимо соблюдение правил асептики при проведении инъекций препарата. ! Внимание: Необходимо установить поршень на отметке 0,05 мл. |
||
| Описание предварительно заполненного шприца | 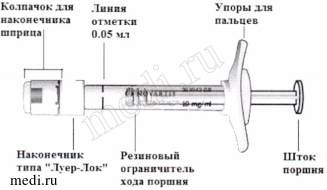
|
|
| Подготовка | 1. Раскройте упаковку шприца, удалив с нее пленочную крышку. 2. Осторожно извлеките предварительно заполненный шприц из блистера, соблюдая правила асептики. |
|
|
Проверьте шприц |
3. Убедитесь, что: |
|
|
Удалите колпачок для наконечника шприца |
5. Отломите (не поворачивая и не откручивая) колпачок для наконечника шприца (см. рис. 1). |
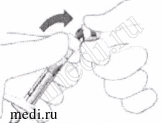 Рис.1. 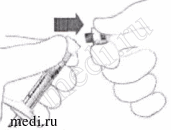 Рис.2. |
|
Присоедините иглу |
7. Присоедините иглу для инъекции к предварительно заполненному шприцу, плотно прикрутив к наконечнику типа «Луер-Лок» (см. рис. 3). |
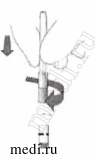 Рис.3.  Рис.4. |
|
Удалите из шприца пузырьки воздуха |
9. Удерживайте шприц в вертикальном положении. |
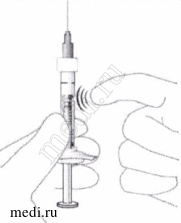 Рис.5. Рис.5. |
|
Отмерьте дозу |
11. Удерживая шприц на уровне глаз, осторожно надавите на поршень до тех пор, пока нижний край купола резинового ограничителя хода поршня не сравняется с линией отметки 0,05 мл (см. рис. 6). |
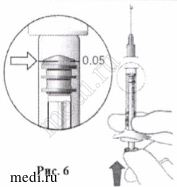 Рис.6. Рис.6. |
|
Выполните интравитреальную инъекцию |
12. Препарат Луцентис® следует вводить в стекловидную камеру глаза на 3,5-4 мм кзади от лимба, избегая горизонтального меридиана и направляя иглу к центру глазного яблока. |
|
Комментарии
ПРАКТИКА ПЕДИАТРА