Лектофунгин - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер:
ЛП-008105
Торговое наименование:
Лектофунгин.
Международное непатентованное или группировочное наименование:
каспофунгин.
Лекарственная форма:
лиофилизат для приготовления концентрата для приготовления раствора для инфузий.
Состав
Состав на 1 флакон
| Наименование вещества | Количество | |
| Дозировка 50 мг | Дозировка 70 мг | |
| Действующее вещество* | ||
| Каспофунгина ацетат | 60,6 мг | 83,9 мг |
| в пересчете на каспофунгин | 54,6 мг | 75,6 мг |
| Вспомогательные вещества | ||
| Сахароза | 39 мг | 54 мг |
| Маннитол | 26 мг | 36 мг |
| Уксусная кислота ледяная | 2 мг | 2,7 мг |
| Натрия гидроксид | до pH 5,7-6,3 | до pH 5,7-6,3 |
* Включая избыток (9,2% и 8,0%) для обеспечения соответствующей дозировки действующего вещества (50 мг и 70 мг соответственно).
Описание
Порошок или пористая масса от белого до белого с желтоватым оттенком цвета. Восстановленный раствор (содержимое флакона в 10,5 мл воды) прозрачный, от бесцветного до светло-желтого цвета.
Фармакотерапевтическая группа:
противогрибковое средство.
Код АТХ:
J02AX04.
Фармакологические свойства
Фармакодинамика
Каспофунгина ацетат представляет собой полусинтетическое липопептидное соединение (эхинокандин), синтезированное из продукта ферментации Glarea lozoyensis. Каспофунгина ацетат ингибирует синтез β-(1,3)-D-глюкана – важнейшего компонента клеточной стенки многих мицелиальных грибов и дрожжей. В клетках млекопитающих β-(1,3)-D-глюкан не присутствует.
In vitro каспофунгин обладает активностью против различных патогенных грибов рода Aspergillus (включая Aspergillus fumigatus, Aspergillus flavus, Aspergillus niger, Aspergillus nidulans, Aspergillus terreus и Aspergillus candidus) и Candida (включая Candida albicans, Candida dubliniensis, Candida glabrata, Candida guilliermondii, Candida kefyr, Candida krusei, Candida lipolytica, Candida lusitaniae, Candida parapsilosis, Candida rugosa и Candida tropicalis).
Исследования на чувствительность проводились двумя модифицированными методами – М38-А2 (для рода Aspergillus) и М27-АЗ (для рода Candida) Института клинических и лабораторных стандартов (CLSI).
Стандарты интерпретации для каспофунгина против грибов рода Candida применимы для микродилюции бульона методом М27-АЗ (только для процедуры CLSI) для определения минимальной подавляющей концентрации (МПК), которую рассчитывают в конечной точке частичного ингибирования (24 ч). Величину МПК каспофунгина, полученную с помощью микродилюции бульона методом М27-АЗ, следует интерпретировать в соответствии с критериями, указанными в Таблице 1.
Таблица 1. Критерии чувствительности для каспофунгина против грибов рода Candida.

* Категория «чувствительные» указывает на высокую вероятность ингибирования патогенных грибов при достижении ожидаемой концентрации антимикробного препарата в крови.
† Резистентная категория для эхинокандинов не установлена; изоляты с более высоким значением МПК могут характеризоваться как нечувствительные.
Для применения метода Европейского комитета по тестированию антимикробной чувствительности (EUCAST) стандарты интерпретации для каспофунгина против грибов рода Candida не установлены.
Для дрожжевых грибов комитетом EUCAST были разработаны стандартизированные методики определения чувствительности. Для грибов рода Aspergillus и других мицелиальных грибов не разработано стандартизированных методик определения чувствительности или стандартов интерпретации методами CLSI или EUCAST. In vivo выявлена активность каспофунгина при парентеральном введении животным с нормальным и сниженным иммунитетом, инфицированных Aspergillus и Candida. Применение каспофунгина в этих случаях способствует увеличению продолжительности жизни животных (Aspergillus и Candida) и эрадикации патогенных грибов (Candida) в пораженных органах. Каспофунгин также активен у животных с иммунодефицитом, зараженных Candida glabrata, Candida krusei, Candida lusitaniae, Candida parapsilosis, Candida tropicalis, у которых достигается эрадикация патогенных грибов (Candida) в пораженных органах. Каспофунгин проявляет высокую активность при профилактике и лечении легочных аспергиллезов, подтвержденную в исследованиях на моделях летальных легочных инфекций in vivo.
Перекрестная устойчивость. Каспофунгин активен в отношении штаммов грибов Candida, резистентных к препаратам, имеющим другой механизм действия: флуконазолу, амфотерицину В или флуцитозину.
Лекарственная устойчивость. МПК ≤2 мкг/мл каспофунгина (категория «чувствительные» по Таблице 1) при использовании CLSI метода М27-АЗ указывает на высокую вероятность ингибирования изолятов Candida при достижении терапевтической концентрации каспофугнина. Прорывные инфекции, вызванные изолятами Candida, для подавления роста которых требуются концентрации каспофунгина >2 мкг/мл, были изучены на модели мышей с инфекцией С. albicans. Также у некоторых пациентов в процессе лечения препаратом были обнаружены изоляты Candida со сниженной чувствительностью к каспофунгину (МПК >2 мкг/мл каспофунгина при использовании CLSI стандартизированной методики определения МПК). Некоторые из этих изолятов имели мутации в гене FKS1/FKS2. Хотя частота таких случаев низкая, они как правило связаны с неблагоприятными клиническими исходами. У грибов рода Aspergillus обнаружено развитие in vitro лекарственной устойчивости к каспофунгину. В ходе клинического применения препарата обнаружена лекарственная устойчивость к каспофунгину у пациентов с инвазивным аспергиллезом. Механизм резистентности не установлен. Частота случаев лекарственной устойчивости различных клинических изолятов Candida и Aspergillus низка.
Лекарственные взаимодействия. Исследования каспофунгина in vitro и in vivo в комбинации с амфотерицином В демонстрируют отсутствие антагонизма в отношении противогрибковой активности в отношении A. fumigatus или С. albicans. Результаты исследований in vitro позволяют предположить наличие аддитивного влияния / отсутствие влияния или синергизма против A. fumigatus и наличие аддитивного влияния / отсутствие влияния против С. albicans. Клиническая значимость полученных результатов неизвестна.
Фармакокинетика
Распределение. После однократной внутривенной инфузии в течение 1 часа концентрация каспофунгина в плазме снижается многофазно. Сразу после инфузии наступает короткая α-фаза, за которой следует β-фаза с периодом полувыведения (Т1/2) от 9 до 11 часов, которая является главной характеристикой профиля распределения препарата и имеет отчетливую логарифмически-линейную зависимость между 6 и 48 часами после введения. За этот период концентрация препарата в плазме существенно снижается. Также имеется дополнительная γ-фаза с Т1/2 от 40 до 50 часов. Распределение в большей степени, чем экскреция или биотрансформация, оказывает влияние на плазменный клиренс. Каспофунгин в значительной степени связывается с белками плазмы крови (приблизительно на 97%) при минимальном связывании с эритроцитами. Около 92% меченого [3Н]-каспофунгина ацетата обнаруживается в тканях через 36-48 часов после введения разовой дозы 70 мг. В течение первых 30 часов после введения экскреция и биотрансформация каспофунгина незначительны.
Метаболизм. Каспофунгин медленно метаболизируется путем гидролиза и N-ацетилирования с образованием пептидного соединения с открытым кольцом. В более поздние сроки (через 5 и более дней после введения разовой дозы меченого [3Н]-каспофунгина ацетата) в плазме отмечается низкий уровень (менее 7 пкмоль/мг белка, или 1,3% или менее от введенной дозы препарата) ковалентно связанного с белками меченого [3Н]-каспофунгина ацетата, что обусловлено образованием двух активных промежуточных продуктов распада каспофунгина. Дальнейший процесс метаболизма включает в себя гидролиз до составляющих аминокислот и их производных с образованием дигидроксигомотирозина и N-ацетил-дигидроксигомотирозина. Эти производные тирозина обнаруживают только в моче, что указывает на высокий почечный клиренс этих метаболитов.
Выведение. Выведению из организма подвергается около 75% препарата (фармакокинетическое исследование с радиоактивно меченым каспофунгином): 41% с мочой и 34% с фекалиями. Концентрации в плазме метки и каспофунгина в течение первых 24-48 часов после введения дозы не различаются, затем концентрация препарата снижается быстрее, причем снижение его концентрации ниже уровня количественного определения наблюдается через 6-8 дней после введения дозы, а радиоактивной метки – через 22,3 недели. Небольшое количество каспофунгина выделяется в неизмененном виде с мочой (приблизительно 1,4% дозы). Почечный клиренс исходного препарата низкий и составляет приблизительно 0,15 мл/мин.
Фармакокинетические особенности у отдельных групп пациентов
В зависимости от половой принадлежности. Концентрация каспофунгина в плазме у здоровых мужчин и женщин в 1-й день после введения разовой дозы 70 мг одинаковая. После 13 ежедневных введений по 50 мг концентрация каспофунгина в плазме у некоторых женщин была приблизительно на 20% выше, чем у мужчин.
У пожилых. Содержание каспофунгина в плазме крови здоровых мужчин и женщин пожилого возраста (65 лет и старше) выше на 28% (оценка по показателю площади под кривой «концентрация-время» – AUC) по сравнению со здоровыми молодыми людьми. У пациентов пожилого возраста с инвазивным кандидозом или на фоне эмпирической терапии наблюдались такие же умеренные изменения концентрации препарата в плазме, как и в группе здоровых пожилых добровольцев по сравнению со здоровыми добровольцами молодого возраста. Коррекция режима дозирования для пожилых (65 лет и старше) пациентов не требуется.
У пациентов с печеночной недостаточностью. Концентрация каспофунгина в плазме пациентов с легкой степенью печеночной недостаточности (5-6 баллов по шкале Чайлд-Пью) после введения разовой дозы 70 мг увеличивалась приблизительно на 55% (AUC) по сравнению со здоровыми лицами. Введение препарата этим пациентам в течение 14 дней (70 мг в 1 день с последующим ежедневным введением по 50 мг) сопровождалась повышением концентрации каспофунгина в плазме на 19-25% (AUC) на 7 и 14 день по сравнению со здоровыми добровольцами. У взрослых пациентов с печеночной недостаточностью средней степени (7-9 баллов по шкале Чайлд-Пью), получавших разовую дозу препарата 70 мг, концентрация каспофунгина в плазме увеличивалась приблизительно на 76% (AUC) по сравнению со здоровыми добровольцами.
У детей. Фармакокинетика каспофунгина изучена у детей до 18 лет (первоначально исследование у подростков 12-17 лет и детей 2-11 лет, затем – у детей младшего возраста (3-23 месяца), у новорожденных и детей первых трех месяцев жизни). У подростков (12-17 лет), получавших каспофунгин в дозе 50 мг/м² (максимальная суточная доза – 70 мг), экспозиция препарата в плазме крови (AUC0-24) в целом соответствовала экспозиции препарата у взрослых, принимавших 50 мг каспофунгина в сутки. Все подростки получали каспофунгин в дозе выше 50 мг, и шесть из восьми пациентов получали максимальную суточную дозу 70 мг. Концентрация каспофунгина в плазме крови у этих пациентов была ниже по сравнению с концентрацией у взрослых, получавших препарат в суточной дозе 70 мг, т.е. дозе, которая наиболее часто назначалась подросткам. У детей в возрасте 2-11 лет, получавших каспофунгин в дозе 50 мг/м² в день (максимальная суточная доза 70 мг в день), его экспозиция в плазме крови (AUC0-24) была сравнима с аналогичным показателем у взрослых пациентов, которым вводили каспофунгин в дозе 50 мг в день. В первый день применения экспозиция препарата в плазме крови (AUC0-24) была несколько выше у детей по сравнению со взрослыми (на 37% при сравниваемых дозах 50 мг/м² и 50 мг один раз в сутки). Однако необходимо подчеркнуть, что экспозиция препарата в плазме крови (AUC0-24) у детей в первый день была все же ниже, чем у взрослых при длительном лечении.
У детей в возрасте 3-23 месяцев, которым назначали каспофунгин в суточной дозе 50 мг/м² (максимальная доза – 70 мг), концентрация каспофунгина в плазме крови при длительном применении была сопоставима с концентрацией у взрослых, которым назначалась доза препарата 50 мг/сутки. Как и у более старших детей, у детей данной возрастной группы, получавших каспофунгин в дозе 50 мг/м², концентрация препарата в плазме крови была выше в первый день лечения по сравнению со взрослыми, получавшими стандартную дозу каспофунгина 50 мг. Фармакокинетические параметры каспофунгина в дозе 50 мг/м² у детей младшей возрастной группы (3-23 месяца) и более старшей группы (2-11 лет) при одинаковом режиме дозирования были сопоставимы.
У новорожденных и детей до 3 месяцев, которым каспофунгин назначали в дозе 25 мг/м², пиковая концентрация каспофунгина (С1) и его пороговая концентрация (С24ч) после повторных введений соответствовали аналогичным показателям у взрослых, получавших препарат в дозе 50 мг в день. В первый день пиковая концентрация С24ч была сопоставима со взрослыми, а пороговая концентрация С24ч была умеренно увеличена у новорожденных и детей грудного возраста по сравнению с соответствующими показателями у взрослых. Определение экспозиции препарата в плазме крови (AUC0-24) не проводилось в данном исследовании из-за сложностей отбора проб. Следует учесть, что изучение эффективности и безопасности в ходе проспективных адекватных клинических исследований каспофунгина у новорожденных и детей до 3 месяцев не проводилось.
Показания к применению
- Эмпирическая терапия у пациентов с фебрильной нейтропенией при подозрении на грибковую инфекцию (вызванную Candida или Aspergillus).
- Инвазивный кандидоз (в т.ч. кандидемия) у пациентов с нейтропенией и без нее.
- Инвазивный аспергиллез у пациентов, рефрактерных к другой терапии или не переносящих ее, включая амфотерицин В, в т.ч. липосомальный, и/или итраконазол.
- Эзофагеальный кандидоз.
- Орофарингеальный кандидоз.
Противопоказания
- Повышенная чувствительность к каспофунгину и к другим компонентам препарата.
- Детский возраст до 3 месяцев.
- Редкие наследственные заболевания непереносимости фруктозы или сахаразо-изомальтазная недостаточность (препарат содержит сахарозу).
С осторожностью
- Одновременное применение с циклоспорином.
- Пациенты с печеночной недостаточностью средней степени (от 7 до 9 баллов по шкале Чайлд-Пью).
Нет достаточных данных о применении каспофунгина у детей и взрослых при эндокардите, остеомиелите и менингите, вызванных патогенными штаммами грибов рода Candida, а также у детей в качестве терапии первой линии при инвазивном аспергиллезе.
Применение при беременности и в период грудного вскармливания
Клинического опыта по применению препарата у беременных и женщин в период грудного вскармливания нет.
Беременность. В исследованиях на крысах применение каспофунгина в дозах, токсичных для беременных самок (5 мкг/кг/день), приводило к уменьшению массы тела плода и увеличению случаев неполной оссификации черепа и туловища. Кроме того, при применении каспофунгина в тех же дозах у крыс зафиксировано увеличение числа случаев формирования шейного ребра. У животных каспофунгин проникает через плацентарный барьер.
Каспофунгин не должен назначаться женщинам во время беременности, кроме случаев, когда назначение препарата является жизненно необходимым.
Период грудного вскармливания. Поскольку нет данных о поступлении каспофунгина в молоко, при необходимости назначения препарата в период лактации следует прекратить грудное вскармливание.
Способ применения и дозы
Взрослые
Суточная доза каспофунгина вводится взрослым (>18 лет) путем медленной внутривенной инфузии (≥1 часа) 1 раз в сутки.
Эмпирическая терапия. В первый день вводится разовая нагрузочная доза 70 мг, во второй и последующие дни лечения суточная доза составляет 50 мг в сутки. Продолжительность лечения зависит от клинической и микробиологической эффективности препарата. У пациентов с фебрильной нейтропенией эмпирическая терапия должна проводиться до полного разрешения нейтропении. При подтверждении грибковой инфекции пациенты должны получать препарат не менее 14 дней; терапию следует продолжать не менее 7 дней после исчезновения клинических проявлений как грибковой инфекции, так и нейтропении. Суточную дозу каспофунгина можно увеличить до 70 мг в том случае, если суточная доза 50 мг хорошо переносится пациентом, но не дает ожидаемого клинического эффекта. Несмотря на то, что увеличение суточной дозы до 70 мг не продемонстрировало увеличения эффективности, данные по безопасности предполагают, что прием препарата в вышеуказанной дозе имеет хорошую переносимость.
Инвазивный кандидоз. В первый день вводится разовая нагрузочная доза 70 мг, во второй и последующие дни лечения суточная доза составляет 50 мг в сутки. Продолжительность лечения инвазивного кандидоза определяется клиническим эффектом и микробиологической эффективностью. Общим правилом является продолжение противогрибковой терапии не менее 14 дней после последнего получения положительного результата гемокультуры. Пациентам с персистирующей нейтропенией может потребоваться более длительное лечение до разрешения нейтропении. Безопасность и эффективность многократного применения суточных доз до 150 мг (диапазон: от 1 до 51 дня, среднее: 14 дней) были изучены у 100 взрослых пациентов с инвазивным кандидозом. Высокая доза каспофунгина хорошо переносилась пациентами, однако эффективность препарата в высокой дозе была в целом схожа с эффективностью препарата у пациентов, принимавших препарат в суточной дозе 50 мг.
Инвазивный аспергиллез. В первый день вводится разовая нагрузочная доза 70 мг, во второй и последующие дни лечения суточная доза составляет 50 мг в сутки. Продолжительность лечения зависит от тяжести основного заболевания, степени восстановления пациента от иммуносупрессии и клинического эффекта. Информация об эффективности введения суточной дозы 70 мг пациентам, у которых суточная доза 50 мг не приводит к ожидаемому клиническому ответу, отсутствует. Данные по безопасности указывают на хорошую переносимость при увеличении суточной дозы до 70 мг. Эффективность доз выше 70 мг у пациентов с инвазивным аспергиллезом изучена недостаточно.
Эзофагеальный и орофарингеальный кандидоз. Суточная доза составляет 50 мг в сутки, терапию следует продолжать не менее 7-14 дней после исчезновения симптомов. Информация об эффективности введения нагрузочной дозы 70 мг отсутствует.
Пожилые пациенты. Пожилым пациентам (65 лет и старше) коррекция дозы не требуется.
Снижение функции почек, половые и расовые различия. Не требуют коррекции дозы.
Пациенты с печеночной недостаточностью. Взрослым пациентам с легкой степенью печеночной недостаточности (5-6 баллов по шкале Чайлд-Пью) коррекции дозы не требуется. При печеночной недостаточности средней степени (от 7 до 9 баллов по шкале Чайлд-Пью) поддерживающая суточная доза каспофунгина уменьшается до 35 мг в сутки (на основании фармакокинетических данных), однако в первые сутки лечения должна вводиться нагрузочная доза 70 мг, если имеются соответствующие показания. Клинического опыта применения препарата у взрослых пациентов с тяжелой печеночной недостаточностью (более 9 баллов по шкале Чайлд-Пью) нет.
При одновременном применении каспофунгина с индукторами клиренса лекарственных препаратов (рифампицином, эфавирензом, невирапином, фенитоином, дексаметазоном или карбамазепином) должна рассматриваться возможность повышения суточной дозы препарата до 70 мг/м² для указанной группы пациентов (но не превышая допустимую дозу 70 мг).
Дети
Эффективность и безопасность применения каспофунгина у детей с 3 месяцев до 18 лет коррелирует с достаточной доказательной базой клинических исследований у взрослых пациентов, исследованиями фармакокинетики у детей и дополнительными данными проспективных исследований, на основании которых препарат успешно применяется у детей по тем же показаниям, что и у взрослых пациентов (см. раздел «Показания к применению»). Нет данных о безопасности и эффективности каспофунгина у новорожденных детей и детей младше 3 месяцев.
Суточная доза каспофунгина вводится детям (от 3 месяцев до 18 лет) путем медленной внутривенной инфузии (≥1 часа) 1 раз в сутки.
Доза препарата рассчитывается с учетом площади поверхности тела пациента по формуле Мостеллера (см. раздел «Приготовление раствора препарата для внутривенных инфузий детям»).
Для всех показаний в первый день вводится разовая нагрузочная доза 70 мг/м² (не должна превышать допустимую дозу 70 мг), в последующие дни – 50 мг/м² в сутки (не должна превышать допустимую дозу 70 мг). Продолжительность терапии определяется индивидуально и зависит от показания к применению (см. общие рекомендации по применению у взрослых пациентов в данном разделе).
Суточную дозу можно увеличить до 70 мг/м² в том случае, если суточная доза 50 мг/м² хорошо переносится пациентом, но не дает ожидаемого клинического эффекта (но не должна превышать допустимую суточную дозу 70 мг). Несмотря на то, что увеличение суточной дозы до 70 мг/м² не продемонстрировало увеличения эффективности, данные по безопасности предполагают, что прием препарата в вышеуказанной дозе имеет хорошую переносимость.
При одновременном применении каспофунгина с индукторами клиренса лекарственных препаратов (рифампицином, эфавирензом, невирапином, фенитоином, дексаметазоном или карбамазепином) должна рассматриваться возможность повышения суточной дозы каспофунгина до 70 мг/м² для детей (но не превышая допустимую суточную дозу 70 мг).
Клинического опыта применения препарата у детей с любой степенью печеночной недостаточности нет.
Инструкция по приготовлению раствора
НЕ ИСПОЛЬЗУЮТСЯ РАСТВОРИТЕЛИ, СОДЕРЖАЩИЕ ДЕКСТРОЗУ (α-D-ГЛЮКОЗУ), поскольку в инфузионных растворах, содержащих декстрозу, каспофунгин нестабилен. КАСПОФУНГИН НЕ СМЕШИВАЕТСЯ И НЕ ВВОДИТСЯ ОДНОВРЕМЕННО С ЛЮБЫМИ ДРУГИМИ ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ, поскольку нет данных о его совместимости с другими препаратами для внутривенного введения.
Приготовление раствора препарата для внутривенных инфузий взрослым
Этап 1. Приготовление первичного раствора во флаконе
Перед разведением холодный флакон с препаратом необходимо согреть до комнатной температуры. Затем с соблюдением правил асептики добавить 10,8 мл одного из следующих совместимых растворителей: стерильная вода для инъекций, 0,9% раствор натрия хлорида для инфузий, бактериостатическая вода для инъекций с метилпарабеном, пропилпарабеном или бактериостатическая вода для инъекций с 0,9% бензиловым спиртом. Концентрация каспофунгина в растворе составит 7,0 мг/мл (флакон 70 мг) или 5,0 мг/мл (флакон 50 мг).
Порошок должен полностью раствориться.
Осторожно встряхивают флакон до полного растворения препарата и получения прозрачного раствора. Осматривают первичный раствор, чтобы убедиться в отсутствии взвешенного осадка или изменения цвета.
Приготовленный с использованием стерильной воды для инъекций или 0,9% раствора натрия хлорида первичный раствор препарата можно хранить во флаконе до 24 часов в холодильнике (2-8 °С). Первичный раствор препарата, приготовленный с использованием других совместимых растворителей, следует использовать сразу после приготовления.
Этап 2. Приготовление конечного инфузионного раствора
Раствор для инфузий готовится в условиях соблюдения асептики. В качестве совместимых растворителей используются 0,9% раствор натрия хлорида для инфузий или раствор Рингера с лактатом. Для приготовления конечного инфузионного раствора, предназначенного для введения пациенту, в емкость для внутривенных инфузий, содержащую 250 мл стерильного 0,9% раствора натрия хлорида для инфузий или раствора Рингера с лактатом, добавляют соответствующее количество подготовленного на 1 этапе первичного раствора препарата (как показано в Таблице 2 ниже). При введении суточной дозы 50 мг или 35 мг объем добавляемого растворителя может быть уменьшен до 100 мл. Нельзя использовать мутный или содержащий осадок раствор.
Готовый конечный инфузионный раствор препарата, приготовленный с использованием 0,9% раствора натрия хлорида, следует использовать в течение 48 часов, если он хранится в холодильнике (2-8°С). Готовый конечный инфузионный раствор препарата, приготовленный с использованием раствора Рингера с лактатом, следует использовать сразу после приготовления.
Готовый конечный инфузионный раствор препарата вводится путем медленной внутривенной инфузии (≥1 часа).
Таблица 2. Приготовление конечного инфузионного раствора препарата для взрослых.
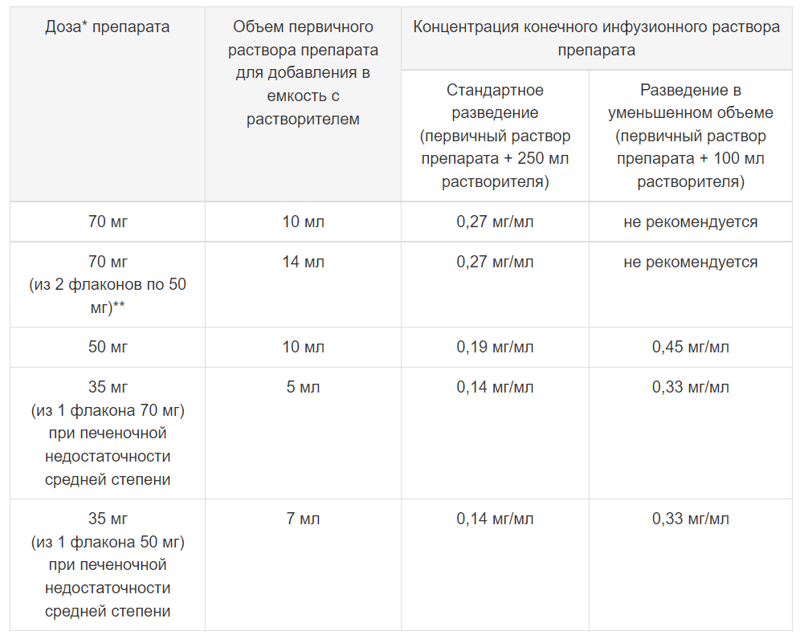
* во флакон с препаратом всегда добавляют 10,8 мл растворителя независимо от его дозы (50 мг или 70 мг);
** при отсутствии флакона по 70 мг дозу можно приготовить из 2 флаконов по 50 мг.
Приготовление раствора препарата для внутривенных инфузий детям
Определение площади поверхности тела (ППТ) для расчета дозы у детей
Перед приготовлением инфузионного раствора необходимо рассчитать площадь поверхности тела (ППТ) ребенка по следующей формуле (формула Мостеллера):

Подготовка препарата для введения детям в возрасте старше 3 месяцев (используя флакон 70 мг)
1. Определяют необходимую для данного ребенка нагрузочную дозу, используя ППТ (рассчитанную как описано выше) и следующее уравнение:
ППТ (м²) × 70 мг/м² = Нагрузочная доза
Максимальная нагрузочная доза в первый день лечения не должна превышать 70 мг, независимо от расчетной дозы для данного пациента.
2. Перед разведением холодный флакон с препаратом необходимо согреть до комнатной температуры.
3. С соблюдением правил асептики добавляют 10,5 мл одного из следующих совместимых растворителей: стерильная вода для инъекций, 0,9% раствор натрия хлорида для инфузий, бактериостатическая вода для инъекций с метилпарабеном, пропилпарабеном или бактериостатическая вода для инъекций с 0,9% бензиновым спиртом. Концентрация каспофунгина в первичном растворе препарата составит 7,2 мг/мл.
Приготовленный с использованием стерильной воды для инъекций или 0,9% раствора натрия хлорида первичный раствор препарата можно хранить во флаконе до 24 часов в холодильнике (2-8 °С). Первичный раствор препарата, приготовленный с использованием других совместимых растворителей, следует использовать сразу после приготовления.
4. Извлекают из флакона объем первичного раствора препарата, равный рассчитанной нагрузочной дозе (пункт 1). В асептических условиях переносят этот объем (мл) в емкость для внутривенных инфузий, содержащую 250 мл 0,9%, 0,45% или 0,225% раствора натрия хлорида для инъекций, либо раствор Рингера с лактатом для инъекций. При необходимости объем добавляемого растворителя может быть уменьшен так, чтобы итоговая концентрация каспофунгина в готовом конечном инфузионном растворе препарата не превышала 0,5 мг/мл.
Готовый конечный инфузионный раствор препарата, приготовленный с использованием 0,9% раствора натрия хлорида, следует использовать в течение 48 часов, если он хранится в холодильнике (2-8 °С). Готовый конечный инфузионный раствор препарата, приготовленный с использованием других совместимых растворителей, следует использовать сразу после приготовления.
5. Если величина нагрузочной дозы, определенная по приведенной выше формуле, составляет менее 50 мг, тогда можно приготовить инфузионный раствор из флакона 50 мг (см. ниже пункты 2-4 раздела «Подготовка препарата для введения детям в возрасте старше 3 месяцев (используя флакон 50 мг)»). При использовании флакона 50 мг концентрация каспофунгина в первичном растворе препарата составит 5,2 мг/мл.
Подготовка препарата для введения детям в возрасте старше 3 месяцев (используя флакон 50 мг)
1. Определяют необходимую для данного ребенка суточную поддерживающую дозу, используя ППТ (рассчитанную, как описано выше) и следующее уравнение:
ППТ (м²) × 50 мг/м² = Суточная поддерживающая доза
Суточная поддерживающая доза не должна превышать 70 мг, независимо от расчетной дозы для данного пациента.
2. Перед разведением холодный флакон с препаратом необходимо согреть до комнатной температуры.
3. С соблюдением правил асептики добавляют 10,5 мл одного из следующих совместимых растворителей: стерильная вода для инъекций, 0,9% раствор натрия хлорида для инфузий, бактериостатическая вода для инъекций с метилпарабеном, пропилпарабеном или бактериостатическая вода для инъекций с 0,9% бензиловым спиртом. Концентрация каспофунгина в первичном растворе препарата составит 5,2 мг/мл.
Приготовленный с использованием стерильной воды для инъекций или 0,9% раствора натрия хлорида первичный раствор препарата можно хранить во флаконе до 24 часов в холодильнике (2-8 °С). Первичный раствор препарата, приготовленный с использованием других совместимых растворителей, следует использовать сразу после приготовления.
4. Извлекают из флакона объем первичного раствора препарата, равный рассчитанной нагрузочной дозе (пункт 1). В асептических условиях переносят этот объем (мл) в емкость для внутривенных инфузий, содержащую 250 мл 0,9%, 0,45% или 0,225% раствора натрия хлорида для инъекций, либо раствор Рингера с лактатом для инъекций. При необходимости объем добавляемого растворителя может быть уменьшен так, чтобы итоговая концентрация каспофунгина в готовом конечном инфузионном растворе препарата не превышала 0,5 мг/мл.
Готовый конечный инфузионный раствор препарата, приготовленный с использованием 0,9% раствора натрия хлорида, следует использовать в течение 48 часов, если он хранится в холодильнике (2-8 °С). Готовый конечный инфузионный раствор препарата, приготовленный с использованием других совместимых растворителей, следует использовать сразу после приготовления.
5. Если вычисленная суточная поддерживающая доза составляет более 50 мг, то можно использовать флакон 70 мг (см. выше пункты 2-4 раздела «Подготовка препарата для введения детям в возрасте старше 3 месяцев (используя флакон 70 мг)»), при этом концентрация каспофунгина в первичном растворе препарата составит 7,2 мг/мл.
Побочное действие
Имеются отдельные сообщения о реакциях гиперчувствительности (анафилаксия и аллергические реакции) (см. раздел «Особые указания»).
У пациентов с инвазивным аспергиллезом были зарегистрированы отек легких, респираторный дистресс-синдром, инфильтраты на рентгенограмме.
У взрослых. В клинических исследованиях 1865 взрослых пациентов принимали однократную или многократные дозы каспофунгина: 564 пациента с фебрильной нейтропенией (исследование по эмпирической терапии), 382 пациента с инвазивным кандидозом, 228 пациентов с инвазивным аспергиллезом, 297 пациентов с локализованными инфекциями, вызванными Candida, и 394 пациента, зарегистрированных в 1 фазе исследований. В исследование по эмпирической терапии были включены пациенты, проходившие курс химиотерапии по поводу злокачественных новообразований, или пациенты после трансплантации гемопоэтических стволовых клеток (включая 39 случаев аллогенной трансплантации). В исследованиях, включавших пациентов с инфекциями, вызванными Candida, большинство пациентов с инвазивным кандидозом находились в тяжелом состоянии (например, онкогематологические заболевания или другие формы злокачественных новообразований, недавно перенесенная обширная хирургическая операция, ВИЧ), требующем применения сопутствующей комплексной лекарственной терапии. Пациенты с инфекциями, вызванными Aspergillus, часто находились в тяжелом состоянии (например, трансплантация костного мозга или периферических стволовых клеток, онкогематологическое заболевание, опухоли солидных органов или трансплантация органов), требующем применения сопутствующей комплексной лекарственной терапии.
У пациентов всех популяций частым побочным эффектом в месте введения был флебит, а также другие местные реакции, включая эритему, боль/болезненность, зуд и чувство жжения.
Выявленные побочные реакции, связанные с применением препарата, обычно имели легкое течение и редко требовали отмены препарата.
Зарегистрированные побочные эффекты классифицированы по частоте: очень часто (≥1/10), часто (≥1/100, <1/10) и нечасто (≥1/1000, <1/100).
Со стороны кроветворной и лимфатической системы: часто – снижение гемоглобина, снижение гематокрита, снижение числа лейкоцитов; нечасто – анемия, тромбоцитопения, коагулопатия, лейкопения, повышение числа эозинофилов, снижение числа тромбоцитов, повышение числа тромбоцитов, снижение числа лимфоцитов, повышение числа лейкоцитов, снижение числа нейтрофилов.
Со стороны обмена веществ и питания: часто – гипокалиемия; нечасто – гиперволемия, гипомагниемия, анорексия, нарушение электролитного баланса, гипергликемия, гипокальциемия, метаболический ацидоз.
Со стороны психики: нечасто – тревога, дезориентация, бессонница.
Со стороны нервной системы: часто – головная боль; нечасто – головокружение, нарушение вкуса, парестезия, сонливость, тремор, гипестезия.
Со стороны органа зрения: нечасто – желтушность склер, нечеткость зрения, отек век, повышенное слезотечение.
Со стороны сердца: нечасто – ощущение сердцебиения, тахикардия, аритмия, фибрилляция предсердий, застойная сердечная недостаточность.
Со стороны сосудов: часто – флебит; нечасто – тромбофлебит, гиперемия («прилив крови»), повышение артериального давления, снижение артериального давления.
Со стороны дыхательной системы, органов грудной клетки и средостения: часто – одышка; нечасто – заложенность носа, боль в горле, учащенное дыхание, бронхоспазм, кашель, пароксизмальная ночная одышка, гипоксия, хрипы, свистящее дыхание.
Со стороны желудочно-кишечного тракта: часто – тошнота, диарея, рвота; нечасто – боль в животе, боль в верхней части живота, ощущение сухости во рту, диспепсия, ощущение дискомфорта в желудке, вздутие живота, асцит, запор, затрудненное глотание, метеоризм.
Со стороны печени и желчевыводящих путей: часто – повышение функциональных показателей печени (аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (ACT), щелочная фосфатаза, прямой и непрямой билирубин); нечасто – холестаз, гепатомегалия, гипербилирубинемия, желтуха, нарушение функции печени, гепатотоксичность, поражение печени.
Со стороны кожи и подкожных тканей: часто – сыпь, зуд, эритема, повышенная потливость; нечасто – мультиформная эритема, макулезная сыпь, макулопапулезная сыпь, зудящая сыпь, крапивница, аллергический дерматит, генерализованный зуд, эритематозная сыпь, генерализованная сыпь, кореподобная сыпь, поражение кожи.
Со стороны скелетно-мышечной и соединительной ткани: часто – артралгия; нечасто – боль в спине, боль в конечности, боль в костях, мышечная слабость, миалгия.
Со стороны почек и мочевыводящих путей: нечасто – почечная недостаточность, острая почечная недостаточность.
Общие расстройства и нарушения в месте введения: часто – лихорадка, озноб, зуд в месте введения; нечасто – боль, боль в месте введения, утомление, ощущение холода, ощущение жара, эритема в месте введения, уплотнение в месте введения, припухлость в месте введения, флебит в месте введения, периферический отек, слабость, ощущение дискомфорта в грудной клетке, боль в грудной клетке, отек лица, ощущение изменения температуры тела, уплотнение, экстравазация в месте введения, раздражение в месте введения, сыпь в месте введения, крапивница в месте введения, отек в месте введения, недомогание, отек.
Лабораторные и инструментальные данные: часто – уменьшение содержания калия в крови, уменьшение концентрации альбумина в крови; нечасто – повышение концентрации креатинина в крови, наличие эритроцитов в моче, уменьшение концентрации общего белка, наличие белка в моче, увеличение или уменьшение протромбинового времени, увеличение или уменьшение содержания натрия в крови, увеличение или уменьшение содержания кальция в крови, уменьшение или увеличение содержания хлоридов в крови, увеличение концентрации глюкозы в крови, уменьшение содержания магния в крови, уменьшение или увеличение содержания фосфора в крови, увеличение концентрации мочевины в крови, увеличение активности гамма-глутамилтрансферазы, увеличение частичного тромбопластинового времени, уменьшение содержания гидрокарбонатов в крови, увеличение содержания калия в крови, увеличение артериального давления, уменьшение концентрации мочевой кислоты в крови, патологические дыхательные шумы, снижение концентрации углекислого газа, повышение концентрации иммуносупрессивных препаратов, увеличение международного нормализованного соотношения, цилиндрурия, наличие лейкоцитов в моче, повышение pH мочи.
В исследованиях применения каспофунгина в суточной дозе 150 мг (до 51 дня) принимали участие 100 взрослых пациентов. Проводилась сравнительная оценка применения каспофунгина в суточной дозе 50 мг (с использованием нагрузочной дозы 70 мг в первый день) и в суточной дозе 150 мг при лечении инвазивного кандидоза. Профиль безопасности каспофунгина в высокой дозе в целом сопоставим с таковым при применении препарата в суточной дозе 50 мг. В обеих группах пропорциональное соотношение числа пациентов с серьезными побочными эффектами, связанными с применением препарата, или с побочными эффектами, приведшими к отмене применения препарата, было сопоставимым.
У детей. Данные 5 клинических исследований с участием 171 ребенка указывают, что общая частота побочных эффектов (26,3%; 95% доверительный интервал – 19,9; 33,6) не превышала таковую при лечении каспофунгином взрослых пациентов (43,1%; 95% доверительный интервал – 40,0; 46,2). Однако в сравнении со взрослыми пациентами дети имеют иной профиль побочных эффектов. Наиболее частыми побочными реакциями, зафиксированными при применении каспофунгина у детей, были лихорадка (11,7%), сыпь (4,7%) и головная боль (2,9%).
Зарегистрированные побочные эффекты классифицированы по частоте: очень часто (≥1/10), часто (≥1/100, <1/10).
Со стороны кроветворной и лимфатической системы: часто – повышение числа эозинофилов.
Со стороны нервной системы: часто – головная боль.
Со стороны сердца: часто – тахикардия.
Со стороны сосудов: часто – гиперемия, снижение артериального давления.
Со стороны печени и желчевыводящих путей: часто – повышение активности «печеночных» ферментов в плазме крови (аланинаминотрансферазы, аспартатаминотрансферазы).
Со стороны кожи и подкожных тканей: часто – сыпь, зуд.
Общие расстройства и нарушения в месте введения: очень часто – лихорадка; часто – озноб, боль в месте введения.
Лабораторные и инструментальные данные: часто – уменьшение содержания калия в крови, уменьшение содержания магния в крови, увеличение концентрации глюкозы в крови, уменьшение содержания фосфора в крови, увеличение содержания фосфора в крови.
Пострегистрационный опыт применения
В пострегистрационной практике сообщалось о следующих нежелательных эффектах:
Со стороны печени и желчевыводящих путей: нарушение функции печени.
Со стороны кожи и подкожных тканей: токсический эпидермальный некролиз, синдром Стивенса-Джонсона.
Общие расстройства и нарушения в месте введения: припухлость и периферический отек.
Лабораторные и инструментальные данные: увеличение содержания кальция в крови, повышение активности гамма-глутамилтрансферазы.
Передозировка
В клинических исследованиях хорошо переносилась самая высокая из испытанных доз – однократная разовая доза 210 мг (6 здоровых добровольцев).
Также была показана хорошая переносимость препарата при его введении в суточной дозе 150 мг в течение 51 дня (100 здоровых добровольцев).
При передозировке каспофунгина диализ не показан (не удаляется при диализе).
Взаимодействие с другими лекарственными средствами
В исследованиях in vitro установлено, что каспофунгин не является ингибитором какого либо фермента системы цитохрома Р450 (CYP), а также не является индуктором метаболизма других препаратов, опосредованного изоферментами CYP3A4. В клинических исследованиях установлено, что каспофунгин не является субстратом для Р-гликопротеина и представляет собой слабый субстрат для ферментов цитохрома Р450.
В двух клинических исследованиях у взрослых пациентов циклоспорин (однократная доза 4 мг/кг или две дозы 3 мг/кг) увеличивал AUC каспофунгина приблизительно на 35%. Увеличение AUC, вероятно, связано с уменьшением печеночной экстракции каспофунгина. Каспофунгин не увеличивал концентрацию циклоспорина в плазме крови. При совместном применении этих препаратов было отмечено транзиторное повышение активности ACT и АЛТ. В ретроспективном исследовании 40 пациентов, принимавших каспофунгин и/или циклоспорин длительностью до 290 дней (в среднем 17,5 дней), не было отмечено серьезных нежелательных явлений со стороны печени (см. раздел «Особые указания»).
В клинических исследованиях у взрослых здоровых добровольцев установлено, что итраконазол, амфотерицин В, микофенолата мофетил, нелфинавир или такролимус не оказывают влияния на фармакокинетику каспофунгина. В свою очередь каспофунгин не оказывает влияния на фармакокинетические показатели итраконазола, амфотерицина В, рифампицина или активных метаболитов микофенолата мофетила.
Каспофунгин снижает показатель 12-часовой концентрации (С12час) в крови такролимуса на 26%. У пациентов, получающих оба препарата, рекомендуется контролировать концентрацию такролимуса в крови и при необходимости корректировать его дозу.
Результаты двух клинических исследований взаимодействий лекарственных препаратов у взрослых здоровых добровольцев показывают, что рифампицин может как ускорять, так и замедлять распределение каспофунгина. В одном из исследований рифампицин и каспофунгин назначали в течение 14 дней одновременно с первого дня лечения. Отмечалось преходящее увеличение концентрации каспофунгина в плазме крови в первый день (увеличение AUC приблизительно на 60%). Во втором исследовании первоначально назначали только рифампицин в течение 14 дней до достижения равновесной концентрации препарата в плазме крови, а затем в течение еще 14 дней оба препарата применяли одновременно. Наблюдался обратный эффект: на этапе равновесной концентрации рифампицина было отмечено лишь незначительное изменение AUC каспофунгина или его концентрации в момент завершения инфузии, однако остаточная концентрация каспофунгина снижалась приблизительно на 30%.
Кроме того, результаты фармакокинетического скрининга у взрослых пациентов показывают, что одновременное применение каспофунгина с индукторами клиренса лекарственных препаратов (эфавиренз, невирапин, фенитоин, дексаметазон или карбамазепин) может приводить к клинически значимому снижению концентрации каспофунгина. Имеющиеся данные свидетельствуют о том, что индуцированное этими препаратами снижение концентрации каспофунгина происходит скорее за счет ускорения элиминации, нежели метаболизма. Поэтому у взрослых пациентов при одновременном применении каспофунгина с эфавирензом, нелфинавиром, невирапином, рифампицином, дексаметазоном, фенитоином или карбамазепином следует рассмотреть возможность сохранения суточной дозы каспофунгина 70 мг, не снижая ее после нагрузочной дозы 70 мг, назначаемой в первые сутки лечения. У детей результаты регрессивного анализа фармакокинетических данных показывают, что совместное применение дексаметазона и каспофунгина может сопровождаться клинически значимым снижением пороговой концентрации каспофунгина. Эти данные могут указывать на то, что при одновременном применении с индукторами клиренса лекарственных препаратов у детей будет отмечаться такое же снижение концентрации каспофунгина, как и у взрослых пациентов. Одновременное назначение с каспофунгином индукторов клиренса лекарственных препаратов (рифампицин, эфавиренз, невирапин, фенитоин, дексаметазон или карбамазепин) у детей, как и у взрослых, требует увеличения суточной дозы до 70 мг/м² (суточная доза не должна превышать 70 мг, независимо от величины расчетной дозы для данного пациента).
Особые указания
При применении каспофунгина наблюдались случаи возникновения анафилаксии. При развитии анафилаксии применение препарата должно быть прекращено и назначено соответствующее лечение. Имеются отдельные сообщения об аллергических реакциях, включающих сыпь, отек лица, ангионевротический отек, зуд, ощущение жара и бронхоспазм, при возникновении которых может потребоваться прекращение применения препарата и/или назначение соответствующего лечения.
Случаи развития синдрома Стивенса-Джонсона и токсического эпидермального некролиза были зарегистрированы в ходе пострегистрационного мониторинга применения каспофунгина. Препарат следует применять с осторожностью у пациентов с аллергическими реакциями со стороны кожи в анамнезе.
Одновременное применение каспофунгина и циклоспорина изучалось на взрослых здоровых добровольцах и взрослых пациентах. У некоторых здоровых взрослых добровольцев, принимавших две дозы циклоспорина 3 мг/кг с каспофунгином, наблюдалось транзиторное повышение активности АЛТ и ACT (не более чем в 3 раза по сравнению с верхней границей нормы), которое исчезало при отмене препаратов. Также при одновременном применении каспофунгина и циклоспорина наблюдалось увеличение показателя AUC для каспофунгина приблизительно на 35% без изменения концентрации циклоспорина. В ретроспективном исследовании 40 пациентов, которым каспофунгин и циклоспорин одновременно назначались в течение 1-290 дней (в среднем 17,5 дней), не было отмечено серьезных нежелательных явлений со стороны печени. Как и следовало ожидать, у пациентов с аллогенной трансплантацией гемопоэтических стволовых клеток или трансплантацией цельного органа отклонения со стороны «печеночных» ферментов встречались в большинстве случаев, однако ни у одного пациента не было отмечено повышения активности АЛТ, связанного с применением препарата. Повышение активности ACT, возможно связанное с терапией каспофунгином и/или циклоспорином, было отмечено у 5 пациентов, но во всех случаях не более чем в 3,6 раза по сравнению с верхней границей нормы. У 4 пациентов препарат был отменен в связи с отклонениями показателей активности «печеночных» ферментов по различным причинам. Из них 2 случая отмены могли быть обусловлены как терапией каспофунгином и/или циклоспорином, так и другими возможными причинами. В исследованиях инвазивного аспергиллеза принимали участие 6 взрослых пациентов, которым терапия каспофунгином и циклоспорином совместно проводилась в течение 2-56 дней; ни у одного из этих пациентов не отмечалось повышения активности «печеночных» ферментов. Полученные данные позволяют предположить, что каспофунгин может назначаться одновременно с циклоспорином в тех случаях, когда потенциальная польза такого назначения превышает возможный риск.
Влияние на способность управлять транспортными средствами, механизмами
Нет данных о влиянии препарата на способность управлять транспортными средствами и работать с механизмами.
Форма выпуска
Лиофилизат для приготовления концентрата для приготовления раствора для инфузий 50 мг, 70 мг.
50 мг, 70 мг действующего вещества во флаконы вместимостью 10 мл, 20 мл из бесцветного прозрачного стекла, герметично укупоренные пробками резиновыми, обжатые колпачками алюминиевыми или комбинированными.
1 или 5 флаконов с инструкцией по применению в пачке картонной.
10 флаконов с инструкцией по применению в коробке картонной.
Для стационаров: 50 флаконов с равным количеством инструкций по применению в коробке картонной.
Условия хранения.
В защищенном от света месте при температуре нс выше 8 °С.
Хранить в недоступном для детей месте.
Срок годности.
2 года.
Не применять по истечении срока годности.
Условия отпуска.
Отпускают по рецепту.
Производитель/Владелец регистрационного удостоверения/Организация, принимающая претензии от потребителей
ПАО «Красфарма», Россия, 660042, Красноярский край, г. Красноярск, ул. 60 лет Октября, зд. 2.
Производитель/Фасовщик (первичная упаковка)/Упаковщик (вторичная (потребительская) упаковка)
ПАО «Красфарма», Россия, Красноярский край, г. Красноярск, ул. 60 лет Октября, зд. 2/53.
Выпускающий контроль качества
ПАО «Красфарма», Россия, Красноярский край, г. Красноярск, ул. 60 лет Октября, зд. 2/13.
Комментарии
ПРАКТИКА ПЕДИАТРА
