Калетра таблетки 100/25 - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер:
ЛП-000116Торговое наименование:
КалетраМеждународное непатентованное или группировочное наименование:
Лопинавир + РитонавирЛекарственная форма:
Таблетки покрытые пленочной оболочкойСостав
Каждая таблетка содержит:
Активные вещества
Лопинавир - 100,0 мг, ритонавир - 25,0 мг;
Вспомогательные вещества
Коповидон К 28 - 426,9 мг; сорбитана лаурат - 41,95 мг; кремния диоксид коллоидный - 6,0 мг; второй слой: натрия стеарилфумарат - 6, 15 мг; кремния диоксид коллоидный - 4,0 мг; пленочное покрытие: Опадрай II розовый 85 F 14399 - 15,0 мг (поливиниловый спирт - 40,00 %, титана диоксид - 24,85 %, тальк - 14,80 %, макрогол 3350 - 20,20 %, краситель железа оксид красный Е 172 - 0,15 %).
Описание
Овальные таблетки, покрытые пленочной оболочкой бледно-розового цвета. На одной стороне таблетки выдавлены символы «АС» и 
Фармакотерапевтическая группа
Противовирусное (ВИЧ) средство
Код АТХ
J05ARI0
Фармакологические свойства
Фармакодинамика
Препарат Калетра® - это комбинированный препарат, который содержит в своем составе лопинавир и ритонавир.
Лопинавир является ингибитором протеазы ВИЧ-1 и ВИЧ-2 вируса иммунодефицита человека (ВИЧ) и обеспечивает противовирусную активность препарата. Препарат Калетра®, таблетки, покрытые пленочной оболочкой, производится по технологии MELTREX®с использованием вспомогательного вещества коповидон К 28 (от 65 до 75 вес %). Ингибирование ВИЧ протеаз препятствует синтезу белков вируса и предотвращает расщепление полипептида gag-pol, что приводит к образованию незрелого и неспособного к инфицированию вируса.
Влияние на показатели электрокардиограммы
В рандомизированном перекрестном исследовании с контролем по плацебо и активному препарату (моксифлоксацин 400 мг 1 раз в сутки) у 39 здоровых взрослых добровольцев проводилась оценка влияния препарата на интервал QTcF, включавшая 10 измерений в течение 12 ч на 3-й день исследования. Максимальная средняя величина различия в интервале QTcF (верхняя граница 95 % доверительного интервала) по сравнению с группой плацебо, составила 3,6 (6,3) и 13,1 (15,8) для групп, получающих дозу 400/100 мг 2 раза в сутки и дозу, превышающую терапевтическую (800/200 мг 2 раза в сутки) лопинавира/ритонавира соответственно. Удлинение интервала QRS на 6-9,5 мс при приеме высоких доз лопинавира/ритонавира (800/200 мг 2 раза в сутки) способствует удлинению интервала QT. На 3 день приема препаратов этот показатель был примерно в 1,5 раза и 3 раза выше, чем при рекомендованном приеме LPV/r 1 или 2 раза в сутки в равновесном состоянии. Ни у одного из пациентов не наблюдалось увеличения интервала QTcF более чем на 60 мс от исходного значения или интервала QTcF, превышающего потенциально клинически значимый порог 500 мс.
На 3 день того же исследования у испытуемых, получавших лопинавир/ритонавир, также было отмечено умеренное удлинение интервала PR. Среднее изменение интервала PR относительно исходного составляло 11,6-24,4 мс в течение 12-часового интервала после приема дозы. Максимальный интервал PR составил 286 мс, а блокады сердца второй или третьей степени не наблюдалось (см. раздел Особые указания).
Противовирусная активность in vitro
Противовирусная активность лопинавира in vitro против лабораторных штаммов ВИЧ и клинических изолятов ВИЧ была изучена на остро инфицированных лимфобластных клеточных линиях и лимфоцитах периферической крови соответственно. В отсутствие сыворотки крови человека среднее значение IС50 лопинавира в отношении 5 различных лабораторных штаммов ВИЧ-1 составило 19 нМ. В отсутствие и в присутствии 50% сыворотки крови человека среднее значение IC50 лопинавира в отношении ВИЧ-IIIIВ в МТ4-клетках составило 17 нМ и 102 нМ соответственно. В отсутствие сыворотки крови человека среднее значение IC50 лопинавира в отношении нескольких клинических изолятов ВИЧ-1 составило 6,5 нМ.
Резистентность
Выделение резистентных штаммов in vitro
ВИЧ-1 изоляты со сниженной чувствительностью к лопинавиру были выделены in vitro. ВИЧ-1 был пассирован in vitro отдельно с лопинавиром или комбинацией лопинавира с ритонавиром в концентрациях, эквивалентных концентрациям в плазме, наблюдаемым при лечении препаратом Калетра® Генотипический и фенотипический анализ выделенных в этих пассажах вирусов, показывает, что присутствие ритонавира при таком соотношении концентрации не оказывает значительного влияния на выделение резистентных к лопинавиру вирусов.
В целом, изучение in vitro характеристик фенотипичной перекрестной резистентности между лопинавиром и другими ингибиторами протеазы дает основания полагать, что снижение чувствительности к лопинавиру тесно связано со снижением чувствительности к ритонавиру и индинавиру, но не сопряжено со снижением чувствительности к ампренавиру, саквинавиру и нелфинавиру.
Анализ резистентности у пациентов, ранее не получавших антиретровирусную терапию
В клинических исследованиях с ограниченным числом проанализированных штаммов не было отмечено селективной резистентности к лопинавиру у пациентов, ранее не получавших антиретровирусную терапию без выраженной резистентности к ингибиторам протеазы в начале исследования.
Анализ резистентности у пациентов, получавших лечение ингибиторами протеазы (ИП)
Возникновение резистентности к лопинавиру у пациентов, прошедших безуспешно лечение ингибиторами протеазы, изучалось на основе изолятов, выделенных в ходе проспективного наблюдения у 19 пациентов, получавших ингибиторы протеазы, в двух исследованиях II фазы и одном исследовании III фазы. У пациентов наблюдалась неполная супрессия вируса или феномен вирусной отдачи, возобновление симптомов, являющийся результатом первоначального ответа на препарат Калетра" и показавший нарастающую резистентность in vitro между исходным уровнем и отдачей (определяется как возникновение новых мутаций или двукратное изменение фенотипической чувствительности к лопинавиру). Нарастающая резистентность была свойственна пациентам, характеризовавшимся наличием исходных штаммов, претерпевших несколько мутаций при лечении ингибиторами протеазы, при не более чем в 40 раз сниженной изначальной чувствительностью к лопинавиру. Наиболее часто проявляются мутации V82A, 154V и M46I. Также наблюдались мутации L33F, 150V и V321 в сочетании с 147V/A. У 19 штаммов отмечено 4,3-кратное увеличение IC50 по сравнению с исходными штаммами (6,2-43-кратное изменение по сравнению с вирусом дикого типа).
Существует генотипическая корреляция снижения фенотипической чувствительности к лопинавиру у вирусов, выделенных после лечения другими ингибиторами протеазы. Была проведена оценка противовирусной активности лопинавира in vitro в отношении 112 клинических изолятов, выделенных у пациентов, безуспешно прошедших лечение одним или несколькими ингибиторами протеазы. В пределах данной группы следующие мутации в протеазе ВИЧ были связаны со снижением in vitro чувствительности к лопинавиру: L10F/I/R/V, K20M/R, L24I, M46I/L, F53L, I54L/T/V, L63P, А711 L/T/V, V82A/F/T, 184V и L90M. Медиана ЕС50 лопинавира в отношении изолятов с мутациями 0-3, 4-5, 6-7 и 8-10 в вышеуказанных аминокислотных позициях была в 0,8, 2,7, 13,5 и 44,0 раза выше, чем ЕС50 в отношении дикого типа вируса ВИЧ соответственно. Все 16 типов вируса, у которых отмечено повышение чувствительности более чем в 20 раз, имели мутации в позициях 10, 54, 63 и 82 и (или) 84. Кроме того, медиана числа мутаций в аминокислотных позициях 20, 24, 46, 53, 71 и 90 составила 3. Дополнительно к вышеуказанным мутациям, мутации V32I и I47A были отмечены у характеризующихся рецидивами штаммов со сниженной чувствительностью к лопинавиру у пациентов, прошедших лечение ингибиторами протеазы и получающих лечение препаратом Калетра®. У пациентов, принимавших препарат Калетра®, были выявлены мутации I47A и L76V у рецидивирующих штаммов со сниженной чувствительностью к лопинавиру.
Оценка важности отдельных мутаций или наборов мутаций может меняться с получением дополнительных данных. Рекомендуется всегда консультироваться по поводу текущей системы оценки результатов исследований резистентности.
Противовирусная активность препарата Калетра® у пациентов, безуспешно прошедших лечение ингибиторами протеазы
Клиническая значимость снижения чувствительности к лопинавиру in vitro исследовалась методом оценки вирусологического ответа на лечение препаратом Калетра" с учетом исходного вирусного генотипа и фенотипа у 56 пациентов, не получивших положительного эффекта от лечения различными ингибиторами протеазы. ЕС50 лопинавира в отношении 56 исходных вирусных изолятов превысило ЕС50 в отношении дикого типа ВИЧ в 0,6-96 раз. После 48 недель лечения препаратом Калетра® эфавирензом и нуклеозидными ингибиторами обратной транскриптазы уровень в плазме РНК ВИЧ составил ≤ 400 копий/мл у 93 % (25/27), 73 % (11/15), и 25 % (2/8) пациентов с менее чем 10-кратным, 10-40-кратным и более чем 40-кратным снижением чувствительности к лопинавиру соответственно по сравнению с исходным уровнем.
Кроме того, вирусологический ответ наблюдался у 91 % (21/23), 71 % (15/21) и 33 % (2/6) пациентов с 0-5, 6-7 и 8-10 мутациями из вышеуказанного списка мутаций в протеазе ВИЧ, связанными со снижением чувствительности к лопинавиру in vitro. Поскольку эти пациенты ранее не получали лечение лопинавиром/ритонавиром или эфавирензом, частично эффект может быть приписан антивирусной активности эфавиренза, особенно для пациентов с высокорезистентным типом вируса. Исследование не включало контрольную группу пациентов, не получающих лечение препаратом Калетра®.
Перекрестная резистентность
Эффективность других ингибиторов протеазы против штаммов, выработавших нарастающую резистентность к лопинавиру после лечения препаратом Калетра" у принимавших ингибиторы протеазы пациентов: Наличие перекрестной резистентности к другим ингибиторам протеазы была проанализирована у 18 рецидивирующих штаммов, продемонстрировавших повышение резистентности к лопинавиру в течение трех исследований II фазы и одного исследования III фазы по изучению применения препарата Калетра® у пациентов, ранее получавших ингибиторы протеазы. Медиана IC50 лопинавира для этих 18 изолятов в исходном состоянии и при феномене вирусологической отдачи оказалась выше в диапазоне от 6,9 до 63 раз соответственно по сравнению с дикими типами вируса. Как правило, штаммы с вирусологической отдачей либо сохраняют (при исходной перекрестной резистентности), либо развивают существенную перекрестную резистентность к индинавиру, саквинавиру, атазанавиру. Умеренное снижение активности ампренавира было замечено при медиане кратности повышения IC50 от 3,7 до 8 для исходных и рецидивирующих штаммов соответственно. Штаммы сохранили чувствительность к типранавиру с медианой повышения IC50 на исходном уровне и при феномене вирусологической отдачи с кратностью 1,9 и 1,8 соответственно по сравнению с дикими типами вируса. Для получения дополнительной информации по типранавиру, включая генотипические показатели ответа при лечении резистентной к лопинавиру ВИЧ-1 инфекции следует обратиться к инструкции по применению для типранавира.
Фармакокинетика
Фармакокинетику лопинавира в комбинации с ритонавиром изучали у здоровых добровольцев и ВИЧ-инфицированных пациентов; существенных различий между двумя группами не выявили. Лопинавир практически полностью метаболизируется под действием изофермента CYP3A. Ритонавир ингибирует метаболизм лопинавира и вызывает увеличение его концентраций в плазме. При применении лопинавира/ритонавира в дозе 400/100 мг два раза в день средние равновесные концентрации лопинавира в плазме у ВИЧ-инфицированных пациентов в 15-20 раз превышали таковые ритонавира, а концентрация ритонавира в плазме составляла менее 7 % от концентрации при приеме ритонавира в дозе 600 мг два раза в день. ЕС50 лопинавира in vitro примерно в 10 раз ниже таковой ритонавира. Таким образом, противовирусная активность комбинации лопинавира и ритонавира определяется лопинавиром.
Всасывание
В фармакокинетическом исследовании с участием ВИЧ-положительных пациентов при приеме 400/100 мг лопинавира/ритонавира два раза в день совместно с пищей в течение 2 недель определено среднее значение максимальной концентрации лопинавира в плазме (Стах) 12,3 ± 5,4 мкг/мл, отмечающейся спустя приблизительно четыре часа после приема препарата. Средняя равновесная концентрация перед утренней дозой составляла 8,1 ± 5,7 мкг/мл. Площадь под кривой «концентрация-время» (AUC) лопинавира в течение 12 часов после приема препарата составляла в среднем 113,2 ± 60,5 мкг х ч/мл. Абсолютная биодоступность лопинавира в комбинации с ритонавиром в организме человека установлена не была.
Влияние пищи на всасывание при приеме внутрь
Прием однократной дозы 400/100 мг препарата Калетра® в лекарственной форме таблетки после приема пищи (высокой жирности, 872 ккал, из них 56 % поступили с жиром) не приводил к существенным изменениям Сmах и AUCinf по сравнению с приемом натощак. Поэтому препарат Калетра" в лекарственной форме таблетки можно принимать как с пищей, так и без нее.
Распределение
В равновесном состоянии приблизительно 98-99 % лопинавира находятся в связи с белками плазмы. Лопинавир связывается с альфа!-кислым гликопротеином (АКГ) и альбумином, однако, у лопинавира более высокое сродство к АКГ. В равновесном состоянии связывание лопинавира с белками плазмы остается постоянным в диапазоне зарегистрированных концентраций, создающихся после приема 400/100 мг лопинавира/ритонавира два раза в день, и является сопоставимым у здоровых добровольцев и ВИЧ-положительных пациентов.
Метаболизм
В исследованиях in vitro показано, что лопинавир преимущественно подвергается окислительному метаболизму с участием системы цитохрома Р450 гепатоцитов, в основном под воздействием изофермента CYP3A. Ритонавир - мощный ингибитор изофермента CYP3A, который ингибирует метаболизм лопинавира. что обеспечивает увеличение концентраций лопинавира в плазме крови. После однократного приема 400/100 мг лопинавира/ритонавира (с меченым 14С-лопинавиром), 89 % радиоактивности обеспечено исходным лекарственным препаратом. В организме человека было выявлено, по крайней мере, 13 окислительных метаболитов лопинавира. Ритонавир способен индуцировать изоферменты цитохрома Р450, что приводит к индукции его собственного метаболизма. В ходе длительного применения концентрации лопинавира перед приемом следующей дозы снижались со временем, стабилизируясь приблизительно через 10-14 дней.
Выведение
После приема 400/100 мг 14С-лопинавира/ритонавира через восемь дней приблизительно 10,4 ± 2,3 % и 82,6 ± 2,5 % от принятой дозы 14С-лопинавира обнаруживаются в моче и кале соответственно. При этом 2,2% и 19,8% от принятой дозы неизмененного лопинавира обнаруживаются в моче и кале соответственно. После длительного применения менее 3 % дозы лопинавира экскретируется в неизмененном виде через почки. Эффективный период полувыведения составляет в среднем 5-6 часов. Клиренс (CL/F) лопинавира при приеме внутрь составляет от 6 до 7 л/ч.
Прием один раз в день
Фармакокинетика лопинавира/ритонавира с кратностью приема один раз в день была оценена у ВИЧ-инфицированных пациентов, не получавших ранее антиретровирусную терапию. Лопинавир/ритонавир 800/200 мг применялся в комбинации с эмтрицитабином 200 мг и тенофовиром 300 мг один раз в день ежедневно. При длительном приеме 800/200 мг лопинавира/ритонавира один раз в день в течение 2 недель во время приема пищи средняя максимальная концентрация лопинавира в плазме (Сmах) составила 14,8 ± 3,5 мкг/мл и достигалась приблизительно через 6 часов после приема. Средняя равновесная концентрация лопинавира перед приемом утренней дозы составляла 5,5 ± 5,4 мкг/мл. AUC лопинавира при 24 часовом интервале приема составляла в среднем 206,5 ± 89,7 мкг ч/мл. При применении 1 раз в сутки происходит снижение Cmin/Ctrough на 50% по сравнению с режимом дозирования 2 раза в сутки.
Особые группы пациентов
Дети
Данные о фармакокинетике у детей в возрасте до 2 лет ограничены.
Была изучена фармакокинетика при приеме таблеток лопинавира/ритонавира 100/25 мг дважды в день, с режимом дозирования на основании массы тела без невирапина у 53 детей. Среднее значение лопинавира в равновесном состоянии AUC, Сmах и С12 составило 112,5 ± 37,1 мкг*ч / мл, 12,4 ± 3,5 мкг/мл и 5,71 ± 2,99 мкг/мл, соответственно.
Прием два раза в день с дозированием на основании массы тела без невирапина обеспечивает концентрацию лопинавира в плазме равную полученным данным у взрослых пациентов, принимавших 400/100 мг два раза в день без невирапина.
Пол, раса и возраст
Фармакокинетика лопинавира не была изучена у пожилых пациентов. Никаких зависящих от пола фармакокинетических различий у взрослых пациентов не наблюдалось. Никаких клинически значимых фармакокинетических различий, зависящих от расы, не установлено.
Беременность и послеродовой период
В открытом фармакокинетическом исследовании 12 ВИЧ-инфицированных беременных женщин, с менее 20 неделями беременности принимавших комбинированную антиретровирусную терапию первоначально получали лопинавир/ритонавир 400 мг / 100 мг (две таблетки 200/50 мг) два раза в день до гестационного возраста 30 недель. В 30 недель гестации доза была увеличена до 500/125 мг (две таблетки по 200/50 мг плюс одна таблетка по 100/25 мг) два раза в день, до того момента пока, не наступил период 2 недели до родов. Концентрации лопинавира в плазме крови измеряли в течение четырех 12-часовых периодов во втором триместре (20-24 недели беременности), третьем триместре до увеличения дозы (30 недель беременности), третьем триместре после увеличения дозы (32 недели беременности) и через 8 недель после родов. Увеличение дозы не привело к значительному увеличению концентрации лопинавира в плазме.
В другом открытом фармакокинетическом исследовании 19 ВИЧ-инфицированных беременных женщин получали лопинавир/ритонавир по 400/100 мг дважды в день в рамках комбинированной антиретровирусной терапии во время беременности и до зачатия. Для фармакокинетического анализа общего и несвязанного уровней концентрации лопинавира в плазме крови была собрана серия проб крови: в течение 12 часов в триместре 2 и триместре 3, при рождении и 4-6 недель после родов (у женщин, продолжавших лечение после родов). Фармакокинетические данные, полученные у ВИЧ-1-инфицированных беременных женщин, получающих таблетки, покрытые пленочной оболочкой, 400/100 мг лопинавир/ритонавир два раза в день, представлены в таблице ниже:
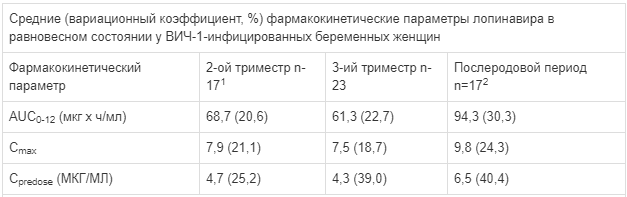 Cpredose - концентрация препарата в крови до приема очередной дозы.
Cpredose - концентрация препарата в крови до приема очередной дозы.
1- n=18 для Сmах
2 - n = 16 для Cpredose
Почечная недостаточность
Фармакокинетика лопинавира не была изучена у пациентов с почечной недостаточностью; однако, так как почечный клиренс лопинавира незначителен, снижения общего клиренса у пациентов с почечной недостаточностью не ожидается.
Печеночная недостаточность
В ходе сравнительного исследования фармакокинетические показатели лопинавира у ВИЧ-инфицированных пациентов с легкой и средней степенью печеночной недостаточности сравнивали с таковыми у ВИЧ-инфицированных пациентов с нормальной функцией печени при многократном применении лопинавира/ритонавира 400/100 мг дважды в сутки. Наблюдалось ограниченное увеличение общей концентрации лопинавира приблизительно на 30 %, что, предположительно, не имеет клинического значения.
Показания к применению
Лечение ВИЧ-инфекции у взрослых и детей от 3-х лет в составе комбинированной терапии.
Противопоказания
С осторожностью
Вирусный гепатит В и С.
Цирроз печени.
- Легкая и средней степени тяжести печеночная недостаточность.
Повышение активности «печеночных» ферментов.
Панкреатит.
Гемофилия А и В.
Дислипидемия (гиперхолестеринемия, гипертриглицеридемия).
Пожилой возраст (старше 65 лет). - Пациенты с органическими заболеваниями сердца, пациенты с расстройствами проводящей системы сердца в анамнезе или пациенты, принимающие препараты. удлиняющие интервал PR (такие как верапамил и атазанавир).
- Совместное применение не рекомендуется со следующими препаратами (см. разделы «Особые указания» и «Взаимодействие с другими лекарственными средствами»):
аторвастатин;
тадалафил (для лечения легочной гипертензии);
риоцигуат;
ворапаксар:
фузидовая кислота при костно-суставных инфекциях;
салметерол;
ривароксабан;
рифампицин;
флутиказон или другие глюкокортикоиды. которые метаболизируются СУРЗА4 (такие как будесонид и триамцинолон);
фосампренавир, фосампренавир/ритонавир;
типранавир/ритонавир;
кетоконазол (высокие дозы > 200 мг в день);
итраконазол (высокие дозы> 200 мг в день);
боцепревир;
симепревир;
телапревир.
Следует избегать совместного применения со следующими препаратами (см. разделы «Особые указания» и «Взаимодействие с другими лекарственными средствами»):
бедаквилин;
вориконазол;
ибрутиниб. - Следует применять с осторожностью со следующими препаратами (см. разделы «Особые указания» и «Взаимодействие с другими лекарственными средствами»):
дигоксин;
бепридил;
лидокаин;
хинидин;
кларитромицин;
эритромицин;
хлорфенирамин;
афатиниб;
церитиниб;
фенитоин;
карбамазепин;
фенобарбитал;
тразодон;
мидазолам (для парентерального введения);
силденафил, тадалафил (для лечения эректильной дисфункции);
розувастатин;
бозентан.
Применение при беременности и в период грудного вскармливания
Беременность
Как правило, при принятии решения использовать антиретровирусные препараты для лечения ВИЧ-инфекции у беременных женщин и, следовательно, для снижения риска вертикальной передачи ВИЧ новорожденному, необходимо учитывать данные исследований на животных, а также клинический опыт применения у беременных женщин для оценки безопасности и рисков для плода.
Лопинавир/ритонавир был изучен с участием 3000 беременных женщин, в том числе с участием более 1000 в течение первого триместра.
В пострегистрационном наблюдении при анализе Регистра по применению антиретровирусных препаратов во время беременности, утвержденном с января 1989 года, повышенный риск развития врожденных дефектов на фоне приема препарата Калетра® не был зарегистрирован среди более 1000 женщин, получавших препарат в течение первого триместра. Распространенность врожденных дефектов после применения лопинавира в течение любого триместра сравнима с распространенностью, наблюдаемой среди населения в целом. Не наблюдалось ни одной закономерности, указывающей на общую этиологию врожденных дефектов. В ходе исследований токсичности на животных было установлено токсическое воздействие на репродуктивную функцию. Основываясь на данных, указанных выше, такой риск маловероятен у людей. Применение лопинавира при беременности возможно только в том случае, когда предполагаемая польза для матери превосходит потенциальный риск для плода.
Период грудного вскармливания
В исследованиях на крысах показано, что лопинавир проникает в грудное молоко. Данные о выведении данного лекарственного препарата с женским молоком отсутствуют. ВИЧ-инфицированным женщинам не следует кормить грудью детей, чтобы избежать передачи ВИЧ-инфекции.
Фертильность
Исследования на животных не показали влияния препарата на фертильность. Данных касательно влияния лопинавира/ритонавира на фертильность у человека нет.
Способ применения и дозы
Внутрь, независимо от приема пищи. Таблетки препарата Калетра® следует проглатывать целиком, не разжевывая, не разламывая или измельчая.
Взрослые
Рекомендуемая пероральная доза препарата Калетра® составляет:
- По четыре таблетки препарата Калетра" 100/25 мг (400/100 мг) два раза в день независимо от приема пищи.
- По восемь таблеток препарата Калетра" 100/25 мг (800/200 мг) один раз в день независимо от приема пищи для пациентов, у которых выявлено менее 3-х мутаций, связанных с развитием резистентности к лопинавиру. Недостаточно данных для применения лопинавира/ритонавира один раз в день у взрослых пациентов с 3-мя и более мутациями, связанными с развитием резистентности к лопинавиру.
Сопутствующая терапия
Применение таблеток препарата Калетра" в сочетании с омепразолом и ранитидином не требует коррекции дозы.
У пациентов с подозреваемой пониженной чувствительностью к лопинавиру (показанной клинически или лабораторно), получавших ранее антиретровирусную терапию, в сочетании с эфавирензом, невирапином, ампренавиром или нелфинавиром необходимо увеличить дозу таблеток препарата Калетра" до 500/125 мг (5 таблеток по 100/25 мг) 2 раза в день. При одновременном применении с данными препаратами таблетки препарата Калетра® не следует назначать 1 раз в день.
Дети
Применение препарата Калетра" один раз в день пациентами детского возраста противопоказано.
Взрослая доза таблеток препарата Калетра" (400/100 мг дважды в день) без одновременного применения эфавиренза, невирапина, нелфинавира или ампренавира может применяться у детей с массой тела 35 кг и более или с площадью поверхности тела (ППТ) 1,4 м2 и более. Для определения дозы для детей с массой тела менее 35 кг или с ППТ от 0,6 до 1,4 м2 рекомендуется использовать приведенные ниже таблицы.
Для детей с ППТ менее 0,6 м2 или для детей младше 3-х лет существует раствор препарата Калетра® для приема внутрь.
Таблицы 1 и 2 содержат руководства по дозированию таблеток Калетра® препарата 100/25 мг, основанные на ППТ.
Таблица № 1
|
Принципы дозирования для детей, основанные на ППТ, без одновременного применения эфавиренза, невирапина, нелфинавира или ампренавира |
|
|
Площадь поверхности тела* (м2) |
Рекомендуемое количество таблеток по 100/25 мг при приеме два раза в день |
|
≥ 0,6 до <0,9 |
2 таблетки (200/50 мг) |
|
≥ 0,9 до <1,4 |
3 таблетки (300/75 мг) |
|
≥ 1,4 |
4 таблетки (400/100 мг) |
* Площадь поверхности тела может быть рассчитана по следующей формуле: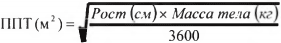
Таблица № 2
Принципы дозирования для детей, основанные на ППТ, при одновременном применении с препаратами эфавиренз, невирапин, нелфинавир или ампренавир | |
Площадь поверхности тела (м2) | Рекомендуемое количество таблеток по 100/25 мг при приеме два раза в день |
≥ 0,6 до 0,8 | 2 таблетки (200/50 мг) |
≥ 0,8 до 1,2 | 3 таблетки (300/75 мг) |
≥ 1,2 до 1,7 | 4 таблетки (400/100 мг) |
≥ 1,7 | 5 таблеток (500/125 мг) |
Таблицы № 3 и 4 содержат руководства по дозированию таблеток препарата Калетра® 100/25 мг по массе тела.
Таблица № 3
|
Принципы дозирования для детей по массе тела, без одновременного применения препаратов эфавиренз, невирапин, нелфинавир или ампренавир |
|
|
Масса тела (кг) |
Количество таблеток 100/25 мг для приема два раза в день |
|
От 7 до <15 кг |
Прием таблеток не рекомендуется. Следует применять раствор для приема внутрь. |
|
От 15 до 25 кг |
2 |
|
> 25 до 35 кг |
3 |
|
> 35 кг |
4# |
# Альтернативно, пациентам, которые могут проглотить большую таблетку, можно применять две таблетки 200/50 мг.
Таблица № 4
Принципы дозирования для детей по массе тела, при одновременном применении препаратов эфавиренз, невирапин, нелфинавир или ампренавир | |
Масса тела (кг) | Количество таблеток 100/25 мг для приема два раза в день |
От 7 до <15 кг | Прием таблеток не рекомендуется. Следует применять раствор для приема внутрь. |
От 15 до 20 кг | 2 |
> 20 до 30 кг | 3 |
> 30 до 45 кг | 4# |
> 45 кг | 5 |
# Альтернативно, пациентам, которые могут проглотить большую таблетку, можно применять две таблетки 200/50 мг.
Применение во время беременности и в послеродовом периоде
По данным ряда клинических исследований не требуется коррекции дозы препарата Калетра" во время беременности и в послеродовой период. Применение препарата один раз в день противопоказано у беременных женщин в связи с недостаточностью фармакокинетических и клинических данных.
Побочное действие
Краткий обзор профиля безопасности
Безопасность препарата Калетра® была изучена у более чем 2600 пациентов в клинических исследованиях П-IV фазы, из которых более 700 пациентов получали дозу 800/200 мг (6 капсул или 4 таблетки) 1 раз в сутки. Наряду с нуклеозидными ингибиторами обратной транскриптазы (НИОТ), в некоторых исследованиях препарат Калетра® назначался в сочетании с эфавирензом или невирапином.
Наиболее частыми нежелательными реакциями, связанными с лечением препаратом Калетра® во время клинических испытаний, были диарея, тошнота, рвота, гипертриглицеридемия и гиперхолестеринемия. При приеме препарата Калетра" 1 раз в сутки может быть повышен риск диареи. Диарея, тошнота и рвота могут возникать в начале лечения, в то время как гипертриглицеридемия и гиперхолестеринемия могут развиться позднее. Проявление нежелательных явлений привело к преждевременному прекращению лечения у 7 % пациентов в исследованиях II-IV фазы.
Важно отметить, что случаи панкреатита были зарегистрированы у пациентов, получающих препарат Калетра®, включая пациентов, у которых развилась гипертриглицеридемия. Кроме того, были зарегистрированы редкие случаи увеличения интервала PR в ходе лечения препаратом Калетра" (см. раздел «Особые указания»).
Перечень нежелательных реакций
Нежелательные реакции, обнаруженные в ходе клинических исследований и периода пострегистрационного наблюдения у взрослых пациентов и детей:
Следующие нежелательные явления были определены в качестве побочных действий. В категории, выделенные по частоте проявления, включены все сообщаемые нежелательные реакции от умеренных до тяжелых, независимо от индивидуальной оценки причинно-следственной связи. Побочные действия приводятся с разбиением по классам систем органов. По частоте проявления побочные действия представлены в порядке убывания серьезности: очень часто (≥ 1/10); часто (≥ 1/100 до < 1/10); нечасто (≥ 1/1000 до < 1/100): неизвестно (оценка не может быть проведена по имеющимся данным).Побочные действия, частота проявления которых неизвестна, были выявлены с помощью пострегистрационного наблюдения.
Таблица 1
Побочные действия, выявленные по данным клинических исследований и в период пострегистрационного наблюдения у взрослых пациентов
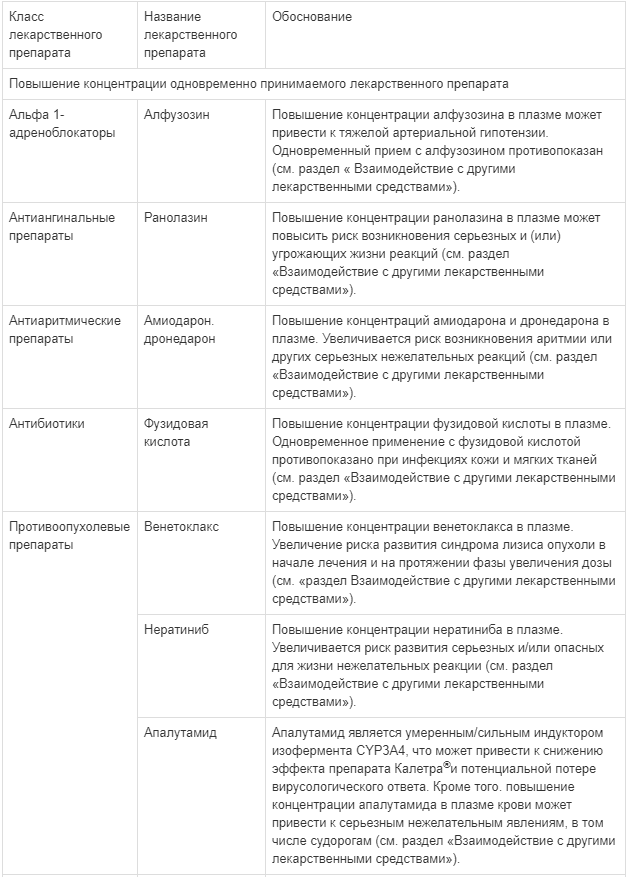
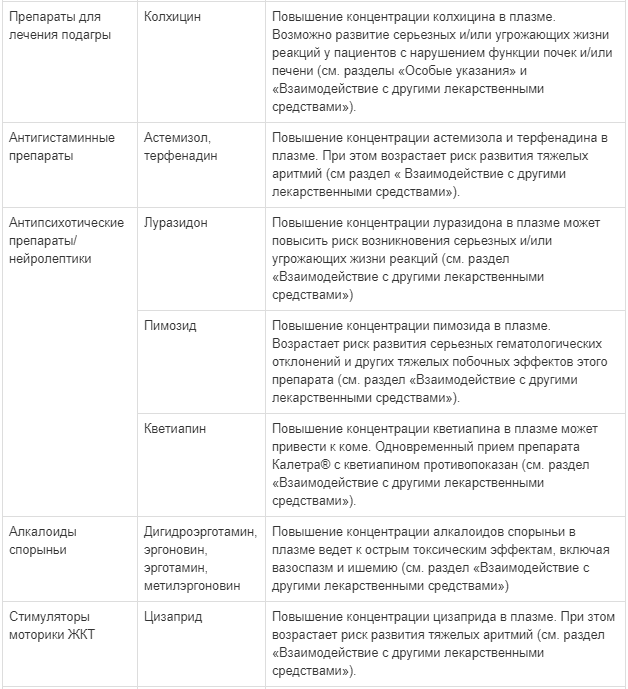
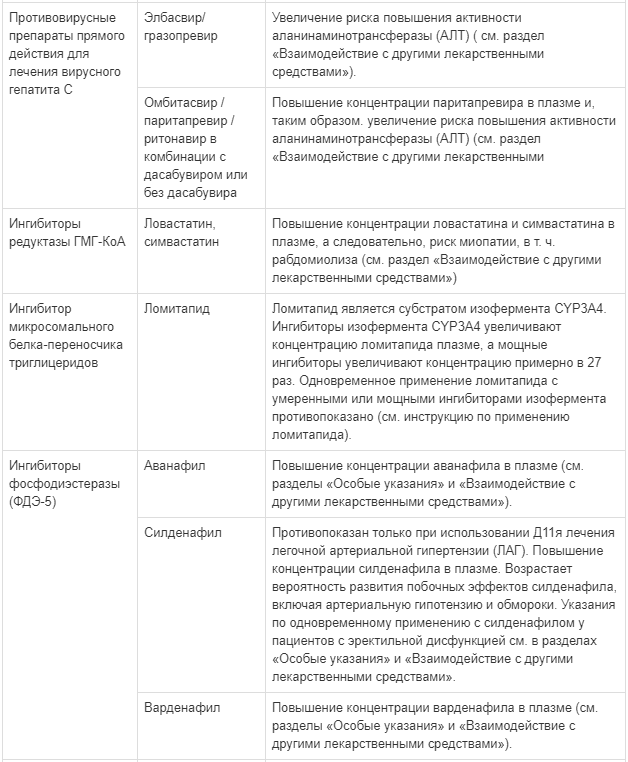
 1См. раздел «Особые указания»: панкреатит и липиды
1См. раздел «Особые указания»: панкреатит и липиды
Описание отдельных нежелательных реакций
Сообщалось о развитии синдрома Иценко-Кушинга у пациентов, получавших ритонавир совместно с флутиказона пропионатом в виде ингаляций или интраназально; такие явления могут наблюдаться и при использовании других глюкокортикостероидов, метаболизм которых осуществляется по пути Р450 ЗА, например, будесонида (см. раздел «Особые указания» и «Взаимодействие с другими лекарственными средствами»).
Повышение уровня креатинфосфокиназы (КФК), миалгия, миозит и редко рабдомиолиз были зарегистрированы с ингибиторами протеазы, особенно в сочетании с ингибиторами нуклеозидными ингибиторами обратной транскриптазы.
Показатели обмена веществ
Во время антиретровирусной терапии может возрастать масса тела и концентрация липидов и глюкозы крови (см. раздел «Особые указания»).
У ВИЧ-инфицированных пациентов с тяжелым иммунодефицитом на момент начала комбинированной антиретровирусной терапии (КАРТ) может развиваться воспалительная реакция на бессимптомные или остаточные оппортунистические инфекции. Также сообщается об аутоиммунных нарушениях (например, болезни Грейвса). Однако время до наступления таких нарушений варьирует, и они могут развиться много месяцев спустя после начала лечения (см. раздел «Особые указания»).
Поступали сообщения о случаях остеонекроза, особенно у пациентов с общепризнанными факторами риска, ВИЧ-инфекцией поздней стадии и продолжительной комбинированной антиретровирусной терапией (КАРТ). Частота развития остеонекроза не установлена (см. раздел «Особые указания»).
Применение у детей
У детей в возрасте 3 лет и старше профиль безопасности аналогичен профилю, наблюдаемому у взрослых (см. таблицу I выше).
Передозировка
В настоящее время клинический опыт острой передозировки лопинавиром/ритонавиром у людей ограничен. Специального антидота не существует. Лечение должно включать общую поддерживающую терапию, включая контроль основных показателей жизнедеятельности и наблюдение за клиническим статусом пациента. При необходимости удаляют неабсорбированный лекарственный препарат с помощью промывания желудка и назначают активированный уголь. Так как лопинавир/ритонавир в высокой степени связывается с белками плазмы крови, то применение диализа нецелесообразно.
Взаимодействие с другими лекарственными средствами
Препарат Калетра® содержит лопинавир и ритонавир. являющиеся ингибиторами изофермента СУРЗА цитохрома Р450 in vitro. Совместное применение препарата Калетра® и других лекарственных средств, преимущественно метаболизируемых изоферментом СУРЗА, может привести к повышению концентрации в плазме данных лекарственных средств, и, как следствие, к усилению или продлению их терапевтического эффекта и нежелательных реакций. Препарат Калетра® не ингибирует изоферменты CYP2D6. СУР2С9. СУР2С19, CYP2E1, СУР2В6 или СУР1А2 в клинически значимых концентрациях (см. раздел «Противопоказания»).
Было показано. что препарат Калетра® индуцирует свой собственный метаболизм in vivo и увеличивает биотрансформацию некоторых препаратов, метаболизирующихся ферментами цитохрома Р450 (включая изоферменты СУР2С9 и СУР2С19) и путем глюкуронизации. Это может привести к снижению концентрации препарата в плазме и вероятному снижению эффективности назначаемых совместно лекарственных средств.
Лекарственные препараты, которые противопоказаны в связи с ожидаемым увеличением взаимодействия и потенциальным развитием серьезных побочных эффектов, перечислены в разделе «Противопоказания».
Все исследования взаимодействий, если не сказано иное, проводили с применением капсул препарата Калетра®. прием которых приводил к системному воздействию лопинавира. приблизительно на 20 % более низкому. чем при применении таблеток в дозировке 200/50 мг.
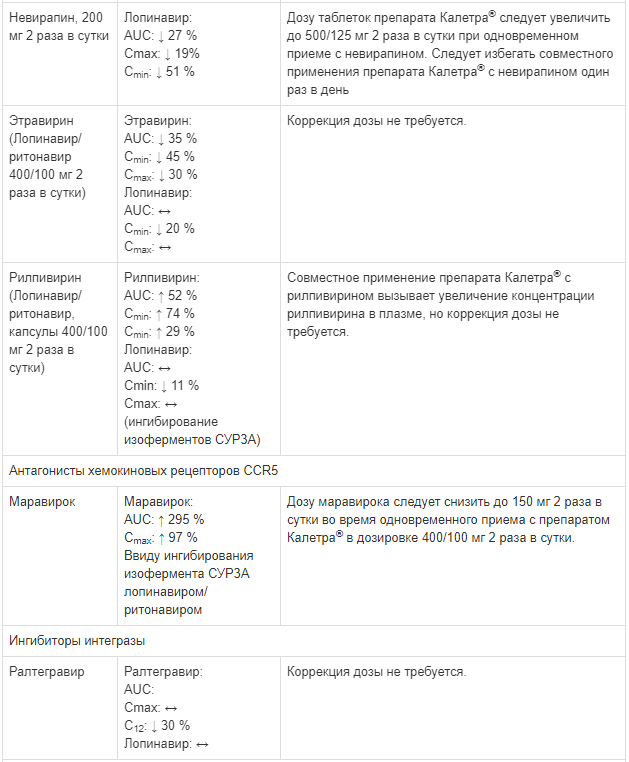
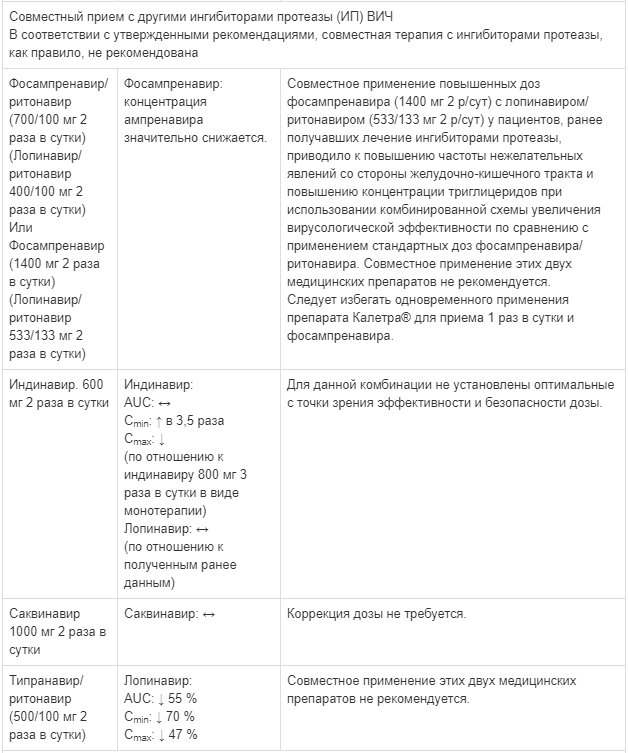
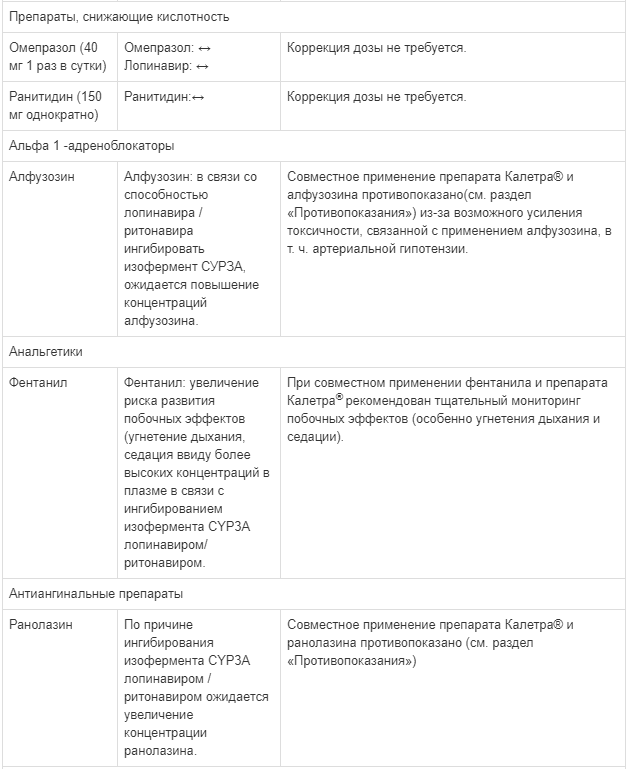
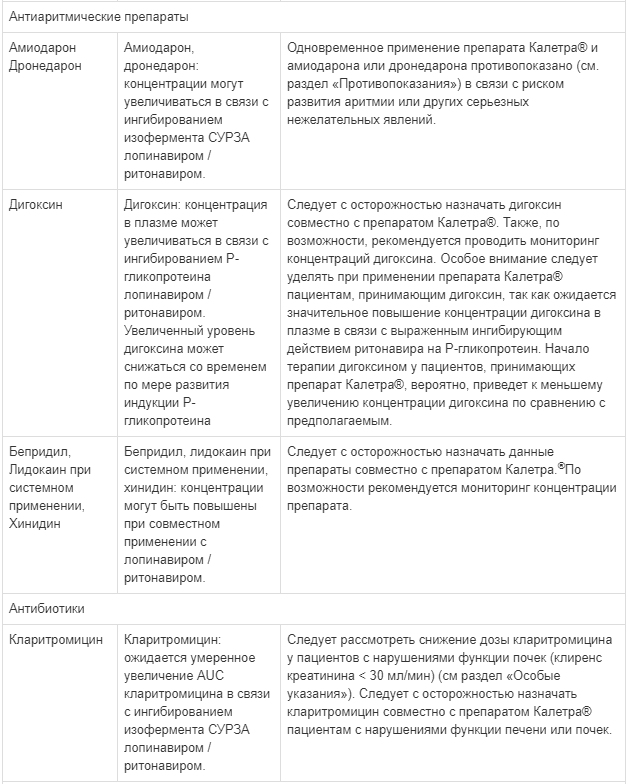
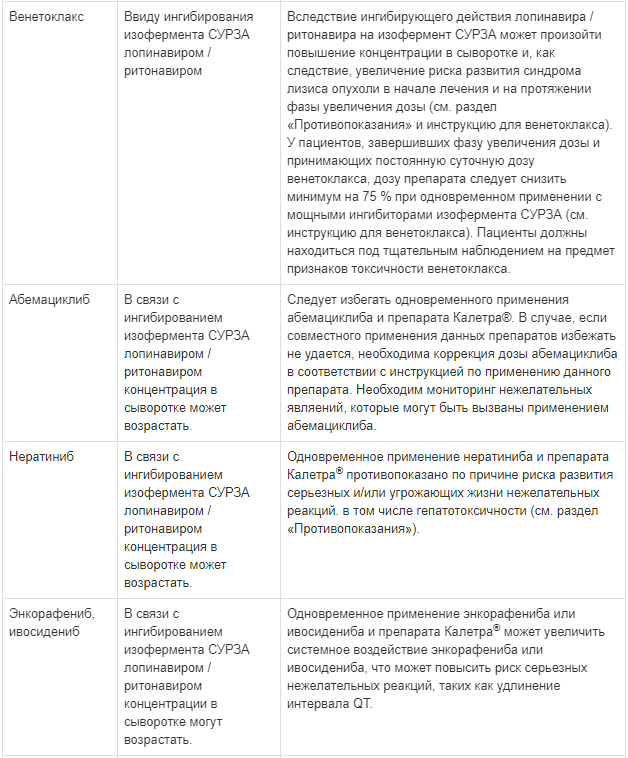
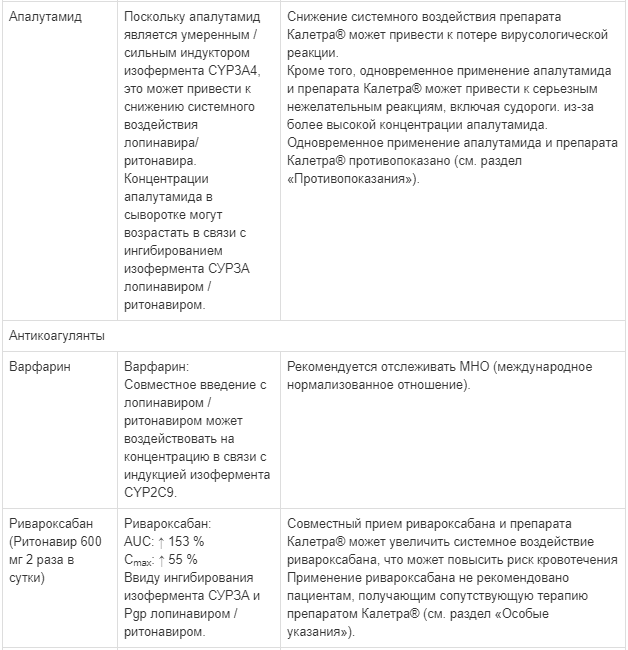
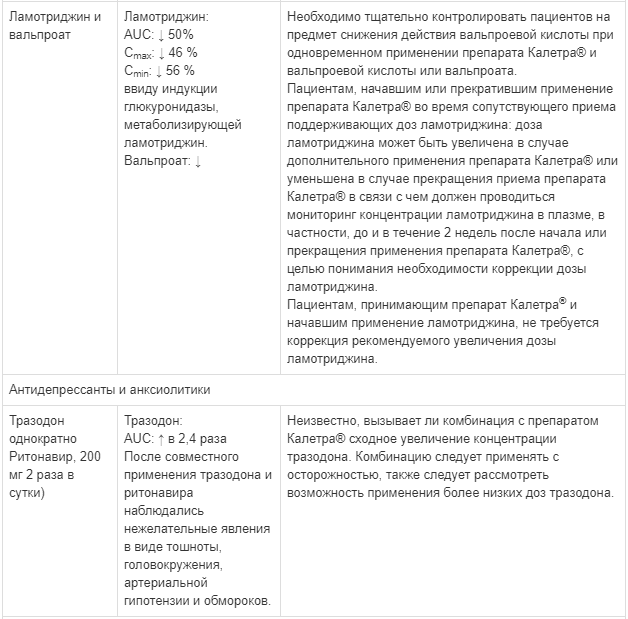
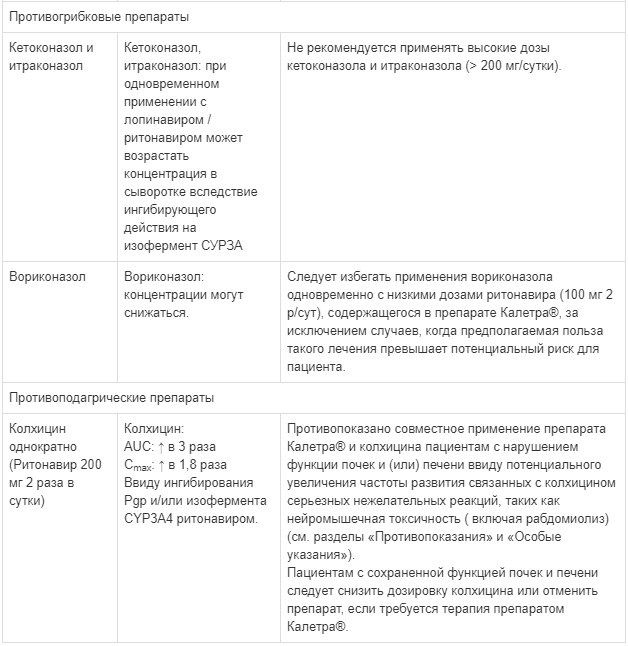
Известные и теоретически возможные взаимодействия с выбранным антиретровирусным препаратом и неантиретровирусными лекарственными средствами перечислены в таблице ниже.
Данные о лекарственных взаимодействиях
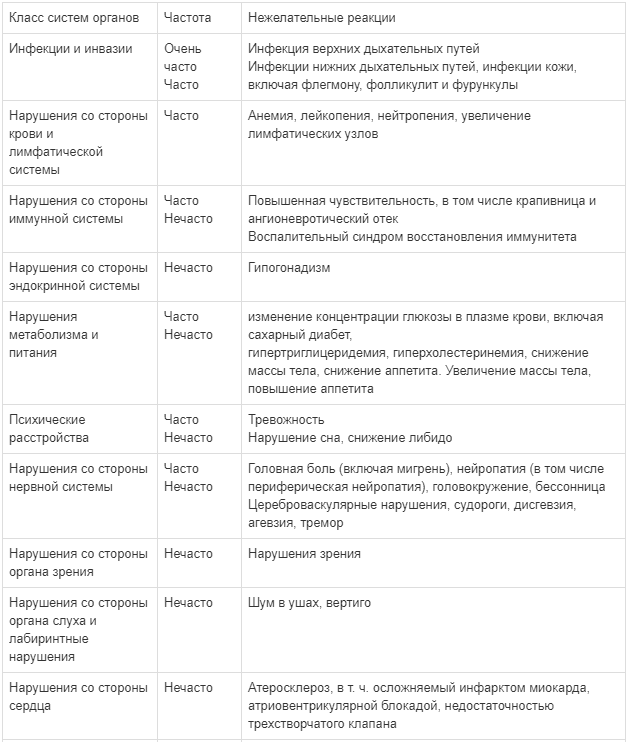
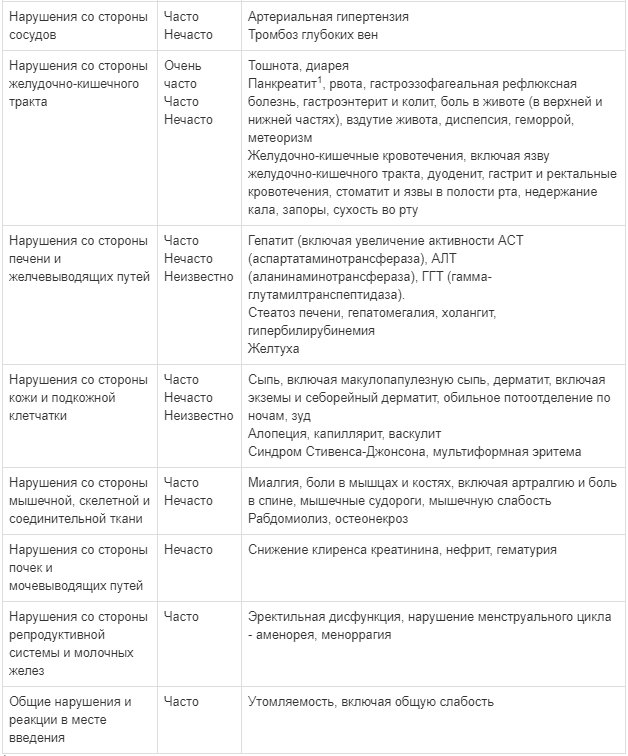
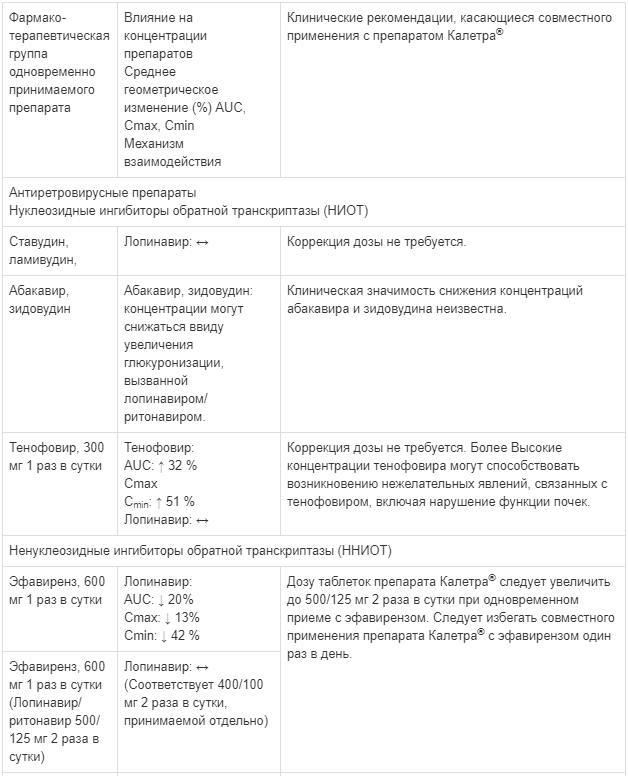
Взаимодействия между препаратом Калетра® и одновременно вводимыми лекарственными средствами представлены в таблице ниже, при этом увеличение обозначено как «↑», снижение - «↓», без изменений - «↔».
Если не указано иное, исследования. обозначенные ниже, проведены со стандартной рекомендуемой дозой лопинавира/ритонавира (т. е. 400/100 мг 2 раза в сутки).



Особые указания
Пациенты с сопутствующими заболеваниями
Нарушение функции печени
Безопасность и эффективность препарата Калетра® не была установлена у пациентов со значимыми нарушениями функции печени. Препарат Калетра® противопоказан пациентам с тяжелыми нарушениями функции печени (см. раздел «Противопоказания»).
Пациенты с хроническим гепатитом В или С, получающие комбинированную антиретровирусную терапию, имеют повышенный риск развития тяжелых и потенциально опасных для жизни нежелательных реакций со стороны печени. При проведении сопутствующей противовирусной терапии гепатитов В и С необходимо следовать указаниям соответствующих инструкций по применению.
У пациентов с уже существующим нарушением функции печени, включая пациентов с хроническим активным гепатитом, чаще развиваются нарушения функции печени на фоне комбинированной антиретровирусной терапии. Такие пациенты должны наблюдаться в соответствии со стандартной клинической практикой. В случае ухудшения или обострения заболевания печени у таких пациентов следует рассмотреть необходимость прерывания или прекращения лечения.
Сообщалось о повышении уровня трансаминаз с повышением или без повышения концентрации билирубина у ВИЧ-1 моноинфицированных пациентов и у лиц, получавших профилактическое лечение после интенсивного курса лечения через 7 дней после начала терапии лопинавиром/ритонавиром в сочетании с другими антиретровирусными препаратами. В некоторых случаях нарушения функции печени носили тяжелый характер.
До начала лечения лопинавиром/ритонавиром должны быть проведены соответствующие лабораторные исследования. За такими пациентами следует установить тщательный контроль во время лечения.
Нарушение функции почек
Поскольку почечный клиренс лопинавира и ритонавира незначителен, не ожидается повышение концентрации в плазме крови у пациентов с нарушением функции почек. Поскольку лопинавир и ритонавир прочно связываются с белками плазмы крови, маловероятно, что они будут значимо удалены с помощью гемодиализа или перитонеального диализа.
Гемофилия
Сообщалось об усилении кровотечений, включая спонтанные кожные гематомы и гемартроз у пациентов с гемофилией типа А и В. получавших лечение ингибиторами протеазы. Некоторым пациенты дополнительно применяли фактор VIII. Более чем в половине зарегистрированных случаев лечение ингибиторами протеазы было продолжено или возобновлено после приостановки лечения. Была установлена причинно-следственная связь, хотя ее механизм остается невыясненным. Пациентов с гемофилией необходимо предупредить о вероятности усиления кровотечений.
Панкреатит
Сообщалось о случаях панкреатита у пациентов, получавших препарат Калетра®, включая пациентов, у которых развилась гипертриглицеридемия. В большинстве случаев у пациентов в анамнезе присутствовал панкреатит и (или) сопутствующее лечение другими лекарственными средствами, связанными с развитием панкреатита.
Выраженное повышение концентрации триглицеридов является фактором риска развития панкреатита. Пациенты с ВИЧ-инфекцией поздней стадии могут иметь более высокий риск повышения концентрации триглицеридов и развития панкреатита.
Возможность развития панкреатита необходимо иметь в виду при появлении клинических симптомов (тошнота, рвота, боль в животе) или отклонений лабораторных показателей от нормы (повышение концентрации липазы или амилазы в сыворотке). Пациенты с перечисленными признаками или симптомами должны пройти дополнительное обследование, а в случае подтверждения диагноза панкреатита лечение препаратом Калетра® следует приостановить (см. раздел «Побочное действие»).
Синдром восстановления иммунитета
У ВИЧ-инфицированных пациентов с тяжелым иммунодефицитом на момент начала комбинированной антиретровирусной терапии (КАРТ) может развиться воспалительная реакция на бессимптомные или остаточные оппортунистические инфекции, что ведет к серьезным клинически значимым состояниям или усугублению симптомов. Такие реакции обычно наблюдаются в первые несколько недель или месяцев после начала КАРТ. В качестве примера можно привести цитомегаловирусный ретинит, диссеминированные и (или) локализованные микобактериальные инфекции и пневмонию, вызванную Pneumocystis jiroveci. Следует дополнительно оценить любые воспалительные симптомы и при необходимости назначить лечение.
Также на фоне синдрома восстановления иммунитета сообщалось о развитии аутоиммунных заболеваний (таких как болезнь Грейвса). Однако время до наступления таких нарушений варьирует, и они могут развиться много месяцев спустя после начала лечения.
Остеонекроз
Хотя этиология считается многофакторной (включая применение глюкокортикостероидов, употребление алкоголя, тяжелую иммуносупрессию, высокий индекс массы тела), случаи остеонекроза были зарегистрированы у пациентов с ВИЧ-инфекцией поздней стадии и (или) получающих в течение длительного времени комбинированную антиретровирусную терапию (КАРТ). Пациентам следует обратиться к врачу в случае появления ломоты, боли или скованности в суставах и при затруднении движения.
Удлинение интервала PR
Ритонавир/лопинавир может вызывать умеренное бессимптомное удлинение интервала PR у некоторых здоровых взрослых добровольцев. Сообщалось о редких случаях атриовентрикулярной блокады 2-й и 3-й степени у пациентов, получающих ритонавир/лопинавир, с сопутствующими органическими заболеваниями сердца и существующими ранее отклонениями отклонениями со стороны проводящей системы сердца, или у пациентов, принимающих лекарственные препараты, которые удлиняют интервал PR (например, верапамил и атазанавир). Таким пациентам препарат Калетра* следует назначать с осторожностью.
Масса тела и показатели обмена веществ
На фоне антиретровирусной терапии может увеличиваться масса тела, концентрация липидов и глюкозы в плазме крови. Такие изменения частично могут быть связаны с контролем заболевания и образом жизни. Существуют значимые свидетельства влияния лечения на увеличение концентрации липидов. Однако убедительных данных о связи увеличения массы тела с каким-либо конкретным лечением нет. Мониторинг концентрации липидов и глюкозы в плазме крови необходимо проводить в соответствии с разработанными руководствами по лечению ВИЧ-инфекции. Нарушения липидного обмена необходимо корректировать в соответствии с клинической необходимостью.
Взаимодействие с другими лекарственными препаратами
Препарат Калетра® содержит в составе лопинавир и ритонавир, оба из которых являются ингибиторами изофермента CYP3A цитохрома Р450. Вероятнее всего, препарат Калетра® повышает концентрации в плазме препаратов, метаболизируемых преимущественно CYP3A. Повышение концентрации одновременно назначаемых препаратов в плазме может привести к усилению или продлению их терапевтического действия и развитию нежелательных явлений (см. разделы «Противопоказания» и «Взаимодействие с другими лекарственными средствами»).
Мощные ингибиторы CYP3A4, такие как ингибиторы протеазы, могут усиливать действие бедаквилина, что потенциально может увеличить риск развития побочных реакций, связанных с бедаквилином. Таким образом, применения бедаквилина одновременно с лопинавиром/ритонавиром следует избегать. Тем не менее, если ожидаемая польза такого лечения превышает потенциальный риск, следует проявлять осторожность при одновременном применении бедаквилина с лопинавиром/ритонавиром. Рекомендуется более частый электрокардиографический мониторинг и контроль за уровнем трансаминаз (см. раздел «Взаимодействие с другими лекарственными средствами» и инструкцию по применению для бедаквилина).
Совместное применение деламанида с мощными ингибиторами CYP3A (такими как лопинавир/ритонавир) может усиливать действие метаболита деламанида, который, как известно, может удлинять интервал QTc. В связи с этим при одновременном применении деламанида и лопинавира/ритонавира требуется очень частый мониторинг ЭКГ на протяжении всего периода лечения деламанидом (см. раздел «Взаимодействие с другими лекарственными средствами» и инструкцию по применению для деламанида).
Сообщалось об угрожающих жизни реакциях и смертельных исходах по причине лекарственных взаимодействий у пациентов, получавших одновременно колхицин и мощные ингибиторы CYP3A, такие как ритонавир. Применение препарата Калетра® одновременно с колхицином, пациентам с нарушением функции почек или печени, противопоказано (см. разделы «Противопоказания» и «Взаимодействие с другими лекарственными средствами»).
Прием препарата Калетра® в сочетании со следующими лекарственными препаратами:
- Тадалафил: не рекомендуется назначать для лечения легочной артериальной гипертензии (см. раздел «Взаимодействие с другими лекарственными средствами»);
- Риоцигуат: не рекомендуется назначать вместе с препаратом Калетра® (см. раздел «Взаимодействие с другими лекарственными средствами»);
- Ворапаксар: не рекомендуется назначать вместе с препаратом Калетра® (см. раздел «Взаимодействие с другими лекарственными средствами»);
- Фузидовая кислота: не рекомендуется назначать при инфекционных заболеваниях костей и суставов (см. раздел «Взаимодействие с другими лекарственными средствами»);
- Салметерол: не рекомендуется назначать вместе с препаратом Калетра® (см. раздел «Взаимодействие с другими лекарственными средствами»);
- Ривароксабан: не рекомендуется назначать вместе с препаратом Калетра® (см. раздел «Взаимодействие с другими лекарственными средствами»).
Одновременное применение препарата Калетра® с аторвастатином не рекомендуется. При необходимости одновременного применения препарата Калетра® с аторвастатином должны применяться наименьшие эффективные дозы аторвастатина. Следует проявлять осторожность и назначать более низкие дозы при одновременном применении препарата Калетра® и розувастатина. При необходимости проведения лечения ингибитором редуктазы ГМГ-КоА рекомендуется назначать правастатин или флувастатин (см. раздел «Взаимодействие с другими лекарственными средствами»).
Ингибиторы фосфодиэстеразы 5 типа (ФДЭ-5)
Следует с осторожностью применять силденафил или тадалафил для лечения эректильной дисфункции у пациентов, принимающих препарат Калетра®. Одновременное применение этих лекарственных средств с препаратом Калетра" может сопровождаться существенным повышением их концентрации и появлением нежелательных явлений, таких как артериальная гипотензия, обморок, нарушение зрения и длительная эрекция (см. раздел «Взаимодействие с другими лекарственными средствами»). Одновременное применение аванафила или варденафила с лопинавиром/ритонавиром противопоказано (см. раздел «Противопоказания»). Одновременное применение силденафила с препаратом Калетра® противопоказано пациентам с легочной артериальной гипертензией (см. раздел «Противопоказания»).
Особую осторожность следует проявлять при применении препарата Калетра® и лекарственных средств, вызывающих удлинение интервала QT, таких как хлорфенирамин, хинидин, эритромицин и кларитромицин. В действительности, прием препарата Калетра® может привести к увеличению концентрации одновременно принимаемых препаратов и увеличению частоты развития нежелательных реакций со стороны сердца, вызванных применением этих препаратов. В доклинических исследованиях препарата Калетра® сообщалось о нежелательных реакциях со стороны сердца, поэтому потенциальное воздействие на сердце препарата Калетра® не может быть полностью исключено (см. раздел «Побочное действие»).
Совместное применение препарата Калетра® с рифампицином не рекомендуется. Рифампицин в сочетании с препаратом Калетра® приводит к выраженному снижению концентрации лопинавира, что может значительно уменьшить терапевтический эффект лопинавира. Достаточное действие лопинавира/ритонавира может быть достигнуто с увеличением дозы препарата Калетра®, но это также связано с повышенным риском токсического поражения печени и желудочно-кишечного тракта. За исключением крайней необходимости, такие препараты не следует назначать одновременно (см. раздел «Взаимодействие с другими лекарственными средствами»).
Не рекомендуется одновременное применение препарата Калетра* с флутиказоном или другими глюкокортикостероидами, которые метаболизируются CYP3A4, такими как будесонид, триамцинолон кроме случаев, когда потенциальная польза лечения превышает риск развития системных эффектов глюкокортикостероидов, включая синдром Иценко-Кушинга и подавление функции надпочечников (см. раздел «Взаимодействие с другими лекарственными средствами»).
Другое
Препарат Калетра® не излечивает ВИЧ-инфекцию или СПИД. Несмотря на установленное существенное снижение риска передачи инфекции половым путем на фоне эффективной вирусной супрессии во время антиретровирусной терапии, остаточный риск не может быть исключен. С целью предотвращения передачи инфекции необходимо соблюдать меры предосторожности в соответствии с национальными руководствами. У пациентов, принимающих препарат Калетра®, по-прежнему, могут развиться инфекции или другие заболевания, связанные с заболеванием ВИЧ и СПИД.
Влияние на способность к вождению автотранспорта, управлению механизмами
Исследования влияния на способность к вождению автотранспорта и управлению механизмами не проводились. Пациентов следует предупредить, что при лечении препаратом Калетра" отмечены случаи возникновения тошноты (см. раздел «Побочное действие»).
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 100 мг + 25 мг.
60 таблеток во флаконе из полиэтилена высокой плотности с завинчивающимся колпачком.
По 1 флакону вместе с инструкцией по применению в картонной пачке.
Срок годности
3 года. Не использовать после истечения срока годности, указанного на упаковке.
Условия хранения
При температуре от 15 до 30 °C. Хранить в местах, недоступных для детей.
Условия отпуска
Отпускается по рецепту.
Владелец регистрационного удостоверения / организация, принимающая претензии от потребителей:
ООО «ЭббВи»
125196, г. Москва, ул. Лесная, д.7,
БЦ «Белые Сады», здание «А»
Производитель
Производитель готовой лекарственной формы, фасовщик (первичная упаковка), упаковщик (вторичная упаковка), выпускающий контроль качества
ЭббВи Дойчланд ГмбХ и Ко.КГ,
Кнолльштрассе, 67061 Людвигсхафен, Германия /
AbbVie Deutschland GmbH & Co.KG,
Knollstrasse. 67061 Ludwigshafen, Germany
В случае упаковки выпускающего контроля качества на территории РФ указывают:
Производитель ютовой лекарственной формы. фасовщик (первичная упаковка)
ЭббВи Дойчланд ГмбХ и Ко.КГ.
Кнолльштрассе. 67061 Людвигсхафен. Германия /
AbbVie Deutschland GmbH & Co.KG.
Knollstrasse. 67061 Ludwigshafen. Germany
Упаковщик (вторичная упаковка), выпускающий контроль качества
АО «ОРТАТ», Россия
157092, Костромская обл., Сусанинский район, с. Северное, мкр. Харитоново.
Упаковано
ЭббВи Дойчланд ГмбХ и Ко.КГ, 67061 Людвигсхафен,
Кнолльштрассе, Германия
AbbVie Deutschland GmbH & Со.КС, 67061 Ludwigshafen,
Knollstrasse, Germany
или
АО «ОРТАТ», Россия
157092, Костромская обл., Сусанинский р-н, с. Северное, мкр-н Харитоново.
Наименование и адрес организации, уполномоченной принимать претензии на лекарственный препарат:
ООО «ЭббВи»
125047, г. Москва, ул. Лесная, д.7,
БЦ «Белые Сады», здание «А»
Комментарии
ПРАКТИКА ПЕДИАТРА
