Интрон A - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер: П N014632/01-150109
Торговое название препарата:
Международное непатентованное название (МНН): Интерферон альфа-2b (interferon alfa-2b)
Препарат представляет собой водорастворимый глобулярный белок с молекулярной массой около 19300 дальтон, синтезированный штаммом Escherichia coli, содержащим плазмидный гибрид, полученный методами генной инженерии, в генетический аппарат которого встроен ген человеческого лейкоцитарного интерферона альфа-2b.
Лекарственная форма: Раствор для внутривенного и подкожного введения
Состав:
Активное вещество:
Препарат во флаконах
10 млн ME (1 доза 10 млн ME) рекомбинантного интерферона альфа-2b в 1 мл раствора для инъекций
18 млн ME (6 доз по 3 млн ME) рекомбинантного интерферона альфа-2b в 3 мл раствора для инъекций
25 млн ME (5 доз по 5 млн ME) рекомбинантного интерферона альфа-2b в 2,5 мл раствора для инъекций.
Препарат в шприц-ручках
18 млн ME (6 доз по 3 млн ME) рекомбинантного интерферона альфа-2b в шприц-ручке
30 млн ME (6 доз по 5 млн ME) рекомбинантного интерферона альфа-2b в шприц-ручке
60 млн ME (6 доз по 10 млн ME) рекомбинантного интерферона альфа-2b в шприц-ручке.
Полезный объем раствора в шприц-ручке составляет 1,2 мл (для всех дозировок). Вспомогательные вещества:
Препарат во флаконах и шприц-ручках
Натрия гидрофосфат безводный, натрия дигидрофосфата моногидрат, динатрия эдетат, натрия хлорид, метакрезол (консервант), полисорбат-80, вода для инъекций.
Описание: Прозрачный бесцветный раствор
Фармакотерапевтическая группа: Иммуностимуляторы, цитокины и иммуномодуляторы, интерферон альфа-2b
Код ATX L03AB05
ФАРМАКОЛОГИЧЕСКИЕ И ИММУНОЛОГИЧЕСКИЕ СВОЙСТВА
Интерфероны оказывают действие на клетки за счет связывания со специфическими рецепторами на их поверхности.
Результаты нескольких исследований свидетельствуют о том, что после связывания с клеточной мембраной, интерферон вызывает сложную последовательность внутриклеточных реакций, в том числе индукцию определенных ферментов. Полагают, что хотя бы частично эти процессы и определяют клеточные эффекты интерферона, включая подавление репликации вирусов в инфицированных клетках, угнетение пролиферации клеток, а также иммуномодулирующие свойства интерферона, такие как усиление фагоцитарной активности макрофагов и нарастание специфической цитотоксичности лимфоцитов по отношению к клеткам-мишеням. Эти эффекты определяют терапевтическое действие интерферона.
Рекомбинантный интерферон альфа-2b оказывает антипролиферативное действие как в отношении культуры клеток человека и животных, так и в отношении ксенотрансплантатов опухолей человека и животных. Показана значительная иммуномодулирующая активность рекомбинантного интерферона альфа-2b in vitro. Рекомбинантный интерферон альфа-2b также подавляет репликацию вирусов in vitro и in vivo.
Фармакодинамика
Хотя точный механизм противовирусного действия рекомбинантного интерферона альфа-2Ь не известен, установлено, что он нарушает метаболизм клетки, в которую проник вирус. Это приводит к подавлению репликации вируса, а в случаях, когда репликация все же происходит, вирионы с поврежденным геномом не способны покинуть клетку.
Хронический гепатит В
Клинические исследования применения интерферона альфа-2b в течение 4-6 мес показывают, что терапия может привести к элиминации ДНК вируса гепатита В (HBV) и улучшению гистологической картины печени.
Хронический гепатит С
Применение Интрона® А в виде монотерапии или в комбинации с рибавирином изучали в 4 рандомизированных клинических исследованиях III фазы у 2552 пациентов с хроническим гепатитом С, не получавших ранее терапию интерфероном. В ходе исследований сравнивалась эффективность монотерапии или комбинированной терапии с рибавирином. Эффективность терапии определялась на основании отсутствия репликации вируса через 6 мес после окончания лечения.
Все пациенты имели хронический гепатит С, подтвержденный положительной ПЦР-реакцией на РНК вируса гепатита С (HCV) (более 100 копий/мл), данными биопсии печени с гистологическим подтверждением хронического гепатита и отсутствием какой-либо другой причины для его возникновения, и повышением активности AЛT.
Интрона® А назначали в дозе 3 млн ME 3 раза в неделю в качестве монотерапии или в комбинации с рибавирином. Большая часть пациентов получала лечение в течение года. Все пациенты наблюдались в течение 6 мес после окончания терапии для определения продолжительности сохранения результатов. Данные этих двух исследований приведены в таблице 1.
Комбинированная терапия рибавирином и Интрона® А значительно повышала эффективность терапии у всех подгрупп пациентов. Генотип HCV и количество РНК вируса перед началом терапии являются прогностическими факторами. Улучшение результатов при применении комбинированной терапии отмечают особенно у пациентов трудно поддающихся лечению (с генотипом 1 вируса и высоким содержанием РНК HCV в сыворотке крови).
Таблица 1. Число больных, достигших устойчивого вирусологического ответа (%) после годичного курса лечения
| HCV генотип | I* (n=503) C95−132/I95−143 |
I/R** (n=505) С95−132/195−143 |
I/R** (n=505) С/198−580 |
| Все генотипы | 16% | 41% | 47% |
| Генотип 1 | 9% | 29% | 33% |
| Генотип 1. Число копий<2 млн/мл |
25% | 33% | 45% |
| Генотип 1. Число копий>2 млн/мл |
3% | 27% | 29% |
| Генотип 2/3 | 31% | 65% | 79% |
* Интрона® А (3 млн ME 3 раза в неделю)
** Интрона® А (3 млн ME 3 раза в неделю) и рибавирин (1/1,2 г в сутки)
Строгое соблюдение схемы проводимой терапии значительно улучшает результаты лечения. Независимо от генотипа вируса, пациенты, получившие 80% и более курсовой терапии (рибавирин + Интрона® А) имели лучшие отдаленные результаты, чем пациенты, которые получили менее 80% курсовой терапии (устойчивый вирусологический ответ в 56% случаев по сравнению с 36% - по данным исследования CI98/580).
Лечение рецидивов: 345 пациентов получали в ходе исследований Интрона® А в виде монотерапии или в комбинации с рибавирином по поводу рецидива. У этой группы больных добавление рибавирина к Интрону® А вызывало 10-кратное увеличение эффективности лечения по сравнению с монотерапией Интроном® А (48,6% и 4,7%), что проявлялось элиминацией РНК HCV из сыворотки крови (менее 100 копий/мл при проведении ПЦР-реакции), уменьшением воспаления печени и нормализацией AЛT. Причем эти результаты сохранялись через 6 мес после окончания терапии (устойчивый вирусологический ответ).
Фармакокинетика
Фармакокинетику Интрона® А изучали у здоровых добровольцев при однократном введении в дозе 5 млн МЕ/м2 внутримышечно, подкожно и посредством внутривенной инфузии в течение 30 мин. Средние концентрации интерферона в сыворотке крови были сравнимы после подкожного и внутримышечного введения. При этом максимальная сывороточная концентрация достигалась через 3-12 ч; период полувыведения как после внутримышечного, так и после подкожного введения составил приблизительно 2-3 ч; содержание интерферона через 16-24 ч в сыворотке крови не определялось. Биодоступность препарата при подкожном введении составила 100%.
После внутривенного введения концентрация интерферона в плазме достигала максимальных величин (135-273 МЕ/мл) в конце инфузии, затем снижалась несколько быстрее, чем после подкожных или внутримышечных инъекций, и не определялась через 4 ч после окончания инфузии; период полувыведения составлял около 2 ч.
Концентрация интерферона в моче была ниже определяемой величины независимо от пути введения.
У пациентов, получавших Интрон® А в ходе проведения контролируемых клинических исследований, определяли интерферон-нейтрализующие антитела. Частота их выявления составляла 2,9% у больных, получавших терапию Интроном® А по поводу онкологического заболевания, и 6,2% у пациентов с хроническим гепатитом. Титры антител были низкими практически во всех случаях, а их выявление не связывалось со снижением эффективности терапии или с другими аутоиммунными нарушениями.
Доклинические данные по безопасности препарата
Несмотря на то, что интерферон считается видоспецифичным веществом, были проведены исследования его токсичности у животных.
Введение человеческого рекомбинантного интерферона альфа-2b в течение 3 мес не сопровождалось признаками токсичности у мышей, крыс, кроликов. Введение препарата обезьянам cynomolgus в течение 3 мес ежедневно в дозе 20х106 МЕ/кг/сутки также не привело к появлению заметных признаков токсичности. Увеличение дозы у обезьян до 100x106 МЕ/кг/сутки в течение 3 мес приводило к токсическому эффекту. В исследованиях с применением интерферона у нечеловекообразных приматов наблюдались нарушения менструального цикла.
Результаты исследований влияния интерферона альфа-2b на репродуктивность у животных указывают на отсутствие тератогенного эффекта у крыс и кроликов. Препарат также не влияет на течение беременности, развитие плода и на репродуктивную функцию у потомства леченых крыс.
В исследованиях, проведенных на макаках-резусах, показано, что применение высоких доз (превышающих рекомендуемые в 90 и 180 раз) интерферона альфа-2b вызывает аборты. При проведении соответствующих исследований не установлено мутагенного действия интерферона альфа-2b.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Хронический гепатит В
Лечение взрослых и детей (от 1 года) с хроническим гепатитом В с подтвержденной репликацией вируса гепатита В (наличие ДНК HBV или HBeAg в сыворотке крови) в сочетании с повышением активности АЛТ в плазме крови и гистологически подтвержденным активным воспалительным процессом и/или фиброзом печени.
Хронический гепатит С
Монотерапия или в комбинации с рибавирином у взрослых больных хроническим гепатитом С, у которых повышена активность трансаминаз, отсутствуют признаки декомпенсации функции печени, и определяется РНК HCV или антитела к вирусу гепатита С (anti-HCV) в сыворотке крови.
При хроническом гепатите С у детей (от 3 лет) с компенсированным заболеванием печени, ранее не получавших лечение интерфероном альфа-2b, и у взрослых больных с рецидивом после терапии интерфероном альфа-2b предпочтительнее назначать Интрон® А в комбинации с рибавирином.
Перед началом комбинированной терапии следует ознакомиться с инструкцией по применению рибавирина.
Папилломатоз гортани
Лечение взрослых и детей от 1 года с папилломатозом гортани.
Волосатоклеточный лейкоз
Лечение волосатоклеточного лейкоза у взрослых в виде монотерапии или в комбинации с рибавирином.
Хронический миелолейкоз
Монотерапия: лечение взрослых пациентов с хроническим миелолейкозом при наличии филадельфийской хромосомы (Ph+) или транслокации bcr/abl.
Клинические данные показывают, что гематологическая ремиссия и цитогенетический ответ (большой/малый) достигается у большинства пациентов. При этом большой цитогенетический ответ определяют как количество Рh+-лейкозных клеток в костном мозге <34%, а малый - от 34% до 90%.
Комбинированная терапия: назначение Интрона® А в сочетании с цитарабином во время первых 12 мес лечения позволяет существенно увеличить число больших цитогенетических ответов и значительно увеличить общую выживаемость больных по сравнению с монотерапией интерфероном альфа-2b после 3 лет лечения.
Тромбоцитоз у больных хроническим миелолейкозом (XMЛ)
Тромбоцитоз часто возникает при хроническом миелолейкозе. Интрон® А применяли с некоторым эффектом у взрослых больных с тромбоцитозом, связанным с XMЛ.
Множественная миелома
В качестве поддерживающей терапии у взрослых пациентов, достигших частичного ответа (уменьшение уровня парапротеина в сыворотке крови на 50%) после начальной индукционной терапии.
Поддерживающая терапия удлиняет фазу плато, однако влияние препарата на общую выживаемость окончательно не установлено.
Фолликулярная лимфома (неходжкинская лимфома)
Лечение фолликулярной лимфомы с высокой опухолевой массой - в сочетании с адекватной индукционной химиотерапией (например, СНОР-режимом) у взрослых больных. К данной группе относятся фолликулярные лимфомы при наличии хотя бы одного из перечисленных признаков: большой размер опухоли (>7 см), вовлечение 3 или более лимфатических узлов (каждый >3 см), общие симптомы (снижение массы тела более чем на 10%, повышение температуры тела более 38 °С в течение более чем 8 дней, повышенное потоотделение по ночам), спленомегалия (граница селезенки выходит за область пупка), сдавление важных органов или возникновение компрессионного синдрома, вовлечение эпидурального пространства или орбитальной области, лейкемия, значительный выпот.
Эффективность терапии Интроном® А у пациентов с фолликулярными неходжкинскими лимфомами низкой степени злокачественности и низкой опухолевой нагрузкой не была установлена.
Саркома Капоши, связанная с синдромом приобретенного иммунодефицита (СПИД)
Лечение больных саркомой Капоши на фоне СПИД при отсутствии оппортунистических инфекций, если число клеток CD4 превышает 250/мм3.
Рак почки
Лечение взрослых больных с прогрессирующим раком почки.
Карциноидные опухоли
Лечение карциноидных опухолей у взрослых больных при вовлечении лимфоузлов или с метастазами в печени и с «карциноидным синдромом».
Злокачественная меланома
Адъювантная терапия взрослых больных прооперированных по поводу первичной опухоли, при наличии высокого риска системного рецидива.
ПРОТИВОПОКАЗАНИЯ
- повышенная чувствительность к любому компоненту препарата.
- тяжелые заболевания сердечно-сосудистой системы (т.ч. сердечная недостаточность в стадии декомпенсации, недавно перенесенный инфаркт миокарда, тяжелые аритмии).
- выраженные нарушения функции печени или почек, в т.ч. вызванные метастазами, хронический гепатит с циррозом печени в стадии декомпенсации, хронический гепатит у пациентов, получавших или получающих иммунодепрессанты (за исключением кратковременного курса терапии глюкокортикостероидами), аутоиммунный гепатит.
- эпилепсия и другие нарушения функции ЦНС, психические заболевания и расстройства у детей и подростков.
- аутоиммунное заболевание в анамнезе.
- применение иммунодепрессантов после трансплантации.
- заболевание щитовидной железы в случае, если оно не контролируется соответствующей терапией.
- клиренс креатинина ниже 50 мл/мин - при назначении в комбинации с рибавирином.
- беременность и лактация.
- назначение мужчинам, партнёрши которых беременны.
- при назначении Интрона® А в комбинации с рибавирином следует также учитывать противопоказания, указанные в инструкции по применению рибавирина.
- Психические заболевания в анамнезе.
Лечение назначает врач, имеющий опыт лечения соответствующего заболевания. По решению врача пациент может самостоятельно вводить себе препарат подкожно для продолжения подобранного режима терапии.
Хронический гепатит В
Рекомендуемая доза для взрослых составляет от 30 до 35 млн ME в неделю подкожно, либо в дозе 5 млн ME ежедневно, либо 10 млн ME три раза в неделю в течение 4 месяцев (16 недель).
Детям от 1 года до 17 лет включительно Интрон® А вводится подкожно в начальной дозе 3 млн МЕ/м2 три раза в неделю (через день) в течение первой недели лечения с последующим увеличением дозы до 6 млн МЕ/м2(максимум до 10 млн МЕ/м2) три раза в неделю (через день). Продолжительность курса лечения 4-6 месяцев (16-24 недели).
Лечение прекращают при отсутствии положительной динамики (по данным исследования ДНК вируса гепатита В (HBV)) после 3-4 мес лечения препаратом в максимальной переносимой дозе.
Рекомендации по коррекции дозы:
Дозу препарата следует уменьшить на 50% при развитии нарушений со стороны системы кроветворения (лейкоциты менее 1500/мм3, гранулоциты менее 1000/мм3 у детей и менее 750/мм3 у взрослых, тромбоциты менее 100000/мм3 у детей и менее 50000/мм3 у взрослых). Терапию следует прекратить в случае выраженной лейкопении (лейкоциты менее 1200/мм3), нейтропении (гранулоциты менее 750/мм3 у детей и менее 500/мм3 у взрослых) или тромбоцитопении (тромбоциты менее 70000/мм3 у детей и менее 30000/мм3 у взрослых). Лечение может быть возобновлено в прежней дозе после нормализации или возврата к исходному уровню числа лейкоцитов, гранулоцитов и тромбоцитов.
Хронический гепатит С
Интрон® А назначают подкожно в дозе 3 млн ME 3 раза в неделю (через день) в качестве монотерапии или в комбинации с рибавирином (дозы и рекомендации по их подбору - см. инструкцию по применению рибавирина в капсулах в составе комбинированной терапии).
Лечение больных с рецидивом после курса монотерапии альфа-интерфероном. Интрон® А назначают только в комбинации с рибавирином. На основании результатов клинических исследований, проводившихся в течение 6 мес, рекомендуемая продолжительность комбинированного лечения с рибавирином составляет 6 мес.
Лечение больных, ранее не получавших терапии. Эффективность Интрона® А повышается при одновременном применении с рибавирином. Монотерапию препаратом проводят только при наличии противопоказаний к применению или непереносимости рибавирина.
Применение Интрона® А в комбинации с рибавирином. На основании результатов клинических исследований, проводившихся в течение 12 мес, рекомендуемая продолжительность комбинированной терапии с рибавирином составляет, по крайней мере, 6 мес.
У пациентов с генотипом 1 вируса и высоким содержанием РНК вируса (по результатам исследования, проведенного до начала терапии), у которых к концу первых 6 мес терапии в сыворотке крови не определяется РНК вируса гепатита С (РНК HCV), лечение продолжают еще 6 мес (т.е. в общей сложности 12 мес). При принятии решения о проведении комбинированной терапии в течение 12 мес следует также принимать во внимание другие отрицательные прогностические факторы: возраст старше 40 лет, мужской пол, прогрессирующий фиброз.
При проведении клинических исследований установлено, что у пациентов, у которых после 6 мес терапии по-прежнему определяется РНК HCV, продолжение лечения не приводит к элиминации РНК HCV.
При использовании Нитрона® А в комбинации с рибавирином следует проводить тщательное наблюдение за пациентами с нарушениями функции печени и пациентами старше 50 лет в связи с возможным развитием анемии.
Детям от 3 лет и старше Интрон® А назначают подкожно по 3 млн МЕ/м2 два раза в неделю в комбинации с пероральным приёмом рибавирина в дозе 15 мг/кг ежедневно, разделяя эту дозу на утреннюю и вечернюю.
Монотерапия Нитроном® А. Интрон® А рекомендуют применять в течение, по крайней мере, 3-4 мес, после этого следует провести определение РНК HCV. Затем лечение продолжают только в том случае, если РНК HCV не выявлена.
Для пациентов, хорошо переносящих терапию, с нормализацией AЛT на 16 неделе лечения, рекомендуемый курс лечения составляет от 18 до 24 мес.
Папилломатоз гортани
Рекомендуемая доза Нитрона® А составляет 3 млн МЕ/м2 подкожно три раза в неделю (через день). Лечение начинают после хирургического (лазерного) удаления опухолевой ткани. Дозу увеличивают с учетом переносимости препарата. Для достижения положительного ответа может потребоваться проведение терапии в течение более чем 6 мес.
Волосатоклеточный лейкоз
Рекомендуемая доза Интрона® А для подкожного введения пациентам после спленэктомии и без нее составляет 2 млн МЕ/м2 3 раза в неделю. В большинстве случаев нормализация одного и более гематологических показателей наступает через 1-2 месяца лечения. Для нормализации показателей периферической крови (числа лейкоцитов, тромбоцитов и уровня гемоглобина) может потребоваться до 6 месяцев лечения Интроном® А. Этого режима дозирования следует придерживаться постоянно, если только при этом не происходит быстрое прогрессирование заболевания или возникновение тяжелой непереносимости препарата.
Хронический миелолейкоз
Рекомендуемая доза Интрона® А составляет от 4 до 5 млн МЕ/м2 ежедневно, подкожно.
В некоторых случаях эффективной является комбинация Интрона® А в дозе 5 млн МЕ/м2, назначаемого ежедневно подкожно, с цитарабином (Ara-С) в дозе 20 мг/м2 подкожно в течение 10 дней в месяц (максимальная суточная доза 40 мг). После нормализации числа лейкоцитов Интрон® А вводят в максимальной переносимой дозе (от 4 до 5 млн МЕ/м2 в сутки) для поддержания гематологической ремиссии.
Интрон® А следует отменить через 8-12 недель лечения, если к этому времени не достигнута, по крайней мере, частичная гематологическая ремиссия или клинически значимое снижение числа лейкоцитов.
Тромбоцитоз у больных хроническим миелолейкозом
Рекомендуются те же дозы, что и при лечении хронического миелолейкоза. Коррекция дозы, используемая для контроля числа лейкоцитов, может также применяться для контроля числа тромбоцитов.
Клинические данные свидетельствуют о том, что примерно у одной четверти (26%) больных хроническим миелолейкозом отмечается сопутствующий тромбоцитоз (число тромбоцитов более 500x109/л). Снижения числа тромбоцитов удавалось добиться у всех больных после 2 месяцев лечения. Число тромбоцитов никогда не было менее 80x109/л, при ежемесячном контроле.
Множественная мислома
Поддерживающая терапия: пациентам, у которых в результате индукционной терапии достигнута фаза плато (уменьшение парапротеина более чем на 50%), Интрон® А можно назначать в качестве монотерапии - подкожно в дозе 3-5 млн МЕ/м2 3 раза в неделю.
Фолликулярная лимфома
Интрон® А назначают в сочетании с химиотерапией подкожно в дозе 5 млн ME 3 раза в неделю (через день) в течение 18 мес. Клинические данные имеются только по применению схемы CHVP (комбинация циклофосфамида, доксорубицина, тенипозида и преднизолона) в виде 6-месячных циклов и последующих 6 циклов, проводимых 1 раз в 2 мес.
Саркома Капоши, связанная со СПИД
Оптимальная доза не установлена. Показана эффективность Интрона® А в дозе 30 млн МЕ/м2, при введении 3-5 раз в неделю подкожно. Препарат также применяли в меньших дозах (10-12 млн МЕ/м2/сутки) без заметного снижения эффективности. Если заболевание стабилизируется или отмечается клинический эффект, терапию продолжают до тех пор, пока не будет отмечен рост опухоли или не потребуется отмена препарата из-за развития тяжелой оппортунистической инфекции или побочного эффекта. Терапия Интроном® А этих больных может проводиться в амбулаторных условиях.
Одновременное применение с зидовудином. В клинических исследованиях больные со СПИДом и саркомой Капоши получали Интрон® А в сочетании с зидовудином. В большинстве случаев хорошо переносилась пациентами следующая схема лечения: Интрон® А в дозе 5-10 млн МЕ/м2 ежедневно; зидовудин 100 мг каждые 4 ч. Основным токсическим эффектом, ограничивавшим дозу, была нейтропения.
Лечение Интроном® А можно начать с дозы 3-5 млн МЕ/м2/сутки. Через 2-4 недели доза Интрона® А может быть увеличена на 5 млн МЕ/м2/сутки - до 10 млн МЕ/м2/сутки, с учетом переносимости; доза зидовудина может быть повышена до 200 мг/4 ч.
Дозу следует подбирать индивидуально - с учетом эффективности и переносимости.
Рак почки
Монотерапия. Оптимальная доза и схема применения не установлены. Интрон® А применяли подкожно в дозах от 3 до 30 млн МЕ/м2 три или пять раз в неделю или ежедневно. Максимальный эффект наблюдался при подкожном применении Интрона® А в дозах от 3 до 10 млн МЕ/м2 три раза в неделю.
В комбинации с другими лекарственными средствами - такими, как интерлейкин-2. Оптимальная доза не установлена. В комбинации с интерлейкином-2 Интрон® А применяли подкожно в дозах от 3 до 20 млн МЕ/м2. В клинических исследованиях частота ответа на лечение была максимальной при подкожном введении Интрона® А в дозе 6 млн МЕ/м2 три раза в неделю; дозу подбирали индивидуально во время лечения.
Карциноидные опухоли
Стандартная доза Интрона® А составляет 5 млн ME (3-9 млн ME) подкожно 3 раза в неделю (через день). У пациентов с распространённым процессом модет потребоваться применение дозы до 5 млн ME ежедневно.
При хирургическом лечении терапию Интроном® А временно приостанавливают - на время операции и восстановительного периода после нее. Терапию препаратом продолжают до тех пор, пока наблюдается клинический ответ на проводимое лечение.
Злокачественная меланома
Для индукции постоперационной ремиссии Интрон® А назначают внутривенно в разовой дозе 20 млн МЕ/м2 в сутки 5 дней в неделю на протяжении 4 недель. Рассчитанную таким образом дозу добавляют к 100 мл 0,9% раствора натрия хлорида и вводят в виде инфузии в течение 20 мин. Лечение следует начинать в течение 56 дней после хирургического вмешательства. Для поддерживающей терапии рекомендуемая разовая доза составляет 10 млн МЕ/м2, её вводят подкожно 3 раза в неделю (через день) в течение 48 недель. При развитии тяжелых побочных эффектов во время терапии Интроном® А (в частности при снижении числа гранулоцитов менее 500/мм3 или повышении AЛT/ACT до значений, превышающих верхнюю границу нормы в 5 раз) применение препарата временно прекращают до нормализации показателей. Затем лечение возобновляют, используя дозу, уменьшенную на 50%. Если непереносимость сохраняется, или если число гранулоцитов уменьшается до 250/мм3, или активность AЛT и/или ACT возрастает до значений, превышающих верхнюю границу нормы в 10 раз, препарат отменяют.
Хотя оптимальная (минимальная) доза для достижения адекватного клинического эффекта не установлена, Интрон® А следует назначать в рекомендуемых дозах с учетом их возможной коррекции из-за токсического действия, как описано выше.
ПРАВИЛА ПРИГОТОВЛЕНИЯ И ВВЕДЕНИЯ РАСТВОРОВ
Перед введением необходимо визуально убедиться в отсутствии видимых частиц и изменения цвета раствора.
Содержимое флакона или шприц-ручки используют для лечения только одного пациента. Интрон®А раствор для инъекций во флаконах можно использовать для внутривенного или подкожного введения сразу же после набора из флакона необходимой дозы с помощью стерильного шприца для инъекций (стеклянного или пластикового).
Приготовление раствора для внутривенного введения. Инфузию следует проводить немедленно после приготовления раствора. Для измерения требуемой дозы препарата можно использовать флакон любого объема; при этом конечная концентрация интерферона альфа-2b в растворе натрия хлорида должна быть не менее 0,3 млн МЕ/мл. Соответствующую дозу препарата набирают из флакона, добавляют к 100 мл 0,9% раствора натрия хлорида в мешок из ПВХ или в стеклянный флакон для инфузий и вводят в/в капельно в течение 20 мин.
Недопустимо одновременное введение других препаратов вместе с Интроном® А.
Применение других других растворителей недопустимо.
Интрон® А раствор для инъекций в шприц-ручках вводят подкожно сразу же после присоединения иглы для инъекций и набора необходимой дозы.
Препарат следует достать из холодильника за 30 мин до проведения инъекции, чтобы раствор нагрелся до комнатной температуры (до 25°С).
После вскрытия упаковки препарат рекомендуется использовать в течение 4 недель при условии хранения при температуре от 2 до 8°С. Для введения каждой дозы следует использовать новую иглу. После инъекции иглу следует выбросить, а ручку немедленно поместить в холодильник.
Утилизацию использованных флаконов и шприц-ручек проводят в соответствии с действующим порядком.
ПОБОЧНОЕ ДЕЙСТВИЕ
В клинических исследованиях проведенных при широком спектре показаний и с большим диапазоном доз (от 6 млн МЕ/м2 в неделю при волосатоклеточном лейкозе до 100 млн МЕ/м2 в неделю при меланоме) наиболее часто встречающимися нежелательными явлениями были лихорадка, усталость, головная боль, миалгия. Лихорадка и усталость проходили через 72 час после прекращения введения препарата. Хотя лихорадка может быть одним из симптомов так называемого «гриппоподобного синдрома», часто встречающегося при лечении интерферонами, следует провести обследование с тем, чтобы исключить другие возможные причины персистирующей лихорадки.
Приведенный ниже профиль безопасности был получен при проведении 4 клинических исследований у пациентов с хроническим гепатитом С. получавших Интрон® А в виде монотерапии или в комбинации с рибавирином в течение 1 года. Все пациенты получали 3 млн ME Интрона® А 3 раза в неделю. В таблице 2 приведены нежелательные явления, отмечавшиеся с частотой большей или равной 10% у пациентов, ранее нелеченных и получавших Интрон® А (или Интрон® А в комбинации с рибавирином) в течение 1 года. В основном отмеченные нежелательные явления были легкими или умеренно выраженными.
Таблица 2
| Нежелательные явления | Интрон® А (n=806) |
Интрон® А + рибавирин (n=1010) |
| Местные реакции | ||
| Воспалительные реакции в месте введения | 9-16% | 6-17% |
| Другие реакции в месте введения | 5-8% | 3-36% |
| Общие реакции | ||
| Головная боль | 51-64% | 48-64% |
| Усталость | 42-79% | 43-68% |
| Озноб | 15-39% | 19-41% |
| Лихорадка | 29-39% | 29-41% |
| Гриппоподобный синдром | 19-37% | 18-29% |
| Астения | 9-30% | 9-30% |
| Снижение массы тела | 6-11% | 9-19% |
| Реакции со стороны ЖКТ | ||
| Тошнота | 18-31% | 25-44% |
| Анорексия | 14-19% | 19-26% |
| Диарея | 12-22% | 13-18% |
| Боли в животе | 9-17% | 9-14% |
| Рвота | 3-10% | 6-10% |
| Реакции со стороны костно-мышечной системы | ||
| Миалгия | 41-61% | 30-62% |
| Артралгия | 25-31% | 21-29% |
| Боли в костях и мышцах | 15-20% | 11-20% |
| Реакции со стороны ЦНС | ||
| Депрессия | 16-36% | 25-34% |
| Раздражительность | 13-27% | 18-34% |
| Бессонница | 21-28% | 33-41% |
| Беспокойство | 8-12% | 8-16% |
| Нарушение способности к концентрации внимания | 8-14% | 9-21% |
| Эмоциональная лабильность | 8-14% | 5-11% |
| Реакции со стороны кожи | ||
| Алопеция | 22-31% | 26-32% |
| Зуд | 6-9% | 18-37% |
| Сухость кожи | 5-8% | 10-21% |
| Сыпь | 5-7% | 15-24% |
| Реакции со стороны дыхательной системы | ||
| Фарингит | 3-7% | 7-13% |
| Кашель | 3-7% | 8-11% |
| Диспное | 2-9% | 10-22% |
| Прочие | ||
| Головокружение | 8-18% | 10-22% |
| Вирусная инфекция | 0-7% | 3-10% |
Нежелательные явления, наблюдавшиеся у пациентов с вирусным гепатитом С, соответствуют тем, которые были отмечены при применении Интрона® А по другим показаниям с некоторым дозозависимым увеличением по частоте развития.
При применении Интрона®А по другим показаниям (в клинических исследованиях и вне клинических исследований) редко (>1/10000, <1/1000) или очень редко (<1/10000) наблюдались следующие нежелательные явления:
Со стороны организма в целом: очень редко - отек лица.
Сообщалось об астенических состояниях (астении, недомогании и усталости), обезвоживании, сердцебиении, псориазе, грибковой инфекции и бактериальной инфекции (включая сепсис).
Со стороны иммунной системы: очень редко - саркоидоз или обострение саркоидоза.
При применении альфа-интерферонов сообщалось о развитии различных аутоиммунных и опосредованных иммунной системой нарушений, в т.ч. идиопатической тромбоцитопенической пурпуры, тромботической тромбоцитопенической пурпуры, ревматоидного артрита, системной красной волчанки, васкулита и синдрома Фогта-Коянаги-Харады.
Сообщалось о случаях острых реакций гиперчувствительности, включая крапивницу, ангионевротический аллергический отёк и анафилаксию.
Со стороны сердечно-сосудистой системы: редко - аритмии (обычно возникали у пациентов с предшествующими заболеваниями сердечно-сосудистой системы в анамнезе или с предшествующей кардиотоксической терапией), преходящая обратимая кардиомиопатия (отмечена у пациентов без отягощенного анамнеза со стороны сердечно-сосудистой системы); очень редко - артериальная гипотензия, ишемия миокарда и инфаркт миокарда.
Co стороны ЦНС и периферической нервной системы: редко - суицидальные наклонности, очень редко - агрессивное поведение, в т.ч. направленное на других людей, суицидальные попытки, суицид, психоз (в т.ч. галлюцинации), нарушения сознания, нейропатии, полинейропатии, энцефалопатия, цереброваскулярная ишемия, цереброваскулярная геморрагия, периферические невропатии, судороги.
Со стороны органа слуха: очень редко - нарушение слуха.
Со стороны эндокринной системы: очень редко - сахарный диабет, ухудшение течения имеющегося сахарного диабета.
Со стороны ЖКТ: очень редко - панкреатит, повышение аппетита, кровоточивость десен, колит.
Со стороны печени и желчевыводящих путей: очень редко - гепатотоксичность (в том числе с летальным исходом).
Изменения со стороны зубов и периодонта. У пациентов, получавших комбинированную терапию Интроном® А и рибавирином, отмечались патологические изменения со стороны зубов и периодонта. Сухость во рту при длительной комбинированной терапии рибавирином и Интроном® А может способствовать повреждению зубов и слизистой оболочки полости рта. Пациенты должны чистить зубы щеткой 2 раза в день и регулярно проходить осмотр у стоматолога. Кроме того, у некоторых пациентов может наблюдаться рвота.
Со стороны обмена веществ: редко - гипергликемия, гипертриглицеридемия.
Со стороны костно-мышечной системы: редко - рабдомиолиз (иногда тяжелый), судороги в ногах, боль в спине, миозит.
Со стороны кожи: очень редко - мультиформная эритема, синдром Стивенса-Джонсона, токсический эпидермальный некролиз, некроз в месте инъекции.
Со стороны дыхательной системы: редко - пневмония, очень редко - легочные инфильтраты, пневмониты.
Со стороны мочевыделителъной системы: очень редко - нефротический синдром, нарушения функции почек, почечная недостаточность.
Со стороны системы кроветворения: очень редко при применении Интрона® А в виде монотерапии или в комбинации с рибавирином отмечались апластическая анемия и полная аплазия красного костного мозга.
Co стороны органа зрения: редко - кровоизлияния в сетчатку, очаговые изменения глазного дна, тромбоз артерий и вен сетчатки, снижение остроты зрения, уменьшение полей зрения, неврит зрительного нерва, отек диска зрительного нерва.
Клинически значимые изменения лабораторных показателей: (чаще отмечались при назначении препарата в дозах более 10 млн ME в сутки) - снижение числа гранулоцитов и лейкоцитов, снижение уровня гемоглобина и числа тромбоцитов, повышение активности ЩФ, ЛДГ, уровня креатинина и азота мочевины сыворотки крови. Повышение активности АЛТ и ACT в плазме крови отмечается как патологическое при применении по всем показаниям, кроме гепатитов, а также у некоторых пациентов с хроническим гепатитом В при отсутствии ДНК HBV.
Если во время применения Интрона® А по любому показанию развиваются нежелательные явления, следует уменьшить дозу или временно прервать лечение до тех пор, пока нежелательные явления не будут ликвидированы. Если развивается постоянная или повторная непереносимость при применении адекватного режима дозирования, или заболевание прогрессирует, терапию Интроном® А следует отменить.
ОСОБЫЕ УКАЗАНИЯ
Для всех пациентов
В случае развития реакций гиперчувствительности немедленного типа (крапивница, ангионевротический отек, бронхоспазм, анафилаксия) при применении Интрона® А, препарат следует немедленно отменить и назначить соответствующее лечение. Преходящая кожная сыпь не требует прекращения лечения.
При развитии тяжелых и среднетяжелых побочных эффектов может потребоваться коррекция режима дозирования или, в некоторых случаях, прекращение терапии. В случае появления на фоне применения Интрона® А признаков нарушения функции печени за больным необходимо установить тщательное наблюдение и при прогрессировании симптомов отменить препарат.
На фоне применения Интрона® А или в течение 2 дней после отмены лечения возможно развитие артериальной гипотензии, требующей назначения соответствующей терапии.
При лечении Интроном® А необходимо обеспечить адекватную гидратацию организма путем дополнительного введения жидкости, т.к. в некоторых случаях артериальная гипотензия может развиться в результате уменьшения ОЦК.
Лихорадка может быть проявлением гриппоподобного синдрома, часто встречающего при применении интерферона альфа-2Ь, однако следует исключить другие причины ее возникновения.
Интрон® А с осторожностью назначают пациентам с тяжелыми хроническими заболеваниями, такими как хронические обструктивные болезни легких, сахарный диабет со склонностью к кетоацидозу. Особая осторожность требуется при применении препарата у пациентов с нарушениями свертываемости крови (в т.ч. с тромбофлебитами, тромбоэмболиями легочной артерии), а также при выраженной миелосупрессии.
У пациентов, получавших терапию интерфероном альфа (в т.ч. и Интроном® А), в редких случаях наблюдаются пневмониты и пневмонии (в некоторых случаях с летальным исходом) неясной этиологии. Подобные симптомы встречались чаще на фоне применения «шосаикото» - средства китайской народной медицины растительного происхождения. Любому пациенту с кашлем, лихорадкой, одышкой или другими симптомами со стороны дыхательной системы необходимо провести рентгенологическое исследование грудной клетки. При выявлении инфильтрата или других нарушений функции легких за пациентом следует тщательно наблюдать, и при необходимости, отменить терапию Интроном® А. Своевременная отмена интерферона альфа и назначение ГКС способствует купированию легочных синдромов.
Нарушения со стороны органа зрения появляются обычно после нескольких месяцев лечения, но их возникновение описано и после менее продолжительной терапии. Всем пациентам необходимо провести офтальмологическое обследование до начала терапии. При жалобах на нарушение зрения, изменение полей зрения или любые другие офтальмологические нарушения, необходима немедленная консультация окулиста. Пациентам с заболеваниями, при которых могут происходить изменения сетчатки, например сахарным диабетом или артериальной гипертензией, рекомендуется во время терапии Интроном® А регулярно проходить офтальмологический осмотр. При появлении или усугублении расстройств зрения следует рассмотреть вопрос о прекращении терапии Интроном® А
Серьезные психические нарушения, в частности депрессия, суицидальные мысли и попытки, психоз, включая галлюцинации, агрессивное поведение, т.ч. направленное на других людей, являются известными побочными эффектами альфа-интерферонов. Суицидальные мысли и попытки чаще отмечались у пациентов детского, в первую очередь подросткового возраста (2,4%), чем у взрослых (1%).
Следует с осторожностью применять препарат у пациентов с анамнестическими указаниями на наличие психических расстройств.
В случае развития у пациента изменений со стороны психической сферы и/или ЦНС, включая развитие депрессии, рекомендуется наблюдение врача за таким пациентом в течение всего периода лечения, а также в течение 6 мес после его окончания. Указанные побочные эффекты обычно являются быстро обратимыми после прекращения терапии, однако в некоторых случаях требовалось до 3 недель для их полного обратного развития. Если симптомы расстройства психики не регрессируют или ухудшаются, появляются суицидальные мысли или агрессивное поведение, направленное на других людей, рекомендуется прекратить лечение Интроном® А и обеспечить консультацию психиатра.
У некоторых пациентов, особенно пожилых, получавших препарат в высоких дозах, наблюдались нарушение сознания, кома и судороги, включая случаи развития энцефалопатии. В случае неэффективности снижения дозы и/или медикаментозной коррекции этих нарушений, следует решить вопрос о прекращении терапии Интроном® А.
Пациентам с заболеваниями сердечно-сосудистой системы (например, инфарктом миокарда, хронической сердечной недостаточностью, аритмиями) требуется тщательное медицинское наблюдение при назначении Интрона® А. Пациентам с заболеваниями сердца и/или прогрессирующим онкологическим заболеванием рекомендуется проведение ЭКГ до и во время терапии Интроном® А. Возникающие аритмии (в основном наджелудочковые), как правило, поддаются стандартной терапии, но могут потребовать и отмены Интрона® А.
Интрон® А не назначают пациентам с псориазом и саркоидозом из-за возможности обострения этих заболеваний, за исключением случаев, когда предполагаемая польза от лечения оправдывает потенциальный риск.
Предварительные данные свидетельствуют о том, что терапия .интерфероном альфа может повысить риск отторжения трансплантата почки. Сообщалось также об отторжении трансплантата печени, однако причинно-следственной связи этого явления с терапией альфа-интерфероном не установлено.
При лечении альфа-интерферонами отмечались появление аутоантител и возникновение аутоиммунных заболеваний. Риск этих явлений выше у пациентов с имеющейся предрасположенностью к аутоиммунным заболеваниям. При появлении симптомов, схожих с проявлениями аутоиммунных заболеваний, следует провести тщательное обследование пациента и оценить возможность продолжения терапии интерфероном.
При монотерапии Нитроном®А редко наблюдались гипо- или гипертиреоз. В клинических исследованиях у 2,8% пациентов, получавших Интрон® А, развивалась патология щитовидной железы, которая контролировалась соответствующей терапией. Механизм развития такого действия неизвестен. Перед началом терапии Интроном® А следует определить концентрацию ТТГ. При выявлении любой патологии необходимо провести соответствующее лечение. Если медикаментозная терапия позволяет поддерживать ТТГ на уровне нормы, то назначение Интрона® А возможно. Если во время лечения возникло подозрение на нарушение функции щитовидной железы, следует определить уровень ТТГ. При нарушенной функции щитовидной железы лечение Интроном® А может быть продолжено, если уровень ТТГ удается поддерживать в пределах нормы при помощи медикаментозных средств. Отмена Интрона® А не приводила к восстановлению функции щитовидной железы.
Необходимо прекратить терапию Интроном® А пациентов с хроническим гепатитом при удлинении времени свертывания крови, т.к. это может быть признаком декомпенсации функции печени.
Для пациентов с хроническим гепатитом С
При применении Нитрона®А в комбинации с рибавирином следует руководствоваться также Инструкцией по медицинскому применению рибавирина.
В клинических испытаниях всем пациентам перед началом терапии Интроном® А проводили биопсию печени. Однако в определенных случаях (в том числе у больных с генотипами 2 и 3 вируса) лечение может быть начато без гистологического подтверждения диагноза. При решении вопроса о необходимости предварительного проведения биопсии следует руководствоваться существующими рекомендациями по тактике ведения таких больных.
Сочетанное инфицирование вирусом гепатита С и ВИЧ
У пациентов, инфицированных одновременно вирусом гепатита С и ВИЧ и получающих высокоактивную антиретровирусную терапию (ВААРТ) может развиваться молочнокислый ацидоз. В связи с этим при назначении Интрона® А и рибавирина в дополнение к ВААРТ следует проявлять повышенную осторожность.
При наличии сформированного цирроза риск декомпенсации функции печени и смерти у больных, инфицированных одновременно вирусом гепатита С и ВИЧ, повышен. Назначение Интрона® А (без рибавирина или в комбинации с рибавирином) в дополнение к проводимой терапии у данной группы больных может еще более увеличить этот риск.
Одновременное проведение химиотерапии
Применение Интрона® А в комбинации с химиотерапевтическими препаратами (цитарабин, циклофосфамид, доксорубицин, тенипозид) повышает риск развития токсических эффектов (способствует усилению их тяжести и увеличению продолжительности), которые могут угрожать жизни или привести к летальному исходу (вследствие повышенной токсичности при совместном применении препаратов). Наиболее частыми токсическими эффектами являются мукозиты, диарея, нейтропения, нарушения функции почек и электролитного баланса. Учитывая риск и тяжесть токсических эффектов, необходимо тщательно подбирать дозы Интрона® А и химиотерапевтических средств.
Данные лабораторных исследований
Перед началом лечения Интроном® А и систематически в процессе терапии всем пациентам проводят общий клинический анализ крови (с определением лейкоцитарной формулы и числа тромбоцитов), биохимических показателей крови, включая определение уровня электролитов, печеночных ферментов, билирубина, общего белка и креатинина.
Во время терапии пациентов с хроническим гепатитом В или С рекомендуется следующая схема проведения контроля лабораторных показателей: 1, 2, 4, 8, 12, 16 недели и затем ежемесячно, даже после прекращения терапии, до решения врача о его необходимости. Если AЛT повышается до величины, вдвое или более превышающей исходное значение, лечение Интроном® А можно продолжать, при условии отсутствия признаков печеночной недостаточности. При этом определение ACT, протромбинового времени, щелочной фосфатазы, альбумина и билирубина следует проводить через каждые 2 недели.
У пациентов со злокачественной меланомой функцию печени и число лейкоцитов следует контролировать каждую неделю во время первой фазы лечения (индукции ремиссии) и ежемесячно - при проведении поддерживающей терапии.
При назначении Интрона® А в комбинации с рибавирином пациентам со сниженной функцией почек и в возрасте старше 50 лет, за ними следует установить тщательное наблюдение в связи с возможным развитием анемии.
Применение в педиатрии
Интрон® А может применяться у детей от 1 года при хроническом гепатите В и папилломатозе гортани. Клинические данные о применении Интрона® А у детей с другой патологией отсутствуют.
Применение при беременности и в период грудного вскармливания
Клинические данные о применении интерферона альфа-2b во время беременности отсутствуют.
В экспериментальных исследованиях на животных выявлено токсическое действие на репродуктивность. Значение этих данных для человека не известно.
Во время беременности Интрон® А применяют только в тех случаях, когда ожидаемая польза от терапии для матери превышает потенциальный риск для плода.
Не известно, выделяются ли компоненты препарата Интрон® А с грудным молоком.
Из-за возможного риска нежелательных эффектов препарата у младенцев, находящихся на грудном вскармливании, при необходимости применения препарата у матери следует прекратить кормление грудью.
Пациенты женского пола и партнёрши пациентов мужского пола должны применять два способа контрацепции во время лечения и в течение 6 мес после его завершения. У женщин, получавших терапию человеческим лейкоцитарным интерфероном, отмечалось снижение уровня эстрадиола и прогестерона.
Препарат следует с осторожностью применять у мужчин репродуктивного возраста.
ВЛИЯНИЕ НА СПОСОБНОСТЬ К УПРАВЛЕНИЮ ТРАНСПОРТНЫМИ СРЕДСТВАМИ И МЕХАНИЗМАМИ
Пациента необходимо предупредить в возможности развития слабости, сонливости, нарушений сознания на фоне терапии и рекомендовать избегать управления транспортными средствами и механизмами.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ
С осторожностью следует применять Интрон® А одновременно с опиоидными анальгетиками, снотворными и седативными средствами, с препаратами, потенциально оказывающими миелосупрессивный эффект, такими как зидовудин.
Интерфероны могут влиять на окислительные метаболические процессы. Это следует учитывать при одновременном применении с препаратами, метаболизирующимися путем окисления (в т.ч. с производными ксантина - аминофиллином и теофиллином). При одновременном применении Интрона® А с теофиллином необходимо контролировать концентрацию последнего в сыворотке крови, и при необходимости корректировать режим дозирования.
При применении Интрона® А в комбинации с химиотерапевтическими препаратами (цитарабин, циклофосфамид, доксорубицин, тенипозид) повышается риск развития токсических эффектов (их тяжести и продолжительности), которые могут быть угрожающими для жизни или привести к летальному исходу (вследствие повышенной токсичности при совместном применении препаратов).
При совместном применении Интрона® А и гидроксимочевины может повышаться частота развития кожного васкулита. Фармацевтическое взаимодействие
Интрон® А нельзя смешивать с другими лекарственными веществами кроме 0,9% раствора натрия хлорида.
ИНФОРМАЦИЯ О ПЕРЕДОЗИРОВКЕ
До настоящего времени не описано случаев передозировки, сопровождающихся какими-либо клиническими симптомами. Однако, как и при передозировке любого лекарственного средства, следует проводить симптоматическую терапию с мониторированием функций жизненно-важных органов и с регулярным контролем состояния пациента.
ФОРМА ВЫПУСКА
Во флаконах:
По 10 млн МЕ/1 мл (1 доза); 18 млн МЕ/3 мл (6 доз по 3 млн. ME); 25 млн МЕ/ 2,5 мл (5 доз по 5 млн ME) во флаконах бесцветного стекла.
По 1 флакону вместе с инструкцией по применению в картонной пачке.
В шприц-ручках:
По 18 млн МЕ/1,2 мл (6 доз по 3 млн ME); 30 млн МЕ/1,2 мл (6 доз по 5 млн ME); 60 млн МЕ/1,2 мл (6 доз по 10 млн ME) в шприц-ручках.
По 1 шприц-ручке в комплекте с 6 иглами и 6 салфетками (для дезинфекции кожи в месте введения) в пластиковом поддоне вместе с инструкцией по применению и листком-вкладышем с рекомендациями для пациентов по подготовке и выполнению подкожной инъекции в картонной пачке.
УСЛОВИЯ ХРАНЕНИЯ
При температуре от 2 до 8°С. Не замораживать.
Хранить в недоступном для детей месте.
УСЛОВИЯ ТРАНСПОРТИРОВАНИЯ
При температуре от 2 до 8°С.
Допускается транспортирование при температуре до 25°С не более 7 дней. В течение этого периода препарат может быть возвращен на дальнейшее хранение в холодильник (температура хранения от 2 до 8°С), срок годности препарата при этом сохраняется. Если же препарат не был использован и не был возвращен на хранение в холодильник в течение 7 дней, то дальнейшему применению он нe подлежит.
СРОК ГОДНОСТИ
Препарат во флаконах
10 млн ME - 1,5 года,
18 млн ME и 25 млн ME - 2 года;
Препарат в шприц-ручках
1 год 3 месяца
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК
По рецепту
НАЗВАНИЕ И ЮРИДИЧЕСКИЙ АДРЕС ПРОИЗВОДИТЕЛЯ
Шеринг-Плау Лабо Н.В.,
Индуштриепарк 30, Б - 2220, Хейст-оп-ден-Берг, Бельгия
(собственный филиал Шеринг-Плау Корпорейшн/США)
ДИСТРИБЬЮТОР
Шеринг-Плау Сентрал Ист АГ, Люцерн, Швейцария
По вопросам качества и побочного действия обращаться
в ФГУН «ГИСК им. Л.А. Тарасевича Роспотребнадзора» по адресу:
119002, Москва, пер. Сивцев-Вражек, д. 41,
или в Представительство «Шеринг-Плау Сентрал Ист АГ» по адресу:
119048, Москва, ул. Усачева, 33, строение 1 (юридический адрес) или
117049, Москва, ул. Шаболовка, д. 10, строение 2 (фактический адрес)
|
|
Рекомендации для пациентов по подготовке и выполнению подкожной инъекции при помощи шприц-ручки ИНТРОН А
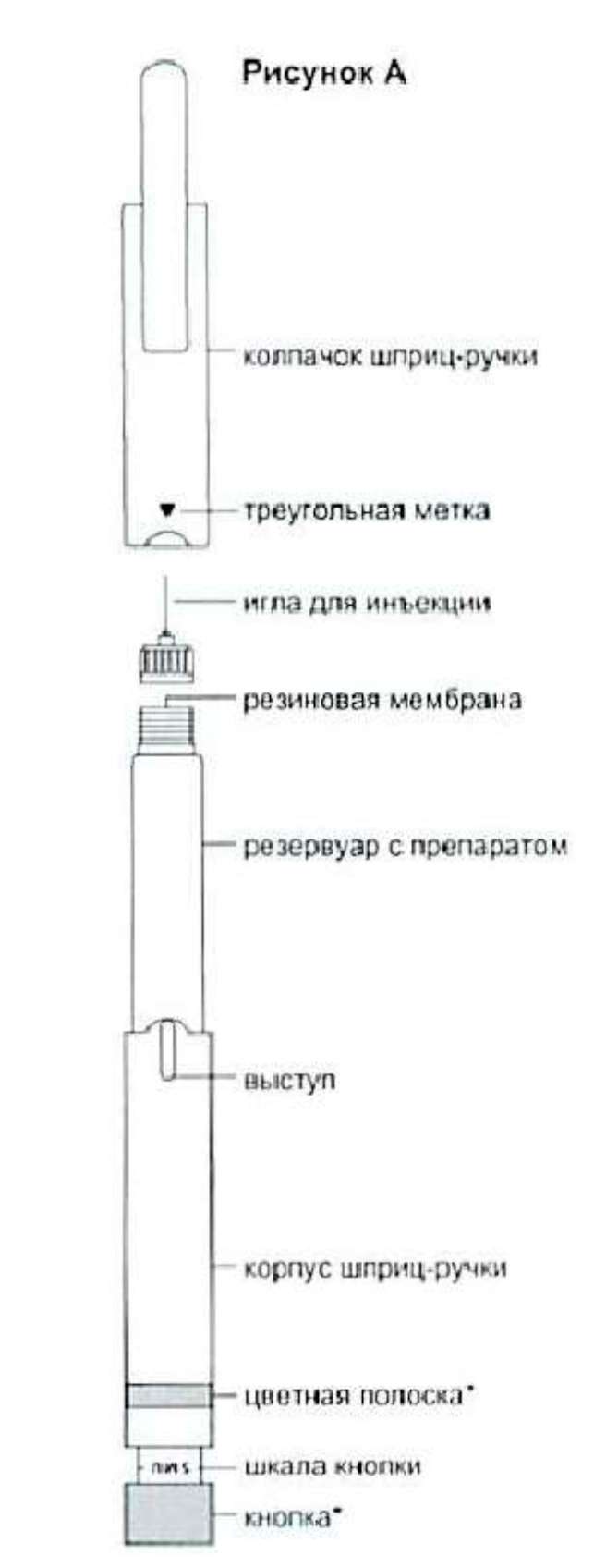
Шприц-ручки Интрон А бывают трех видов, в зависимости от содержания в них активного вещества - рекомбинантного интерферона альфа-2Ь - 18 млн МЕ, 30 млн МЕ или 60 млн МЕ. Каждая шприц-ручка предназначена для введения нескольких терапевтических доз. Объём дозы для каждого введения Вам укажет врач.
Устройство шприц-ручки:
* Примечание: цвет полоски, расположенной по окружности корпуса шприц-ручки, и кнопки индивидуален для каждого вида шприц-ручки и зависит от ее дозировки -коричневый для 18 млн МЕ, голубой для 30 млн МЕ и розовый для 60 млн МЕ.
Непосредственно перед введением препарата шприц-ручку необходимо подготовить следующим образом:
1. Вначале убедитесь в том, что Вы пользуетесь шприц-ручкой именно той дозировки, которую Вам выписал врач. Для этого проверьте цвет полоски и кнопки и дозировку, указанную на упаковке.
Шприц-ручку следует вынуть из холодильника за 30 минут до инъекции, чтобы раствор нагрелся до комнатной температуры.
Вымойте руки, продезинфицируйте место, на которое Вы будете класть шприц-ручку и ее детали, откройте коробку
2. Снимите колпачок со шприц-ручки.
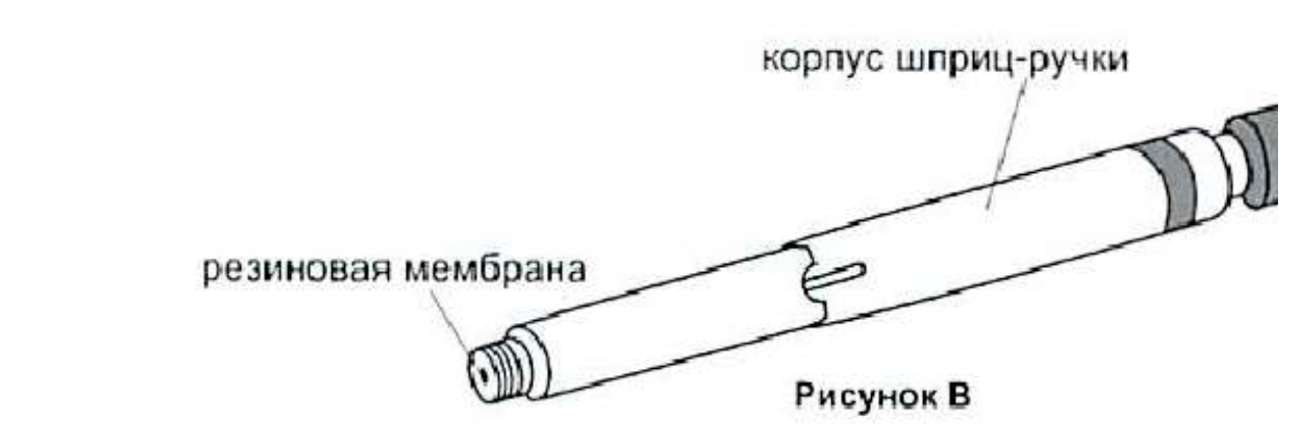
Убедитесь в том, что раствор в шприц-ручке бесцветный и прозрачный. Протрите резиновую мембрану спиртовой салфеткой для дезинфекции.
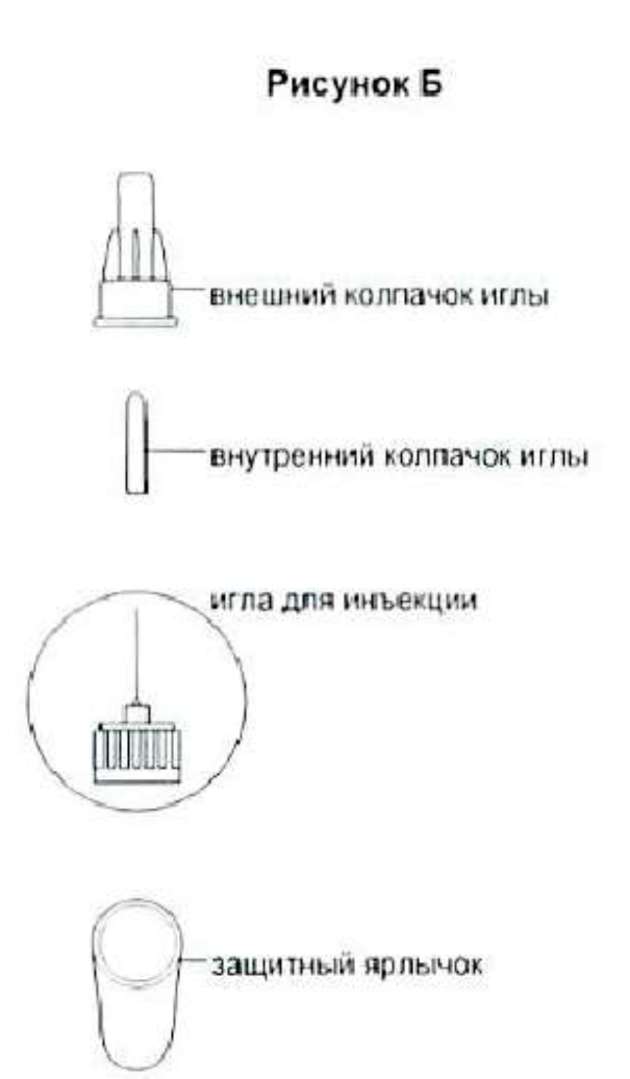
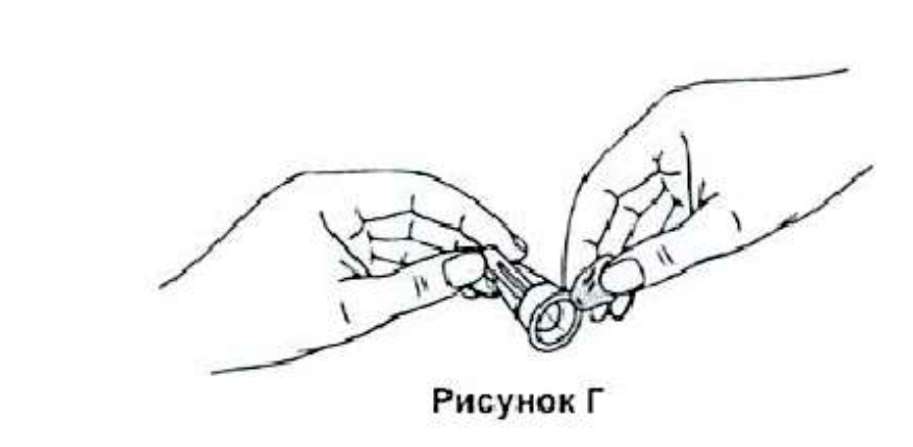
3. Снимите защитный ярлычок с иглы. При этом будет видна канюля иглы. Не снимайте внешний колпачок иглы на этом этапе.
4. Осторожно насадите иглу на шприц-ручку. При этом канюля иглы (см. этап 3) проколет резиновую мембрану, которую Вы ранее продезинфицировали. Теперь прикрутите иглу к ручке, вращая иглу по часовой стрелке.
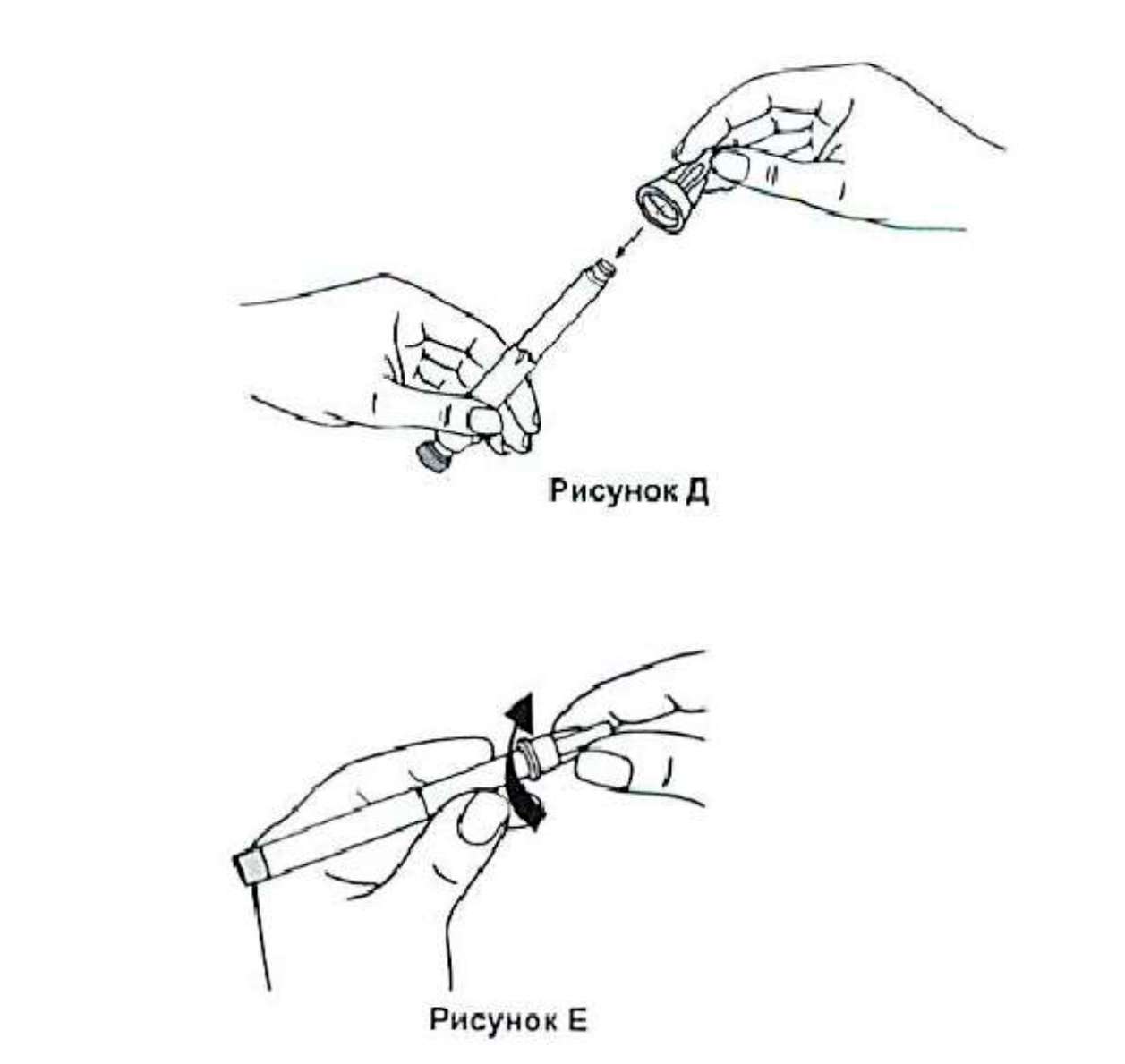
5. Аккуратно снимите с иглы внешний, а затем внутренний колпачки. Будьте осторожны, так как игла уже открыта. Сохраните внешний колпачок для безопасной утилизации иглы после ее использования.
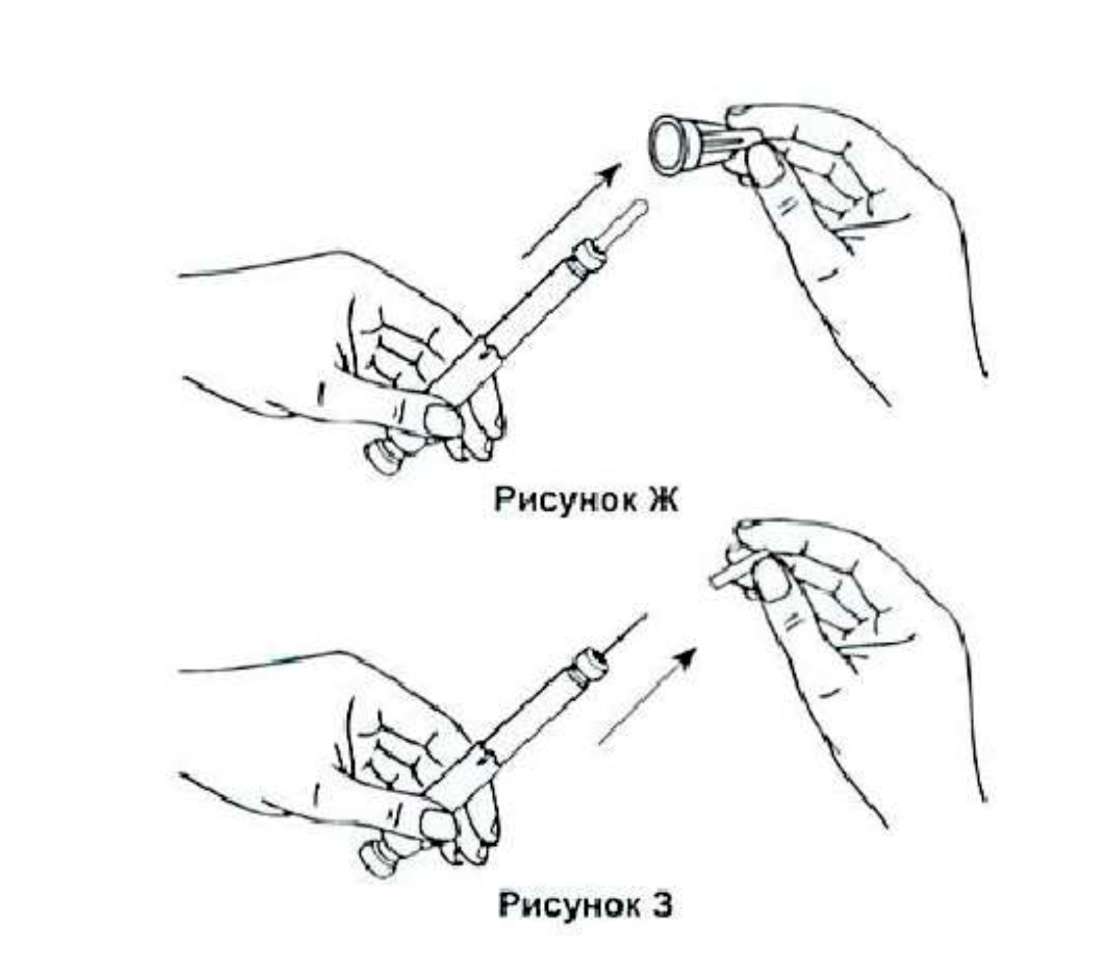
6. Шприц-ручка готова к применению. Во время хранения в игле и резервуаре может скопиться небольшое количество воздуха, пузырьки которого следует удалить перед инъекцией. Для этого:
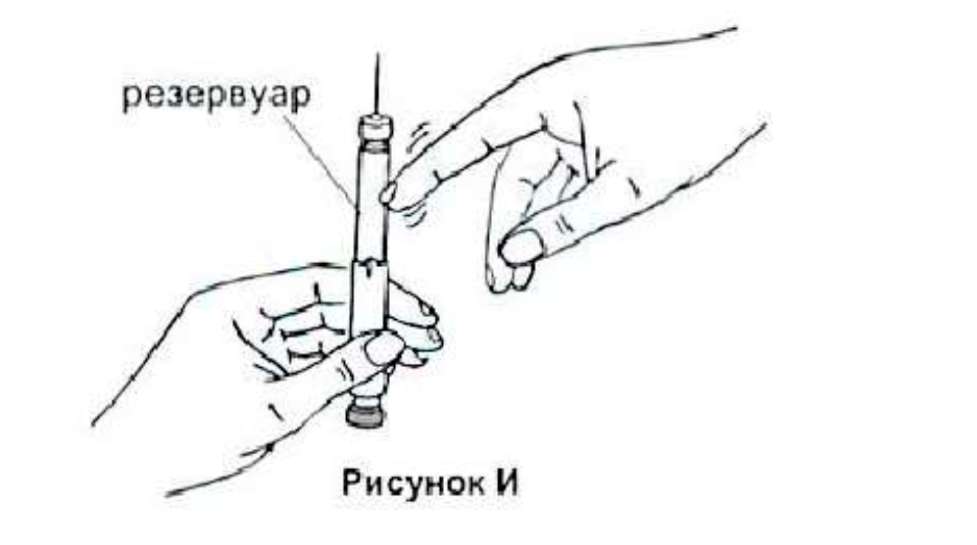
7. Держите шприц-ручку иглой вверх.
8. Постучите аккуратно по резервуару пальцем, чтобы пузырьки воздуха поднялись вверх и собрались под иглой.
Рисунок И
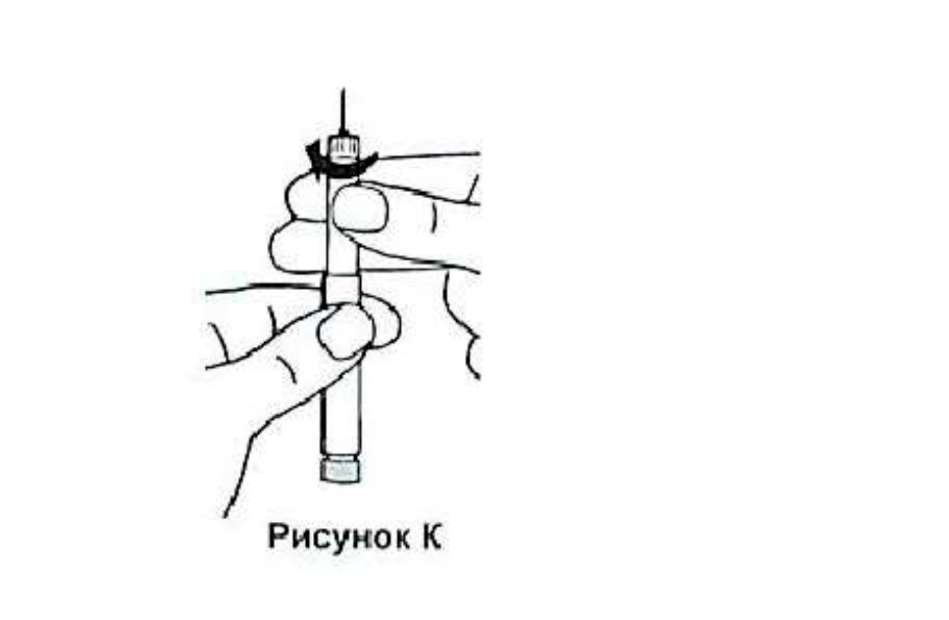
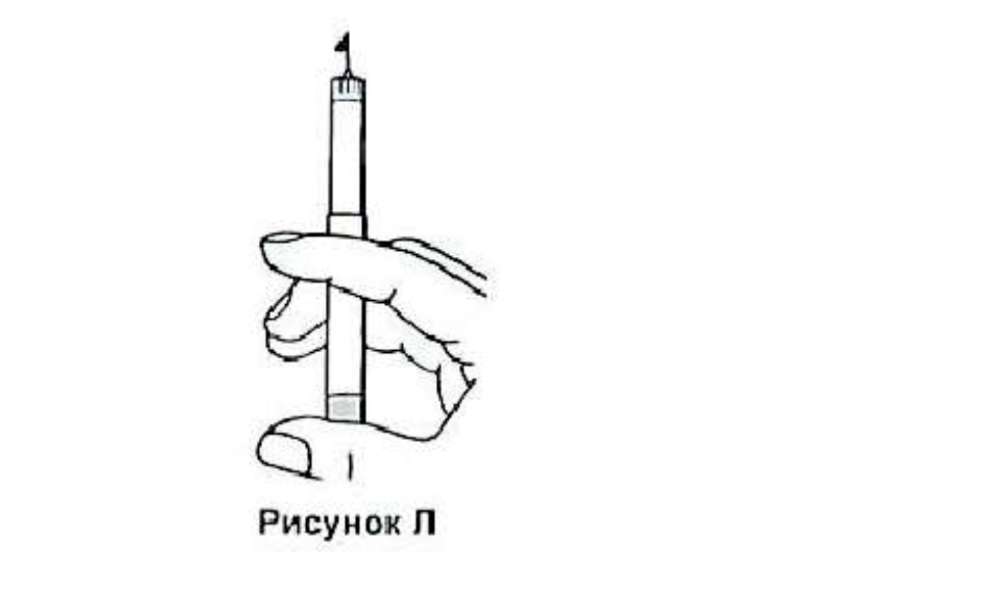
9. Удерживая шприц-ручку за корпус, поверните резервуар по часовой стрелке до щелчка.
10. Удерживая шприц-ручку иглой вверх, нажмите на кнопку. При этом на кончике иглы должна появиться капля.
11. Если капля не появится, то повторите этапы 7, 8 и 9.
Примечание: В шприц-ручке может остаться небольшое количество воздуха, однако это не важно, так как Вы удалили воздух из иглы, что позволит ввести точную дозу.
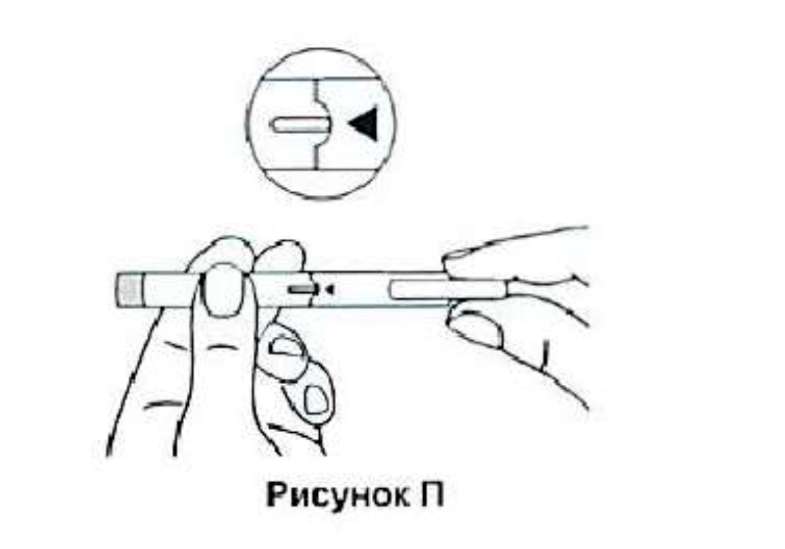
12. Закройте шприц-ручку колпачком. При этом треугольник должен находиться напротив выступа ручки.
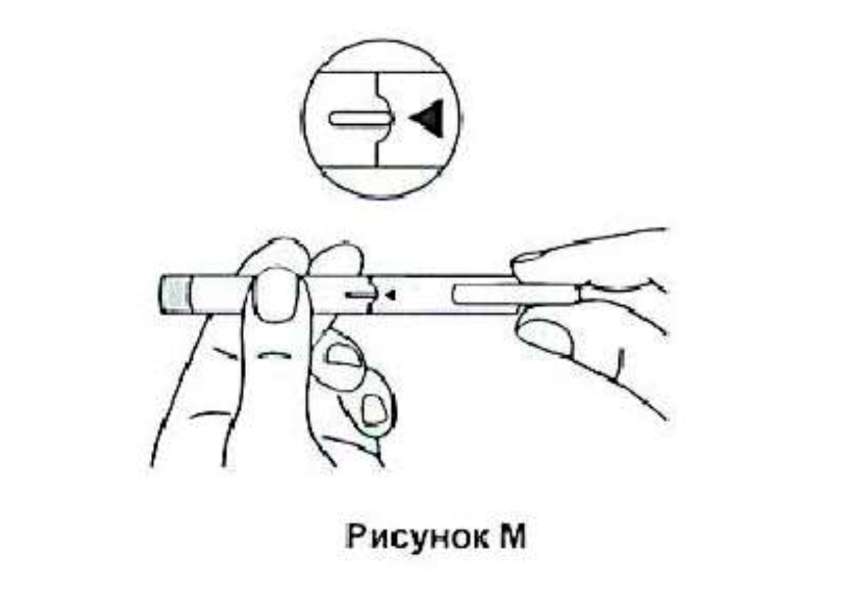
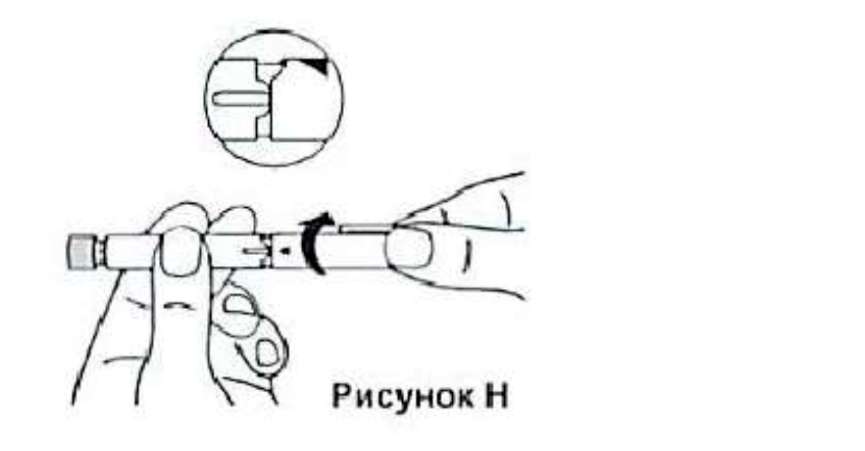
13.
Теперь Вы можете установить дозу. При выполнении следующего этапа удерживайте шприц-ручку за среднюю часть корпуса. Это обеспечит свободное движение кнопки и позволит установить необходимую дозу. 14. Чтобы установить дозу, одной рукой держите шприц-ручку за корпус горизонтально. Другой рукой поверните колпачок по часовой стрелке, как показано на рисунке. При этом кнопка начнет сдвигаться, что указывает на установку дозы. Чтобы установить необходимую дозу, поверните колпачок требуемое количество раз (см. таблицу ниже).
Шкала кнопки показывает установленную дозу. Убедитесь в том, что Вы установили ее правильно.
|
Число полных оборотов (и число щелчков) |
|
Шприц-ручка |
| Шприц-ручка |
||
|
18 млн МЕ |
30 млн МЕ |
60 млн МЕ |
|
1(5) 1,5 |
2,5 |
5 |
|
2(10) 3,0 |
5,0 |
10 |
|
3(15) 4,5 |
7,5 |
15 |
|
4(20) 6,0 |
10,0 |
20 |
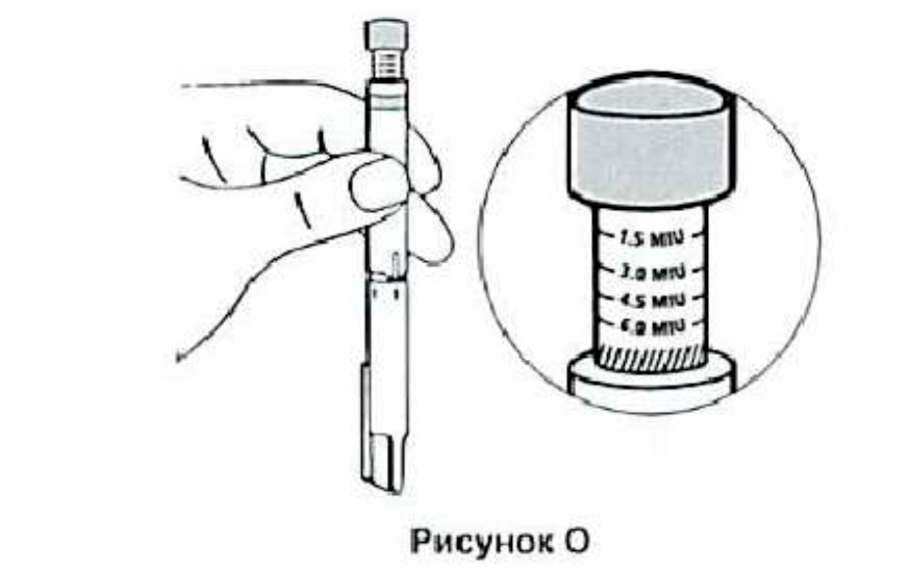
15. После каждого полного поворота колпачка треугольник должен находиться напротив выступа ручки. Если Вы установили дозу неправильно, то просто проворачивайте колпачок против часовой стрелки до тех пор, пока кнопка не вернется в исходное положение, а затем начните все сначала. Когда будет установлена необходимая доза, Вы можете произвести инъекцию.
16. Выберите место для инъекции. Рекомендуется производить инъекцию под кожу бедра, наружной поверхности плеча или живота (кроме области пупка и талии). Если подкожно-жировая клетчатка в области живота у Вас недостаточно развита, используйте для инъекции только бедро или наружную поверхность плеча (для инъекции в эту область Вам может понадобиться посторонняя помощь). Каждый раз выбирайте новое место для инъекции.
Протрите место для инъекции новой спиртовой салфеткой, дождитесь, пока кожа высохнет.
Снимите колпачок со шприц-ручки, осторожно соберите кожу в складку и воткните в неё иглу под углом около 45° как Вам ранее показывали врач или медсестра. Затем нажмите кнопку до упора.
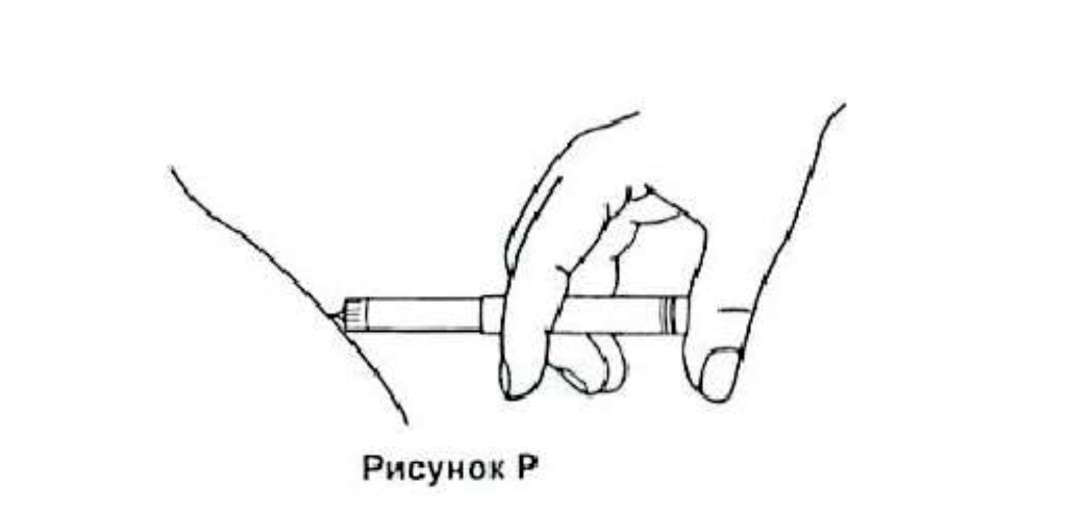
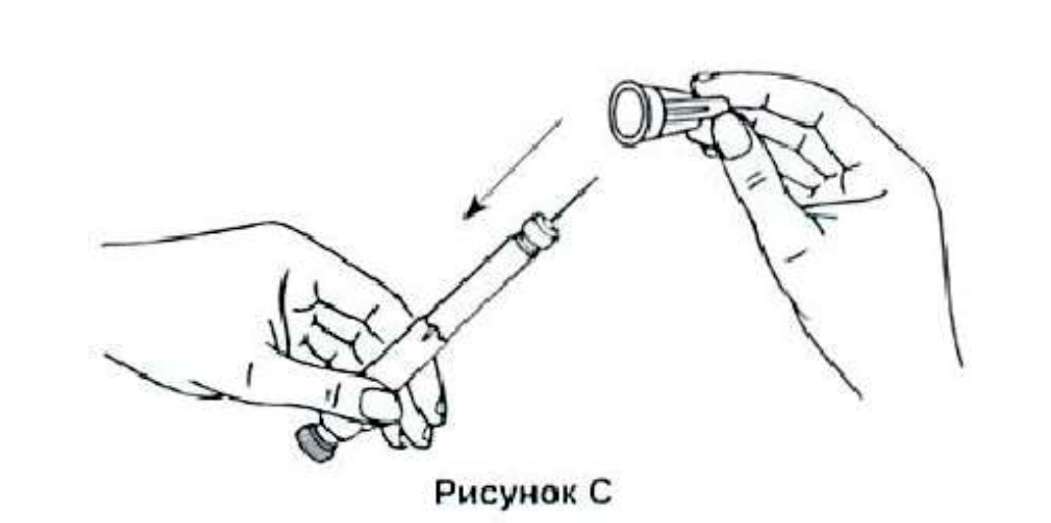
17. Не удаляйте иглу в течение нескольких секунд, чтобы раствор попал под кожу.
18. Осторожно закройте иглу внешним колпачком.
19. Открутите иглу от шприц-ручки, вращая ее против часовой стрелки. Затем осторожно отсоедините иглу и выбросьте.
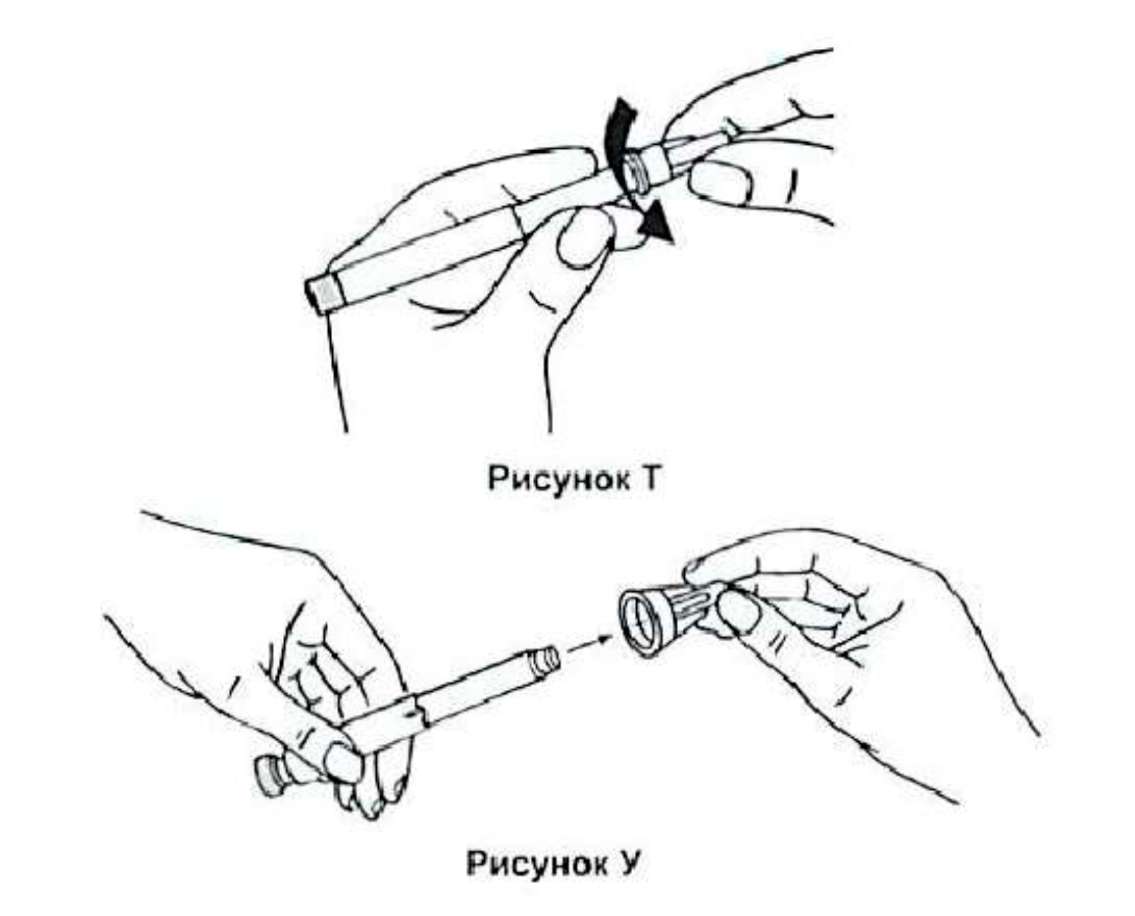
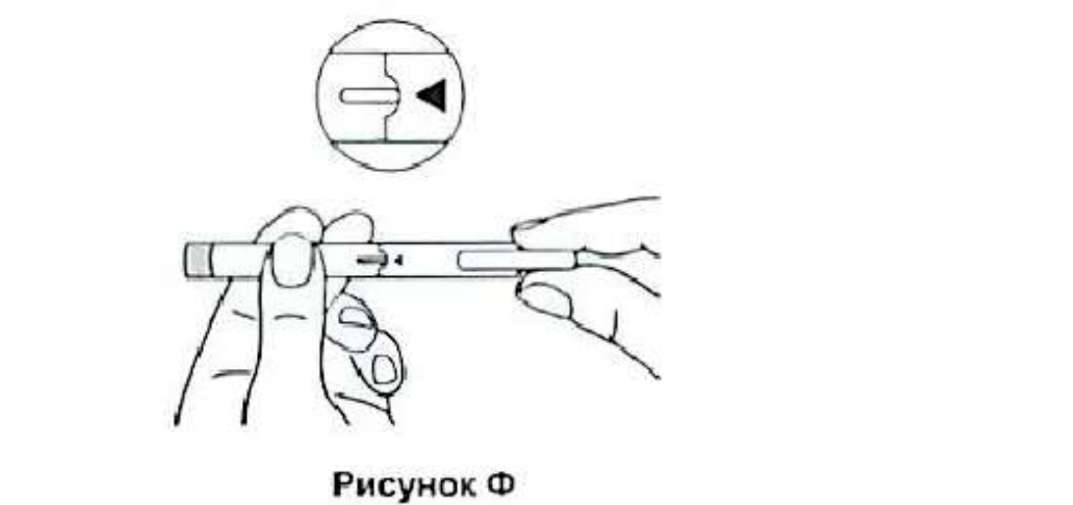
20. Закройте шприц-ручку колпачком шприц-ручки (треугольник должен находиться напротив выступа ручки) и положите ее в коробку. Поместите коробку в холодильник.
ВАЖНО
После того, как Вы введете себе полное число доз из шприц-ручки (обычно 6 или столько, сколько Вам скажет врач), в ней останется небольшое количество раствора.
Этим остатком пользоваться нельзя, учитывая невозможность точного дозирования.
Наличие избыточного количества раствора необходимо для того, чтобы вы могли удалить воздух из иглы перед инъекцией (этапы 5 - 10), сохранив при этом необходимое количество доз.
Комментарии
ПРАКТИКА ПЕДИАТРА
