Инстанил - инструкция по применению
См. откуда получены инструкции МЕДИ РУ
Регистрационный номер:
ЛП-005682Торговое наименование:
Инстанил®
МНН:
Фентанил
Лекарственная форма:
спрей назальный дозированный
Состав
Одна доза спрея назального (100 мкл) содержит:
Дозировка 50 мкг/доза:
Действующее вещество: фентанила цитрат – 78,50 мкг (эквивалентно фентанилу 50,0 мкг).
Вспомогательные вещества: натрия дигидрофосфата дигидрат, динатрия фосфата дигидрат, вода очищенная.
Дозировка 100 мкг/доза:
Действующее вещество: фентанила цитрат – 157,0 мкг (эквивалентно фентанилу 100,0 мкг).
Вспомогательные вещества: натрия дигидрофосфата дигидрат, динатрия фосфата дигидрат, вода очищенная.
Дозировка 200 мкг/доза:
Действующее вещество: фентанила цитрат – 314,0 мкг (эквивалентно фентанилу 200,0 мкг).
Вспомогательные вещества: натрия дигидрофосфата дигидрат, динатрия фосфата дигидрат, вода очищенная.
Описание
Бесцветный прозрачный раствор.
Фармакотерапевтическая группа
Анальгезирующее наркотическое средство. Относится к Списку II Перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в РФ.
Код ATX:
N02AB03
Фармакологические свойства
Фармакодинамика
Фентанил является синтетическим опиоидным анальгетиком, агонистом опиатных рецепторов (преимущественно μ-рецепторы) центральной нервной системы (ЦНС), спинного мозга и периферических тканей. Повышает активность антиноцицептивной системы, увеличивает порог болевой чувствительности. Интраназальное применение препарата Инстанил® сопровождается быстрой системной абсорбцией фентанила в фиксированной дозе и позволяет достичь скорого начала действия препарата. Он также обладает низкой аффинностью к опиатным δ- и κ-рецепторам. Основным терапевтическим эффектом фентанила является обезболивание. Вторичными фармакологическими эффектами являются угнетение дыхания, брадикардия, гипотермия, ригидность мышц, запор, миоз, физическая зависимость и эйфория. В отличие от других опиоидных анальгетиков значительно реже вызывает гистаминоподобные реакции.
Фармакокинетика
Линейность дозы
Фентанил обладает линейной кинетикой. У здоровых исследуемых линейность была показана для доз от 50 мкг до 400 мкг фентанила в форме назального спрея.
Исследование лекарственных взаимодействий было проведено с местным деконгестантом (оксиметазолином). Пациенты с аллергическим ринитом применяли назальный спрей оксиметазолина за один час до введения назального спрея фентанила. При сравнении показателей в группе с предварительным введением оксиметазолина и группе без предварительного введения оксиметазолина достигались сравнимые значения биодоступности (AUC) фентанила, хотя в присутствии оксиметазолина Сmax фентанила снижалась, а Тmax удлинялась приблизительно в два раза. Суммарные системные уровни фентанила у пациентов с аллергическим ринитом, не получавших ранее назальных вазоконстрикторов, сравнимы с таковыми у здоровых людей. Совместного использования с назальными вазоконстрикторами следует избегать (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Всасывание
Фентанил является высоколипофильным веществом. Кинетика распределения фентанила описывается трехкамерной моделью. Данные, полученные на животных, показывают, что после абсорбции фентанил быстро распределяется в головном мозге, сердце, легких, почках и селезенке, после чего следует более медленное распределение по мышцам и жировой ткани. Фентанил связывается с белками плазмы крови приблизительно на 80%. Абсолютная биодоступность фентанила в форме назального спрея составляет около 89%.
Согласно клиническим данным, фентанил очень быстро всасывается через слизистую оболочку носа. Введение одной дозы препарата Инстанил® в диапазоне от 50 мкг до 200 мкг фентанила на одну дозу онкологическим пациентам с толерантностью к опиоидным средствам приводит к быстрому достижению уровней Сmax от 0,35 до 1,2 нг/мл. Соответствующее среднее значение Тmax составляло 12-15 минут. Вместе с тем у здоровых добровольцев в исследовании зависимости системных уровней от вводимой дозы, наблюдались более высокие значения Тmax.
Распределение
После внутривенного введения фентанила изначальный период полураспределения составляет около 6 минут, сходный период полураспределения наблюдается после введения фентанила интраназально. Период полувыведения (Т1/2) фентанила в форме назального спрея у онкологических пациентов составляет приблизительно от 3 до 4 часов.
Метаболизм
Фентанил метаболизируется преимущественно в печени с помощью ферментов CYP3A4. Все метаболиты неактивны.
Выведение
Около 75% фентанила выводится с мочой, большей частью в виде неактивного метаболита, при этом на долю неизмененного активного вещества приходится менее 10%. Около 9% дозы обнаруживается в кале, главным образом в виде метаболитов.
Показания к применению
Препарат Инстанил® показан для купирования прорывной боли у взрослых пациентов, которые уже получают обезболивающую терапию опиоидными средствами по поводу хронической боли, связанной с наличием злокачественного новообразования.
Прорывная боль – это временное усиление боли, которое развивается на фоне персистирующего болевого синдрома, контролируемого пролонгированными формами анальгетиков и/или другими видами терапии.
Пациентами, которые уже получают обезболивание опиоидными средствами, считаются те, которые получают не менее 25 мкг/час фентанила в форме трансдермального пластыря или перорально в сутки: не менее 60 мг морфина, не менее 30 мг оксикодона, не менее 8 мг гидроморфона, или эквивалентную дозу другого опиоидного средства в течение одной недели или дольше.
Противопоказания:
- детский возраст до 18 лет;
- гиперчувствительность к действующему веществу или другим компонентам препарата;
- пациенты, не получающие поддерживающую опиоидную терапию (из-за повышенного риска угнетения дыхания);
- терапия острой боли, отличной от прорывной;
- тяжелое угнетение дыхания или тяжелое обструктивное заболевание легких;
- перенесенная ранее радиотерапия лицевой области;
- рецидивы носового кровотечения (см. раздел «Особые указания»).
Применение во время беременности и в период грудного вскармливания
Беременность
Достаточные данные по применению фентанила у беременных женщин отсутствуют. Исследования у животных показали наличие у препарата токсических свойств в отношении репродуктивной функции. Возможный риск подобных явлений для человека неизвестен. Препарат не следует применять в период беременности без крайней необходимости.
Длительная терапия фентанилом во время беременности может вызывать синдром отмены у новорожденного ребенка. Фентанил не рекомендуется применять во время родовой деятельности и родов (включая кесарево сечение), поскольку препарат проникает через плаценту и может привести к угнетению дыхания у плода. Если фентанил все же используется, должен быть приготовлен антидот для ребенка.
Лактация
Фентанил экскретируется с грудным молоком и может вызывать седативные эффекты и угнетение дыхания у детей, находящихся на грудном вскармливании.
Кормящим матерям не следует применять фентанил, и кормление грудью не следует начинать ранее, чем через 5 дней после последнего введения фентанила.
Фертильность
Данных по влиянию на фертильность у людей нет. В исследованиях на животных фертильность самцов и самок нарушалась при введении седативных доз препарата.
Способ применения и дозы
Лечение должно назначаться и контролироваться врачом, имеющим опыт применения опиоидной терапии у пациентов с онкологическими заболеваниями.
Врач должен учитывать потенциальную возможность злоупотребления фентанилом.
Способ применения
Препарат Инстанил® предназначен для интраназального введения. При введении препарата пациенту рекомендуется находиться в вертикальном положении, держа голову и туловище прямо. После каждого использования необходимо очищать наконечник назального спрея. Перед первым использованием препарата Инстанил® необходимо предварительно произвести несколько нажатий до появления мелкодисперсного аэрозоля, обычно требуется 3-4 нажатия.
Если препарат не использовался в течение более 7 дней, следует предварительно произвести одно нажатие перед введением первой дозы.
Во время предварительных нажатий препарат распыляется в воздух. Поэтому пациент должен быть проинструктирован о том, что распыление должно проводиться в хорошо проветриваемом помещении, не направляя флакон на людей, а также на удаленном расстоянии от поверхностей и предметов, с которыми могут контактировать люди, особенно дети.
Некоторое количество раствора может оставаться во флаконе после использования. Дальнейшие действия с использованными и неиспользованными флаконами препарата осуществляются в соответствии с действующим законодательством.
Пациент или его доверенное лицо несет персональную ответственность за использование наркотического средства с момента его получения.
Дозы
Для каждого пациента нужно проводить индивидуальное титрование дозы для достижения адекватного обезболивания на фоне переносимых нежелательных побочных реакций. Необходимо тщательное наблюдение за пациентами в период подбора дозы препарата. Титрование в сторону повышения дозы должно выполняться под контролем врача.
В клинических исследованиях доза препарата Инстанил® для купирования прорывной боли не зависела от суточной поддерживающей дозы опиоидных средств.
Максимальная суточная доза
Максимальная суточная доза препарата Инстанил® не должна превышать дозу, необходимую для купирования 4-х эпизодов прорывной боли, при этом не более 2-х доз на каждый из эпизодов прорывной боли с промежутком не менее 10 минут между дозами.
Как во время периода подбора дозы, так и во время поддерживающей терапии, пациенту необходимо подождать 4 часа перед введением следующей дозы препарата Инстанил®. В исключительных случаях, когда новый эпизод возникает раньше, пациент может использовать препарат Инстанил® снова, но перед применением должно пройти не менее 2 часов с момента последнего введения. Следует рассмотреть коррекцию дозы фоновой опиоидной терапии, если у пациента часто случаются эпизоды прорывной боли, интервалы между которыми менее 4 часов или если у пациента более 4-х эпизодов прорывной боли в течение 24 часов.
Титрование дозы
Прежде чем начинать подбор дозы препарата Инстанил®, следует удостовериться, что фоновая хроническая боль у пациента контролируется применением опиоидных анальгетиков на постоянной основе и у него наблюдается не более 4-х эпизодов прорывной боли в сутки.
Метод титрования дозы
Первоначальная доза должна составлять 50 мкг, которая вводится в один носовой ход с титрованием дозы по мере необходимости в диапазоне доступных дозировок (50. 100 и 200 мкг). Если адекватного обезболивания достичь не удалось, повторное введение такой же дозы можно производить не ранее чем через 10 минут. Каждый этап подбора дозы должен оцениваться на нескольких эпизодах прорывной боли.
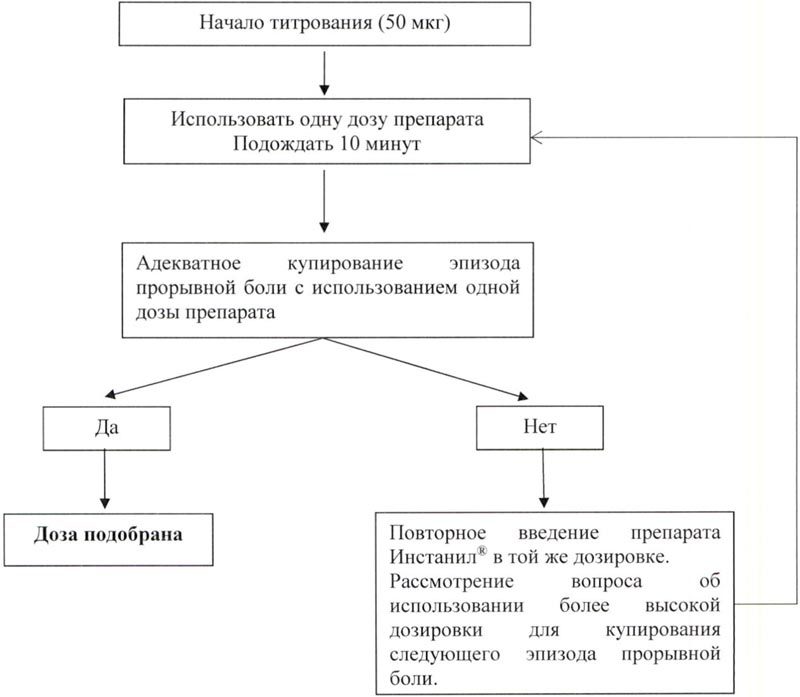
Поддерживающая терапия
После того, как в соответствии с вышеописанными шагами доза была определена, пациент должен оставаться на этой дозировке препарата Инстанил®. Если достаточного обезболивания не наступило, повторное введение такой же дозы препарата можно производить не ранее чем через 10 минут.
Коррекция дозы
Как правило, если пациенту для купирования прорывной боли требуется более одной дозы на один эпизод в течение нескольких эпизодов подряд, поддерживающую дозировку препарата Инстанил® следует повысить.
Если у пациента часто наблюдаются эпизоды прорывной боли с промежутком менее 4 часов или более 4-х эпизодов прорывной боли в течение 24 часов, следует рассмотреть возможность коррекции дозы фоновой опиоидной терапии с последующей оценкой боли. Если нежелательные реакции непереносимы или сохраняются в течение длительного времени, следует снизить дозу препарата Инстанил® или заменить его другими анальгетиками.
Прекращение терапии
Если эпизоды прорывной боли больше не повторяются, терапию препаратом Инстанил® необходимо немедленно прекратить. Терапию непрерывной фоновой боли следует оставить без изменений.
Полное прекращение терапии опиоидными средствами (при возникновении такой необходимости) должно проводиться постепенно с нисходящим титрованием дозы под тщательным наблюдением лечащего врача во избежание синдрома отмены.
Особые популяции пациентов
Лица пожилого возраста (65 лет и старше)
Количество данных по фармакокинетике, эффективности и безопасности использования препарата Инстанил® у лиц пожилого возраста ограничено. У данной группы пациентов может быть снижен клиренс, удлинен период полувыведения или может выявляться более высокая чувствительность к фентанилу по сравнению с более молодыми пациентами.
Следует проявлять осторожность при терапии пожилых, истощенных или ослабленных пациентов.
В клинических исследованиях у пожилых пациентов наблюдается тенденция в сторону титрования дозы до более низкой эффективной дозы по сравнению с пациентами моложе 65 лет. При подборе дозы препарата Инстанил® у пожилых пациентов следует проявлять особую осторожность.
Дети
Безопасность и эффективность применения препарата Инстанил® у детей младше 18 лет не установлены. Данные отсутствуют.
Нарушение функции почек
Следует проявлять осторожность при применении препарата Инстанил® у пациентов с умеренными и тяжелыми нарушениями функции почек (см. раздел «Особые указания»).
Нарушение функции печени
Следует проявлять осторожность при применении препарата Инстанил® у пациентов с умеренными и тяжелыми нарушениями функции печени (см. раздел «Особые указания»).
Инструкция по использованию контейнера с защитой от вскрытия детьми.
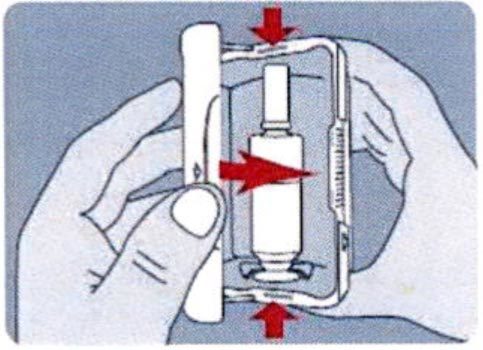
- Возьмите контейнер и удалите защитный элемент первого вскрытия.
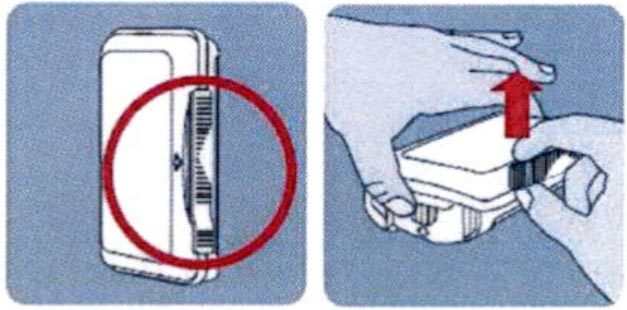
- Поместите большой и средний пальцы на боковые выступы, обозначенные стрелками ↑, и надавите внутрь.
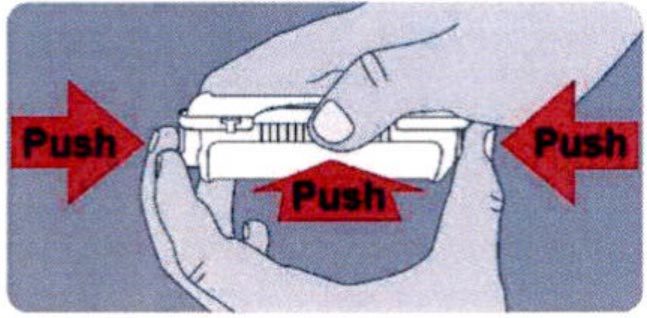
- Одновременно надавите внутрь другим большим пальцем на боковой выступ на передней поверхности, обозначенный стрелкой ↓.
- Продолжайте надавливать на все три точки.
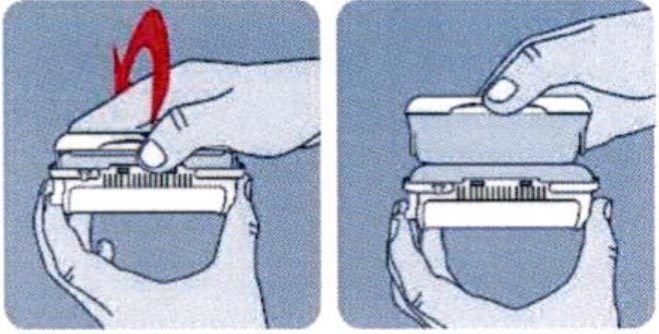
- Потяните за крышку и откройте ее.
- После применения зафиксируйте флакон в держателе и закройте пластиковый контейнер.
- Закрывая упаковку, убедитесь, что боковые выступы вошли обратно в прорези.
- Надавите с силой до щелчка, подтверждающего, что боковые выступы встали на место.
- Поставьте галочку в ячейке после применения каждой дозы препарата.
Карточки с ячейками для 10, 20 или 40 доз.
Инструкция по использованию многодозового флакона препарата Инстанил®.
- Перед применением необходимо очистить носовые ходы.
- Препарат Инстанил® применяется в вертикальном положении (сидя или стоя), держа голову и туловище прямо.
- Снимите защитный колпачок с флакона.
- Перед первым применением необходимо сделать 3-4 нажатия на помповое дозирующее устройство до появления мелкодисперсного облака. Недопустимо распыление спрея в направлении других людей.
- Флакон необходимо держать вертикально.
- Слегка наклоните голову вперед. Зажав один носовой ход, поместите назальный наконечник флакона в противоположный носовой ход (на глубину приблизительно 1 см). Если через 10 минут вам необходимо принять вторую дозу препарата Инстанил® для адекватного купирования эпизода прорывной боли, ее необходимо ввести в другой носовой ход.
- Во время спокойного вдоха через нос быстро и однократно нажмите на помповое дозирующее устройство. Даже если Вы не ощутили поступление лекарственного средства в носовую полость, при нажатии на помповое дозирующее устройство Вы получили необходимую дозу препарата.
- После применения всегда помещайте флакон в контейнер с защитой от вскрытия детьми.
Побочное действие
При применении препарата Инстанил® следует ожидать развития типичных для опиоидных средств нежелательных реакций. Зачастую большинство из этих реакций проходят или степень их тяжести снижается на фоне продолжающегося использования лекарственного препарата. Наиболее серьезными нежелательными реакциями являются угнетение дыхания (которое может привести к апноэ или остановке дыхания), недостаточность кровообращения, гипотензия и шок, следует тщательно наблюдать всех пациентов на предмет их развития.
Клинические исследования препарата Инстанил® проводились для оценки безопасности и эффективности его применения при купировании прорывных болей. С целью купирования хронической фоновой боли все пациенты также параллельно получали такие опиоидные средства, как морфин длительного высвобождения или трансдермальный пластырь с фентанилом. В связи с этим выделить отдельно нежелательные реакции препарата Инстанил® не представляется возможным. В таблице ниже указаны нежелательные реакции, которые были связаны с применением фентанила в форме назального спрея и/или других фентанилсодержащих лекарственных форм.
Частота побочных эффектов препарата оценивается следующим образом:
очень частые: ≥1/10;
частые: ≥1/100, <1/10;
нечастые: ≥1/1000, <1/100;
редкие: ≥1/10000, <1/1000;
очень редкие: <1/10000;
неизвестно (нельзя рассчитать по имеющимся данным).
Внутри каждой группы по частоте нежелательные реакции представлены в порядке уменьшения их серьезности.
| Системно-органный класс | Часто | Нечасто | Неизвестно |
| Нарушения психики | Зависимость, бессонница | Галлюцинации | |
| Нарушения со стороны нервной системы | Сонливость, головокружение, головная боль | Седация, миоклонус, парестезия, дизестезии, извращение вкуса | Судороги |
| Нарушения со стороны органа слуха и лабиринтные нарушения | Головокружение | Укачивание в транспорте | |
| Нарушения со стороны сердечно-сосудистой системы | Приливы крови, горячие приливы | Гипотензия | |
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Першение в горле | Угнетение дыхания, носовое кровотечение, изъязвления слизистой носа, ринорея | Перфорация перегородки носа |
| Нарушения со стороны желудочно-кишечного тракта | Тошнота, рвота | Запор, стоматит, сухость во рту | Диарея |
| Нарушения со стороны кожи и подкожных тканей | Гипергидроз | Болезненность кожных покровов, кожный зуд | |
| Общие расстройства и нарушения в месте введения | Повышение температуры | Утомляемость, недомогание, периферические отеки, синдром отмены* | |
| Травмы, интоксикации и осложнения | Падения |
*При введении фентанила интраназально наблюдались такие симптомы синдрома отмены опиоидных средств, как тошнота, рвота, диарея, тревожность, озноб, тремор, потливость. Если любые из указанных в инструкции нежелательных реакций усугубляются, или Вы заметили любые другие нежелательные реакции, не указанные в инструкции, сообщите об этом врачу.
Передозировка
Симптомы
Ожидается, что симптомы передозировки фентанила будут являться продолжением его фармакологических эффектов (например, летаргия, кома и тяжелое угнетение дыхания). Другие симптомы могут включать гипотермию, снижение мышечного тонуса, брадикардию и гипотензию. Признаками токсического действия являются глубокая седация, атаксия, миоз, судороги, а также угнетение дыхания, которое является основным симптомом.
Лечение
При появлении признаков угнетения дыхания немедленно должны быть приняты меры, которые включают физическое или вербальное воздействие на пациента. За этими мерами должно следовать введение специфического антагониста опиатных рецепторов, например налоксона. Угнетение дыхания после передозировки может сохраняться дольше, чем действие опиоидного антагониста. Период полувыведения антагониста может быть коротким, поэтому может возникнуть потребность в повторном введении или продолжительной инфузии налоксона. Прекращение наркотического эффекта фентанила может привести к резкому появлению боли и выбросу катехоламинов.
В случае клинической необходимости следует обеспечить и поддерживать проходимость дыхательных путей, возможно с помощью ротоглоточного воздуховода или эндотрахеальной трубки, также может потребоваться применение кислорода и искусственная вентиляция легких. Следует поддерживать надлежащую температуру тела и поступление достаточного количества жидкости.
При развитии тяжелой или длительной гипотензии следует оценить уровень гиповолемии и начать парентеральное введение необходимых количеств жидкости.
Взаимодействие с другими лекарственными средствами
Совместное применение фентанила с серотонинергическими препаратами, такими как селективные ингибиторы обратного захвата серотонина (СИОЗС) или ингибиторы обратного захвата серотонина и норадреналина (ИОЗСН), или ингибиторы моноаминоксидазы (ИМАО), может привести к повышению риска развития потенциально опасного для жизни состояния – серотонинового синдрома.
Ингибиторы моноаминооксидазы (МАО) потенцируют эффект опиоидных анальгетиков, поэтому не следует применять фентанил во время всего периода назначения ингибиторов МАО, а также в течение 14 дней после их отмены.
Фентанил преимущественно метаболизируется у человека посредством системы изофермента цитохрома Р450 ЗА4 (CYP3A4), поэтому возможно взаимодействие фентанила с параллельно применяемыми лекарственными препаратами, влияющими на работу CYP3A4. Совместное использование с лекарственными препаратами, индуцирующими CYP3A4, может снизить эффективность препарата Инстанил®. Совместное использование фентанила с сильными ингибиторами CYP3A4 (например, ритонавиром. кетоконазолом, итраконазолом, тролеандомицином, кларитромицином и нелфинавиром) или умеренными ингибиторами CYP3A4 (например, ампренавиром, апрепитантом, дилтиаземом, эритромицином, флуконазолом, фосампренавиром и верапамилом) может привести к повышению концентраций фентанила в плазме крови, что может привести к серьезным нежелательным реакциям, включая угнетение дыхания с летальным исходом.
Пациентов, получающих фентанил, совместно с умеренными или мощными ингибиторами С YP3A4, следует тщательно наблюдать в течение продолжительного периода времени. При повышении дозы следует проявлять осторожность.
В исследовании фармакокинетических взаимодействий было обнаружено, что при совместном использовании с оксиметазолином максимальная концентрация фентанила при интраназальном введении снижалась приблизительно на 50%, а время достижения Сmax (Тmax) удваивалось. ЭТО может снизить эффективность препарата Инстанил®.
Рекомендуется избегать одновременного применения препарата Инстанил® и назальных деконгестантов.
Совместное использование с другими лекарственными препаратами, подавляющими активность центральной нервной системы, включая другие опиоидные средства, седативные или снотворные, общие анестетики, фенотиазины, транквилизаторы, миорелаксанты, антигистаминные препараты с седативным действием и алкоголь, может привести к аддитивному седативному эффекту.
Совместное использование с частичными опиоидными агонистами/антагонистами (например, бупренорфином, налбуфином, пентазоцином) не рекомендуется. Они обладают высоким сродством к опиатным рецепторам и относительно низкой внутренней активностью, и поэтому могут уменьшать анальгетический эффект фентанила, а также способны провоцировать симптомы отмены у пациентов с зависимостью к опиоидным средствам.
Совместное использование фентанила с другими лекарственными препаратами (кроме оксиметазолина), вводимыми интраназально, в клинических исследованиях не изучалось. Для совместного лечения сопутствующих заболеваний вместо препаратов, вводимых интраназально, рекомендуется использовать альтернативные лекарственные формы.
Особые указания
Аддиктивный потенциал и зависимость
При повторном использовании таких опиоидных средств, как фентанил, может развиваться толерантность, а также физическая и/или психологическая зависимость. Тем не менее при опиоидной терапии боли, связанной со злокачественным новообразованием, ятрогенная зависимость развивается редко.
Симптомы синдрома отмены
Симптомы синдрома отмены могут развиться при введении препаратов с антагонистическим действием на опиатные рецепторы (например, налоксона) или с комбинированным агонистическим/антагонистическим анальгетическим действием (например, пентазоцин, буторфанол, бупренорфин, налбуфин).
Угнетение дыхания
При использовании опиоидных анальгетиков может развиваться клинически значимое угнетение дыхания, поэтому следует наблюдать за пациентами на предмет выявления подобных эффектов. У пациентов, получающих длительную опиоидную терапию, развивается устойчивость к угнетению дыхания, следовательно риск угнетения дыхания у таких пациентов снижается. Совместное использование препаратов, подавляющих центральную нервную систему, может привести к повышению риска угнетения дыхания (см. раздел «Взаимодействие с другими лекарственными средствами»).
Хроническая обструктивная болезнь легких (ХОБЛ)
У пациентов с хронической обструктивной болезнью легких могут развиваться более тяжелые нежелательные реакции на опиоидные анальгетики. У таких пациентов опиоидные средства могут снижать активность дыхательного центра и повышать сопротивление в дыхательных путях.
Нарушение функции почек или печени
Следует проявлять осторожность при применении фентанила у пациентов с умеренными и тяжелыми нарушениями функции печени и почек. Оценка влияния нарушений функции печени и почек на фармакокинетику препарата Инстанил® не проводилась. Тем не менее было показано, что при внутривенном введении клиренс фентанила при нарушении функции печени и почек изменяется, что связано с изменениями со стороны метаболического клиренса и состава белков плазмы крови.
Повышение внутричерепного давления
Следует проявлять осторожность при использовании фентанила у пациентов с признаками повышения внутричерепного давления, нарушениями сознания и находящихся в коме.
У пациентов с опухолями головного мозга и травмами головы фентанил следует использовать с осторожностью.
Заболевания сердца
Фентанил может вызывать брадикардию, поэтому у пациентов с предшествующей или текущей брадиаритмиями фентанил следует использовать с осторожностью. Опиоидные средства могут приводить к гипотензии, особенно у пациентов с гиповолемией, поэтому фентанил у пациентов с гипотензией и/или гиповолемией следует использовать с осторожностью.
Серотониновый синдром
Следует проявлять осторожность при совместном использовании фентанила и препаратов, влияющих на серотонинергическую нейромедиаторную систему.
При совместном использовании с серотонинергическими препаратами, такими как селективные ингибиторы обратного захвата серотонина (СИОЗС), ингибиторы обратного захвата серотонина и норадреналина (ИОЗСН), и другими препаратами, нарушающими метаболизм серотонина (включая ингибиторы МАО), может развиться потенциально опасный для жизни серотониновый синдром. Это может произойти даже при использовании рекомендованных доз.
Серотониновый синдром может включать изменения психического состояния (например, возбуждение, галлюцинации, кому), нестабильность вегетативной нервной системы (например, тахикардию, колебания артериального давления, гипертермию), нервно-мышечные отклонения (например, усиление рефлексов, нарушение координации, ригидность) и/или симптомы желудочно-кишечного тракта (например, тошноту, рвоту, диарею). При подозрении на серотониновый синдром терапию фентанилом следует прекратить.
Заболевания носовой полости
Если у пациента во время применения препарата Инстанил® наблюдаются рецидивы носового кровотечения или неприятные ощущения в носу, следует рассмотреть возможность использования альтернативной лекарственной формы для купирования прорывной боли.
Простуда
Суммарные системные уровни фентанила у пациентов с простудой, не получавших ранее назальных сосудосуживающих средств, сравнимы с таковыми у здоровых людей. Для получения информации по совместному использованию с назальными сосудосуживающими средствами см. раздел «Взаимодействие с другими лекарственными средствами».
Влияние на способность управлять транспортными средствами и механизмами
Пациенты должны быть предупреждены о том, что им не следует управлять транспортными средствами и иными механизмами во время применения препарата Инстанил®, так как фентанил в форме назального спрея может вызывать головокружение, сонливость, нарушения зрения и негативно влиять на умственные и/или физические способности, необходимые для управления транспортными средствами и иными механизмами.
Форма выпуска
Спрей назальный дозированный 50 мкг/доза. 100 мкг/доза, 200 мкг/доза.
По 1,8 мл, 2,9 мл, 5,0 мл препарата (с расходом на 10, 20, 40 доз соответственно) во флаконе коричневого стекла (тип I) объемом 10 мл, снабженном помповым дозирующим устройством с наконечником и защитным колпачком из полипропилена. По 1 флакону с инструкцией по применению помещают в полипропиленовый контейнер с защитой от вскрытия детьми.
На фронтальную и оборотную стороны полипропиленового контейнера наклеивают этикетки. На фронтальной стороне часть этикетки прикреплена специальной липкой лентой, которая позволяет приподнимать этикетку. Под подвижную часть этикетки, край которой фиксирован к контейнеру, помещен вкладыш с указанием состава препарата, карточкой для учета доз и инструкции по использованию контейнера с защитой от вскрытия детьми. На контейнер под вкладыш наклеивают дополнительную этикетку.
Условия хранения
Хранить при температуре не выше 30 °С.
Хранить в соответствии с правилами хранения наркотических средств, внесенных в Список II Перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в РФ.
Хранить флакон строго вертикально!
Не замораживать.
Не использовать по истечении срока годности.
Хранить в недоступном для детей и посторонних лиц месте.
После применения всегда помещайте флакон в пластиковый контейнер с защитой от вскрытия детьми.
Срок годности
3 года. Препарат нельзя использовать по истечении срока годности.
Условия отпуска
Отпускают по рецепту, с ограничениями, предусмотренными для наркотических препаратов.
Владелец регистрационного удостоверения:
Такеда Фарма А/С,
Дюбендаль Алле 10, DK-2630 Тааструп, Дания
Takeda Pharma A/S,
Dybendal Alle 10, DK-2630 Taastrup, Denmark
Производитель/Выпускающнй контроль качества:
Такеда ГмбХ,
Такеда (завод Зинген), Роберт-Бош-Штрассе 8, 78224 Зинген, Германия
Takeda GmbH,
Takeda (Werk Singen), Robert-Bosch-Strasse 8, 78224 Singen, Germany
Претензии потребителей направлять по адресу:
ООО «Такеда Фармасьютикалс»
119048 Москва, ул. Усачева, д. 2, стр. 1;
Комментарии
ПРАКТИКА ПЕДИАТРА
