Современные возможности эффективного лечения ротавирусной инфекции у детей раннего возраста (результаты двойного слепого плацебоконтролируемого исследования лечебной эффективности анаферона детского)
СтатьиОпубликовано в журнале:
«Педиатрия » № 1, Том 91 2012
Н.Х. Тхакушинова, Н.Г. Соболева
Специализированная клиническая детская инфекционная больница, г. Краснодар, РФ
В ходе двойного слепого плацебоконтролируемого исследования у детей в возрасте от 2 до 3 лет со среднетяжелой формой ротавирусной инфекции (РВИ) доказана клиническая и противовирусная эффективность препарата Анаферон детский. Установлено, что 5-дневный курс лечения Анафероном детским, назначенный в течение первых 48 ч от начала заболевания в комплексе с базисными патогенетическими средствами, приводил к значимому сокращению длительности симптомов РВИ - рвоты, диареи, явлений метеоризма, болевого синдрома, лихорадки и других проявлений токсикоза, а также катаральных явлений со стороны респираторного тракта, по сравнению с плацебо-терапией, проводимой на фоне базисного лечения. Положительная динамика клинической картины сочеталась с ускорением элиминации ротавируса (РВ) из желудочно-кишечного тракта, что подтверждалось отрицательным результатом иммуноферментного анализа на антиген РВ у 90% детей на 5-е сутки лечения.
Ключевые слова: дети раннего возраста, ротавирусная диарея, вирусный гастроэнтерит, Анаферон детский.
Double-blind placebo-controlled trial performed in children aged 2-3 years with moderate rotaviral infection (RVI) proved clinical and anti-viral effect of Anaferon for children. The study showed that 5-days course of Anaferon for children started within 48 hours after RVI manifestation in combination with basic pathogenetic treatment, leaded to significant reduce of such RVI signs as vomit, diarrhea, flatulence, abdominal pain, fever and other signs of infectious toxicosis and catarrhal changes of respiratory tract in comparison with control group, receiving basic treatment and placebo. Positive dynamic of clinical presentations was associated with accelerated Rotaviruc (RV) clearance from gastrointestinal tract, which was confirmed by negative result of immunoassay on RV antigen in 90% of patients after 5 days of treatment.
Key words: infants, rotaviral diarrhea, viral gastroenteritis, Anaferon for children.
Острые кишечные инфекции (ОКИ) занимают ведущее место среди инфекционной патологии, уступая по частоте лишь гриппу и острым респираторным заболеваниям [1-3]. По данным международной статистики, до 70% гастроэнтеритов вызываются вирусами, причем основное значение среди вирусных диарей у детей принадлежит ротавирусной инфекции (РВИ) [4-8]. По оценкам экспертов ВОЗ, практически каждый ребенок в течение первых 5 лет жизни переносит ротавирусный гастроэнтерит. Дети младше 3 лет составляют до 70-80% заболевших РВИ [4, 5, 7, 8]. Спорадические заболевания РВИ регистрируются в течение всего года, однако большинство заболеваний, в отличие от других ОКИ, регистрируется в зимне-весенний период [6, 7]. Отчасти это объясняется высокой устойчивостью ротавирусов (РВ) во внешней среде, особенно при замораживании.
В течение последних 10 лет в Краснодарском крае возрос удельный вес РВИ в структуре ОКИ у детей от 0 до 14 лет. Соотношение РВИ к ОКИ бактериальной этиологии увеличилось от 1:10 в 2001 г. до 1:2,5 в 2010 г., что связано прежде всего с широким внедрением методов вирусологической диагностики. Повсеместное распространение в регионе имеют 4 серотипа РВ группы А (P8G1, P8G3, P8G4, P4G2), чаще всего вызывающие развитие ротавирусной диареи.
РВ, поражающие «зрелый» эпителий микроворсинок тонкого кишечника, приводят к развитию дисахаридазной недостаточности. Не всосавшиеся вещества с высокой осмотической активностью нарушают реабсорбцию воды и электролитов, следствием чего является водянистая диарея - основной симптомом РВИ [4, 5]. Важно, что диарея возникает уже при низких уровнях вирусной нагрузки, поскольку воспалительные изменения в слизистой оболочке кишечника не играют роли в ее развитии [9, 10].
Ведущую роль в противовирусной защите, начиная с самого раннего этапа проникновения РВ в слизистую оболочку желудочно-кишечного тракта (ЖКТ), принадлежит системе интерферонов (ИФН). Благодаря ингибированию процессов транскрипции и трансляции вирусных матриц они способны подавлять репликацию многих РНК- и ДНК-содержащих вирусов [9, 11].
В настоящее время в педиатрической практике широко применяется индуктор эндогенных ИФН - Анаферон детский, разработанный специально для лечения вирусных инфекций у детей [12-14].
Принимая во внимание имеющийся опыт применения Анаферона детского при лечении кишечных инфекций вирусной этиологии [15], в настоящем исследовании мы оценивали эффективность данного препарата при лечении РВИ у детей раннего возраста. Клиническая эффективность Анаферона детского в лечении РВИ изучали в ходе рандомизированного двойного слепого плацебоконтролируемого клинического исследования (КИ) в параллельных группах. С целью оценки противовирусной активности препарата проводили исследование вирусовыделения в динамике наблюдения.
Материалы и методы исследования
Под нашим наблюдением находились 137 детей в возрасте от 1 месяца до 6 лет, поступивших в Специализированную клиническую детскую инфекционную больницу г. Краснодара по поводу РВИ средней степени тяжести. В КИ включали детей в возрасте от 2 до 3 лет, поступивших в стационар не позднее 2 суток от начала заболевания, у которых выявлялся синдром поражения ЖКТ по типу гастроэнтерита в сочетании с повышением температуры тела >38°C, интоксикационным синдромом и катаральными явлениями со стороны верхних дыхательных путей.
После подписания информированного согласия родителями/законными представителями пациента на этапе скрининга пациентам проводили начальное обследование, включавшее сбор данных анамнеза, оценку витальных функций, физикальное и лабораторное обследования. Этиологию заболевания подтверждали обнаружением антигенов РВ в фекалиях с помощью иммуноферментного анализа (ИФА) до начала терапии. Кроме РВ (54%), методом ИФА в фекалиях больных выявляли аденовирусы (11,7%), норовирусы (14,6%), сальмонеллы (8,8%), микст-инфекцию (РВ+другие возбудители - 10,9%). В ходе исследования пациент ежедневно осматривался врачом, фиксировали температуру тела, кратность рвоты и стула, степень выраженности других симптомов заболевания.
Пациентов не включали в КИ при подозрении/ наличии бактериальной инфекции или тяжелого заболевания, требующего назначения антибактериальных препаратов, обострении или декомпенсации хронических заболеваний, поливалентной аллергии в анамнезе.
Всем больным назначали базисную патогенетическую терапию: диетотерапию, оральную регидратацию, энтеросорбенты, дезинтоксикационные средства; кроме того, использовали пробиотики и биопрепараты, прокинетики, ферментативные препараты, отхаркивающие средства.
После включения в КИ пациентов рандомизировали в группу приема Анаферона детского либо группу плацебо. Анаферон детский/плацебо назначали по схеме: в первые сутки лечения -8 таблеток (в первые 2 ч по 1 таблетке каждые 30 мин, затем в оставшееся время суток еще 3 раза через равные промежутки времени), со 2-х по 5-е сутки препарат принимали 3 раза в день.
В окончательный анализ вошли результаты наблюдения 53 пациентов, которые соответствовали всем критериям включения, и у них отсутствовали все критерии исключения. Группу Анаферона детского составили 33 пациента, группу плацебо - 20 детей. Обе группы исходно были сопоставимы по всем демографическим и клинико-лабораторным данным, включая возраст (2-3 года), тяжесть заболевания (среднетяжелые формы), топике поражения кишечника (гастроэнтерит), этиологии (РВИ) и типу диареи («секреторная»).
Эффективность лечения в обеих группах оценивали на основании выраженности и длительности каждого из симптомов РВИ.
Статистическую обработку данных проводили с помощью статистического пакета Statistica 6.0 (StatSoft Inc.). Использовали методы параметрической (для непрерывных и интервальных переменных) и непараметрической (частотный анализ по категориальным переменным) статистики.Результаты и их обсуждение
Основными гастроинтестинальными симптомами у пациентов обеих групп были рвота (92%) и диарея (100%). Рвота появлялась одновременно с диареей или опережала ее, у 66% больных она была повторной и многократной (до 5-7 раз в сутки). Диарея выявлялась у всех детей; стул был обильным, водянистым, желтого цвета, без видимых патологических примесей; кратность дефекации колебалась от 3 до 8 раз в сутки. Более чем у половины пациентов клиническая картина заболевания проявлялась болевым абдоминальным синдромом (55%), вздутием живота (60%), урчанием по ходу кишечника (89%), метеоризмом (60%). Лихорадка выше 39 0С отмечалась у 9% больных, у остальных детей повышение температуры тела было в пределах 38,1-39 0С. У всех пациентов при поступлении в клинику выявлялись признаки эксикоза умеренной степени выраженности, синдром интоксикации в виде вялости, адинамии, снижения аппетита и умеренные катаральные проявления со стороны верхнего отдела респираторного тракта (затрудненное носовое дыхание, ринорея, кашель).
Анализ полученных результатов показал, что применение Анаферона детского в комплексе базисной терапии приводило к более быстрой положительной клинической динамике (рис. 1, 2). Так, уже на 2-й день лечения у 80% пациентов прекратилась рвота (против 60% в группе плацебо; р<0,05), на 3-и сутки она отмечалась лишь у 5% детей (против 25% детей группы плацебо; р<0,05).
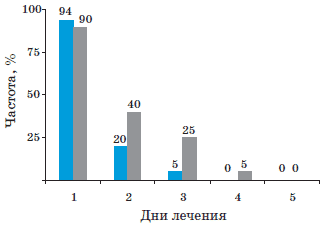
Здесь и на рис. 4 и 5: 1-й столбик - Анаферон детский, 2-й столбик - плацебо.
В группе больных, получавших Анаферон детский, уже к концу первых суток терапии в 55%, а на 2-й день - в 88% случаев водянистый характер стула сменился на кашицеобразный (против 15 и 39% в группе плацебо соответственно; р<0,05). Одновременно с более быстрой нормализацией характера стула происходило сокращение и его частоты (рис. 2). На 2-е сутки применения Анаферона детского 45% пациентов имели однократный стул, на 3-й день эта цифра достигла 65%, на 4-й - 75% (против 20; 40 и 50% в группе плацебо соответственно; р<0,05).
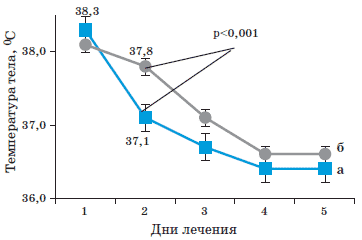
На рис. 3 представлена динамика среднесуточных значений температуры тела у пациентов обеих групп, которая отражает позитивное влияние Анаферона детского в комплексной терапии РВИ. Результатом включения препарата в схему лечения явилась более быстрая нормализация температуры тела, которая прогрессивно снижалась в течение первых 2 суток от начала терапии.
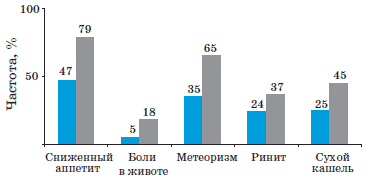
Частота регистрации других симптомов заболевания в двух сравниваемых группах также была в пользу Анаферона детского. В группе Анаферона значимо быстрее нивелировались такие симптомы, как сниженный аппетит, боли в животе, метеоризм, катаральные явления со стороны верхних дыхательных путей (ринит и сухой кашель). Частота выявления этих признаков РВИ на 3-и сутки наблюдения в зависимости от вида терапии представлена на рис. 4.
Итогом применения Анаферона детского в комплексе терапии РВИ явилась более быстрая обратная динамика всех симптомов инфекционно-воспалительного процесса. Уже на 3-й день лечения у 65% пациентов наступило клиническое выздоровление, а к 5-м суткам все дети данной группы клинически были здоровы.
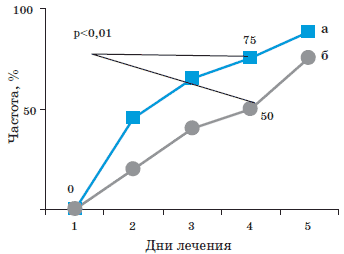
Здесь и на рис. 3: а - Анаферон детский, б - плацебо.
Рис. 3. Динамика температурной кривой в 1-5-й дни лечения наблюдаемых пациентов.
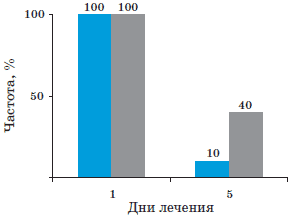
Отмеченная положительная динамика клинической картины РВИ на фоне терапии Анафероном детским сочеталась и во многом объяснялась быстрой элиминацией РВ из ЖКТ. Повторное исследование методом ИФА на 5-е сутки лечения свидетельствовало о том, что у 90% детей вирусовыделение прекращалось. Комплекс базисной терапии без включения Анаферона детского не позволял достичь подобного результата и антиген РВ в копрофильтрате повторно определялся у 40% пациентов группы плацебо (рис. 5).
Следует подчеркнуть, что в группе Анаферона детского нежелательных явлений зарегистрировано не было, все дети хорошо перенесли курс лечения, что еще раз подтвердило известную безопасность этого лекарственного средства.
Таким образом, проведенное КИ показало, что включение на ранних сроках в комплексную терапию РВИ Анаферона детского обладает выраженной терапевтической эффективностью. Доказано положительное влияние препарата на длительность и степень выраженности основных клинических симптомов РВИ - рвоты, диареи, явлений метеоризма, болевого синдрома, лихорадки и других проявлений токсикоза, а также катаральных изменений со стороны респираторного тракта. Клиническая эффективность Анаферона детского обусловлена его активирующим влиянием на противовирусную резистентность и иммунный ответ [8, 12, 13, 15], что обеспечивает ускоренную санацию организма от РВ, несмотря на известную склонность последнего к длительной персистенции [5, 6, 8]. Применение Анаферона детского в течение 5-дневного курса терапии приводило к элиминации вируса у 90% больных. Полученная противовирусная эффективность объясняется хорошо изученными и описанными эффектами препарата на продукцию ИФН α/γ и рецепцию ИФНγ, а также функциональную активность фагоцитов и NK-клеток [8, 12, 13, 15]. Интерфероногенная активность Анаферона детского, как доказано в многочисленных исследованиях, в том числе при РВИ у детей [8], оказывает позитивное влияние на различные звенья гуморального и клеточного противовирусного иммунного ответа: повышает продукцию антител (включая секреторный IgA), активизирует функции Т-эффекторов, Т-хелперов, повышает выработку цитокинов T-хелперами первого (ИФНγ, ИЛ2) и второго (ИЛ4, 10) типа, нормализует (модулирует) их баланс. Итогом антивирусной и иммуномодулирующей активности Анаферона детского при РВИ является снижение концентрации вируса в пораженных тканях ЖКТ и повышение скорости элиминации вируса.
Быстрая санация организма на фоне лечения Анафероном детским имеет важное значение и для конкретного пациента, и для детской популяции в целом, поскольку предотвращает пролонгированное вирусовыделение реконвалесцентами и способствует снижению уровня спорадической и вспышечной заболеваемости РВИ.
Противовирусная и клиническая эффективность Анаферона детского, а также его безопасность, подтвержденная результатами проведенного исследования, позволяют использовать препарат для лечения вирусных диарей у детей, в том числе, у детей раннего возраста.
Литература
- Atkins KE, Shim E, Pitzer VE, Galvani AP. Impact of rotavirus vaccination on epidemiological dynamics in England and Wales. Vaccine. 2012; 30 (3): 552-564.
- Kamiya H, Nakano T, Kamiya H, et al. The Rotavirus Epidemiology Study Group. Rotavirus-Associated Acute Gastroenteritis Hospitalizations among Japanese Children Aged<5 Years: Active Rotavirus Surveillance in Mie Prefecture, Japan. Jpn. J. Infect. Dis. 2011; 64 (6): 482-487.
- Tai IC, Huang YC, Lien RI, et al. Clinical manifestations of a cluster of rotavirus infection in young infants hospitalized in neonatal care units. J. Microbiol. Immunol. Infect. 2011. Dec. 9. [http://www.sciencedirect.com/science/article/ pii/S1684118211001782].
- Wilhelmi I, Roman Е, Sanchez-Fauquier А. Viruses causing gastroenteritis. Clin. Microbiol. Infect. 2003; 9: 247-262.
- Guarino A, Dupont C, Gorelov AV, et al. The management of acute diarrhea in children in developed and developing areas: from evidence base to clinical practice. Expert. Opin. Pharma-cother. 2012; 13 (1): 17-26.
- Васильев Б.Я., Васильева Р.И., Лобзин Ю.В. Острые кишечные заболевания. Ротавирусы и ротавирусная инфекция. СПб.: Лань, 2000: 267 с.
- Учайкин В.Ф. Решенные и нерешенные проблемы инфекционной патологии у детей. Детские инфекции. 2003; 4: 3-7.
- Тихомирова О.В., Сергеева Н.В., Агсенов ОА. Рота-вирусная инфекция у детей. Рос. вестн. перинатологии и педиатрии. 2004; 49 (5): 51-56.
- Yu TH, Tsai CN, Lai MW, еt al. Antigenemia and cytokine expression in rotavirus gastroenteritis in children. J. Microbiol. Immunol. Infect. 2011. Dec. 12. [http://www.sciencedirect.com/ science/article/pii/S1684118211002325].
- Lunch М, Shieh WJ, Tatti K, et al. The pathology of rotavirus-associated deaths, using new molecular diagnostics. Clin. Infect. Dis. 2003; 37: 1327-1333.
- Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы. М.: Гэотар-Медиа, 2005: 356 с.
- Эпштейн О.И. Сверхмалые дозы (история одного исследования). М.: Изд-во РАМН, 2008: 336 с.
- Dugina Y, Tarasov S, Elfimova U, et al. Clinical efficacy of anaferon, a novel oral antibody therapeutic, in pediatric acute viral gastroenteritis. 25th International Congress of Pediatrics. Athens - Greece, 2007: 526.
- Martyushev-Poklad AV, Sergeeva SA, Dugina JL, Epstein OI. Anaferon an oral anti-interferon gamma antiviral clinical efficacy in common pediatric viral infections. Acta Pharmacologica Sinica. 2006; 27 (Suppl. 1): 52.
- Тихомирова О.В., Ныркова О.И., Раздьяконова И.В. и др. Место противовирусной терапии в лечении острых кишечных инфекций у детей. Детские инфекции. 2008; 4: 51-55.
Комментарии
ПРАКТИКА ПЕДИАТРА
