Контролируемая пациентом аналгезия - эффективный и безопасный метод обезбливания в послеоперационном периоде
Статьи| Предупреждение! Препарат рецептурного отпуска! Использовать только после назначения врача! |
Авторы: Никода В.В.
Издание: Российский научный центр хирургии РАМН
Аналгезия, контролируемая пациентом
В раннем послеоперационном периоде одной из основных причин неадекватного обезболивания является рутинное применение опиоидных аналгетиков "при болях" или в виде "плановых" инъекций в стандартных дозах, которые, по нашим данным, у 36-59% пациентов оказываются недостаточными (Лебедева Р.Н., Никода В.В., 1998). Психологические и личностные особенности пациента, его клиническое состояние, необходимость врачей или медсестры оценивать интенсивность боли и выбирать дозу аналгетика - далеко неполный перечень причин, затрудняющих подбор эффективной дозы аналгетика в послеоперационном периоде.
Важным направлением оптимизации эффективности обезболивающей терапии является разработка новых способов и методов "доставки" аналгетических средств в организм. Наряду с традиционными способами введения опиоидных аналгетиков - внутривенным, внутримышечным, подкожным, в настоящее время применяются трансдермальные наклейки (фентанил, бупренорфин), интраназальный спрей (буторфанол), таблетированные формы с пролонгированным действием (трамадол) и т.д. К методам "высоких технологий" обезболивания следует отнести регионарную аналгезию/анестезию, контролируемую пациентом аналгезию. Аналгезия, контролируемая пациентом (Patient Controlled Analgesia, PCA) или обезболивание "по-требованию", является альтернативой традиционно применяемому - "по показаниям" или плановому назначению аналгетика
Cущность метода
Принцип метода
Пациент самостоятельно, путем заранее установленных врачом доз осуществляет введение аналгетика (например, внутривенно) при помощи программируемого шприцевого перфузора. Обезболивание достигается в результате повторных введениий малых доз аналгетика. По сути при возникновении боли пациент титрует введение аналгетика, оценивает его эффект и определяет для себя наиболее приемлемый уровень боли. Принцип работы с КПА легко усваивается пациентами и 87% предпочитают его рутинному назначению "при болях".
Предпосылки разработки метода:
- метод введения малых доз опиоидов с коротким интервалом времени между инъекциями оказался более эффективным и безопасным способом обезболивания по сравнению со стандартной схемой назначения аналгетиков;
- индивидуальные потребности в аналгетике широко варьируют;
- пациент может наиболее объективно оценить интенсивность боли и эффективность проводимого лечения;
Основными преимуществами КПА перед традиционным назначением аналгетиков являются: обеспечение эффективного обезболивания согласно индивидуальным потребностям больного, быстрое достижение желаемого эффекта, сокращение времени, в течение которого пациент находится без обезболивания, стабильная концентрацию аналгетика в плазме крови, экономия времени медицинского персонала, снижение частоты развития побочных эффектов.
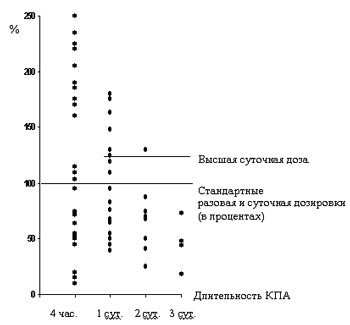
Прогнозирование эффективной разовой и суточной доз опиоидного аналгетика для каждого пациента является невыполнимой задачей. Оценка потребления морфина у оперированных пациентов в различные сроки послеоперационного периода показала его широкую вариабельность (рис.1). Заслуживающим внимания представляет тот факт, что в первые сутки, а особенно в первые часы начала КПА, потребность в морфине, значительно превышала стандартно рекомендуемые дозы. За первые 4 часа проведения КПА доза 10 мг морфина (стандартная разовая доза) оказалась достаточной только у 41% больных. В первые сутки послеоперационного периода рутинно назначаемая врачами доза (средняя суточная) морфина оказывается достаточной у 43% больных. У остальных пациентов для достижения адекватного обезболивания потребовались более высокие дозы. В последующие сутки расход морфина значительно снижается и составляет 10-30 мг/сут. Интересным представляется тот факт, что, несмотря на различную интенсивность боли в послеоперационном периоде, для безболивания потребовалось приблизительно одинаковое количество морфина. Таким образом, метод КПА обеспечивает адекватное обезболивание согласно индивидуальным потребностям пациента.
Рис. 1. Потребление морфина (выраженное в % к стандартным дозировкам) пациентами в различные сроки проведения КПА.
КПА позволяет быстро получить необходимый эффект. На схеме 1 (а) показано, что пациенту нет необходимости дожидаться действий медицинского персонала, как это происходит в случае традиционного обезболивания 1 (б). Пациент самостоятельно нажимает кнопку своего пульта и болеутоляющее действие развивается через 10-15 мин., в то время как после стандартного введения обезболивающего средства его эффект будет иметь место в лучшем случае через 45 мин.
Схема 1 (а). Контролирумая пациентом аналгезия: быстрое достижение обезболивающего эффекта.
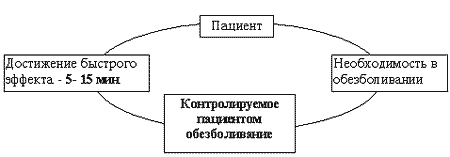
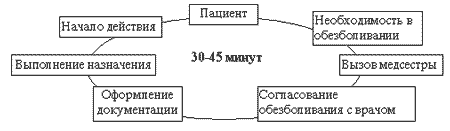
Схема 1 (б). Достижение обезболивающего эффекта при стандартном назначении аналгетика - внутримышечно при болях (адап. по Graves, 1983).
Введение малой, титрующей дозы опиоидного аналгетика позволяет поддерживать у пациентов его стабильную концентрацию в крови, что является существенным фактором, определяющим частоту, характер и тяжесть побочных эффектов при обезболивании в раннем послеоперационном периоде. Определяя у больных пожилого возраста концентрацию морфина в плазме крови при внутримышечном введении по "показаниям" и при внутривенном КПА в течение первых послеоперационных суток , Egbert A.M. (1990) показывает, что при последнем методе, колебания морфина в крови менее значимы. В результате при внутримышечном введении морфина отмечались чаще, чем при КПА, легочные осложнения (соответственно, 10% против 0%), выраженный снотворный эффект ( соответственно, 18% и 2,3%).
Cхема 2. Изменение содержания аналгетика в крови в зависимости от метода обезболивания: стандартная схема - "при болях", КПА (по Rue R.C. et al, 1996) - указаны внутримышечные инъекции аналгетика.
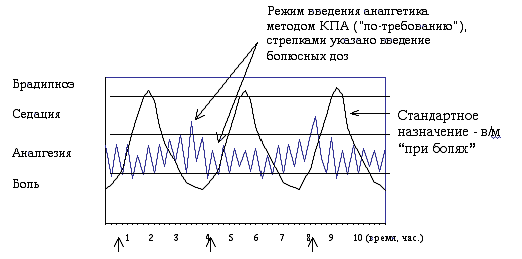
Очевидно, что при применении обычного способа обезболивания, назначаемого врачом "по показаниям", интенсивность боли изменяется волнообразно и пик приходится на момент обращения пациента к медицинскому персоналу с просьбой сделать "обезболиващее" (схема 2). Преимущество метода КПА в безопасности особенно заметно в ближайшие часы после поступления пациента из операционной, когда у пациента боль отсутствует или слабая по интенсивности. В этих случаях, на фоне остаточного действия аналгетиков или анестетиков, используемых интраоперационно, введение стандартных доз морфиноподобных обезболивающих средств представляет определенную опасность и неоправданно. Больному целесообразнее предложить КПА, при этом начальная доза не вводится. По мере нарастания боли пациент самостоятельно, посредством нажатия кнопки пульта, титрует болюсную дозу аналгетика до достижения эффекта.
КПА может применяться:
Правила и условия проведения КПА
В России имеется широкий выбор перфузоров с возможностью управления введения лекарственного средства самим пациентом. Введение лекарственного средства может осуществляться посредством стационарного или портативного перфузоров. Выпускаются одноразовые системы с различной модификацией введения лекарственных средств, в том числе аналгетиков.
В настоящее время важным аспектом применения КПА является выбор наиболее эффективных и безопасных аналгетиков, определение режима их введения. Для программирования введения аналгетика (например, промедола) врач должен установить его концентрацию после разведения аналгетика в физиологическом растворе. Выбор концентрации зависит от пути введения препарата, применяемого шприца и т.д. Наиболее удобной концентрацией для внутривенного введения является разведение 1-2 мг аналгетика в 1 мл физиологического раствора. Данный параметр выводится на экране прибора.
Начальная доза (НД) или насыщающая доза (мг или мкг) - первая доза аналгетика, вводимая пациенту посредством перфузора. Как правило, уже этой дозой удается заметно снизить интенсивность болевого синдрома у пациента.
Болюсная доза (БД) аналгетика (мл или мг, мкг) - объем раствора (соответственно, доза), поступающая пациенту при нажатии им кнопки пульта.
Скорость постоянной инфузии (мл/час или мг/час) - постоянное введение аналгетика, поступающего дополнительно с болюсными дозами независимо от участия пациента.
Для предотвращения у пациента развития возможной передозировки введения препарата в приборе предусмотрено программирование целого ряда показателей (локаут интервал, 4, 6 часовая предельно допустимая доза и т.д.).
Локаут интервал (минуты) - период времени, в течение которого повторное нажатие пациентом кнопки пульта не сопровождается введением обезболивающего лекарственного средства.
Максимально допустимая доза за фиксированный интервал времени (мг, мкг) - лимитированная (предельно допустимая) доза аналгетика, при превышении которой, введение аналгетика автоматически приостанавливается, а прибор подает звуковой сигнал.
Например,
| Аналгетик | Объем шприца | Кол-во промедола | Кол-во физиологич р-ра | Кон-ция промедола | Начальная доза | Болюсная доза | Локат интервал | Мax 4- час. доза | Скорость постоянной инфузии |
| Промедол | 50 мл | 100 мг (5 амп) | 45 мл | 2 мг/мл | 5 мг | 3 мг | 5-10 мин. | 40-50 мг | 0-0,5 мг/час |
В отделении интенсивной терапии и реанимации РНЦХ РАМН контролируемая пациентом аналгезия рутинно применяется в течение последних 5-ти лет. Нами изучена эффективность практически всех аналгетиков. В общей сложности применение КПА проводили у 215 пациентов (96% после операций), в том числе с использованием опиоидов - у 197 пациентов.
Контролируемое пациентом обезболивание является методом, который дает возможность в зависимости от вводимого аналгетика у 82-95% пациентов путем титрования подобрать эффективную индивидуальную дозу и осуществлять самоконтроль болевых ощущений. Интересно, что для обеспечения адекватного обезболивания в покое и при активизации пациентам могут требоваться дозы аналгетиков в 1,5-2,5 раза больше стандартно рекомендуемых (Ленбедева Р.Н., Никода В.В., 1998).
Результаты наших исследований по оценке эффективности КПА в зависимости от интенсивности болевого синдрома показывают, что обезболивание необходимо начинать как можно раньше. У пациентов, которым начинали КПА на фоне слабых болей (в покое), хорошие результаты имели место на 31% чаще, чем у пациентов с сильной болью (p меньше 0,004). Неадекватное обезболивание зарегистрировано нами у 18% пациентов при применении КПА на фоне сильной или невыносимой боли. В то же время, если начало КПА проводилось на фоне отсутствия или слабой боли в покое, неэффективное обезболивание отмечалось реже - у 3% (p меньше 0,05) пациентов.
Оценка качества КПА с применением различных опиоидных аналгетиков показывает, что использование пиритрамида более предпочтительно по сравнению с буторфанолом, промедолом, бупренорфином.
Показатель качества аналгезии (соотношение хороших результатов обезболивания к частоте нежелательных явлений) для промедола составил 1,6, а бупренорфина - 1,4, в то время как для пиритрамида он составил 3,7. Для промедола, морфина, бупренорфина, буторфанола тактика увеличения дозы нежелательна, поскольку с повышением дозы возрастает частота побочных явлений. В таких случаях необходимо сочетанное назначение опиоидных и неопиоидных аналгетиков. Мы согласны с мнением Rawal N. (1995), что эффективное обезболивание не столько нормализует функцию внешнего дыхания в послеоперационном периоде, сколько позволяет проведению физиотерапию, которая является особенно необходимой у пациентов после обширных операций на органах брюшной или грудной полости
По-видимому, важное значение в эффективности метода играет психологический фактор, поскольку пациент уверен, что в любой момент самостоятельно может "справиться с болью". Неотъемлемым требованием для проведения данной методики является адекватное сознание больного. Противопоказаниями для проведения метода контролируемой пациентом аналгезии являются:
Несомненно, данный метод обезболивания заслуживает самого пристального внимания клиницистов.
Безопасность применения КПА
Безопасность метода КПА складывается из 4-х основных факторов:
- наличие знаний у врачей и среднего медицинского персонала, обеспечивающего обезболивание в послеоперационном периоде (фармакология аналгетиков, программирование работы перфузора, прогнозируемые осложнения и т.д.);
- возможность наблюдения за состоянием пациента (периодичность осмотра средним медицинским персоналом и врачом - регистрация интенсивности боли, АД, ЧСС, ЧД, клинического состояния пациента и т.д.);
- технические неисправности перфузора и систем для введения препаратов;
- нежелательные реакции, обусловленные введением того или иного аналгетика.
Безопасность метода КПА во многом определяется выбранным аналгетиком и его дозой, которая потребуется для достижения адекватного обезболивания. Мы считаем, что обеспечение безопасности при проведении КПА опиоидными аналгетиками должно основываться на применении препаратов, в меньшей степени влияющих на состояние кардиореспираторной системы.
К другим мероприятиям, повышающим безопасность КПА, являются: раннее начало лечения боли, сочетанное введение аналгетиков с различным механизмом действия, использование в случае необходимости антидотов к аналгетикам (налоксон, доксапрам), мониторинг жизненно важных функций организма (ЧД, АД, ЧСС). Особую значимость эти меры приобретают у пациентов пожилого возраста, больных с хроническими обструктивными заболеваниями легких, сердечно-сосудистыми заболеваниями, страдающими ожирением и др. - в случаях, когда тактика повышения дозы опиоидного аналгетика с целью получения адекватного эффекта обезболивания усиливает риск развития нежелательных явлений: выраженной седации, угнетение дыхания, тошноты, рвоты, пареза ЖКТ, дисфункции желче- и мочевыводящих путей. Чтобы избежать возникновения побочных эффектов при назначении опиоидов, врач вынужден ограничивать суточную дозу препарата, что является одной из основных причин неадекватного обезболивания. Двойственность положения заставляет клиницистов применять дополнительно препараты других лекарственных групп, способных потенцировать обезболивающий эффект опиоидов. Важным аспектом при этом, является возможность снижения дозы опиоидов.
В наших исследованиях назначение НПВС (лорноксикама, кеторолака, кетопрофена) в виде плановых инъекций или постоянной внутривенной инфузии приводило к снижению потребления промедола, в раннем послеоперационном периоде, обеспечивало высокую аналгетическую эффективность. В этой связи, при отсутствии противопоказаний, группу НПВС мы рассматриваем в качестве "басиных" аналгетиков для послеоперационного обезболивания.
Не менее важной проблемой является необходимость теоретических знаний и практических навыков у врачей и среднего медицинского персонала для проведения этого метода обезболивания. Существуют специальные протоколы обезболивания пациентов в послеоперационном периоде. Оценку интенсивности боли в раннем послеоперационном периоде, стараться осуществлять не реже регистрации ЧСС, АД, ЧД.
Конечно, не совсем правильно считать, что проблему боли можно решить только внедрением высоко технологичных методов. В повышении эффективности обезболивания, не менее важен вопрос организации в ведущих клиниках, в много коечных больницах специализированной службы, занимающихся исключительно данной проблемой. Эффективность проводимой обезболивающей терапии, несмотря на некоторую условность такого выделения, рассматривается в качестве одного из основных факторов, прямо или косвенно влияющих на частоту и тяжесть осложнений, длительность пребывания больного в стационаре, на экономические затраты. Список литературы
1. Лебедева Р.Н., Никода В.В.// Фармакотерапия острой боли// Из-во Аир-Арт, Москва, 1998, стр. 184.
2. Rawal N. // Eur. J Anaesthesiol Suppl 1995 May; 10:47-52. Analgesia technique and post-operative morbidity.


