Ведение пациентов с последствиями ишемического инсульта
Статьи Опубликовано в журнале:«CONSILIUM MEDICUM»; ТОМ 13; № 2; стр. 72-76.
В.В.Захаров1, А.Ю.Ковтун2
Каждый год в мире регистрируется не менее полумиллиона новых случаев инсульта. 75% пациентов, перенесших острое нарушение мозгового кровообращения (ОНМК), выживают, однако у подавляющего большинства из них развивается большая или меньшая степень функционального ограничения. По официальной статистике, на сегодняшний день число инвалидов вследствие перенесенного инсульта превышает 2 миллиона человек [3]. Всемирная организация здравоохранения сделала предположение, что распространенность инсультов к 2025 г. возрастет не менее чем на 30%, в том числе в экономически благополучных странах [8]. Приведенные эпидемиологические данные обусловливают высокую актуальность проблемы ОНМК для неврологов и врачей других специальностей.
Не вызывает сомнений, что пациенты с последствиями инсульта составляют значительную долю амбулаторных неврологических больных, в особенности в старших возрастных группах. При ведении подобных больных необходимо руководствоваться двумя стратегическими задачами:
- осуществление вторичной профилактики повторных ОНМК;
- проведение медикаментозного и немедикаментозного лечения, коррекции имеющихся неврологических расстройств.
Вторичная профилактика повторного ишемического инсульта
Согласно современным преставлениям, ишемический инсульт (ИИ) не является самостоятельным заболеванием, но представляет собой патогенетически неоднородное осложнение различных сердечнососудистых заболеваний. В анамнезе ИИ означает серьезное неблагополучие сердечно-сосудистой системы, свидетельствует о декомпенсации имеющихся соматических заболеваний. Поэтому ИИ в анамнезе является важным предиктором повторного ОНМК и других ишемических событий (инфаркт миокарда, периферические тромбозы) в ближайшем будущем. По статистике, повторный ИИ развивается не менее чем у 25% пациентов, выживших после первичного нарушения мозгового кровообращения. Вероятность повторного ИИ в 15 раз превышает вероятность развития первичного ИИ среди лиц того же пола и возраста. При этом максимальный риск отмечается в первый год после перенесенного инсульта. Поэтому уже с первых часов ИИ необходимо начинать мероприятия, направленные на вторичную профилактику повторных ОНМК [7].
Вторичная профилактика ИИ должна включать модификацию образа жизни с целью воздействия на корригируемые факторы риска сосудистых событий (табл. 1) и медикаментозную терапию имеющихся сердечно-сосудистых заболеваний.
Таблица 1.
Немедикаментозные методы вторичной профилактики ИИ - модификация образа жизни
| - отказ от курения - отказ от злоупотребления алкоголем - снижение массы тела - умеренные физические нагрузки - сбалансированная диета с уменьшенным содержанием животных жиров |
Медикаментозная профилактика повторного ИИ, согласно общепринятым рекомендациям, должна включать использование антитромбоцитарных или антикоагулянтных препаратов, антигипертензивную и гиполипидемическую терапию (рис. 1) [7].
Рис. 1. Медикаментозная профилактика повторного ИИ. 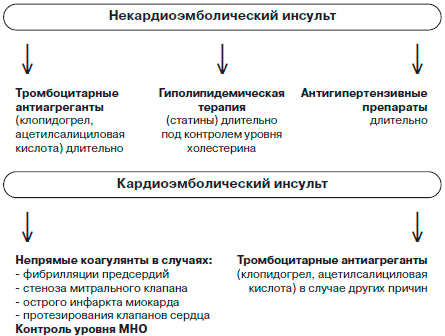
Ацетилсалициловая кислота должна быть назначена всем пациентам, перенесшим ИИ, как можно раньше (в первые часы возникновения симптоматики). Обычная доза составляет 75-150 мг/сут. Сочетание ацетилсалициловой кислоты с дипиридамолом достоверно понижает риск повторных нарушений мозгового кровообращения по сравнению с монотерапией ацетилсалициловой кислотой, но может вызвать обострение ишемической болезни сердца у пациентов со стенозом коронарных артерий. Альтернативным препаратом является клопидогрел в дозе 75 мг/сут, который в исследовании CAPRIE продемонстрировал больший профилактический эффект по сравнению с ацетилсалициловой кислотой [8, 11]. Предпринимались попытки использования комбинации ацетилсалициловой кислоты и клопидогреля, однако при этом достоверно чаще возникали серьезные геморрагические осложнения (исследование MATCH) [8, 11]. Антитромбоцитарные препараты (ацетилсалициловая кислота, дипиридамол, клопидогрель) не показаны пациентам, получающим тромболитическую или антикоагулянтную терапию.
У пациентов, перенесших кардиоэмболический инсульт вследствие фибрилляции предсердий, острого инфаркта миокарда, ревматического митрального стеноза, осложнений протезирования камер сердца, антикоагулянты предпочтительней антитромбоцитарных лекарственных средств. Препаратом первого выбора является непрямой антикоагулянт варфарин. Терапию антикоагулянтами проводят строго под контролем международного нормализованного отношения (МНО), которое должно держаться на уровне 2-3, а в случае с пациентами, имеющими протезированные клапаны сердца, 3-4 [7].
Антигипертензивные препараты показаны пациентам с ИИ в анамнезе как при наличии артериальной гипертензии, так и при так называемом высоком нормальном артериальном давлении (130-135 мм рт ст.). В настоящее время отдается предпочтение ингибиторам ангиотензинпревращающего фермента, антагонистам рецепторов к ангиотензинпревращающему ферменту типа 1 и антагонистам кальция [7].
Другим классом препаратов, необходимых для эффективной вторичной профилактики ИИ у пациентов, перенесших инсульт, являются гиполипидемические препараты или группы статинов. На основании результатов многочисленных исследований (в частности, SPARCL, 2006 г.), статины показаны всем пациентам с ИИ в анамнезе, независимо от уровня холестерина [19].
Важной проблемой для практикующего невролога является тактика ведения пациентов со стенозированием экстракраниальных артерий. Всем пациентам с ИИ в анамнезе необходима оценка состояния магистральных артерий головы. С этой целью может использоваться дуплексное сканирование экстракраниальных сосудов, компьютерная томография или магнитно-резонансная ангиография, по показаниям - рентгеноконтрастная ангиография. Сегодня доказана эффективность хирургической коррекции при стенозировании каротидных сосудов более чем на 70% при наличии транзиторных ишемических атак или ИИ в анамнезе (так называемый симптомный стеноз). В то же время консервативное ведение предпочтительней у пациентов со стенозами менее 50%. У пациентов со стенозами средней степени (50-69%) эффективность оперативного лечения попадает в многофакторную зависимость и степень стеноза не является единственной определяющей необходимость хирургического вмешательства [7].
Немедикаментозная реабилитация в восстановительном периоде ИИ
Инсульт занимает первое место в списке причин хронической инвалидизации. По эпидемиологическим данным, не менее чем у 40% пациентов, перенесших ИИ, формируется зависимость от членов семьи и/или медицинского персонала в повседневной жизни. Естественное течение инсульта таково, что в первые несколько месяцев (по некоторым данным, до 2-3 лет) после ОНМК наблюдается больший или меньший регресс неврологических нарушений. Важная задача нейропсихологов, логопедов и других специалистов -всячески способствовать более быстрому и значительному восстановлению поврежденных функций в это время.
Клиническое улучшение после перенесенного ИИ может быть связано с истинным восстановлением поврежденной функции или с достижением компенсации за счет неповрежденных функций. Согласно современным представлениям, в основе как истинного восстановления, так и достижения компенсации функционального дефекта лежат механизмы нейропластичности. Последнее определяется как способность различных отделов центральной нервной системы к реорганизации, а нейронов - к структурно-функциональным изменениям.
Восстановление нарушенных функций в первые дни после ИИ связано в основном со следующими факторами:
- регресс отека мозга;
- улучшение кровообращения в областях, пограничных с очагом повреждения;
- растормаживание функционально не действующих, но морфологически сохранных нейронов (прекращение диашиза) [5].
Одновременно или несколько позже происходит изменение баланса между торможением и возбуждением в пораженных участках головного мозга. Ранее находившиеся под тормозящим влиянием зоны резко повышают свою активность, влияя на другие отделы головного мозга. Наблюдаются значительные изменения синаптической передачи и возбудимости нейрональных мембран. При этом раньше всего репаративные процессы начинаются в месте повреждения и прилегающих к ней корковым областям и связям, а затем они затрагивают противоположное интактное полушарие. [17]. Так, функциональные нейровизуализационные исследования показывают, что уже через 7 дней в противоположной очагу гемисфере отмечается гипервозбудимость [11].
В подострую и хроническую фазы после перенесенного ИИ происходит образование дополнительных связей между нейронами за счет коллатерального спраутинга и формирования новых синапсов. Коллатеральный спраутинг начинает играть значительную роль на 2-3-й неделе после ОНМК. Существенное увеличение числа дендритов в контралатеральной коре возникает уже на 18-й день после инсульта, а увеличение числа синапсов - на 30-й день [11, 14, 15, 19, 20].
Важную роль в репаративных процессах играет также активация дополнительной моторной и премоторной коры. Исследования, проведенные через 2-4 мес от начала инсульта, свидетельствуют о значительной реорганизации моторной коры к этому времени [6]. Так, методом транскраниальной магнитной стимуляции было показано, что в процессе реабилитационных мероприятий в пораженном полушарии смещается центр двигательной проекционной области. Эти изменения носят стойкий характер и играют важную роль в восстановлении утраченных двигательных функций [6]. На фоне реабилитационных мероприятий церебральная реорганизация может происходить в более короткие сроки, что способствует более быстрому и полному восстановлению двигательного дефекта [16]. Показано также, что интенсивная нагрузка паретичной конечности вызывает повышение возбудимости нейрональных сетей в пораженной гемисфере. [17]. При хорошем восстановлении со временем происходит нормализация межполушарной асимметрии и снижение (или прекращение) участия двигательных отделов неповрежденного полушария в осуществлении движений, связанных с поврежденным полушарием.
Течение
Период восстановления неврологических функций после инсульта может длиться по-разному - от нескольких месяцев до нескольких лет. Наиболее активное восстановление двигательных функций происходит в первые 3 мес, а функциональное улучшение продолжается до 6-12 мес. Условно восстановительный период инсульта можно разделить на острую, подострую и хроническую фазы. На рис. 2 указаны ведущие механизмы восстановления в каждую из данных фаз.
Рис. 2. Механизмы восстановления поврежденных функций после перенесенного ИИ.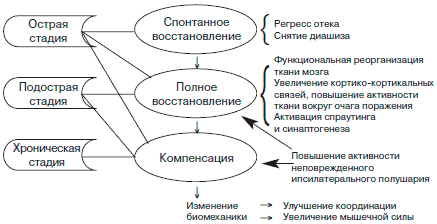
Восстановление движений
Одной из основных задач реабилитации пациентов, перенесших инсульт, является восстановление движений. Так, центральный гемипарез выявляется в 80-90% случаев ОНМК. При этом лишь около 30% больных могут самостоятельно передвигаться в первые недели после перенесенного инсульта.
На сегодняшний момент проведено большое количество исследований, направленных на поиски эффективных методик двигательной реабилитации. В частности, Van Peppen и соавт. суммировали результаты более 120 рандомизированных плацебо-контролируемых клинических исследований [12]. Целью реабилитационных мероприятий в указанных исследованиях было восстановление мышечной силы и двигательной активности пораженных конечностей. Было показано, что при восстановлении двигательной активности наиболее эффективными являются методики с ориентацией на усвоение определенного конкретного навыка (task-oriented), терапия вынужденного движения и билатеральный тренинг.
Методики с ориентацией на конкретный навык основаны на разработке и усвоении пациентом наиболее эффективной и экономичной двигательной стратегии для решения определенной задачи.
В основе терапии вынужденного движения лежит иммобилизация непораженной конечности, в связи с чем пострадавшая конечность вынуждена совершать движения, связанные с повседневной бытовой активностью. Данный метод был изучен в нескольких рандомизированных клинических исследованиях с включением большого количества пациентов, где была доказана его эффективность [13]. При этом было показано, что эффект данной методики сохранялся в течение 1-2 лет после ее проведения [10]. Недостаток терапии вынужденного движения заключается в необходимости практически постоянного надзора и помощи медицинского персонала и не всегда возможен в условиях стационара.
Билатеральный тренинг включает одновременное выполнение двигательных задач пораженной и непораженной конечностями. Данная методика применяется недавно, однако клиническими исследованиями доказана ее эффективность в отношении увеличения амплитуды движений, ловкости и координации в паретичной конечности [12].
Немаловажным фактором, увеличивающим скорость реабилитации и влияющим на эффективность тренировки, является эмоциональная окраска и индивидуальный подход к пациенту. Двигательная задача должна выбираться с учетом особенностей трудового анамнеза и бытовой активности пациента и мотивировать его на выполнение наиболее важных и интересных задач.
Восстановление речевых расстройств
Другой важной проблемой является восстановление речевых расстройств. Опыт реабилитации больных показывает, что центральным дефектом при всех формах афазии является нарушение коммуникативной функции речи, в сложных случаях приводящее к полной неспособности больных к вербальной форме общения. Нарушение проявляется в дефектах не только внешних форм коммуникации, но и внутренних -нарушается общение пациента с самим собой. При афазии у больного нарушаются понимание речи, повторение, называние, самостоятельные речевые высказывания, произношение, чтение, письмо, счетные операции, меняется социальный и семейный статус больного, его отношение к своей личности и окружающей действительности, поэтому основной задачей речевой реабилитации является не только восстановление речи, но и социальная реадаптация.
Максимальная эффективность достигается при начале речевой реабилитации в первые 3 месяца, при проведении реабилитационных мероприятий не менее 3 ч каждую неделю в течение 5 мес и дольше. В ряде случаев постепенное улучшение речи продолжается и в сроки выше 6 мес (до 2-х лет) [23].
Выбор конкретной технологии речевой реабилитации зависит от периода и этапа восстановления речевой функции. Задачи этапа реабилитации, определяемые индивидуальным планом (программой реабилитации), соответствуют характеру и степени нарушения речи.
В остром и раннем периоде восстановительная работа ведется при относительно пассивном участии больного в процессе восстановления речи. На более поздних этапах восстановления от пациента требуется активное участие в реабилитации.
В остром периоде работа логопеда заключается в установлении контакта с больным, нейропсихологическом обследовании, направленном на выявление его речевых, интеллектуальных возможностей, остаточных возможностей высших психических функций, изучении эмоционально-волевой сферы. В этот период занятия с логопедом должны носить преимущественно психотерапевтический характер. Первое время занятия рекомендуется проводить шепотом.
На раннем этапе восстановления применяются методики:
- стимулирования понимания речи на слух (при разных формах афазии);
- расторможения экспрессивной стороны речи при моторной афферентной и эфферентной афазии (автоматизированные речевые ряды, пословицы, песни, фразы с жестким контекстом, речевые задания побудительного характера, образцы речевых оборотов, необходимых для элементарного общения, чтение коротких фраз и стихов);
- предупреждения аграмматизма (телеграфный стиль) - стимулирование употребления в ответах глагольной лексики;
- стимулирования чтения и письма [21, 22].
На поздних, резидуальных этапах логотерапии более активно используется механизм компенсации; речевая функция не восстанавливается в прежнем виде, а меняет свое строение.
В настоящее время проведено немало исследований по изучению факторов, влияющих на скорость восстановления речевых расстройств. Доказанные факторы представлены на рис. 3. [18]. Их следует учитывать при прогнозе оценки и определении длительности реабилитационных мероприятий. Желательным для всех пациентов считается регулярные занятия в стационаре, а затем и в амбулаторных условиях не менее 2-х лет после инсульта.
Рис. 3. Факторы, влияющие на речевую реабилитацию после ИИ.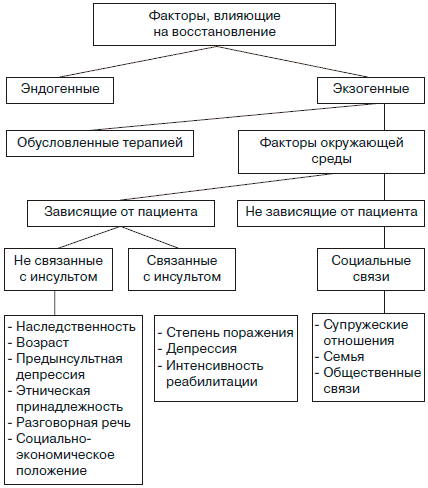
Медикаментозная терапия в восстановительном периоде ИИ
Эмпирически в первые месяцы после перенесенного ИИ широко назначаются препараты, улучшающие церебральную микроциркуляцию и нейрональный метаболизм. Предполагается, что активная сосудистая и нейрометаболическая терапия в восстановительном периоде ИИ способствует более полному и более быстрому регрессу неврологических расстройств. Следует отметить, что число проведенных контролируемых клинических исследований указанных лекарственных средств к настоящему времени невелико. Это связано, в том числе, с этическими трудностями проведения подобных исследований: необходимостью назначения плацебо с последующей оценкой инвалидизации в сравнении с активным веществом. Тем не менее, несмотря на недостаточное число исследований, мы считаем, что в первые 6-12 мес после ИИ целесообразно непрерывное проведение вазоактивной и нейрометаболической терапии (табл. 2). Традиционно назначается комбинация сосудистого и метаболического препаратов [7].
Таблица 2.
Вазоактивные и нейрометаболические препараты, применяемые в восстановительном периоде ИИ
| Вазоактивные препараты | Нейрометаболические препараты |
| Пентоксифиллин, винпоцетин, экстракт гинкго билоба, нимодипин, циннаризин, ницерголин, Вазобрал | Пирацетам, актовегин, церебролизин, кортексин, холинальфасцерат, цитиколинпирибедил, Вазобрал |
Принимая во внимание разнообразие патогенетических механизмов, лежащих в основе нарушений мозгового кровообращения, целесообразно применение лекарственных препаратов, оказывающих комбинированное действие, назначение которых позволяет решать одновременно сразу несколько проблем. К числу таких препаратов относится Вазобрал - препарат, оказывающий как вазоактивное, так и нейрометаболическое действие. Действующими веществами данного препарата являются дигидроэргокриптин и кофеин. Дигидроэргокриптин является неселективным блокатором α1- и α2-адренорецепторов, с чем связан его сосудорасширяющий эффект. Кроме того, блокада пресинаптических α-блокаторов в головном мозге вызывает активацию церебральной норадренергической системы, что имеет большое значение для процессов реорганизации функциональной активности нейронов в восстановительном периоде ИИ, о которых говорилось выше. Кофеин, будучи ингибитором фосфодиестеразы, улучшает венозный отток, что также способствует оптимизации церебральной микроциркуляции. Показан также благоприятный реологический эффект Вазобрала в отношении форменных элементов крови. В клинической практике Вазобрал показал большую эффективность и безопасность применения у пациентов с последствиями ОНМК, при дисциркуляторной энцефалопатии, а также для профилактики мигрени.
В заключение хотелось бы подчеркнуть, что только совместные усилия реабилитологов, врачей поликлиник, социальных работников, а также родных и близких позволят пациентам после ИИ более полно восстановить нарушенную или утраченную функцию, вернуть качество жизни, близкое к доинсультному периоду.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Бейн Э.С., Бурлакова МК, Визель ТТ. Восстановление речи у больных с афазией. М., 1981.
2. Бурлакова МК Коррекционно-педагогическая работа при афазии. М, 1991.
3. Дж Тул. Сосудистые заболевания головного мозга. М, 2007.
4. Кадыков АС, Черникова Л.А. Реабилитация после инсульта. 2004.
5. Марковская Е.П. Современные аспекты речевой реабилитации при афазии. 2008.
6. Харченко ЕП, Клименко МИ. Пластичность и регенерация мозга. Неврол. журн. 2006; 11 (6): 37-45.
7. Яхно НН. и соавт. Болезни нервной системы. Руководство для врачей. М: Медицина 2005.
8. Amarenco P et al. N Engl J Med 2006; 355:549.
9. Jill S, McClung1, Leslie J, Gonzalez Rothi, Stephen E. Ambient experience in restitutive treatment of aphasia. Nadeau. 2009.
10. Cicinelii P, Traversa R, Rossini PM. Post-stroke reorganization of brain motor output to the hand: a 2-4 month follow-up with focal magnetic transcranial stimulation. EEG Clin Neurophysiol 1997; 105:438-50.
11. Cremonesi A et al. Stroke 2006; 3 7:2400.
12. Hallet M. Plasticity of human motor cortex and recovery from stroke. Brain Res Rev 2001; 36:169-74.
13. Infeld B, Davis SM, Lichtensten M et al. Crossed cerebellar diaschisis and brain recovery after stroke. Stroke 1995;26:90-5.
14. Johansson BB. Brain plasticity and stroke rehabilitation. Stroke 2000; 20: 223-30.
15. Liepert J, Bauder H, Miltner W et al. Treatment-induced cortical reorganization after stroke in humans. Stroke 2000; 31:1210-20.
16. Miyani I, Yagura H, Hatakenaka M et al. Longitudinal optical imaging study for locomotor recovery after stroke. Stroke 2003; 34:2866-70.
17. Sacco RL et al. Stroke 2006; 37:577.
18. Taub E, Uswatte G, King DK, Morris D et al. Aplacebo-controlled trial of constraint-induced movement therapy for upper extremity after stroke. Stroke 2006; 37 (4): 1045-9.
19. The Stroke Prevention by Aggresive Reduction in Cholesterol Level (SPARCL) Investigators «High-dose atorvastatin after stroke or transient ischemic attack». New Engl J Med 2006;355:549-59.
20. Technology-assisted training of arm-hand skills in stroke: concepts on reacquisition of motor control and therapist guidelines for rehabilitation technology design.
21. Van Peppen RP, Kwakkel G, Wood-Dauphinee S, Hendriks HJ et al. The impact of physical therapy on functional outcomes after stroke: what's the evidence? Clin Rehabil 2004; 18 (8): 833-62.
22. Wolf SL, Winstein CJ, Miller JP, Taub E et al. Effect of constraint-induced movement therapy on upper extremity function 3 to 9 months after stroke: the EXCITE randomized clinical trial. Jama 2006; 296 (17): 2095-104.
23. Yan T, Hui-Chan CWY, Li LSW. Functional electrical stimulation improves motor recovery of the lower extremity and walking ability of subjects with first acute stroke. Stroke 2005; 36: 80-5.
