Сравнительный анализ эффективности применения селективного β-адреноблокатора небиволола и блокатора рецепторов ангиотензина II валсартана у мужчин с артериальной гипертонией, метаболическим синдромом и эректильной дисфункцией
СтатьиОпубликовано в журнале:
Кардиосоматика, 2013, том 4, № 2
С.В.Недогода, А.С.Саласюк, И.Н.Барыкина, А.А.Ледяева, В.В.Цома, Е.В.Чумачек
Волгоградский государственный медицинский университет Резюме. Целью исследования была оценка антигипертензивной эффективности и влияния на метаболические показатели и эректильную функцию небиволола и валсартана у больных артериальной гипертензией, метаболическим синдромом и эректильной дисфункцией. Материалы и методы. В слепое рандомизированное контролируемое сравнительное исследование в параллельных группах (небиволол против валсартана на протяжении 12 нед) было включено 40 больных артериальной гипертензией, метаболическим синдромом и эректильной дисфункцией. Результаты. Достоверных различий между препаратами по антигипертензивной эффективности выявлено не было. На показатели кардио- и ангиопротекции и показатели липидного и углеводного обмена более выраженное положительное влияние оказал небиволол. Не было отмечено отрицательного влияния β-адреноблокаторов небиволола на метаболические показатели. Терапия небивололом в отличие от валсартана оказала выраженное положительное влияние на содержание андрогенов в крови и степень эректильной дисфункции. Кроме того, показатели качества жизни в группе небиволола также достоверно улучшились. При оценке переносимости и побочных эффектов в 2 группах побочных эффектов не зарегистрировано.
Ключевые слова: артериальная гипертензия, метаболический синдром, эректильная дисфункция, небиволол, валсартан, Бинелол.
Comparative analysis of the efficiency of the selective-blocker nebivolol and the angiotensin II receptor blocker valsartan in men with hypertension, metabolic syndrome, and erectile dysfunction
S.V.Nedogoda, A.S.Salasyuk, I.N.Barykina, A.A.Ledyaeva, V.V.Tsoma, E.V.Chumachek
The Volgograd State Medical University Summary. Objective: to evaluate the antihypertensive efficacy and effect of nebivolol and valsartan on metabolic parameters and erective function in patients with hypertension, metabolic syndrome, and erectile dysfunction. Subjects and methods. A 12-week randomized, blind, controlled, parallel-group, comparative (nebivolol versus valsartan) trial enrolled 40 patients with hypertension, metabolic syndrome, and erectile dysfunction. Results. There were no significant differences between the drugs in their antihypertensive efficiency. Nebivolol exerted a more pronounced positive effect on cardio- and angioprotection and lipid and carbohydrate metabolic parameters. It had no negative effect on metabolic parameters. Therapy with nebivolol versus valsartan produced a pronounced positive effect on blood androgen levels and erectile function. Moreover, the quality-of-life indicators also showed a significant improvement in the nebivolol group. Evaluation of the tolerability and adverse reactions of the drugs demonstrated no side effects in both groups.
Key words: hypertension, metabolic syndrome, erectile dysfunction, nebivolol, Binelol, valsartan.
Сведения об авторах
Недогода Сергей Владимирович – д-р мед. наук, проф., проректор по лечебной работе ГБУЗ ВПО ВолгГМУ, зав. каф. терапии и эндокринологии ФУВ ВолгГМУ
Саласюк Алла Сергеевна – аспирант, ассистент каф. терапии и эндокринологии ФУВ ВолгГМУ.
Барыкина Ирина Николаевна – канд. мед. наук, ассистент каф. терапии и эндокринологии ФУВ ВолгГМУ.
Ледяева Алла Александровна – канд. мед. наук, ассистент каф. терапии и эндокринологии ФУВ ВолгГМУ.
Цома Вера Владимировна – канд. мед. наук, ассистент каф. терапии и эндокринологии ФУВ ВолгГМУ
Чумачек Елена Валерьевна – аспирант, ассистент каф. терапии и эндокринологии ФУВ ВолгГМУ.
Факторы, вызывающие метаболический синдром (МС), артериальную гипертензию (АГ) и эректильную дисфункцию (ЭД), связаны между собой. Так, снижение уровня тестостерона является фактором риска развития сердечно-сосудистых заболеваний (ССЗ). Многочисленные корреляционные исследования не смогли прояснить, что является первичным – андрогенный дефицит или увеличение массы висцеральной жировой ткани. Проспективные исследования подтверждают, что андрогенный дефицит у мужчин является предиктором развития висцерального ожирения [28] и что низкий уровень тестостерона имеет достоверную обратную связь с уровнем артериального давления (АД), тощаковой глюкозы, триглицеридов (ТГ) и индекса массы тела (ИМТ), а также положительно коррелирует с уровнем липопротеидов высокой плотности (ЛПВП) у мужчин [33]. Пятилетнее исследование, проведенное в Швеции, выявило, что низкий уровень тестостерона у мужчин ассоциирован с увеличением риска сердечно-сосудистых событий и риска развития сахарного диабета (СД) типа 2 [28].
Одновременно с этим доказано, что тестостерон опосредованно стимулирует выработку NO [38].
Выяснение биологических механизмов является необходимым компонентом понимания связи между ЭД и МС.
Предполагается, что поражение сосудистой системы полового члена является основным патофизиологическим механизмом развития ЭД при МС. Так как эрекция полового члена критически зависит от функции эндотелия, то в результате эндотелиальной дисфункции может возникать ЭД. Таким образом, коррекция компонентов МС, в особенности АГ, должна проводиться с учетом влияния препарата на эндотелий и показатели углеводного и липидного обмена.
Кроме того, терапия АГ у мужчин может быть неэффективна из-за низкой комплаентности пациентов в результате нарушений сексуальной функции на фоне терапии. Практикующие врачи часто не уделяют должного внимания данной проблеме, фокусируясь на основных целях и задачах лечения [27].
Таким образом, антигипертензивные препараты, применяемые у пациентов с МС, должны отвечать следующим требованиям:
- оказывать пролонгированное действие в течение суток (улучшение суточного профиля АД со снижением как дневного, так и ночного АД);
- способствовать регрессу поражения органов-мишеней (в частности, уменьшению гипертрофии левого желудочка);
- обладать метаболически положительными эффектами.
Кроме того, необходимо учитывать тот факт, что до 40% нелеченых пациентов и до 60% пациентов с АГ на фоне лечения имеют нарушения сексуальной функции разной степени выраженности [10]. Препараты, применяемые у мужчин с АГ и МС, должны дополнительно корректировать ЭД и уровень тестостерона.
Позитивное влияние на сексуальную функцию ингибиторов ангиотензинпревращающего фермента (ИАПФ) и блокаторов рецепторов ангиотензина II (БРА II) было продемонстрировано в российских и зарубежных исследованиях.
Согласно рекомендациям Всероссийского научного общества кардиологов препаратами первой линии коррекции АГ у лиц с МС, СД и ЭД обоснованно являются именно данные группы препаратов, а также антагонисты кальция в сочетании с тиазидными диуретиками [47].
Однако наличие при МС повышенной активности симпатической нервной системы (СНС) ставит вопрос о необходимости применения β-адреноблокаторов (БАБ) у данной категории пациентов [35]. АГ как компонент МС имеет специфические особенности. Они обусловлены влиянием гиперинсулинемии: нарушением транспорта ионов, активацией СНС, ренин-ангиотензин-альдостероновой системы, усиленным синтезом свободных жирных кислот и дисфункцией эндотелия.
В ряде исследований показано, что применение БАБ I–II поколения, равно как и диуретиков и препаратов центрального действия (метилдопа, клонидина) сочетается с большей частотой половой дисфункции, в особенности у мужчин [15].
Известно, что неселективные БАБ I поколения неблагоприятно влияют на углеводный [19] и липидный [20] обмен. Другим нежелательным побочным эффектом терапии БАБ I–II поколения является их способность вызывать прибавку массы тела [29]. Данная особенность этой группы препаратов хорошо изучена [5, 32]. Кроме того, многие селективные β1-адреноблокаторы утрачивают свою селективность в больших дозах, и их антагонизм проявляется и в отношении β2-адренорецепторов. При блокаде β2-адренорецепторов поджелудочной железы может происходить уменьшение высвобождения инсулина.
Однако появление высокоселективного БАБ III поколения небиволола значительно расширило границы применения БАБ за счет благоприятных метаболических и сосудистых эффектов.
Небиволол отличается от других БАБ способностью оказывать самостоятельное сосудорасширяющее действие, которое не связано с β-блокирующей активностью препарата, а является результатом высвобождения эндотелийзависимого релаксирующего фактора (EDRF). Механизм данного эффекта связан с тем, что небиволол, соединяясь с L-аргинином, способствует высвобождению NO эндотелием сосудов, с последующей физиологической вазодилатацией [6]. Эта же особенность небиволола позволяет говорить о нем как об одном из приоритетных препаратов для лечения больных СД и МС. Кроме того, его выраженный вазодилатирующий эффект вследствие повышения NО-зависимой вазодилатации приводит к снижению общего периферического сопротивления сосудов и улучшению чувствительности периферических рецепторов к инсулину, что вызывает улучшение обменных процессов.
В настоящее время известны следующие механизмы влияния небиволола на функцию эндотелия [14, 16, 18, 37, 39, 44, 48]:
- увеличение экспрессии эндотелиальной NO-синтазы (еNOS);
- замедление снижения NO супероксидными радикалами;
- активация β3-адренорецепторов в коронарных микрососудах, опосредуя увеличение ионов кальция, необходимого для активации eNOS;
- взаимодействие с рецепторами к эстрадиолу, расположенными на эндотелиальных клетках, активация простагландинового пути за счет индукции PGI2;
- стимуляция пуриновых рецепторов, ведущая к высвобождению NO из эпителия микрососудов почечных клубочков;
- устранение оксидативного стресса, повышение содержания адипонектина и снижение Р-селектина.
Применение небиволола приводит к нормализации функции эндотелия и устранению окислительного стресса, при этом улучшается чувствительность периферических тканей к инсулину, снижается уровень глюкозы на 16%, инсулина – на 10–20%, инсулинорезистентность – на 18–20%.
Кроме того, в нескольких исследованиях отмечено положительное влияние на уровень андрогенов и эректильную функцию у пациентов при терапии небивололом. Небиволол, модулируя выработку NO эндотелием, приводит к мягкой вазодилатации периферических сосудов, в том числе сосудов кавернозных тел и половых желез у мужчин, что усиливает выработку андрогенов железами как напрямую, так и за счет активации гипоталамо-гипофизарной оси вследствие улучшения эректильной функции [45]. Небиволол не содержит в инструкции указаний на снижение эректильной функции и либидо, что уменьшает риск отказа мужчин от ежедневного приема антигипертензивных препаратов.
Наличие гиперсимпатикотонии при МС и АГ требует оценить возможность применения в этой клинической ситуации нового высокоселективного β1-адреноблокатора III поколения, обладающего, помимо гипотензивного, дополнительными независимыми плейотропными эффектами и способностью улучшать выработку NO.
При исследовании нами эффективности терапии АГ у мужчин с МС был проведен сравнительный анализ эффектов селективного БАБ небиволола и БРА II валсартана.
Валсартан был выбран в качестве препарата, доказавшего свою эффективность, метаболическую нейтральность и положительное действие на сексуальную функцию у данной группы больных [43].
Материалы и методы
Для изучения влияния небиволола и валсартана на уровень АД, степень выраженности ЭД, уровень андрогенов у мужчин с МС нами было проведено открытое рандомизированное контролируемое сравнительное исследование в параллельных группах.
В исследование было включено 40 больных АГ 1–2-й степени, у которых не достигнут целевой уровень АД в течение не менее 3 мес предшествующей антигипертензивной монотерапии.
Больные были рандомизированы на 2 группы в соотношении 1:1. Рандомизация «методом конвертов». В итоге по 20 пациентов получали терапию небивололом в дозе 5/7,5 мг или валсартаном в дозе 80/120 мг. Увеличение дозы производилось при необходимости через 4 нед после начала терапии.
Пациент включался в исследование при соблюдении правил Качественной клинической практики (Good clinical practice – GСP), при условии подписания информированного согласия и соответствия критериям включения, а также при отсутствии критериев исключения.
Критерии включения
- Возраст: мужчины в возрасте от 30 до 60 лет (включительно).
- Наличие АГ 1–2-й степени с уровнем систолического АД 140–160 мм рт. ст. и проведение антигипертензивной монотерапии любым классом антигипертензивных препаратов не менее 3 мес.
- Наличие МС по критериям Европейского института метаболического синдрома.
- Наличие ЭД: снижение показателей по шкале МИЭФ-5>21 балла.
- Письменное согласие больного на участие в программе.
Критерии исключения
Пациенты, имеющие по крайней мере один из нижеперечисленных признаков, не могут быть включены в исследование:
- Возраст моложе 30 и старше 60 лет.
- Наличие противопоказаний или отмеченной ранее непереносимости БАБ, БРА.
- Симптоматическая АГ.
- Заболевания, нарушающие кишечную непроходимость и/или абсорбцию.
- СД типа 1 и некомпенсированный инсулинзависимый СД типа 2.
- Любые тяжелые заболевания с развитием печеночно-почечной недостаточности.
- Злокачественные новообразования.
- Клинически значимая бронхиальная обструкция.
- Неспособность понять суть программы и дать обоснованное согласие на участие в ней.
Схема исследования
Схема программы представлена на рис. 1.
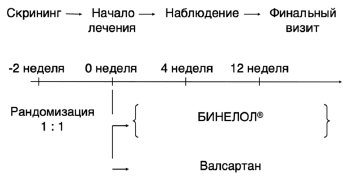
Рис. 1. Схема исследования.
Исходно на визите 0 была проведена оценка клинического состояния больных, критериев включения и исключения, оценка регулярности антигипертензивной терапии и подписано согласие на участие в исследовании. Дозы антигипертензивных препаратов были стабильны на протяжении всего двухнедельного периода скрининга.
После периода скрининга больные (визит 1) были рандомизированы на 2 группы: 1-я группа – на терапии небивололом (Бинелол®, BELUPO d.d) по 5 мг в день, 2-я группа – на терапии валсартаном по 80 мг в день.
Контрольные визиты с оценкой клинического состояния обследуемых проводились через 4 нед (визит 2) и 12 нед (визит 3) после начала лечения.
Прием другой гипотензивной терапии, средств, влияющих на эрекцию (ингибиторы фосфодиэстеразы-5, заместительная терапия препаратами тестостерона), и коррекция доз гиполипидемических препаратов были критерием исключения из исследования.
Всем пациентам было проведено общеклиническое обследование, включающее физикальный осмотр, анализ жалоб, анамнеза, выяснялось наличие наследственности и вредных привычек, фиксировались все принимаемые лекарственные препараты. Определялись рост, масса тела, окружность талии (ОТ), рассчитывался ИМТ по формуле: ИМТ = масса тела в кг/(рост в м)².
Для определения количества жировых отложений методом биоэлектрического импеданса будет использоваться жироанализатор OMRON BF-306, BF-400.
Уровни общего тестостерона и сексстероидсвязывающего глобулина (СССГ) исследовались на автоматическом анализаторе «IMMULITE 1000» (США) стандартным иммунохемилюминесцентным способом. Забор крови проводился в пробирки типа «вакутейнер» в утреннее время натощак из локтевой вены. Для исключения влияния пульсирующей секреции гормона на определение результата забор крови производился троекратно с интервалом в 20 мин, в качестве результата брался наименьший показатель. Уровень свободного тестостерона определяли расчетным методом по известным математическим формулам (патент №2439578 от 10.01.2012).
Также гормональное обследование включало определение пролактина, тиреотропного гормона (ТТГ), С-пептида, которое проводилось на автоматическом анализаторе «ARCHITECT 2000» (Германия). Биохимический анализ крови с определением уровней холестерина, ТГ, ЛПВП, липопротеидов низкой плотности (ЛПНП), глюкозы проводился на биохимическом анализаторе «ARCHITECT 8000» (Германия) фотоколориметрическим методом.
В настоящей работе исследование суточного профиля АД проводили с помощью суточного регистратора АД BR-102 plus фирмы SсhillerAG (Швейцария), в основу работы которого положены два принципа работы: по Короткову/аускультативный (главный) с осциллометрическим дублированием. Регистрация АД осуществлялась в течение 25–26 ч, так как первые 1–2 ч в анализ не включаются.
Влияние на углеводный обмен оценивали с помощью анализа показателей суточного профиля мониторирования уровня глюкозы, регистрируемого с помощью глюкометра One Touch Select, Johnson & Johnson, минимум в 12 точках измерения в сутки, и системы обработки результатов самоконтроля пациентов «Глюкопринт», ФГБУ ЭНЦ РФ.
Также для выявления психологических нарушений и оценки качества жизни проводились тесты оценки (шкала МИЭФ-5, шкала HADS, опросник AMS).
Все обследуемые получали устные и письменные рекомендации по изменению пищевого поведения и усилению физической активности (рекомендовалось как минимум 150 мин в неделю умеренной физической активности).
Длительность наблюдения больного в исследовании составляла 12 нед.
Статистическая обработка полученных данных была проведена с использованием пакета прикладных программ STATISTICA (StatSoft Inc, США, версия 10.0). Абсолютные значения исследованных показателей представлены в виде средних значений и их стандартного отклонения (М±s).
Для анализа вида распределений применялись критерии Шапиро–Уилка и Лиллиефорса, дисперсии распределений признаков оценивались с помощью F-критерия в процедуре дисперсионного анализа ANOVA. Сравнение двух не связанных между собой групп по количественным признакам осуществлялось непараметрическим методом с использованием U-критерия Манна–Уитни. Статистически значимыми считали различия при р<0,05. Анализ связи (корреляции) двух количественных признаков осуществлялся непараметрическим методом ранговой корреляции по Спирмену.
Для качественных признаков был применен либо точный критерий Фишера (Fisher), либо тест χ², в зависимости от количества наблюдений в каждой ячейке таблицы сопряженности.
Результаты исследования
Клинико-демографические характеристики больных, включенных в исследование, представлены в табл. 1. Как видно из представленных данных, по основным показателям сравниваемые группы достоверно не различались между собой.
Таблица 1. Общая характеристика пациентов, включенных в исследование
| Небиволол, n=20 | Валсартан, n=20 | |
| Возраст, лет | 50,95±8,97 | 50,85±8,99 |
| Масса тела, кг | 99,15±21,08 | 99,00±13,7 |
| ИМТ, кг/м² | 32,06±5,98 | 31,39±3,98 |
| ОТ, см | 112,4±12,62 | 110,85±9,04 |
| САД средн., мм рт. ст. | 148,15±8,15 | 150,9±6,10 |
| ДАД средн., мм рт. ст. | 92,3±5,26 | 93,5±6,13 |
| ЧСС, уд/мин | 70,9±7,16 | 77,10±11,33 |
| СПВ CF, м/с | 9,31±2,79 | 10,35±3,01 |
| Общий тестостерон, нмоль/л | 11,38±2,94 | 11,13±2,90 |
| СССГ, нмоль/л | 33,23±12,8 | 32,90±11,70 |
| Мочевая кислота, мкмоль/л | 368,55±57,66 | 357,65±63,20 |
| ОХ, ммоль/л | 5,85±1,3 | 5,31±0,83 |
| Глюкоза плазмы натощак, ммоль/л | 5,15±1,06 | 5,41±0,95 |
| Гликемический показатель | 4,53±0,62 | 4,84±1,44 |
Обследуемые были рандомизированы в соотношении 1:1:
- Пациенты 1-й группы получали небиволол 5 мг 1 раз в сутки, после оценки достижения целевого уровня АД доза могла быть увеличена до 7,5 мг 1 раз в сутки (Бинелол®, BELUPO d.d.).
- Пациенты 2-й группы получали валсартан 80 мг 1 раз в сутки, после оценки достижения целевого уровня АД доза могла быть увеличена до 120 мг 1 раз в сутки.
После процедуры рандомизации провели оценку изучаемых параметров исходно и спустя 12 нед терапии. На визите 4-й нед оценивалась степень эффективности антигипертензивной терапии и при необходимости осуществлялось увеличение дозы препарата в рамках протокола исследования.
Пациенты считались «достигшими целевого уровня», если достигалось снижение уровня АД до менее 140/90 мм рт. ст. спустя 4 нед терапии. В группе небиволола целевых уровней АД достигли 45% пациентов, в группе валсартана – 35%. При недостижении целевых уровней АД обследуемым на визите 2 увеличивали дозу небиволола до 7,5 мг, валсартана до 120 мг.
Увеличение дозы потребовалось 9 (45%) пациентам в группе небиволола и 13 (65%) пациентам в группе валсартана (рис. 2).
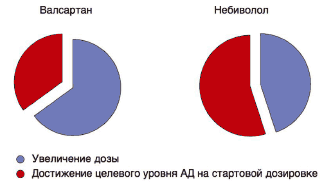
Рис. 2. Процент достижения целевого АД у пациентов исследуемых групп спустя 4 нед терапии.
Все пациенты, которым потребовалась коррекция первоначальной дозы антигипертензивных препаратов, в 2 группах исходно имели ИМТ>25 кг/м² и более выраженную степень абдоминального ожирения по сравнению с пациентами, которым коррекция дозы не потребовалась.
Более высокий процент тестируемых, которым потребовалось увеличение дозы в группе валсартана, связан, возможно, с тем, что терапия небивололом, положительно влияющая на андрогенный профиль, способствует улучшению ответа на гипотензивную терапию у пациентов с МС и андрогенным дефицитом.
После этого на визите 12 нед оценили показатели контроля АГ (табл. 2).
Таблица 2. Динамика показателей АД и ЧСС через 12 нед терапии в исследуемых группах
| Показатель | Небиволол | Валсартан | ||
| исходно/12 нед | % изменения | исходно/12 нед | % изменения | |
| САДср, мм рт. ст. | 148,15±8,15/132,05±4,77 | -12,2* | 150,9±6,10/132,65±3,80 | -13,7* |
| ДАДср, мм рт. ст. | 92,3±5,26/82,8±5,48 | -11,5* | 93,5±6,13/82,95±4,33 | -12,7* |
| ЧСС, уд/мин | 70,9±7,16/62,25±3,06 | -13,9*# | 77,10±11,33/73,1±6,69 | -5,4*# |
После коррекции терапии целевых уровней АД удалось достичь у 95% пациентов в группе небиволола и у 95% – в группе валсартана (рис. 3).
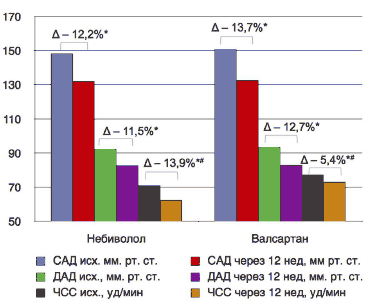
Рис. 3. Динамика показателей АД и ЧСС исходно/через 12 нед терапии в группе небиволола и валсартана.
В ходе лечения небивололом по сравнению с лечением валсартаном были выявлены достоверные различия в коррекции частоты сердечных сокращений (ЧСС). Средняя ЧСС сидя на фоне терапии небивололом снизилась за 12 нед на 13,9% (p<0,05), в то время как в группе валсартана средняя ЧСС значимо не изменилась, снижение составило 5,4%.
При анализе данных суточного мониторирования артериального давления (СМАД) отмечалась определенная динамика (табл. 3).
Таблица 3. Динамика показателей СМАД исходно/через 12 нед терапии в группе валсартана
| Показатель | Небиволол | Валсартан | ||
| исходно/12 нед | % изменения | исходно/12 нед | % изменения | |
| САД дневн., мм рт. ст. | 146,1±7,3/125,50±4,11 | -16,4# | 146,7±7,92/128,20±6,09 | -14,4* |
| ДАД дневн., мм рт. ст. | 90,35±6,85/77,15±3,92 | -17,1* | 90,45±11,71/76,55±4,87 | -18,2* |
| САД ночн., мм рт. ст. | 130,55±13,75/117,20±4,48 | -11,4* | 132,2±11,04/117,30±4,95 | -12,7* |
| ДАД ночн., мм рт. ст. | 80,0±10,82/68,60±3,99 | -16,6* | 77,05±8,31/68,90±4,34 | -11,8* |
Данные СМАД подтверждают отсутствие достоверных различий между группами небиволола (Бинелол®) и валсартана по снижению дневного систолического (САД) и диастолического АД (ДАД). Степень снижения средних показателей САД и ДАД в ночные часы также статистически значимо не различались.
Целевых уровней АД в дневные часы по данным СМАД (менее 130/85 мм рт. ст.) в группе небиволола достигли 75% пациентов, в группе валсартана – 60%, в ночные часы (менее 120/70 мм рт. ст.) – в 2 группах 30% (табл. 4).
Таблица 4. Достижение целевых уровней АД по данным СМАД в исследуемых группах
| Показатель | В группе небиволола, % | В группе валсартана, % |
| САД/ДАД дн., мм рт. ст. | 75 | 30 |
| САД/ДАД ноч., мм рт. ст. | 60 | 30 |
Динамика антропометрических показателей за 12 нед терапии в 2 группах не отличалась между собой (p>0,05), незначительное изменения массы тела, ОТ и данных импедансометрии было обусловлено изменением образа жизни под воздействием проводимых с пациентами бесед и не отличалось от такового у здоровых добровольцев при соблюдении диеты и увеличении уровня физической активности (табл. 5).
Таблица 5. Динамика антропометрических показателей за 12 нед терапии в исследуемых группах
| Показатель | Небиволол. Исходно/12 нед | Валсартан. Исходно/12 нед |
| Масса тела, кг | 99,15±21,08/97,1±18,8 | 99,00±13,7/98,65±13,74 |
| ИМТ, кг/м² | 32,06±5,98/31,4±5,4 | 31,39±3,98/31,29±4,04 |
| ОТ, см | 112,4±12,62/110,3±10,9 | 110,85±9,04/109,75±8,40 |
| Жировая масса, верх, % | 33,43±5,85/32,9±5,5 | 32,82±4,38/32,49±4,41 |
| Жировая масса, низ, % | 33,23±5,75/32,9±5,5 | 32,93±4,53/32,61±4,41 |
Был проведен анализ динамики изменений биохимических показателей на различных вариантах лечения (табл. 6).
Таблица 6. Динамика изменений биохимических показателей на различных вариантах лечения
| Показатель | Небиволол | Валсартан | ||
| исходно/12 нед | % изменения | исходно/12 нед | % изменения | |
| Мочевая кислота, мкмоль/л | 368,55±57,66/345,05±39,99 | -6,8*# | 357,65±63,20/324,10±44,27 | -10,4*# |
| ОХ, ммоль/л | 5,85±1,3/5,65±1,21 | -3,5* | 5,31±0,83/5,28±0,82 | -0,7* |
| ЛПВП, ммоль/л | 0,89±0,17/0,98±0,12 | 9,1*# | 0,94±0,27/0,96±0,21 | 2,1*# |
| ТГ, ммоль/л | 2,37±1,18/1,98±1,02 | -19,7* | 2,32±1,00/2,01±0,72 | -15,4* |
| ЛПНП, ммоль/л | 4,01±1,15/3,77±1,09 | -6,4* | 3,31±0,78/3,40±0,71 | 2,6* |
При терапии небивололом достоверно (p<0,05) и клинически значимо снизились уровни общего холестерина (ОХ), ЛПНП на 3,5 и 6,4% соответственно. В группе валсартана также отмечалось достоверное, однако клинически мало выраженное снижение данных показателей.
В группах небиволола и валсартана отмечены положительные изменения липидного спектра. При оценке влияния на уровень ТГ отмечалось равнозначное и достоверное по сравнению с исходными показателями снижение ТГ на 19,7 и 15,4% в группах небиволола и валсартана соответственно. Обращает на себя внимание статистически значимое (р=0,00031) увеличение уровня ЛПВП (на 9,1%) в группе небиволола. По влиянию на ЛПВП небиволол превосходил валсартан.
По влиянию на уровень мочевой кислоты были выявлены достоверные различия. В группе валсартана было выявлено снижение ее уровня на 10,4% против 6,8% в группе терапии небивололом (р<0,05), что является класс-специфичным эффектом для препаратов группы БРА II.
При анализе влияния различных режимов терапии на углеводный обмен выявлено незначительное, но статистически достоверное снижение среднесуточной гликемии в 2 группах, что, по-видимому, связано со стабилизацией показателей АД. В отличие от валсартана в группе небиволола отмечено достоверное снижение амплитуды гликемии на 17,3% (p<0,05). В группе валсартана также отмечалось снижение амплитуды гликемии, однако оно было статистически недостоверным. В последнее время большее внимание уделяется неблагоприятному эффекту колебаний гликемии, поэтому положительное влияние на этот показатель является важным критерием при подборе антигипертензивной терапии.
Анализируя динамику изменений содержания общего, свободного и биодоступного тестостерона в крови (рис. 4), нужно отметить, что в группе валсартана статистически значимые изменения отсутствовали (p>0,05), тогда как в группе небиволола прирост уровня общего тестостерона составил 3,11%, свободного – 7,87%, биодоступного – 6,9% (p<0,001 во всех трех случаях); табл. 7.
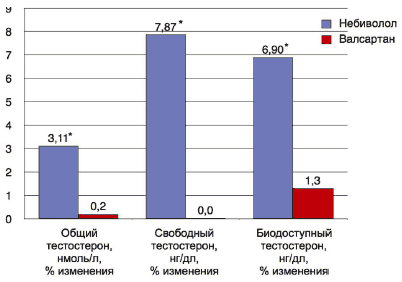
Рис. 4. Динамика уровня свободного и биодоступного тестостерона на терапии в группе небиволола и валсартана, исходно/12 нед; *p<0,001 по сравнению с исходными данными.
Таблица 7. Динамика показателей уровня ОТ, СТ, БТ и СССГ в 2 группах терапии, исходно/через 12 нед терапии
| Показатель | Небиволол | Валсартан | ||
| исходно/12 нед | % изменения | исходно/12 нед | % изменения | |
| Общий тестостерон, нмоль/л | 11,38±2,94/11,74±2,82 | 3,11*# | 11,13±2,90/11,15±2,89 | 0,2# |
| СССГ, нмоль/л | 33,23±12,8/30,82±10,07 | -7,8*# | 32,90±11,70/32,48±12,16 | -1,3# |
| Свободный тестостерон, нг/дл | 0,23±0,05/0,25±0,05 | 7,87*# | 0,23±0,05/0,23±0,05 | 0,02# |
| Свободный тестостерон, % | 2,07±0,44/2,14±0,39 | 3,4*# | 2,06±0,37/2,09±0,43 | 1,4# |
| Биодоступный тестостерон, нг/дл | 5,38±1,24/5,78±1,22 | 6,9*# | 5,29±1,28/5,36±1,27 | 1,3# |
| Биодоступный тестостерон, % | 48,47±10,21/50,2±9,29 | 3,4*# | 48,25±8,65/48,88±10,02 | 1,3# |
По-видимому, этот эффект связан с тем, что небиволол, модулируя выработку NO эндотелием, приводит к мягкой вазодилатации периферических сосудов, в том числе сосудов кавернозных тел и половых желез у мужчин, что усиливает выработку тестостерона железами как напрямую, так и за счет активации гипоталамо-гипофизарной оси вследствие улучшения эректильной функции.
При изучении динамики изменений эмоционального состояния обследуемых по данным опросников МИЭФ, AMS и HADS на различных вариантах лечения получены следующие данные: см. табл. 8.
Таблица 8. Динамика изменений эмоционального состояния пациентов по данным опросников МИЭФ, AMS и HADS на различных вариантах лечения
| Показатель | Небиволол | Валсартан | ||
| исходно/12 нед | % изменения | исходно/12 нед | % изменения | |
| МИЭФ | 15,3±2,96/16,4±2,39 | 7,19*# | 14,55±2,98/14,6±2,66 | 0,34# |
| AMS | 48,5±8,41/42,15±7,63 | -13,09*# | 51,05±8,49/49,95±7,61 | -2,15*# |
| HADS, шкала тревоги | 8,1±3,82/6,3±3,25 | -22,22*# | 7,5±3,63/6,85±2,8 | -8,67# |
| HADS, шкала депрессии | 7,65±3,66/6,2±3,16 | -18,95* | 6,85±3,83/5,8±2,88 | -15,33* |
Отмечено статистически значимое различие между группами по шкалам, отражающим степень ЭД и возрастных изменений у мужчин, – увеличение количества баллов по шкале МИЭФ-5 в группе небиволола составило 7,19% против 0,34% в группе валсартана, снижение по шкале AMS – 13,9% против 2,15% соответственно (p<0,05). Эти данные подтверждают положительные изменения уровня андрогенов на фоне приема небиволола, приведенные выше (рис. 5).
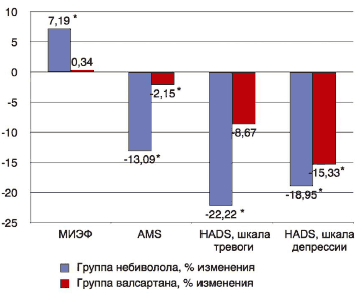
Рис. 5. Динамика изменения показателей уровня жизни в группе небиволола и валсартана, исходно/12 нед; *p<0,001 по сравнению с исходными данными.
Особое внимание обращает на себя изменение уровня тревоги по шкале HADS – отмечено достоверное (p<0,05) снижение уровня тревоги в группе небиволола на 22,2%. В группе валсартана достоверных изменений по данному показателю выявлено не было.
По шкале депрессии отмечается достоверное снижение показателя в 2 группах (p<0,05), различий между группами по степени снижения уровня депрессии не выявлено.
За все время приема пациентами небиволола и валсартана не было зарегистрировано нежелательных явлений и побочных реакций. По данным электрокардиограммы (ЭКГ) не было зарегистрировано нарушений проводимости и выраженной брадикардии.
Обсуждение результатов
Анализ полученных нами данных показал, что лечение АГ у больных с МС как небивололом, так и валсартаном привело к хорошему мягкому гипотензивному эффекту с улучшением суточного профиля АД. При исследовании влияния небиволола и валсартана на АД при приеме этих препаратов на протяжении 12 нед выявлено, что оба препарата в одинаковой степени снижают АД и одинаково хорошо переносятся, однако небиволол более выражено влияет на ЧСС, при этом не было отмечено чрезмерной брадикардии и нарушения проводимости при анализе ЭКГ. Средняя ЧСС сидя на фоне терапии небивололом снизилась за 12 нед на 13,9% (p<0,05), в то время как в группе валсартана средняя ЧСС значимо не изменилась. Полученные данные можно объяснить действием небиволола на симпатикотонию, отсутствующим у валсартана.
Это различие небиволола и валсартана особенно важно для больных с МС, которые характеризуются симпатикотонией вследствие инсулинорезистентности. Следствием различного влияния на уровень ЧСС можно объяснить и тот факт, что увеличение дозы потребовалось меньшему количеству пациентов в группе небиволола: 9 (45%) и 13 (45%) пациентам в группе валсартана. Это подтверждает роль ЧСС как показателя активности СНС и самостоятельного фактора риска сердечно-сосудистых осложнений.
Базальная активность СНС, как важного регулятора кардиоваскулярного гомеостаза, определяется генетикой, образом жизни, а также специфическими особенностями лекарственной терапии. Стимуляция СНС происходит при воздействии стресса, холода, боли, физической активности и некоторых заболеваний. Достоверно выяснено, что в большинстве случаев АГ сопровождается гиперсимпатикотонией. Результаты последних исследований свидетельствуют о том, что у 2/3 больных АГ отмечена тахикардия, как основной маркер гиперактивности СНС [52, 53].
Кроме того, показано, что степень реакции СНС в ответ на раздражение обусловлена наследственной предрасположенностью [54].
Доказано, что концентрация медиаторов СНС в крови обратно пропорциональна выживаемости [55]. Еще большую важность данному показателю придает тот факт, что была выявлена достоверная зависимость между ЧСС и степенью выраженности коронарного атеросклероза [57, 58], а также риском разрыва атеросклеротической бляшки [59]. Таким образом, одной из важнейших задач антигипертензивной терапии становится снижение активности СНС.
В национальных клинических исследованиях [60] также была показана прямая зависимость между продолжительностью жизни и ЧСС и, соответственно, снижением сердечно-сосудистого риска и смертностью при приеме ЧСС-снижающих препаратов, в частности БАБ [61, 62]. В исследованиях BEAUTIFUL (Mor Biditymortality EvAlUaTion of the If inhibitor ivabradine in patients with coronary disease and left ventricULar dysfunction) [63] и INVEST (INternational VErapamil-SR/trandolapril STudy) [64] одной из основных задач стало определение зависимости между этими параметрами. Результаты данных исследований показали, что превышение риска кардиоваскулярной смерти и госпитализации по поводу СН, увеличение госпитализации по поводу ИМ (фатального и нефатального) и частота коронарной реваскуляризации были напрямую связаны с ЧСС.
Классическими препаратами для снижения симпатической активности и ЧСС в последние десятилетия справедливо считают БАБ, однако они обладают наименьшей комплаентностью среди всех антигипертензивных препаратов в связи с вызываемыми ими побочными эффектами. Полученные нами данные соответствуют имеющимся свидетельствам о положительной корреляции между уровнем ЧСС и течением заболевания у пациентов с АГ [26]. Кроме того, более высокий процент обследуемых, которым потребовалась коррекция дозы в группе валсартана, возможно связан с тем, что терапия небивололом, положительно влияющая на андрогенный профиль, способствует улучшению ответа на гипотензивную терапию у пациентов с МС и андрогенным дефицитом.
Помимо этого, отмечено статистически значимое положительное влияние небиволола на уровень андрогенов и психоэмоциональное состояние мужчин с ЭД и АГ. Анализируя динамику изменений содержания общего, свободного и биодоступного тестостерона в крови, было отмечено, что в группе валсартана статистически значимые изменения отсутствовали, тогда как в группе небиволола отмечался достоверный прирост уровня общего тестостерона на 3,11%, свободного тестостерона на 7,87%, биодоступного тестостерона на 6,9% (p<0,001 во всех трех случаях).
Вышеописанные данные подтверждает также динамика психоэмоционального состояния мужчин. Отмечено статистически значимое различие между группами по шкалам, отражающим степень ЭД и возрастных изменений у мужчин – увеличение количества баллов по шкале МИЭФ в группе небиволола составило 7,19% против 0,34% в группе валсартана, снижение по шкале AMS – 13,9% против 2,15% соответственно (p<0,05). Было отмечено достоверное снижение уровня тревоги в группе небиволола, в группе валсартана достоверных изменений по данному показателю выявлено не было. По шкале депрессии отмечается достоверное снижение показателя в 2 группах.
В нашем исследовании за 12 нед выявлены достоверные положительные метаболические эффекты двух препаратов. При оценке влияния на уровень ТГ отмечалось равнозначное и достоверное по сравнению с исходными показателями снижение ТГ в 2 группах. При этом в группе небиволола, в отличие от валсартана, произошло более значимое достоверное повышение ЛПВП. Разница в изменении данного показателя связана, по-видимому, с влиянием на симпатикотонию, эндотелиальную функцию и уровень андрогенов и, как следствие, улучшением метаболических процессов на фоне приема небиволола.
Как известно, БАБ I–II поколений повышают уровень ТГ, снижают содержание ЛПВП и повышают или не изменяют концентрацию ЛПНП [20].
В нашем исследовании при терапии БАБ III поколения небивололом достоверно (p<0,05) и клинически значимо снизились уровни ОХ, ЛПНП на 3,5 и 6,4% соответственно. В группе валсартана также отмечалось достоверное, однако клинически мало выраженное снижение данных показателей.
Полученные данные подтверждают, что небивололу не присущи класс-специфические для БАБ неблагоприятные воздействия на углеводный [19] и липидный [20] обмен. Также, в отличие от классических БАБ, вызывающих прибавку массы тела [29], небиволол, как и валсартан, нейтрален в отношении антропометрических показателей.
Таким образом, результаты нашей работы показали большую эффективность небиволола у мужчин с АГ, МС и ЭД, в сравнении с валсартаном. Полученные нами результаты можно объяснить высокой селективностью небиволола, превышающей все другие известные препараты этой группы, и его дополнительным механизмом действия, способным стимулировать синтез NO эндотелием сосудов.
Небиволол в настоящее время является высокоэффективным и безопасным представителем класса БАБ для лечения АГ у больных с нарушением углеводного и липидного обмена и андрогенным дефицитом. С клинической точки зрения небиволол показан в первую очередь мужчинам с симпатикотонией и метаболическими нарушениями.
Выводы
- При исследовании влияния небиволола и валсартана на АД у мужчин с МС показано, что оба препарата в одинаковой степени снижают АД. Однако небиволол более выражено влияет на ЧСС и реже требует повышения дозы для достижения целевого АД у данной группы пациентов (избыточная масса тела).
- Отмечено статистически значимое и клинически выраженное положительное влияние небиволола на уровень андрогенов, эректильную дисфункцию и психоэмоциональное состояние мужчин с АГ и МС.
- Отмечено статистически значимое и более выраженное положительное влияние небиволола на уровень ЛПВП.
Список использованной литературы
- Andersen P, Seljeflot I, Herzog A et al. Effects ofdoxazosin and atenolol on atherothrombogenic risk profile in hypertensive middleaged men. J Cardiovasc Pharmacol 1998; 31: 677–83.
- Ayta IA, McKinlay JB, Krane RJ. The likely worldwide increase in erectile dysfunction between 1995 and 2025 and some possible policy consequences. BJU Int 1999; 84 (1): 50–6.
- Basaria S, Muller DC, Carducci MA et al. Hyperglycemia and insulin resistance in men with prostate carcinoma who receive androgendeprivation therapy. Cancer 2006; 106 (3): 581–8.
- Braun M, Wassmer G, Klotz T et al. Epidemiology of erectile dysfunction: results of the Cologne Male Survey. Int J Impot Res 2000; 12 (6): 305–8.
- Davis BR, Oberman A, Blaufox MD et al. Effect of antihypertensive therapy on weight loss: the Trial of Antihypertensive Interventions and Management Research Group. Hypertension 1992; 19: 393–9.
- De Boer RA, Voorsl AA, van Veldhuisen DJ. Nebivolol: third-generation b-blockade. Exp Opin Pharmacother 2007; 8 (10): 1539–50.
- Della Chiesa A, Pfiffner D, Meier B, Hess OM. Sexual activity in hypertensive men. J Hum Hypertens 2003; 17 (8): 515–21.
- Dusing R. Effect of the angiotensin II antagonist valsartan on sexual function in hypertensive men. Blood Press Suppl 2003; 2: 29–34.
- Fagard R, Van Den Enden M, Leeman M, Warling X. Survey on treatment of hypertension and implementation of World Health Organization/ International Society of Hypertension risk stratification in primary care in Belgium. J Hypertens 2002; 20 (7): 1297–302.
- Ferrario CM, Levy P. Sexual dysfunction in patients with hypertension: implications for therapy. J Clin Hypertens Greenwich 2002; 4 (6): 424–32.
- Fogari R, Preti P, Derosa G et al. Effect of antihypertensive treatment with valsartan or atenolol on sexual activity and plasma testosterone in hypertensive men. Eur J Clin Pharmacol 2002; 58 (3): 177–80.
- Fogari R, Zoppi A, Corradi L et al. Sexual function in hypertensive males treated with lisinopril or atenolol: a cross-over study. Am J Hypertens 1998; 11 (10): 1244–7.
- Fogari R, Zoppi A, Poletti L et al. Sexual activity in hypertensive men treated with valsartan or carvedilol: a crossover study. Am J Hypertens 2001; 14 (1): 27–31.
- Garban HJ, Buga GM, Ignarro LJ. Estrogen – receptor mediated vascular responsiveness to nebivolol: a novel endothelium-related mechanism of therapeutic vasorelaxation. J Cardiovasc Pharmacol 2004; 43: 638–44.
- Grimm RH Jr., Grandits GA, Prineas RJ et al. Long-term effects on sexual function of five antihypertensive drugs and nutritional hygienic treatment in hypertensive men and women. Treatment of Mild Hypertension Study (TOMHS). Hypertension 1997; 29 (1 Pt. 1): 8–14.
- Jgnarro LJ. Experimental evidences of nitric oxide-dependent vasodilatatory activity of nebivolol, a third-generation beta-blocker. Blood Press Suppl 2004; 1: 2–16.
- Julius S et al. The hemodynamic link between insulin resistance and hypertension. J Hypertens 1991; 9 (II): 983–6.
- Kalinowski L et al. Third – generation beta-blockers stimulate nitric oxide release from endothelial cells through ATP efflux: f novel mechanism for antihypertensive action. Circulation 2003; 107 (21): 2747–52.
- Kaplan NM. Effects of antihypertensive therapy on insulin resistance. Hypertension 1992; 19 (Suppl. I): I-116–I-118.
- Kasiske B, Ma JZ, Kalil RSN, Louis TA. Effects of antihypertensive therapy on serum lipids. Ann Intern Med 1995; 122: 133–41.
- Khaw KT, Barret-Connor E. Endogenous sex hormones, high density lipoprotein cholesterol and other lipoprotein fractions in men. Arterioscler Thromb 1991; 11: 489–94.
- Llisterri JL, Lozano Vidal JV et al. Sexual dysfunction in hypertensive patients treated with losartan. Am J Med Sci 2001; 321 (5): 336–41.
- MRC trial of treatment of mild hypertension: principal results. Medical Research Council Working Party. Br Med J Clin Res Ed 1985; 291 (6488): 97–104.
- NIH Consensus Conference: Impotence. JAМА 1993; 270: 83–90.
- Ohlslein E, Brooks D, Feuerstein G, Ruffolo RJr. Inhibition of sympathetic outflow by the angiotensin II receptor antagonist, eprosartan, but not losartan, valsartan or irbesartan: relationship to differences in prejunctional angiotensin II receptor blockade. Pharmacology 1997; 55: 244–51.
- Palatini P. Impact of increased heart rate on clinical outcomes in hypertension: implications for antihypertensive drug therapy. P.Palatini, A.Benetos, S.Julius. Drugs 2006; 66: 133–44.
- Rosen RC. Sexual dysfunction as an obstacle to compliance with antihypertensive therapy. Blood Press Suppl 1997; 1: 47–51.
- Rosmond R, Wallerius S, Wanger P et al. A 5-year follow-up study of disease incidence in men with an abnormal hormone pattern. J Intl Med 2003; 254 (4): 386–90.
- Rossner S, Taylor CL, Byington RP, Furberg CD. Long term propranolol treatment and changes in body weight after myocardial infarction. BMJ 1990; 300: 902–3.
- Sharma AM, Pischon T, Hardt S et al. Hypothesis: Beta-adrenergic receptor blockers and weight gain. A systematic analysis. Hypertension 2001; 37: 250–4.
- Stellato RK, Feldman HA, Hamdy O et al. Testosterone, sex hormonebinding globulin, and the development of type 2 diabetes in middleaged men: prospective results from the Massachusetts Male Aging Study, Diabetes Care 2000; 23 (4): 490–4.
- Wilhelmsen L, Berglund G, Elmfeldt D et al. Beta-blockers versus diuretics in hypertensive men: main results from the HAPPHY trial. J Hypertens 1987; 5: 561–72.
- Zmuda JM, Cauley JA, Kriska A et al. Longitudinal relation between endogenous testosterone and cardiovascular disease risk factors in middle-aged men: a 13-year follow-up of former multiple risk factor intervention trial participants. American Journal of Epidemiology 1997; 146 (8): 609–17.
- Бойцов С.А. Особенные органопротективные свойства блокаторов рецепторов ангиотензина II. Сердце. 2008; 6 (4).
- Верткин А.Л., Лоран О.Б., Тополянский А.В. и др. Клиническая эффективность и влияние β-адреноблокаторов на копулятивную функцию у больных с артериальной гипертензией. Кардиология. 2002; 42 (9): 39–42.
- Гапон Л.И., Прилепова А.А., Цыгольник М.Д. Оценка влияния небиволола на показатели церебральной гемодинамики и суточный профиль артериального давления у больных артериальной гипертонией. Кардиология. 2005; 45 (10): 18–22.
- Конради А.О., Бернгардт Э.Р., Смирнова Е.Н. β-Адреноблокаторы при артериальной гипертонии: взгляд третьего тысячелетия. Cons. Med. 2005; 11 (1): 13–6.
- Мазо Е.Б., Гамидов С.И., Сотникова Е.М, Коротеев Р.В. Влияние андрогенов на эндотелиальную функцию у больных эректильной дисфункцией и возрастным андрогенным дефицитом. VI Международная медицинская выставка «Мужское здоровье и долголетие», Москва, 19–20 февраля 2008; с. 63.
- Маколкин В.И. Определено ли место β-адреноблокаторов при лечении артериальной гипертонии. Cons. Med. 2006; 4: 43–7.
- Мамедов М.Н., Горбунов В.М., Джахангиров Т.Ш. Суточный профиль АД при метаболическом синдроме: сравнительный анализ эффективности монотерапии эналаприлом и неконтролируемой гипотензивной терапии. РФК. 2006; 1.
- Мамедов М.Н. Артериальная гипертония в рамках метаболического синдрома: особенности течения и принципы медикаментозной коррекции. Кардиология. 2004; 44 (4): 95–100.
- Маркова Л.И., Самсонова И.В., Самойленко Т.Н., Радзевич А.Э. Влияние небиволола на микроциркуляцию, гемореологию, липидный спектр крови у больных артериальной гипертензией. Мед. пом. 2009; 1: 34–6.
- Мравян С.Р., Калинин А.П. Патогенез артериальной гипертонии при сахарном диабете и побочные действия применяемых гипотензивных средств. Рос. кард. журн. 2001; 1: 66–70.
- Небиеридзе Д.В. Клиническое значение дисфункции эндотелия при артериальной гипертонии. Сons. Med. (Прил.) Системные гипертензии. 2005; 1: 31–8.
- Нурмамедова Г.С., Гумбатов Н.Б., Мустафаев И.И. Уровень гормонов гипофизарно-гонадной оси, пенильный кровоток и половая функция у мужчин с артериальной гипертонией при монотерапии бисопрололом и небивололом. Кардиология. 2007; 47 (6): 50–3.
- Ольбинская Л.И., Вартанова О.А., Хапаев Б.А. Антигипертензивная эффективность и безопасность долгосрочной терапии β1-кардиоселективным адреноблокатором небивололом при монотерапии или в комбинации с гидрохлоротиазидом у больных мягкой и умеренной артериальной гипертензией. Рос. кард. журн. 1999.
- Российское медицинское общество по артериальной гипертонии (РМОАГ), Всероссийское научное общество кардиологов (ВНОК). Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр). 2010.
- Савенков М.П., Волков А.С., Иванов С.Н. и др. Уродинамические эффекты бета-адреноблокаторов: преимущества небиволола. Рац. фармакотер. в кардиол. 2008; 3: 60–5.
- Фогарти Р., Прети П., Дероза Г. Влияние антигипертензивной терапии валсартаном или атенололом на сексуальную активность и уровни тестостерона в плазме у мужчин с гипертензией. Артериальная гипертензия. 2011; 1 (15).
- Чазова И.Е., Ратова Л.Г. Бета-адреноблокаторы с уникальными характеристиками – небиволол. Системные гипертензии. 2008; 3: 55–8.
- Шестакова М.В., Бутрова С.А., Сухарева О.Ю. Метаболический синдром как предвестник развития сахарного диабета типа 2 и сердечно-сосудистых заболеваний. Тер. архив. 2007; 10: 5–8.
- Farinaro E, DellaValle E, Ferrantino G. PLasma lipids and cardiovascular risk: lesions in the community. Ann Ital Med Int 1995: 10 (Suppl.): 31–4.
- Kolloch R, Legler U, Champion A et al. Impact of resting heart rate on outcomes in hypertensive patients with coronary artery disease: findings from the International VErapamil-SR/trandolapril STudy (INVEST). Eur Heart J 2008; 29: 1327–34.
- Mo R, Nordrehaug J, Omvick P, Lund-Johansen P. The Berg blood pressure study: prehypertensive changes in cardiac structure and function in offspring of hypertensive families. Blood Pressure 1995; 4: 1017–27.
- Cohn JN, Levine TB, Olivari MT et al. Plasma norepinephrine as a guide to prognosis in patients with chronic congestive heart failure. N Engl J Med 1984; 311: 819–23.
- Shell W, Sobel B. Deleterious effects of increased heart rate on infarct size in the conscious dog. Am J Cardiol 1973; 31: 474–9.
- Levy RL, White PD, Strod WD, Hillman CC. Transient tachycardia: prognostic significance alone and in association with transient hypertension. JAMA 1945; 129: 585–8.
- Perski A, Hamsten A, Lindvall K, Theorel T. Heart rate correlates with severity of coronary atherosclerosis in young postinfarction patients. Am Heart J 1988; 116: 1369–73.
- Heidland UE, Stauer BE. Left ventricular muscle mass and elevated heart rate are associated with coronary plaque dysruption. Circulation 2001; 104: 1477–82.
- Шальнова С.А., Деев А.Д., Оганов Р.Г. и др. Частота пульса и смертность от сердечно-сосудистых заболеваний у российских мужчин и женщин. Результаты эпидемиологического исследования. Кардиология. 2005; 10: 45–50.
- Palatini P. Heartrateas a risk factor foratherosclerosisandcardiovascularmortality: the effect ofantihypertensivedrugs. Drugs 1999; 57: 713–24.
- CIBIS II Investigators and committers. The cardiac insufficiency bisoprolol study II (CIBIS II): a randomized trial. Lancet 1999; 353: 9–13.
- Fox K, Ford I, Steg PG et al. Heart rate as a prognostic risk factor in patients with coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a subgroup analysis of a randomized controlled trial. Lancet 2008; 372: 817–21.
- Kolloch R, Legler U, Champion A et al. Impact of resting heart rate on outcomes in hypertensive patients with coronary artery disease: findings from the International VErapamil-SR/
