Влияние нестероидного противовоспалительного препарата нимесулида на акцептор свободных радикалов глутатион s-трансферазы у пациентов с остеоартритом коленного сустава
Статьи W. Kullicha, N. Fagerera and H. SchwannbaЦентр ревматологии, бальнеологии и реабилитации, Институт реабилитации внутренних болезней имени Людвига Болцманна, Саалфельден, Австрия
bСпециализированная клиника, Центр реабилитации ревматоидных заболеваний, Саалфельден, Австрия
Адрес для контакта: Univ.-Doz.Dr.W.Kullich, Director, Ludwig Boltzmann Institut fur Rehabilitation interner Erkrankungen, ThorerstraBe 26, 5760 Saalfelden, Austria.
КЛЮЧЕВЫЕ СЛОВА: GST-MMP-Нимесулид-НПВС-остеоартрит-акцептор-TIMP
КРАТКИЙ ОБЗОР
Цель: Остеоартрит (ОА) коленного сустава является вторичным воспалительным, болезненным заболеванием коленного сустава с увеличивающимся разрушением суставного хряща. При воспалительном процессе формирование свободных радикалов (реактивные формы кислорода, РФК) играет большую роль в прогрессировании заболевания, и в последующем разрушении суставного хряща. Целью этого поискового исследования было изучение антиоксидантной активности нестероидного противовоспалительного препарата (НПВС) нимесулида на глутатион S-трансферазу (GST), акцептор свободных радикалов фермента. Кроме того, определяли эффекты на матриксную металлопротеиназу ММР-3 и её антагонист, тканевый ингибитор матриксной металлопротеиназы 3 (TIMP-1).
Дизайн и методы исследования: Это открытое, поисковое исследование с участием 20 пациентов (в возрасте 41-71 лет) с болезненным остеоартритом коленного сустава, которые получали нимесулид в дозе 100 мг два раза в сутки в течение 3 недель. Двадцать три здоровых добровольца (в возрасте 23-57 лет), не соответствующих по возрасту, служили в качестве группы сравнения. GST, ММР-3 и TIMP-1 определяли методами энзимного иммунного анализа. Клинические симптомы и функцию сустава оценивали по индексу WOMAC.
Результаты: За трехнедельный период терапии нимесулидом в дозе 100 мг два раза в сутки уровень акцепторов GST и соотношение TIMP-1/ММР-3 существенно повысились. Это изменение сопровождалось значимым клиническим улучшением, которое выражалось в уменьшении боли, тугоподвижности сустава и улучшении функции сустава. Два нежелательных явления возможно связаны с применением нимесулида: в одном случае наблюдался умеренный отек век, во втором- умеренная диарея без патологии на эндоскопии.
Заключение: Эти результаты подтверждают антиоксидантные свойства исследуемого препарата, и, что помимо известных противовоспалительных свойств, нимесулид обладает несомненной антиоксидантной активностью, которая оказывает дополнительную поддержку своей ключевой роли в лечении пациентов с ОА (благодаря отсутствию дегенеративных эффектов на хрящ).
ВВЕДЕНИЕ
Остеоартрит (ОА) коленного сустава - это заболевание сустава, характеризующееся болью, тугоподвижностью сустава и ограничением подвижности в результате деградации хряща и наличия местных вторичных воспалительных процессов1-3. Это заболевание является значимым социально-экономическим бременем в связи с затратами на лечение и потерей рабочего времени4.
Лекарственная терапия пациентов с ОА коленного сустава включает применение нестероидных противовоспалительных средств (НПВС), которые часто используются в качестве терапии первой линии5,6. Нимесулид является нестероидным, противовоспалительным препаратом, принадлежащим к классу сульфонанилидов, которые успешно использовались с 1985 года для симптоматического лечения ревматоидных и мышечно-скелетных заболеваний из-за их хорошего противовоспалительного и анальгезирующего действия7-10.
Кроме того, помимо иных свойств нимесулид и его основной метаболит 4-гидроксинимесулид (4-ОН нимесулид) проявляют сильную антиоксидантную активность. Оба соединения действуют как акцепторы на свободные радикалы кислорода (реактивные формы кислорода, РФК), которые формируются в организме, например во время перекисного окисления липидов, воспаления или везикулярного дыхания8-10.
РФК, выработанные хондроцитами, играют большую роль в патогенезе ревматоидных заболеваний11. Результаты исследования, проведенного Zheng et al12, показывают, что нимесулид и 4-ОН нимесулид оказывают не только акцепторное действие на РФК, но могут также ингибировать свободные радикалы, сформированные хондроцитами во время артритического процесса. Эти антиоксидантные свойства могут дополнительно положительно влиять на воспалительные процессы при ОА11,13.
Глутатион S-трансферазы (GST) принадлежат к семейству детоксикационных изоэнзимов14, которые катализируют конъюгацию глутатиона с рядом гидрофобных соединений. Они обеспечивают защиту клеток млекопитающих от токсических и неопластических эффектов РФК и электрофильных метаболитов канцерогенов. Поэтому, статус GST является полезным прогностическим фактором для определения антиоксидантных эффектов различных лекарств, включая антиоксидантные противовоспалительные препараты.
Основываясь на этих более ранних данных важно было установить, может ли нимесулид влиять на уровни GST при остеоартрите, учитывая его антиоксидантные свойства12,15,16.
Вторичные воспалительные механизмы, которые развиваются во время остеоартрита, совместно с реактивными формами кислорода, вырабатываемыми при воспалительной реакции, могут в ходе артритического заболевания провоцировать усиление прогрессирования клеточного поражения, которое способствует разрушению хряща, развитию боли, отека и выпота в сустав (приводящие к активации ОА)1,2,13.
Матриксные металлопротеиназы (ММР) и их ингибиторы (тканевые ингибиторы матриксных металлопротеиназ, TIMP) играют важную роль в трансформации внеклеточного матрикса, и считаются важными факторами в разрушении хряща у пациентов с ОА. Нимесулид может предотвращать формирование ММР, которые разрушают хрящ9,10,17. Изменчивое влияние нимесулида на медиаторы воспаления способствует защите от окислительных радикалов и металлопротеиназ9. При воспалительных процессах ОА антиоксидантные эффекты нимесулида могут уменьшить воспаление и впоследствии влияние соотношения TIMP-1/MMP-3.
Так как соотношение ингибирования вредных металлопротеиназ является хорошим индикатором наличия энзимной атаки на структуры хряща, также интересно исследовать уровень TIMP во время применения нимесулида в течение нескольких недель таким образом, чтобы было возможно лучше оценить эффект на хрящ, вызванный поражающими энзимами.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты
В открытом поисковом исследовании участвовали 20 пациентов (10 мужчин и 10 женщин) с болезненным остеоартритом коленного сустава в ходе их реабилитации в течение нескольких недель в Реабилитационном Центре/ Специализированной больнице (SKA), Саалфельден. Лечение этих пациентов включало применение нимесулида (Аулин, Helsinn Healthcare, Швейцария) в таблетках по 100 мг два раза в сутки в течение 3 недель. Кроме того, всем пациентам проводили стандартизированную программу физиотерапии, включающую лечебную гимнастику и гидротерапевтические упражнения, механотерапию, в том числе силовую тренировку, термотерапию, лечебные ванны и массаж.
Возраст пациентов составлял от 41 до 71 лет, в среднем 54.8 лет. Двадцать три здоровых добровольца без клинических и рентгенологических признаков и симптомов ОА коленного сустава, в возрасте от 23- 57 лет (в среднем 42 года), не получающих лекарственной терапии, служили контрольной группой.
К сожалению, не возможно было набрать контрольную группу здоровых добровольцев такого же возраста, так как почти все люди пожилого возраста нуждаются в лекарственной терапии из-за различных заболеваний (например, нарушение артериального давления, ревматоидные заболевания, нарушение липометаболизма) и/или наличия признаков начала дегенеративного процесса в суставах.
До включения в исследование все пациенты предоставили информированное, письменное согласие на участие в испытании. Исследование проводилось в соответствии с принципами Хельсинкской Декларации Всемирной Медицинской Ассоциации.
СБОР ДАННЫХ
При поступлении в реабилитационный центр врач проводил всестороннее клиническое обследование пациента. Помимо лабораторных анализов симптомы болезни и функциональные ограничения определяли по Индексу WOMAC (индекс остеоартрита Университетов МакМастера и Западного Онтарио)18. Эти обследования проводились до начала приема нимесулида и в конце 1, 2 и 3 недель терапии.
Сбор образцов
Образец венозной крови (натощак) был взят утром (а) при поступлении в центр (1-3 дни) и (b) при выписке (19-21 дни). После отделения сыворотки методом центрифугирования (15 минут, 1.750 х г), часть сыворотки разделили для дальнейших анализов, а часть заморозили при -50°С.
Лабораторные анализы
Скорость оседания эритроцитов через 1 час (СОЭ1), уровень С-реактивного белка (в качестве белка острой фазы), количество эритроцитов и лейкоцитов измеряли в качестве части обычных стандартных лабораторных анализов. Энзимные иммунноанализы использовались для измерения уровня глутатион S-трансферазы (GST), матриксной металлопротеиназы 3 (ММР-3) и ингибитора ММР-3 (TIMP-1).
Глутатион-S-трансферазы-π (GST-π): определяются энзимным иммунноанализом (EIA) компании Иммундиагностик АГ Беншейм, Германия, с использованием поликлональных антител кроликов. Устанавливалось изменение цвета при длине волны 450 нм. Концентрация измерялась в нг/мл.
Матриксная металлопротеиназа 3 (ММР-3, стромели-зин-1): определяется методом ELISA компании Амершам Фармация Биотех, Великобритания. Чувствительность анализа составляется 2.35 нг/мл. Устанавливалось изменение цвета при длине волны 450 нм.
Тканевый ингибитор матриксной металлопротеиназы 3 (TIMP-1): человеческий тканевый ингибитор матриксной металлопротеиназы определяется прямым методом ELISA компании Бендер Мед Системс Венна, Австрия. Измерение проводилось при длине волны 450 нм. Концентрация измерялась в нг/мл.
В анализах использовались фотометр с титрационным микропланшетом (ANTHOS Elisa Reader 2010) и программное обеспечение ADAP, версия 1.6 от компании Антос Лабтех Инструментс ГмбХ, Уолс, Австрия.
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Для оценки использовались программы SYSTAT версия 9.0 Statistics for Windows (SPSS INC., США) и Microsoft Offise Excel 2003 с использованием следующих статистических процессов: описательные статистики (среднее значение, медиана, стандартное отклонение и стандартная ошибка); непараметрическая статистика (ранговый критерий Вилкоксона, критерий Крускаля-Уоллиса); дисперсионный анализ (ANOVA).
РЕЗУЛЬТАТЫ
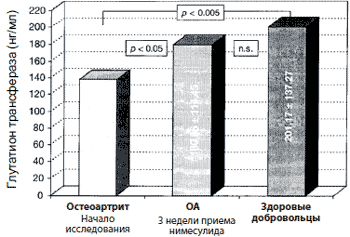
Уровень глутатион-S-трансферазы-π (GST-π): существенно повысился (р<0.05) у пациентов с ОА коленного сустава, получавших нимесулид 100 мг два раза в сутки в течение 3 недель. На рисунке 1 представлены результаты пациентов, получавших нимесулид, и группы здоровых добровольцев, не получавших нимесулид. С помощью критерия Крускаля-Уоллиса показано, что у этих здоровых добровольцев значения GST были существенно выше (p<0.05), чем у пациентов с ОА, не получавших лечения. Через 3 недели терапии нимесулидом по 100 мг два раза в сутки отсутствовало существенное различие между пациентами с ОА, получавшими нимесулид, и здоровыми добровольцами из контрольной группы.
Рисунок 1: Концентрация глутатион-S-трансферазы-π (GST-π) (в нг/мл) до и после 3-недельной терапии нимесулидом (n=20) в клинике. р=уровень значимости. Группа сравнения включает здоровых добровольцев, не получавших нимесулид (n=23).
Уровень С-реактивного белка и скорость оседания эритроцитов, признанные параметрами воспаления, были в пределах нормы, и, преимущественно из-за малого количества случаев с высокими стандартными отклонениями, не возможно было продемонстрировать статистически значимое различие (Таблица 1).
Таблица 1. Результаты лабораторных анализов в начале и конце реабилитации, включающей применение нимесулида
| Параметр | Начало исследования | 3-х недельная терапия | р значение | ||||
| Среднее арифметическое | Стандартное отклонение | Медиана | Среднее арифметическое | Стандартное отклонение | Медиана | ||
| GST-л (нг/мл) | 138.00 | 96.42 | 100.83 | 180.86 | 114.45 | 161.73 | < 0.05 |
| CRP (мг/дл) | 0.76 | 1.40 | 0.20 | 0.33 | 0.35 | 0.20 | n.s. |
| СОЭ1 (мм/час) | 9.90 | 8.70 | 7.50 | 8.63 | 6.22 | 7.00 | n.s. |
| ММР-3 (нг/мл) | 21.12 | 16.42 | 16.00 | 14.66 | 12.42 | 10.70 | < 0.001 |
| TIMP-1 (нг/мл) | 198.83 | 96.84 | 150.66 | 207.44 | 104.52 | 171.55 | n.s. |
| индекс | 14.35 | 13.84 | 10.04 | 36.90 | 58.89 | 14.25 | < 0.03 |
В течение 3 недель терапии существенно (p<0.001) понизился уровень матриксной металлопротеиназы-3, разрушающей хрящ.
Уровень TIMP, ингибитора ММР-3, только незначительно, не значимо изменялся во время периода терапии. Сравнение уровней TIMP-1 у леченных пациентов и здоровых добровольцев показало значимое различие (р=0.037) только во время поступления в больницу, но не во время выписки. У пациентов с ОА значения TIMP-1 стремились достичь уровней, отмеченных в контрольной группе.
В связи с наличием прямой связи между ММР-3 и TIMP-1, рассматривался индекс, соотношение ТIМР-1:ММР-3 (Таблица 1). Чем выше индекс, тем менее тяжелую энзимную атаку на хрящ стоит ожидать. Увеличение индекса отмечено у 64.7% пациентов (> 20%), тогда как у 23.5% больных значение индекса понизилось (> 20%). Только у 12% пациентов значение индекса не изменилось.
Зарегистрировано два нежелательных явления, которые вероятно, но не определенно, связаны с приемом нимесулида (один случай - умеренный отек век; второй случай -умеренная диарея без патологии на эндоскопии).
ОБСУЖДЕНИЕ
Уже было продемонстрировано антиоксидантное действие нестероидного противовоспалительного средства нимесулида и его метаболита 4-ОН нимесулида15,19. Эти исследования in vitro показали, что нимесулид проявлял прямую ОН· и О2· акцепторную активность, которой столь же очевидно обладал и его основной метаболит М1, даже, если и в меньшей степени, чем основной препарат. Интересно, что М1 и М2 метаболиты проявляли более высокую акцепторную активность по сравнению с нимесулидом в отношении других реактивных повреждающих радикалов, таких как R·, RO· и ROO· 19. Другие исследования показали, что нимесулид может ограничивать выработку супероксид радикалов (О2·), что приводит к уменьшению количества их окислительных производных пероксида водорода (Н2О2) и хлорноватистой кислоты (HOCl)10,16,20,21. Более того, нимесулид ингибирует активность миелопероксидазы, участвующей в конверсии Н2О2 в HOCl22. Таким образом, основываясь на выше приведенных данных, противовоспалительная терапия нимесулидом может уменьшать плазменный уровень свободных радикалов у пациентов с ОА, что приводит к положительному влиянию на эндогенные энзимы, обладающие антиоксидантным эффектом, такие как глутатион S-трансферазы (GST). Глутатион S-трансферазы (альфа, му, пи, фета) катализируют перенос глутатиона (GSH, клеточного акцептора, к окислительным метаболитам, примесям и лекарствам, которые таким образом нейтрализуются. GSН предоставляет электроны этим молекулам с продукцией глутатион дисульфата (GSSG) в его окисленной форме14.
У пациентов с раком GST могут нейтрализовать химиотерапевтические препараты в раковых клетках, таким образом, способствуя развитию резистентности 23.
В связи с повышенным окислительным стрессом и усиленным формированием свободных радикалов, как в случае с воспалительными процессами, возникнет повышенная потребность в GSН и, следовательно, в GST. Однако, увеличение активности GST через повышенные экспрессию гена и синтез белка не может компенсировать снижение концентрации GST, вызванное усиленным поглощением GST воспаленными суставами. Кроме того, уменьшение концентрации GST приводит к нарушению гомеостаза GSWGSSG со снижением уровня GSH14.
Как показало наше исследование концентрации GST повышались в течение 3 недель терапии нимесулидом, в среднем на 64.26%. Отсюда можно допустить, что, в результате высокой антиоксидантной активности нимесулида, продемонстрированной в нашем исследовании, препарат может способствовать повышению уровня глутатион трансфераз за счет уменьшения ОН· и О2· радикалов, и их метаболитов (Н2О2, НОСL)15,20,21.
В соответствии с нашими предыдущими данными24 и наблюдениями Bevilacqua и Manicourt за пациентами с ОА17,25 при применении нимесулида в период реабилитации существенно понизился (p < 0.001) уровень матриксной металлопротеиназы 3 (ММР-3) (Таблица 1). Металлопротеиназы являются цинк-зависимыми эндопептидазами, которые участвуют в разрушении внеклеточного матрикса. В частности, ММР-3 (стромелизин-1) влияет на фрагменты распада человеческого коллагена типа II, уже инициированного ММР-1. Деградация внеклеточного матрикса в хряще является признаком развития остеоартрита26,27. Результаты по ММР-3, полученные в нашем исследовании, показывают, что нимесулид может уменьшать деградацию хрящевого матрикса путем ингибирования синтеза металлопротеиназ. Тканевые ингибиторы матриксных металлопротеиназ (TIMPs) действуют как антагонисты для ММР. Одним из основных ингибиторов металлопротеиназ в суставе является TIMP-1. Эти гликопротеины блокируют энзимную активность, активно связывая активированные металлопротеиназы, и таким образом, могут поддерживать баланс между деградацией новым формированием матрикса28,29. В этом процессе ММР и TIMP формируют, так называемые комплексы энзимных ингибиторов 1:1. В воспалительных процессах ОА антиоксидантные эффекты нимесулида могут уменьшать воспаление и далее влиять на соотношение TIMP-1/ММР-3.
В экстрактах хряща пациентов с остеоартритом обнаружены повышенная экспрессия ММР с нарушением баланса активности TIMP с потерей хряща30. В соответствии с результатами, полученными Bevilacqua et al17 и Manicourt et al25 не возможно было установить существенное увеличение сывороточного уровня TIMP, но с другой стороны соотношение TIMP/ММР указывало на то, что нимесулид не влияет на активизированный распад хряща. Тщательно разработанный нами индекс (Индекс TIMP-1/ММР-3) показывает связь между обоими параметрами (Таблица 1). Высокое значение индекса обозначает высокое соотношение TIMP-1 к ММР-3, что в результате приводит к меньшей энзимной деградации внеклеточного матрикса31; это показано по увеличению после 3 недель терапии.
Индекс WOMAC ОА использовался для оценки клинической картины: боли и ограничения подвижности пациента. Более раннее исследование, проведенное в 2002 году24, уже продемонстрировало значительное улучшение в трех областях (боль, тугоподвижность сустава и функция сустава) (Таблица 2) при применении нестероидного противовоспалительного препарата нимесулида. Следует также заметить, что помимо нимесулида свою положительную роль на индекс WOMAC может играть также стандартизированная программа физиотерапии.
Таблица 2. Боль, тугоподвижность и функция сустава из показателя WOMAC. Значения представлены в виде средних арифметических значений ± стандартное отклонение
| Терапия | Показатель WOMAC | ||
| Боль | Тугоподвижность сустава | Функция сустава | |
| До приема нимесулида | 25.2 ± 7.3 | 9.4 ± 4.4 | 88.5 ±26.9 |
| Через 1 неделю | 15.9 ± 8.1 | 5.5 ± 3.8 | 56.8 ± 25.3 |
| Через 2 недели | 10.5 ± 6.2 | 4.8 ± 4.3 | 40.3 ± 27.1 |
| Через 3 недели | 8.5 ± 8.5 | 3.9 ± 4.4 | 30.9 ± 29.6 |
| Значимость (Р) | 0.001 | 0.016 | 0.029 |
ЗАКЛЮЧЕНИЕ
Это открытое, поисковое исследование с включением группы сравнения, в которой участники не соответствовали по своему возрасту пациентам с ОА, и относительно небольшим количеством больных. Для полного подтверждения результатов, полученных при приеме нимесулида в дозе 100 мг два раза в сутки, и оценки, насколько реабилитация в стационаре с её условиями пониженного стресса может влиять на GST активность или на окислительный стресс, необходимо провести дополнительные исследования.
Тем не менее, антиоксидантные свойства нимесулида, продемонстрированные в этом исследовании, особенно его активность в отношении GST, подтверждают хорошие противовоспалительные свойства препарата и дополнительно укрепляют профиль эффективности нимесулида, поддерживаемый более 20-летними клиническими испытаниями.
БЛАГОДАРНОСТЬ
Заявление об интересе: Эта работа поддерживалась из общего бюджета компании Людвиг Болцманн (Австрия) в научных интересах и за счет грантов, полученных из Управления Пенсионным Страхованием (Австрия). Авторы благодарят Helsinn Healthcare за согласие оплатить опубликование статьи. Авторы также благодарят B. Schweiger за техническую помощь в лабораторных исследованиях. ССЫЛКИ
1. Wieland НА, Michaelis М, Kirschbaum BJ, Rudolphi КА. Osteoarthritis - an untreatable disease? Nature Rev Drug Discoy 2005;4:331-44
2. Kean WF, Kean, R, Buchanan WW. Osteoarthritis: symptoms, signs and source of pain. Inflammopharmacology 2004,12: 3-31
3. Felson DT. The sources of pain in knee osteoarthritis. Curr Opin Rheumatol 2005;17:624-8
4. WHO Scientific Group. The burden of musculoskeletal conditions at the start of the new millennium. World Health Organ Tech Rep Ser 2003;919:1-218
5. Pavelka K. Symptomatic treatment of osteoarthritis: paracetamol or NSAIDs? Int J Clin Pract 2004;58:5-12
6. Jordan KM, Arden NK, Doherty M, et al. EULAR Recommendations 2003; an evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for International Studies Including Therapeutic Trials (ESCISIT). Ann Rheum Pis 2003;62: 1145-55
7. Davis R, Brogden RN. Nimesulide - an update of its pharmacodynamic and pharmacokinetic properties, and therapeutic efficacy. Drugs 1994;48:431-54
8. Bennett A. Nimesulide: a well-established cyclooxygenase-2 inhibitor with many other pharmacological properties relevant to inflammatory diseases. In: Vane JJ, Botting RM eds. Therapeutic Roles of Selective COX-2 Inhibitors. London: William Harvey Press, 2001:524-40
9. Rainsford KD. The discovery, development and novel actions of nimesulide. In: Rainsford KD, ed. Nimesulide, Actions and Uses. Basel, Boston, Berlin: Birkhauser Verlag, 2005
10. Rainsford KD; Members of the Consensus Report Group Med Res Opin 2006;22:1161-70
11. Ostalowska A, Birkner E, Wiecha M, et al. Lipid peroxidation and antioxidant enzymes in synovial fluid of patients with primary and secondary osteoarthritis of the knee joint. Osteoarthr Cartil 2006;14:139-45
12. Zheng SX, Monithys-Mickalad A, et al. In vitro study of the antioxidant properties of nimesulide and 4-OH nimesulide: effects on HRP- and luminal dependent chemoluminescence produced by human chondrocytes. Osteoarthri Cartil 2000;8:419-25
13. Yudoh K, Nguyen T, Nakamura H, et al. Potential involvement of oxidative stress in cartilage senescence and development of osteoarthritis: oxidative stress induces chondrocyte telomere instability and down regulation of chondrocyte function. Arthritis Res Ther 2005;7:R380-91. Epub 2005 Jan 26
14. Kidd PM. Glutathione: systemic protectant against oxidative and free radical damage. Alt Med Rev 1997;2:155-76
15. Maffei Facino R, Carini M, Aldini G, et al. Differential inhibition of superoxide, hydroxyl and peroxyl radicals by nimesulide and its main metabolite 4-hydroxynimesulide. Arzneimittelforschung 1995;45:1102-10
16. Bevilacqua M, Vago T, Baldi G, et al. Nimesulide decreases superoxide production by inhibiting phosphodiesterase type IV. Eur J Pharmacology, 1994,268:415-23
17. Bevilacqua M, Devogelaer JP, Righini V, et al. Effect of nimesulide on the serum levels of hyaluronan and stromelysin-1 in patients with osteoarthritis: a pilot study. Int J Clin Pract Suppl 2004;144:13-19
18. Stucki G, Meier D, Stucki S, et al. Evaluation of a German version of WOMAC (Western Ontario und McMaster Universities) Arthrosis Index. Z Rheumatol 1996;55:40-9 [German]
19. Maffei-Facino R, Carini M, Aldini G. Anti-oxidant activity of nimesulide and its main metabolites. Drugs 1993;46(Suppl 1): 15-21
20. Ottonello L, Dapino P, Pastorino G, et al. Nimesulide as a down-regulator of the activity of neutrophil myeloperoxidase pathway. Drugs 1993;46:29-33
21. de Mello SB, Laurindo IM, Cossermelli W. Action of the 4-nitro-2-phenoximethanesulphonamide (nimesulide) on neutrophil chemotaxis and superoxide production. Sao Paulo Med J 1994;112:489-94
22. Ottonello L, Uapino P, Scirocco MC, et al. Sulfonamides as anti-inflammatory agents: old drugs for new therapeutic strategies in inflammation? Clin Sci 1995; 88:331-6
23. Su F, Hu X, Jia W, et al. Glutathion S transferase pi indicates chemotherapy resistance in breast cancer. J Surg Res 2003;113:102-8
24. Kullich WC, Niksic F, Klein G. Effect of nimesulide on metalloproteinases and matrix degradation in osteoarthritis: a pilot study. Int J Clin Suppl 2002;128:24-9
25. Manicourt DH, Bevilacqua M, Righini V, et al. Comparative effect of nimesulide and ibuprofen on the urinary levels of collagen type II C-Telopeptide degradation products and on the serum levels of hyaluronan and matrix metalloproteinases-3 and -13 in patients with flare-up of osteoarthritis. Drugs R D 2005;6:261-71
26. Sandy JD. Proteolytic degradation of normal and osteoarthritic cartilage. In: Brandt KD, Doherty M, Lohmander LS, eds. Osteoarthritis, 2nd edn. Oxford: Oxford University Press, 2003:82-92
27. Clark IM, Murphy G. Matrix Proteinases. In: Seibel MJ, Robins SP, Bilezikian JP, eds. Dynamics of Bone and Cartilage Metabolism. San Diego: Academic Press, 1999:137-50
28. Cawston ТЕ. Metalloproteinase inhibitors and the prevention of connective tissue breakdown. Pharmacol Ther 1996;3: 163-82
29. Brew K, Dinarkarpandian D, Nagase H. Tissue inhibitors of metalloproteinases: evolution, structure and function, Biochim Biophys Acta 2000;1477:267-83
30. Dean DD, Martel-Pelletier J, Felletier JP, et al. Evidence for metalloproteinase and metalloproteinase inhibitor imbalance in human osteoarthritic cartilage. J Clin Invest 1989;84:678-85
31. Dawson T, Roman D. Tissue destruction and repair. In: Hochberg MC, Silman AJ, Smolen JS, et al. Rheumatology, 3rd edn. Mosby Verlag, 2003
Комментарии
ПРАКТИКА ПЕДИАТРА
