Комбинация паклитаксела и цисплатина для лечения больных раком яичника на стадиях III и IV
СтатьиУ. Л. МакГуайр, У. Д. Хоскинс, М. Ф. Брэди, П. Р. Куцера, Е. Е. Партридж, К. Й. Лук, Д. Л. Кларк-Пирсон, М. Дэвидсон
New England Journal of Medicine 334: 1-6 (1996)
Методы
Характеристики больных
Результаты
Доставленная доза и переносимость препарата
Токсичность
Ремиссии
Обсуждение
Литература
История вопроса. Химиотерапевтические комбинации, содержащие алкилирующий агент и координационное соединение платины, обеспечивают высокий процент ремиссий при распространенном раке яичника. Однако такие комбинации дают длительный контроль заболевания лишь у немногих больных. Мы провели сравнение двух комбинаций, а именно цисплатина в сочетании с циклофосфамидом и циклофосфамида в сочетании с паклитакселом, у женщин с раком яичника.
Методы. Статистически случайным образом 410 женщин с распространенным раком яичника и остаточной опухолью размером более 1 см после исходной хирургии направлялись в группу; получавшую цисплатин (750мг/м2 площади поверхности тела) в сочетании с циклофосфамидом (135 мг/м2) или с паклитакселом (135 мг/м2, вводимым на протяжении 24 часов).
Результаты. 386 женщин отвечали всем критериям для участия в испытании. Известные прогностические факторы в двух группах были одинаковыми. Такие побочные эффекты, как алопеция, нейтропения, повышение температуры тела и аллергические реакции, отмечались чаще в группе цисплатина и паклитаксела. Среди 216 женщин с поддающимся количественной оценке заболеванием 73 процента в группе цисплатин-паклитаксел дали ремиссию по сравнению с 60 процентами в группе цисплатин-циклофосфамид(Р=0,01). Частота подтвержденных патологом полных ремиссий была одинаковой для обеих групп. Выживание в условиях отсутствия прогрессирования заболевания было достоверно более длительным (Р<0,001) в группе цисплатин-паклитаксел по сравнению с группой цисплатин-циклофосфамид (средние значения (медиана) 18 и 13 месяцев). Выживаемость также была достоверно более длительной (Р<0,001) в группе цисплатин-паклитаксел (медиана - 38 месяцев по сравнению с 24 месяцами).
Выводы. Включение паклитаксела в схему химиотерапии первой линии увеличивает продолжительность периода, свободного от прогрессии заболевания, и общую выживаемость у женщин с не полностью удаленным раком яичника на стадиях III и IV.
Стандартной формой лечения женщин с распространенным эпителиальным раком яичника в Соединенных Штатах является использование алкилирующего агента в сочетании с цисплатином. Комбинированная терапия на основе цисплатина оказалась более эффективной по сравнению с лечением только алкилирующими агентами [1] или комбинациями без цисплатина [2,3] при определении с помощью таких критериев, как процент клинических ремиссий и продолжительность безрецидивного периода. Однако данные, касающиеся преимуществ в плане общей выживаемости, являются менее убедительными. Когда алкилирующие агенты или комбинации, не содержащие соединений платины, используются для лечения распространенного рака яичника, ожидаемый средний процент ремиссий составляет от 40 до 50 процентов (от 10 до 20 процентов полных ремиссий по хирургической оценке), причем среднее время выживания составляет от 12 до 15 месяцев. У женщин, получающих лечение комбинациями, содержащими цисплатин в качестве первичной терапии, процент ремиссий составляет от 60 до 80 процентов, причем полные ремиссии чаще всего отмечаются у женщин, которым было проведено адекватное хирургическое лечение [5].
Единственное крупное проспективное рандомизированное исследование по сравнению цисплатина и комбинаций, содержащих цисплатин, при распространенном раке яичника позволило предположить, что цисплатин сам по себе является столь же эффективным, как и комбинации, содержащие соединения платины [6], но является менее токсичным и будет с меньшей вероятностью приводить к появлению вторичных опухолей. Однако анализ рандомизированных терапевтических испытаний позволил предположить, что комбинации, содержащие платину, дают лучшие результаты по сравнению с использованием цисплатина в форме монотерапии [7]. У больных с распространенным раком яичника комбинация цисплатина и циклофосфамида в настоящее время представляет собой стандартную форму лечения. К сожалению, длительный контроль заболевания при использовании этой схемы наблюдается менее чем у 10 процентов женщин с не полностью удаленной опухолью на стадии III и менее чем у 5 процентов женщин на стадии IV [8].
После того, как цисплатин появился как активный препарат для лечения эпителиального рака яичника, прошло более 10 лет, прежде чем был разработан другой препарат, который мог давать ремиссии у женщин с опухолью, резистентной к соединениям платины. В 1989 г. появилось сообщение, что паклитаксел дает 24 процента ремиссий у женщин с раком яичника, резистентным к соединениям платины (общий процент ремиссий составлял 30 процентов) [9]. Активность препарата была подтверждена в группе больных, предшествующая химиотерапия у которых была менее интенсивной и которые получали более высокую исходную дозу [10]. Процент ремиссий у этих женщин составлял 37 процентов, так что паклитаксел стал наиболее активным индивидуальным препаратом, который когда-либо оценивался группой по гинекологической онкологии (ГГО) в рамках исследования рака яичника по фазе II. В последующем испытание комбинации паклитаксела и цисплатина в рамках фазы 1 показало, что оба эти препарата можно безопасно комбинировать друг с другом, причем паклитаксел вводится сначала путем 24-часового вливания, а непосредственно за ним следует введение цисплатина [II]. Применение паклитаксела при эпителиальном раке яичника было предметом недавних обзоров [12,13].
Воспроизводимая активность паклитаксела в качестве терапии последнего выбора дает возможность легко и безопасно комбинировать его с цисплатином, а неудовлетворительные отдаленные результаты стандартного лечения привели ГГО к мысли о необходимости начать проспективное рандомизированное испытание по фазе III для сравнения комбинации цисплатина и паклитаксела со стандартным лечением женщин с не полностью удаленным раком яичника на стадии III или IV.
МЕТОДЫ
Кандидатами для включения в исследование были женщины с хирургически подтвержденным эпителиальным раком яичника на стадии III (пограничные опухоли исключались), которым проводилось хирургическое лечение и присутствовала остаточная масса опухоли (размер 1 см) или женщины с опухолью на стадии IV. У них могла присутствовать клинически количественно характеризуемая опухоль или опухоль, не поддающаяся количественному измерению (но поддающаяся оценке). Другие критерии включения в исследование включали отсутствие ранее проводившейся химиотерапии, получение информированного согласия, балл функционального статуса GOG [14] равный 0, 1 или 2, содержание клеток белой крови по крайней мере 3000/мм3, содержание тромбоцитов по крайней мере 100000/мм3; содержание креатинина сыворотки 2,0 мг/дл (177 мкмоль/л) или менее и значения сывороточного билирубина и сывороточной аспартатаминотрансферазы, не более чем вдвое превышающие верхние пределы для соответствующего медицинского центра. Больные должны были начать участие в испытании в пределах 6 недель после операции и им не должна была проводиться предварительная химиотерапия или лучевая терапия по поводу рака яичника или по поводу какой-либо другой опухоли за исключением рака кожи (кроме меланомы). Женщины с кардиоаритмиями в анамнезе или недавно принимавшие антиаритмические препараты исключались из числа участников испытания. Материалы просматривались патологом в центре для того, чтобы подтвердить, что материал соответствовал поставленному диагнозу. Аналогичным образом каждая больная анализировалась в отношении адекватности исходной хирургической процедуры, и один из нас осуществил анализ всей информации, полученной от хирурга и патолога для оценки объема опухоли до хирургической операции и после нее, а также для рассмотрения данных, полученных при повторной обзорной лапаротомии.
После включения в число участниц испытания у женщин проводили анализ истории болезни, физическое обследование и выполняли лабораторные анализы. Перед началом лечения и после каждого второго курса лечения с помощью соответствующих методов визуализации оценивали степень заболевания.
Женщины в группе стандартной терапии получали циклофосфамид (750 мг/м2 площади поверхности тела внутривенно) и цисплатин (75 мг/м2 площади поверхности тела внутривенно со скоростью введения 1 мг в минуту) через каждые три недели, всего проводилось шесть курсов лечения. Женщины в группе экспериментальной терапии получали паклитаксел (135 мг/м2 внутривенно путем 24-часового непрерывного вливания) и цисплатин (75 мг/м2 внутривенно со скоростью введения 1мг/мин) с интервалом в три недели, всего проводилось шесть курсов. Женщинам, включенным в экспериментальную группу, проводили премедикациюдексаметазоном (20 мг перорально или внутривенно за 14 и 7 часов перед началом вливания паклитаксела). Как дифенгидрамин (50 мг), так и антагонисты гистаминовых Н2-рецепторов вводили внутривенно за 30 минут до вливания паклитаксела.
Схема лечения назначалась на основе рандомизации Статистической службой группы по гинекологической онкологии, причем после стратификации в зависимости от медицинского учреждения и возможности клинической количественной оценки заболевания вероятность попадания в обе группы была одинакова. Группа женщин с клинически измеримым заболеванием составила основу для определения процента клинических ремиссий. Больные, заболевание у которых не поддавалось количественной клинической оценке, и те, заболевание у которых поддавалось клинической оценке, но в конце назначенного курса лечения наступала полная клиническая ремиссия, должны были пройти повторную лапаротомию для определения ремиссии по оценке патолога.
Все побочные эффекты оценивались в соответствии с критериями токсичности GOG [14]. Содержание клеток белой крови у женщин должно было составлять по крайней мере 3000/мм3, а содержание тромбоцитов по крайней мере 100000/мм3 перед началом следующего курса лечения. Курс лечения мог быть отложен на одну или несколько недель до тех пор, пока не достигалось указанное содержание форменных элементов крови. Если такая задержка превышала три недели, женщина снималась с испытания. Задержки последующих курсов лечения не разрешались по поводу токсичности в отношении ЖКТ, периферической нейротоксичности 1 или 2 степени, легкой формы почечной токсичности (уровень креатинина сыворотки 52 мг/дл) [177мкмоль/л] или при значении креатининовогоклиренса а 50 мл/мин), а также при легкой форме ототоксчности (снижение дискриминационной функции в области высоких частот »10 дб). Более тяжелые неврологические, слуховые и почечные токсические эффекты, которые не исчезали к моменту введения следующей дозы, требовали снятия женщины с исследования, однако наблюдение за ней продолжалось. О кардиологических токсических эффектах (за исключением симптоматической синусовой брадикардии) докладывалось председателю испытания и они рассматривались как аргумент для прекращения лечения. Тяжелые аллергические реакции (бронхоспазм, гипотония или диффузная крапивница) во время вливания паклитаксела были показанием к немедленному прекращению вливания и снятию женщины с экспериментальной схемы лечения. Снижение доз циклофосфамида или паклитаксела (снижение дозы цисплатина не разрешалось) во время последующих курсов лечения было основано на минимальном содержании (надир) форменных элементов крови во время предыдущего курса лечения. Гематологическая токсичность степени 4 (характеризующаяся содержанием клеток белой крови 51000/мм3, абсолютное содержание нейтрофилов 5500/мм3 или содержание тромбоцитов 525000/мм3 в минимуме) требовала снижения дозы циклофосфамида до 500 мг/м2 или дозы паклитаксела до 110 мг/м2 во время последующего курса с повторным увеличением в ходе более поздних курсов, если значения содержания в минимуме не соответствовали указанной выше степени 4.
ХАРАКТЕРИСТИКИ БОЛЬНЫХ
Таблица 1. Характеристики больных в зависимости от группы лечения
| Характеристика |
Цисплатин + циклофосфамид (N=202) |
Цисплатин + паклитаксел (N=184) |
| Возраст в годах | ||
| Медиана | 60 | 59 |
| Интервал | 27-80 | 20-84 |
| Функциональный статус по GOG* | ||
| 0 | 55 (27) | 56 (30) |
| 1 | 109 (54) | 97 (53) |
| 2 | 38(19) | 31 (17) |
| Клеточный тип | ||
| Серозная аденокарцинома | 130 (64) | 140 (76) |
| Аденокарцинома эндометриоида | 26 (13) | 15 (8) |
| Муцинозная аденокарцинома | 10 (5) | 4 (2) |
| Светлоклеточная аденокарцинома | 5 (2) | 3 (2) |
| Прочее | 31 (15) | 22 (12) |
| Стадия опухоли | ||
| 1 | 15 (7) | 7 (4) |
| 2 | 82 (41) | 82 (45) |
| 3 | 105 (52) | 93 (51) |
| Количественно измеряемое заболевание | ||
| Да | 116 (57) | 100 (54) |
| Нет | 86 (43) | 84 (46) |
| Стадия | ||
| III | 129 (64) | 123 (67) |
| IV | 73 (36) | 61 (33) |
| Асцит ( 100 мл) | ||
| Нет | 29 (14) | 21 (11) |
| Да | 173 (86) | 163 (89) |
| * Объяснения относительно характеристик возможных баллов см. в статье Blessing [14]. | ||
Клиническая ремиссия оценивалась только у больных с клинически измеримым заболеванием в соответствии с ранее определенными критериями [15]. У женщин, которым проводилась повторная лапаротомия, оценку проводил патолог, и заболевание относилось к одной из трех категорий: полная ремиссия, частичная ремиссия с микроскопическим заболеванием и персистирующее заболевание. Женщин, которым не проводилась повторная хирургическая оценка, поскольку у них было персистирующее по клинической симптоматике заболевание, или же прогрессия отмечалась до момента проведения повторной лапаротомии, относились к группе с персистирующим заболеванием.
Таблица 2. Число завершенных курсов и время лечения в зависимости
от группы лечения
| Группа | Цисплатин + циклофосфамид | Цисплатин + паклитаксел | ||
| Число женщин на курс |
Среднее количество дней между курсами | Число женщин на курс |
Среднее количество дней между курсами | |
| 1 | 201 | — | 184 | — |
| 2 | 196 | 21 | 175 | 21 |
| 3 | 187 | 25 | 168 | 21 |
| 4 | 175 | 27 | 166 | 21 |
| 5 | 166 | 28 | 163 | 21 |
| 6 | 158 | 28 | 160 | 21 |
| Средняя (медиана) общая доза составляла 442 мг/м2 цисплатина и 417,6 мг/м2 циклофосфамида. Средняя (медиана) общая доза составляла 441 мг/м2 цисплатина и 751 мг/м2 паклитаксела. Одна женщина лечению не подвергалась. |
||||
Общий срок выживания и выживание в отсутствие прогрессии заболевания определялось начиная с даты рандомизаций. Продолжительность выживания определялась вплоть до даты смерти или до даты последнего контакта с женщиной, если женщина была жива на момент последнего контакта. Продолжительность заболевания в отсутствие прогрессии болезни определялась как минимальный срок до начала клинической прогрессии, летального исхода или до последнего контакта. Все соответствующие критериям больные были включены в анализ выживаемости и выживаемости в отсутствие прогрессии заболевания, если не оговорено по-иному. Все причины смерти были использованы для оценки выживания, а оценки кумулятивной выживаемости были основаны на процедурах по Каплану-Мейеру [16]. Независимость времени выживания в отсутствие симптомов прогрессии болезни, общего выживания и рандомизированного лечения оценивалась с помощью двустороннего логарифмического рангового теста [17] при стратификации в соответствии с критерием возможности количественного измерения заболевания. Линейный анализ пропорционального риска использовался для получения оценок по относительному риску с корректировкой на другие факторы, предшествовавшие лечению [18]. Наконец, анализ пропорционального риска с членом взаимодействия использовался для оценки однородности результатов лечения для различных прогностических групп.
Только отвечающие всем критериям женщины, получившие по крайней мере один курс лечения, были включены в группу по оценке токсичности. Одна женщина лечения не получала. Ранговый тест Крускаль-Валлис [19], скорректированный на связанные ранговые переменные, использовался для тестирования предположения о независимости степени токсичности по отношению к назначенной схеме лечения. Тест хи-квадрат Пирсона [20] использовался для проверки гипотезы о независимости ремиссии и лечения. В случае 12 женщин, по шесть в каждой группе лечения, оценка могла быть проведена лишь частично и они были отнесены к группе, в которой клинических ремиссий не наблюдалось для анализа в отношении "всех исходных" больных. Обычно этим женщинам проводили один или два курса лечения, у них отмечались токсические эффекты и в дальнейшем они получали альтернативную форму лечения или отказывались от какого-либо дальнейшего лечения еще до наступления какой-либо объективной ремиссии.
Таблица 3. Побочные эффекты в зависимости от тяжести и группы
лечения
| Побочный эффект | Цисплатин + циклофосфамид | Цисплатин + паклитаксел | ||||||||||
| Степень тяжести | Число женщин |
Степень тяжести | Число женщин |
|||||||||
| 0 | 1 | 2 | 3 | 4 | 0 | 1 | 2 | 3 | 4 | |||
| процент | процент | |||||||||||
| Уменьшение клеток белой крови или нейтрофилов | 3 | 4 | 9 | 22 | 61 | 197 | 2 | 2 | 4 | 14 | 78 | 179 |
| Снижение тромбоцитов | 60 | 39 | 7 | 1 | 2 | 198 | 47 | 45 | 4 | 3 | 0 | 180 |
| Анемия | 38 | 17 | 36 | 8 | 0 | 200 | 33 | 15 | 43 | 8 | <1 | 182 |
| Симптомы со стороны ЖКТ | 29 | 18 | 42 | 6 | 3 | 201 | 28 | 14 | 42 | 12 | 3 | 184 |
| Лихорадка | 88 | 3 | 8 | 0 | 0 | 201 | 80 | 5 | 11 | 3 | <1 | 184 |
| Алопеция | 63 | 10 | 27 | — | — | 201 | 37 | 9 | 54 | — | — | 184 |
| Симптомы со стороны почек | 93 | 3 | 2 | 1 | <1 | 201 | 96 | 2 | 1 | <1 | 0 | 184 |
| Неврологические симптомы | 79 | 13 | 3 | 3 | 1 | 201 | 72 | 15 | 9 | 4 | 0 | 184 |
| Аллергия | 99 | 0 | 1 | 0 | 0 | 201 | 92 | 2 | 2 | 2 | 2 | 184 |
| Результаты повторных определений лейкоцитов или гранулоцитов отсутствовали для десяти женщин. Результаты повторных определений тромбоцитов отсутствовали для семи женщин. Результаты повторных определений гемоглобина или гематокрита отсутствовали для трех женщин. В связи с округлением не во всех случаях сумма процентов раняется 100. Ранговый тест Круссаль-Валлиса показывает, что этот эффект был более тяжелым в группе, получавшей цисплатин+ паклитаксел (Р=0,05). |
||||||||||||
РЕЗУЛЬТАТЫ
Характеристики больных
В исследование вошло 410 женщин, страдавших эпителиальной формой рака яичника. Двадцать четыре женщины не отвечали критериям участия, в трех случаях, поскольку их опухоль находилась не на нужной стадии, в 13 случаях, поскольку первичная опухоль не соответствовала критериям, в трех случаях, поскольку клеточный тип опухоли не соответствовал требуемому, в четырех случаях, поскольку у них наблюдались опухолевые заболевания в истории болезни, и в одном случае, поскольку больной была проведена неправильная хирургическая операция. Остальные 386 женщин, удовлетворяющих критериям участия в испытании, статистически случайным образом назначались в группу цисплатин-циклофосфамид или в группу цисплатин-паклитаксел. Две группы были сбалансированы в отношении ряда прогностических факторов (Таблица 1).
Доставленная доза и переносимость препарата
Запланированная общая доза цисплатина была одинаковой (450 мг на квадратный метр) для обеих групп лечения. 25-й, 50-й и 75-й процентили фактически введенной дозы цисплатина составляли 410, 442 и 450 мг/м2, соответственно, для женщин в группе цисплатин-циклофосфамид и 425, 441 и 449 мг/м2, соответственно, для женщин в группе цисплатин-паклитаксел. В отношении общей введенной дозы цисплатина различий между группами не наблюдалось.
В Таблице 2 показано число женщин, которые проходили лечение на каждой стадии лечения и указаны промежутки времени между последовательными циклами. Большее количество женщин завершило схему на основе паклитаксела (160 из 184 [87 процентов]) по сравнению со стандартной схемой цисплатин-циклофосфамид (158 из 202 [78 процентов]). Двадцать три женщины (11 процентов) в группе, получавшей стандартную схему лечения, и 9 женщин (5 процентов) в группе паклитаксела не завершило полного числа (шести) курсов химиотерапии в связи с прогрессией заболевания или летальным исходом. У 21 женщины в группе, получавшей стандартную схему лечения (10 процентов), и у 15 женщин (8 процентов) в группе паклитаксела не удалось завершить шесть курсов лечения в результате токсических эффектов или в результате того, что они отказались от продолжения лечения.
Токсичность
Частота побочных эффектов для 385 женщин, удовлетворяющих критериям испытания и получивших по крайней мере один курс лечения, представлена в Таблице 3. Тяжесть нейтропении, фебрильной нейтропении,алопеции и периферической нейротоксчности заметно различалась для двух групп лечения (Р< 0,05), причем большее количество токсических эффектов наблюдалось в группе, получавшей цисплатин-паклитаксел. Хотя нейтропения степени 3 или 4 развилась у большинства женщин в группе цисплатин-паклитаксел, частота фебрильной нейтропении была низкой и это соответствовало наблюдению о небольшой продолжительности миелосупрессии, индуцированной паклитакселом. Периферическая нейротоксичность была более частой в группе паклитаксела, однако в целом имела очень легкий характер. У 10 женщин летальный исход по крайней мере отчасти был обусловлен лечением: у шести женщин в группе цисплатин-циклофосфамид и у четырех в группе цисплатин-паклитаксел. Поскольку у больных, получавших лечение паклитакселом, сообщалось о брадиаритмиях с атриовентрикулярной блокадой и возбуждением желудочка [21], на исходных стадиях настоящего испытания требовалось, чтобы все женщины, входившие в состав группы цисплатин-паклитаксел, проходили кардиомониторинг. Однако только у семи женщин в группе паклитаксела наблюдались кардиологические симптомы второй степени или более тяжелые, такие как блокада сердца первой степени или ишемические эпизоды без других симптомов и без инфаркта. Поэтому требование о мониторинге сердечной деятельности было снято незадолго до конца исследования.
Таблица 4. Клинические ремиссии в зависимости от группы лечения
| Клиническая ремиссия | Цисплатин + циклофосфамид (N=116) | Цисплатин + паклитаксел (N=100) |
| Число (процент)' | ||
| Полные | 36 (31) | 51 (51) |
| Частичные | 34 (29) | 22 (22) |
| Отсутствует | 46 (40) | 27 (27) |
| 'Цифры показывают число больных и процент женщин с заболеванием, поддающимся клиническому измерению. | ||
Таблица 5. Результаты повторной лапаротомии в зависимости
от группы лечения
Результат повторной оценки |
Цисплатин + циклофосфамид (N=116) | Цисплатин+ паклитаксел (N=100)' |
| Отрицательный | 35 (20) | 42 (28) |
| Микроскопически положительный | 7 (4) | 23 (14) |
| Персистирующее заболевание | 136 (76) | 95 (59) |
| Процедура противопоказана или отказ от процедуры | 24 | 24 |
| Всего: | 202 | 184 |
| Значения в скобках относятся к проценту оцененного числа больных. Проценты не включают 24 женщин в этой группе лечения, которые отказались от повторной операции. В связи с округлением сумма процентов не во всех случаях равняется 100. Эта категория включает клинически персистирующее и крупномасштабное по клиническим критериям заболевание. |
||
Ремиссии оценивались у 216 женщин, которые вошли в испытание с заболеванием, поддающимся клиническому измерению (Таблица 4). Общий процент ремиссий в группе, получавшей цисплатин и циклофосфамид, составлял 60 процентов, а в группе, получавшей цисплатин и паклитаксел, 73 процента. Полные клинические ремиссии отмечались чаще среди женщин, получавших лечение комбинацией цисплатина и паклитаксела (51 процент) по сравнению с теми, которые получали лечение цисплатином и циклофосфамидом (31 процент) (Р= 0,01, хи-квадрат).
Женщины с полными клиническими ремиссиями или те, у которых в начале испытания заболевание не было клинически характеризуемым количественно и у которых не отмечалось его прогрессии, должны были в соответствии с протоколом пройти лапаротомию для повторной оценки. Из 386 женщин 48 (по 24 в каждой группе) не прошли эту процедуру в связи с нежеланием или противопоказаниями (Таблица 5). Для двух групп лечения не отмечалось значительных различий в относительном количестве лапаротомии, давших отрицательный ответ (20 и 26 процентов, соответственно).
На Рисунке 1 и Рисунке 2 приведены кривые, иллюстрирующие выживание в отсутствие прогрессирования болезни и общее выживание для всех женщин, удовлетворяющих критериям. Средняя продолжительность (медиана) наблюдения за женщинами на момент последнего контакта составляла 37 месяцев (интервал от 5до 56). Для обоих определенных выше сравнений наблюдалось статистически достоверное различие между группами лечения. Средняя продолжительность выживания (медиана) в отсутствие симптомов прогрессирования болезни в группе, получавшей цисплатин-циклофосфамид, составляла 13 месяцев (95% доверительный интервал, от 11 до 15); в группе, получавшей цисплатин-паклитаксел, эта цифра составляла 18 месяцев (95% доверительный интервал, от 16 до 21 месяца) (относительный риск 0,7; 95% доверительный интервал, от 0,5 до 0,8; Р< 0,001). Среднее общее выживание женщин, получавших комбинацию цисплатина и циклофосфамида, составляло 24 месяца (95 % доверительный интервал, от 21 до 30), а для женщин, получавших комбинацию цисплатина и паклитаксела, 38 месяцев (95% доверительный интервал, от 32 до 44) (относительный риск, 0,6; 95% доверительный интервал, от 0,5 до 0,8; Р< 0,001). Включение тех 24 женщин, которые были сочтены не удовлетворяющими критериям настоящего испытания, существенно не повлияло на эти результаты.
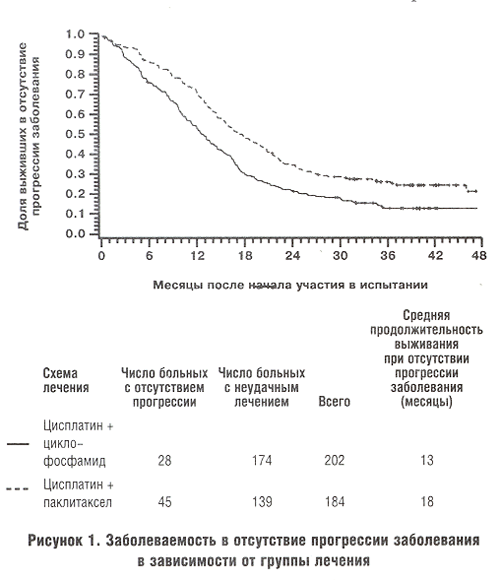
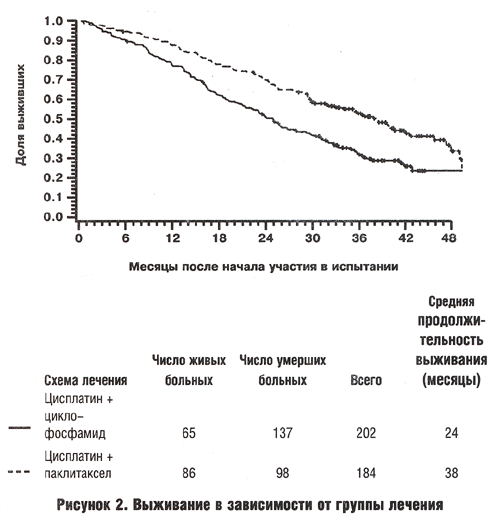
Была проведена также оценка (данные не приводятся) общей выживаемости женщин с клинически поддающимся количественной оценке заболеванием и при отсутствии возможности такой оценки для каждой группы лечения, а также оценка общей выживаемости в целом в зависимости от стадии заболевания. Не было получено указаний на то, что комбинация цисплатина и паклитаксела была менее эффективна по сравнению с цисплатином и циклофосфамидом в этих прогностических подгруппах.
Предыдущие исследования, проведенные группой GOG на женщинах с не полностью удаленной опухолью на стадиях III и IV позволяют предположить, что больные с муцинозными или светлоклеточными аденокарциномами имели тенденцию к плохому прогнозу [22]. Исключение таких больных из сравнения по выживаемости в отсутствие прогрессии заболевания и из сравнения по общей выживаемости не изменяло результаты.
ОБСУЖДЕНИЕ
Результаты настоящего испытания представляют убедительные данные, что использованная нами схема цисплатин-паклитаксел является более эффективной по сравнению со схемой на основе цисплатина и циклофосфамида для лечения женщин с распространенной формой рака яичника. Для двух групп лечения наблюдалась хорошая сбалансированность известных прогностических факторов, и различия выживаемости, выживаемости в отсутствие признаков прогрессии заболевания и процента полных ремиссий нельзя было объяснить ошибкой случайных выборок. Полученные нами результаты сходны с результатами, полученными в работе, являвшейся предшественником настоящего испытания, т.е. в исследовании, когда аналогичная выборка женщин подвергалась лечению аналогичными дозами цисплатина и паклитаксела [23]. Представляется, что относительные преимущества паклитаксела в нашем испытании не были обусловлены более плохим по сравнению с ожидаемым результатом среди женщин, получавших стандартное лечение. Также нет указаний на то, что преимущество цисплатина и паклитаксела ограничивается женщинами, заболевание у которых поддается количественному измерению или женщинами, у которых опухоль находится на стадии III. В клинических условиях токсичность препаратов не выходила за приемлемые рамки.
Когда активный новый препарат идет на клиническое применение, его влияние на выживание может казаться заниженным в связи с переводом больных со старого стандарта лечения на лечение новым препаратом. Может наблюдаться аналогичное, однако менее выраженное воздействие на выживаемость в отсутствие симптомов прогрессии заболевания, когда перевод осуществляется до появления признаков клинической прогрессии, например после положительных результатов повторной лапаротомии. Такая ситуация отмечалась, когда цисплатин, уже выпущенный в практику, был включен в схемы первичного лечения опухолей [3]. Это может объяснить, почему воздействие на выживание не было более выраженным, когда цисплатин был впервые включен в схемы первичного лечения опухолей. Эффект перекреста возможно затронул и наше испытание, однако в меньшей степени, чем обычно, поскольку паклитаксел имелся в ограниченном количестве во время ранней фазы накопления больных в исследовании, и женщины в группе цисплатин-циклофосфамид часто не могли получать паклитаксел до тех пор, пока им не была проведена терапия третьей или четвертой линии.
Результаты этого испытания носят обнадеживающий характер, однако мы озабочены тем обстоятельством, что варианты схемы цисплатин-паклитаксел в настоящее время принимаются без надлежащей оценки. Некоторые клиницисты заменили цисплатин на карбоплатин даже несмотря на то обстоятельство, что комбинация карбоплатин-паклитаксел находится в испытаниях по Фазе 1 [24].
Еще более серьезную озабоченность у нас вызывает сокращение сроков вливания паклитаксела до 3 часов или менее. Эта практика основана главным образом на испытании паклитаксела, применяемого индивидуально в качестве средства лечения второй или третьей линии, когда была продемонстрирована аналогичная эффективность для трехчасового и 24-часового вливания и меньшая гематологическая токсичность при более коротких сроках вливания [25]. Такой подход может предпочитаться больными, может иметь финансовые преимущества, однако эффективность трехчасового вливания паклитаксела не была верифицирована. Наша озабоченность в связи с этим имеет свои основания, поскольку данные, полученные in vitro, показывают, что продолжительность экспозиции паклитакселу является гораздо более важным фактором, чем максимальная концентрация, при которой проводится экспозиция [26].
Приложение
В настоящем исследовании участвовали следующие учреждения Группы по гинекологической онкологии: Центр медицинских наук штата Орегон, Онкологический центр Джонса Хопкинса, Университет штата Алабама в Бирмингаме, Медицинский центр Университета Дюк, Фонд медицинской помощи штата Колорадо, Медицинская школа БоуманГрэй Университета УэйкФорест, больница Центра медицинских наук Университета Темпл, Медицинская школа Университета штата Миннесота, Медицинский центр Университета штата Миссиссиппи, Медицинский центр Калифорнийского Университета в г. Ирвайн, Армейский медицинский центр УолтерРид, Больницы и клиники Университета штата Айова, Университет штата Кентукки, Больница штата Пеннсильвания, Школа медицины Вашингтонского Университета, Университетский Медицинский центр Купер, Фонд клиник Кливленд, Онкологический центр МД. Андерсон, Университет штата Техас, Университетская больница Джорджтаун, Медицинский центр Рочестерского Университета, Медицинский центр Университета Южной Калифорнии в Лос-Анжелесе, Медицинский центр Тафтс-Нью Ингланд, Онкологический совет Коламбус, Медицинский колледж Университета в Цинцинатти, Медицинский колледж Университета Юнион, Онкологический центр штата Иллинойс, Университетская школа медицины Уэйн, школа медицина МилтонХерши Университета штата Пеннсильвания, Медицинский центр в Лос-Анджелесе Калифорнийского Университета, Медицинская школа Университета Южной Каролины, Медицинский центр Университета штата Массачусетс, Медицинский Университет Южной Каролины, Женский онкологический центр Северной Калифорнии, Центр медицинских наук Университета штата Оклахома, Онкологический центр ФокеЧейз, школа медицины Университета Майами, Центр медицинских наук Техасского Университета в Далласе, Медицинский центр Нью-Йоркского Университета Даунстейт, Медицинская школа Восточной Вирджинии и Университет штата Нью-Йорк в Стони-Брук.
Литература
1. Williams CJ, Macbeth FR, et al. Cisplatin combination chеmotherapy versus chlorambucil in advanced ovarian carcinoma: mature results of a randomized trial. J Clin Oncol 1985; 3:455-462.
2. Neijt JP, ten Bokkel Huinnik WW, van der Burg ME, et al. Randomized trial comparing two combination chemotherapy regimens (Hexa-CAP vs. CHAP-S) in advanced ovarian carcinoma. Lancet 1984; 2:594-600.
3. Ornura GA, Blessing JA, Ehrlich CE, et al. A randomized trial of cyclophosphamide and doxorubicin with or without cisplatin in advanced ovarian carcinoma: a Gynecologic Oncology Group Study. Cancer 1986; 57: 1725-1730.
4. Advanced Ovarian Cancer Trialists Group. Chemotherapy in advanced ovarian cancer: an overview of randomized clinical trials. BMJ 1991; 303: 884-893.
5. Thigpen JT, Blessing JA, Vance RB, Lambuth BW. Chemotherapy in ovarian carcinoma: present role and future prospects. Semin Oncol 1989; 16: 58-65.
6. GICOG (Gruppo Interregionale Cooperativo Oncologico Gynecologica). Long-term results of a randomized trial comparing cisplatin with cisplatin and cyclophosphamide with cisplatin, cyclophosphamide, and adriamycin in advanced ovarian cancer. Gynecol Oncol 1992; 45: 115-117.
7. Williams CJ, Stewart L, Parmar M, Guthrie D.Meta-analysis of the role of platinum compounds in advanced ovarian carcinoma: the Advanced Ovarian Cancer Trialists Group. Semin Oncol 1992; 19: Suppl 2: 120-128.
8. Sutton GP, Stehman FB, Einhorn HL, Roth LM, Blessing JA, Ehrlich CE. Ten-year follow-up of patients receiving cisplatin, doxorubicin, and cyclophosphamide chemotherapy for advanced epithelial ovarian carcinoma. J Clin Oncol 1989; 7: 223-229.
9. McGuire WP, Rowinsky EK, Rosenshein NB, et al. Taxol: a unique antineoplastic agent with significant activity in advanced ovarian epithelial neoplasms. Ann Intern Med 1989; III: 273-279.
10. Thigpen JT, Blessing JA, Ball H, Hummel SJ, Barret RJ. Phase II trial of paclitaxel in patients with progressive ovarian carcinoma after platinum-based chemotherapy: a Gynecologic Oncology Group study. J Clin Oncol 1994; 12: 1748-1753.
II. Rowinsky EK, Gilbert MR, McGuire WP, et al. Sequences of taxol and cisplatin: a phase I and pharmacologic study. J Clin Oncol 1991; 9:1691-1703.
12. McGuire WP. Taxol: a new drug with significant activity as a salvage therapy in advanced epithelial ovarian carcinoma. Gynecol Oncol 1993; 51: 78-85.
13. Rowinsky ER, Donehower RC. Paclitaxel (Taxol). N Eng J Med 1995; 332:1004-1014.
14. Blessing EA. Design, analysis and interpretation of chemotherapy trials in gynecologic cancer. In: DeppeG, ed. Chemotherapy of gynecologic cancer, 2nd ed. New York: Wiley-Liss, 1990:63-97.
15. WHO handbook for reporting results of cancer treatment. Geneva: World Health Organization, 1979.
16. Kaplan EL, Meier P. Nonparametric estimation from incomplete observations. J AM Stat Assoc 1958; 53:457-481.
17. Mantel N. Evaluation of survival data and two new rank order statistics arising in its consideration. Cancer Chemother Rep 1966; 50:163-170.
18. Сох DR. Regression models and life-tables. J R Stat Soc[B] 1972; 34:187-220.
19. Kniskal WH,Wallis WA Use of ranks in one-criterion variance analysis. J Am Stat Assoc 1952; 47: 583-621.
20. Agresi A. Categorical data analysis. New York: John Wiley, 1990.
21. Rowinsky EK, McGuire P, Guarnieri T, Fisherman JS, Christian MC, Donehower RC. Cardiac disturbances during the administration of taxol. J Clin Oncol 1991; 9: 1704-1712.
22. Ornura GA, Brady ME, Homesley HD, et al. Long-term follow-up and prognostic factor analysis in advanced ovarian carcinoma: the Gynecologic Oncology Group experience. J Clin Oncol 1991; 9:1138-1150.
23. McGuire WP, Hoskins WJ, Brady MF, et al. An assessment of dose-intensive therapy in suboptimally debulked ovarian cancer: A gynecologic Oncology Group study. J Clin Oncol 1995; 13: 1589-1599.
24. Bookman MA, McGuire WP, Kilpatrick E, et al. Phase I Gynecologic Oncology Group (GOG) study of 3-h and 24-h paclitaxel with carboplatin as initial therapy for advanced epithelial ovarian cancer (OvCA). J Clin Oncol (in press).
25. Eisenhauer EA, ten Bokkel Huinnik WW, Swenerton KD, et al. European-Canadian randomized trial of paclitaxel in relapsed ovarian cancer: high-dose versus low-dose and long versus short infusion. J Clin Oncol 1994; 12: 2654-2666.
26. Liebermann JE, Cook JA, Lipschultz C, Teague D, Fisher J, Mitchell JB.Cytotoxic studies of paclitaxel (Taxol) in human tumour cell lines. Br J Cancer 1993; 68:1104-1109.
Комментарии
ПРАКТИКА ПЕДИАТРА
