Релиз-активные лекарственные препараты — новое направление в лечении острых респираторных вирусных инфекций (обзор литературы)
Статьи Опубликовано в журнале:
« ПРАКТИЧЕСКАЯ МЕДИЦИНА » 7 (83) сентябрь 2014 г. Дмитриев Анатолий Николаевич — доктор медицинских наук, профессор кафедры внутренних болезней и эндокринологии
Уральский государственный медицинский университет, 620102, г. Екатеринбург, ул. Волгоградская, д. 189.
В обзоре литературы представлены теоретические основы и технологические особенности создания релиз-активных форм лекарственных препаратов – нового класса фармакологических средств, разработанных и производимых ООО «НПФ «Материа Медика Холдинг» (Россия) для профилактики и лечения многофакторных заболеваний и острых респираторных вирусных инфекций. В настоящий обзор включена информация об особенностях, преимуществах и привлекательных для современной медицины свойствах препаратов на основе релиз-активных антител, базирующаяся на результатах более 50 доклинических и клинических исследований, опубликованных в русско- и англоязычных источниках. На примере лекарственного препарата Эргоферон, созданного на основе релиз-активных антител к ИФН-гамма, гистамину, CD4, детально рассмотрены особенности механизма действия, результаты экспериментального и клинического изучения эффективности и безопасности в лечении широкого спектра острых респираторных вирусных инфекций, включая грипп.
Ключевые слова: релиз-активность, релиз-активные лекарственные препараты, Эргоферон, острые респираторные вирусные инфекции (ОРВИ), лечение.
Успехи фармакологии последних десятилетий, связанные с использованием высоких технологий (генная терапия, рекомбинантные технологии и др.), повысили результативность лечения ряда заболеваний, однако радикально не решили проблему эффективности и безопасности лекарственных средств. Последнее определяет актуальность поиска принципиально новых подходов и создания на этой основе оригинальных лекарственных препаратов. Одним из таких подходов, активно и всесторонне обсуждающихся в последние годы, является использование малых и сверхмалых доз [1-6] и релиз-активных (от англ. «release» — высвобождение) форм препаратов [7-9].
История изучения фармакотерапевтических эффектов малых доз лекарственных средств насчитывает не одно десятилетие — от Н.П. Кравкова (1924) [10] до А.М. Кузина (1997) [11], однако результаты этих изысканий не оправдали ожиданий не только клиницистов, но и фармакологов. Причиной тому могли быть ограниченные исследовательские возможности прежних лет. В то же время логические посылки и альтернативная гомеопатии идеология инициировали углубление данного направления научных исследований. Их итогом явилось изучение терапевтического действия сверхмалых доз на клеточном уровне [12], а позже — обоснование новой технологии производства и эффективности релиз-активных форм препаратов [7-9]. Неоценимым теоретическим и практическим вкладом авторов в разрабатываемую проблему явилось обоснование и доказательство того, что фармакологической активностью обладают высокоразбавленные растворы лишь тех лекарственных средств, технология производства которых сочетает последовательное многократное разведение исходного раствора лекарственного средства с его внешней обработкой (механическим воздействием, включая ультразвук, электромагнитное поле). Ранее было показано, что их формы, не подвергавшиеся специальной технологической обработке, включая механическое воздействие, фармакологической активностью не обладают [12, 13]. Многократное разведение в сочетании с особой технологической обработкой приводит к появлению (высвобождению) в сверхразведениях исходного вещества специфической активности, названной исследователями релиз-активностью. Наличие релиз-активности у различных эндогенных регуляторов (биологически активных веществ) в сверхвысоких разведениях доказано методами иммуноферментного анализа, двухмерной спектроскопии на фоне ЯМР-исследования [8, 9]. Релиз-активность ассоциирована с исходным веществом, но не зависит от его содержания в сверх-разбавленных растворах и не является его дозой, т.к. понятие «доза» подразумевает часть вещества, воспроизводящего его базовые свойства [8]. В серии исследований установлена зависимость эффектов релиз-активных антител от условий технологической обработки и, прежде всего, степени разведения релиз-активной формы, объема разведений, используемых в эксперименте, а в условиях клинической апробации — от количества таблеток и частоты приема релиз-активного препарата. Таким образом, специфическая дозозависимость релиз-активных препаратов подчеркивает их материальность и дискретность носителя релиз-активности [9].
В целом феномен релиз-активности может быть представлен в следующем резюмирующем виде (рис. 1).
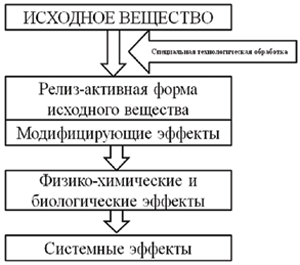
Рисунок 1. Феномен релиз-активности: механизм
Предполагается, что биологические и физико-химические свойства в растворах релиз-активных лекарственных препаратов сохраняются за счет сложных термодинамических процессов, приводящих к специфическим структурным, конформационным изменениям носителя [6, 8, 9]. Крайне важно, что эффекты подвергнутого специальной технологической обработке лекарственного средства в сверхвысоких разведениях качественно идентичны эффектам этого же средства в терапевтических дозах [7], но в редуцированном [2, 14] и/или модифицированном виде [7-9, 15-17]. Технология производства не только сохраняет в сверхразбавленных растворах биологическую активность, но и придает препаратам особые групповые свойства, характеризующиеся модифицирующим феноменом релиз-активных лекарственных препаратов. Благодаря непосредственному воздействию на конформационные характеристики молекул-мишеней, релиз-активные лекарственные формы способны оказывать модифицирующее действие на базовые физико-химические и биологические свойства исходного вещества и структурно близких ему молекул, в том числе посредством модуляции активности соответствующих рецепторов и влияния на лиганд-рецепторные взаимодействия [8, 9].
Не меньшей заслугой разработчиков нового фар-макотерапевтического направления явилось прикладное осмысление единства трех искусственно разделенных регуляторных систем организма: иммунной, эндокринной и нервной, объединенных в организме в одно целое общими регуляторными факторами пептидной и иной природы, общими рецепторными молекулами, сигнальными путями и клеточными элементами [18, 19], и сформулированной И.П. Ашмариным концепции участия ау-тоантител в регуляции физиологических функций организма в качестве молекул, регулирующих постоянство клеточного состава организма [20-22].
Известно, что увеличение уровня аутоантител не всегда сопровождается развитием нарушений функций организма [18, 20, 22, 23]. «Базовая» активность иммунной системы связана не столько с поиском и уничтожением чужеродных микробных факторов, сколько с устранением или блокированием потенциально вредных для гомеостаза факторов, в первую очередь, эндогенной (например, аутоиммунной) природы [23]. Продукция аутоантител различной специфичности регулируется по принципу отрицательной обратной связи содержанием соответствующих антигенов. В результате формируется индивидуальный набор антител (АТ), содержащихся в крови — своеобразный «образ» иммунитета, названный А.Б. Полетаевым «иммункулус» [25, 26].
Благодаря этому иммунная система может осуществлять регуляторные функции в отношении клеточной пролиферации и других генетически детерминированных функций собственных клеток путем создания специфических аутоантител к биологически активным соединениям организма [24, 25]. К настоящему времени получены и охарактеризованы в эксперименте специфические АТ к ядерным и рецепторным антигенам эндокриноцитов и других клеток, способные направленно влиять на их рост и секрецию, изменяя экспрессию определенных генов. Также доказано их проникновение в ядра живых клеток-мишеней in vivo. Предполагается, что биологически активные соединения и их ядерные и мембранные рецепторы (вместе с аутоантителами к ним) входят в единую систему идиотип-антиидиотипических взаимодействий, обеспечивающих пре-цизионно скоординированную реализацию генетических программ в разных клетках организма [27].
В отличие от аутоантител к белковым или иным по природе мембранным и внутриклеточным компонентам клеток, регуляторная роль аутоантител к растворимым биологически активным соединениям менее изучена. Предполагается, что АТ к эндогенным биологически активным соединениям могут как связывать и снижать количество соответствующих биологически активных соединений, так и повышать их количество и выраженность влияний [28, 29]. Феномен усиления выраженности соответствующих регуляторных процессов может быть объяснен компенсаторным повышением синтеза и обмена соответствующих регуляторных факторов (при их изначальном снижении при действии аутоантител), а также сенситизацией соответствующих рецепторов органа-мишени и модификацией лиганд-рецепторного взаимодействия [16].
Таким образом, теоретическим обоснованием нового направления явились доказательства участия АТ в многофакторной регуляции естественных функций [20], транспорте эндогенных регуляторных пептидов к мембранным рецепторам и предохранении их от преждевременного протеолиза [30], «стабилизирующем» действии естественных АТ на ряд известных регулярных молекул [20, 31], низко- и высокомолекулярных веществ, внутриядерных структур и клеточных мембран [32-35]. А также свидетельства специфической модификации сверхвысокими разведениями релиз-активных АТ функциональной активности тех аутоантител, к которым они были получены, т.е. о своеобразной «регуляции регулятора» [36]. Многочисленными исследованиями показано, что релиз-активные формы АТ к эндогенным регуляторам (гормоны, цитокины, мембранные белки и др.) не блокируют активность молекул, к которым они получены, а модулируют и воспроизводят их специфические эффекты [7-9, 17, 32, 36].
Описанные теоретические предпосылки были положены в основу создания нового класса фармако-терапевтических препаратов, производимых ООО «НПФ «Материа Медика Холдинг» (Россия) — аффинно очищенных релиз-активных (РА) АТ к различным биологически активным субстанциям организма.
Релиз-активные препараты предназначены для лечения и профилактики хронических неинфекционных, многофакторных, заболеваний и инфекций, включая острые респираторные вирусные инфекции (ОРВИ). Данный класс препаратов включает как монопрепараты, например, Тенотен, Тенотен детский (РА АТ к мозгоспецифическому белку S-100), Анаферон и Анаферон детский (РА АТ к γ-интерферону (ИФН), Импаза (РА АТ а к эндотели-альной NO-синтазе), Артрофоон (РА АТ к ФНО-α), Афала — (РА АТ к простат-специфическому антигену), Диетресса — (РА АТ к каннабиноидным рецепторам 1 типа), так и комбинированные лекарственные препараты — Эргоферон (РА АТ к ИФН-γ, СD4, гистамину), Колофорт (РА АТ к ФНО-α, мозгоспецифическому белку S-100 и гистамину), Бризантин (РА АТ к мозгоспецифическому белку S-100 и каннабиноидным рецепторам 1 типа), Диваза (РА АТ к мозгоспецифическому белку S-100 и эндотели-альной NO-синтазе).
Найденные в открытом доступе опубликованные данные по экспериментальному и клиническому изучению эффективности и безопасности релиз-активных лекарственных препаратов позволяют сделать вывод — многочисленными рандомизированными клиническими сравнительными и плацебо-контролируемыми исследованиями, выполненными в соответствии с требованиями надлежащей клинической практики (GCP) и принципами доказательной медицины показано, что относительно недавно появившиеся на отечественном фармацевтическом рынке релиз-активные лекарственные препараты обладают не только доказанной терапевтической эффективностью (классы доказательности от А до С), но и очевидными преимуществами и привлекательными для современной практической медицины свойствами. Среди них наиболее значимыми с клинической точки зрения представляются следующие:
1. Отсутствие токсичности, формирования толерантности, привыкания и пристрастия.
2. Высокая эффективность, сравнимая с фармакологическими «эталонными» препаратами (озельта-мивир, интерфероны, диазепам и др.).
3. Удобное пероральное применение.
4. Оптимальное соотношение высокой терапевтической эффективности с безопасностью применения в клинической практике.
5. Хорошие фармакоэкономические показатели.
6. Возможность длительного применения с профилактической целью и для лечения хронических заболеваний.
7. Возможность безопасного применения у пациентов с сопутствующими заболеваниями как для монотерапии, так и в комплексном лечении.
8. Возможность безопасного применения в педиатрической практике.
Наглядной иллюстрацией описанных преимуществ могут служить, например, результаты ряда отечественных и зарубежных экспериментальных и клинических исследований, доказывающих противовирусную полипотентность, эффективность и безопасность терапии препаратом Эргоферон.
Эргоферон — новый комбинированный препарат, содержащий релиз-активные аффинно очищенные АТ к ИФН-γ человека (РА АТ к ИФН-γ), гистамину (РА АТ к гистамину) и CD4 (РА АТ к CD4), которые наносятся на лактозу в виде смеси трех активных водно-спиртовых разведений субстанции, разведенной соответственно в 10012, 10030, 10050 раз. Фармакологической мишенью Эргоферона являются реакции лиганд-рецепторного взаимодействия ИФН-γ, СD4 и гистамина с их рецепторами на клетках-эффекторах [9]. Эффективность Эргоферона в отношении широкого спектра острых респираторных вирусных инфекций, включая грипп, достигается благодаря сочетанию противовирусного, противовоспалительного и антигистаминного действий [37-40].
Компоненты, входящие в препарат — релиз-активные антитела к важнейшим факторам иммунитета — ИФН-γ и СD4 — и медиатору воспаления гистамину, обладают единым механизмом действия — нормализуют функциональную активность и связывание эндогенных молекул (ИФН-γ, CD4 и гистамина) с рецепторами, а также функциональную активность клеток-продуцентов этих молекул [37].
Экспериментальные исследования эффективности и безопасности препарата и его компонентов проводились в таких ведущих научных центрах, как Институт иммунологии, НИИ гриппа, Центр по интерферону и цитокинам НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи, НИИ фармакологии ТНЦ СО РАМН, а также в целом ряде исследовательских центров в нашей стране и за рубежом — специализированных биотехнологических центрах и научно-исследовательских лабораториях США, Франции, Бельгии, Нидерландов, Великобритании [8, 9, 38-40].
Иммунологические исследования доказали, что РА АТ к ИФН-γ оказывают влияние на выработку ИФН-γ, ИФН-α/β, а также сопряженных с ними интерлейкинов (ИЛ-2, ИЛ-4, ИЛ-10 и др.), улучшают лиганд-рецепторное взаимодействие ИФН [37, 41]. Результатом является увеличение на 50% количества ИФН, связавшегося с рецепторами на клетках– мишенях и увеличение скорости и силы действия ИФН в организме, что обусловливает эффективную противовирусную защиту и снижает выраженность воспаления [8]. Также РА АТ к ИФН-γ способствуют активации фагоцитоза и NK-клеток, восстановлению баланса Th1/Th2 активностей иммунного ответа и В-лимфоцитов с повышением продукции защитных антител — IgG и IgA, в том числе секреторного sIgА, который усиливает местный иммунитет; способствуют торможению выработки аллергических антител — IgЕ [8, 37, 42, 43].
Вирусологические исследования РА АТ к ИФН-γ показали, что они обладают активностью в отношении широкого спектра вирусов, подавляют размножение всех видов вирусов гриппа (в том числе «свиного» А/Н1N1). А также высоко активны в отношении различных возбудителей ОРВИ (аденовирусов, риновирусов, респираторно-синцитиального вируса, вируса парагриппа и др.), в том числе вирусов, поражающих и желудочно-кишечный тракт (коронавирусы, калицивирусы, ротавирусы и др.), обладают противогерпетической активностью (вирусы простого герпеса I и II типа, ветряной оспы, опоясывающего герпеса, вирус Эпштейна — Барр) [37]. Показано, что применение РА АТ к ИФН-γ у зараженных LD50 вируса гриппа А(Н1N1)2009 лабораторных животных приводило к подавлению репликации вируса в легочной ткани (снижению титра вируса гриппа), увеличению продолжительности жизни и снижению летальности.
Противовирусная активность РА АТ к ИФН-γ в отношении пандемического вируса гриппа А(H1N1)2009 была сопоставима с Озельтамивиром. Экспериментальные исследования на модели гриппа А (А/H3N8 и 2 штамма A/H1N1), проведенные в компании APcis S. A. (Франция) в сотрудничестве с Институтом Пастера (Франция), также показали противовирусную эффективность РА АТ к ИФН-γ, сопоставимую с эффективностью Озельтамивира [44, 45].
Второй компонент Эргоферона — РА АТ к CD4, который регулирует активность CD4-рецептора, представленного на Т-хелперах, моноцитах, макрофагах, дендритных клетках, играющих ключевую роль в противовирусном иммунном ответе. В эксперименте показано, что модулирующее влияние РА АТ к CD4 на CD4-клетки системы иммунитета сопровождается повышением их функциональной активности, нормализацией соотношения CD4/CD8 и субпопуляционного состава (СD3, CD4, CD8, CD16, CD20), усилением противовирусной эффективности РА АТ к ИФН-γ, как компонента Эргоферона, формированием адекватного противовирусного ответа [37]. Известно, что различные факторы могут оказывать негативное воздействие на презентацию вирусного антигена CD4-клетками, что в итоге, снижает эффективность противовирусного ответа. Модулирующее влияние РА АТ к CD4 на функциональную активность CD4-клеток, обеспечивая «полноценную» презентацию антигена, эффективно противодействует вирулентной гриппозной инфекции, начиная с самых ранних этапов ее развития. Кроме того, повышая функциональную активность CD4+ Т-лимфоцитов, РА АТ к CD4 препятствуют репликации вируса и способствуют высокой скорости его клиренса [43].
Таким образом, совместное применение двух компонентов Эргоферона (РА АТ к ИФН-γ + РА АТ к CD4) и их воздействие на систему интерферонов в сочетании с активацией процессов распознавания вирусов системой CD4 клеток обеспечивает синергию в реализации противовирусных эффектов — приводит к подавлению репликации вируса и формированию адекватного противовирусного ответа, что практически реализуется в быстром купировании лихорадки — основного клинического маркера виремии при гриппе, а также других клинических симптомов. Также в ходе клинических исследований были подтверждены и описанные иммунотропные свойства Эргоферона [46].
Противовирусная и противовоспалительная эффективность РА АТ к ИФН-γ и РА АТ к CD4 дополняется влиянием третьего компонента Эргоферона — РА АТ к гистамину — на гистамин-опосредованные механизмы инфекционного воспаления (Н1, Н2, Н4 опосредованные эффекты гистамина), что проявляется в активном разрешении респираторных симптомов вирусной инфекции. Так, например, в 2014 году при исследовании влияния Эргоферона на гистамин-индуцированное сокращение ткани легкого в компании Eurofns Panlabs, Inc (США) было показано, что Эргоферон регулирует гистамин-зависимую активность H1-рецепторов [39]. Клинически данное действие проявляется сокращением длительности и выраженности воспалительных изменений слизистых оболочек респираторного тракта, ринореи, заложенности носа, кашля и чихания. В серии экспериментальных исследований также доказано, что РА АТ к гистамину влияют на инфекционно-воспалительный процесс в респираторном тракте, оказывая противоаллергическое, противовоспалительное, спазмолитическое и противокашлевое действие. РА АТ к гистамину способствуют уменьшению сосудистой проницаемости, подавляют высвобождение гистамина из тучных клеток и базофилов, продукцию лейкотриенов, синтез молекул адгезии, снижают хемотаксис эозинофилов и агрегацию тромбоцитов [39].
Особый интерес среди многочисленных и разносторонних экспериментальных исследований Эрго-ферона представляет изучение его противовирусной активности при респираторно-синцитиальной вирусной (РСВ) инфекции. Известно, что РСВ вызывает тяжелые поражения нижних дыхательных путей в детском, особенно младенческом, возрасте. Однако результаты исследований последних лет позволили изменить взгляд на PCВ-инфекцию как сравнительно безопасную для взрослого населения.
В опубликованных результатах исследований, проведенных за рубежом, в частности McClure D.L. et al., 2014; Seo Y.B. et al., 2014, оказалось, что РСВ-инфекция может быть причиной развития тяжелой пневмонии, поражения ЦНС и различных патологических состояний и у взрослых, в т.ч. и при внутрибольничном инфицировании. У пожилых и старых пациентов РСВ-инфекция не только тяжело протекает, но и сопровождается значительной летальностью.
Противовирусная эффективность Эргоферона оценивалась в лабораторных условиях на экспериментальной модели инфицирования клеток линии HeLa РСВ in vitro. Результаты проведенного исследования показали протективное действие Эргоферона на клетки in vitro при инфицировании их различными инфекционными дозами РСВ. В исследовании продемонстрировано, что Эргоферон ингибирует репликацию РСВ, статистически значимо снижая вирусную нагрузку на клетки линии HeLa [47]. Полученные экспериментальные данные нашли подтверждение и в ходе клинических исследований, например, при исследовании такого компонента Эргоферона, как РА АТ к ИФН-γ [48].
Экспериментально доказанная эффективность Эргоферона и его компонентов при гриппе и ОРВИ, а также безопасность нового противовирусного препарата были продемонстрированы в ходе ряда клинических исследований, выполненных в соответствии с принципами доказательной медицины [49-51]. Так, например, в 2011–2012 гг. проведено многоцентровое сравнительное рандомизированное клиническое исследование эффективности Эргофе-рона и Озельтамивира в лечении гриппа. В данном исследовании показано, что клиническая эффективность Эргоферона, который купировал основные респираторные и интоксикационные симптомы гриппа на третьи сутки лечения, сопоставима с эффективностью Озельтамивира в лечении гриппа [49]. Опубликованы и результаты сравнительного изучения эффективности Эргоферона и Умифеновира при ОРВИ, продемонстрировавшие сопоставимость действия Эргоферона с препаратом сравнения [52]. Высокая эффективность и безопасность Эргоферона была показана и в клиническом исследовании у больных аллергологического профиля, находящихся в стационаре по поводу обострения хронических заболеваний легких на фоне ОРВИ [53], в комплексной терапии внебольничных пневмоний [54]. Изучена клиническая эффективность и безопасность Эргоферона при ОРВИ и у пожилых пациентов [55].
Наиболее интересными представляются результаты многоцентрового двойного слепого плацебо-кон-тролируемого, рандомизированного клинического исследования, которое проводили в параллельных группах у взрослых пациентов в 8 медицинских центрах РФ — Федеральном научно-клиническом центре специализированных видов медицинской помощи и медицинских технологий ФМБА, Воронежской ГМА им. Н.Н. Бурденко, РНИМУ им. Н.И. Пирогова, поликлинике № 3 УД Президента РФ, Смоленской ГМА, НИИ вакцин и сывороток им. И.И. Мечникова РАМН, Ярославской ГМА, Московском НИИ эпидемиологии и микробиологии им. Г.Н. Габричевского [43].
Следует отметить, что исследования с подобным дизайном являются «золотым стандартом» доказательной медицины. Результаты данного исследования свидетельствуют о том, что прием Эргоферона достоверно быстрее приводил к нормализации повышенной температуры тела по сравнению с приемом плацебо. Эффект лечения Эргофероном проявлялся с первых суток приема препарата, а к исходу трех суток лечения подавляющее большинство пациентов с ОРВИ имели нормальную температуру тела. В течение пяти дней использования Эргоферона пациенты реже применяли жаропонижающие препараты с целью облегчения выраженности симптомов ОРВИ, начиная с первого дня лечения.
Кроме того, эффективность терапии Эргофероном проявлялась купированием основных катаральных и общеинтоксикационных проявлений ОРВИ в более короткие сроки у большего процента пациентов, чем в группе плацебо. Отчетливый клинический эффект препарата отмечен в отношении астенических проявлений (слабость, недомогание, сонливость) и симптомов со стороны верхних дыхательных путей (заложенность и выделения из носа, чихание).
Эффекты терапии Эргофероном обусловлены вышеописанным противовирусным и иммунотропным влиянием препарата, а также воздействием на гистамин-опосредованный компонент воспалительного процесса дыхательных путей у пациентов с ОРВИ.
Лечение Эргофероном предупреждало развитие бактериальных осложнений, требующих применения антибиотиков. В группе Эргоферона не было зарегистрировано нежелательных явлений, связанных с исследуемой терапией; препарат не оказывал отрицательного влияния на показатели общего и биохимического анализов крови и клинического анализа мочи; не было получено данных о взаимодействии Эргоферона с другими препаратами, принимавшимися пациентами в ходе исследования в качестве сопутствующей терапии.
Опубликованные результаты исследований Эргоферона, выполненных в соответствии с требованиями и принципами доказательной медицины, свидетельствуют о детально исследованной эффективности и безопасности как Эргоферона, так и его компонентов. И позволяют сделать вывод, что данное лекарственное средство отличается высоким профилем безопасности и позволяет решить актуальные вопросы современной практической медицины в области терапии и профилактики ОРВИ, поскольку трехкомпонентный состав Эргоферона воздействует на различные механизмы инфекционно-воспалительного процесса и способствует формированию адекватного противовирусного ответа широкого спектра без риска развития резистентности. Применение Эргоферона проявляется комплексом терапевтических эффектов для лечения ОРВИ: противовирусным, противовоспалительным и антигистаминным, что позволяет обеспечить усиленное противовирусное действие для более полного подавления репликации и удаления вирусов из организма и осуществлять лечение в полном объеме на всех этапах заболевания, т.е. независимо от времени обращения пациента.
Таким образом, краткий обзор литературы свидетельствует о том, что открытый в последние годы феномен релиз-активности является принципиально новым шагом на пути развития фармакологии, обеспечивающим широкие возможности по разработке и созданию целого ряда новых лекарств.
Очевидно, что использование АТ в релиз-активной форме в терапевтической практике является не только новым, но и перспективным направлением. Помимо доказанной в многочисленных экспериментальных и клинических исследованиях эффективности и безопасности релиз-активных лекарственных средств, данный класс препаратов имеет неоспоримые преимущества, также играющие важную роль при выборе препарата в повседневной, рутинной практической деятельности.
Во-первых, использование в качестве лекарственного средства релиз-активных антител к известным антигенам с хорошо изученной активностью в значительной мере облегчает процесс фармакологического скрининга. Во-вторых, исследования показали, что АТ в релиз-активной форме не вызывают привыкания и пристрастия, а побочные действия ограничиваются лишь возможными реакциями повышенной индивидуальной чувствительности к компонентам препарата. В-третьих, релиз-активные антитела к эндогенным биологически активным веществам оказывают щадящее, модифицирующее действие, что позволяет осуществлять тонкое и целостное регуляторное воздействие на те или иные патологические состояния.
Несмотря на то, что явления, лежащие в основе действия релиз-активных лекарственных препаратов, до сих пор находятся в процессе изучения и осмысления, сами препараты, созданные на основе данного феномена, изучены и оценены с позиций современной фармакологии и доказательной медицины. Также накоплен большой опыт их эффективного и безопасного использования, что делает возможным их широкое использование для решения проблемы лечения и профилактики многофакторных заболеваний и острых респираторных вирусных инфекций. ЛИТЕРАТУРА 1. Штарк М.Б. Иммунонейрофизиология. — Л.: Медицина, 1978. — 175 с.
2. Бурлакова Е.Б., Конрадов А.А., Худяков И.Б. Воздействие химических агентов в сверхмалых дозах на биологические объекты // Изв. АН СССР. — 1990. — № 2. — С. 184-194.
3. Ашмарин И.П., Лелекова Т.В., Санжиева Л.Ц. Об эффективности ультрамалых доз и концентраций биологически активных соединений // Изв. РАН. — 1992. — № 4. — С. 531-536.
4. Бурлакова Е.Б., Конрадова А.А., Мальцева Е.Л. Действие сверхмалых доз биологически активных веществ и низкоинтен сивных физических факторов // Химическая физика. — 2003. — Т. 22, № 2. — С. 390-424.
5. Зилов В.Г., Судаков К.В., Эпштейн О.И. Элементы информационной биологии и медицины. — М.: МГУЛ, 2000. — 248 с.
6. Зенин С.В. Структурированное состояние воды как основа управления поведением и безопасностью живых систем: автореф. дисс. … докт. биол. наук. — М., 1999. — 42 с.
7. Эпштейн О.И. Регуляторные возможности сверхмалых доз // Бюл. экспер. биол. и мед. — 2002 (Прил. 4). — С. 8-14.
8. Эпштейн О.И. Релиз-активность — от феномена до создания новых лекарственных средств // Бюл. экспер. биол. — 2012. — Т. 154, № 7. — С. 62-67.
9. Эпштейн О.И. Феномен релиз-активности и гипотеза «пространственного» гомеостаза // Успехи физиол. наук. — 2013. — T. 44, № 3. — C. 54-76.
10. Кравков Н.П. О пределах чувствительности живой про топлазмы // Успехи эксперим. биол. — 1924. — Вып. 3-4. — С. 147-172.
11. Кузин A.M. Вторичные биогенные излучения лучи жизни. — Пущино, 1997. — 37 с.
12. Davenas Е., Poitevin В., Benveniste J. Effect on mouse peritoneal macrophages of orally administered very high dilutions of silica // Europ. J. of Pharmacol. — 1987. — Vol. 135. — P. 313-319.
13. Хариш Г., Диттман И. Особенности фундаментальных исследований в области гомеопатии // Биол. медицина. — 1998. — Вып. 1. — С. 11-13.
14. Бурлакова Е.Б., Архипова Г.В., Чернавская Л.И. Противоположный характер действия М-холинолитика амизила в малой и высокой дозах на состав и антиокислительную активность липидов синаптосомальных мембран // Биол. Мембраны. — 1987. — Т. 4, № 2. — С. 165.
15. Epstein O.I., Beregovoy N.A., Starostina M.V. et al. Membrane and synaptic effects of anti-S-100 are prevented by the same antibodies in low concentrations // Front. Biosci. — 2003. — Vol. 8. — P. 79-84.
16. Эпштейн О.И. Фармакология сверхмалых доз антител к эндогенным регуляторам функций: автореф. дисс. … докт. мед. наук. — Томск, 2003. — 50 с.
17. Эпштейн О.И., Штарк М.Б., Дыгай А.М. и др. Фармакология сверхмалых доз антител к эндогенным регуляторам функций. — М.: Изд-во РАМН, 2005. — 226 с.
18. Судаков К.В. Иммунные звенья системной организации поведения // Успехи физиологических наук. — 2011. — Т. 42, № 3. — С. 81-96.
19. Иммунофизиология / В.А. Черешнев, Б.Г. Юшков, В.Г. Кли-мин, Е.В. Лебедева. — Екатеринбург: УрО РАН, 2002. — 259 с.
20. Ашмарин И.П., Фрейдлин И.С. Гипотеза об антителах как новейших регуляторах физиологических функций, созданных эволюцией // Журн. эвол. биох. и физиол. — 1989. — Т. XV, № 2. — C. 176-181.
21. Умрюхин А.Е. Антитела в механизмах вегетативных и поведенческих функций организма // Фунд. иссл. — 2013. — № 3. — С. 425-430.
22. Ашмарин И.П. Аутоантитела — регуляторы биохимических и физиологических процессов в здоровом организме. Место в фило- генезе и среди других эндогенных регуляторов // Журн. эвол. био-хим. и физиол. — 1997. — Т. 33, № 10. — С. 228-233.
23. Пальцев М.А., Полетаев А.Б., Сучков С.В. Аутоиммунитет и аутоиммунный синдром: границы нормы и патологии // Вестн. РАМН. — 2010. — № 8. — С. 1-3.
24. Полетаев А.Б. Физиологическая иммунология (естественные аутоантитела и проблемы наномедицины). — М.: Миклош, 2010. — 220 с.
25. Полетаев А.Б., Морозов С.Г., Ковалев И.Е. Регуляторная метасистема. Иммуноэндокринная регуляция гомеостаза. — М.: Мед-на, 2002. — 168 с.
26. Полетаев А.Б. Иммунофизиология и иммунопатология. — М.: МИА, 2008. — 208 c.
27. Zaichik A.Sh. Autoimmuneregulation of genetically determined cell functions in health and disease / A.Sh. Zaichik, L.P. Churilov, V.J. Utekhin // Pathophysiology. — 2008. — Vol. 15, № 3. — P. 191-207.
28. Цвиркун Д.В. Влияние аутоантител к тиреоидным гормонам на зависимые от тиреоидного статуса физиологические функции у крыс: автореф. дис. ... канд. мед. наук. — М., 2007. — 26 с.
29. Knight J.G. Autoantibodies against brain septal region antigens specifc to unmedicated schizophrenia? // Biol. Psychiat. — 1990. — Vol. 28, № 6. — P. 464-467.
30. Copping S., Byfeld P.G. The role of thyroid hormone autoantibodies in serum transport // Acta Endocrinol. — 1989. — Vol. 4. — P. 551-559.
31. Эпштейн О.И. Возможные механизмы действия потенцированных лекарственных средств и некоторые вопросы функционирования биосистем // Бюл. СО РАМН. — 1999. — № 1 (91). — С. 132-149.
32. Sakata S., Matsuda M., Ogawa T. et al. Prevalence of thyroid hormone autoantibodies in healthy subjects // Clin. Endocrinol. — 1994. — Vol. 3. — P. 365-370.
33. Nishimura S., Nishiya K., Hisakawa N. Positivity for antinuclear antibody in patients with advanced rheumatoid arthritis // Acta. Med. Okayama. — 1996. — Vol. 50. — P. 261-265.
34. Kim J.G., Sabbagh F., Santanam N. et al. Generation of a poly-clonal antibody against lipid peroxidase modifed proteins // Free Radic. Biol. Med. — 1997. — Vol. 2. — P. 251-259.
35. Elies R., Fu L.X., Eftekhari P. et al. Immunochemical and functional characterization of an agonist like antibody against the M2 ace-tylcholine receptor // Eur. J. Biochem. — 1998. — Vol. 3. — P. 659-666.
36. Эпштейн О.И. Сверхмалые дозы (история одного исследования). — М.: Изд-во РАМН, 2008. — 336 с.
37. Инструкция к лекарственному препарату Эргоферон. — Режим доступа: grls.rosminzdrav.ru.
38. Крылова С.Г., Зуева Е.П., Гурьянова Н.Н. и др. Экспериментальное изучение противовоспалительной активности препарата эргоферон на модели каррагенинового отека лапы у крыс // XXI Российский национальный конгресс «Человек и лекарство». — 2014. — С. 271.
39. Жавберт Е.С., Дугина Ю.Л., Эпштейн О.И. Противовоспалительные и противоаллергические свойства антител к гистамину в релиз-активной форме: обзор экспериментальных и клинических исследований // Детские инфекции. — 2014. — № 1. — С. 40-43.
40. Шиловский И.П., Корнилаева Г.В., Хаитов М.Р. in vitro исследование противовирусной активности эргоферона // XIX Российский национальный конгресс «Человек и лекарство». — М., 2012. — С. 438-439.
41. Шерстобоев Е.Ю., Масная Н.В., Чурин А.А. и др. Иммунотроп-ные эффекты потенцированных антител к интерферону-гамма человека // Бюл. экспер. биол. и мед. — 2002. — Прил. 4. — С. 79-82.
42. Эпштейн О.И., Дыгай А.М., Шерстобоев Е.Ю. и др. Экспериментальное исследование фармакологических эффектов сверхмалых доз антител к эндогенным регуляторам функций // Бюл. экс-пер. биол. и мед. — 2008. — Прил. 2. — С. 82-88.
43. Костинов М.П. Новый препарат для лечения гриппа и ОРВИ // Инф. болезни. — 2011. — Т. 9, № 4. — С. 29-34.
44. Шишкина Л.Н., Сергеев А.Н., Сергеев А.А. и др. Изучение лечебно-профилактического действия сверхмалых доз антител к гамма-интерферону при инфицировании кур вирусом гриппа птиц // XV Российский национальный конгресс «Человек и лекарство». — М., 2008. — С. 732-733.
45. Tarasov S.A., Zarubaev V.V., Gorbunov E.A. et al. Activity of ultra-low doses of antibodies to gamma-interferon against lethal infu-enza A(H1N1)2009 virus infection in mice // Antiviral. Res. — 2012. — Vol. 93 (2). — P. 219-224.
46. Веревщиков В.К., Борзунов В.М., Шемякина Е.К. Оптимизация этиопатогенетической терапии гриппа и ОРВИ у взрослых при применении эргоферона // Антиб. и химиотер. — 2011. — Т. 56, № 9-10. — С. 23-26.
47. Шиловский И.П., Корнилаева Г.В., Хаитов М.Р. Новые возможности в терапии респираторно-синцитиальной вирусной инфекции: данные доклинического исследования препарата «Эрго-ферон» // Иммунология. — 2012. — Т. 33, № 3. — С. 144-148.
48. Головачева Е.Г. Клинико-лабораторное обоснование применения иммунокорригирующей терапии при респираторно-синцити-альной вирусной инфекции у детей: автореф. дисс. ... канд. мед. наук. — СПб, 2003. — 19 с.
49. Аверьянов А.В., Бабкин А.П., Барт Б.Я. и др. Эргоферон и Осельтамивир в лечении гриппа — результаты многоцентрового сравнительного рандомизированного клинического исследования // Антиб. и химиотер. — 2012. — Т. 57, № 7-8. — С. 23-30.
50. Степанищева Л.А., Сосновских И.В., Кучина Т.Ф. и др. Эр-гоферон в лечении ОРВИ у взрослых: результаты рандомизированного клинического исследования // Доктор.Ру. — 2012 (Спец. выпуск XIX Российский национальный конгресс «Человек и лекарство»). — С. 1-7.
51. Гаврюченков Д.В. Новый противовирусный препарат Эрго-ферон в лечении респираторных инфекций // Поликлиника. — 2011. — Т. 5, № 1. — С. 78-81.
52. Тихонова Е.П., Кузьмина Т.Ю., Андронова Н.В., Тихонова Ю.С. Эффективность применения Эргоферона для лечения острых респираторных вирусных инфекций // Практ. медицина. — 2014. — № 1 (77). — С. 179-184.
53. Кареткина Г.Н. Некоторые итоги и уроки эпидемии гриппа и ОРВИ-2012 // Вирусология. — 2013. — С. 46-50.
54. Шестакова Н.В., Загоскина Н.В., Самойленко Е.В. и др. Эффективность и безопасность Эргоферона в комплексной терапии внеболь-ничных пневмоний // Доктор.Ру. — 2012. — Т. 76, № 8. — С. 44-47.
55. Ржанникова Н.И., Ржаникова А.Н., Соловьева Е.Ю. Клиническая эффективность Эргоферона при острых респираторных вирусных инфекциях у пожилых // Акад. Журн. Западной Сибири. — 2012. — № 3. — С. 45 (Юб. научно-практическая конференция «Пожилой человек: качество жизни», посвященная 67-летию победы в Великой Отечественной войне 1941-1945 гг. — Тюмень, 2012.).


