Нооклерин (деанола ацеглумат) в практике купирования алкогольного абстинентного синдрома
СтатьиОпубликовано в журнале :
Наркология. 2016. №5 (173) C. 48—58.
Кожинова Т.А. к.м.н., ведущий научный сотрудник отдела психических расстройств, осложненных патологическими видами зависимости
Гофман А.Г. д.м.н., проф., руководитель отдела психических расстройств, осложненных патологическими видами зависимости
Немкова Т.И. к.м.н., врач-психиатр-нарколог отделения психических расстройств, осложненных патологическими видами зависимости
Шеин В.В. врач-психиатр-нарколог отделения психических расстройств, осложненных патологическими видами зависимости
Ромашкина Н.В. врач-психиатр-нарколог консультативно-диагностического отделения
Московский НИИ психиатрии — филиал ФГБУ «МНИЦПН им. В.П.Сербского» Минздрава России Москва, Потешная ул., 3 Проведено научное исследование, в котором препарат Нооклерин® (деанола ацеглумат) получали 40 больных алкогольной зависимостью в период алкогольного абстинентного синдрома (ААС) в суточной дозе 2000 мг per os. Доказано, что препарат проявляет ноотропное и антиастеническое действие, оказывает выраженный терапевтический эффект, устраняя основные соматоневрологические и аффективные симптомы ААС в более короткие (статистически значимые) сроки по сравнению с контрольной группой (40 больных, получавших стандартную дезинтоксикационную терапию). Активирующий эффект нооклерина не сопровождается усилением патологической тяги к алкоголю. Изучение динамики изменений лабораторных показателей, в том числе ферментативной активности печени выявило положительное влияние препарата на эти показатели в основной группе.
Ключевые слова: алкогольная зависимость, алкогольный абстинентный синдром, терапия алкоголизма, астения, ноотропы, нооклерин, гамма-глутамилтрансфераза
Введение
В настоящее время сохраняется повышенный интерес научной общественности к вопросам изучения патогенетических, нейрометаболических, нейромедиаторных и других механизмов формирования зависимостей, в том числе алкогольной, и возникающих изменений в организме, связанных с патологическим влиянием психоактивных веществ (ПАВ). Интенсивная терапия абстинентного синдрома (АС), как одно из звеньев лечения заболевания, строится на коррекции нарушений метаболизма, которые возникают вследствие систематического приема ПАВ. Известно, что используемые для лечения АС некоторые лекарственные средства порой вызывают неблагоприятные побочные эффекты, утяжеляющие состояние больных. Поэтому постоянно идет поиск новых средств терапии, которые, ускоряя и значительно облегчая симптомы АС, приводили бы к формированию более качественных и продолжительных ремиссий (А.А.Крылов, А.Н.Ибатов, 1992; А.Г.Гофман, А.В.Граженский, Н.В.Александрова, 1998; Ю.Ф.Чуев, 1999; П.С.Балашов, 2003; А.П.Добровольский, 2005 и другие). В связи с этим остается актуальным вопрос повышения эффективности терапии, в том числе ААС, и поиск новых безопасных в применении препаратов, которые не оказывают токсического влияния на печень и обладают сочетанным действием (антиоксидантным, ноотропным, антиастеническим, гепатопротекторным), что позволило бы повысить эффективность проводимой терапии и качество жизни больных.
Деанола ацеглумат (Нооклерин®) — вещество, оказывающее нейрометаболическое действие, влияет на систему возбуждающих аминокислот и обмен холина. Данные научных исследований также свидетельствуют о наличии у этого вещества антиоксидантных и гепатопротекторных свойств [1, 4, 9, 10]. Клинические исследования Нооклерина® [2, 3, 4, 6] свидетельствуют о том, что препарат обладает отчетливой ноотропной и церебропротективной активностью, эффективен при лечении астенических и астенодепрессивных расстройств (соматические заболевания, реакции на острый стресс, инфекции, пограничные состояния, алкоголизм, психоорганические нарушения, эндогенные заболевания). Результаты исследований [5, 8] показали, что деанола ацеглумат (Нооклерин®) вызывает изменения структуры ЭЭГ во всех частотных диапазонах, характер и степень выраженности которых существенно варьируют в зависимости от длительности лечения и особенностей фоновой активности. Отмеченная динамика структуры ЭЭГ в виде усиления основного ритма подтверждает принадлежность препарата к классу нейрометаболических стимуляторов, возможно за счет близости химической структуры препарата к естественным метаболитам головного мозга ГАМК, глутаминовой кислоте.
Препарат Нооклерин® (деанола ацеглумат) включен в перечень стандартов первичной медико-санитарной и специализированной медицинской помощи при заболеваниях и состояниях, связанных с употреблением психоактивных веществ (Приказы Министерства здравоохранения России №№124—135н от 04 сентября 2012 г. о включении Деанола ацеглумат в стандарты терапии острой интоксикации, абстинентного состояния, психотического и амнестического расстройств, пагубного употребления и зависимости от психоактивных веществ). В связи с этим Нооклерин® (Деанола ацеглумат) можно рассматривать как препарат, позволяющий повысить эффективность терапии, направленной на купирование ААС, за счет сочетания ноотропного, антиастенического, антиоксидантного и гепатопротекторного эффектов, а также снизить длительность и стоимость терапии ААС.
Одним из преимуществ препарата Нооклерин® является его форма выпуска в виде раствора для приема внутрь 200 мг/мл, флакон 100 мл. Это позволяет применять препарат для лечения больных, не способных по каким-либо причинам к самостоятельному приему твердых лекарственных форм. Важны показатели фармакокинетики: через 0,5—1 ч после перорального приёма препарат обнаруживается в максимальной концентрации в головном мозге, в несколько меньших количествах в печени, сердце, лёгких, плазме крови, в почках. Препарат выводится почками, что снижает лекарственную нагрузку на печень.
Объект и методы исследования
В ходе научно-исследовательской работы проводилась оценка действия препарата Нооклерин® на скорость купирования основных проявлений алкогольного абстинентного синдрома, воздействия на когнитивные функции и уровень ферментов печени в сыворотке крови у больных алкоголизмом.
Вид исследования: открытое, рандомизированное, сравнительное клинико-фармакологическое исследование.
Характеристика клинической группы больных и сопутствующая терапия
Всего в исследование было включено 80 больных (72 мужчин и 8 женщин).
Критерии включения:
- возраст от 25 до 65 лет;
- наличие алкогольной зависимости средней степени тяжести и алкогольного абстинентного синдрома легкой и средней степени тяжести в соответствии критериям МКБ-10: F 10.2 и F 10.3;
- длительность абстинентного синдрома не более суток;
- отсутствие сопутствующей острой психической патологии и тяжелой неврологической патологии;
- наличие информированного согласия.
Критерии исключения:
- тяжелые, декомпенсированные или нестабильные соматические заболевания (любые заболевания или состояния, которые угрожают жизни больного или ухудшают прогноз);
- больные с установленным диагнозом цирроза печени;
- больные с психическими заболеваниями шизофренического спектра;
- непереносимость исследуемого препарата;
- беременность и лактация;
- одновременное участие в другом клиническом исследовании.
Основная группа (40 чел.): Базовая терапия с включением анксиолитика Феназепама + Нооклерин®.
Группа сравнения или контрольная группа (40 чел.). Базовая терапия + анксиолитик Феназепам.
Основная группа включала 40 пациентов, получавших Нооклерин® (деанола ацеглумат) с 1-го по 10-й день перорально 20%-ный раствор для приема внутрь 100 мл в дозе 2 г в сутки (по 1 г 2 раза в сутки), последний прием не менее чем за 4 часа до сна в сочетании с базовой (дезинтоксикационной) терапией ААС.
Контрольная группа, или группа сравнения, включала 40 пациентов, которые получали базовую (дезинтоксикационную) терапию, включая:
- Инфузионную терапию (детоксикация: полиионные смеси трисоль, хлосоль, физиологический раствор (NaCl 0,9%) от 400 до 800 мл, 5% р-р глюкозы в/в капельно) + 10 мл 25% р-ра сульфата магнезии в/в, витамины: vit B1 6%, vit B6 5% по 2—4 мл в/м; никотиновая кислота в/м; аскорбиновая кислота в/в;
- Бета-адреноблокаторы и гипотензивные (по показаниям) атенолол 50—100 мг per os; капотен или капозид 25—50 мг per os, антагонисты кальция;
- Транквилизаторы: Феназепам до 4 мг в сут.
Данная выборка, учитывая особенности отделения (отделение психических расстройств, осложненных патологическими формами зависимости), была сформирована из пациентов, страдающих алкогольной зависимостью средней степени, поступающих на стационарное лечение в МНИИП с признаками алкогольного абстинентного синдрома. У всех 80 пациентов установлен диагноз F 10.21 (Синдром зависимости от алкоголя) и F 10.30 (Синдром отмены алкоголя). В исследование не включали больных с признаками манифестной шизофрении, органического поражения ЦНС, аффективной патологии в фазе обострения, личностными расстройствами возбудимого круга, а также пациентов с тяжелой степенью алкогольного абстинентного синдрома.
Из 40 обследованных больных основной группы, состоящей из 35 мужчин и 5 женщин, помимо алкогольной зависимости в анамнезе присутствовала следующая психопатология:
- резидуально-органическая недостаточность ЦНС травматического, сосудистого и токсического (алкоголь) генеза, в том числе с указанием на судорожный синдром в структуре ААС в анамнезе 8 больных (2%);
- аффективное расстройство тревожно-тоскливого монополярного круга, в том числе в рамках БАР вне фазы обострения (F 31.3; F 32,1; F 33.4; F 34.0; F 43.2) — 7 больных (17,5%);
- шизотипичеcкое расстройство со склонность к нечетко очерченным аффективным колебаниям (F 21) — 1 больной (2,5%);
- шизоидное личностное расстройство (F 60.1) — 2 больных (5%).
Из 40 обследованных больных контрольной группы, состоящей из 37 мужчин и 3 женщин, помимо алкогольной зависимости в анамнезе следует отметить наличие следующей патологии:
- резидуально-органическая недостаточность ЦНС травматического, сосудистого и токсического (алкоголь) генеза, в том числе с указанием на судорожный синдром в структуре ААС в анамнезе 7 больных (17,5%);
- аффективное расстройство тревожно-тоскливого монополярного круга, в том числе в рамках БАР вне фазы обострения (F 31.3; F 32,1; F 33.4; F 34.0; F 43.2) — 7 больных (17,5%);
- эмоционально-неустойчивое расстройство личности (F 60.3) — 1 больной (2,5%);
- смешанное расстройство личности (F 61.1) — 1 больной (2,5%).
Возрастные и анамнестические данные о больных основной и контрольной групп представлены в табл. 1, из которой следует, что статистически достоверных различий по основным возрастным и анамнестическим показателям в основной и контрольной группах не выявлено, что делает их абсолютно сопоставимыми для проведения сравнительного научного исследования. Иными словами, все классы представлены равномерно.
Таблица 1
Характеристика больных по возрастным и анамнестическим показателям
| Данные анамнеза | Основная группа | Контрольная группа | p |
| Возраст больных (годы) | 43,38 ± 7,1 (29-65) | 44,95 ± 5,6 (30-60) | 0,466254 |
| Длительность заболевания (годы) | 17,38 ± 5,0 (2-40) | 16,53 ± 6,8 (2-35) | 0,274861 |
| Длительность существования похмельного синдрома (годы) | 11,23 ± 5,9 (1-29) | 10,54 ± 6,7 (1-29) | 0,358117 |
| Средняя продолжительность запоев (дни) | 6,84 ± 7,1 (3-15) | 9,0 ± 5,8 (2-30) | 0,000382 |
| Продолжительность последнего запоя (дни) | 7,84 ± 4,3 (3-20) | 8,1 ± 3,1 (2-30) | 0,415984 |
| Доза алкоголя в период последнего запоя в пересчете на водку (литры) | 0,79 ± 0,28 (0,4-2,0) | 0,81 ± 0,20 (0,35-2,0) | 0,603175 |
| Число больных в группе | 40 | 40 |
Таблица 2
Продолжительность существования ведущих симптомов острого периода ААС у пациентов основной и контрольной группп (в днях)
| Симптомы ААС | Основная группа (дни) | Контрольная группа (дни) | U | p |
| Тревога | 2,3 ± 2,1 | 3,6 ± 3,5 | 654,0 | 0,16006 |
| Пониженное настроение | 4,1 ± 2,6 | 6,8 ± 3,3 | 446,5** | 0,00067 |
| Влечение к алкоголю | 2,3 ± 1,2 | 3,4 ± 2,6 | 591,5* | 0,04483 |
| Нарушение засыпания | 3,0 ± 1,7 | 4,6 ± 3,2 | 554,5* | 0,01816 |
| Поверхностный сон | 3,1 ±2,3 | 4,0 ± 2,4 | 560,5* | 0,02119 |
| Тремор | 3,5 ± 2,5 | 5,8 ± 3 | 360,0** | 0,00002 |
| Атаксия в пробе Ромберга | 3,0 ± 1,5 | 4,4 ± 2,6 | 486,0** | 0,00252 |
| Тахикардия | 3,3 ± 1,9 | 4,8 ± 3,1 | 573,5* | 0,02930 |
| Повышение АД | 4,2 ± 2,8 | 5,3 ± 3,5 | 638,0 | 0,11903 |
| Понижение аппетита | 2,1 ± 0,7 | 3,3 ± 2,3 | 457,5** | 0,00098 |
| Жажда | 2,4 ± 0,9 | 2,1 ± 1,5 | 701,0 | 0,34078 |
| Потливость | 2,1 ± 1,2 | 2,9 ± 1,8 | 539,5* | 0,01219 |
| Число больных в группе | 40 | 40 |
Таблица 3
Результаты сравнения выраженности симптомов ААС в течение всего периода лечения в основной группе (Нооклерин®) и группе сравнения (контрольной)
| Группы | Симптомы от 1 к 10 дню | Коэфф. конкордации | χ² | р |
| Основная группа (нооклерин) | Тревога | 0,66 | 132,5* | 0,00000001 |
| Пониженное настроение | 0,68 | 136,04* | 0,00000001 | |
| Влечение к алкоголю | 0,76 | 151,8* | 0,00000001 | |
| Нарушение засыпания | 0,72 | 144,59* | 0,00000001 | |
| Поверхностный сон | 0,72 | 144* | 0,00000001 | |
| Тремор | 0,83 | 165,7* | 0,00000001 | |
| Атаксия в пробе Ромберга | 0,84 | 167,3* | 0,00000001 | |
| Тахикардия | 0,82 | 163,9* | 0,00000001 | |
| Повышение АД | 0,77 | 154,1* | 0,00000001 | |
| Понижение аппетита | 0,8 | 160,7* | 0,00000001 | |
| Жажда | 0,81 | 162,9* | 0,00000001 | |
| Потливость | 0,73 | 145,6* | 0,00000001 | |
| Группа сравнения | Тревога | 0,57 | 113,5* | 0,00000001 |
| Пониженное настроение | 0,53 | 102,8* | 0,00000001 | |
| Влечение к алкоголю | 0,74 | 148,6* | 0,00000001 | |
| Нарушение засыпания | 0,63 | 125,1* | 0,00000001 | |
| Поверхностный сон | 0,72 | 143,9* | 0,00000001 | |
| Тремор | 0,81 | 161,5* | 0,00000001 | |
| Атаксия в пробе Ромберга | 0,78 | 155,7* | 0,00000001 | |
| Тахикардия | 0,79 | 158,1* | 0,00000001 | |
| Повышение АД | 0,74 | 148,9* | 0,00000001 | |
| Понижение аппетита | 0,72 | 143,7* | 0,00000001 | |
| Жажда | 0,61 | 122,1* | 0,00000001 | |
| Потливость | 0,62 | 124,4* | 0,00000001 |
Методы исследования
Использовались клинический, клинико-психопатологический, клинико-фармакологический, экспериментально-психологический, лабораторный и статистический методы исследования.
Для обеспечения стандартизации исследования использовался 3-балльный глоссарий по определению выраженности отдельных проявлений ААС и общей тяжести состояния, разработанный на базе отделения наркологии Московского НИИ психиатрии (Магалиф А.Ю., Крылов Е.Н. и др., 1988).
Экспериментально-психологические методы включали: субъективную шкалу оценки астении (MFI-2Q); методику «счет по Крепелину»; тест «заучивание 10 слов» (А.Р.Лурия).
Лабораторный метод исследования включал биохимический анализ крови с определением параметров, характеризующих функцию печени, в том числе АЛТ, АСТ, ЩФ, ГГТ, билирубина, а также уровень общего белка, альбуминов, креатинина, амилазы и мочевины.
Для реализации поставленных задач были использованы следующие методы математической статистики:
- Оценка среднего арифметического
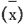 , стандартного отклонения (σ), долей (%);
, стандартного отклонения (σ), долей (%); - Проверка распределения полученных данных на соответствие закону нормального распределения с помощью критерия Шапиро—Уилкса;
- Оценка различий значений количественных показателей между основной группы и группы сравнения проводилась с помощью непараметрического U-критерия Манна—Уитни;
- Оценка сдвигов показателей до и после исследования в основной группе и группе сравнения проводилась с помощью непараметрического T-критерия Вилкоксона и критерия Фридмана с оценкой коэффициента конкордации;
- Для выявления влияния Нооклерина® на выраженность существующих признаков астении и лабораторных показателей был использован непараметрический H-критерий Краскела—Уоллиса (ANOVA), так как в исследуемых группах отсутствует однородность дисперсий.
Математическая обработка осуществлялась с помощью статистического пакета программ Statistica 10.0.
Дизайн и результаты исследования
Все больные, включенные в исследование, учитывая временную динамику состояния (купирование соматоневрологических и психических нарушений ААС на фоне терапии), наблюдались ежедневно в течение первых 5 дней существования алкогольного абстинентного синдрома с момента поступления в отделение.
Для обеспечения стандартизации исследования использовался 3-балльный глоссарий по определению выраженности отдельных проявлений ААС и общей тяжести состояния (Магалиф А.Ю., Крылов Е.Н., 1988) с ежедневным заполнением протоколов исследования. Специальные баллированные анкеты, включающие 12 основных симптомов ААС, выявленных путем факторного анализа, позволяют выявить динамику убывания симптомов алкогольного абстинентного синдрома по сравнению с контрольной группой и оценить эффективность терапии Нооклерином®.
Первое обследование больного проводилось непосредственно при поступлении в стационар до назначения терапии. Фиксировалась прогностическая оценка тяжести ААС (легкая средняя тяжелая). В сравнительное исследование были включены только пациенты с легкой и средней тяжестью алкогольного абстинентного синдрома. Все анамнестические сведения и данные ежедневного обследования пациентов заносились в протоколы исследования для последующего статистического анализа. Проводилось экспериментально-психологическое тестирование, включавшее субъективную шкалу оценки астении (MFI-2Q); методику «счет по Крепелину»; тест «заучивание 10 слов» (А.Р.Лурия). Осуществлялся в/в забор крови для определения уровня следующих биохимических показателей: Alt, Ast, Bilirubin, Alp, Ggt, Amy, Albumin, Protein, Creatinin, Urea Uv. Последнее наблюдение с регистрацией общего состояния больного, проведения экспериментально-психологического тестирования с использованием вышеуказанных методик, позволяющих оценивать уровень общей астении и когнитивные функции, а также повторный забор крови с целью лабораторной диагностики уровня печеночных ферментов и др. биохимических показателей, проводилось на 10 сутки пребывания в стационаре.
При сравнении скорости купирующего эффекта Нооклерина® на фоне стандартной дезинтоксикационной терапии (совместно с феназепамом) в отношении отдельных симптомов ААС с эффективностью обычной базовой терапии (с использованием феназепама) были получены следующие результаты.
Установлено, что у тех пациентов, при лечении которых был использован Нооклерин®, необходимо в среднем меньшее количество дней для полного убывания каждого симптома ААС. Проведенное сравнение с помощью U-критерия Манна—Уитни показало, что при применении Нооклерина® быстрее устраняются следующие симптомы: пониженное настроение, влечение к алкоголю (снижение и полная редукция патологической тяги к алкоголю), нарушение засыпания, поверхностный сон, тремор, атаксия в пробе Ромберга, тахикардия, понижение аппетита, потливость.
Также было исследовано наличие неслучайных различий между изменениями выраженности симптомов ААС в течение всего периода лечения. Для этого был использован непараметрический критерий Фридмана.
В результате проведенного сравнения установлено, что как в основной, так и в группе сравнения по каждому симптому ААС наблюдается наличие не случайных различий между изменениями выраженности симптомов ААС в течение всего периода лечения. Анализ коэффициента конкордации Кенделла показал, что наиболее согласованное снижение выраженности симптомов наблюдается именно у пациентов, получавших Нооклерин® (более высокий коэффициент конкордации).
Проведенное сравнение с помощью T-критерия Вилкоксона показало, что как в основной (Нооклерин®), так и в контрольной группе, наблюдается достоверное снижение значения суммарной выраженности симптомов, по сравнению с началом лечения. Однако в основной группе динамика улучшения состояния с полной редукцией основных симптомов ААС, достоверно быстрее, чем в контрольной группе больных.
В данном случае необходимо подчеркнуть, что при терапии препаратом Нооклерин® в сочетании с феназепамом у больных отсутствовали присущая пациентам, получавшим исключительно феназепам, дневная сонливость и выраженная моторно-идеаторная заторможенность. Это является несомненным преимуществом изучаемого препарата.
В то же время, видимо, за счет выраженного сбалансированного ноотропного эффекта у больных, получавших Нооклерин®, в более короткие, статистически достоверные сроки, улучшались ночное засыпание и качество ночного сна. Данные клинического обследования, в основном, совпадали с субъективной оценкой своего состояния больными достаточно быстро исчезали кошмары и сны алкогольного содержания, утром пациенты отмечали бодрость и чувство отдыха после сна, облегчение общего самочувствия. Эти больные были более активными уже на 2-е сутки пребывания в стационаре, начинали играть в бильярд, настольный теннис. Значительно быстрее, чем у пациентов, находившихся на терапии просто феназепамом, у них редуцировались слабость, вялость, ощущение разбитости и чувство общего дискомфорта.
Таблица 4
Средние значения суммарной выраженности симптомов в основной и контрольной группах больных в баллах и процентах от первоначальной тяжести состояния в первые 5 дней терапии
| Группы больных | Суммарная выраженность симптомов в баллах и процентах | ||||
| 1-й день | 2-й день | 3-й день | 4-й день | 5-й день | |
| Основная группа (Нооклерин®) | 20,5 | 14,2 69%* | 7,7 38%* | 3,6 18%* | 1,5 7%* |
| Контрольная группа | 18,9 | 16,6 88%** | 11,5 61%** | 7,2 38%** | 4,5 24%** |
Однако, следует подчеркнуть, что у 5 пациентов основной (Нооклерин®) группы, которым был выставлен диагноз энцефалопатии сочетанного генеза (сосудистого, токсического, травматического) с указанием на наличие судорожного синдрома в структуре ААС в анамнезе, прием Нооклерина® в дневные часы усиливал имеющийся тремор рук. Выраженность и интенсивность тремора сохранялась практически неизменной в течение всего периода наблюдения (10 дней). Это, видимо, указывает на то, что у таких больных отмечается выраженный активирующий эффект препарата, усиливающий явления ирритации в стволовых структурах мозга и, возможно, увеличивающий реактивность корковых структур. Тем не менее, в процессе лечения не наблюдалось патологического усиления тремора.
Для определения степени выраженности различных форм астении (общей астении, физической астении, пониженной активности, снижения мотивации, психической астении) в структуре алкогольного абстинентного синдрома и сравнительной оценки динамики убывания астенического симптомокомплекса у больных, получающих стандартную дезинтоксикационную терапию с применением транквилизаторов и на фоне приема Нооклерина®, была использована шкала оценки астении (MFI-2Q). С целью изучения влияния Нооклерина® на когнитивные функции, учитывая выраженный ноотропный эффект препарата, были использованы следующие методики: «счет по Крепелину»; тест «заучивание 10 слов». Тестирование проводилось в основной (Нооклерин®) и контрольной группах непосредственно при поступлении в отделение (1-й день госпитализации) и на 10-е сутки исследования, после купирования симптомов алкогольного абстинентного синдрома.
В процессе сравнения было обнаружено, что значимые положительные сдвиги существуют по всем психологическим переменным, как в основной, так и в контрольной группе.
Для того, чтобы узнать, существовали ли изначально различия до исследования в основной группе и группе сравнения и постараться выявить, в какой группе произошли более выраженные изменения, был использован непараметрический U-критерий Манна—Уитни.
В ходе сравнения было установлено, что группы различались уровнем испытываемой физической астении (U = 575,5 при р = 0,030754). Однако после исследования в основной группе произошли более значительные изменения, т.е. более выраженное снижение симптомов общей астении и улучшение когнитивных функций, выявляемых по количеству ошибок при счете по Крепелину и тесту «заучивание 10 слов». Стоит отметить, что количество ошибок при счете по Крепелину и среднее количество слов, запоминаемых больными за 5 попыток, изначально было практически одинаковым, а после лечения препаратом Нооклерин® наблюдается более выраженное снижение количества ошибок, по сравнению с результатами, полученными у пациентов из группы сравнения (контрольной группы), что подтверждает выраженный ноотропный эффект препарата. Учитывая полученные результаты, можно говорить о том, что терапевтический эффект Нооклерина® сказывается на улучшении тех когнитивных функций, ослабление которых является ближайшим следствием интоксикации алкоголем (непосредственное запоминание и устойчивость внимания).
Таблица 5
Результаты проверки переменных астенокомплекса на нормальность распределения
| Переменные | Основная группа (Нооклерин®) | Контрольная группа (сравнения) | |||||
| Mean | W | p | Mean | W | p | ||
| В начале исследования | Общая астения | 18,2 ± 2,2 | 0,75* | 0,000001 | 17,7 ±2,1 | 0,88* | 0,000427 |
| Пониженная активность | 15,7 ± 2,3 | 0,95 | 0,069785 | 15,9 ± 2,5 | 0,95 | 0,107153 | |
| Снижение мотивации | 13,2 ± 3,2 | 0,97 | 0,435279 | 13,2 ± 3,1 | 0,95 | 0,084421 | |
| Физическая астения | 16,4 ± 3,1 | 0,72* | 0,0000001 | 15,5 ± 2,3 | 0,96 | 0,181026 | |
| Психическая астения | 14,9 ± 3,1 | 0,95 | 0,105801 | 13,4 ± 3,9 | 0,95 | 0,097961 | |
| Общее количество баллов | 78,8 ± 8,5 | 0,99 | 0,868389 | 75,7 ± 8,5 | 0,96 | 0,113414 | |
| Счет (ошибки) | 4,7 ± 1,3 | 0,92* | 0,009409 | 4,6 ± 1,4 | 0,81* | 0,000011 | |
| В конце исследования | Общая астения | 5,3 ± 1,4 | 0,84* | 0,000062 | 8,0 ± 2,9 | 0,95 | 0,076579 |
| Пониженная активность | 7,1 ± 1,8 | 0,94* | 0,047633 | 8,4 ± 2,7 | 0,95 | 0,051190 | |
| Снижение мотивации | 6,5 ± 1,8 | 0,90* | 0,002201 | 8,4 ± 2,4 | 0,95 | 0,056041 | |
| Физическая астения | 5,9 ± 1,5 | 0,89* | 0,001254 | 8,9 ± 2,1 | 0,93* | 0,011883 | |
| Психическая астения | 5,3 ± 1,6 | 0,80* | 0,000007 | 7,3 ± 2,4 | 0,99 | 0,994863 | |
| Общее количество баллов | 30,1 ± 6,1 | 0,94* | 0,029747 | 40,8 ± 9,8 | 0,96 | 0,143187 | |
| «Счет по Крепелину» (ошибки) | 0,6 ± 0,3 | 0,72* | 0,0000001 | 1,5 ± 0,9 | 0,86* | 0,000157 | |
| Тест «10 слов» | 7,9 ± 0,6 | 0,83* | 0,000352 | 6,3 ± 0,8 | 0,89* | 0,000314 | |
Для выявления влияния применения Нооклерина® на каждый показатель астенического симптомокомплекса был использован непараметрический H-критерий Краскела—Уоллиса.
Исходя из результатов анализа и основываясь на значениях Н-критерия, можно сделать вывод о том, что применение Нооклерина® оказывает большее влияние на физическую астению, так как соответствующие показатели изменяются в максимально большей степени, чем все остальные проявления астении. Следует подчеркнуть, что на фоне терапии нооклерином происходит более быстрое, статистически достоверное, устранение всех составляющих астенического симптомокомплекса и восстановление общей активности.
Таблица 6
Результаты сравнения показателей основной и контрольной группы (сравнения) в срезах до и после исследований
| Переменные | Rank Sum (основная) | Rank Sum (сравнения) | U | Z | p | |
| В начале исследования | Общая астения | 1728,5 | 1511,5 | 691,5 | 1,0 | 0,296467 |
| Пониженная активность | 1522,5 | 1637,5 | 742,5 | -0,4 | 0,713084 | |
| Снижение мотивации | 1621,0 | 1619,0 | 799,0 | 0,0 | 0,992322 | |
| Физическая астения | 1844,5 | 1395,5 | 575,5* | 2,2 | 0,030754 | |
| Психическая астения | 1793,5 | 1446,5 | 626,5 | 1,7 | 0,095018 | |
| Общее количество баллов | 1766,0 | 1474,0 | 654,0 | 1,4 | 0,160056 | |
| «Счет по Крепелину» (ошибки) | 1615,0 | 1625,0 | 795,0 | 0,0 | 0,961627 | |
| Тест «10 слов» | 1564,2 | 1494,0 | 682,4 | 1,3 | 0,243165 | |
| В конце исследования | Общая астения | 1110,0 | 2130,0 | 290,0** | -4,9 | 0,000001 |
| Пониженная активность | 1414,5 | 1825,5 | 594,5* | -2,0 | 0,047994 | |
| Снижение мотивации | 1274,5 | 1965,5 | 454,5** | -3,3 | 0,000886 | |
| Физическая астения | 1024,5 | 2215,5 | 204,5** | -5,7 | 0,00000001 | |
| Психическая астения | 1225,0 | 2015,0 | 405,0** | -3,8 | 0,000144 | |
| Общее количество баллов | 1097,5 | 2142,5 | 277,5** | -5,0 | 0,0000005 | |
| «Счет по Крепелину» (ошибки) | 1341,0 | 1899,0 | 521,0** | -2,7 | 0,007260 | |
| Тест «10 слов» | 1291,3 | 1978,3 | 498,2 | -2,9 | 0,009431 | |
Таблица 7
Результаты проведения H-критерия Краскела—Уоллиса
| Показатели после Нооклерина® | H | р |
| Общая астения | 24,74** | 0,00000001 |
| Пониженная активность | 4,01* | 0,0452 |
| Снижение мотивации | 11,34** | 0,0008 |
| Физическая астения | 33,37** | 0,00000001 |
| Психическая астения | 15,02** | 0,0001 |
| Общее количество баллов | 25,32** | 0,00000001 |
| Счет (ошибки) | 8,16** | 0,0043 |
Таким образом, улучшение общего самочувствия больных и более быстрое их восстановление на фоне терапии нооклерином по показателям субъективной шкалы оценки астении (MFI-2Q), регистрируемыми самими пациентами, совпадает с объективной оценкой нормализации общего состояния и купированием основных симптомов ААС в более короткие сроки, регистрируемых исследователем путем использования 3-балльного глоссария по определению выраженности отдельных проявлений ААС и общей тяжести состояния (Магалиф А.Ю., Крылов Е.Н., 1988).
C целью изучения гепатопротекторного влияния Нооклерина® в сравнительном исследовании использовался лабораторный метод диагностики с регистрацией ряда биохимических показателей крови, в том числе АЛТ, АСТ, ГГТ, билирубина.
Для выявления различий между основной и контрольной группами и для выявления значимости сдвигов в значениях переменных в каждой исследуемой группе были применены непараметрические критерии, так как проведенный W-критерий Шапиро—Уилкса (был выбран именно этот показатель, как наиболее робастный) показал отсутствие подчиненности закону нормального распределения у большинства переменных.
В ходе выявления существующих сдвигов в основной (Нооклерин®) и контрольной группе до и после исследования было установлено, что в основной группе значимые положительные сдвиги (уменьшение значений) были выявлены по таким показателям, как ALT (T = 77 при р = 0,000021), AST (T = 59 при р = 0,000004), BIL TOT (T = 24,5 при р = 0,0000002), ALP (T = 162,5 при р = 0,004354), GGT (T = 6 при р = 0,0000002).
Таким образом, изучение динамики изменения лабораторных показателей в течение первых 10 дней терапии ААС в основной (Нооклерин®) и контрольной группах выявило улучшение ферментативной активности печени в обеих группах, но с тенденцией к более быстрому восстановлению у пациентов основной группы. Однако эти изменения не достигали степени статистической значимости. Следовательно, оценивая эффективность применения Нооклерина® в данном исследовании, можно говорить о наличии у препарата мягкой гепатопротекторной активности, а также его безопасности.
Таблица 8
Результаты проверки на нормальность распределения лабораторных показателей
| Показатели | Основная группа | Группа сравнения | |||
| W | p | W | p | ||
| В начале исследования | ALT | 0,75* | 0,000001 | 0,60* | 0,0000001 |
| AST | 0,63* | 0,0000001 | 0,78* | 0,000003 | |
| BIL TOT | 0,96 | 0,224272 | 0,94 | 0,028139 | |
| GGT | 0,65* | 0,0000001 | 0,71* | 0,0000001 | |
| В конце исследования | ALT | 0,76* | 0,000001 | 0,63* | 0,0000001 |
| AST | 0,61* | 0,0000001 | 0,81* | 0,000009 | |
| BIL TOT | 0,98 | 0,536811 | 0,97 | 0,394750 | |
| GGT | 0,61* | 0,0000001 | 0,86* | 0,000152 | |
Таблица 9
Результаты выявления сдвигов (различий) до и после исследования
| Группа | До/После | Valid | T | Z | p |
| Основная группа | ALT | 40 | 77,0** | 4,3 | 0,000021 |
| AST | 40 | 59,0** | 4,6 | 0,000004 | |
| BIL TOT | 40 | 24,5** | 5,2 | 0,0000002 | |
| GGT | 40 | 6,0** | 5,2 | 0,0000002 | |
| Группа сравнения | ALT | 40 | 55,0** | 4,7 | 0,000003 |
| AST | 40 | 19,5** | 5,2 | 0,0000002 | |
| BIL TOT | 40 | 62,5** | 4,7 | 0,000003 | |
| GGT | 40 | 2,5** | 5,0 | 0,0000005 |
Видимо, объяснение выраженного положительного метаболического эффекта Нооклерина®, проявляющегося в более быстром устранении соматоневрологической, аффективной и астенической симптоматики ААС, следует относить к воздействию на другие звенья метаболизма, не исключено, к его возможной антиоксидантной, мембраностабилизирующей и ноотропной активности. С другой стороны, учитывая исследования других авторов, не исключено, что для выявления статистически значимого влияния Нооклерина® на динамику улучшения лабораторных показателей необходимо более длительное (не менее трех недель) применение препарата с тщательной сравнительной оценкой биохимических показателей крови.
Оценка безопасности препарата
Следует подчеркнуть хорошую переносимость препарата Нооклерин® пациентами при купировании алкогольного абстинентного синдрома легкой и средней степени тяжести. Отдельные жалобы пациентов (2,5—5% б-х) на наличие запоров, тошноты (без рвоты), головокружения, стойкий тремор пальцев рук являлись неспецифическими и, скорее, определялись наличием сопутствующих алкоголизму заболеваний. У этих пациентов в анамнезе есть указания на наличие хронического гастродуоденита, хронического панкреатита, алкогольной болезни печени, артериальной гипертензии и энцефалопатии сложного генеза (сосудистого, токсического, травматического). Во всех случаях улучшение самочувствия с устранением указанных жалоб не сопровождалось отменой препарата.
Заключение
- Препарат Нооклерин® (деанола ацеглумат) при назначении его больным алкогольной зависимостью в период ААС в суточной дозе 2000 мг per os оказывает выраженный терапевтический эффект, устраняя соматоневрологические и аффективные симптомы ААС в более короткие (статистически значимые) сроки в среднем на 1,5—2,5 дня;
- Установлен ноотропный и антидепрессивный эффект Нооклерина®, что подтверждено статистически достоверными показателями снижения симптомов общей астении и депрессии, улучшения когнитивных функций в остром периоде ААС. Активирующее действие Нооклерина® не сопровождается усилением патологического влечения к алкоголю, а приводит к уменьшению и более быстрому устранению тяги к алкоголю;
- Изучение динамики изменений лабораторных показателей, в том числе ферментативной активности печени на протяжении 10 дней исследования не выявило статистически значимых различий в основной группе по сравнению с контрольной, где проводилась стандартная терапия. Однако следует отметить, что на фоне приема Нооклерина® имеется тенденция более быстрой динамике снижения уровня ферментов, что позволяет говорить о положительном воздействии на печень и безопасности его применения;
- Нооклерин® хорошо переносится больными в сочетании с базовой терапией, уменьшает и устраняет дневную сонливость и заторможенность, значительно улучшает общее состояние больных.
Список литературы
- Абдуллаев Т.Ю. Роль патологии печени в клинике алкоголизма: Автореф. дисс. на соискание ученой степени к.м.н. М., 2001.
- Александровский Ю.А., Аведисова А.С., Ястребов Д.В. и др. Применение препарата Нооклерин в качестве антиастенического средства у больных с функциональной астенией // Психиатрия и психофармакотерапия. 2003. ¹4. С. 164—166.
- Аведисова А.С. Новый отечественный ноотроп Нооклерин в терапии астении и других заболеваний // Фарматека. 2005. ¹6. С. 51—54.
- Альтшулер В.Б., Кравченко С.Л., Коньков Е.М. Инструкция по проведению клинических исследований новых лекарственных средств при лечении больных алкоголизмом // Руководство по проведению клинических исследований новых лекарственных средств. Изд-е ФГУ «НЦ ЭСМП» Росздравнадзора М., 2005. С. 255—270.
- Краснослободцева Л.А., Рогачева Т.А., Мельникова Т.С., Лапин И.А. Динамика электроэнцефалографических параметров у больных с органическим поражением головного мозга под влиянием нейрометаболических стимуляторов // Психиатрия. 2008. ¹1. С. 24—30.
- Альтшулер И.Б., Кравченко С.Л., Корольков А.И., Козырева А.В. О клинической эффективности препарата нооклерин (деанола ацеглумат) при лечении больных алкоголизмом // Наркология. 2013. ¹11. С. 3—8.
- Медведев В.Э. Новые возможности лечения астенических расстройств в психиатрической, неврологической и соматической практике // Психиатрия и психофармакотерапия. 2013. Т. 15. С. 2—7.
- Рогачева Т.А., Мельникова Т.С. Динамика электроэнцефалографических показателей у больных эпилепсией под влиянием ноотропной терапии // Социальная и клиническая психиатрия. 2015. Т. 25, ¹2. С. 50—64.
- Dimpfel W., Wedekind W., Keplinger I. Efficacy of dimethylaminoethanol (DMAE) containing vitamin-mineral drug combination on EEG patterns in the presence of different emotional states // Eur. J. Med. Res. 2003. 30. 8 (5). 183—91.
- Malanga G., Aguiar M.B., Martinez H.D., Puntarulo S. New insigbts on dimethylaminoethanol (DMAE) features as a free radical scavenger // Drug Metab. Lett. 2012. 6 (1). 54—9.
NOOCLERIN® (DEANOL ACEGLUMATE) IN PATIENTS WITH ALCOHOL ABSTINENT SYNDROME
Kozhinova T.A., Gofman A.G., Nemkova T.I., Shein V.V., Romashkina N.V. Scientific research in which a preparation Nooclerin® (INN Deanol aceglumate) 40 patients with alcoholic dependence in the period of alcohol abstinent syndrome (AAS) in a daily dose received 2000 mg of per os is conducted. It is proved that the preparation shows nootropic and anti-asthenic action, renders the expressed therapeutic effect, eliminating the main somatic, neurologic and affective symptoms of AAS in shorter (statistically significant) terms in comparison with control group (40 patients receiving standard detox therapy). The activating effect of Nooclerin® isn’t followed by strengthening of pathological thirst for alcohol. Studying of dynamics of changes of laboratory indicators, including enzymatic activity of a liver has revealed positive influence of a preparation on these indicators in the main group.
Keywords: alcoholic dependence, alcoholic abstinence syndrome, therapy, alcoholism, astenia, nootropos, nooclerin, gammaglutamiltransferaza
