Сывороточные липиды при различных стадиях и морфофункциональных типах сердечной недостаточности у больных, перенесших инфаркт миокарда
СтатьиОпубликовано в журнале:
Российский кардиологический журнал »» N2 2005
Молчанов С.Н.1, Люсов В.А.1, Говорин А.В.2, Неверов И.В.2
Российский государственный медицинский университет, кафедра госпитальной терапии №11;
Читинскаямедицинская академия, кафедра факультетской терапии2.
Резюме
С целью изучения содержания жирных кислот и АТФ венозной крови, а также продуктов перекисного окисления липидов обследованы больные с сердечной недостаточностью, перенесшие инфаркт миокарда. Жирные кислоты и АТФ исследовали при различных стадиях сердечной недостаточности, а также наряду с продуктами перекисного окисления липидов при различных морфофункциональных типах. Показано, что с нарастанием тяжести сердечной недостаточности усугубляется нарушение утилизации жирных кислот, темпы которого можно охарактеризовать по коэффициенту ЖК/глицерин. Величина данного коэффициента зависит от тяжести миокардиальной недостаточности и преобладает у пациентов с дилатационным типом поражения миокарда. С нарастанием тяжести сердечной недостаточности снижается синтез АТФ, что находит свое отражение в уменьшении его уровня в периферической крови. По соотношению ЖК/АТФ можно судить о степени тяжести миокардиальной недостаточности; ее наибольшие значения выявлялись у пациентов с дилатационным типом поражения миокарда. Гипертрофический морфофункциональный тип сердечной недостаточности характеризовался меньшим нарушением утилизации жирных кислот и более выраженной активацией перекисного окисления липидов. Выявлены корреляционные связи между рядом биохимических показателей крови, имеющих отношение к энергетическому обмену, и кардиогемодинамическими параметрами.
Ключевые слова: сердечная недостаточность, систолическая и диастолическая дисфункция, морфофункциональный тип, гемодинамика, жирные кислоты.
В исследованиях последних лет показана существенная роль нарушения расслабления и диастолических свойств в развитии и прогрессировании сердечной недостаточности [3]. В большинстве случаев имеет место сочетание нарушений систолической функции миокарда и диастолы левого желудочка (ЛЖ)[14]. Действительно, трудно себе представить изолированное существование систолических или диастолических расстройств, однако преобладание того или иного компонента на различных этапах развития и прогрессирования сердечной недостаточности (СН), вполне возможно. Если гемодинамические параметры изучены достаточно подробно, то метаболические изменения, которые неизменно должны сопровождать систолическую или диастолическую дисфункцию у больных, перенесших инфаркт миокарда(ИМ), практически не исследовались. В то же время, внедрение в клиническую практику широкого спектра цитопротективных метаболических препаратов требует дифференцированного подхода к их назначению, что является одним из условий профилактики и лечения СН.
В связи этим, становится важным изучение биохимических изменений, которые можно было бы использовать в качестве метаболических критериев не только степени тяжести СН, но и ключевых показателей систолических или диастолических нарушений у больных, перенесших ИМ.
Цель исследования – изучение содержания жирных кислот и АТФ венозной крови и продуктов перекисного окисления липидов у больных с постинфарктной сердечной недостаточностью.
Задачи исследования: – изучить взаимосвязь сывороточных липидов и АТФ венозной крови при различных стадиях постинфарктной сердечной недостаточности. – исследовать морфофункциональные типы СН у больных с постинфарктным кардиосклерозом, основываясь на гемодинамических параметрах, полученных при эхокардиографии. – сопоставить комплекс лабораторных показате лей с кардиогемодинамическими параметрами.
Материалы и методы
В работе представлены результаты обследования 185 человек. Основную группу составили 123 больных мужского пола с СН I– III стадий по Н.Д. Стражеско и В.Х.Василенко; средний возраст – 4,7 ± 3,6 года.
Включен в группу с постинфарктным кардиосклерозом без клинических признаков СН 41 больной, в возрасте от 30 до 65 лет (средний возраст – 45,7 ±2,8 года). Стандартизация показателей проводилась на группе из 21 практически здорового человека в возрасте от 30 до 48 лет (средний возраст – 42,3±2,7 года). В исследование не включались больные сахарным диабетом, воспалительными заболеваниями, тяжелой артериальной гипертензей (АГ), а также пациенты с клинической картиной нестабильной стенокардии. Исследование проводилось через 6 мес. и более после перенесенного ИМ. У 123 пациентов основной группы вследствие ИМ развилась СН: I стадия – у 33 человек (26, 82%), IIА стадия – у 27 человека (21, 5%), IIБ – у 42 пациентов (34, 14%) и III стадия – у 21 человека (17, 07%). В прошлом все пациенты перенесли крупноочаговый ИМ: передней локализации – 81 человек (65,8%), нижней локализации – 42 (34,1%). Вследствие трансмурального ИМ у 34 больных сформировалась хроническая аневризма (у 30 – при переднем ИМ, у 4 – при нижнем перенесенном ИМ). Диагноз ИБС ставился на основании достоверных данных о перенесенном ИМ: при клиническом обследовании, по результатам ЭКГ – исследования (критерии Миннесотского кода) и с помощью ЭхоКГ (наличие зон гипо, акинезий и дискинезий в случае формирования аневризмы). Данные клинических лабораторных методов исследования (общий анализ крови, мочи, АСТ, АЛТ,КФК, МВ КФК, ЛДГ), проведенных у больных, были без отклонений. Морфометрические и кардиогемодинамические параметры определяли с помощью ЭхоКГ на аппарате Sim – 5000 фирмы OTE BIOME ICA. Исследования проводили по стандартной методике, в положении лежа на левом боку. По ЭхоКГ ЛЖ определяли конечный систолический размер (КСР) и конечный диастолический размер (КДР); конечный диастолический объем (КДО) и конечный систолический объем (КСО) соответственно, на основании которых рассчитывали ударный объем (УО), фракцию выброса (ФВ). В конце диастолы ЛЖ определяли толщину миокарда задней стенки (ЗС). Масса миокарда ЛЖ (ММЛЖ) рассчитывалась по формуле Troy (170) в модификации Ю.Н. Беленкова (175), затем проводился расчет индекса объем/масса (ИОМ), предложенный А.В.Сумароковым и соавт. [12] (отношение КДО/ММЛЖ). Диастолическую функцию оценивали по трансмитральному потоку и предсердножелудочковому отношению (отношение размера левого предсердия к конечнодиастолическому размеру (РЛП/КДР). В зависимости от величины индекса объем/масса, больные с постинфарктной СН были разделены на три основные группы: 1 группа – с гипертрофическим морфофункциональным типом СН (ГМТ СН) (1,15%), ИОМ менее 0,67 мл/гр.; 2 группа – с дилатационным типом (ДМФТ СН) (31,6%), ИОМ более 0,85 мл/гр.; 3 группа – со смешанным морфофункциональным типом СН (СМТ СН), (48,3%) при среднем значении этого показателя. Содержание общего холестерина (ОХС) определяли методом Илька, триглицериды (ТГ) – с помощью наборов Биалатест («Лахема»), холестерин липопротеидов высокой плотности (ХС ЛПВП) – после осаждения холестерина липопротеидов очень низкой плотности (ХС ЛПОНП) гепарином в присутствии ионов марганца. Показатели холестерина липопротеидов низкой плотности (ХС ЛПНП) и ХС ЛПОНП получали расчетным методом по А.И.Климову (177): ХС ЛПОНП = ТГ/5. ХС ЛПНП = ОХС – (ХС ЛПВП + ХС ЛПОНП). После этого рассчитывали коэффициент атерогенности (КА): ОХС – ХС ЛПВП/ ХС ЛПВП. Жирные кислоты (ЖК) определяли по Konitzer (164), содержание глицерина в сыворотке крови – микрометодом в модификации И.В.Неверова (173). Малоновый диальдегид (МДА) исследовали по Ritabch, активность глутатионпероксидазы (ГТП) в эритроцитах по методу Paglia и Valentine в модификации В.З.Ланкина (176) в сопряженной глутатионредуктазной системе. Определение аденозинтрифосфата (АТФ) в цельной венозной крови проводили ферментным методом по Lamricht и Stein (165). Для оценки тяжести СН рассчитывались коэффициенты: ЖК/глицерин [], ЖК/АТФ [10], МДА/ГTП [4]. Статистический анализ полученных результатов проводили методом вариационной статистики по Стъюденту, ранговой корреляции по Спирмену, достоверность различий для разных групп больных оценивали по критерию Х по Пирсону.
Результаты и обсуждение
Патогенез застойной сердечной недостаточности продолжает привлекать внимание исследователей, так как наряду с классической, систолической, дисфункцией миокарда назрела необходимость изучения роли нарушений заполнения ЛЖ. В ряде случаев возможно наличие у больного преобладающей диастолической дисфункции ЛЖ, клинические проявления которой подобны таковым при классическом течении СН. Выявление у больных диастолической или систолической дисфункции имеет практическое значение, так как терапевтические подходы к ведению этих групп больных различны. Помимо этого, изучение в данном направлении позволит создать теоретические предпосылки для обоснования дифференцированной цитопротективной терапии у больных постинфарктной СН.
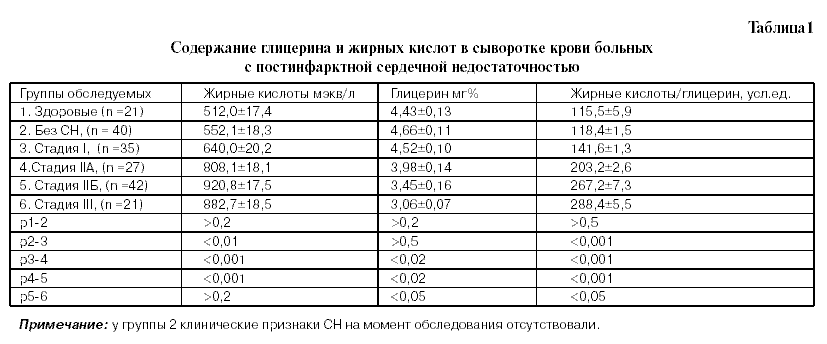
Показатели сывороточных липидов исследованы при различных стадиях постинфарктной сердечной недостаточности (СН) (табл. 1). Уровень ЖК у больных с постинфарктным кардиосклерозом без клинических признаков СН имел тенденцию к повышению и составил 552,1±18,3 мэкв/л, недостоверно отличаясь от показателей здоровых лиц (табл.1). При I стадии постинфарктной СН содержание ЖК существенно увеличивалось, достоверно отличаясь от аналогичного показателя у больных с постинфарктным кардиосклерозом без клинических признаков СН (р<0,01).
В то же время, в группе пациентов со IIА ст. уровень ЖК составил 808,1±18,1 мэкв/л и достоверно отличался (р<0,001) не только от такового у больных постинфарктным кардиосклерозом без клинических признаков СН, но и с I ст. СН (р<0,001). Как видно из данных, представленных в табл. 1, содержание ЖК значительно увеличивалось у больных IIБ ст. постинфарктной СН по сравнению со всеми группами пациентов. Следует отметить, что уровень ЖК при IIА и IIБ ст. также высокодостоверно различался. У больных с терминальной стадией СН содержание ЖК имело тенденцию к уменьшению и составило 882,7±18,5 мэкв/л, недостоверно отличаясь от их уровня у пациентов с IIБ стадией СН.
То есть, уровень ЖК в крови больных постинфарктной СН существенно повышался и зависел от тяжести миокардиальной недостаточности. Известно, что потребление мобилизованных ЖК миокардом в условиях ограниченного коронарного кровотока затруднено, поскольку их утилизация осуществляется только аэробным путем [15]. В этой связи чрезвычайно важно сопоставить увеличение содержания ЖК с уровнем глицерина [8]. Показатели глицерина в крови у больных с СН существенно уменьшались. Его уровень при IIБ и III стадии был существенно ниже, чем у пациентов с I и IIА стадиями СН (табл. 1). Ранее доказано, что после отщепления ЖК глицерин используется для ресинтеза триглицеридов в печени, ферментативно активируясь в альфаглицерофосфат [15]. Уровень свободного глицерина в крови служит показателем активности липолиза триглицеридов, а по соотношению ЖК/глицерин можно судить о тем пах утилизации ЖК [7]. Как видно из данных, представленных в табл.1, коэффициент ЖК/глицерин значительно увеличивается в зависимости от тяжести постинфарктной СН. Наличие четкой закономерности возрастания уровня ЖК, наряду со снижением со держания глицерина в крови и, соответственно, повышением коэффициента ЖК/глицерин, по мере усугубления миокардиальной недостаточности, указывает на нарушение утилизации ЖК миокардом у больных с постинфарктной сердечной недостаточностью, особенно с ее терминальной стадией.
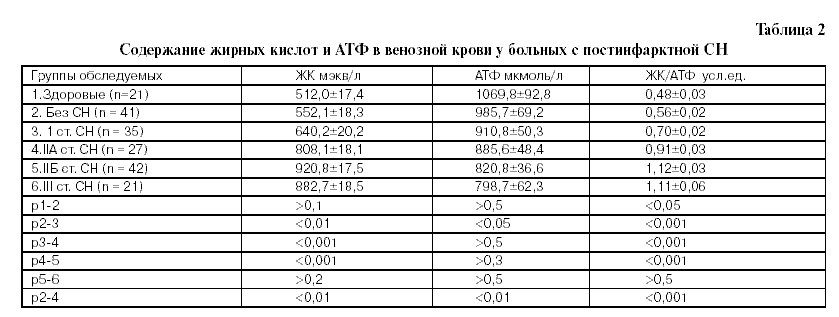
Как было показано, у больных с постинфарктной СН в результате недостатка кислорода и, соответственно, нарушения процессов окислительного фосфорилирования, значительно повышается уровень ЖК в сыворотке крови. Избыточное количество неутилизированных ЖК еще в большей степени повышает потребность миокарда в кислороде и оказывает повреждающее действие на мембраны и ферменты кардиомиоцитов, что способствует существенному снижению образования макроэргов. Уровень АТФ в венозной крови больных с постинфарктной СН изучен в 12 день поступления в стационар. В группе здоровых лиц содержание АТФ составило 106,8±2,8 мкмоль/л (табл. 2). У больных с постинфарктным кардиосклерозом без клинических признаков СН имелась тенденция к снижению содержания АТФ венозной крови по сравнению со здоровыми лицами. В группе пациентов с 1 стадией СН уровень АТФ существенно снижался в отличие от больных с доклинической стадией СН (табл. 2). Как видно из данных, представленных в табл. 2, при IIAIII стадиях СН имелась тенденция к снижению этого показателя в венозной крови, однако достоверности между сравниваемыми группами не отмечено. Наименьший уровень АТФ был выявлен при III стадии СН и составил 78,7±62,3 мкмоль/л.
Учитывая, что нарушение утилизации ЖК на растает по мере утяжеления миокардиальной недостаточности и находится в обратной зависимости от показателей АТФ в сыворотке крови, для оценки выраженности сердечной недостаточности рассчитывался коэффициент ЖК/АТФ. У здоровых лиц онсоставил 0,48±0,03 усл.ед.
Как видно из данных, представленных в таблице 2, коэффициент ЖК/АТФ значительно возрастал по мере усугубления миокардиальной недостаточности и достоверноразличался среди больных с различными стадиями постинфарктной СН (за исключением IIБ – III стадий). Таким образом, по мере нарастания постинфарктной СН, увеличивается содержание ЖК в сыворотке крови, что связано с нарушением их и, соответственно, уменьшением образования макроэргов. Поэтому коэффициент ЖК/АТФ может быть использован как информативный дополнительный тест в оценке тяжести постинфарктной сердечной недостаточности.
У больных постинфарктной СН полученные результаты исследования позволили выделить три типа эхокардиографических изменений в сердце [12] – с преобладанием гипертрофии (ГМФТ СН) (1,15%), с преобладанием дилатации (ДМФТ СН) (31,6%) и смешанный (СМФТ СН) (48,3%). При ГМФТ увеличение массы миокарда ЛЖ, ДМФТ СН – увеличение конечного систолического и диастолического объемов, нарушение сократительной функции миокарда, СМФТ СН – гипертрофическидилатационные признаки (табл. 3).
Первую группу (преимущественно диастолическая дисфункция) составили мужчин с постинфарктным передним крупноочаговым кардиосклерозом в возрасте от 34 до 54 лет. Ранее диагноз ИМ устанавливался по клинической картине, показателям резорбционнонекротического синдрома и электрокардиографическим изменениям. Следует отметить, что у 88,8% больных с постинфарктной СН инфаркту миокарда предществовала артериальная гипертензия. У 7 человек после перенесенного ИМ регистрировались приступы стенокардии 3 функционального класса. Типичный ангинозный приступ удалось ретроспективно установить у всех пациентов. В острый период ИМ у части больных (2 человека) имела место острая левожелудочковая недостаточность (отек легких). В период обследования у всех пациентов сохранялся синусовый ритм. Анализ истории заболевания у больных 1 группы выявил некоторые особенности в клинической картине: чаще встречалась стенокардия напряжения, относительно высокая толерантность к физической нагрузке днем, наличие эквивалентов и приступов сердечной астмы в ночные часы, частое присутствие пресистолического галопа, тяжесть симптомов СН на момент обследования соответствовала III ФК по NYHA (или IIA ст).
Вторую группу (систолическая дисфункция) с преимущественной дилатацией (ДМФТ СН) составили 15 больных в возрасте от 47 до 74 лет с крупноочаговым постинфарктным передним кардиосклерозом.
У этой части пациентов отмечалось редкое предшествование инфаркту миокарда синдрома АГ (2 человека). До развития ИМ у большей части пациентов отмечались приступы стенокардии (12 человек) стабильного течения, однако в послеинфарктном периоде они выявлялись у значительно меньшего количества больных (3 человека). Помимо этого, отмечалось относительно частое наличие в анамнезе астматического варианта ИМ, особенно у лиц с повторным ИМ ( человек). В 53,3% случаев вследствие трансмурального ИМ развилась хроническая аневризма передней стенки ЛЖ, которая не регистрировалась у других групп пациентов. Как и у предыдущей группы больных, в клинической картине СН имелся ряд особенностей: с раннего периода отмечалось наличие астенического синдрома, сердечная недостаточность со ответствовала более тяжелому течению – IIIIV функциональному классу (или IIA ст), имело место частое наличие протодиастолического галопа. Третья группа больных (23 человека) с гипертрофически-дилатационными признаками (систолодиастолические нарушения) ранее также переносилакрупноочаговый передний ИМ. У большей части пациентов (86,5%) заболеванию предшествовала артериальная гипертензия. Приступы стенокардии имели место у 1 человек. Повторный ИМ был у 7 пациентов. На момент обследования у всей группы больных диагностировался IIIII ФК сердечной недостаточности (или IIA ст.). Таким образом, морфофункциональные типы СН у больных, перенесших ИМ, накладывают отпечаток на клинические особенности течения недостаточности кровообращения. Это говорит о целесообразности дифференцированного подхода к изучению патогенеза формирования прогрессирующей недостаточности кровообращения и метаболических изменений при различных эхокардиографических типах поражения миокарда. Наиболее важная роль в регуляции сократительно-расслабительной функции миокарда принадлежит энергетическому обмену. Нарушение энергетического обмена является именно тем начальным и универсальным механизмом развития и прогрессирования СН любой этиологии [5]. В связи с этим, мы изучили показатели жирных кислот и глицерина, а также АТФ венозной крови у больных с различными морфо-функциональными типами постинфарктной сердечной недостаточности.
У пациентов с различными морфофункциональными типами СН отмечалось достоверное увеличение ЖК и уменьшение глицерина в сыворотке крови по сравнению с донорами (p<0,001) (табл. 4). Уровень ЖК при ДМФТ существенно возрастал и достигал своего максимального значения, высокодостоверно отличаясь от такового у больных с преимущественной гипертрофией (ГМФТ тип). У больных с СМФТ СН типом поражения миокарда содержание ЖК в сыворотке крови занимало промежуточное положение.
Содержание глицерина в сыворотке крови у лиц с ДМФТ СН существенно уменьшалось и достигало наименьших значений, достоверно отличаясь от аналогичного показателя у пациентов с гипертрофическим типом (р<0,02). У больных со смешанным поражением миокарда содержание глицерина соответствовало промежуточному положению (табл. 4). Как уже было отмечено, по соотношению ЖК/глицерин можно судить о темпах утилизации ЖК []. Коэффициент значительно увеличивался у всех пациентов, достигая наибольших значений при преимущественной дилатации ЛЖ, и достоверно различался среди всех групп больных. Наличие четкой закономерности возрастания ЖК, наряду со снижением глицерина в крови и, соответственно, повыше нием коэфициента ЖК/глицерин, по мере увеличения дилатации ЛЖ и систолической дисфункции, свидетельствует о более выраженном нарушении утилизации ЖК у пациентов с дилатационным типом постинфарктной СН.
Высокий уровень ЖК у больных с постинфарктной СН в условиях ограниченного коронарного кровотока приводит к нарушению их утилизации, что разобщает окислительное фосфорилирование и снижает образование макроэргов [15]. Преобладание синдрома нарушения утилизации ЖК у пациентов с преимущественной дилатацией, вероятно, способ ствует меньшему синтезу АТФ, а также увеличению атерогенных фракций липопротеинов.

Содержание АТФ венозной крови у всех больных снижалось по сравнению с контрольной группой (табл.4), причем наиболее низкие его показатели выявлены у пациентов с ДМФТ СН. Уровни АТФ у больных с ГМФТ и СМФТ СН были несколько больше и недостоверно отличались друг от друга.
Соотношение ЖК/АТФ, характеризующее степень миокардиальной недостаточности значительно увеличивалось при всех типах СН [10]. Максимальные показатели данного коэффициента выявлены у пациентов с ДМФТ. Ранее установлено, что с нарушением процессов энергообразования и накопления в миокарде предшественников синтеза АТФ его систолическая функция страдает в большей степени; в свою очередь, диастолической дисфункции миокарда предшествует нарушение утилизации синтезированного АТФ [13].
Наиболее выраженное нарушение утилизации ЖК миокардом отмечено у больных с ДМФТ СН, где страдает, в основном, систолическая функция. Это приводит к наибольшей депрессии синтеза АТФ у пациентов с данным типом поражения миокарда, а коэффициент ЖК/АТФ, характеризующий степень миокардиальной недостаточности, вероятно, можно обозначить как показатель «неиспользованых» ЖК в процессе синтеза АТФ. Значительно преобладая у больных с дилатационным типом, коэффициент ЖК/АТФ указывает на более неблагоприятное течение и прогноз этой категории больных.
Итак, у больных с постинфарктной СН в сыворотке крови существенно повышается степень выраженности синдрома нарушения содержания ЖК, утилизация которых значительно преобладает у пациентов с выраженной дилатацией и систолической дисфункцией. Высокий уровень ЖК в условиях коронарной недостаточности приводит к нарушению их использования что, в конечном итоге, снижает образование макроэргов. При преобладании гипертрофии миокарда и диастолических нарушений процессы превращения ЖК посредством Вокисления и цикла Кребса нарушаются в меньшей степени, в отличие от пациентов с выраженной дилатацией ЛЖ и систолической дисфункцией.
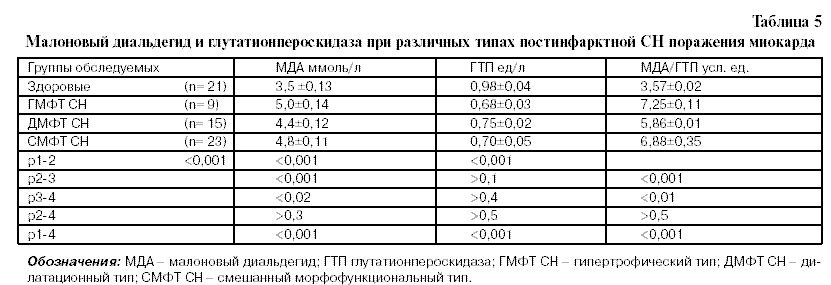
Основные свойства сердечной мышцы в значительной мере зависят от состояния мембран и активности ферментов клеток миокарда. Одним из альтерирующих механизмов биомембран и ферментов является интенсификация перекисного окисления липидов (ПОЛ). Чрезмерная активация ПОЛ обуславливает повреждение белковых и липидных компонентов мембран, а также мембрансвязанных ферментов клеток. Учитывая это, изучалось содержание малонового диальдегида (МДА) и глутатионпероксидазы (ГТП) в крови у больных с различными морфофункциональными типами поражения миокарда. Как видно из табл. 5, уровень МДА венозной крови увеличивался у всех больных, по сравнению с контрольной группой, достигая наибольших величин у пациентов с ГМФТ поражения миокарда. При ДМФТ и смешанном поражении миокарда показатели МДА имели меньшее значение (p<0,001). Активность ГТП эритроцитов у всех категорий больных оказалась снижена по сравнению со здоровыми лицами (p<0,001), причем наиболее выраженное ее уменьшение отмечалось у пациентов с ГМФТ СН и диастолическими нарушениями. Наибольшие различия между сравниваемыми группами отмечены по коэффициенту МДА/ГТП, являющимся интегральным показателем процессов ПОЛ при ИБС [4]. Максимальное его значение выявлялось при гипертрофическом типе поражения миокарда (табл. 5), достоверно отличаясь от такового у других групп больных.
Таким образом, морфофункциональные типы постинфарктной СН характеризуются неодинаковой степенью активации процессов ПОЛ. Преобладание гипертрофии ЛЖ и диастолической дисфункции сопровождается наиболее выраженной их интенсификацией; напротив, при дилатации активация ПОЛ не столь значительна, несмотря на высокое содержание ЖК. Как известно, усиление процессов ПОЛ способствует повышению поступления Са внутрь клетки, что может способствовать развитию гипертрофии миокарда [1]. Помимо этого, выраженность депрессии антиоксидантной системы является фактором, способствующим гипертрофии ЛЖ [2].
Нами проведен анализ взаимосвязи изменений в содержании сывороточных липидов и продуктов ПОЛ с некоторыми параметрами гемодинамики. (табл. 6). Как видно из данных, представленных в таблице, между конечным диастолическим объемом и уровнем ЖК в крови выявлена прямая тесная корреляционная связь (r = 0,72; р < 0,01), что указывает на существенную взаимозависимость нарушения утилизации ЖК и систолической дисфункции. Кроме этого, КДО отрицательно коррелировал с содержанием АТФ (r = –0,66; р < 0,05). Это позволяет предположить, что у больных с илатацией ЛЖ нарушение утилизации ЖК приводит к значительному снижению синтеза АТФ. Между активностью ГТП и гемодинамическими параметрами корреляционной связи выявить не удалось.
Между УО, ФВ и содержанием АТФ в венозной крови отмечалась положительная (r = 0,58УО и r =0,52; р < 0,05) и отрицательная (r = – 0,66; р < 0,05) корреляционная связь между УО и ЖК. Итак, выявленные корреляции между ЖК, АТФ, МДА, активностью ГТП и гемодинамическими параметрами указывают на тесную взаимозависимость биохимических показателей крови и систолодиастолической функцией миокарда. Как известно, ЖК являются основным энергетическим субстратом сердечной мышцы [15].
В результате терминального окисления синтезируется необходимое для клеток количество АТФ. Наличие корреляционных взаимоотношений позволяет предположить, что преобладание дилатации и систолической дисфункции миокарда сопровождается недостаточным использованием ЖК как энергетического субстрата, в результате чего в сердечной мышце снижается количество синтезированного АТФ. Напротив, при преобладающей гипертрофии и диастолической дисфункции продукция АТФ достаточна, но, вероятно, аденозинтрифосфат недостаточно используется в активном расслаблении миокарда.
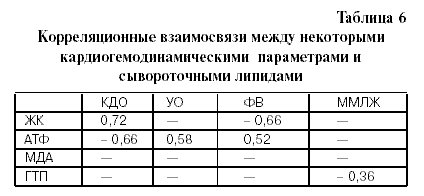
В литературе, как указывалось, имеются сообщения о существенном влиянии активации процессов ПОЛ на развитие гипертрофии ЛЖ [3]. Интенсификация ПОЛ способствует повышению проницаемости мембран кардиоцитов, в результате чего увеличивается поступление ионов Са внутрь клетки, что рассматривается в качестве одного из причинных факторов формирования гипертрофии ЛЖ [5]. Помимо этого, депрессия антиоксидантной системы сама по себе ведет к увеличению массы миокарда ЛЖ. Имеющиеся корреляционные связи между ММЛЖ и ГТП позволяют предполагать значительное влияние процессов ПОЛ на степень гипертрофии ЛЖ и способ ствование диастолическим нарушениям. Также не исключено, что активация ПОЛ и депрессия антиоксидантной системы ведет к инактивации АДФАТФ транслоказы и миозинАТФазы и, оответственно, к нарушению утилизации АТФ, синтезированного в достаточном количестве. Эти процессы могут лежать в основе одного из механизмов диастолической дисфункции ЛЖ при постинфарктной СН. Выявленные взаимосвязи между рядом биохимических показателей и кардиогемодинамическими параметрами позволяют предполагать возможность корригирующей терапии, направленной на те метаболические изменения, которые возникают при различных типах постинфарктной СН.
Выводы
1. У больных с постинфарктной сердечной недостаточностью установлены закономерные изменения сывороточных липидов, процессов перекисного окисления липидов и содержания АТФ венозной крови, характеризующие патогенетические механизмы миокардиальной недостаточности.
2. Общий характер изменений сывороточных липидов обусловлен увеличением содержания ЖК с нарушением их утилизации, снижением содержания в венозной крови АТФ. Степень изменений сывороточных липидов, уровня АТФ венозной крови зависит от тяжести постинфарктной сердечной недостаточности.
3. У пациентов с постинфарктной сердечной недостаточностью выявлены различные морфофункциональные типы поражения сердца: у 1,15% – гипертрофический, у 31,6% – дилатационный и у 48,3% – смешанный. При гипертрофическом типе нарушения кардиогемодинамики связаны с диастолической дисфункцией, при дилатационном – с нарушением систолической функции миокарда; смешанный тип поражения сердечной мышцы характеризовался нарушением как систолической, так и диастолической функций миокарда.
4. Характер изменений сывороточных липидов и процессов ПОЛ зависит от морфофункционального типа поражения миокарда; при гипертрофическом морфофункциональном типе выявлена преимущественная активация процессов перекисного окисления липидов; дилатационный морфофункциональный тип постинфарктной сердечной недостаточности характеризуется выраженным нарушением утилизации ЖК, низкими цифрами АТФ и более низкими показателями перекисного окисления липидов крови; при смешанном морфофункциональном типе отмечено как нарушение утилизации ЖК, так и активация процессов ПОЛ.
Литература
1. Атаханов Ш.Э., Reswick L.M., -evereux R.B. и др. Кальциевый метаболизм и функциональная активность тромбоцитов у больных с гипертоническим сердцем//Кардиология. –1992. - № 1. – С. 66-67.
2. Бобров В.А., Поливода С.Н. Состояние перекисного окисления мембран и антиоксидантной обеспечинности на различных стадиях формирования «гипертензивного сердца»//Кардиология.- 1992.- №3.- С.42-44.
3. Беленков Ю.Н., Агеев Ф.Т., Мареев В.Ю. Знакомьтесь: диастолическая сердечная недостаточность //Сердечная недостаточность. – 2000 - № 1. – С.40-44.
4. Говорин А.В. Нестабильная стенокардия: вопросы патогенеза и принципы фармакотерапии с учетом психопатологических нарушений/ Дис. докт. Мед. Наук. – М., 1992. – 293 с.
5. Меерсон Ф.З. Компенсаторная гипертрофия, гиперфункция и недостаточность сердца. – В кн.: Руководство по кардиологии. – М.: Медицина, 1982. – Т.1. – с.306-330.
6. Моисеев В.С., Шатковский Н.П., Чельцов В.В. Дифференцированное применение вазодилататоров при сердечной недостаточности различного характера //Клин. медицина. – 1993.- №4. – с. 21-25.
7. Неверов И.В., Беляк Л.А., Глашкова Р.П. Жирные кислоты и липиды сыворотки крови в остром периоде инфаркта миокарда//Тер. архив. – 1978.- №9.- с. 125-128.
8. Неверов И.В., Новиков В.Т., Сайдулаева М.Р. Изменения содержания АТФ, АДФ и липидов при различных клинических вариантах ИБС// – Сов. мед. – 1980. - №10.- с. 9-12.
9. Неверов И.В., Новиков В.Т., Спинова Р.П. и др. Содержание жирных кислот и адениннуклеотидов в крови при сердечной
недостаточности у больных ИБС // Клин. Мед.- 1985.- №12.- с.86-89.
10. Неверов И.В., Спинова Р.П., Алиев А.В. Способ определения тяжести стенокардии у больных ИБС// Авт. Свид. №1515110.
– 1988, СССР.
11. Спинова Р.П. Клиническое значение изменений содержания адениннуклеотидов и жирных кислот в крови у больных сердечной недостаточностью/Автореф.. кан. мед. наук. М., 1986. 23с.
12. Сумароков А.В., Стяжкин В.Ю., Нелумба Ж. и др. Некоторые закономерности в развитии хронической сердечной недостаочности при различных морфофункциональных типах поражения миокарда //Тер. Архив.- 1987.- №5.- с.37-41.
13. Шердукалова Л.Ф., Аганжапова И.П., Минасян А.Г. О взаимосвязи энергетической и сократительной функции миокар-
да//Кардиология. – 1991.- №1.- с.62-64.
14. Штегман О.А., Терещенко Ю.А. Систолическая и диастолическая дисфункция левого желудочка – самостоятельные типы сердечной недостаточности или две стороны одного процесса // Кардиология. – 2004.- №2.- с.82-86.
15. Opie L.H. Myocar-ial ischemia – metabolism an- its mo-ificasion//S. Art. me-. J.- 1987.- Vol. 72.- №11.- р.740-747.
Abstract
Venous bloo levels of fatty acis (FA), ATP, an lipi peroxiation proucts, were examine in heart failure (HF) patients after myocarial infarction. These levels were measure at various stages an in various morphofunctional types of HF. In more severe HF, FA metabolism was more isturbe, that coul be assesse by FA/glycerin coefficient, marker of myocarial insufficiency. In severe HF, ATP synthesis ecline, an its level in peripheral bloo reuce. By FA/ATP ratio, severity of myocarial insufficiency coul be assesse; its greater figures were observe in ilate cariomyopathy. Hypertrophic morphofunctional HF type was characterize by less isturbe FA utilization an more pronounce activation of lipi peroxiation. Concentrations of bloo biochemical markers, reflecting energy metabolism, correlate with cariac hemoynamicsparameters.
Keywors: Heart failure, systolic an iastolic ysfunction, morphofunctional type, hemoynamics, fatty acis.
Поступила 17/12/2004
