Современные аспекты диагностики и лечения дегенеративных заболеваний позвоночника и суставов
СтатьиОпубликовано в журнале:
Фарматека № 20 — 2005 1
Н.А. Шостак, А.А. Клименко
Кафедра факультетской терапии им. академика А.И. Нестерова, Москва
ГОУ ВПО РГМУ Росздрава, Москва Реферат
Остеоартроз (ОА) – хроническое прогрессирующее заболевание суставов, характеризующееся первичной дегенерацией суставного хряща с последующим изменением субхондральной кости и развитием краевых остеофитов и сопровождающееся реактивным синовитом. Обсуждаются этиология и патогенез ОА. Рассматриваются клиническая картина и принципы диагностики ОА, в первую очередь спондилоартроза. Представлены современные подходы к лечению ОА. Обосновывается целесообразность применения при ОА препаратов хондроитина сульфата, в частности мази Хондроксид. В клинических исследованиях доказана ее эффективность при синдроме нейродистрофической люмбоишиалгии, обусловленном поясничным спондилоартрозом, а также при ОА I–II стадии периферических суставов. Указывается на целесообразность комбинирования препаратов хондроитина сульфата с нестероидными противовоспалительными средствами.
Остеоартроз (ОА) – хроническое прогрессирующее заболевание суставов, характеризующееся первичной дегенерацией суставного хряща с последующим изменением субхондральной кости и развитием краевых остеофитов и сопровождающееся реактивным синовитом.
ОА – самое распространенное заболевание суставов, поражающее как мужчин, так и женщин. Чаще оно развивается у мужчин в возрасте до 45 лет и женщин в возрасте старше 55 лет [2, 3, 12]. Распространенность ОА одинакова у лиц обоего пола старше 70 лет, и в этом возрасте заболевание встречается практически у каждого. Риск утраты трудоспособности в связи с ОА так же велик, как при сердечно-сосудистой патологии, и выше, чем при любых других заболеваниях у лиц пожилого возраста. В недавнем отчете ВОЗ о социальных последствиях заболеваний указывается, что ОА коленных суставов выходит на 4-е место среди причин нетрудоспособности у женщин и на 8-е – у мужчин [9, 11].
Этиология и патогенез ОА
В развитии ОА существенную роль играют общие конституциональные (старение, пол, ожирение, наследственность, репродуктивные особенности) и неблагоприятные механические (травмы, профессиональные и бытовые вредности, осанка) факторы [12]. Высокая распространенность ОА обусловлена генетическими факторами, что подтверждается высоким индексом наследования заболевания (0,39–0,65 среди близнецов) независимо от предрасполагающих факторов внешней среды или демографических особенностей [12].
Различают первичный и вторичный ОА [2, 9, 13]. Первичный (идиопатический) ОА развивается в периферических суставах, наиболее часто в дистальных и проксимальных межфаланговых суставах кистей (с образованием узелков Гебердена и Бушара), первом запястно-пястном, первом плюснефаланговом, тазобедренном и коленном суставах, межпозвоночных дисках и суставах позвоночника, особенно шейного и поясничного отделов.
В зависимости от распространенности процесса выделяют 2 формы первичного ОА:
- локальная форма характеризуется поражением одного или двух суставов (ОА суставов кистей, стоп; коленного, тазобедренного суставов; спондилоартроз);
- для генерализованной формы характерно поражение 3 и более суставов или группы суставов (проксимальные межфаланговые суставы оценивают как одну группу, а дистальные межфаланговые суставы – как другую).
Вторичный ОА развивается в результате травмы, врожденной дисплазии опорно-двигательного аппарата, эндокринных заболеваний (акромегалия, гиперпаратиреоз), метаболических нарушений (охроноз, гемохроматоз, подагра) и другой костно-суставной патологии (ревматоидный артрит, инфекционные артриты, асептические некрозы костей).
Ведущими патогенетическими факторами при ОА являются дегенерация и деструкция суставного хряща, развивающиеся вследствие несоответствия между механической нагрузкой на суставную поверхность хряща и его способностью выдерживать эту нагрузку [4, 5, 8]. Изменение суставного хряща может быть обусловлено как врожденными и приобретенными внутренними факторами, так и воздействием окружающей среды. Наиболее выраженные патоморфологические изменения при артрозе происходят в хрящевом матриксе. Они приводят к развитию прогрессирующей эрозии хряща и разрушению коллагеновых волокон II типа, а также к деградации протеогликановых макромолекул. В основе нарушения метаболизма хряща лежат количественные и качественные изменения протеогликанов – белковополисахаридных комплексов, обеспечивающих стабильность структуры коллагеновой сети, которая служит основой хрящевого матрикса. Повреждение хряща при артрозе является результатом повышенного синтеза и высвобождения из хондроцитов коллагеназы и стромелизина (металлопротеаз), разрушающих протеогликаны и коллагеновую сеть. Увеличение в пораженном хряще синтеза коллагеназы и стромелизина, которое может быть генетически обусловленным и находится под контролем цитокинов, высвобождаемых из синовиальной мембраны, ведет к дальнейшей деградации матрикса хряща.
Металлопротеазы синтезируются в форме проэнзимов, которые предположительно активируются под влиянием активаторов протеаз. Активатором металлопротеаз является плазмин. В культуральных фрагментах хряща от больных ОА уровень плазмина возрастает за счет урокиназной формы плазминогенного активатора. Одновременно уровень ингибиторов плазминогенного активатора у больных ОА значительно уменьшается, что приводит к нарастанию трансформации плазминогена в плазмин. Плазмин, в свою очередь, превращает прометаллопротеазы в активные энзимы, разрушающие хрящ. С распадом хряща фрагменты коллагена и протеогликана, а возможно, и другие компоненты матрикса попадают в синовиальную жидкость и инициируют либо усиливают воспалительную реакцию в синовиальной ткани. Они могут также стимулировать выработку воспалительных пептидов либо, являясь антигенами, индуцировать аутоиммунный ответ организма или повреждать хондроциты непосредственно.
Воспаление в суставе связано также с уровнем цитокинов, которые часто обнаруживаются в синовиальной жидкости больных ОА. Цитокины, в частности интерлейкин 1, стимулируют хондроциты и способствуют возрастанию синтеза металло- и сериновых протеаз. Кроме того, цитокины способны тормозить продукцию наиболее физиологичных ингибиторов энзимов и блокировать синтез основных элементов матрикса – коллагена и протеогликанов. Снижение уровня ингибиторов и возрастание содержания энзимов приводит к увеличению суммарной активности протеаз, что в комбинации с угнетением синтеза матрикса ведет к дегенерации хряща и развитию ОА.
В последние годы разрабатывается концепция вязкоэластической защиты сустава: упруговязкие свойства синовиальной жидкости зависят от содержания в ней гиалуроната [4]. Способность поглощать и удерживать воду определяет физиологическую роль гиалуроновой кислоты, которая заключается в обеспечении защиты, смазки и механической стабилизации коллагеновой сети и клеток в тканях сустава и на его поверхности. При ОА в суставе нарушается реологический гомеостаз, который связан с вязкоэластическими свойствами среды сустава и обеспечивает условия для его нормального функционирования.
Морфологически при ОА хрящ из прочного, эластичного и голубого превращается в сухой, желтый, тусклый с шероховатой поверхностью. На ранней стадии ОА в местах максимальной нагрузки, как правило, формируются локальные зоны размягчения хряща, на более поздних стадиях происходит фрагментация, в хряще образуются вертикальные трещины. Местами хрящ обызвествляется. Растрескивание хряща приводит к изъязвлению с обнажением подлежащей кости и отделением фрагментов, которые поступают в полость сустава в виде детрита. При истонченном хрящевом покрове распределение давления между суставными поверхностями становится неравномерным. Это ведет к локальным перегрузкам, нарастанию трения между суставными поверхностями.
Клиническая картина и диагностика ОА (спондилоартроза)
Основными клиническими проявлениями ОА являются боль, деформация и тугоподвижность суставов.
Кардинальный клинический симптом ОА – боль в пораженных суставах. Боль носит неоднородный характер и имеет разнообразные механизмы возникновения (табл. 1).
Таблица 1. Предполагаемые причины боли при ОА
| Ткань | Механизм боли |
|---|---|
| Субхондральная кость | Медуллярная гипертензия, микропереломы,воспаление |
| Остеофиты | Травматизация нервных окончаний в периостиуме |
| Связки | Растяжение |
| Энтезисы | Воспаление |
| Суставная капсула | Воспаление, растяжение |
| Околосуставные мышцы | Спазм |
| Синовиальная оболочка | Воспаление |
При ОА описывают 4 основных типа боли:
- “Механический тип боли” характеризуется возникновением под влиянием дневной физической нагрузки и стиханием за период ночного отдыха; связан со снижением амортизационных способностей хряща и костных подхрящевых структур. Это самый частый тип боли при ОА.
- Непрерывные тупые ночные боли чаще в первой половине ночи связаны с венозным стазом в субхондральной спонгиозной части кости и повышением внутрикостного давления.
- Кратковременные (15–20 минут) “стартовые боли” возникают после периодов покоя и проходят на фоне двигательной активности; обусловлены трением суставных поверхностей, на которых оседает детрит – фрагменты хрящевой и костной деструкции. При первых движениях в суставе детрит выталкивается в завороты суставной сумки – “суставная мышь”.
- Постоянные боли обусловлены рефлекторным спазмом близлежащих мышц, а также развитием реактивного синовита.
Для синовита, помимо боли в суставе (как при движении, так и в покое), характерны утренняя скованность, припухлость сустава, локальное повышение кожной температуры. По мере прогрессирования заболевания рецидивы синовита учащаются. Постепенно развиваются деформация и тугоподвижность суставов за счет фиброзно-склеротических и гипотрофических изменений параартикулярных тканей. На ранней стадии ОА нарушения функции сустава обусловлены болевым синдромом и рефлекторным спазмом мышц. При прогрессировании заболевания на снижение объема движений влияют сухожильно-мышечные контрактуры, остеофиты и нарушение конгруэнтности суставных поверхностей [9, 11].
Наиболее значимым в диагностике ОА является рентгенологическое исследование опорно-двигательного аппарата. В настоящее время выделяют:
- обязательные рентгенологические симптомы:
а) сужение суставной щели;
б) остеофиты;
в) субхондральный остеосклероз; - необязательные рентгенологические симптомы:
а) околосуставной краевой дефект костной ткани;
б) субхондральные кисты;
в) внутрисуставные обызвествленные хондромы.
Клиническая картина ОА определяется конкретным суставом, вовлеченным в патологический процесс [9].
Спондилоартроз – это разновидность ОА с локализацией дегенеративного процесса в межпозвоночных суставах, являющихся обычными синовиальными суставами с двумя суставными поверхностями, покрытыми гиалиновым хрящом. В настоящее время доказано, что процессы дегенерации хряща при ОА и спондилоартрозе развиваются по однотипному сценарию [1, 7, 10].
Спондилоартроз – самая частая причина болей в пояснице у лиц пожилого возраста. При артрозе фасеточных суставов боль обычно двухсторонняя, локализуется в отличие от дискогенной паравертебрально, а не по средней линии, усиливается при длительном стоянии и разгибании и уменьшается при ходьбе и сидении [1, 7].
Позвоночный столб выполняет две основные задачи, которые с точки зрения механики кажутся диаметрально противоположными. С одной стороны, позвоночный столб должен быть гибким. С другой стороны, он должен быть жестким и негнущимся, особенно при нагрузке, для того чтобы поддерживать анатомические отношения и защищать нервные элементы. Одна из первых моделей, описывающая создание прочности позвоночника, была развита Panjabi [10]. Согласно этой модели, прочность позвоночника возникает, когда нервная подсистема получает движение, нагрузку и позиционную информацию от рецепторных органов, расположенных в суставах, мышцах и связках [10]. Нервная подсистема определяет специфические требования для контроля положения и движения и активирует мышечную систему. Координация и интеграция центральной (нервной), пассивной (костно-связочной) и активной (мышечной) подсистем обеспечивает сбалансированные реакции, направленные на то, чтобы позволить позвоночному столбу справиться с его двойной ролью. Эти компоненты и их функции кратко представлены в табл. 2.
Таблица 2. Модель прочности позвоночника по Panjabi
| Подсистема | Компоненты | Функции |
|---|---|---|
| Пассивная (костно-связочная) | Позвонки, межпозвоночные диски, межпозвонковые суставы, связки позвоночника, суставные капсулы | Прочность по направлению к крайним амплитудам. Передача информации о позе и нагрузке |
| Активная (мышечная) | Мышцы позвоночника | Генерация силы. Движение. Прочность |
| Контрольная (нервная) | Чувствительные/двигательные рецепторы, локализованные в мышцах, связках, сухожилиях | Обрабатывают информацию от активной и пассивной систем. Координация прочности и движения |
Эти мышечные ответы управляемы контрольными механизмами центральной нервной системы, главным образом, спинальными рефлексами. Костно-связочная структура создает основу, на которой предыдущие системы будут действовать, и это с помощью системы обратной связи обеспечивает информацией о позе и нагрузке. Мышечная система обеспечивает первую линию “защиты” от нефизиологических движений позвоночника. Эта “защита” координируется нервной системой.
Выделение функциональной двигательной единицы позвоночного столба – позвонково-двигательного сегмента (ПДС) – позволяет оценить объем движений на уровне каждого сегмента [10]. Движения в ПДС осуществляются за счет дугоотростчатых суставов и межпозвонковых дисков. Очевидно, что движения в ПДС различны на протяжении позвоночника не только по объему, но и происходят в разных плоскостях. Это объясняется особенностями анатомического строения и пространственной ориентации межпозвонковых суставов.
Доказано, что в дегенеративно-измененном ПДС происходит синтез противоспалительных цитокинов (интерлейкины 1 и 6, фактор некроза опухоли с формированием “неврогенного воспаления”. Этот патогенетический компонент формирования боли является одним из основополагающих при спондилоартрозе. Однако практически на появление болевой импульсации всегда откликаются мышцы, отвечая тонической рефлекторной реакцией, а их избыточное напряжение при длительном болевом синдроме приводит к дисфункции миофасциальных тканей и усугублению боли. Сокращенная мышца выделяет метаболиты, которые в нормальных условиях вымываются кровью. При длительном мышечном спазме нарушается кровоток, и накопленные метаболиты активируют болевые рецепторы. Боль, вызванная локальным мышечным спазмом, сама по себе может являться стимулом, провоцирующим спазм. Из вышесказанного следует, что болевой синдром при спондилоартрозе всегда осложняется формированием рефлекторных мышечно-тонических реакций. Локализация боли при мышечно-тонических синдромах связана с подвергшимся ирритации корешком и особенностями вторичного поражения нервных стволов по компрессионно-ишемическому типу на уровне спазмированных мышц.
Мышечный спазм, возникающий как проявление спондилоартроза, представляет собой базовый патогенетический механизм болевого синдрома, обеспечивающий его поддержание по принципу порочного круга.
Таким образом, существуют 3 основных звена патогенеза болевых синдромов в области позвоночника при спондилоартрозе:
- Раздражение ноцицепторов, расположенных в капсулах суставов, связках, мышцах позвоночника, периосте позвонков, в наружной трети фиброзного кольца межпозвоночного диска, в стенках артериол, вен, а также в сосудах паравертебральных мышц с образованием очагов миоостеофиброза, играющих роль пусковых зон боли, т. е. триггерных зон, формирующих миофасциальный синдром.
- Раздражение ПДС и развитие неврогенного асептического воспаления.
- Мышечный спазм, возникающий в результате накопления метаболитов, в частности молочной кислоты, выделяемой сокращенной мышцей (в нормальных условиях эти метаболиты вымываются кровью, но при продолжающемся мышечном спазме местный кровоток нарушается, и накопленные метаболиты активируют болевые рецепторы).
Классическим методом диагностики ОА позвоночника, помимо оценки клинических проявлений, является рентгенологическое обследование больных. В зарубежных исследованиях рентгенологические параметры при спондилоартрозе часто оцениваются по классификации Kellgren, согласно которой выделяются 4 градации – от 1 (отсутствие остеофитов) до 4 (большие остеофиты, склероз замыкательных пластинок, снижение высоты межпозвонкового диска вплоть до его исчезновения).
Магнитно-резонансная томография (МРТ) является одним из самых современных методов исследования, помогающим точно установить уровень и тяжесть поражения суставов при ОА [4]. Данная методика обладает целым рядом достоинств: хорошее контрастирование мягких тканей, свободный выбор плоскости изображения, трехмерный характер получаемой информации, отсутствие лучевой нагрузки и артефактов от костных структур, воздуха. МРТ обеспечивает контрастность в изображении хрящевого слоя, позволяет идентифицировать поверхностные изменения различных размеров и отклонения в обмене веществ (рис. 1).
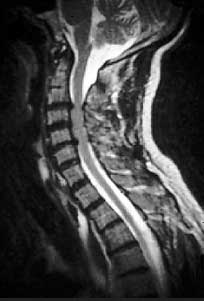
Рис. 1. Спондилоартроз. Стеноз позвоночного канала из-за протрузии межпозвонкового диска в шейном отделе позвоночника (МРТ)
У большинства пациентов со спондилоартрозом, даже при умеренной его симптоматике, при МРТ и компьютерной томографии обнаруживаются значительные дегенеративные изменения фасеточных суставов. Остеоартроз фасеточных суставов может способствовать развитию стеноза позвоночного канала и компрессиинервных корешков (рис. 2). В этом случае могут появиться симптомы люмбоишиалгии, такие как боль, онемение и слабость в ноге [1].
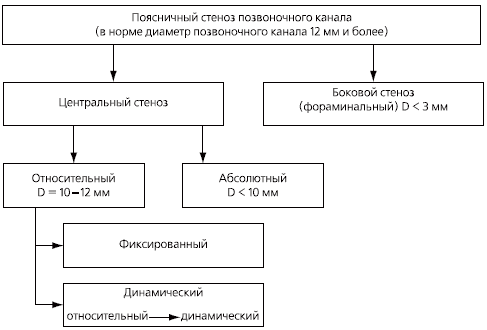
Рис. 2. Виды позвоночного стеноза в поясничном отделе позвоночника
Лечение ОА
Современные подходы к лечению ОА призваны уменьшить патологическую симптоматику, для чего используются следующие методы [3, 11, 13]:
- нефармакологические (образовательные программы, физические упражнения, изменение образа жизни);
- фармакологические (парацетамол, нестероидные противовоспалительные средства – НПВС, местное лечение);
- инвазивные (внутрисуставные и периартикулярные инъекции, лаваж, артропластика).
Основными задачами проводимого лечения являются:
- уменьшение болевого синдрома;
- улучшение функции пораженного сустава, уменьшение степени и снижение частоты нетрудоспособности;
- предотвращение или замедление прогрессирования заболевания и его осложнений.
Медикаментозное лечение ОА направлено на купирование признаков воспаления и болевого синдрома, улучшение внутрикостного и регионарного кровотока, стимуляцию метаболических процессов в организме.
Парацетамол – пероральный анальгетик, с которого должно начинаться лечение ОА, и в случае его эффективности продолжаться в течение длительного времени. Этот препарат может использоваться для самостоятельного лечения легкой и умеренной боли.
НПВС следует назначать пациентам, не ответившим на терапию парацетамолом. У больных с повышенным риском гастроинтестинальных осложнений необходимо комбинировать прием НПВС с гастропротективными средствами.
“Золотым” стандартом среди НПВС считается диклофенак – производное арилуксусной кислоты в виде натриевой и калиевой солей, сочетающий в себе высокую эффективность и безопасность. Для всех препаратов группы диклофенака показано отсутствие отрицательного влияния на метаболизм суставного хряща и, следовательно, межпозвонкового диска, относящегося к хрящевой ткани. При остром течении дорсалгии высокоэффективно применение как пероральных, так и локальных форм препарата. Существует множество лекарственных форм диклофенака для внутривенного и внутримышечного введения, а также для наружного и ректального использования.
Суппозитории ректальные и гель Дикловит, содержащие в качестве активного действующего вещества диклофенак, используются как болеутоляющие и противовоспалительные препараты. Обезболивающий эффект Дикловита, так же как и его противовоспалительная активность, связан в основном с блокированием синтеза простагландинов в периферических тканях. Дикловит подавляет экссудативную и пролиферативную фазы воспаления. При этом снижается образование простагландинов и простациклинов в очагах воспаления, предупреждается образование свободных радикалов из циклических эндоперекисей и перекисей липидов в клеточных мембранах, что приводит к ограничению воспаления.
Эти свойства Дикловита целесообразно использовать при лечении острой и обострении хронической дорсалгии, а также при поражении периферических суставов, обусловленном ОА. В острую фазу процесса рекомендуется использование Дикловита в форме ректальных суппозиториев – по 1 свече (50 мг) 2 раза в сутки – с последующим переходом на Дикловит в форме геля. При этом небольшое количество геля (2–4 г, что соответствует полоске геля 1–2 см) наносят 2–3 раза в сутки тонким слоем на участок кожи над очагом воспаления и слегка втирают до полного всасывания. Курс лечения должен составлять не менее 10 дней.
Опиоидные анальгетики (с парацетамолом или без него) могут применяться у больных, которым противопоказаны НПВС или если НПВС неэффективны и/или плохо переносятся.
Симптоматические препараты замедленного действия для лечения ОА (symptomatic slow acting drug in osteoarthritis – SYSADOA) – генерическое название группы лекарственных средств, включающей глюкозамина сульфат и его производные, хондроитина сульфат (ХС) и диацерин, неомыляемые соединения авокадо/сои. В настоящее время число данных, подтверждающих эффективность глюкозамина сульфата и ХС, неуклонно растет (отнесены к 1А категории доказательности).
ХС, наряду с дерматансульфатом, кератансульфатом, гепарансульфатом и гепараном, относится к соединениям, классифицируемым как гликозаминогликаны. ХС сформирован на основе объединения чередующихся остатков сульфатированных и/или несульфатированных остатков глюкуроновой кислоты и N-ацетилгалактозамина в полисахаридные цепи. Из-за биохимического разнообразия дисахаридов, включенных в первичную структуру цепи полисахарида, ХС рассматривают как гетерогенную группу соединений, имеющих различную молекулярную массу и удельный вес. Наличие переменной первичной структуры позволяет ХС специализировать биологические функции в пределах живого организма.
ХС обеспечивает субстрат для синтеза протеогликанов. Было показано, что ХС способствует существенному увеличению гликозаминогликанов во внеклеточном матриксе хряща, ингибирует деградацию протеогликанов и стимулирует регенерацию хряща после экспериментально вызванного повреждения.
Среди препаратов группы SYSADOA особое место занимает Хондроксид мазь 5 %. Основным действующим веществом препарата является ХС – высокомолекулярный мукополисахарид, замедляющий резорбцию костной ткани и снижающий потерю кальция, а также препятствующий коллапсу соединительной ткани. Кроме того, Хондроксид ингибирует ферменты, вызывающие поражение хрящевой ткани, стимулирует синтез гликозаминогликанов, способствует регенерации суставной сумки и хрящевых поверхностей суставов, увеличивает продукцию внутрисуставной жидкости. Это приводит к уменьшению болезненности и увеличению подвижности пораженных суставов.
Диметилсульфоксид, входящий в состав мази, оказывает противовоспалительное, анальгетическое и фибринолитическое действие, способствует лучшему проникновению ХС через клеточные мембраны, обеспечивая его эффективный трансдермальный транспорт в зоны поражения суставов и позвоночника.
Мазь наносят 2–3 раза в сутки на кожу над очагом поражения, втирая до полного впитывания в течение 2–3 минут. Курс лечения должен составлять не менее 12 недель. В то же время, как показывают клинические наблюдения, длительная – до 3 лет – терапия хондропротекторами дает наилучшие результаты. По клиническим показаниям может быть использована прерывистая схема лечения курсами по 12–16 недель с перерывами на 8–10 недель.
Российскими специалистами уже накоплен весомый опыт клинического применения мази Хондроксид. Так, на базе Казанской государственной медицинской академии было проведено двойное слепое клиническое исследование ее эффективности в сравнении с мазью, содержащей ибупрофен. В исследование были включены 64 пациента с нейродистрофической формой люмбоишиалгии, развившейся на фоне поясничного спондилоартроза. Результаты этого исследования подтвердили высокую анальгетическую активность мази Хондроксид: через 2 недели лечения интенсивность боли в пояснице у больных уменьшалась в среднем в 2 раза. Был сделан вывод, что Хондроксид мазь 5% может рекомендоваться для местного применения при синдроме нейродистрофической люмбоишиалгии, обусловленном поясничным спондилоартрозом, в качестве лечебного и профилактического средства как в амбулаторных, так и в стационарных условиях [7]. Показана высокая эффективность применения мази Хондроксид и у пациентов с остеоартрозом I–II стадии периферических суставов: на фоне лечения отмечалось уменьшение боли в суставах, улучшение их функции, ослабление выраженности явлений синовита и повышение качества жизни пациентов.
Учитывая ведущую роль мышечного спазма в клинической картине болевых синдромов при спондилоартрозе, в их комплексную терапию целесообразно включать миорелаксанты. Миорелаксанты снижают патологическое мышечное напряжение, уменьшают боль, улучшают двигательные функции, облегчают проведение физиотерапевтических мероприятий и лечебной физкультуры. Доказано, что при дорсалгии, возникающей вследствие мышечного спазма, добавление к стандартной терапии (нестероидные противовоспалительные средства, анальгетики, физиотерапия, лечебная гимнастика) миорелаксантов приводит к более быстрому регрессу боли, мышечного напряжения и улучшению подвижности позвоночника.
Таким образом, новейшие исследования позволяют на основании критериев доказательной медицины подтвердить клиническую значимость комплексного подхода к лечению остеоартроза. ХС как в виде препарата для перорального приема, так и наружной мази, в сочетании с НПВП может составлять основу длительной терапии больных с дегенеративными заболеваниями позвоночника и суставов, способной существенно изменить течение болезни.
Литература
Комментарии
ПРАКТИКА ПЕДИАТРА
