Комплексная коррекция артериальной гипертензии и когнитивных нарушений у больных с гипертонической энцефалопатией.
СтатьиОпубликовано в журнале:
«Атмосфера. Нервные болезни», 2009, №4, с. 1-5
А.В. Федотова, О.П. Миронова, Ф.А. Карпов, А.И. Федин
Проблема нарушения когнитивных функций (понятие когнитивных, или познавательных, функций включает в себя память, внимание, речь, праксис, гнозис, интеллект) при самых разных неврологических и соматических заболеваниях является одной из наиболее актуальных в современной неврологии, так как когнитивные расстройства значительно снижают продолжительность жизни пациента, ухудшают качество его жизни, уменьшают приверженность лечению.
Нарушения когнитивных функций при цереброваскулярной патологии обозначают термином “сосудистые когнитивные расстройства” (СКР). СКР разделяют на две группы: СКР при поражении крупных сосудов (разнообразная по характеру и выраженности группа нейропсихологических синдромов) и СКР при поражении мелких сосудов (нейропсихологические симптомы преимущественно лобной дисфункции). Когнитивные нарушения при сосудистой патологии варьируют по выраженности от легких и умеренных когнитивных расстройств до степени деменции. Легкие когнитивные расстройства осознаются больным, вызывая у него беспокойство и озабоченность, незаметны для окружающих, появляются уже в самом начале заболевания и выявляются при тщательном исследовании с применением нейропсихологических методик. Умеренные когнитивные расстройства (УКР) выходят за рамки возрастной нормы, заметны окружающим и диагностируются по следующим критериям:
- снижение памяти (как со слов пациента, так и со слов родственников и сослуживцев);
- низкие показатели мнестических функций (по данным нейропсихологического тестирования);
- сохранность общего когнитивного потенциала;
- отсутствие ограничений в повседневной жизни;
- отсутствие деменции (результат краткой шкалы оценки психического статуса не менее 24 баллов).
Проспективные наблюдения за репрезентативными выборками пациентов показали, что УКР являются прогностически неблагоприятными факторами, так как свидетельствуют о высокой вероятности прогрессирования когнитивных нарушений [16]. Метаанализ серии исследований, посвященных оценке динамики УКР, свидетельствует о том, что в течение каждого последующего года в среднем у 10% пациентов развивается деменция [9]. Через 8–10 лет после дебюта когнитивных нарушений деменция развивается у 50–80% больных с УКР [19].
Артериальная гипертензия (АГ) рассматривается в настоящее время как самый значимый фактор риска развития не только острых нарушений мозгового кровообращения и хронической ишемии мозга, но и расстройств памяти и других когнитивных (познавательных) функций. Многочисленными исследованиями доказана связь стойкого повышения артериального давления (АД) с риском возникновения и прогрессирования когнитивных нарушений. В частности, такая связь установлена не только для тяжелой сосудистой деменции, но и для УКР [21]. Известно, что длительно существующая АГ (без инсульта в анамнезе) часто сопровождается нарушениями когнитивных функций в пожилом возрасте [11]. Так, в исследовании SCOPE было показано, что повышение АД у пожилых людей приводит к ухудшению познавательных функций и развитию деменции [23]. Большинство исследований указывают, что предиктором деменции является повышение систолического АД [24]. В некоторых исследованиях выявлена взаимосвязь между развитием деменции и уровнем диастолического АД. Кроме того, АГ в настоящее время рассматривается как фактор, ускоряющий реализацию генетической предрасположенности к нейродегенеративным заболеваниям [10].
Патологические процессы, происходящие в мозге при АГ, возникают вследствие плазматического и геморрагического пропитывания, а также некроза стенки сосудов с ее последующим истончением. Для хронической гипертонической энцефалопатии (ГЭ) характерно раннее поражение преимущественно белого вещества головного мозга с признаками деструкции миелина, наличием мелких полостей, расширением периваскулярного пространства [13]. Характерные изменения выявляются обычно в зонах терминального кровообращения, особо чувствительных к изменениям АД, т.е. в перивентрикулярных участках головного мозга. В исследовании ARIC было показано, что подобные изменения белого вещества головного мозга встречаются в группе пациентов с АГ в 2 раза чаще, чем у нормотензивных пациентов, а у больных с неконтролируемой АГ по сравнению с пациентами с адекватным контролем АГ – в 1,5 раза чаще. Нередко такие изменения протекают без клинической симптоматики. Продолжительность бессимптомной фазы может быть различной и определяться наличием других факторов риска. Однако даже начальные проявления ГЭ могут приводить к когнитивным нарушениям, которые можно считать маркером цереброваскулярного риска. Такие изменения могут быть выявлены с помощью специальных тестов, что необходимо делать как можно раньше, в период бессимптомной фазы ГЭ, так как возможности лечения и реабилитации больных с СКР в настоящее время весьма ограничены и крайне важным является выявление и лечение додементных форм когнитивных расстройств, когда терапевтические мероприятия максимально эффективны.
Очевидно, что адекватный контроль уровня АД (достижение целевых цифр АД), в первую очередь обусловленный приемом антигипертензивных препаратов, является эффективным способом предупреждения различных сердечно-сосудистых заболеваний. Более противоречивые данные получены в отношении коррекции АД и риска развития сосудистой деменции. В одних исследованиях, в частности в Syst-Eur [15], AWARE [22] и некоторых других, было установлено, что регулярное применение гипотензивных препаратов позволяет не только обеспечить нормализацию АД, но и снизить риск развития СКР. В то же время в серии других исследований (сходных по своему дизайну) убедительных подтверждений восстановления нарушенных когнитивных функций и предупреждения развития сосудистой деменции при нормализации АД не получено (HYVET-COG [20], SHEP [14]). Проведен метаанализ серии исследований (рандомизированных, двойных слепых, плацебоконтролируемых, длительностью не менее 6 мес), посвященных возможности профилактики сосудистой деменции на фоне применения антигипертензивных препаратов. В клинических исследованиях принял участие 12091 пациент. Было показано, что частота случаев развития деменции существенным образом не отличалась в группах проведения активного лечения и назначения плацебо [17]. Получение столь противоречивых данных объясняется тем, что контроль АД обеспечивает защитный эффект в отношении инсульта, но не может предотвратить развитие микроангиопатии с последующим поражением белого вещества головного мозга и развитием когнитивных нарушений [12].
Серьезную проблему в профилактике сосудистых когнитивных нарушений представляет низкая приверженность пациентов гипотензивной терапии. Причины низкой приверженности пациентов к гипотензивной терапии многообразны:
- плохая переносимость гипотензивных препаратов, низкая дисциплинированность пациентов, высокая стоимость лекарства, психологические факторы (нежелание обрекать себя на пожизненный прием лекарств), недостаточная осведомленность об осложнениях основного заболевания и цели приема лекарств;
- уже имеющийся когнитивный дефицит – снижение памяти (забывают принимать лекарство), забывчивость и рассеянность (нерегулярный прием препаратов), снижение критики к своему состоянию;
- гипотензивные препараты не устраняют многих неврологических симптомов (головокружение, головная боль, шаткость при ходьбе, повышенная тревожность, раздражительность), характерных как для ГЭ, так и для хронической ишемии головного мозга.
Указанные причины способны привести к систематическому нарушению приема лекарственных препаратов (нерегулярный прием, уменьшение дозы лекарства), что, в свою очередь, приводит к снижению эффективности лечения (иногда к полному отказу от него) и прогрессированию заболевания.
Таким образом, проблема лечения гипертонической болезни и развивающейся при ней ГЭ стоит весьма остро, учитывая прогрессирующий характер поражения мозга, приводящий к нарастанию расстройств церебральных функций [7, 8].
Одним из вариантов лечебной стратегии, увеличивающим приверженность больных гипотензивной терапии, может быть одновременное (в сочетании с антигипертензивными препаратами) применение лекарственных средств, улучшающих когнитивные и вестибулярные функции и уменьшающих головную боль [4, 6]. В связи с этим представляется перспективным применение лекарственных средств, обеспечивающих улучшение церебральной перфузии и обладающих нейрометаболическим действием. А.И. Фединым (2007) сформулирована концепция нового терапевтического направления в лечении хронической ишемии мозга и ГЭ – мультимодальной фармакотерапии, подразумевающей (с учетом многозвеньевого патогенеза этих заболеваний) назначение лекарств с несколькими фармакологическими эффектами. Наиболее соответствующей поставленной задаче (по многообразию клиникофармакологических эффектов и широте терапевтического спектра) является группа ноотропных препаратов.
На сегодняшний день препараты пирацетама и его комбинаций наиболее широко представлены на рынке ноотропных средств, причем их перечень продолжает неуклонно расширяться. Подобная популярность объясняется тем, что в настоящее время именно пирацетам по сравнению с другими препаратами данной группы обладает максимальной широтой фармакологического спектра ноотропной активности в сочетании с наличием определенного вазотропного действия, что имеет своим следствием исключительное многообразие его клинического применения.
Основные фармакологические эффекты пирацетама следующие:
- нейропротекторное действие;
- активация пластических процессов в мозге за счет стимуляции синтеза РНК и белков;
- влияние на мозговую гемодинамику (с увеличением объемного мозгового кровотока) и церебральную микрогемоциркуляцию (с улучшением деформируемости эритроцитов);
- нейромедиаторные и нейромодуляторные эффекты;
- антиоксидантное действие [2, 3, 18].
Спектр клинического применения пирацетама широк и включает в себя улучшение умственной деятельности человека при различных формах нарушения мозгового кровообращения (инсульт, дисциркуляторная энцефалопатия, преходящие нарушения мозгового кровообращения), нейроде-генеративных и других заболеваниях, нейроинтоксикации. Пирацетам уменьшает головокружения различного генеза, восстанавливает темп психического развития у детей с его задержкой, положительно влияет на возрастные нарушения интегративных функций мозга и памяти, а также повышает устойчивость организма к экстремальным воздействиям (хронические и острые психоэмоциональные стрессы) [1, 5, 25]. При перечисленных состояниях пирацетам эффективно способствует нормализации когнитивных функций и памяти, редукции остаточных явлений неврологического дефекта, психопатологической и депрессивной симптоматики, устранению нарушений вегетативной регуляции, астенизации, инсомнии, улучшению общего самочувствия и работоспособности.
В настоящее время считается доказанным, что диапазон эффективных терапевтических доз пирацетама при курсовом применении составляет 1,2–9,6 г, однако наиболее эффективной в большинстве случаев оказывается доза 2,4–4,8 г (при острых формах патологии, например при инсульте, назначаемые дозы могут быть существенно выше) [1, 3, 5]. Однако многие врачи стандартно назначают пирацетам по 1 таблетке 3 раза в день, не принимая во внимание, что большинство представленных на рынке пирацетамов низкодозированы (200–400 мг) и, соответственно, недостаточно эффективны в этой суточной дозе.
В связи со всем вышеизложенным интересной и важной представляется оценка влияния различных доз пирацетама на когнитивные функции, качество жизни и приверженность пациентов с ГЭ гипотензивной терапии.
Целью данного мультицентрового исследования, проведенного в 65 поликлиниках 39 городов Российской Федерации (Москва, Пермь, Ярославль, Нижний Новгород, Смоленск, Иркутск, Красноярск, Владивосток, Тюмень, Воронеж, Саратов и др.), было определение целесообразности назначения пирацетама (Луцетама) больным ГЭ (с доминирующей активной жалобой на снижение памяти) с целью увеличения приверженности их гипотензивной терапии.
Материал и методы исследования
В исследовании принимали участие практикующие врачи (неврологи и терапевты) первичного (поликлинического) звена здравоохранения. Перед началом исследования все врачи, принимающие в нем участие, прошли подготовительный инструктаж с координаторами работы по проведению исследования (критерии отбора больных, ведение протокола и т.д.). Все полученные данные обработаны в одном центре с использованием статистического пакета программ Statistica 6.
Исследование пациентов проводилось по стандартному протоколу после периода двухнедельной отмены всех препаратов (кроме базовой гипотензивной терапии). В исследовании использовались высокодозовые лекарственные формы пирацетама в виде препарата Луцетам производства компании “Эгис” (Венгрия), представляющего собой таблетки, содержащие 800 мг и 1200 г пирацетама.
Включенным в исследование пациентам проводилось фоновое анкетирование, после чего назначался двухмесячный курс Луцетама, и после его окончания осуществлялось повторное исследование. Доза препарата жестко не регламентировалась и оставлялась на усмотрение лечащего врача. Минимальная суточная доза составляла 1200 мг.
Критериями включения в исследование были возраст старше 20 лет, активно предъявляемые пациентами жалобы на снижение памяти, концентрацию внимания, рассеянность; наличие гипертонической болезни, подтвержденное инструментальными методами; наличие как минимум двух факторов риска сердечно-сосудистых заболеваний, желание и готовность пациента принимать участие в исследовании. Критериями исключения из исследования являлись перенесенные инсульты, воспалительные или травматические поражения головного мозга со стойким неврологическим дефицитом, выраженные когнитивные нарушения, затрудняющие профессиональную и повседневную деятельность, соматические заболевания в стадии декомпенсации, одновременный прием других препаратов с цереброваскулярным и нейропротективным действием.
В общий анализ были включены: демографические данные; нозологический диагноз; наличие АГ и ее длительность; адекватность коррекции АГ (показатели АД в момент исследования и “рабочее” АД); факторы, влияющие на некомплаентность больных; субъективная оценка пациентом по десятибалльной визуальной аналоговой шкале (ВАШ) снижения памяти, концентрации внимания и работоспособности, частоты и интенсивности головной боли, шаткости при ходьбе и эмоциональной лабильности; отдельно оценивались нежелательные эффекты. Динамика вышеуказанных параметров оценивалась в зависимости от назначенной дозы Луцетама. От врачей поликлиник получено 1310 протоколов обследования пациентов в возрасте от 20 до 99 лет (средний возраст 59,7 ± 11,8 года). Девять пациентов не включены в окончательный анализ данных, так как не соответствовали критериям включения - возраст моложе 20 лет, отсутствие АГ. В анализ также не включены пациенты, перенесшие инфаркт миокарда или инсульт (73 больных), пациенты с хронической ишемией мозга атеросклеротического характера без АГ (70 больных). Таким образом, для последующего анализа результатов исследования оставлены протоколы 1183 больных АГ.
Результаты и обсуждение
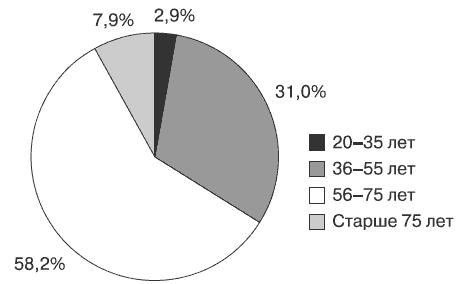
На рис. 1 представлено распределение пациентов в исследованной группе по возрасту. Как видно на рисунке, более половины обследованных были в возрастной группе от 56 до 75 лет.
Рис. 1. Распределение обследованных больных по возрасту.
Все обследованные пациенты были разделены на две группы: 1-я - пациенты с ГЭ на фоне гипертонической болезни (242 больных); 2-я - пациенты с ГЭ на фоне гипертонической болезни и атеросклероза, у которых при ультразвуковой допплерографии определялись признаки атеросклеротического поражения мозговых артерий (941 больной).
У всех пациентов были жалобы на когнитивные нарушения в виде расстройства памяти, преимущественно оперативной, снижения концентрации внимания, умственной работоспособности. Частыми жалобами были головная боль, головокружение, нарушение координации движений.
Пациенты исследованных групп достоверно не отличались по полу и возрасту.
Длительность артериальной гипертензии в годах представлена в табл. 1.
Таблица 1. Длительность АГ в годах в исследуемых группах
| Длительность АГ | 1-я группа (n = 242) | 2-я группа (n = 941) | Всего |
| Менее 5 лет | 40 (16,5%) | 116 (12,3%) | 156 (13,1%) |
| 5-10 лет | 86 (35,5%) | 292 (31,0%) | 378 (31,9%) |
| 10-15 лет | 70 (28,9%) | 306 (32,5%) | 376 (31,8%) |
| Более 15 лет | 46 (19,1%) | 227 (24,2%) | 273 (23,2%) |
Сто тридцать семь (11,6%) пациентов с АГ на момент исследования не получали гипотензивной терапии. Из 1046 пациентов (88,4%), получавших гипотензивную терапию, целевые цифры АД были достигнуты у 366 больных (34,9%). За целевые цифры АД в этом исследовании, учитывая разный возраст больных, принимался показатель 149/90 мм рт. ст. Среди пациентов, не достигших целевых цифр АД, 313 больных (29,9%) самостоятельно снижали дозу назначенных им лекарств, 334 (31,9%) принимали препараты нерегулярно, 292 (27,9%) принимали не все назначенные врачом препараты. У 106 пациентов (10,1%) имела место неадекватно подобранная врачом терапия.
При анализе основных причин некомплаентности больных были получены следующие данные: 930 пациентов (88,9%) недостаточно ясно представляли себе и понимали суть заболевания и его возможные последствия, 439 (41,9%) полностью не выполняли рекомендации врача изза боязни в последующем “пожизненного” приема препаратов, 482 (46,0%) опасались развития побочных эффектов, 407 (38,9%) самостоятельно из- меняли схему терапии из-за плохой переносимости гипотензивных препаратов, 348 (33,2%) ссылались на высокую стоимость лечения.
Перед началом приема Луцетама с пациентами была проведена разъяснительная беседа, назначена или откорректирована гипотензивная терапия. После двухмесячного курса лечения у 55% пациентов были достигнуты целевые цифры АД. Из 137 пациентов, не получавших гипотензивную терапию до начала исследования, 30 пациентов отказались от длительной терапии гипотензивными препаратами. При повторном интервьюировании 1153 больных ГЭ, продолживших гипотензивную терапию, 554 из них (48,1%) отметили субъективно лучшую переносимость гипотензивных препаратов на фоне приема Луцетама (уменьшились частота и интенсивность головной боли и головокружения).
При анализе основных симптомов заболевания, оцениваемых пациентами по ВАШ до и после лечения, было получено прогнозируемое улучшение самочувствия по всем параметрам как в каждой группе, так и в целом по выборке (табл. 2).
Таблица 2. Динамика основных неврологических симптомов заболевания на фоне лечения
| Симптомы | 1 -я группа (n = 242) | 2-я группа (n = 941) | Всего | |||
| до лечения | после лечения | до лечения | после лечения | до лечения | после лечения | |
| Снижение памяти | 5,1 ± 2,10 | 2,6 ± 1,8* | 5,4 ± 1,9 | 3,3 ± 1,7* | 5,3 ± 2,1 | 3,0 ± 1,3* |
| Снижение работоспособности | 5,0 ± 2,25 | 2,4 ± 1,8* | 5,3 ± 2,1 | 3,3 ± 1,7* | 5,1 ± 2,1 | 2,8 ± 1,1* |
| Выраженность эмоциональной лабильности | 4,8 ± 2,25 | 2,2 ± 1,7* | 5,1 ± 2,1 | 2,8 ± 1,7* | 5,0 ± 2,2 | 2,7 ± 1,5* |
| Головная боль (интенсивность) | 5,9 ± 2,1 | 2,1 ± 1,6* | 4,9 ± 2,1 | 1,6 ± 0,6* | 5,1 ± 2,0 | 2,4 ± 1,6* |
| Головокружение | 4,4 ± 2,4 | 1,7 ± 0,7* | 5,1 ± 2,2 | 2,5 ± 1,3* | 4,9 ± 2,3 | 2,2 ± 1,1* |
| Нарушение координации движений | 3,4 ± 1,2 | 1,5 ± 0,2* | 4,4 ± 2,3 | 2,1 ± 1,4* | 4,1 ± 2,5 | 1,9 ± 0,9* |
* Достоверное улучшение симптоматики после лечения (р
Как видно из табл. 2, после курса лечения Луцетамом в обеих группах получено существенное улучшение когнитивных функций, уменьшение головной боли, головокружения, нарушения координации движений, эмоциональной лабильности (p В 1-й группе больных жалобы на головную боль предъявляли 238 пациентов (98,3%), после 2-месячного курса лечения головная боль регрессировала полностью у 16 пациентов (6,7%). Во 2-й группе жалобы на головную боль были у 925 человек (98,3%), из них у 121 (12,8%) после курса лечения цефалгия полностью регрессировала.
Частота головной боли в группах до и после лечения представлена в табл. 3.
Таблица 3. Частота головной боли до и после лечения Луцетамом
| Частота головной боли | 1 -я группа (n = 242) | 2-я группа (n = 941) | ||
| до лечения | после лечения | до лечения | после лечения | |
| Постоянная | 27(11%) | - | 116(12,8%) | 9(1,1%) |
| Частая | 144(60,5%) | 23(10,4%) | 470 (52,3%) | 93(11,8%) |
| Редкая | 67 (28,5%) | 199(89,6%) | 314(34,9%) | 688(87,1%) |
Частота головной боли в обеих группах больных до лечения существенно не различалась (см. табл. 3). На фоне лечения Луцетамом отмечается достоверное уменьшение головной боли по частоте ее возникновения в обеих исследуемых группах.
В связи с тем, что в начале исследования доза назначаемого Луцетама не регламентировалась, диапазон назначенных суточных доз варьировал от 1200 до 4800 мг/сут. Доза 1200 мг была назначена 19 пациентам (1,6%), 1600 мг – 79 (6,6%), 2400 мг – 742 (62,7%), 3200 мг – 56 (4,7%), 3600 мг – 167 (14,1%) и 4800 мг – 120 (10,3%) пациентам. Нами был проведен анализ динамики улучшения основных исследуемых параметров в зависимости от назначенной дозы Луцетама. Результаты представлены в табл. 4.
Таблица 4. Динамика неврологических расстройств в зависимости от суточной дозы Луцетама
| Симптомы | Суточные дозы Луцетама | ||||||||
| 1200-1600 мг(n = 98) | 2400-3200 мг (n = 798) | 3600-4800 мг (n = 287) | |||||||
| 1 | 2 | Δ | 1 | 2 | Δ | 1 | 2 | Δ | |
| Снижение памяти | 5,2 ±2,2 | 3,6 ±2,3* | 30,7 | 5,4 ±1,9 | 2,6 ±1,8* | 51,8 | 5,3 ±2,1 | 2,1 ±1,3* | 60,4 |
| Снижение работоспособности | 5,5 ±2,3 | 3,9 ±1,8 | 29,1 | 5,3 ±2,1 | 2,1 ±1,7* | 60,3 | 5,1 ±2,1 | 2,2±1,1* | 56,7 |
| Выраженность эмоциональной лабильности | 4,8 ±2,2 | 3,8 ±1,7 | 20,8 | 4,9 ±2,1 | 3,2 ±1,7 | 34,6 | 5,0 ±2,2 | 3,3 ±1,5 | 34,0 |
| Головная боль (интенсивность) | 5,3 ±2,1 | 4,4 ±1,6 | 16,9 | 4,9 ±2,1 | 2,9 ±1,6* | 40,8 | 5,1 ±2,0 | 3,4 ±1,6* | 52,9 |
| Головокружение | 4,7 ±2,1 | 2,8± 1,1* | 31,9 | 5,1 ±2,2 | 1,8±1,3* | 64,7 | 4,9 ±2,3 | 2,0±1,1* | 59,2 |
| Нарушение координации движений | 4,3 ±1,2 | 2,8 ±0,9* | 34,8 | 4,4 ±2,3 | 1,9 ±1,4* | 56,8 | 4,1 ±2,5 | 1,9 ±0,9* | 53,6 |
Примечание. Показатели шкалы ВАШ в баллах: 1 - до лечения, 2 - после 2-месячного курса Луцетама; Л - разница показателей до и после лечения в %. * Статистически значимое (р
Из табл. 4 видно, что назначение Луцетама в суточной дозе 1200–1600 мг приводило к улучшению памяти, регрессу головокружения и нарушения координации движений (p 0,05). Аналогичный дозозависимый эффект Луцетама отмечен при головной боли, головокружении и координаторных нарушениях.
Рис. 2. Дозозависимая динамика (А) когнитивных и астенических расстройств после курсового лечения Луцетамом. Подгруппы больных ГЭ с суточными дозами Луцетама: 1 - 1200-1600 мг; 2 - 2400-3200 мг; 3 -3600-4800 мг.
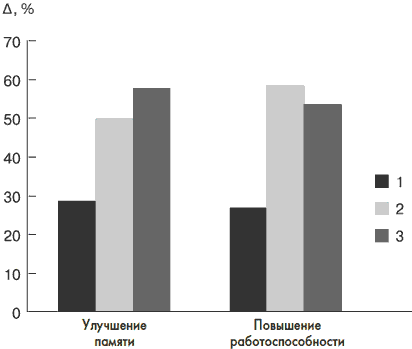
Не прослежен эффект Луцетама в отношении эмоциональных нарушений при всех назначаемых его дозировках (см. табл. 4).
В проведенном исследовании была отмечена хорошая переносимость Луцетама. Побочные эффекты (тошнота, легкие диспептические явления, головная боль), не приводившие к отказу от лечения, были выявлены лишь у 104 пациентов (7,8%). У 53 пациентов (51%) они регрессировали в течение первых 2 нед терапии, у 20 пациентов (19,2%) значительно уменьшились в течение первых 2 нед терапии, у 30 (28,8%) сохранялись на протяжении всего лечения. Двенадцать пациентов принимали Луцетам в дозе 3600 мг и 18 – в дозе 4800 мг. Чрезвычайно важным было отсутствие взаимодействия Луцетама с другими лекарственными препаратами, что позволяло проводить адекватную гипотензивную терапию. Удобство дозирования – высокое содержание активного вещества (дозировка 1200 мг) в одной таблетке – является важным фактором, увеличивающим приверженность больных к лечению.
Проведенное исследование позволяет сделать вывод о целесообразности как можно более раннего начала нейротропной терапии у больных ГЭ с целью улучшения когнитивных функций, уменьшения выраженности других неврологических расстройств и увеличения их приверженности гипотензивной терапии. Полученные нами данные требуют дальнейшего, более углубленного исследования, однако на данном этапе представляется целесообразным включение Луцетама в комплексное лечение больных ГЭ.
ЛИТЕРАТУРА
1. Аведисова А.С. и др. // Рос. психиатр. журн. 2001. № 1. С. 46.
2. Бурчинский С.Г. // Журн. практ. лікаря. 2002. № 3. С. 71.
3. Бурчинский С.Г. // Журн. практ. лікаря. 2005. № 2. С. 51.
4. Гуревич К.Г. // Качественная клиническая практика. 2003. №4. С. 53.
5. Захаров В.В., Яхно Н.Н. Когнитивные расстройства в пожилом и старческом возрасте: Метод. пособие для врачей. М., 2005.
6. Румянцева Г.М. и др. // Качественная клиническая практика. 2002. № 1. С. 28.
7. Севастьянова Е.В., Повереннова И.Е. // Неврол. вестн. 2008. Т. XL. Вып. 1. С. 21.
8. Федин А.И. // Атмосфера. Нервные болезни. 2006. № 4. С. 22.
9. Федин А.И., Путилина М.В. Луцетам в лечении цереброваскулярных заболеваний: Метод. рекомендации. М., 2006.
10. Филатова Е.Г. // Лечение нервных болезней. 2003. № 8. С. 25.
11. Bruscoli M., Lovestone S. // Int. Psychogeriatr. 2004. V. 16. P. 129.
12. Cerebrovascular Disease, Cognitive Impairment and Dementia /Ed. by J. O’Brien et al. L., 2004.
13. Cicconetti P. et al. // Clin. Exp. Hypertens. 2000. V. 22. P. 583.
14. Cherubini A. et al. // Am. J. Ther. 2007. V. 14. P. 533.
15. Di Bari M. et al. // Am. J. Epidemiol. 2001. V. 153. P. 72.
16. Forette F. et al. // Arch. Intern. Med. 2002. V. 162. P. 2046.
17. Morris J. et al. // Arch. Neurol. 2001. V. 58. P. 397.
18. McGuinness B. et al. // Cochrane Database Syst. Rev. 2006. V. 2.CD004034.
19. Muller W.E. et al. // Pharmacopsychiatry. 1999. V. 32. Suppl. 1. P. 2.
20. Petersen R. et al. // Arch. Neurol. 2001. V. 58. P. 1985.
21. Peters R. et al. // Lancet Neurol. 2008. V. 7. P. 683.
22. Reitz C. et al. // Arch. Neurol. 2007. V. 64. P. 1734.
23. Schrader J. et al. // Med. Klin. (Munich). 2008. V. 103. P. 491.
24. Skoog I. et al. // Lancet. 1996. V. 347. P. 1141.
25. Swan G.T. et al. // Stroke. 1998. V. 29. P. 2334.
26. Waegemans T. et al. // Dement. Geriatr. Cogn. Disord. 2002. V. 13. P. 217.
