Оценка иммунитета в обосновании иммунотропной терапии энтеровирусных менингитов
СтатьиОпубликовано в журнале:
«Инфекционные болезни», 2009, т.7, №3, с. 20-24
Н.А.Бацкалевич1, В.К.Веревщиков2, Ю.Г.Лагерева3
1Городская клиническая больница №40, Екатеринбург; 2Уральская государственная медицинская академия, Екатеринбург; 3Клинико-диагностический центр, Екатеринбург
В исследовании проанализирован характер иммунного ответа при менингеальной форме энтеровирусной инфекции у подростков и взрослых больных. Проведена прогностическая оценка показателей иммунитета. На основании выявленного дисбаланса в иммунной реактивности для проведения иммунотропной терапии предложен препарат Анаферон, относящийся к группе комплексных иммуномодуляторов и индукторов интерферонов. Ключевые слова: энтеровирусная инфекция, менингит, интерферон-гамма, Анаферон
Immunity evaluation in a rationale for immunotropic therapy of enterovirus meningitis
N.A.Batskalevich1, V.K.Verevshchikov2, Yu.G.Lagereva3
1City Clinical Hospital No.40, Yekaterinburg; 2Urals State Medical Academy, Yekaterinburg; 3Clinical and Diagnostic Center, Yekaterinburg
The study analyzed the character of immune response in the meningeal form of enterovirus infection in adolescent and adult patients. A prognostic evaluation of immunity values is made. Based on the revealed imbalance of immune reactivity the drug Anaferon belonging to the group of complex immunomodulators and inductors of interferons has been proposed for immunotropic therapy. Key words: enterovirus infection, meningitis, interferon-gamma, Anaferon
Энтеровирусная инфекция (ЭВИ) относится к тем заболеваниям, с которыми врач чаще сталкивается, чем ставит этот диагноз, что связано с повсеместным распространением, пантропизмом энтеровирусов и, следовательно, манифестацией данной инфекции в виде различных клинических вариантов с возможным поражением одного или нескольких органов и систем [1–6].
Одной из наиболее частых причин госпитализации при ЭВИ является поражение нервной системы от легких энцефалитических синдромов до тяжелых энцефалитов с летальным исходом. С улучшением диагностических тестов стало известно, что от 80 до 92% всех асептических менингитов вызываются энтеровирусами [2, 3, 6, 7].
С одной стороны, энтеровирус как антигенный раздражитель стимулирует развитие иммунной реактивности, с другой стороны, как внутриклеточный паразит подавляет функциональную активность иммунокомпетентных клеток и превращает их в мишень для действия цитотоксических клеток [7, 8].
Основное значение в защите от вирусных инфекций имеет клеточный иммунитет. Ведущим механизмом освобождения от зараженных вирусом клеток является действие натуральных киллеров (NK-клетки) и цитотоксических лимфоцитов. Цитотоксические лимфоциты (CTL) и NK-клетки распознают свои мишени разными способами. CTL, относящиеся к СВ8+-лимфоцитам, распознают вирусные пептиды на мембране клеток, презентированные молекулами системы гистосовместимости (МНС) класса I. Некоторые CD4+-лимфоци-ты, обладающие цитотоксическими свойствами, распознают антиген, экспрессированный на мембране клеток в комплексе с молекулами МНС класса II [7, 10–13].
Специфический иммунный ответ сопряжен с продукцией цитокинов, которые влияют на течение и исход иммунного ответа, осуществляют взаимосвязь между неспецифическими защитными реакциями и клеточным иммунитетом, определяют преимущественную его направленность по гуморальному или клеточному типу. Многочисленные факты указывают на наличие тесной взаимосвязи между уровнем продукции этих молекул и клиническими характеристиками инфекционного процесса [7, 9].
Интерферон-гамма (ИФН-γ) – важнейший провоспалительный цитокин, который продуцируется активированными Т-лимфоцитами и натуральными киллерами. Продукция ИФН-у Т-лимфоцитами запускается при распознавании комплекса антигенного пептида с собственными молекулами гистосовместимости и регулируется другими цитокинами: типичным стимулятором - интерлейкином-2 (ИЛ-2) и типичным ингибитором - ИЛ-10. Уровень продукции ИФН-у при иммунном ответе в значительной степени определяется доминированием определенной субпопуляции Т-хелперов: Th1- или Th2- [12, 14]. Функция ИФН-у- активация макрофагов: их микробицидности и цитотоксичности, продукции ими цитокинов, супероксидных и нитроксидных радикалов, простагландинов [9, 12].
ИФН-у повышает функциональную активность цитотоксических Т-лимфоцитов (CTL, CD8+), характер влияния на функции Т-хелперов зависит от уровня экспрессии соответствующих рецепторов [13, 15]. Очевидно, что ИФН-у является главным медиатором клеточного иммунитета. Высокий уровень его продукции обычно ассоциируется с эффективным иммунным ответом против внутриклеточных патогенов [15-17].
Целью нашей работы стало выявление показаний к назначению иммунокорригирующей терапии больным менингеальной формой ЭВИ на основании изучения состояния клеточного и гуморального звеньев иммунитета.
Пациенты и методы
В клинике инфекционных болезней УГМА на базе ГКБ №40 г. Екатеринбурга методом случайной выборки были сформированы 2 группы больных энтеровирусным менингитом (ЭМ): 1-я группа - 37 чел. в возрасте 19–40 лет (мужчин - 19, женщин - 18) и 2-я - 36 больных подросткового возраста (девушки - 13, юноши - 23). Диагноз ЭВИ верифицировался результатами полимеразной цепной реакции (ПЦР), направленной на обнаружение РНК энтеровирусов в спинномозговой жидкости [2]. Комплексная оценка иммунного статуса проводилась дважды: на 1-й неделе госпитализации, на 3-й неделе лечения (период ранней реконвалесценции). Контрольной группой послужили доноры (35 чел.), сопоставимые по полу и возрасту с исследуемыми группами. Помимо стандартных показателей оценивались уровни CD3+-лимфоцитов, содержащих в цитоплазме провоспалительные (ИЛ-2, ИФН-у, и фактор некроза опухолей-а (ФНО-а) и противовоспалительные (ИЛ-4) цитокины, при их спонтанном синтезе и в ответ на стимуляцию. Статистическая обработка результатов проводилась в пакете прикладных программ STATISTICA 6,0 фирмы StatSoft Inc. (США). Сравнение групп по качественным признакам реализовалось с помощью построения таблиц сопряженности и дальнейшим анализом на предмет проверки гипотезы о случайности распределения частот с использованием методов X2 по Пирсону, X2 с поправкой Йетса, точного критерия Фишера [18].
Результаты исследования и их обсуждение
Развитие воспалительного процесса при ЭМ у подростков характеризовалось изменениями в неспецифическом и клеточном звеньях: лейкопения (p Таблица. Показатели клеточного и гуморального иммунитета у больных энтеровирусными менингитами
| Показатель x109/л | Подростки (M ± m) n = 36 | Взрослые (M ± m) n = 37 | ||
| 1-я неделя | 3-я неделя | 1-я неделя | 3-я неделя | |
| Лейкоциты, 109/л | 5,9 ± 0,24↓* | 6,53 ± 0,24 | 5,8 ± 0,4 | 5,66 ± 0,45 |
| Лимфоциты, 109/л | 1,96 ± 0,1↓* | 1,94 ± 0,1↓ | 1,7 ± 0,16↓* | 1,9 ± 0,11↓ |
| Гранулоциты, 109/л | 3,57 ± 0,2 | 4,1 ± 0,29 | 3,7 ± 0,38 | 3,38 ± 0,38 |
| Моноциты, 109/л | 0,36 ± 0,02 | 0,45 ± 0,05 | 0,36 ± 0,03 | 0,37 ± 0,04 ↑ |
| Активность фагоцитоза нейтрофилов, 109/л | 3,05 ± 0,22 | 3,5 ± 0,25 | 3,19 ± 0,3 | 3,1 ± 0,3 |
| Активность фагоцитоза моноцитов, 109/л | 0,25 ± 0,02 | 0,33 ± 0,05 | 0,27 ± 0,03↑* | 0,28 ± 0,04↑ |
| Бактерицидная активность, % | 41,2 ± 3,1 | 35,48 ± 1,7 ↓ | 41,8 ± 2,7 | 33,7 ± 3,02↓ |
| НСТ спонтанный, % | 15,4 ± 2,0↑* | 12,04 ± 1,5↑ | 13,2 ± 2,02 | 9,5 ± 1,86 |
| НСТ стимулир, % | 20,4 ± 2,3 | 20,9 ± 2,4 | 21,4 ± 3,04 | 16,0 ± 2,75 |
| IgG, г/л | 11,0 ± 0,69 | 9,5 ± 0,6 | 11,8 ± 1,3 | 10,35 ± 1,4 |
| IgA, г/л | 1,63 ± 0,17↓* | 1,4 ± 0,12↓ | 1,8 ± 0,19 | 1,75 ± 0,2 |
| IgM, г/л | 1,66 ± 0,11↑* | 1,67 ± 0,11↑ | 2,0 ± 0,21 ↑* | 2,2 ± 0,2↑ |
| ЦИК, Е/мл. | 72,8 ± 5,4 | 72,1 ± 5,1 | 94,1 ± 13,4 | 84,4 ± 14,3 |
| CD20, 109/л | 0,38 ± 0,03 | 0,29 ± 0,03↓ | 0,23 ± 0,03 | 0,26 ± 0,03 |
| CD3+, 109/л | 1,37 ± 0,11↓* | 1,44 ± 0,08↓ | 1,3 ± 0,14↓* | 1,46 ± 0,1↓ |
| CD4+, 109/л | 0,84 ± 0,07 | 0,87 ± 0,04 | 0,83 ± 0,11 | 0,94 ± 0,09 |
| CD8+, 109/л | 0,45 ± 0,04↓* | 0,5 ± 0,04↓ | 0,43 ± 0,05↓* | 0,44 ± 0,05↓ |
| NK, 109/л | 0,12 ± 0,01↓* | 0,08 ± 0,009↓** | 0,15 ± 0,02↓* | 0,16 ± 0,026↓ |
* сравнение групп с показателем возрастной нормы, ** сравнение групп на 1-й и 3-й неделях заболевания, ↑ и ↓ – достоверное отклонение от нормы (р
Количество В-лимфоцитов, концентрации IgG и IgA сохранялись в пределах возрастной нормы в течение первых 3 недель болезни как у взрослых больных, так и у подростков. Повышение стартового уровня IgM (p Нами впервые была предпринята попытка исследования субпопуляций CD3+-лимфоцитов, содержащих в цитоплазме провоспалительные и противовоспалительные цитокины у пациентов разного возраста. Полученные данные свидетельствуют, что в острый период заболевания у подростков с ЭМ отмечается увеличение уровней CD3+/ФНО-а+ и CD3+/ИЛ-4+-лимфоцитов (pРисунок. Отклонения от нормы содержания цитокинов в цитоплазме CD3+-лимфоцитов при спонтанном (sp) и стимулированном (st) синтезе при энтеровирусном менингите у подростков и взрослых. * – уровень у здоровых доноров.
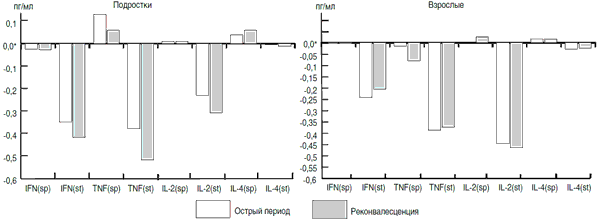
Результаты исследования клеточного и гуморального звеньев иммунитета представлены в таблице. Зависимость основных клинических симптомов от уровня CD3+-клеток, содержащих провоспалительные цитокины, подтверждена положительной связью между длительностью и интенсивностью головной боли и числом CD3+/ФНО-а+-лимфоцитов (r = 0,61; p Выявлена обратная связь между стартовым уровнем CD3+/ФНО-а+-лимфоцитов, а также CD3+/ИФН-у+-лимфоцитов и уровнем цитоза ликвора (r = -0,64; p Регуляторные функции цитокинов в формировании иммунного ответа в острый период заболевания отражены в связях между CD3+/ИЛ-2+, CD3+/ИФН-γ+-лимфоцитами и поглотительной активностью макрофагов (r = 0,65; p Общей закономерностью иммунологической перестройки субпопуляций CD3-клеток, продуцирующих провоспалительные цитокины ИЛ-2, ФНО-α, ИФН-γ, явилась их низкая функциональная активность и резервная возможность (рисунок). Эта тенденция проявляется как в острый период заболевания, так и в периоде ранней реконвалесценции.
Прямая зависимость между резервной возможностью CD3+/ФНО-α+– и CD3+/ИФН-γ+–лимфоцитов и уровнем цитотоксических лимфоцитов прослеживается в острый период при активации клеточно-опосредованных механизмов реализации иммунного ответа (r = 0,66; p Таким образом, на основании проведенного анализа можно выделить следующие иммунологические особенности течения ЭМ у взрослых больных и подростков:
1) снижение абсолютного количества лимфоцитов периферической крови, снижение содержания CD3-, CD8-лимфоцитов и натуральных киллеров;
2) низкая функциональная активность и резервная возможность CD3+-лимфоцитов, содержащих провоспалительные цитокины;
3) зависимость выраженности и длительности регистрации основных клинических симптомов заболевания от уровня CD3+-клеток, содержащих в цитоплазме провоспалительные цитокины.
Общеизвестно, что основные клинические симптомы при ЭМ купируются в течение 1-й недели заболевания. Показателем выздоровления считается нормализация показателей ликвора. Проведенное исследование выявило, что у 56% подростков и 40% взрослых при ЭМ на 18–20-й день заболевания уровень цитоза ликвора превышает 20 х 106/л, в нашем исследовании он составил 23,6 ± 4,1 х 106/л у подростков, 28,0 ± 5,2 х 106/л - у взрослых больных. Проведен анализ зависимости времени санации ликвора от показателей врожденного и адаптивного иммунитетов.
При анализе таблицы сопряженности цитоза ликвора (цитоз 20 клеток), а также показателей гемо-, иммунограммы выявлены следующие особенности:
1) при снижении стартового уровня лимфоцитов периферической крови ниже 2,0 х 109/л не наблюдалось санации ликвора на 3-й неделе заболевания в 64% случаев (p 2) при условии одновременного снижения стартового уровня NK и цитотоксических лимфоцитов на 18-20-й день болезни санация ликвора не происходит (цитоз > 20 клеток) (p 6/л;
3) при условии сохранения уровня стартовых показателей цитотоксических лимфоцитов и NK-клеток в пределах возрастной нормы или выше, цитоз ликвора на 3-й неделе заболевания был менее 20 клеток у всех пациентов и составил на 18-20-й день: М = 11,0; о = 4,1; т = 1,4 x 106/л;
4) при уровне NK ниже 0,097 x 109/л не было отмечено санации ликвора на 18-20-й день болезни;
5) при условии санации ликвора уровень CD3+/ИФН-a+-лимфоцитов составил: М = 0,05; о = 0,03; т = 0,01 х 109/л, при повышенном цитозе на 3-й неделе заболевания: М = 0,025; о = 0,015; т = 0,06 х 109/л (p Таким образом, снижение при энтеровирусном менингите, прежде всего, показателей врожденного иммунитета обуславливает задержку санации ликвора.
Учитывая зависимость времени санации ликвора от уровня СD3+-клеток, низкую функциональную активность CD3+/ИНФ-у+-лимфоцитов, особое место ИНФ-у среди цитокинов, обладающих контрольно-регуляторными функциями, который является специализированным индуктором активации макрофагов, индуцирует и активирует продукцию провоспалительных цитокинов, в комплексной терапии менингеальной формы ЭВИ целесообразно использовать иммунотропные средства, регулирующие интерфероновый профиль.
В качестве такого препарата мы рассмотрели возможность применения Анаферона («Материа Медика», Россия), являющегося иммуномодулятором с противовирусной активностью. Выбор Анаферона был обоснован фармакологическими свойствами и высокой безопасностью. Анаферон содержит сверхмалые дозы антител к у-ИФН человека в виде активной формы водно-спиртовой смеси, что обеспечивает его высокую безопасность. Анаферон индуцирует и регулирует образование эндогенных ИФН, прежде всего, ИФН-у. Способность препарата выступать не стимулятором, а регулятором синтеза последнего подтверждается тем, что он является индуктором смешанного Тh1- и Тh2-типа иммунного ответа: повышает выработку цитокинов Th1 и Тh2, модулирует баланс Тh1-/Тh2-активностей. Кроме того, Анаферон повышает функциональный резерв фагоцитов, NК-клеток, Т-хелперов, а так же других клеток, участвующих в иммунном ответе. Влияние Анаферона на гуморальное звено проявляется повышением продукции антител (включая секреторный IgA).
Ранее нами был получен опыт применения Анаферона (в качестве противовирусного препарата) в комплексе с общепринятой схемой лечения ЭМ. Данный препарат назначался нами с 2-4-го дня болезни в течение 7 дней по схеме: в 1-е сутки 5 приемов по 1 таблетке с интервалом 30 мин, затем 3 приема по 1 таблетке с интервалом 2-3 ч. В последующие дни - по 1 таблетке 3 раза в день. Для анализа результатов нами ретроспективно было проведено сравнительное исследование. Всего было отобрано 30 историй болезни взрослых больных, получавших Анаферон в комплексной терапии ЭМ, и столько же историй болезни взрослых больных, которым препарат не назначался. Данные группы были сравнимы между собой по полу, возрасту и другим параметрам, влияющим на результаты лечения (сроки госпитализации и начала лечения, наличие сопутствующей патологии). Согласно данным анализа, клинический эффект Анаферона проявился сокращением продолжительности лихорадочного периода (5,0 ± 0,8 против 7,2 ± 0,9 сут. в группе сравнения, p Таким образом, результаты проведенного исследования позволили охарактеризовать иммунологические особенности ЭМ у подростков и взрослых. Учет стартового уровня цитотоксических лимфоцитов и натуральных киллеров, или, как минимум, уровня лимфоцитов периферической крови, может позволить оптимизировать сроки проведений контрольного исследования ликвора и, как следствие, оптимизации стационарного лечения при ЭМ, определить показания к проведению иммунологического исследования и назначению иммунокорригирующей терапии. Результаты клинической оценки эффективности применения Анаферона позволяют поставить дальнейшие задачи в обосновании его ис- пользования в лечении ЭМ. С учетом наличия у Анаферона не только противовирусной активности, но и выраженного иммуномодулирующего компонента, а также способности индуцировать и регулировать синтез ИФН-у, мы считаем перспективным продолжить исследовать возможность его применения у больных энтеровирусным энцефалитом, у которых имеются снижения стартовых уровней CD3+/ИФН-у+-лимфоцитов, а также NK-клеток и цитотоксических лимфоцитов, в проспективном исследовании.
ЛИТЕРАТУРА
1. Бочаров Е.Ф., Ерман Б.А., Фомин В.В., и др. Энтеровирусная инфекция: Новые аспекты. Новосибирск: Наука. Сиб. отделение РАМН. 1990; 224.
2. Энтеровирусные заболевания: клиника, лабораторная диагностика, эпидемиология, профилактика: Методические указания (МУ 3.1.1.2130-06). М., 2006.
3. Лобзин Ю.В., Пилипенко В.В., Громыко Ю.Н. Менингиты и энцефалиты. СПб., 2001; 55-110.
4. Лашкевич В.А., Дроздов С.Г., Грачев В.П., и др. Неполиомиелитные энтеровирусные инфекции: эпидемиология, характеристика энтеровирусов, клиника, диагностика, профилактика: Методическое пособие. Федеральный центр Госсанэпиднадзора РФ. М., 2004.
5. Демина А.В., Маркович Н.А., Нетесов СВ. Энтеровирусы. Часть 1: история открытия, таксономия, строение генома, эпидемиология. Бюллетень СО РАМН. 2008; 1: 92-100.
6. Михайлов Е.В., Штейнберг А.В., Еремеева И.Г. Менингиты энтеровирусной этиологии у детей: современные подходы к диагностике и особенности клинического течения. Инфекционные болезни 2008; 6(1): 31–4.
7. Игнатов П.Е. Иммунитет и инфекция. М.: «Время», 2002; 352.
8. Фомин В.В., Чеснакова О.А., Ерман Б.А., и др. Энтеровирусные инфекции у детей. Екатеринбург, 1991; 38-98.
9. Кетлинский С.А., Калинина Н.М. Цитокины мононуклеарных фагоцитов в регуляции реакций воспаления и иммунитета. Иммунология 1995; 3: 30–44.
10. Кетлинский С.А., Симбирцев А.С., Воробьев А.А. Эндогенные иммуномодуляторы. СПб.: Гиппократ, 1992; 94.
11. Железникова Г.Ф. Роль цитокинов в патогенезе и диагностике инфекционных заболеваний. Инфекционные болезни 2008; 6(3): 70-6.
12. Хаитов Р.М., Пинегин Б.В. Современные представления о защите организма от инфекции. Иммунология 2000; 1: 62–4.
13. Ройт А., Бростофф Дж., Мейл Д. Иммунология. Пер с англ. В.И.Кандрора, А.Н.Маца, Л.А.Певницкого, М.А.Серовой. М.: Мир, 2000; 592.
14. Змушко Е.В., Белозёров Е.С., Митин Ю.А. Клиническая иммунология: руководство для врачей. СПб.: Питер, 2001; 576.
15. Кетлинский С.А., Калинина Н.М.. Иммунология для врача. СПб., 1998; 156.
16. Фрейдлин И.С. Иммунная система и ее дефекты: руководство для врачей. СПб., 1998; 113.
17. Billiau A. Interferon-y in autoimmunity. Cytokine & Growth Factor 1996; 7: 25-34.
18. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. М.: Медиа Сфера, 2006; 305.
Комментарии
ПРАКТИКА ПЕДИАТРА
