Кеппра в лечении эпилепсии
СтатьиМонография
Л.Р. Зенков
Оглавление
- Предисловие
-
1.1. Механизмы действия и фармакодинамика
1.2. Фармакокинетика и основные клинические характеристики - Глава 2. Клиническая эффективность Кеппры (леветирацетама)
-
2.1. Двойные слепые исследования политерапии резистентных припадков
2.1.1. Политерапия резистентных фокальных припадков
2.1.2. Политерапия резистентных генерализованных припадков
2.1.3 Леветирацетам в лечении некоторых специальных типов эпилептических припадков
2.2. Леветирацетам в монотерапии эпилептических припадков
2.3. Леветирацетам нормализует электрическую активность мозга
2.4. Действие леветирацетама на качество жизни и определяющие его психические, нейропсихологические и поведенческие функции мозга
2.5. Леветирацетам в лечении форм и синдромов эпилепсии
2.5.1. Леветирацетам в лечении идиопатических фокальных эпилепсий
2.5.2. Леветирацетам в лечении симптоматических и предположительно симптоматических фокальных эпилепсий
2.5.3. Кеппра (леветирацетам) в лечении идиопатических генерализованных эпилепсий
2.5.3.1. Эпилепсия с генерализованными тонико-клоническими припадками
2.5.3.2. Эпилепсии детского и юношеского возраста с абсансами
2.5.3.3. Доброкачественная миоклоническая эпилепсия в младенчестве
2.5.3.4. Юношеская миоклоническая эпилепсия
2.5.3.5. Эпилепсия с миоклонико-астатическими припадками и эпилепсия с миоклоническими абсансами
2.5.3.6. Эпилепсия с миолклонией век с абсансами
2.5.4. Леветирацетам в лечении фотосензитивных эпилепсий
2.5.5. Леветирацетам в лечении эпилептических энцефалопатий
2.5.5.1. Эпилептические энцефалопатии в младенческом возрасте
2.5.5.2. Синдром Леннокса-Гасто
2.5.5.3. Эпилептическая афазия Ландау-Клеффнера и другие расстройства речи, связанные с эпилепсией
2.5.5.4. Эпилепсия с постоянными комплексами спайк-волна в медленноволновом сне
2.5.5.5. Непароксизмальные психические, нейропсихологические и поведенческие эпилептические расстройства
2.5.6. Леветирацетам в лечении прогрессирующих миоклонических эпилепсий
2.5.7. Леветирацетам в лечении эпилептического статуса
2.5.8. Леветирацетам в специальных группах пациентов
2.5.8.1. Леветирацетам у детей
2.5.8.2. Леветирацетам у пожилых пациентов
2.5.8.3. Леветирацетам у женщин
Эндокринные функции и фертильность
Беременность и вскармливание
Косметические и эстетические факторы
2.5.9. Леветирацетам в особых ситуациях - Глава 3. Тактика клинического применения Кеппры (леветирацетама)
-
3.1. Выбор Леветирацетама
3.2. Подбор дозы
3.3. Переносимость леветирацетама и побочные эффекты - Заключение
- Предисловие
- На рубеже тысячелетий разработано и внедрено в клиническую практику не менее двух десятков новых эффективных препаратов для лечения эпилепсии, шесть из которых зарегистрированы для применения в Российской Федерации. Дополняя уже применяемые препараты первого и второго поколения, они создают новые возможности успешного лечения подбором для каждого пациента индивидуальной терапии. Это позволяет получить уже на раннем этапе контроль припадков и коррекцию межприступных эпилептических симптомов, предотвращает вторичную истинную фармакорезистентность из- за длительного безуспешного лечения неправильно выбранным препаратом или из-за иррациональной политерапии. Реализация такой идеологии требует правильности диагноза формы эпилепсии, знания особенностей выбора препарата при данной форме эпилепсии и, в особенности, полного знания фармакологических и терапевтических свойств применяемого препарата. Изложению в этом ключе необходимых знаний об одном из самых успешных новых противоэпилептических препаратов – Леветирацетаме (Кеппре) посвящена настоящая монография.
Леветирацетам характеризует оптимальное соотношение эффективности и безопасности. Он обладает принципиально новыми механизмами действия, широким спектром действия при всех основных формах эпилепсии и типах эпилептических припадков в поли- и монотерапии даже в случаях, когда все другие традиционные и новые препараты оказываются неэффективными. Будучи вначале предложен как препарат для лечения фокальных симптоматических эпилепсий, в процессе клинических испытаний и последующего практического применения он оказался эффективным при широком круге других эпилептических расстройств, включая многообразные формы генерализованных эпилепсий и тяжелых эпилептических энцефалопатий детского возраста. Важнейшим его свойством является высокая скорость титрования, позволяющая уже в первые дни назначения получить хороший терапевтический эффект, что особенно важно при лечении наиболее тяжелых случаев с частыми жизнеугрожающими припадками. Важной его клинической особенностью является минимум побочных эффектов и устойчивость терапевтического действия, что обеспечивает значительно больший процент долгосрочного удержания на препарате, чем у многих других противоэпилептических средств. Леветирацетам практически не взаимодействует с другими лекарствами, что делает его предпочтительным при сочетанной терапии [26, 61]. Терапевтический эффект сопровождается нормализацией электроэнцефалограммы и подавлением эпилептиформной активности, что обеспечивает не только контроль припадков, но и улучшение межприступного функционирования и соответственно качества жизни, предотвращает прогрессирование заболевания и способствует его излечению. Кеппрой с успехом пролечены сотни тысяч пациентов, и этот успех определяется уникальными фармакологическими свойствами препарата [80].
- Глава 1
Фармакологические свойства Кеппры (леветирацетама) -
- 1.1. Механизмы действия и фармакодинамика
- Леветирацетам был синтезирован в процессе исследований по усовершенствованию свойств ноотропа пирацетама (ноотропил). Леветирацетам является S-энантомером пирролидонового производного и имеет формулу: α-этил-2-окси-1-пирролидин ацетамид. Если в отношении ноотропных свойств его эффективность не ясна, то его противосудорожный и противоэпилептический потенциал в эксперименте и клинических испытаниях оказался чрезвычайно высоким, хотя был обнаружен не сразу. Объясняется это тем, что он не показал эффективности в обычных классических животных моделях острых судорог, вызванных химическими агентами и максимальным электрошоком, не изменял нормальную нейротрансмиссию. Однако испытания на других экспериментальных моделях выявили его высокий противоэпилептический потенциал.
Леветирацетам оказался высокоэффективным в экспериментальной эпилепсии, вызванной у мышей киндлингом (повторными электростимуляциями роговицы или введением пентилентетразола). Он также снижает тяжесть и число припадков при экспериментальных припадках, вызванных систематическим введением пилокарпина, каиновой кислоты, эффективен при фокальных припадках, вызванных киндлингом амигдалы [90 – 92, 100, 101].
Леветирацетам подавляет аудиогенные припадки у мышей с генетической предрасположенностью, предотвращая как неукротимый бег, так и последующие тонико-клонические судороги. Эффективность в этой модели является надежным предиктором клинической эффективности [66, 67]. Это положение было подтверждено многочисленными экспериментальными и клиническими испытаниями при разных формах эпилепсии [100]. Леветирацетам был высокоэффективен в лечении абсансной генетической эпилепсии крыс как в отношении клинических проявлений, так и в подавлении спайк-волновых разрядов [66]. Эта эффективность была убедительно показана в клинике при лечении детской и юношеской абсансной эпилепсии [22, 30, 35, 98, 100]. Как в отношении ЭЭГ, так и в поведенческих проявлениях леветирацетам в экспериментах не оказывал влияния на нормальную мозговуюактивность, за исключением легкой седации при чрезмерно высоких дозах [66].
Доклинические испытания заставляют предполагать антиэпилептогенную эффективность леветирацетама, что отличает его от большинства других противоэпилептических препаратов. Это значит, что он не просто подавляет актуальную эпилептическую активность в мозге, но может препятствовать ее возникновению и прогрессированию. Это было обнаружено в экспериментах, где созданию киндлинговой модели эпилепсии у мышей предшествовало введение им леветирацетама. Такая предподготовка значительно снижала наклонность к развитию экспериментальной эпилепсии вследствие киндлинга, как на фоне продолжающегося лечения леветирацетамом, так и после его прекращения [110, 166].
Удивительным образом при уже показанной высокой экспериментальной и клинической эффективности фармакодинамические механизмы противоэпилептического действия леветирацетама длительно оставались неясными. Фармакодинамикой препарата называется его взаимодействие с нейрональным субстратом на уровне мембран нейронов и синаптических образований, обусловливающее его специфический лечебный эффект или побочные действия. С этой точки зрения леветирацетам представляет собой достаточно необычный препарат. Обнаружились его уникальные свойства в отношении ряда важнейших механизмов эпилептогенеза, отличающие его от других антиконвульсантов (Рис. 1).
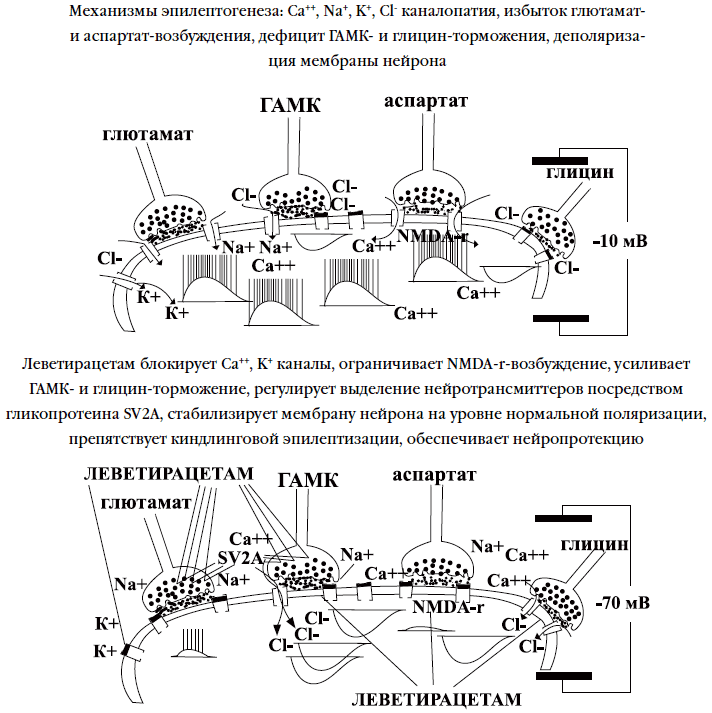
Рис.1. Механизмы действия Кеппры (см. Таблицу 1)Таблица 1.
Известные к настоящему времени механизмы противоэпилептического действия Леветирацетама.1 Регуляция выделения нейротрансмиттера из синаптических пузырьков посредством взаимодействия с активным гликопротеином синаптических везикул SV2A 2 Усиление ГАМК-эргического и глицинэргического торможения блокированием эф- фекта цинка и карболинов, восстановление тем самым притока хлоридов через ГАМК- и глициновые рецепторы и стабилизация мембраны нейронов 3 Блокирование эпилептических разрядов, вызванных бикукуллином и активацией NMDA-рецепторов, не влияя на нормальное проведение возбуждения 4 Торможение высоковольтных Са++каналов N- и P/Q-типа, что приводит к подавлению пароксизмальных деполяризационных сдвигов, характерных для эпилептических нейронов 5 Подавление пароксизмальных деполяризационных сдвигов и эпилептических спайковых разрядов нейронов гиппокампа , обусловленное снижением тока в зависимых от напряжения К+ каналах 6 Блокирование киндлинговой эпилептогенной экспрессии генов 7 Подавление эпилептиформной активности и эпилептической синхронизации нейронов 8 Нейропротекция в отношении эксайтотоксического действия активации NMDA-рецепторов Было показано его связывание с гликопротеином синаптических везикул SV2A, содержащимся в сером веществе головного и спинного мозга. Посредством этого связанного с синаптическими пузырьками белка леветирацетам регулирует динамику в синаптической бляшке и выброс нейротрансмиттеров в синаптическую щель, снижая эпилептическую активность нейрона [108].
Другим механизмом действия леветирацетама является модуляция ГАМК-эргических и глициновых рецепторов, которые снижают возбудимость нейрона, причем ГАМК-эргическое взаимодействие является главным механизмом торможения в мозге, обеспечивающим лечебный эффект многих противоэпилептических препаратов. Тормозной эффект ГАМК и глицина осуществляется в значительной мере за счет активации притока ионов хлора внутрь нейрона, чем достигается эффект тормозной гиперполяризации. В блокаде притока хлоридов в ГАМК-эргических и глицинэргических рецепторах участвуют цинк и R-карболины. Леветирацетам является единственным противоэпилептическим препаратом, который противодействует блокирующему притоку ионов хлора эффекту цинка и R-карболинов, тем самым восстанавливает приток хлоридов через ГАМК- и глициновые рецепторы и приводит к усилению торможения в нейронах [48].
Помимо активации тормозных эффектов в мозге леветирацетам блокирует в культуре ткани эпилептические разряды, вызванные бикукуллином и активацией NMDA-рецепторов, не влияя при этом на нормальное проведение возбуждения [20]. Это может объяснять хорошую переносимость препарата и отсутствие существенных седативных эффектов при терапевтичнеских дозировках при лечении больных [92]. Избыточный приток ионов кальция внутрь клетки, приводящий к ее избыточной импульсной активности, является механизмом эпилептического возбуждения, а также влечет пластическое эпилептогенное перерождение нейронов и их эксайтотоксическую гибель. Леветирацетам специфически тормозит высоковольтные кальциевые каналы N- и частично P/Q-типа, в отличие от других противоэпилептичеких препаратов, блокирующих Т-каналы. Это действие Леветирацетама приводит к сокращению амплитуды и длительности вызываемых интрацеллюлярным притоком йонов кальция пароксизмальных деполяризационных сдвигов, характерных для эпилептических нейронов [136].
M.Madeja et al. (2003) в культуре ткани области CA1 гиппокампа показали достоверное снижение пароксизмальных деполяризационных сдвигов и эпилептических спайковых разрядов нейроновпод влиянием леветирацетама, обусловленное снижением тока в зависимых от напряжения калиевых каналах [112].
Одним из механизмов эпилептогенеза и возникновения некурабильной эпилепсии является изменение генной экспрессии, возникающее по механизму киндлинга в нейронах, подвергающихся возбуждению посредством эпилептической афферентации. J. Gu et al. исследовали на модели, вызванной киндлингом амигдалы височной эпилепсии у мышей. Снижение эффекта киндлинга под влиянием леветирацетама сопровождалось снижением эпилептической генной экспрессии в нейронах, показавшим, что антиэпилептогенный эффект леветирацетама осуществляется на генном уровне [71]. Этот фармакодинамический генный механизм, очевидно, является основой упомянутого выше антиэпилептогенного действия леветирацетама [110,111].
Исследования суммарной спайковой эпилептиформной активности в культуре ткани высоко эпилептогенной гиппокампальной зоны CA3 показали уникальную способность леветирацетама подавлять эпилептическую синхронизацию нейронов, в отличие от других противоэпилептических препаратов, использовавшихся в тех же экспериментах [116]. Эффективное подавление эпилептиформной активности выявлено также при лечении больных эпилепсией [58].
Наконец, в исследовании изменений мозга при экспериментальной окклюзии средней мозговой артерии было показано, что леветирацетам уменьшает объем инфаркта на треть, что связывают с нейропротекцией в отношении эксайтотоксического действия активации NMDA-рецепторов в зоне ишемии [75].
Известные к настоящему времени механизмы противоэпилептического действия Леветирацетама.
Таким образом, к настоящему времени выяснены некоторые важные механизмы противоэпилептического действия леветирацетама. Основной особенностью его является значительное отличие по этим механизмам от известных традиционных и новых препаратов. Именно это делает леветирацетам высокоэффективным, причем и в случаях резистентности к другим препаратам. Наиболее важными особенностями его действия являются регуляторная активность в отношении динамики нейротрансмиттеров, связанная с гликопротеином синаптических везикул SV2A, регуляция токов в кальциевых и калиевых каналах, способность противодействовать патологической нейрональной синхронизации, лежащей в основе эпилептического процесса, противодействие эпилептогенезу, обусловленному киндлингом, в том числе на уровне эксперссии генов. Те же антикиндлинговые механизмы вкупе с блокадой кальциевых каналов и модуляцией активности NMDA-рецепторов определяют нейропротекторные свойства леветирацетама [92, 171].
- 1.2. Фармакокинетика и основные клинические характеристики
- Фармакокинетикой называется перемещение и метаболизм препарата от момента введения в организм до его вывода, разрушения или ассимиляции. Фармакокинетика определяется абсорбцией препарата, связыванием протеинами плазмы, метаболизмом печени, скоростью разрушения и экскрецией. Леветирацетам хорошо растворим, благодаря полному всасыванию, носящему линейный характер, концентрация в плазме может быть предсказана в зависимости от примененной дозы [37]. Биодоступность близка к 100%. После приема 1000 мг максимальная концентрация достигается через 1,3 ч и составляет 31 мкг/мл при однократном приеме; после повторного приема (2 раза в день) – 43 мкг/мл. Равновесное состояние достигается через 2 сут. при приеме препарата 2 раза в день.
Прием пищи не влияет на степень всасывания, но снижает максимальную концентрацию на 20% и увеличивает время достижения максимальной концентрации на 1,5 часа [51].
Леветирацетам и его основной метаболит не связываются в значительных количествах с белками плазмы (<10%). Объем распределения леветирацетама составляет приблизительно 0,5 – 0,7 л/кг. Образование первичного фармакологически неактивного метаболита (ucb L057) происходит без участия цитохрома P450 печени, поэтому леветирацетам практически не взаимодействует с индукторами или ингибиторами ферментов печени. Леветирацетам не влияет на ферментативную активность гепатоцитов. Время снижения концентрации препарата в крови до половинной в плазме крови взрослого человека составляет 7±1 часов и не изменяется в зависимости от дозы, способа применения или кратности приема. Средний клиренс – 0,96 мл/мин; 95% препарата выводится почками. Почечный клиренс леветирацетама и ucb L057 составляет 0,6 и 4,2 мл/мин/кг соответственно.
У пожилых людей период полувыведения увеличивается на 40% (10 – 11 ч), что связано с ухудшением функции почек у этой категории лиц. В процессе 4-часового диализа удаление леветирацетама достигает 51%. У больных с легкой и средней степенью нарушения функции печени видимых изменений в клиренсе леветирацетама не обнаружено. У большинства больных с тяжелыми нарушениями функции печени клиренс леветирацетама снижается более чем на 50% из-за сопутствующей почечной недостаточности [25].
В настоящее время в России препарат зарегистрирован в качестве дополнительной терапии для лечения больных парциальной эпилепсией (с парциальными припадками со вторичной генерализацией или без нее). Вместе с тем при информированном согласии пациента не противопоказано использование его и в монотерапии эпилепсии.
Противопоказанием к применению является повышенная чувствительность к леветирацетаму или другим производным пирролидона, а также к любым компонентам препарата. Препарат не рекомендуют применять во время беременности, однако, по данным сводного регистра беременности при эпилепсии Великобритании, при лечении леветирацетамом не зарегистрировано ни одного случая больших мальформаций плода, в отличии от других противоэпилептических препаратов [123]. Как и при лечении другими противосудорожными средствами, вопрос о переходе на другой препарат во время беременности должен решаться взвешиванием рисков лечения леветирацетамом или обострения эпилепсии при переходе на другой препарат, относительная безопасность которого сравнительно с леветирацетамом не доказана. Хотя препарат не рекомендуется применять в период грудного вскармливания, в специальных исследованиях показано, что хотя он в значительном объеме попадает в молоко матери, концентрации его в плазме вскармливаемого младенца клинически незначимы из-за высокой скорости элиминации [82].
Хотя препарат не рекомендуется пациентам в возрасте до 16 лет, имеются десятки публикаций, посвященных лечению детей леветирацетамом в поли и монотерапии, начиная с младенчества, свидетельствующих о высокой эффективности и безопасности применения его в этой возрастной группе.
Кратко основные фармако-клинические характеристики леветирацетама приведены в таблице 2.
Таблица 2.
Основные фармако-клинические характеристики ЛеветирацетамаРодовое название: Леветирацетам (Levetiracetam) Химическая формула: Sэнантомер пирролидонового производного с формулой: α-этил-2-окси-1-пирролидин ацетамид Механизм действия: Модулирует динамику тормозных и возбуждающих нейротрансмиттеров посредством взаимодействия с гликопротеином синаптических везикул SV2A, модулирует N-кальциевые каналы, усиливает ГАМК-эргическое и глицинэргическое торможение блокированием активности цинка и карболинов Торговое название: Кеппра Содержание в торговых формах: Таблетки: Кеппра 250 мг, 500 мг, 1000 мг; 20% раствор для приема внутрь, раствор для внутривенного введения (две последние формы в России – в стадии регистрации) Эффективен: Эпилепсии с фокальными, фокальными с нарушением сознания, вторично-генерализованными, первично-генерализованными припадками, эпилептические энцефалопатии Период полувыведения: 7±1 час Время выравнивания концентрации: 2 дня при двухразовом в сутки приеме Концентрация в плазме: После приема 1000 мг через 1,3 часа – 31 мкг/мл, после повторного за сутки приема – 43 мкг/мл Терапевтическая доза: Пациенты старше 12 лет: первые 2 недели: 500 мг два раза в день.
При необходимости – увеличение дозы на 500 мг не ранее 2 недель.
Допустимая доза – 1500 мг 2 раза в деньКратность приема: 2 раза в день Взаимодействие: Не взаимодействует с другими противоэпилептическими препаратами (фенитоин, карбамазепин, вальпроевая кислота, фенобарбитал, ламотриджин, габапентин, примидон).
Леветирацетам в суточной дозе 1000 мг не изменяет фармакокинетику пероральных контрацептивов (этинилэстрадиол, левоноргестрел) и в суточной дозе 2000 мг – дигоксина и варфарина
В связи с приемом пищи темп всасывания несколько замедляетсяПобочные действия: Наиболее часто – сонливость, астенический синдром, головокружение; реже – головная боль, анорексия, диарея, диспепсия, тошнота, атаксия, судороги, депрессивный синдром, эмоциональная неустойчивость, агрессивность, бессонница, нервозность, тремор, кожная сыпь, диплопия Дополнительные замечания:
Пожилым пациентам и больным с почечной недостаточностью рекомендуется индивидуальный подбор дозы.
При необходимости отмены лечения рекомендуется постепенное прекращение приема препарата (разовая доза уменьшается на 500 мг каждые 2 – 4 недели).
В период лечения необходимо воздерживаться от вождения автотранспорта и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (исследований по воздействию препарата на способность управлять автомашиной или иными механизмами не проводилось).Способ применения:
Таблетки с пленочным покрытием следует принимать внутрь, запивая достаточным количеством жидкости, вне зависимости от приема пищи.Режим дозирования:
При дуо- или политерапии 1000 – 3000 мг в сутки в два приема. Начальная лечебная доза – 500 мг 2 раза в сутки.
Суточная доза может быть увеличена в зависимости от клинической реакции и переносимости до 1500 мг 2 раза в сутки.
Изменение дозы на 500 мг может осуществляться каждые 2 – 4 недели.
При монотерапии стартовая доза 250 мг 2 раза в сутки.Передозировка:
Симптомы: сонливость, тревога, агрессия, угнетение сознания, угнетение дыхания, кома.
Лечение: первая помощь – прием активированного угля и промывание желудка. При необходимости проводится симптоматическое лечение в условиях стационара с использованием гемодиализа (выводится на 60%). Специфического антидота не существует.Таким образом, фармакологические свойства леветирацетама позволяют характеризовать его как препарат эффективный в лечении разнообразных экспериментальных форм фокальной и генерализованной вызванной киндлингом и генетически обусловленной эпилепсии. Это согласуется с клиническими данными, о его эффективности при широком спектре форм эпилепсии и типов эпилептических припадков. Леветирацетам имеет прекрасные фармакокинетические свойства, обеспечивающие быстрое всасывание после приема внутрь, превосходную биодоступность, линейную кинетику в плазме, минимальное связывание белками плазмы, быстрое достижение устойчивой концентрации, отсутствие взаимодействия с другими противоэпилептическими препаратами, хорошую переносимость и низкий риск токсичности [37, 61, 80, 127, 168].
- Глава 2
Клиническая эффективность Кеппры (леветирацетама) -
- 2.1. Двойные слепые исследования политерапии резистентных припадков
- Любой новый препарат, по соображениям деонтологии, испытывается сначала только в качестве дополнительного в политерапии у пациентов, у которых терапия другими препаратами в моно- и политерапии не эффективна. Испытания леветирацетама в этой парадигме первоначально проводились при фокальных эпилептических припадках.
- 2.1.1. Политерапия резистентных фокальных припадков
-
Начало использования Кеппры (леветирацетама) при лечении фокальных припадков обусловливалось их наибольшей распространенностью и наиболее частой фармакорезистентностью к традиционным и другим новейшим препаратам. Эффективность его в этой парадигме была показана в нескольких исследованиях. Решающими, по принятым критериям, являются данные, полученные в плацебо-контролируемых двойных слепых исследованиях. В двойном слепом рандомизированном плацебо-контролированном мультицентровом параллельном исследовании J.J. Cereghino et al (2000) и Американской группы по исследованию леветирацетама оценивали эффективность и безопасность суточных доз в 1000 мг и 3000 мг в течение 14 недель лечения в политерапии у пациентов с частыми резистентными к другим препаратам припадками. 268 рандомизированных пациентов прошли полный курс исследования. Высоко значимое (p В Великобритании в аналогичном мультицентровом исследовании оценивали результаты применения доз 2000 и 4000 мг/сутки, принимавшихся в течение 24 дней. Значимое уменьшение числа припадков было получено у 48,1% и 28,6% соответственно, обе дозы переносились достаточно хорошо, хотя на большей чаще наблюдалась сомноленция [17].
Итоги испытаний в двойных слепых плацебо-контролированных исследованиях, проведенных к 2001 году, показали, что леветирацетам является высокоэффективным и безопасным препаратом в лечении рефрактерных к другим противосудорожным лекарствам фокальных и вторичногенерализованных припадков как дополнительный препарат в дозах 1000 – 3000 мг/кг в сутки. Была показана эффективность леветирацетама в дополнительной терапии детей (дозы – 10 – 40 мг/кг/день) с рефрактерными фокальными припадками. Суммарное количество побочных эффектов не превышало таковое при приеме плацебо, отсутствие фармакокинетического взаимодействия обеспечивает удобство применения в политерапии [50, 80, 127, 138]. Эти общие выводы были в дальнейшем неоднократно подтверждены в исследованиях первого класса доказательности [47, 56, 105, 157]. В контролированном исследовании O. Devinsky и C. Elger (2003) при применении суточных доз 1000 – 3000 мг в комбинированной терапии результаты оказались лучше, чем в первых, цитированных выше: у 54% пациентов наблюдалось снижение числа припадков на 50% и более, у 35% достигнуто полное их прекращение [47].
Важные особенности терапевтического эффекта леветирацетама выявлены в двойных слепых контролированных исследованиях J. French et al. [56]. При анализе результатов трехмесячного лечения ими отмечено достижение хорошего эффекта уже в первые дни приема целевой дозы, причем эффект этот нарастает в течение первой недели. Достигнутое улучшение было стабильным на протяжении всего трехмесячного периода наблюдения. Долгосрочная стойкость положительного клинического эффекта показана при анализе результатов самостоятельного продолжения лечения леветирацетамом пациентов, закончивших участие в двойных слепых контролированных исследованиях. В этом долгосрочном не сравнительном открытом исследовании, включавшем 36 населенных пунктов США, оценивалась эффективность продолжения комбинированного лечения леветирацетамом в дозах 1000 – 4000 мг/сутки у 280 пациентов каждые 12 недель в течение 4 лет. 71,1% к концу срока продолжали принимать препарат благодаря его эффективности [3].
В сравнительном мета-анализе всех доступных публикаций по эффективности и отказу от лечения леветирацетамом, окскарбазепином, ремацемидом и зонизамидом, включавшем данные 1023, 961, 388 и 499 пациентов соответственно, показано наилучшее отношение эффективность/переносимости для леветирацетама [117]. В другом мета-анализе сравнивали леветирацетам, габапентин, ламотриджин, окскарбазепин, тиагабин, топирамат и зонизамид в качестве дополнительных в лечении фармакорезистентных фокальных эпилептических припадков, по данным рандомизированных плацебо-контролированных исследований. Леветирацетам оказался лучше по показателю эффективности и переносимости, чем габапентин и ламотриджин, равноэффективен с остальными препаратами и лучше переносимым, чем тиагабин и зонизмид. Ни от одного из препаратов по показателям эффективности и переносимости он не отличался в худшую сторону [132]. По данным аудита, проводившегося для сравнения леветирацетама, ламотриджина и топирамата как дополнительных препаратов, наиболее и равно эффективными оказались и леветирацетам и топирамат, однако леветирацетам переносился значительно лучше [33].
- 2.1.2. Политерапия резистентных генерализованных припадков
-
Первоначально леветирацетам изучался как препарат при фокальных припадках, но вскоре обнаружилась его высокая эффективность в лечении первично-генерализованных эпилептических приступов. В отдельных наблюдениях и открытых исследованиях было показано, что леветирацетам в дополнительной терапии подавляет абсансы и соответствующие им эпилептиформные разряды в ЭЭГ, снижает частоту генерализованных тонико-клонических, миоклонических припадков, в частности, при часто некурабильном постаноксическом и постэнцефалитическом миоклонусе [30, 39, 83, 118, 140, 146, 154, 155, 167]. S. Kumar и P. Smith приводят данные лечения в течение не менее шести месяцев 22 пациентов с генерализованными припадками, включая 13 пациентов с юношеской миоклонической эпилепсией. У 68% наблюдалось улучшение, у трех из них – полное прекращение припадков [99]. G. Krauss et al. лечили в течение 12 недель 55 пациентов с идиопатическими генерализованными припадками (миоклоническими, тонико-клоническими и абсансами). У 76% отмечалось >50% снижение числа припадков, у 40% – полное прекращение [98]. По данным B. Chappell и P. Crawford, леветирацетам как дополнительный препарат наиболее эффективен в лечении идиопатических генерализованных припадков [33]. В проведенном W.E. Rosenfeld et al. (2006)* o мультицентровом рандомизированном двойном слепом плацебо-контролированном исследовании у пациентов с первично-генерализованными эпилепсиями присоединение в качестве дополнительного препарата леветирацетама дало уменьшение числа припадков на ≥50% у 72,2% пациентов и полное прекращение – у 24,1%.
* Rosenfeld W.E. et al. Efficacy and Safety of Levetiracetam 3000 mg/day (Pediatric Target Dose 60 mg/kg/ day) as Adjunctive Therapy in Adult and Pediatric Idiopathic Generalized Epilepsy Patients Experiencing Primary Generalized Tonic-Clonic Seizures // // 58 th Annual Meeting American academy of Neurology (AAN 58 th Annual Meeting),San Diego, California (USA) April 1-8, 2006. - 2.1.3. Леветирацетам в лечении некоторых специальных типов эпилептических припадков
-
В оценке эффективности любого нового препарата особый интерес представляет его способность оказывать помощь при возможно более широком круге эпилептических припадков, и в этом отношении имеют значение не столько массовые рандомизированные статистические исследования, сколько наблюдения, касающиеся разнообразных припадков, может быть, не самых частых, но представляющих особый интерес из-за их тяжести и некурабильности другими препаратами.
Драматически впечатляющее улучшение отметили P. Gelisse et al. при лечении леветирацетамом одного из наиболее труднокурабильных типов припадков – негативного миоклонуса. Негативным миоклонусом называется внезапная кратковременная (доли секунды) утрата постурального тонуса, приводящая к падению или внезапному изменению позы. У женщины, с возраста 2 лет страдавшей приступами внезапного падения и внезапного обвисания рук, не поддававшимися лечению другими препаратами в достаточных дозах в моно- и политерапии, добавление к вальпроату 2000 мг/сутки леветирацетама привело к практическому прекращению припадков (за год – 1 приступ) [59].
Особое значение имеет показанное во многих исследованиях значительное улучшение в случаях некурабильного миоклонуса при дегенеративных заболеванияхи других энцефалопатиях [44, 57].
Таким образом, в серии контролированных исследований первого класса надежности была доказана эффективность леветирацетама в качестве дополнительного препарата при разнообразных (тонических, тонико-клонических, атонических, миоклонических) фокальных и генерализованных припадках. Эти данные были подтверждены в многочисленных открытых исследованиях, которые позволили оценить истинную клиническую эффективность препарата и выявили лучшие результаты, поскольку врач имеет возможность индивидуально выбирать тактику лечения и дозы препарата. Успешность препарата была показана в том числе при наиболее тяжелых, обычно некурабильных типах припадков, в частности при симптоматическом миоклонусе. Убедительно показана стойкость клинического эффекта на протяжении многих месяцев и лет лечения [68].
- 2.2. Кеппра (леветирацетам) в монотерапии эпилептических припадков
- Основным правилом лечения вновь диагностированной эпилепсии является монотерапия правильно выбранным препаратом. Длительный период безуспешной терапии неправильным препаратом (всегда предшествующий периоду политерапии) влечет вторичную резистентность, чем и объясняет я относительно меньший успех в начальных испытаниях новых препаратов в политерапии. Хотя, по процедурным соображениям, леветирацетам в России пока рекомендован в качестве дополнительного противоэпилептического препарата в политерапии фармакорезистентных припадков, в большинстве стран он зарегистрирован как препарат для монотерапии эпилепсии. Имеется ряд работ, показывающих эффективность при переходе от политерапии к монотерапии леветирацетамом, а также при первоначальной монотерапии. T. Alsaadi et al. наблюдали 9 пациентов на первоначальной монотерапии и 28 переведенных с поли- на монотерапию фокальных эпилептических припадков, леченных в этом режиме не менее 6 лет. У 13 наступила ремиссия и у 15 отмечалось снижение числа припадков более чем на половину [7]. J. Cohen использовал леветирацетам в дозах 1250 – 3000 мг/сутки для монотерапии резистентных к другим препаратам первично-генерализованных эпилепсий с абсансами, миоклоническими и тонико-клоническими припадками. У всех пациентов на монотерапии леветирацетамом наблюдалось полное прекращение припадков на период не менее 6 месяцев наблюдения и прекращение эпилептиформной спайк-волновой активности в ЭЭГ [35].
E. Ben-Menachem и U. Falter опубликовали результаты мультицентрового двойного слепого плацебо-контролированного исследования монотерапии резистентных к другим препаратам эпилепсий с фокальными припадками, проведенного в рамках работы Европейской группы по исследованию леветирацетама. Оценивали эффективность монотерапии дозой 3000 мг/сутки в течение 12 недель. Отмечалось снижение числа припадков по группе на 73.8% (p = 0,037). Из 69 получавших монотерапию леветирацетамом пациентов у 59,2% отмечалось уменьшение числа припадков более чем на 50%, у 18,4% отмечалась ремиссия [15].
Эффективность леветирацетама (245 пациентов) в монотерапии вновь диагностированной эпилепсии оценивалась в проведенном E. Ben-Menachem et al. (2006)* o рандомизированном двойном слепом исследовании в сравнении с традиционным препаратом – карбамазепином с контролируемым высвобождением (291 пациент). Результаты оказались одинаковыми: из больных с вновь диагностированными парциальными или генерализованными припадками ремиссия, продолжительностью 6 месяцев, была достигнута при лечении леветирацетамом у 73,0%, карбамазепином – у 72,8%, годичная ремиссия – у 56,6% и 58,5%, соответственно. Это исследование, помимо первого класса доказательности, имеет важное значение в плане тактики лечения. Очень высокий процент ремиссии, в отличие от других исследований, очевидно, объясняется тем, что исследованные группы были представлены ранее не получавшими противоэпилептической терапии пациентами. Это значит, что для получения наилучших результатов в лечении эпилепсии леветирацетамом наиболее целесообразно использовать его как препарат первого выбора в монотерапии.
Таким образом, как в плацебо-контролированных, так и в открытых исследованиях показана высокая эффективность и безопасность леветирацетама в монотерапии в дозах не больших, чем при политерапии у пациентов при начальном лечении и с резистентными к другим препаратам фокальными и первично-генерализованными припадками.
*Ben-Menachem E., Brodie M.J., Perucca E. (LEV N1061 Study Group). Efficacy of Levetiracetam Monotherapy; Randomized Double-Blind Headto-Head-Comparison with Carbamazepine-CR in Newly Diagnosed Epilepsy Patients with Partial Onset or Generalized Tonic-Clonic Seizures // 58 th Annual Meeting American academy of Neurology (AAN 58 th Annual Meeting),San Diego, California (USA).
- 2.3. Кеппра (леветирацетам) нормализует электрическую активность мозга
- В настоящее время при лечении эпилепсии уделяется значительное внимание влиянию препаратов на нейрофизиологическое функционирование мозга. Особое значение имеет подавление в ЭЭГ межприступной эпилептиформной активности, поскольку она свидетельствует о персистировании в мозге эпилептических разрядов, поддерживающих посредством киндлинга эпилептический процесс и вызывающих нарушения, нередко необратимые, основных функций мозга, то есть приводящих к эпилептической энцефалопатии [1]. Леветирацетам в этом отношении обладает уникальными свойствами, не наблюдаемыми в отношении других противоэпилептических препаратов в эксперименте. In vitro показано подавление леветирацетамом пароксизмальных деполяризационных сдвигов с избыточными разрядами спайков в одиночных клетках и гиперсинхронии и эпилептиформных разрядов в группах нейронов, как в культурах гиппокампа крыс [116, 130], так и при исследовании эпилептогенной новой коры, удаленной при хирургическом лечении эпилепсии у человека [65]. Исследования in vitro подтверждены подавлением под влиянием леветирацетама в терапевтических дозах эпилептиформных разрядов спайк-волна на генетических моделяхэпилепсии у крыс [23].
В соответствии с экспериментальными исследованиями в многочисленных клинических работах показано эффективное подавление леветирацетамом эпилептиформной активности в ЭЭГ, чему соответствует клиническое улучшение как в отношении припадков, так и межприступных когнитивных и поведенческих нарушений [12, 35, 58, 85, 103, 142].
Подавление эпилептиформных разрядов при лечении леветирацетамом было показано в исследовании первого класса доказательности (двойном слепом плацебоконтролированном): леветирацетам эффективно подавлял эпилептиформную активность как при принятии единичной дозы 500 мг, так и при долгосрочном лечении [158]. Исчезновение эпилептиформной активности мы систематически наблюдали у наших пациентов при лечении леветирацетамом (Кеппрой) (Рис. 2).
Подавление эпилептических разрядов, детектируемых в ЭЭГ как эпилептиформная активность, приводит к прекращению явления киндлинга, способствующего поддержанию и прогрессированию эпилептического процесса, и препятствует развитию эпилептической энцефалопатии, являющейся следствием межприступных эпилептических разрядов в ЭЭГ [1, 71, 111].
Рис. 2.Изменения электроинцефалограммы в процессе лечения пациента 33 лет с лобнодолевой эпилепсией с комплексными парциальными припадками из орбитофронтальной коры
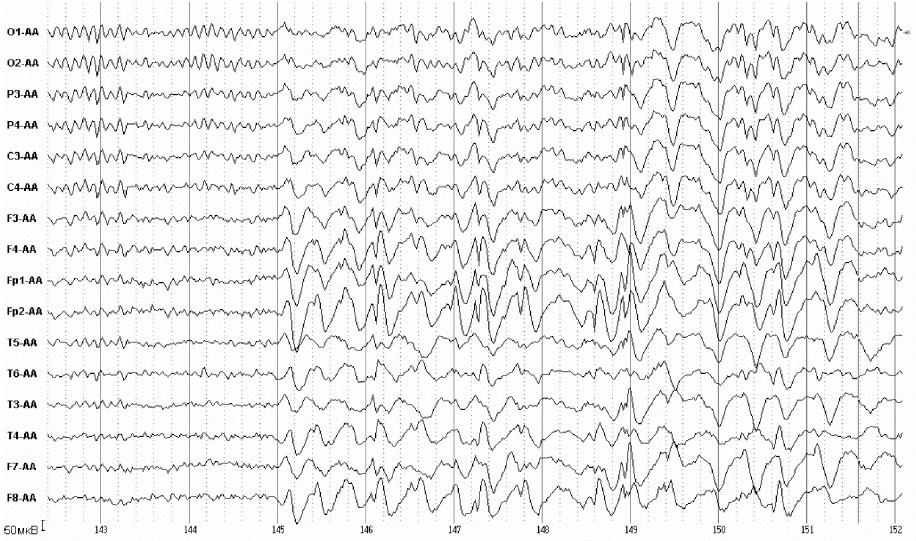
1) Генерализованные билатерально-синхронные разряды комплексов острая волна-медленная волна до 250 мкВ амплитудой по типу паттернов эпилептического припадка, следующие с интервалами 20 – 90 секунд. По 5 – 6 клинических припадков в день. Получает 800 мг финлепсина в сутки.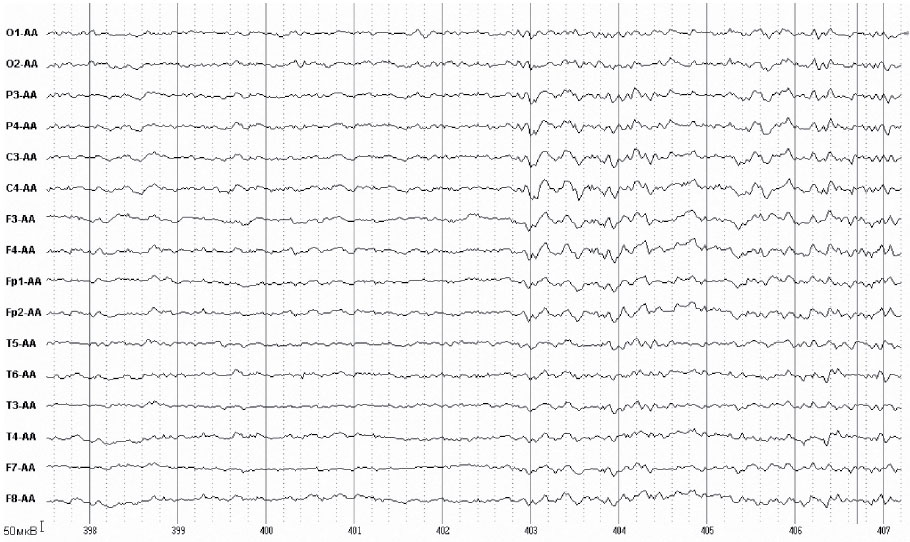
2) Отменен финлепсин; на 2500 мг/сутки Кеппры – значительная нормализация ЭЭГ: вспышки медленных волн и редуцированных острых волн до 50 – 70 мкВ амплитудой наблюдаются с интервалами в 5 – 10 мин. Уменьшение частоты клинических припадков до 1 в 2 недели.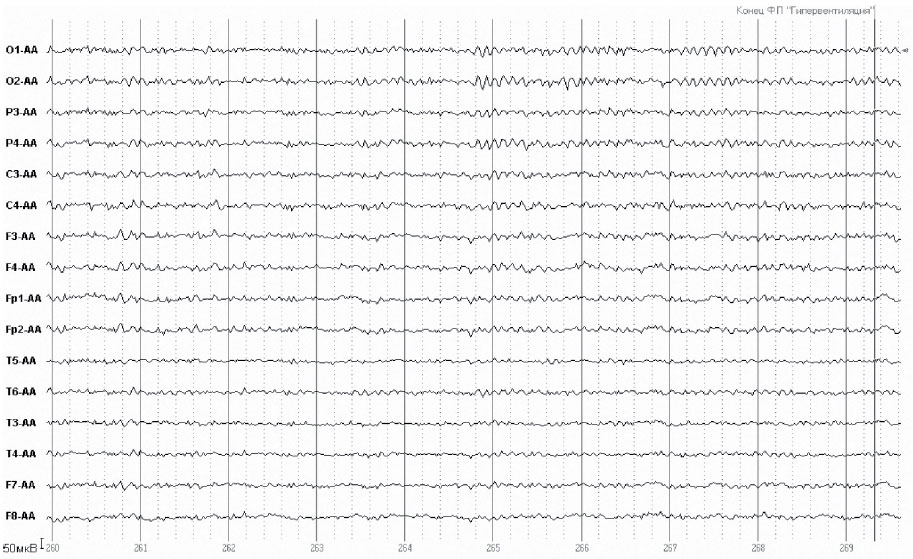
3) Комбинированное лечение Ламикталом 300 мг/сутки+Кеппра 2500 мг/сутки привело к полной нормализации ЭЭГ. Ремиссия припадков в течение 1,5 лет наблюдения. - 2.4. Действие Кеппры (леветирацетама) на качество жизни и определяющие его психические, нейропсихологические и поведенческие функции мозга
- Леветирацетам обладает благоприятным воздействием на психические параметры, определяющие качество жизни пациента. Сравнение с плацебо при лечении леветирацетамом в дополнительной терапии показало достоверное улучшение общего рейтинга качества жизни по показателю уменьшения общего дистресса (P<0,0001). Максимальное и статистически значимое улучшение касалось социального функционирования и когнитивных функций [40, 43]. A.Piazzini et al. сравнивали нейропсихологические показатели у 35 пациентов с фокальной эпилепсией. Отмечалось статистически значимое улучшение когнитивных параметров в группе и в сравнении с группой контроля, не получавшей за тот же период леветирацетама. Значимое улучшение касалось уровня внимания, вербальной беглости и других языковых функций. Авторы в качестве одного из механизмов эффекта предполагают ноотропный эффект, аналогичный действию пирацетама, дериватом которого является леветирацетам [136]. Позитивный эффект леветирацетама в отношении когнитивных и, в частности, речевых функций делает его препаратом выбора у пациентов с трудностями обучения, задержкой развития, нарушениями речи, психическими расстройствами, при лечении которых отмечается улучшение настроения, внимания, речевых функций, сна, аппетита, ясности сознания, поведения, исчезает психотическая симптоматика [11, 19, 78, 85, 159]. В нескольких исследованиях показано улучшение речевых функций при лечении леветирацетамом, включая эпилептическую афазию Ландау-Клеффнера, речевую диспраксию при атипичных идиопатических эпилепсиях детского возраста, заикании у детей и взрослых [28, 104, 150].
Учитывая особую роль эпилептической дисфункции мозга в развитии аутизма [1], леветирацетам используется в попытках лечения детского аутизма. Отмечалось статистически значимое улучшение в отношении дефицита внимания, гиперактивности и импульсивности, оценивавшимся по шкале внимания Ахенбаха, полной шкале DSM-IV Коннера и шкале индекса расстройства дефицита внимания и гиперактивности. Отмечалась стабилизация настроения по шкалам глобального индекса эмоциональной лабильности Коннера и глобального индекса Коннера. Отмечалось также улучшение по шкале агрессии Ахенбаха у детей, безуспешно лечившихся от аутизма рисперидоном, карбамазепином и дезипрамином [144].
- 2.5. Кеппра (леветирацетам) в лечении форм и синдромов эпилепсии
- Лечение эпилепсии следует проводить исходя из формы эпилепсии, поскольку недоучет этого фактора повлечет неэффективность или даже вызовет утяжеление заболевания. Поэтому для лечения леветирацетамом особое значение имеет опыт его применения при конкретных формах и синдромах эпилепсии.
- 2.5.1. Кеппра (леветирацетам) в лечении идиопатических фокальных эпилепсий
- Леветирацетам эффективен в лечении идиопатической эпилепсии детского возраста с центротемпоральными спайками. Эта форма эпилепсии часто дает осложнения в виде речевых и других нейропсихологических и поведенческих расстройств. При неэффективности других препаратов, обычно применяемых для лечения этого заболевания, присоединение леветирацетама подавляет эпилептиформную активность в ЭЭГ, обеспечивает контроль припадков и коррекцию межприступных нарушений [13]. G. Coppola et al. применяли монотерапию леветирацетамом в дозе 500 мг в однократном вечернем приеме после отмены неэффективной терапии карбамазепином или вальпроевой кислотой у детей с идиопатической эпилепсией детского возраста с центротемпоральными спайками. Из 14 леченных пациентов у 12 полностью прекратились припадки, еще у одного рецидив возник после 4 месяцев и припадки прекратились при увеличении дозы до 1000 мг/сутки [38].
Leiz S. et al. у 6 пациентов с резистентной к другим препаратам детской эпилепсией с центротемпоральными спайками и 9 пациентов с атипичными идиопатическими эпилепсиями детского возраста отмечал уменьшение числа припадков более чем на 50% у 33% пациентов и улучшение когнитивных функций у 36% [104].
- 2.5.2. Кеппра (леветирацетам) в лечении симптоматических и предположительно симптоматических фокальных эпилепсий
- Cимптоматические и предположительно симптоматические (ранее называвшиеся криптогенными) фокальные эпилепсии составляют большинство эпилептических расстройств и одновременно наиболее трудно поддающиеся лечению формы эпилепсий, наиболее часто оказывающиеся фармакорезистентными. Поэтому чрезвычайно важными являются показанные во многих исследованиях первого класса доказательности высокая эффективность и устойчивость улучшения при применении леветирацетама именно при этих формах эпилепсии [3, 31, 47, 50, 56, 105]. В мультицентровом двойном слепом рандомизированном плацебоконтролированном исследовании Европейской группы по изучению пирацетама у 324 пациентов с фокальными фармакорезистентными эпилепсиями было показано значимое уменьшение числа припадков на дозах леветирацетама в дополнительной терапии 1000 – 2000 мг в сутки [151]. В другом мультицентровом двойном слепом плацебо контролированном исследовании при анализе 1023 случаев подтверждена высокая эффективность леветирацетама и показан достоверный рост эффективности с увеличением дозы от 1000 до 3000 мг/сутки [32].
Наиболее адекватную оценку практической эффективности препарата дают открытые исследования, в которых индивидуальный подбор дозы позволяет получить лучшие результаты лечения [147, 149]. В открытом мультицентровом исследовании M. Morrell et al. оценивали эффективность лечения 1030 пациентов в возрасте старше 16 лет с фармакорезистентными фокальными эпилепсиями с постепенным подбором дозы в зависимости от эффекта с максимумом 1500 мг два раза в день. За 16 недель наблюдения отмечалось уменьшение числа припадков на ≥50% у 57,9% пациентов, на – 75% у 40,1% и у 20% прекращение припадков [122]. В мультицентровом исследовании исследовательской группы DACH-LEV, объединяющем участников из Австрии, Германии и Швейцарии, одной из основных целей которого было определение оптимальной дозы леветирацетама, из 178 пациентов 16 лет и старше с фармакорезистентной к другим препаратам фокальной симптоматической и криптогенной эпилепсией полное прекращение припадков было достигнуто у 16,6%, сокращение числа припадков более 50% – у 4,1%. Сокращение числа припадков по группе составило 46,5%. Отмечено хорошее удержание на препарате, составившее 85%. Эффективными оказались дозы в диапазоне от 1000 (минимальная применявшаяся) до 3000 мг/сутки [157]. При сравнении в мета-анализе эффективности новых противоэпилептических препаратов в лечении фокальных симптоматических и криптогенных эпилепсий показано, что леветирацетам в дополнительной терапии более эффективен, чем ламотриджин и тиагабин, и лучше переносится, чем все другие новейшие препараты [132].
Хотя леветирацетам рекомендован в основном как препарат для дополнительной терапии, имеется мультицентровое двойное слепое плацебо-контролированное исследование монотерапии резистентной к другим препаратам фокальной эпилепсии. Отмечалось очень значительное снижение общего числа припадков по группе (73,8%), у 18,4% припадки прекратились, число пациентов со снижением числа припадков на 50% и более составило 59,2% [15]. В исследовании B. AbouKhalil и L. Schaich, проследивших результаты лечения леветирацетамом в монотреапии, следовавшей за отменой дополнительного препарата, у 280 пациентов с резистентной к другим препаратам фокальной эпилепсией показано долгосрочное сохранение эффекта снижения числа или прекращение припадков при сроках наблюдения до четырех лет [3].
- 2.5.3. Кеппра (леветирацетам) в лечении идиопатических генерализованных эпилепсий
-
Эффективность леветирацетама в лечении практически всех форм идиопатических генерализованных эпилепсий показана в многочисленных исследованиях [22, 35, 58, 70, 83, 98, 100]. При идиопатических генерализованных эпилепсиях с миоклоническими припадками A. Labate et al. (2006) из 35 пациентов, как с впервые диагностированной первично генерализованной эпилепсией в монотерапии, так и в дополнительной терапии резистентных к другим препаратам случаев, включавших юношескую миоклоническую эпилепсию, тяжелую миоклоническую эпилепсию младенчества, синдром Леннокса-Гасто, эпилепсию с миоклонико-астатическими припадками, с миоклоническими абсансами, с доброкачественной миоклонической эпилепсией младенчества, у 82% получили значительное улучшение и у 42% полное прекращение припадков [100]. G. Krauss et al. в смешанной группе идиопатических генерализованных эпилепсий, включавших значительную пропорцию генерализованных тонико-клонических припадков, значительное улучшение наблюдали у 76% и ремиссию у 40% [98].
2.5.3.1. Эпилепсия с генерализованными тонико-клоническими припадками
Об успешном лечении идиопатической эпилепсии с генерализованными тонико-клоническими припадками сообщают многие авторы. Препарат эффективен в 70 – 80% леченных больных [98, 99]. В небольших по объему открытых исследованиях сообщается о частом полном прекращении припадков на дополнительном лечении леветирацетамом у пациентов, безуспешно леченных вальпроатом, ламотриджином или топираматом [120].2.5.3.2. Эпилепсии детского и юношеского возраста с абсансами
Об эффективности лечения леветирацетамом идиопатической эпилепсии детского возраста с абсансами при резистентности к другим препаратам сообщают многие авторы [22, 98]. Прекращение припадков сопровождается исчезновением типичных паттернов абсансов в ЭЭГ [22].
В исследованиях J. Cohen (2003) и C. Di Bonaventura et al. (2005) сообщается об успешном лечении юношеской абсансной эпилепсии леветирацетамом в моно- и дополнительной терапии. Клиническое улучшение проявлялось прекращением как абсансов, так и генерализованных тонико-клонических припадков и сопровождалось нормализацией ЭЭГ [22, 35].2.5.3.3. Доброкачественная миоклоническая эпилепсия в младенчестве
Доброкачественная миоклоническая эпилепсия возникает в возрасте 1–2 лет, проявляется короткими припадками генерализованных миоклоний и острыми волнами, спайками, комплексами спайк-волна, острая волна-медленная волна, преобладающими в ранних стадиях сна. Обычно прогноз заболевания благоприятный, однако иногда припадки оказываются слишком частыми и не контролируются традиционными препаратами. В таких случаях A. Labate et al. наблюдали значительное улучшение при лечении леветирацетамом [100].2.5.3.4. Юношеская миоклоническая эпилепсия
Леветирацетам является высокоэффективным препаратом при юношеской миоклонической эпилепсии. В двойном слепом рандомизированном плацебоконтролируемом мультицентровом международном исследовании при лечении леветирацетамом в комбинации с ранее назначенным противоэпилептическим препаратом в течение 12 недель из 122 пациентов уменьшение числа припадков более чем на 50% было у 58,3%, у 12 из них – полное прекращение [164]. В открытом исследовании у 10 пациентов, безуспешно леченных вальпроатом, ламотриджином или топираматом, наблюдавшихся на дополнительном лечении леветирацетамом не менее 12 и до 46 месяцев, у пяти припадки полностью прекратились и у четырех число их уменьшилось на 75% [120]. При лечении леветирацетамом в качестве дополнительного препарата или в монотерапии в течение не менее 10 месяцев и до 2 лет наблюдения 43 пациентов, ранее безуспешно получавших ламотриджин или (и) вальпроат, у 37% наблюдалось полное прекращение припадков, у 41% прекратились миоклонические и у 69% – генерализованные тонико-клонические припадки [156]. Сходные по эффективности результаты как в поли-, так и в монотерапии леветирацетамом юношеской миоклонической эпилепсии получили и другие исследователи. Вообще в отношении успешного лечения данной формы первично-генерализованной идиопатической эпилепсии литература наиболее обширна [22, 98 – 100, 119].2.5.3.5. Эпилепсия с миоклонико-астатическими припадками и эпилепсия с миоклоническими абсансами
Об успешности применения леветирацетама при лечении идиопатических первично-генерализованных эпилепсий с миоклонико-астатическими припадками и с миоклоническими абсансами, нередко оказывающимися резистентными к традиционным и другим новым препаратам, сообщили A. Labate et al [100].2.5.3.6. Эпилепсия с миоклонией век с абсансами
Под этим названием объединяют группу расстройств, пока не получивших окончательной идентификации в классификации эпилепсий и характеризующихся обычно приуроченностью к детскому возрасту, наличием абсансов, сочетающихся с миоклонусом век, нередко присутствием генерализованных тонико-клонических припадков, обычно протекающих с задержкой развития и другими психическими нарушениями, и в большинстве случаев фармакорезистентных. Поэтому имеет значение успешное применение при этом расстройстве леветирацетама, показанное в работе C. Di Bonaventura et al. [22]. - 2.5.4. Кеппра (леветирацетам) в лечении фотосензитивных эпилепсий
- Леветирацетам показал высокую эффективность в лечении рефлекторных фотосензитивных эпилепсий и припадков. L.M. Specchio et al. при лечении миоклонической юношеской эпилепсии у половины пациентов отмечали прекращение фотосензитивных припадков [156]. A. Fels и F.Habetswaller получили значительное улучшение у пациента с симптоматической эпилепсией с провоцируемыми мелькающим светом эпилептическими припадками [52]. D.G. Kasteleijn-Nolst Trenite et al. провели специальное исследование эффективности леветирацетама у больных с фотосензитивной эпилепсией. В течение трех дней лечения по стандартному протоколу. Применяли разовые дозы 250, 500 или 1000 мг. Дополнительно четыре пациента получали в течение 3 – 5 дней дозы 250 мг утром и вечером. У 3 пациентов наблюдалось значимое снижение и у 6 – полное прекращение фотосензитивных припадков и прекращение фотопароксизмального ответа в ЭЭГ. Эффект был дозозависимым, и полное прекращение припадков было только при дозах 750 мг и более. У части пациентов отмечалось в качестве дополнительного эффекта улучшение настроения [84].
- 2.5.5. Кеппра (леветирацетам) в лечении эпилептических энцефалопатий
- Рабочей группой по классификации и терминологии Международной противоэпилептической лиги в проект новой классификации эпилептических синдромов введена рубрика «Эпилептические энцефалопатии». В этот раздел отнесены эпилепсии и эпилептические синдромы, «при которых эпилептиформные нарушения приводят к прогрессирующей мозговой дисфункции» [1]. В раздел «эпилептические энцефалопатии» помимо эпилептической афазии Ландау-Клеффнера и эпилепсии с постоянными комплексами спайк-волна во время медленноволнового сна, которые в значительном числе случаев протекают без припадков и клинически проявляются только тяжелым нарушением речи (в первом случае) и умственной деградацией (во втором), включаются эпилептические расстройства, которые проявляются только психическими, когнитивными и поведенческими нарушениями, обусловленными постоянными эпилептическими разрядами в мозге, детектируемыми электроэнцефалографией или магнетоэнцефалографией в виде эпилептиформной активности при отсутствии эпилептических припадков. Важнейшим свойством противоэпилептического препарата для их лечения является способность подавлять эпилептиформную активность в ЭЭГ, поскольку именно отображающиеся в ней эпилептические разряды и вызывают тяжелые нарушения функции [1]. В этом отношении даже на основании фармакодинамических особенностей действия леветирацетама следует ожидать его высокой эффективности при лечении этой группы эпилептических расстройств. Как отмечено в разделах 1.1, 2.3 и 2.4, леветирацетам подавляет эпилептиформную активность в ЭЭГ и влечет улучшение психических показателей таких как настроение, поведение, общее качество жизни пациента, социальное функционирование, когнитивные функции, способность к обучению [40, 41, 43, 136, 163]. Помимо нормализующего влияния на нейрональную активность за счет подавления эпилептической активности, усматривается также вероятный ноотропный эффект препарата, принимая во внимание его генетическое родство с известным ноотропом пирацетамом. Это проявляется в улучшении уровня внимания, вербальной беглости и других языковых функций. Значительное улучшение наблюдается при лечении им эпилептических расстройств, связанных с трудностями обучения, задержкой развития, нарушениями речи, психическими расстройствами. У пациентов отмечается улушение настроения, внимания, речевых функций, сна, аппетита, ясности сознания, поведения, исчезает психотическая симптоматика [11, 28, 78, 85, 104, 150, 159].
Поскольку персистирование эпилептических разрядов в мозге при неправильно леченной или не леченной эпилептической энцефалопатии ведет к прогрессированию заболевания по механизму киндлинга с развитием пластических и структурных изменений в мозге, обусловленных нарушениями генной экспрессии, аксональным спрутингом, патологическим нейрогенезом, обнаруженные в экспериментах антиэпилептогенные и нейропротекторные свойства леветирацетама, очевидно, могут играть важную роль в нормализации мозговых систем при лечении этой группы наиболее тяжелых энцефалопатий [1, 71, 92, 110, 166, 171]. Изложенные выше соображения подтверждаются в большом количестве клинических наблюдений. Особенно знаменательно выявление эффективности леветирацетама при эпилептических энцефалопатиях – эпилепсиях, при которых эпилептическая активность в мозге ведет к тяжелой прогрессирующей деградации мозговых функций. Некоторые из этих расстройств из-за своей тяжести, фармакорезистентности и неблагоприятного прогноза получили определение «катастрофические». К ним относятся синдром Уэста, синдром Леннокса-Гасто, эпилепсия с постоянными комплексами спайк-волна во сне и др.
2.5.5.1. Эпилептические энцефалопатии в младенческом возрасте
К этой группе расстройств относятся злокачественная миоклоническая эпилепсия в младенчестве, синдром злокачественных мигрирующих фокальных припадков раннего младенческого возраста, синдром Уэста и некоторые другие. Они отличаются чрезвычайной тяжестью и частотой припадков, выраженной задержкой психомоторного развития, высокой летальностью, очень низким процентом курабильности и плохим отдаленным прогнозом в случаях выживания пациента. О возможности успешного применения леветирацетама при лечении этих расстройств сообщает ряд авторов [36, 76, 100, 103, 173].
Синдром злокачественных мигрирующих фокальных припадков раннего младенческого возраста, описанный Coppola G. et al., характеризуется появлением с первых недель жизни (до 6 месяцев) многократных в течение дня мультифокальных припадков с эпилептическими фокусами в ЭЭГ, мигрирующими из одного полушария в другое [39]. С возрастом припадки учащаются. Заболевание сопровождается тетраплегией и отсутствием прогресса в психическом развитии, в 30% заканчивается летально. Фармакотерапия в большинстве случаев неэффективна, поэтому особый интерес представляет сообщение об успешном применении при этой энцефалопатии леветирацетама, приведшем к значительному сокращению числа припадков и улучшению межприсутпного статуса [76].
Улучшение при лечении синдрома Уэста леветирацетамом показано в исследовании K.M. Lawlor and A.M. Devlin. Отмечалось прекращение инфантильных спазмов и исчезновение гипсаритмии в ЭЭГ [103].2.5.5.2. Синдром Леннокса-Гасто
Синдром Леннокса-Гасто, наблюдающийся у детей старше 3 лет и характеризующийся сочетанием нескольких типов припадков, среди которых наиболее тяжелые – астатические и тонические, картины гипсаритмии в ЭЭГ и тяжелого расстройства психомоторного развития. Особенно неприятной его особенностью является дозозависимая нейротоксичность, часто из-за идиосинкразических реакций препятствующая лечению основными противосудорожными препаратами. Об улучшении при лечении леветирацетамом больных с синдромом Леннокса-Гасто в составе групп пациентов с другими формами эпилепсии сообщается в нескольких исследованиях [78, 100, 167]. Специально исследованию эффективности в лечении синдрома Леннокса-Гасто посвящена работа E.C. De Los Reyes et al. При лечении леветирацетамом в качестве дополнительной терапии шести пациентов у всех отмечено прекращение миоклонических припадков, у четырех – прекращение генерализованных тонико-клонических и у двух более чем наполовину уменьшилось количество атонических приступов. Лечение не повлияло на тонические приступы [45]. B. Huber et al. отмечали также улучшение психических функций [78].2.5.5.3. Эпилептическая афазия Ландау-Клеффнера и другие расстройства речи, связанные с эпилепсией
Одна из самых тяжелых в плане когнитивных расстройств эпилептических энцефалопатий – эпилептическая афазия Ландау-Клеффнера, приводящая при несвоевременном или неправильном лечении к пожизненной афазии, возникает в возрасте 3 – 7 лет и составляет около 0,5% всех эпилептических расстройств. Границы синдрома окончательно не определены, и к нему примыкает широкий круг расстройств речи, связанных с эпилепсией. В нескольких публикациях показана высокая эффективность леветирацетама при этих расстройствах.
E. Kossoff et al. наблюдали быстрое прекращение припадков, нормализацию ЭЭГ и восстановление речи при эпилептической афазии Ландау-Клеффнера при переходе на монотерапию леветирацетамом в дозе 60 мг/кг в день [94].
S. Leiz et al. отмечали при присоединении леветирацетама улучшение речи у пациентов с эпилептической афазией Ландау-Клеффнера, резистентной к другим препаратам. [104]. Показано улучшение речевых функций при лечении леветирацетамом речевой диспраксии при атипичных идиопатических эпилепсиях детского возраста, при связанном с эпилепсией заикании у детей и взрослых [28, 104, 150].2.5.5.4. Эпилепсия с постоянными комплексами спайк-волна в медленноволновом сне
Заболевание возникает в возрасте 2-10 лет, проявляется атипичными абсансами и фокальными и генерализованными припадками во сне. Во время сна: постоянные генерализованные комплексы спайк-волна или множественные спайкиволна, занимающие 85% III – IV стадии сна. При этой форме эпилепсии одним из основных проявлений заболевания являются нарушения способности к обучению и прогрессирующая умственная отсталость. Характерно развитие социальных нарушений, утрата способности к выполнению плановых последовательностей действий, исполнительных функций, так что заболевание трактуется как лобный синдром или аутизм [1]. Эти нарушения связаны с эпилептической активностью во сне, препятствующей нормальной переработке информации мозгом и консолидации долговременной памяти. Поэтому лечение должно быть направлено не только на прекращение припадков (которых в части случаев вообще не бывает), а на подавление межприступной эпилептической активности в ЭЭГ. Leiz S. et al. отмечали при присоединении леветирацетама уменьшение числа припадков и улучшение когнитивных функций у 4 пациентов с резистентной к другим препаратам эпилепсией с постоянными комплексами спайк-волна в медленноволновом сне [104]. G. Capovilla et al. лечили трех детей с резистентной к другим препаратам эпилепсией с постоянными комплексами спайк-волна в медленноволновом сне леветирацетамом. В двух случаях наблюдалась полная электроэнцефалографическая и клиническая нормализация, в одном уменьшение ночной эпилептиформной активности [29]. При лечении 12 пациентов 50 мг/кг/сутки в дополнительной терапии A. Aeby et al. у семи отметили значительную нормализацию ЭЭГ, у трех из них наблюдалось нейропсихологическое улучшение, у остальных с особенно тяжелыми нейропсихологическими нарушениями, не позволявшими протестировать их количественно, отмечалось улучшение поведения и настроения. Еще у двух пациентов наблюдалось нейропсихологическое улучшение, вопреки отсутствию значительного эффекта в отношении ЭЭГ [4]. Успешность лечения этого синдрома леветирацетамом отмечена в работе T. Hoppen et al. [77].2.5.5.5. Непароксизмальные психические, нейропсихологические и поведенческие эпилептические расстройства
К эпилептическим энцефалопатиям относят также разнообразные психические, нейропсихологические и поведенческие эпилептические расстройства, не сопровождающиеся типичными эпилептическими припадками, такие как эпилептический приобретенный лобнодолевой синдром, речевая диспраксия при центротемпоральных спайках, приобретенный аутистический синдром и др. [1]. Наряду с вальпроевой кислотой леветирацетам эффективен в их лечении. Параллельно нормализации электроэнцефалограммы наблюдается улучшение высших психических функций, нарушенных вследствие эпилептических разрядов, к подавлению которых приводит лечение леветирацетамом. S. Leiz et al. (2005) из 5 пациентов без судорог, но с когнитивными и поведенческими проблемами, безуспешно леченных другими препаратами, у трех наблюдали значительное улучшение когнитивных, языковых функций и поведения при добавлении леветирацетама [104].
Учитывая особую роль эпилептической дисфункции мозга в развитии аутизма [1], представляет особый интерес успешное использование леветирацетама в лечении этого тяжелого расстройства развития. Отмечалось статистически значимое улучшение внимания, уменьшение гиперактивности и импульсивности, оценивавшихся по шкале проблем внимания Ахенбаха, полной шкале DSM-IV Коннера и шкале индекса расстройства дефицита внимания и гиперактивности. Отмечалась стабилизация настроения по шкалам индекса эмоциональной лабильности Коннера и глобального индекса Коннера. Отмечалось также улучшение по шкале агрессии Ахенбаха у детей, безуспешно леченных до этого рисперидоном, карбамазепином и дезипрамином [144]. - 2.5.6. Кеппра (леветирацетам) в лечении прогрессирующих миоклонических эпилепсий
- Особое значение имеет применение леветирацетама в лечении прогрессирующих миоклонических эпилепсий. К этой группе в Предложениях по классификации эпилепсий относят многочисленные тяжелые прогрессирующие энцефалопатии, обусловленные генетическими заболеваниями в основном с рецессивным наследованием, дегенеративными нарушениями, тяжелой интоксикацией или гипоксией [44, 60, 148]. P. Kinrions et al. сообщили об успешном лечении одной из наиболее труднокурабильных форм миоклонуса – при миоклонус-эпилепсии Унферрихта-Лундборга [89]. A. Magaudda et al. при лечении 13 пациентов с болезнью Унферрихта-Лундборга более года отметили значительное уменьшение миоклонуса у восьми из них [113]. Леветирацетам оказался эффективным в подавлении миоклонуса даже при таком тяжелейшем расстройстве, как болезнь Крейцфельда-Якоба [79].
M.Mancuso et al. лечили леветирацетамом пациента с MERRF-синдромом (миоклонус-эпилепсия с рваными красными мышечными волокнами). При этом заболевании миоклонус подавляется вальпроевой кислотой, однако, учитывая митохондриальную природу заболевания, применение ее связано с риском, поскольку вальпроевая кислота противопоказана при этого типа генетических расстройствах. Замена вальпроевой кислоты леветирацетамом привела к почти полному прекращению миоклонических припадков и улучшению качества жизни пациента. Учитывая отсутствие влияния леветирацетама на митохондриальные функции, авторы считают его препаратом выбора при данном заболевании [114].
G.L. Krauss et al. успешно лечили постгипоксическую и постэнцефалитическую миоклоническую эпилепсию леветирацетамом и считают препарат перспективным в плане уменьшения инвалидизации пациентов, особенно в отношении акционного миоклонуса нарушающего моторные функции [97]. Эффективность лечения постгипоксического миоклонуса, показана L. Lim и A. Ahmed [107]. Успешность лечения миоклоний леветирацетамом может обусловливаться не только егодействием на уровне церебральных механизмов, но и на нижележащие мехнизмы, что следует из его эффективности в лечении миоклонуса при спинальной эпидуральной компрессии, поперечном миелите и герпесном радикулоневрите. Очевидно, его эффективность обусловлена специфической способностью усиливать тормозные эффекты глицина (см. раздел 1.1) – главного тормозного нейротрансмиттера спинного мозга [86].
P. Striano et al. наблюдали значительное уменьшение коркового миоклонуса у всех леченных ими 14 больных. Отмечалось достоверное снижение амплитуды «гигантских» сомато-сенсорных вызванных потенциалов, что является прямым указанием на снижение корковой возбудимости под влиянием лечения [160].
- 2.5.7. Кеппра (леветирацетам) в лечении эпилептического статуса
- Эпилептический статус представляет одну из наиболее тяжелых проблем эпилептологии. К примеру, в Соединенных Штатах в год регистрируется 126 000 случаев, 10 000 из которых заканчиваются летальным исходом, составляя главную причину смертности при эпилепсии. Основные препараты, применяемые в лечении статуса – бензодиазепины – характеризуются наличием комулятивного эффекта, что в сочетании с влиянием на витальные функции регуляции дыхания и кардиоциркуляторную систему, чревато опасностью витальных побочных эффектов [2]. Поэтому сохраняется необходимость поиска альтернативного лечения этого тяжелого осложнения эпилепсии. Имеющиеся к настоящему времени данные об использовании леветирацетама в лечении эпилептического статуса говорят о его эффективности в случаях неуспешности стандартных методов лечения. Наиболее целесообразным представляется применение поддерживающего внутривенного введения леветирацетама после начальной терапии диазепамом [88, 143, 173], причем упешное применение препарата отмечается в лечении как взрослых, так и детей [145].
- 2.5.8. Кеппра (леветирацетам) в специальных группах пациентов
-
2.5.8.1. Кеппра (леветирацетам) у детей
Хотя леветирацетам зарегистрирован в большинстве стран в качестве препарата, рекомендуемого для лечения пациентов от 18 лет и старше, в многочисленных исследованиях показана его безопасность и эффективность у детей любых возрастных групп, начиная с новорожденности и первого года жизни в моно- и политерапии [24, 50, 101 – 103, 115, 141].
J.W. Wheless и Y.T. Ng при лечении 39 детей (средний возраст 8,6 лет) с резистентными к другим препаратам эпилепсиями отмечали уменьшение тяжести и числа припадков, у 25% наблюдалось также улучшение познавательных функций и поведения [169]. В открытом исследовании L. Lagae et al. леветирацетама в дополнительной терапии в дозах от 10 до 60 мг/кг в день при лечении 21 ребенка у 47% отметили снижение числа припадков более 50%. Препарат был эффективен при всех типах приступов, в особенности – миоклонических [101]. В обзоре 2003 г., посвященном лечению детей, T.A. Glauser и O. Dulac отмечали, что в опубликованных к тому времени исследованиях показана высокая эффективность, хорошая переносимость леветирацетама и особенно отмечалось отсутствие идиосинкразических эффектов. Более высокая скорость метаболизма у детей требует более высоких, чем у взрослых, доз по отношению к весу тела [64]. В дальнейших исследованиях и публикациях подтверждена высокая эффективность и хорошая переносимость препарата в лечении детей [69, 95, 161, 165].
M.W. Koukkari и E.J. Guarino специально отмечали хорошую переносимость удетей доз леветирацетама выше 40 мг/кг в день, включая дозы до 315 мг/кг в день [95].
По данным мультицентрового открытого исследования в Германии при лечении 285 детей с рефракторными генерализованными и фокальными эпилепсиями при наблюдении в среднем в течение 6 лет не выявилось серьезных побочных эффектов. За время наблюдения не менее 12 недель у 6,2% отмечена ремиссия, у 18,7% было снижение числа припадков более чем на 50%. В 8,6% отмечался положительный психомоторный эффект [131].2.5.8.2. Кеппра (леветирацетам) у пожилых пациентов
Пожилой возраст – период наибольшей относительной частоты эпилепсии, при этом лечение пожилых пациентов связано с дополнительными факторами. В связи со значительным снижением активности печеночных ферментов разрушение препаратов происходит медленнее, а из-за высокой коморбидности большинство пациентов регулярно принимают другие лекарства, что осложняет лекарственное взаимодействие и фармакокинетику. В этом отношении весьма важны многочисленные сообщения о хорошей переносимости и эффективности применения леветирацетама в этом возрасте [24]. J.A. Ferrendelli et al. в открытом исследовании IV фазы оценивали эффективность леветирацетама в дополнительном лечении у 78 пациентов старше 64 лет. Общее уменьшение числа припадков составило 80,1%. У 76,9% пациентов уменьшение составило ≥50%, у 56,9% – ≥75% и у 40,0% отмечалась ремиссия. Авторы отметили хорошую переносимость препарата. Основным побочным эффектом была сонливость (16,7%) и головокружение (7,9%), [53]. J.A. Cramer et al., сравнивая побочные эффекты у лиц младше и старше 65 лет, отметили общую хорошую переносимость в обеих группах. В старшей группе отмечались чаще головная боль и тремор [42]. Эффективность леветирацетама показана при постинсультной эпилепсии [152]. T.M. Alsaadi et al. показали эффективность леветирацетама в лечении фокальной симптоматической эпилепсии у пожилых. У 61,5% достигнута ремиссия, у 30,7% отмечено более чем 50% снижение числа припадков. Эффективные дозы варьировали в пределах 500 – 3000 мг/день (в среднем – 1839,2 мг/день) [5].2.5.8.3. Кеппра (леветирацетам) у женщин
Фармакотерапия эпилепсии у женщин требует учета дополнительных условий: 1) влияние на фертильную функцию, 2) особенности периода вынашивания в отношении беременной и плода, 3) особенности периода вскармливания, 4) эстетические и косметические факторы. Эндокринные функции и фертильность
При эпилепсии чаще, чем в общей популяции, наблюдается полициклический овариальный синдром, частота которого колеблется от 3,1% до 26%. Доказательных данных о роли отдельных препаратов или комбинациифакторов до настоящего времени не получено [81]. Нет данных о большей чем у других препаратов активности леветирацетама и дополнительной его опасности в этом отношении.
Леветирацетам не влияет на фармакокинетику оральных контрацептивов и, соответственно, может безопасно комбинироваться с этими препаратами [18, 50, 139].Беременность и вскармливание
Хотя в официальных аннотациях препарата отмечается необходимость взвешивания рисков и преимуществ при решении вопроса применения леветирацетама в связи с беременностью, D.E. Briggs и J.A. French на основе экспертной оценки опубликованных до 2004 г. данных характеризуют возможности применения леветирацетама при беременности как весьма обнадеживающие [24].
Основной проблемой фармакотерапии при беременности является тератогенез плода. Немногочисленные публикации не обнаруживают тератогенеза у младенцев, родившихся у матерей, принимавших леветирацетам [82, 109, 162]. В проспективном исследовании регистра лечения 3607 беременных женщин от эпилепсии разными препаратами не зарегистрировано ни одного случая больших мальформаций плода при монотерапии леветирацетамом за все время его применения [123]. Следует все же иметь в виду малое число наблюдений (25) сравнительно с другими препаратами.
Согласно данным S.I. Johannessen et al., соотношение концентраций леветирацетама в плазме пупочной артерии/сыворотке матери составляет 1,14, а соотношение молоко матери/сыворотка плазмы матери на 3-й день и до 10-го месяца от рождения – 0,76-1,38, что свидетельствует о свободном поступлении препарата в организм плода и младенца как в пренатальном периоде, так и в период лактации [135]. Однако, концентрация препарата в плазме младенца составляет не более 10 – 15 mkM за весь период вскармливания молоком матери, чему соответствует отсутствие каких-либо признаков побочного действия препарата в отношении младенца. Это объясняется чрезвычайно быстрым метаболизированием леветирацетама в организме ребенка [82].Косметические и эстетические факторы
Из побочных эффектов, связанных с применением противоэпилептических препаратов, для женщин большое значение имеют нередко наблюдающиеся огрубление черт лица, гирсутизм или истончение (или выпадение) волос, неконтролируемое увеличение или снижение веса тела. Преимущество леветирацетама заключается в отсутствии каких-либо побочных эффектов из перечисленных выше, поэтому при возникновении таких нарушений показан перевод женщины на лечение леветирацетамом. Идиосинкразические высыпания на лечении леветирацетамом возникают реже, чем при лечении некоторыми другими противоэпилептическими препаратами. - 2.5.9. Кеппра (леветирацетам) в особых ситуациях
- Лечение конкретного пациента заставляет учитывать множество индивидуальных факторов, накладывающих нередко необходимые ограничения по применению того или иного препарата, поэтому существенной характеристикой препарата является возможно более широкий спектр ситуаций, в которых он может быть применен. Важнейшим свойством леветирацетама является отсутствие гепатотоксичности. Исследование фармакокинетики у пациентов с алкогольным циррозом печени не выявило различий в зависимости от степени печеночной недостаточности по классификации тяжести Child-Pugh от A до С, за исключением снижения клиренса, на 57% меньшего у пациентов с самой тяжелой степенью цирроза сравнительно с нормой, что объясняется почечной недостаточностью, наблюдающейся у этих пациентов. Эффектов гепатотоксичности леветирацетама не выявлено. Данные исследования говорят о целесообразности половинных начальных доз леветирацетама при лечении пациентов с самыми тяжелыми стадиями цирроза [25]. Применение леветирацетама у пациентов с припадками, подвергнутых операции трансплантации печени, не только безопасно и эффективно, но и позволяет применять меньшие дозы иммуносуппрессантных препаратов для предупреждения эффекта отторжения [63].
Показана безопасность и высокая эффективность леветирацетама в лечении эпилептических припадков при латентной печеночной порфирии, экзацербировавшей под влиянием вальпроата и примидона [134], а также возможность успешного лечения эпилептического статуса при острой перемежающейся порфирии [172].
Специальные исследования показывают, что у пациентов с почечной недостаточностью по показателям креатинина требуются меньшие дозы леветирацетама [54].
Особенно проблемную группу составляют пациенты с рефракторными тяжелыми фокальными припадками, у которых хирургическое лечение оказалось неэффективным. Среди этих пациентов добавление леветирацетама к лечению другими противосудорожными привело к улучшению в 76,1%, причем у 47,6% достигнута ремиссия [124].
Отсутствие характерных для многих препаратов некоторых специфических противопоказаний и побочных эффектов иногда делает леветирацетам препаратом единственного выбора и позволяет добиться успеха в чрезвычайно сложных ситуациях. Характерный случай описали S.C. Stoner et al. У пациентки 46 лет с припадками и расстройствами настроения под влиянием лечения карбамазепином или окскарбазепином развивалась гипонатриемия, попытка лечения вальпроатом вызвала гипераммонемию, лечение топираматом сопровождалось неприемлемыми когнитивными нарушениями. Лечение леветирацетамом дало прекращение припадков и психическую нормализацию [159].
Таким образом, в настоящее время показана эффективность леветирацетама при основных формах эпилепсий, типах эпилептических припадков и внеприступных эпилептических расстройств. Леветирацетам равноэффективен с остальными традиционными и новыми противосудорожными препаратами широкого профиля и превосходит многие из них по безопасности и приемлемости для пациентов. Все это определяет растущую роль леветирацетама среди новейших препаратов и непрерывное расширение ниши его применения среди всех противосудорожных препаратов. По данным аудита, предназначенного для сравнительной оценки трех основных новых препаратов ламотриджина, топирамата и леветирацетама, несколько более успешными и равноэффективными оказались два последних препарата, однако у леветирацетама значительно лучшая переносимость, чем у топирамата [33].
Исследование соотношения стоимость/эффективность показало, что некоторое его увеличение в пересчете на дополнительный свободный от припадков день в год в значительной степени компенсируется повышением качества жизни, экономией за счет уменьшения расходов на госпитализацию, амбулаторную и скорую помощь, нейрохирургию, другие противосудорожные препараты и социальное обслуживание [21].
- Глава 3.
Тактика клинического применения Кеппры (леветирацетама) -
- 3.1. Выбор Кеппры (леветирацетама)
- В некоторых странах леветирацетам зарегистрирован для политерапии с 4 лет, в России – с 16 лет (Разрешение на применение с 4 лет в нашей стране – в процессе регистрации). Для монотерапии препарат разрешен для применения в Европе с 16 лет. Хотя препарат зарегистрирован в качестве дополнительного и для пациентов 16 лет и старше, в случаях индивидуальной непереносимости или неприемлемых побочных эффектов других препаратов, а также при некурабильных эпилептических расстройствах у детей возможно применение леветирацетама в монотерапии и в детском возрасте при информированном согласии пациента или лица, о нем заботящегося. Многочисленные исследования показывают безопасность и высокую эффективность такого применения леветирацетама [6, 7, 13, 101].
- 3.2. Подбор дозы
- Рекомендуемые стандарты лечения эпилепсии леветирацетамом публикуются в аннотациях к препаратам и приведены в таблице 2. Их следует принимать за основу при подборе дозы препарата. Вместе с тем в каждом случае следует исходить из индивидуальных особенностей пациента и соответственно корректировать лечение, исходя из сложившейся практики и собственного опыта. Эффективные дозы широко варьируют в диапазоне 500 – 4000 мг/сутки [17]. Пожилым пациентам и лицам с печеночной недостаточностью рекомендуются уменьшенные наполовину начальные дозы [16]. Детям, благодаря ускоренному метаболизму, рекомендуют дозы до 60 мг/кг/день и более. Возможность начала лечения сразу с высокой суточной дозы препарата обеспечивает уникальный эффект снижения частоты припадков уже с первого дня лечения [55]. Препарат назначается в двух равных дневных дозах – утром и вечером, независимо от прием пищи, который только несколько снижает максимальную концентрацию и увеличивает время ее достижания на 1,5 часа [51]. В рандомизированном двойном слепом плацебо-контролированном исследовании T. Betts et al. назначали пациентам с первого дня дозы 1000 или 2000 мг два раза в день с хорошим лечебным эффектом, отмечавшимся с первого дня лечения. Наблюдалась хорошая переносимость с процентом побочных эффектов, незначительно отличавшимся от других стратегий лечения [17].
Взрослым и детям старше 12 лет при монотерапии Леветирацетам назначают с первого дня и далее в дозе 500 мг утром и вечером. Далее при повторении припадков дозу увеличивают на 250 – 500 мг, но не чаще, чем через каждые две недели до достижения максимального терапевтического эффекта. По достижении контроля припадков дополнительная корректировка дозы может производиться по результатам исследования ЭЭГ. Если сохраняется выраженная эпилептиформная активность, доза увеличивается до возможно полного подавления эпилептиформной активности, однако при этом следует соблюдать разумный баланс между терапевтическим эффектом и риском появления неблагоприятных побочных эффектов. Кроме того, при подборе поддерживающей дозы следует ориентироваться также на вес тела пациента.
- 3.3. Переносимость Кеппры (леветирацетама) и побочные эффекты
- Леветирацетам относится к препаратам с низкой токсичностью и соответственно хорошей переносимостью. В двойных слепых контролированных исследованиях показано, что суммарное количество побочных эффектов не превышает таковые при приеме плацебо [50]. У взрослых в большинстве случаев хорошо переносятся дозы до 4000 мг/сутки, у детей – до 315 мг/кг в день [95]. Есть сообщение о благоприятном исходе преднамеренного разового приема 60 таблеток по 500 мг леветирацетама пациенткой 38 лет. Клинически 4 часа спустя после приема отмечалась рвота, снижение сухожильных рефлексов, спутанность, ослабление дыхания, по поводу чего пациентка была интубирована. Концентрация в крови леветирацетама составляла 400 мкг/мл через 6 часов, 72 мкг/мл через 18 часов и 60 мкг/мл через 20,5 часа (терапевтическая концентрация 10 – 37 мкг/мл). На второй день отмечалась полная нормализация состояния без каких-либо последствий [9].
При применении Леветирацетама возможны следующие основные побочные эффекты. Со стороны ЦНС: сонливость, астенический синдром, головокружение; реже – головная боль, атаксия, судороги, депрессивный синдром, эмоциональная неустойчивость, агрессивность, бессонница, нервозность, тремор, анорексия, диплопия. Соматические побочные эффекты: диарея, диспепсия, тошнота, кожная сыпь. Побочные эффекты обычно появляются в течение первого месяца от начала лечения, не зависят существенно от дозы, выражены слабо или умеренно, обычно прекращаются без отмены лечения и прекращаются сразу при отмене препарата [24].
Сравнения, проведенные в отношении леветирацетама, карбамазепина, окскарбазепина у здоровых волонтеров, показали, что леветирацетам дает наименьшее количество побочных проявлений [121]. Полиграфические исследования сна у здоровых волонтеров не выявили существенных отклонений при применении леветирацетама [10, 12]. При исследовании больных, леченных леветирацетамом, одним из обсуждаемых осложнений являются психические и поведенческие нарушения. В большинстве случаев они носят характер преходящих эпизодов, проявляются в виде умеренной раздражительности, реже принимают форму выраженной агрессии с насилием, суицидальным поведением, психотических и кататонических нарушений с галлюцинациями [34, 49, 125]. Возникновение психических и поведенческих расстройств, очевидно, обусловлено конституционными особенностями, достоверно связано с психическими расстройствами в прошлом, фебрильными судорогами в анамнезе. Показано также, что протективным эффектом в отношении психических расстройств обладает совместная терапия ламотриджином [125]. Более медленное титрование дозы уменьшает риск их возникновения [41, 170].
Леветирацетам не вызывает заметных метаболических нарушений. В обширном обзоре D.E. Briggs и J.A. French не отмечают значимых изменений со стороны крови и биохимических показателей [24]. Имеется единичное сообщение о возникновении гипонатриемии в связи с приемом леветирацетама у пациента с синдромом предрасположенности к избыточному выделению антидиуретического гормона [128].
Хотя большинство авторов отмечают отсутствие какого-либо влияния леветирацетама на вес тела [24, 62], имеется одна публикация с описанием 4 случаев снижения веса вследствие лечения леветирацетамом. В трех из них небольшое уменьшение дозы привело к стабилизации веса без снижения противосудорожного эффекта, в одном случае пациентка перестала принимать препарат и вес восстановился [73].
Имеются единичные случаи проявления некоторых побочных действий других противоэпилептических препаратов при сочетании с леветирацетамом. Описано 4 случая токсических эффектов карбамазепина при сочетании с леветирацетамом [153]. Мы наблюдали случай возникновения высыпаний, связанных с ламотриджином, при присоединении леветирацетама.
Как и при лечении другими противоэпилептическими препаратами, при лечении леветирацетамом в отдельных случаях наблюдается в качестве парадоксального эффекта утяжеление эпилептических припадков, включая возникновение бессудорожного эпилептического статуса. Этот эффект чаще наблюдается у пациентов с задержкой когнитивного развития, возникает в течение первых двух месяцев лечения и на высоких дозах [8, 19, 126].
Завершая раздел побочных действий, следует отметить некоторые положительные побочные эффекты леветирацетама. При лечении этим препаратом улучшается качество сна и его субъективная оценка [12]. Показана возможность лечения эссенциального тремора леветирацетамом [27, 74]. Учитывая близость патофизиологических механизмов вальпроатного и эссенциального тремора [72], можно полагать, что дуотерапия с леветирацетамом позволит облегчить это осложнение терапии вальпроатом.
Важнейшей характеристикой противоэпилептического препарата является устойчивость лечебного эффекта, которая характеризуется показателем удержания на препарате, представляющим собой процент пациентов, продолжающих в долгосрочном катамнезе принимать препарат, от числа тех, кому он был первоначально назначен. Для леветирацетама он значительно лучше, чем для других новых препаратов и составляет от 58% при трехгодичном и до 85% при годичном наблюдении [19, 96, 97, 117, 132, 157].
- Заключение
-
Кеппра (леветирацетам) является высокоэффективным и безопасным препаратом широкого спектра действия, превосходя в этом отношении большинство новейших противосудорожных препаратов. В большинстве стран он рекомендуется как препарат в дополнительной терапии при резистентных к другим препаратам формах эпилепсии, однако доказана его высокая эффективность и в монотерапии во всех возрастных группах. Использование комбинации леветирацетама с другими традиционными и новейшими препаратами уже в первые дни лечения позволяет получить хороший эффект. Чрезвычайно важно свойство леветирацетама длительно сохранять свою эффективность, что резко отличает его в положительную сторону от других препаратов нового поколения по показателю длительного удержания на препарате, который свиделельствует о высокой субъективной и объективной оценке пациентами и врачами эффективности и безопасности препарата (Табл. 3).
Таблица 3.
Рейтинг удержания на препарате в течение 3-х лет от начала лечения и доля ремиссии припадковПрепарат % удерживающихся
на препарате 3 года
от начала лечения% ремиссии
3 года от начала
леченияАвторы Топирамат 30 3.5 S.Lhatoo et al.[106] Ламотриджин 29 2 Габапентин 9 0.6 Леветирацетам 58 17 B. Steinhoff,
E. Trinka [157]
Литература
- Зенков Л.Р. Непароксизмальные эпилептические расстройства. М.: МЕДпрессинформ. 2006.
- Карлов В.А. Судорожный эпилептический статус. М.: МЕДпрессинформ. 2003.
- AbouKhalil B., Schaich L. Longterm efficacy of levetiracetam for partial seizures // Seizure. – 2005. – V. 14. – P. 577-585.
- Aeby A., Poznanski N., Verheulpen D. et al. Levetiracetam efficacy in epileptic syndromes with continuous spikes and waves during slow sleep: experience in 12 cases // Epilepsia. – 2005. – V. 46. – P. 1937-1942.
- Alsaadi T.M., Koopmans S., Apperson M., Farias S. Levetiracetam monotherapy for elderly patients with epilepsy // Seizure. – 2004. – V. 13. – P. 58-60.
- Alsaadi T.M., Thieman C. Levetiracetam monotherapy for newly diagnosed epilepsy patients. Seizure. – 2003. – V. 12. – P. 1541-56.
- Alsaadi T.M., Thieman Catherine, Zusman Edie E. Levetiracetam monotherapy for adults with localizationrelated epilepsy // Epilepsy Behav. – 2002. – V. 3. – P. 471-474.
- Atefy R., Tettenborn B. Nonconvulsive status epilepticus on treatment with levetiracetam // Epilepsy Behav. – 2005. – V. 6. – P. 613-616.
- Barrueto Jr F., Williams K., Howland M.A. et al. A case of levetiracetam (Keppra) poisoning with clinical and toxicokinetic data. J Toxicol Clin Toxicol. – 2002. – V. 40. – P. 881884 10. Bazil C.W., Battista J., Basner R.C. Effects of levetiracetam on sleep in normal volunteers // Epilepsy Behav. – 2005. – V. 7. – P. 539-542.
- Bell G.S., Mitchell T., Koepp M.J., Duncan J.S., Sander J.W. The long term retention of levetiracetam in a large cohort of patients with epilepsy // Journal of Neurology, Neurosurgery, and Psychiatry. – 2006. – P. 77. – P.101-103.
- Bell C., Vanderlinden H., Hiersemenzel R. et al. The effects of levetiracetam on objective and subjective sleep parameters in healthy volunteers and patients with partial epilepsy // J Sleep Res. – 2002. – P.11. – P. 255-263.
- BelloEspinosa L.E., Roberts S.L. Levetiracetam for benign epilepsy of childhood with centrotemporal spikesthree cases // Seizure. – 2003. – P.12. – P. 157-159.
- BenMenachem E., Edrich P., Van Vleymen B. et al. Evidence for sustained efficacy of levetiracetam as addon epilepsy therapy // Epilepsy Res. – 2003. – V.53. – P. 57-64.
- BenMenachem E., Falter U. Efficacy and tolerability of levetiracetam 3000 mg/d in patients with refractory partial seizures: a multicenter, doubleblind, responderselected study evaluating monotherapy. European Levetiracetam Study Group // Epilepsia. – 2000. – V. 41. – P. 1276-1283.
- Bergey Gregory K. Initial treatment of epilepsy: Special issues in treating the elderly // Neurology. – 2004. – V.63. – P. S40 – S48.
- Betts T., Waegemans T., Crawford P. A multicentre, doubleblind, randomized, parallel group study to evaluate the tolerability and efficacy of two oral doses of levetiracetam, 2000 mg daily and 4000 mg daily, without titration in patients with refractory epilepsy // Seizure. – 2000. – V.9. – P. 80-87.
- Beyenburg S., Bauer J., Reuber M. New drugs for the treatment of epilepsy: a practical approach // Postgrad. Med. J.. – 2004. – V.80. – P. 581 – 587.
- Bird J.M., Joseph Z.A. Levetiracetam in clinical usea prospective observational study // Seizure. – 2003. – V.12 – P. 613-616.
- Birnstiel S., Wulfert E., Beck S.G. Levetiracetam (ucb LO59) affects in vitro models of epilepsy in CA3 pyramidal neurons without altering normal synaptic transmission. Naunyn Schmiedebergs // Arch Pharmacol. – 1997. – V.356 – P. 611-618.
- Blais L., Sheehy O., StHilaire J.M. et al. Economic evaluation of levetiracetam as an addon therapy in patients with refractory epilepsy. Pharmacoeconomics. – 2005. – V. 23. – P. 493-503
- Bonaventura C.Di., Fattouch J., Mari F. et al. Clinical experience with levetiracetam in idiopathic generalized epilepsy according to different syndrome subtypes // Epileptic Disord. – 2005. – V.7. – P. 231-215.
- Bouwman B.M., van Rijn C.M. Effects of levetiracetam on spike and wave discharges in WAG/Rij rats // Seizure. – 2004. – V.13. – P. 591-594.
- Briggs D.E., French J.A. Levetiracetam safety profiles and tolerability in epilepsy patients // Expert Opin Drug Saf. – 2004. – V. 3. – P. 415-424.
- Brockmoller J., Thomsen T., Wittstock M. et al. Pharmacokinetics of levetiracetam in patients with moderate to severe liver cirrhosis (ChildPugh classes A, B, and C): characterization by dynamic liver function tests // Clin Pharmacol Ther. – 2005. – V. 77. – P. 529-541.
- Browne T.R., Szabo G.K., Leppik I.E. et al. Absence of pharmacokinetic drug interaction of levetiracetam with phenytoin in patients with epilepsy determined by new technique // The Journal of Clinical Pharmacology. – 2000. – V. 40. – P.590595
- Bushara Khalafalla O., Malik Taimur, Exconde Rupert E. The effect of levetiracetam on essential tremor // NEUROLOGY. – 2005. – V.64. – P.10781080
- Canevini Maria Paola, Chifari Rosanna, Piazzini Ada. Improvement of a patient with stuttering on levetiracetam // Neurology. – 2002. – V.59. – P. 1288.
- Capovilla G., Beccaria F., Cagdas S. et al. Efficacy of levetiracetam in pharmacoresistant continuous spikes and waves during slow sleep. Acta Neurol Scand. – 2004. – V. 110. – P. 144147.
- Cavitt Jennifer, Privitera Michael. Levetiracetam Induces a Rapid and Sustained Reduction of Generalized SpikeWave and Clinical Absence // Arch Neurol. – 2004. – V. 61. – P.16041607.
- Cereghino J.J., Biton V., AbouKhalil B.et al. and the United States Levetiracetam Study Group. Levetiracetam for partial seizures Results of a doubleblind, randomized clinical trial // Neurology. – 2000. – V.55. – P.236242 32. Chaisewikul R., Privitera M.D., Hutton J.L., Marson A.G. Levetiracetam addon for drugresistant localization related (partial) epilepsy // Cochrane Database Syst Rev. – 2001. – V.1. – P. CD001901.
- Chappell B., Crawford P. An audit of lamotrigine, levetiracetam and topiramate usage for epilepsy in a district general hospital // Seizure. – 2005. – V. 14. – P. 422428.
- Chouinard M.J., Nguyen D.K., Clement J.F., Bruneau M.A. Catatonia induced by levetiracetam // Epilepsy Behav. – 2006. – V. 8. – P. 303307.
- Cohen J. Levetiracetam monotherapy for primary generalised epilepsy // Seizure. – 2003. – V. 12 – P. 150153
- Conry J.A. Pharmacologic treatment of the catastrophic epilepsies // Epilepsia. – 2004. – V. 45, Suppl 5. – P. 1216.
- Contin M., Albani F., Riva R., Baruzzi A. Levetiracetam therapeutic monitoring in patients with epilepsy: effect of concomitant antiepileptic drugs // Ther Drug Monit. – 2004. – V. 26. – P. 375379.
- Coppola G., Federico R., Auricchio G. et al. Levetiracetam as monotherapy in newly diagnosed benign rolandic seizueres in children: an openlabel pilot trial // Epilepsia. – 2005. – V.46, Suppl. 6. – P. 102103
- Coppola G., Mangano S., Tortorella G. et al. Levetiracetam during 1year followup in children, adolescents, and young adults with refractory epilepsy // Epilepsy Res. – 2004. – V. 59. – P. 3542.
- Cramer J.A., Arrigo C., Van Hammee G. et al. Effect of levetiracetam on epilepsyrelated quality of life. N132 Study Group // Epilepsia. – 2000. – V. 41. – P. 868874.
- Cramer J.A., De Rue K., Devinsky O. et al. A systematic review of the behavioral effects of levetiracetam in adults with epilepsy, cognitive disorders, or an anxiety disorder during clinical trials // Epilepsy Behav. – 2003. – V. 4. – P. 124132.
- Cramer J.A., Leppik I.E., Rue K.D. et al. Tolerability of levetiracetam in elderly patients with CNS disorders // Epilepsy Res. – 2003. – V. 56. – P. 135145.
- Cramer J.A., Van Hammee G. and N132 Study Group. Maintenance of improvement in healthrelated quality of life during longterm treatment with levetiracetam // Epilepsy Behav. – 2003. – V. 4. – P. 118-123.
- Crest C., Dupont S., Leguern E. et al. Levetiracetam in progressive myoclonic epilepsy An exploratory study in 9 patients // NEUROLOGY. – 2004. – V. 62. – P.640643
- De Los Reyes E.C., Sharp G.B., Williams J.P., Hale S.E. Levetiracetam in the treatment of LennoxGastaut syndrome. Pediatr Neurol. – 2004. – V. 30 – P. 254-256.
- Depondt C., Yuen A.W.C., Bell G.S. et al. The long term retention of levetiracetam in a large cohort of patients with epilepsy // Journal of Neurology, Neurosurgery, and Psychiatry. – 2006. – V. 77. – P.101103
- Devinsky O., Elger C. Efficacy of levetiracetam in partial seizures // Epileptic Disord. – 2003. – V. 5, Suppl 1. – P. S2731.
- Dimova S. (Ed). Levetiracetam. Product monograph // UCB SA. – 2004.
- Dinkelacker V., Dietl T., Widman G. et al. Aggressive behavior of epilepsy patients in the course of levetiracetam addon therapy: report of 33 mild to severe cases. Epilepsy Behav. – 2003. – V. 4 – P. 537-547.
- Dooley M., Plosker G.L. Levetiracetam. A review of its adjunctive use in the management of partial onset seizures // Drugs. – 2000. – V. 60. – P. 871893.
- Fay M.A., Sheth R.D., Gidal B.E. Oral absorption kinetics of levetiracetam: the effect of mixing with food or enteral nutrition formulas // Clin Ther. – 2005. – V. 27. – P. 594598.
- Fels A., Habetswaller F. Efficacy of levetiracetam in a patient with symptomatic epilepsy with spontaneous and photically induced seizures // Epilepsia. – 2005. – V.46, Suppl. 6. – P. 105
- Ferrendelli J.A., French J., Leppik I. et al. Use of levetiracetam in a population of patients aged 65 years and older: a subset analysis of the KEEPER trial // Epilepsy Behav. – 2003. – V. 4. – P. 702-709.
- French J. Use of levetiracetam in special populations // Epilepsia. – 2001. – V. 42, Suppl 4. – P. 40-43.
- French J., Arrigo C. Rapid onset of action of levetiracetam in refractory epilepsy patients // Epilepsia. – 2005. – V. 46 – P. 324326.
- French J., di Nicola S., Arrigo C. Fast and sustained efficacy of levetiracetam during titration and the first 3 months of treatment in refractory epilepsy // Epilepsia. – 2005. – 46(8. – P. 13047.
- Frucht Steven J., Elan D. Louis, Chuang Cathy, Fahn Stanley. A pilot tolerability and efficacy study of levetiracetam in patients with chronic myoclonus // Neurology. – 2001. – V. 57. – P.11121114
- Gallagher M.J., Eisenman L.N., Brown K.M. et al. Levetiracetam reduces spikewave density and duration during continuous EEG monitoring in patients with idiopathic generalized epilepsy // Epilepsia. – 2004. – V. 45. – P. 9091.
- Gelisse P., Crespel A., Genton P., BaldyMoulinier M. Dramatic effect of levetiracetam on epileptic negative myoclonus // Acta Neurol Scand. – 2003. – V. 107. – P. 302303.
- Genton P., Gelisse P. Antimyoclonic effect of levetiracetam // Epileptic Disord. – 2000. – V. 2. – P.209212.
- Gidal B.E., Baltes E., Otoul C., Perucca E. Effect of levetiracetam on the pharmacokinetics of adjunctive antiepileptic drugs: a pooled analysis of data from randomized clinical trials // Epilepsy Res. – 2005. – V. 64. – P. 111.
- Gidal B.E., Sheth R.D., Magnus L., Herbeuval A.F. Levetiracetam does not alter body weight: analysis of randomized, controlled clinical trials // Epilepsy Res. – 2003. – V. 56. – P. 121126.
- Glass G.A., Stankiewicz J., Mithoefer A. et al. Levetiracetam for seizures after liver transplantation // NEUROLOGY. – 2005. – V. 64. – P.10841085
- Glauser T.A., Dulac O. Preliminary efficacy of levetiracetam in children // Epileptic Disord. – 2003. – V.5, Suppl 1. – P. S4550.
- Gorji A., Hohling J.M., M. Madeja, Straub H., Kohling R. et al. Effect of levetiracetam on epileptiform discharges in human neocortical slices // Epilepsia. – 2002. – V. 43. – P. 14801487.
- Gower A.J., Hirsch E., Boehrer A., Noyer M., Marescaux C. Effects of levetiracetam, a novel antiepileptic drug, on convulsant activity in two genetic rat models of epilepsy // Epilepsy Research 1995. – V. 22. – P. 207213.
- Gower A.J., Noyer M., Verloes R., Gobert J., W_lfert E. ucb L059, a novel anticonvulsant drug: pharmacological profile in animals // European Journal of Pharmacology. – 1992. – V. 222. – P. 193203.
- Grant R., Shorvon S.D. Efficacy and tolerability of 10004000 mg per day of levetiracetam as addon therapy in patients with refractory epilepsy // Epilepsy Res. – 2000. – V. 42. – P. 8995.
- Grosso S., Franzoni E., Coppola G. et al. Efficacy and safety of levetiracetam: an addon trial in children with refractory epilepsy // Seizure. – 2005. – V. 14. – P. 248253.
- Grunewald R. Levetiracetam in the treatment of idiopathic generalized epilepsies // Epilepsia. – 2005. – V. 46, Suppl 9. – P. 154160.
- Gu J., Lynch B.A., Anderson D. et al. The antiepileptic drug levetiracetam selectively modifies kindlinginduced alterations in gene expression in the temporal lobe of rats // Eur J Neurosci. – 2004. – V. 19. – P. 334345.
- HabiburRehman. Diagnosis and Management of Tremor // Archives of Internal Medicine. – 2000. – V. 160. – P. 2438 – 2444.
- Hadjikoutis S., Pickersgill T.P., Smith P.E.M. // Weight loss associated with levetiracetam // BMJ. – 2003. – V.327. – P.905
- Handforth A., Martin F.C. Pilot efficacy and tolerability: a randomized, placebocontrolled trial of levetiracetam for essential tremor // Mov Disord.. – 2004. – V. 19. – P. 12151221.
- Hanon E., Klitgaard H. Neuroprotective properties of the novel antiepileptic drug levetiracetam in the rat middle cerebral artery occlusion model of focal cerebral ischemia // Seizure. – 2001. – V.10. – P. 287293.
- Hmaimess G., Kadhim H., Nassogne M.C. et al. Levetiracetam in a neonate with malignant migrating partial seizures // Pediatr Neurol. – 2006. – V. 34. – P. 5559.
- Hoppen T., Sandrieser T., Rister M. Successful treatment of pharmacoresistent continuous spike wave activity during slow sleep with levetiracetam // Eur J Pediatr. – 2003. – 162. – P. 5961.
- Huber B., Bommel W., Hauser I. et al. Efficacy and tolerability of levetiracetam in patients with therapyresistant epilepsy and learning disabilities // Seizure. – 2004. – V. 13. – P. 168175.
- Imperiale D., Bortolotto S., Cucatto A. et al. Levetiracetam control of myoclonus in a patient with CreutzfeldtJakob disease // Eur Neurol. – 2003. – V. 49. – P. 189190.
- Jain K.K. An assessment of levetiracetam as an antiepileptic drug // Expert Opin Investig Drugs. – 2000. – V. 9. – P. 16111624.
- Joffe Hadine, Taylor A.E., Hall J.E. EDITORIAL: Polycystic Ovarian SyndromeRelationship to Epilepsy and Antiepileptic Drug Therapy // The Journal of Clinical Endocrinology & Metabolism. – 2001. – V. 86. – P. 29462949
- Johannessen S.I., Helde G., Brodtkorb E. Levetiracetam concentrations in serum and in breast milk at birth and during lactation // Epilepsia. – 2005. – V. 46. – P. 775777.
- KasteleijnNolst Trenite D.G., Hirsch E. Levetiracetam: preliminary efficacy in generalized seizures // Epileptic Disord. – 2003. – V. 5 Suppl 1. – P. S3944.
- KasteleijnNolst Trenit_ D.G., Marescaux C., Stodieck S. et al. Photosensitive epilepsy: a model to study the effects of antiepileptic drugs. Evaluation of the iracetam analogue, levetiracetam // Epilepsy Res 1996. – V.25. – P.225330
- Kelly K., Stephen L.J., Brodie M.J. Levetiracetam for people with mental retardation and refractory epilepsy // Epilepsy Behav. – 2004. – V. 5. – P. 878883.
- Keswani S.C., Kossoff E.H., Krauss G.L., Hagerty C. Amelioration of spinal myoclonus with levetiracetam // Journal of Neurology Neurosurgery and Psychiatry 2002. – V.73. – P.457458
- Khalafalla O. Bushara, Taimur Malik, Rupert E. Exconde. The effect of levetiracetam on essential tremor // NEUROLOGY. – 2005. – V.64. – P.10781080
- Kilickap Saadettin, Cakar Mustafa, Onal Ibrahim K. et al. Nonconvulsive Status Epilepticus Due to Ifosfamide // Ann. Pharmacother. . – 2006. – V. 40. – P. 332 – 335.
- Kinrions P., Ibrahim N., Murphy K. et al. Efficacy of levetiracetam in a patient with UnverrichtLundborg progressive myoclonic epilepsy // Neurology. – 2003. – V. 60. – P. 1394.
- Klitgaard H. Levetiracetam: the preclinical profile of a new class of antiepileptic drugs? // Epilepsia. – 2001. – V. 42 Suppl 4. – P. 1318.
- Klitgaard H., Matagne A., Gobert J., W_lfert E. Evidence for a unique profile of levetiracetam in rodent models of seizures and epilepsy // European Journal of Pharmacology. – 1998. – V. 353. – P. 191206.
- Klitgaard H., Pitkanen A. Antiepileptogenesis, neuroprotection, and disease modification in the treatment of epilepsy: focus on levetiracetam // Epileptic Disord. – 2003. – V. 5 Suppl 1. – P. S916.
- Kossoff E.H., Bergey G.K., Freeman J.M., Vining E.P. Levetiracetam psychosis in children with epilepsy // Epilepsia. – 2001. – V. 42. – P. 16111613.
- Kossoff E.H., Boatman D., JM Freeman J.M. LandauKleffner syndrome responsive to levetiracetam // Epilepsy Behav. – 2003. – V. 4. – P. 571575.
- Koukkari M.W., Guarino E.J. Retrospective study of the use of levetiracetam in childhood seizure disorders // J Child Neurol. – 2004. – V. 19. – P. 944947.
- Krakow Karsten., Walker M., Otoul C., Sander J.W.A.S. Longterm continuation of levetiracetam in patients with refractory epilepsy // Neurology 2001. – V.56. – P.17721774
- Krauss G.L., Bergin A., Kramer R.E. et al. Suppression of posthypoxic and postencephalitic myoclonus with levetiracetam // Neurology 2001. – V.56. – P.411412
- Krauss G.L., Betts T., AbouKhalil B. et al. Levetiracetam treatment of idiopathic generalised epilepsy // Seizure. – 2003. – V. 12. – P. 617620.
- Kumar S.P., Smith P.E. Levetiracetam as addon therapy in generalised epilepsies // Seizure. – 2004. – V. 13. – P. 475477.
- Labate A., Colosimo E., Gambardella A. et al. Levetiracetam in patients with generalised epilepsy and myoclonic seizures: An open label study // Seizure. – 2006. – V. 15. – P. 214218.
- Lagae L., Buyse G., Deconinck A., Ceulemans B. Effect of levetiracetam in refractory childhood epilepsy syndromes // Eur J Paediatr Neurol. – 2003. – V. 7. – P. 123128.
- Lagae L., Buyse G, Ceulemans B. Clinical experience with levetiracetam in childhood epilepsy: an addon and monotherapy trial // Seizure. – 2005. – V. 14. – P. 6671.
- Lawlor K.M., Devlin A.M. Levetiracetam in the treatment of infantile spasms // Eur J Paediatr Neurol. – 2005. – V. 9. – P. 1922.
- Leiz S., VanStulpnagel C., Orden D. Levetiracetam as addon therapy in idiopathic focal epilepsies // Epilepsia. – 2005. – V.46, Suppl. 6. – P. 103
- Leppik I.E., Biton V., Sander J.W., Wieser H.G. Levetiracetam and partial seizure subtypes: pooled data from three randomized, placebocontrolled trials // Epilepsia. – 2003. – V. 44. – P. 15851587.
- Lhatoo S.D., Wong I.C., Polizzi G., Sander J.W. Longterm retention rates of lamotrigine, gabapentin, and topiramate in chronic epilepsy // Epilepsia, Dec 2000. – V. 41. – P. 15926.
- Lim L.L., Ahmed A. Limited efficacy of levetiracetam on myoclonus of different etiologies // Parkinsonism Relat Disord. – 2005. – V. 11. – P. 135137.
- Lynch Berkley A. T he synaptic vesicle protein SV2A is the binding site for the antiepileptic drug levetiracetam // PNAS. – 2004. – V. 101. – P. 98619866
- Long L. Levetiracetam monotherapy during pregnancy: a case series // Epilepsy Behav. – 2003. – V. 4. – P. 447448.
- L_scher W, H_nack D. Profile of ucb L059, a novel anticonvulsant drug, in models of partial and generalized epilepsy in mice and rats // European Journal of Pharmacology 1993. – V. 232. – P. 147158.
- L_scher W, H_nack D, Rundfeldt C. Antiepileptogenic effects of the novel anticonvulsant levetiracetam (ucb L059. – P. in the kindling model of temporal lobe epilepsy // The Journal of Pharmacology and Experimental Therapeutics 1998. – V. 284. – P. 474479.
- Madeja M., Margineanu D.G., Gorji A. et al. Reduction of voltageoperated potassium currents by levetiracetam: a novel antiepileptic mechanism of action? // Neuropharmacology. – 2003. – V. 45. – P. 661671.
- Magaudda A., Gelisse P., Genton P. Antimyoclonic effect of levetiracetam in 13 patients with UnverrichtLundborg disease: clinical observations // Epilepsia. – 2004. – V. 45. – P. 678681.
- Mancuso M., Galli R., Pizzanelli C. et al. Antimyoclonic effect of levetiracetam in MERRF syndrome // J Neurol Sci. – 2006. – V. 243. – P. 9799.
- Mandelbaum D.E., Bunch M., Kugler S.L., Venkatasubramanian A., Wollack J.B. Efficacy of levetiracetam at 12 months in children classified by seizure type, cognitive status, and previous anticonvulsant drug use // J Child Neurol. – 2005. – V. 20. – P. 590594.
- Margineanu D.G., Klitgaard H. Inhibition of neuronal hypersynchrony in vitro differentiates levetiracetam from classical antiepileptic drugs // Pharmacol Res, 2000. – V. 42. – P. 281285.
- Marson A.G., Hutton J.L., Leach J.P. et al. Levetiracetam, oxcarbazepine, remacemide and zonisamide for drug resistant localizationrelated epilepsy: a systematic review // Epilepsy Res. – 2001. – V. 46. – P. 259270.
- Martin Peter, Guth Christoph. Unusual devastating selfinjurious behaviour in a patient with a severe learning disability: treatment with citalopram// Psychiatr. Bull. . – 2005. – V. 29. – P. 108 – 110.
- Mart_nezJu_rez Iris E., Alonso Mar_a Elisa, Medina Marco T. et al. Juvenile myoclonic epilepsy subsyndromes: family studies and longterm followup // Brain . – 2006. – 10.1093/brain/awl048.
- Mauri J.J., Tajero C., Pinol G., Mostacero E. Levetiracetam in idiopathic generalised epilepsies // Epilepsia 2005. – V.46, suppl 6. – P. 101
- Mecarelli Oriano, Vicenzini Edoardo, Pulitano Patrizia et al. Clinical, Cognitive, and Neurophysiologic Correlates of ShortTerm Treatment with Carbamazepine, Oxcarbazepine, and Levetiracetam in Healthy Volunteers // The Annals of Pharmacotherapy. – 2004. – V. 38. – P. 18161822.
- Morrell M.J., Leppik I., French J. et al. The KEEPER trial: levetiracetam adjunctive treatment of partialonset seizures in an openlabel communitybased study // Epilepsy Res . – 2003. – V. 54. – P. 153161.
- Morrow J., Russell A., Guthrie E. et al. Malformation risks of antiepileptic drugs in pregnancy: a prospective study from the UK Epilepsy and Pregnancy Register // Journal of Neurology, Neurosurgery, and Psychiatry. – 2006. – V.77. – P.193198
- Motamedi M., Nguyen D.K., Zaatreh M. et al. Levetiracetam efficacy in refractory partialonset seizures, especially after failed epilepsy surgery // Epilepsia. – 2003. – V. 44. – P. 211214
- Mula M., Trimble M.R., Yuen A. et al. Psychiatric adverse events during levetiracetam therapy // Neurology. – 2003. – V.61. – P.704706
- Nakken K.O., Eriksson A.S., Lossius R., Johannessen S.I. A paradoxical effect of levetiracetam may be seen in both children and adults with refractory epilepsy // Seizure. – 2003. – V. 12. – P. 4246.
- Nash E.M., Sangha K.S. Levetiracetam American Journal of HealthSystem // Pharmacy. – 2001. – V. 58. – P. 11951199
- Nasrallah K., Silver B. Hyponatremia associated with repeated use of levetiracetam // Epilepsia. – 2005. – V. 46. – P. 972973.
- Nicolson Andrew, Lewis Sheila A., Smith David F. A prospective analysis of the outcome of levetiracetam in clinical practice // NEUROLOGY. – 2004. – V.63. – P.568570
- Niespodziany I., Klitgaard H., Margineanu D.G. Desynchronizing effect of levetiracetam on epileptiform responses in rat hippocampal slices // Neuroreport. – 2003. – V. 14. – P. 12731276.
- Opp J., Tuxhorn I., May T. et al. Levetiracetam in children with refractory epilepsy: a multicenter open label study in Germany // Seizure. – 2005. – V. 14. – P. 476484.
- Otoul C., Arrigo C., van Rijckevorsel K., French J.A. Metaanalysis and indirect comparisons of levetiracetam with other secondgeneration antiepileptic drugs in partial epilepsy // Clin Neuropharmacol. – 2005. – V. 28. – P. 7278.
- PastorMilan E., GonzalezTorres V., Vilches R. The value of levetiracetam in epileptic status // Rev Neurol. – 2005. – V. 41. – P. 508509.
- Paul F., Meencke H.J. Levetiracetam in focal epilepsy and hepatic porphyria: a case report // Epilepsia. – 2004. – V. 45. – P. 559560.
- Pennell Page B. Antiepileptic drug pharmacokinetics during pregnancy and lactation // Neurology. – 2003. – V.61. – P.S35S42
- Piazzini A., Chifari R., Canevini M.P. et al. Levetiracetam: An improvement of attention and of oral fluency in patients with partial epilepsy // Epilepsy Res . – 2006. – V. 68. – P. 181188.
- Pisani A., Bonsi P., Martella G. et al. Intracellular calcium increase in epileptiform activity: modulation by levetiracetam and lamotrigine // Epilepsia. – 2004. – V. 45. – P. 719728.
- Privitera M. Efficacy of levetiracetam: a review of three pivotal clinical trials // Epilepsia. – 2001. – V. 42, Suppl 4. – P. 3135.
- RagueneauMajlessi I., Levy R.H., Janik F. Levetiracetam does not alter the pharmacokinetics of an oral contraceptive in healthy women // Epilepsia. – 2002. Литература – V. 43. – P. 697702.
- Renganathan R., Delanty N. Juvenile myoclonic epilepsy: underappreciated and underdiagnosed // Postgrad Med. J. – 2003. – V. 79. – P. 78.
- Riviello Jr James J. Pharmacology Review: Drug Therapy for Neonatal Seizures: Part 2 // NeoReviews. – 2004. – V. 5. – P. e262 – e268.
- Rocamora R., SchulzeBonhage A. Levetiracetam reduces interictal activity frequency and duration in patients with primary generalised epilepsy // Epilepsia. – 2005. – V.46, Suppl. 6. – P. 102
- Rossetti A.O., Bromfield E.B. Levetiracetam in the treatment of status epilepticus in adults: a study of 13 episodes // Eur Neurol. – 2005. – V. 54. – P. 3438.
- Rugino T.A., Samsock T.C. Levetiracetam in autistic children: an openlabel study // J Dev Behav Pediatr. – 2002. – V. 23. – P. 225230.
- Sahin Mustafa., Menache Caroline C., Holmes Gregory L., Riviello, Jr. James J. Prolonged treatment for acute symptomatic refractory status epilepticus: Outcome in children // Neurology. – 2003. – V. 61. – P. 398.
- Saiju Jacob, Darren Martin, Rajabally Yusuf A. Juvenile myoclonic epilepsy in an elderly patient // Age Ageing. – 2006. – V. 35. – P. 194 – 196.
- SalasPuig J., Serratosa J.M., Viteri C., GilNagelRein A., and Grupo Espanol del Estudio SKATE // Safety of levetiracetam as adjunctive therapy in epilepsy: the SKATE trial in Spain // Rev Neurol. – 2004. – V. 38. – P. 11171122.
- Schauer R., Singer M., Saltuari L. et al. Suppression of cortical myoclonus by levetiracetam // Mov Disord. – 2002. – V. 17. – P.411415.
- SchulzeBonhage A., Feil B., Fauser S., Homberg V. Levetiracetam in combined therapy for focal epilepsy: experience with 80 patients // Nervenarzt. – 2004. – V. 75. – P. 749754.
- Sechi G.P., Deiana G.A., Deriu M.G. et al. Nonfluent speech in patients with partial epilepsy: benefitial effect of levetiracetam // Epilepsia. – 2005. – V.46, Suppl. 6. – P.105
- Shorvon S.D., Lowenthal A., Janz D. et al. Multicenter doubleblind, randomized, placebocontrolled trial of levetiracetam as addon therapy in patients with refractory partial seizures. European Levetiracetam Study Group // Epilepsia. – 2000. – V. 41. – P. 11791186.
- Silverman Isaac E., Restrepo Lucas, Mathews Gregory C. Poststroke Seizures // Arch Neurol. – 2002. – V.59. – P.195201.
- Sisodiya S.M., Sander J.W., Patsalos P.N. Carbamazepine toxicity during combination therapy with levetiracetam: a pharmacodynamic interaction // Epilepsy Res. – 2002. – V. 48. – P. 217219.
- Smith K., Bettz T. The effect of add on therapy with leveteracetam (UCBL059. – P.) on patients with resistant juvenile myoclonic epilepsy (abstract) // Fourth Eilat Conference on New Antiepileptic Drugs. – 1998. – P. 57.
- Smith K., Betts T., Pritchett L. Levetiracetam, a promising option for the treatment of juvenile myoclonic epilepsy // Epilepsia 2000. – V.41, suppl. – P.39.
- Specchio L.M., Gambaedella A., Giallonardo A.T. et al. Openlabel pragmatic study in the treatment of juvenile myoclonic epilepsy // Epilepsia. – 2005. – V.46, Suppl. 6. – P. 102
- Steinhoff B.J., Trinka E., Wieser H.G., and for the DACHLEV Study Group. Levetiracetam in patients with refractory epilepsy: results of the SKATE trial in Austria, Germany and Switzerland // Seizure. – 2005. – V. 14. – P. 490496.
- Stodieck S., Steinhoff B.J., Kolmsee S., van Rijckevorsel K. Effect of levetiracetam in patients with epilepsy and interictal epileptiform discharges // Seizure. – 2001. – V. 10. – P. 583587.
- Stoner Steven C, Lea Jessica W., Wolf Angel L., Berges Arnaldo A. Levetiracetam for Mood Stabilization and Maintenance of Seizure Control Following Multiple Treatment Failures // The Annals of Pharmacotherapy. – 2005. – V. 39. – P. 19281931.
- Striano P., Manganelli F., Boccella P. et al. Levetiracetam in patients with cortical myoclonus: a clinical and electrophysiological study // Mov Disord. – 2005. – V. 20. – P. 16101614.
- Tan M.J., Appleton R.E. Levetiracetam is a new antiepileptic drug that is cur rently not licensed for use in children // Seizure. – 2004. – V. 13. – P. 142145.
- ten Berg K., Samren E.B., van Oppen A.C. et al. Levetiracetam use and pregnancy outcome // Reprod Toxicol. – 2005. – V. 20. – P. 175178.
- Turjanski Nora, Lloyd Geoffrey G. Psychiatric sideeffects of medications: recent developments Advan // Psychiatr. Treat. – 2005. – V. 11. – P. 58 – 70.
- Vendru P., Wajgt A., Schiemann J., Noachtar S. Efficacy and safety of levetiracetam 3000 mg/d as adjunctive treatment in adolescents and adults suffering from idiopathic generalised epilepsy with myoclonic seizures // Epilepsia 2005. – V.46, suppl 6. – P. 5657
- Vigevano F. Levetiracetam in pediatrics // J Child Neurol. – 2005. – V. 20. – P. 8793.
- Walker M.C., Sander J.W. Overtreatment with antiepileptic drugs // CNS Drugs. – 1994. – V. 2. – P. 335340.
- Weber S., Beran R.G. A pilot study of compassionate use of Levetiracetam in patients with generalised epilepsy // J Clin Neurosci. – 2004. – V. 11. – P. 728731.
- Welty T.E., Gidal B.E., Ficker D.M., Privitera M.D. Levetiracetam: a different approach to the pharmacotherapy of epilepsy // Ann. Pharmacother. – 2002. – V. 36: 296304.
- Wheless J.W., Ng Y.T. Levetiracetam in refractory pediatric epilepsy // J Child Neurol. – 2002. – V. 17. – P. 413415.
- White J.R., Walczak T.S., Leppik I.E. et al. Discontinuation of levetiracetam because of behavioral side effects A casecontrol study // NEUROLOGY. – 2003. – V.61. – P.12181221
- Yan H.D., Jiqun C., Ishihara K. et al. Separation of antiepileptogenic and antiseizure effects of levetiracetam in the spontaneously epileptic rat (SER) // Epilepsia. – 2005. – V. 46. – P. 11701177.
- Zaatreh M.M. Levetiracetam in porphyric status epilepticus: a case report // Clin Neuropharmacol. – 2005. – V. 28. – P. 243244.
- Zupanc M.L. Infantile spasms // Expert Opin Pharmacother. – 2003. – V. 4. – P. 20392048.
