Химиотерапия паклитакселом в сочетании с препаратом платины по сравнению с обычной химиотерапией препаратом платины у женщин с рецидивом рака яичников: испытание ICON4/AGO-OVAR-2.2
СтатьиОпубликовано в журнале: Lancet, 361: 2099-2106 (2003)
Участники испытаний ICON и AGO*
РЕЗЮМЕ
История вопроса.
Несмотря на успехи в лечении рака яичников, у большинства больных в пределах трех лет после постановки диагноза развивается рецидив заболевания. Единого мнения относительно лечения второй линии в случае рецидива в настоящее время нет. Мы провели оценку комбинации паклитаксела с препаратом платины в качестве схемы для такого лечения.
Методы.
В параллельных международных многоцентровых рандомизированных испытаниях с января 1996 по март 2002 г.г. из 119 больниц пяти стран в испытание было включено 802 больных с рецидивом чувствительного к препаратам платины рака яичников. Рецидив у больных произошел после шестимесячного периода, в течение которого лечение им не проводили. Эти больные были рандомизированы на химиотерапию комбинацией паклитаксел/платина или на обычную химиотерапию препаратом платины. Анализ, за исключением учета токсических эффектов, проводился по отношению ко всем исходно намеченным для лечения больным.
Результаты.
За медианный срок наблюдения, составлявший 42 месяца, скончалось 530 больных. Кривые выживания говорят о преимуществе комбинации паклитаксел/платина (отношение риска 0,82 [95%-ный доверительный интервал 0,69-0,97], р=0,02), что дает абсолютную разницу для выживания за два года, равную 7%, между группой паклитаксел/платина и группой обычного лечения (57 и 50% [95%-ный ДИ 1-12]), и разницу в медианном выживании, равную 5 месяцам (29 и 24 месяца) [1-11]. У 717 больных отмечалась прогрессия заболевания или они скончались. Кривые выживаемости в отсутствие прогрессии заболевания обнаруживают различие в пользу комбинации паклитаксел/платина (отношение риска 0,76 [0,66-0,89], р=0,0004), что соответствует абсолютной разности для годичного выживания при отсутствии прогрессии, равной 10% (50 и 40% [4-15]) и для разности медианной выживаемости в отсутствие прогрессии заболевания, равной 3 месяцам (13 и 10 месяцев [1-5]).
Интерпретация.
Комбинация паклитаксел/платина дает лучшую, по сравнению с обычной химиотерапией препаратом платины, общую выживаемость и выживаемость без прогрессии заболевания среди больных с рецидивом чувствительного к препарату платины рака яичников.
Введение
Рак яичников является четвертым по распространенности раком среди женщин, отвечающим (по оценочным данным) за 114 000 летальных исходов во всем мире на 2000 год.1 Лечение этого заболевания на протяжении последних тридцати лет улучшилось за счет успехов в проведении хирургической операции и химиотерапии на основе препаратов платины, однако у большинства женщин с раком яичников развивается рецидив, и они умирают в пределах пяти лет.
Единое мнение относительно оптимального лечения второй линии при рецидиве заболевания отсутствует, несмотря на несколько имеющихся препаратов. Лечение первой линии осуществляют путем химиотерапии, основанной на препаратах платины, причем все чаще используют карбоплатин (в комбинации с таксаном или без него), а не цисплатин, поскольку карбоплатин обладает меньшей токсичностью при одинаковой активности.2,3 При рецидиве заболевания вероятность ответа на повторную химиотерапию, основанную на препарате платины, зависит от длительности периода, в течение которого препарат платины не применялся.4 Когда такой период превышает шесть месяцев, многие клиницисты предпочитают повторное лечение больных препаратом платины с использованием ранее применявшегося препарата или переводя больную с карбоплатина на цисплатин или наоборот. Женщины, заболевание которых прогрессировало в условиях исходного лечения препаратом платины, а также те, у которых рецидив развивается в пределах шести месяцев после исходного лечения препаратом платины, редко отвечают на продолжение лечения препаратом платины и считаются имеющими заболевание, резистентное к платине. Для таких больных в качестве активного лекарственного препарата и был впервые предложен паклитаксел.5 Этот препарат обычно хорошо переносится, наиболее частыми побочными эффектами являются алопеция, миелосупрессия и нейропатии.
У большинства больных заболевание не является резистентным к платине, однако в пределах шести месяцев или более длительного срока после лечения первой линии у них развивается рецидив.6 Неясно, будет ли применение такого препарата, как паклитаксел, обладающего иным механизмом действия, чем препараты платины, полезным для этих больных (при использовании в сочетании с платиной) в большей степени, чем повторение обычной схемы химиотерапии на основе платины. В исследованиях на больных с рецидивами заболевания, чувствительного к платине, после применения комбинации карбоплатин/паклитаксел ответ составлял до 90%.7,8 Однако нам неизвестны какие-либо проводившиеся ранее рандомизированные испытания по сравнению комбинации паклитаксел/платина и обычной химиотерапии на основе платины у больных с раком яичников, дающих рецидив через шесть или более месяцев после химиотерапии. В рандомизированных испытаниях ICON4 и AGO-OVAR-2.2 мы поставили вопрос об эффективности комбинации паклитаксел/платина у больных с ранее леченым раком яичников. Наша задача заключалась в том, чтобы выяснить, следует ли добавлять паклитаксел к препарату платины для лечения больных с заболеванием, чувствительным к платине, и которых в противном случае лечили бы обычными схемами на основе препарата платины.
Больные и методы
Испытания ICON4 и AGO-OVAR-2.2 проводились как параллельные испытания.
Испытание ICON4 координировалось Институтом Марио Негри (Милан, Италия) (IRFMN) и Отделом клинических испытаний Совета по медицинским исследованиям (Лондон, Великобритания) (MRC CTU). Испытание AGO-OVAR- 2.2 координировалось AGO (Карлсруэ, Германия).
Больные
Больных набирали в испытание в период с января 1996 года по март 2002 года из 119 больниц в пяти странах. Больных направляли на один из трех протоколов; один из них был координирован MRC CTU для больниц Великобритании, Норвегии и Швейцарии; один был координирован IRFMN для Италии, и один проводился под эгидой AGO. Критерии для включения больных в испытание были следующими: рецидивировавший эпителиальный рак яичников, требовавший химиотерапии; ранее проводившаяся химиотерапия с использованием препарата платины; отсутствие лечения в течение срока, превышавшего 6 месяцев (>12 месяцев для группы ICON4 в Италии); отсутствие одновременного или возникшего ранее злокачественного заболевания, могущего повлиять на лечение или его результаты; полученное после информирования письменное согласие больной на участие в испытании.
Критерии, которым должны были удовлетворять больные для участия в испытании слегка отличались для трех протоколов. По протоколу MRC CTU больным в прошлом могла проводиться более чем одна линия химиотерапии, в то время как больным, рандомизированным в соответствии с итальянским протоколом AGO, разрешалось иметь только одну предшествовавшую линию химиотерапии. Для больных, рандомизированных в соответствии с итальянскими протоколами, требовалось наличие измеряемой опухоли; это требование отсутствовало для протоколов MRC CTU или AGO. Диагноз рецидива заболевания на момент включения в испытание у 18 больных по протоколу MRC CTU был основан на повышенном уровне СА125. Больные, рандомизированные на протокол AGO, должны были ранее лечиться на схеме цисплатин/паклитаксел или карбоплатин/паклитаксел; в испытании ICON4 требовалось, чтобы больные прошли предшествовавшую химиотерапию препаратом платины с паклитакселом или без него.
Методы
Больных, рандомизировали на обычную химиотерапию препаратом платины или на аналогичную дозу препарата платины с паклитакселом, причем лечение начинали в возможно более короткие сроки после рандомизации. В соответствии со всеми протоколами курсы лечения проводились раз в три недели. В соответствии с протоколом MRC CTU каждой больной следовало провести по крайней мере шесть курсов. По итальянскому протоколу, больным назначалось по крайней мере три курса, а дальнейшие три курса назначались в зависимости от ответа на лечение. По протоколу AGO, больным назначалось, как минимум, шесть курсов и максимум восемь курсов лечения, оценка ответа на лечение проводилась после второго и четвертого курсов. Все препараты вводились внутривенно в первый день каждого из курсов. Дозу карбоплатина определяли с помощью метода площади под кривой (AUC), описанного Кальвертом с соавт.9, и она составляла, как минимум, 5 (СГФ+25) мг, где СГФ представляет собой СГФ, определявшуюся радиоизотопным методом или путем сбора суточной мочи. Если скорость гломерулярной фильтрации определяли по формуле Кокрофта, доза карбоплатина составляла, как минимум, 6 (СГФ+25) мг. Запланированная минимальная доза цисплатина только для больных испытания ICON4 составляла 75 мг/м2 при введении цисплатина в качестве единственного препарата, и 50 мг/м2, когда его вводили в комбинации с другими препаратами. Больные в испытании ICON4, назначенные на лечение комбинацией паклитаксел/платина, должны были получать паклитаксел в дозе 175 мг/м2 путем 3-часового вливания с последующим вливанием карбоплатина или цисплатина в вышеуказанной дозе. Больные в протоколе AGO, назначенные в группу лечения паклитакселом/карбоплатином, должны были получать паклитаксел в дозе 185 мг/м2 в форме 3-часового вливания с последующим вливанием карбоплатина в дозе, указанной выше.
Рандомизацию для трех протоколов проводили независимо. О всех больных собирали одинаковую информацию. Отношение рандомизации между группами лечения составляло 1:1. Для рандомизации, выполнявшейся по телефону или факсу, использовали метод минимизации на компьютере. В двух протоколах испытания ICON4 (MRC CTU и итальянский) стратификация проводилась в отношении одних и тех же факторов, а именно учреждения, возраста больного, последней проводившейся химиотерапии, времени после завершения последней химиотерапии и запланированного лечения препаратом платины. Запланированная схема лечения препаратом платины должна была быть определена до рандомизации. В протоколе AGO стратификацию проводили относительно времени после завершения последней химиотерапии, а также относительно того, проводилась или не проводилась больной вторая операция циторедукции (уменьшения массы опухоли.
Для испытания ICON4 был создан независимый комитет по мониторингу данных и этике, состоявший из двух клиницистов и одного статистика, не связанных с испытанием. Ход испытания и его незакрытые результаты, а также все прочие важные внешние данные рассматривались ориентировочно раз в год на протяжении периода записи больных в испытание. Комитет не следовал заранее определенным статистическим правилам для остановки. Для испытания AGO, комитет по мониторингу данных и этике не создавали, но протокол рецензировался и принимался местными комитетами по этике каждого из участвовавших центров.
Данные, относящиеся к периоду до лечения, собирали во время рандомизации.
Данные о лечении собирали для каждого курса. Данные последующих обследований собирали раз в три месяца на протяжении первых двух лет и раз в шесть месяцев в дальнейшем. Для сбора данных этих обследований мы использовали одностраничный формуляр, содержащий вопросы относительно заболевания, жизненного статуса, симптоматики, побочных эффектов и лечения, после последнего отчета. Все эти данные собирались, проверялись и хранились в электронном виде группами, участвовавшими в испытании.
Данные о качестве жизни собирали для всех больных, лечившихся по протоколу MRC CTU и AGO. Мы использовали анкету о качестве жизни QLQ-C30 (версия 2.0), разработанную Европейской организацией по исследованию и лечению рака (EORTC). Больные, лечившиеся по протоколу MRC CTU, заполняли анкету исходно, перед каждым курсом лечения по протоколу, а также во время визитов через 6, 9 и 12 месяцев. Больные, получавшие лечение по протоколу AGO, заполняли анкету исходно, перед вторым и третьим курсами лечения по протоколу, в конце лечения по протоколу и раз в три месяца на протяжении года после завершения лечения по протоколу.
Мы выполнили несколько анализов для подгрупп. Критерии для подгрупп включали группу рандомизации, время после завершения последней химиотерапии, число предшествовавших линий химиотерапии, проводившееся ранее лечение таксанами, препарат платины, запланированный для лечения, возраст и функциональный статус.
Статистический анализ
Главным учетным критерием была общая выживаемость; вторичными критериями были выживание без прогрессии заболевания и качество жизни. Когда проводились расчеты размеров исходной выборки, имелись лишь немногочисленные данные относительно исхода рецидивировавшего рака яичников. Мы ожидали, что двухлетняя выживаемость будет составлять около 5% для контрольной группы, а абсолютные различия в выживаемости за два года не будут превышать 5-10%.
Всего мы запланировали для испытания 800 больных, чтобы уверенное выявить абсолютные различия в выживаемости за два года, составляющие 5% (5-10%) с уверенностью 95% при уровне достоверности в 5%; это соответствует отношению риска 0,77. На завершающем заседании 8 февраля 2001 года Комитет по мониторингу данных и этике отметил, что выживание в контрольной группе было значительно более высоким, чем при исходных расчетах уверенности. Двухлетнее выживание в группе, где проводилось обычное лечение, составляло 50%. Поэтому мы пересмотрели этот вопрос. Мы рассчитали, что 800 больных будет достаточно для надежной идентификации абсолютных различий, составляющих 11% для выживаемости за два года (50-61%) с вероятностью 90% при уровне достоверности в 5%, что дает отношение риска, равное 0,71. Поэтому запланированное для испытания число больных осталось без изменений.
Мы сравнили кривые Каплана-Мейера для общей выживаемости и выживаемости без прогрессии заболевания с вариантом лог- рангового критерия Мантел-Кокса при стратификации на три группы рандомизации. Общее выживание определялось как время от момента рандомизации до летального исхода от любой причины; больные, о которых было известно, что они живы на момент анализа, учитывали на момент последнего обследования. Мы определили время выживания без прогрессии заболевания как время от момента рандомизации до первого проявления прогрессии заболевания или летального исхода от любой из причин; больные, о которых было известно, что они живы и не имеют признаков прогрессии заболевания на момент анализа, учитывали на момент проведения последнего обследования. Само по себе повышение концентрации СА125, т.е.
повышение при отсутствии клинических или радиологических признаков прогрессирующего заболевания, не считалось указанием на прогрессию заболевания. Абсолютное преимущество на конкретный момент времени рассчитывалось по выживаемости, оцененной в контрольной группе по Каплану- Мейеру на этот момент времени (выживание в контроле) и отношению риска с использованием следующего выражения: абсолютное преимущество=exp(отношение риска х log[выживание в контроле])- выживание в контроле.
Этот же подход был принят для выживания без прогрессии заболевания. Хотя такой подход косвенно предполагает наличие пропорциональных рисков, он является более предпочтителен чем учет различий между кривыми по Каплану- Мейеру в индивидуальные моменты времени. Мы рассчитывали различия в отношении медиан аналогичным образом, однако, с использованием выражения: разность медиан=(медиана контроля/отношение риска) – медиана контроля. Этот подход исходит из тог, что значения времени выживания имеют приблизительно экспоненциальное распределение.
Мы оценили относительные преимущества химиотерапии препаратами платины для выживания в опытном порядке в подгруппах, определенных на основе группы рандомизации, времени после завершения последней химиотерапии, числа предыдущих линий химиотерапии, предшествовавшего применения таксанов, препарата платины, запланированного для лечения, т.е. карбоплатина или цисплатина, возраста и функционального статуса. Для того, чтобы оценить различия в относительной величине эффекта для различных подгрупп, мы использовали критерий χ2 для взаимодействия или, в тех случаях, когда это было возможно, критерий χ2 для тренда.
Для анализа данных по качеству жизни, как это было рекомендовано, мы использовали пять функциональных шкал (физическую, ролевую, эмоциональную, когнитивную и социальную), девять шкал симптоматики (чувство усталости, тошнота и рвота, боли, одышка, бессонница, потеря аппетита, запор, понос и финансовые трудности), а также общий статус здоровья. С учетом характера рака яичников нас особенно интересовали чувство усталости, тошнота/рвота и болевая симптоматика, а также общее (глобальное) состояние здоровья в качестве общего критерия. Для каждого критерия мы анализировали два набора суммарных статистических параметров: наихудший балл и площадь под кривой за первые шесть месяецв.11 Для анализа использовался непараметрический критерий Манна- Уитни.12 Мы выбрали значение р=0,005 в качестве значения для выявления достоверности (из-за множественных сравнений).
Анализы проводились для всех больных, включенных в испытание (в англоязычной литературе -- критерий "намерение лечить"), за исключением анализа токсических эффектов. Анализы в отношении токсических эффектов ограничивались больными, получившими по крайней мере один курс назначенного лечения. Все значения р являются двусторонними. Анализ был проведен с помощью пакета SAS (версия 8.20).
Роль источника финансирования
Спонсоры испытания не играли роли в планировании испытания, сборе данных, анализе данных, интерпретации данных или написании отчета.
Результаты
В испытание было включено 802 больных. Длитеьность периода поступления больных в испытание варьировал для трех протоколов: для итальянской группы ICON4 – с января 1996 по март 2002 г.г.; для группы MRC CTU ICON4 – с мая 1996 по март 2002 г.г., и для AGO – с октября 1996 по сентябрь 1999 г.г. Четыреста десять больных было включено в группу, получавшую обычную химиотерапию на основе препаратов платины, и 392 больных в группу паклитаксел/платина (Рис. 1).
Характеристики до лечения были одинаковыми для обеих групп (Таблица 1).
Типы полученного лечения указаны в Таблице 2. 580 больных (72%) в обеих группах лечения получили минимум шесть курсов химиотерапии (Рис. 1). Причины незавершения шести курсов лечения включали следующее: прогрессия заболевания или летальный исход (109 [56%]), токсические эффекты во время лечения 77 [39%]) и желание больной (9 [5%]). Только три больные не получили назначенной химиотерапии (Рис. 1). 123 (41%) из 300 больных в группе, получавшей обычное лечение, и 129 (40%) из 322 больных, получавших лечение паклитакселом и карбоплатином, получили более 90% запланированной общей дозы, а 54 (18%) из 300 больных и 76 (23%) из 330 больных, соответственно, получили более 90% общей дозы карбоплатина. Соответствующие цифры для паклитаксела в группе, получавшей паклитаксел/карбоплатин, составляли 266 (71%) из 376 больных в отношении общей дозы и 160 (43%) из 376 в отношении общей интенсивности дозы.
В Таблице 3 приведена доля больных, у которых во время лечения отмечался умеренный или тяжелый побочный эффект. Как и можно было ожидать, комбинация паклитаксел/платина давала более высокий процент алопеции по сравнению с обычной химиотерапией препаратом платины. Процент токсических эффектов умеренной или тяжелой степени в отношении кроветворения был более высоким среди больных, получавших обычную химиотерапию препаратом платины, по сравнению с группой, где лечение проводилось комбинацией паклитаксел/платина. Умеренные или тяжелые неврологические токсические эффекты отмечались у 76 (20%) больных, получавших комбинацию паклитаксел/платина. Прочие токсические эффекты были редкими в обеих группах лечения.
К марту 2003 года (среднее медианное время наблюдения 42 месяца) умерли 530 больных (66%). Кривые выживаемости соответствуют отношению риска 0,82 (95% ДИ 0,69-0,97, р=0,02; Рис. 2), что соответствует абсолютной разности в двухгодичной выживаемости, составляющей 7% в пользу химиотерапии комбинацией паклитаксел/препарат по сравнению с обычным лечением (57 и 50% [95% ДИ для разности 1-12]). Для медианного выживания отношение риска соответствует разности, равной 5 месяцам (29 и 24 месяца [1-9]). У 717 больных (89%) развилось прогрессирующее заболевание или они скончались. Кривые выживания без прогрессии заболевания, приведены на Рис. 3. Отношение риска, составляющее 0,76 (0,66-0,89, р=0004) в пользу схемы паклитаксел/препарат платины, соответствует оценочной абсолютной разности значений годичного выживания без прогрессии заболевания, составляющей 10% (40 и 50% [4-15]). Этот результат соответствует абсолютной разности для медианного выживания без признаков прогрессии заболевания, составляющей 3 месяца в пользу схемы паклитаксел/препарат платины (9 и 12 месяцев [1-4]).
У 69 (54%) из 128 больных в группе, получавшей обычную химиотерапию, наблюдался полный или частичный ответ на лечение, по сравнению с 78 (66%) из 119 больных в группе, получавшей схему паклитаксел/препарат платины.
Соответственно, ответ на лечение представляется лучшим для группы паклитаксел/препарат платины (разность 12% [-0,1% до 24%], р=0,06). Мы не отметили каких-либо четких признаков того, что схема паклитаксел/платина была более эффективной или менее эффективной по сравнению с обычной химиотерапией препаратом платины для любой из подгрупп по критериям общей выживаемости или выживаемости без признаков прогрессии заболевания (Рис. 4 и 5).
Детали лечения, проводившегося во время прогрессии заболевания, имелись для 437 из 536 больных. Всего 70 (31%) больных в обычной группе лечения получали при прогрессии лечение на основе препаратов таксана. В группе, получавшей комбинацию паклитаксел/платины, 16 (8%) больных продолжали получать при прогрессии дальнейшее лечение схемой на основе таксана.
В группе, использовавшей протокол MRC CTU ICON4, 482 (90%) из 536 больных заполнили анкету по оценке качества жизни исходно до начала лечения. Все шкалы для двух групп лечения были сбалансированными. Большинство больных не имели функциональных затруднений или они были незначительны, число симптомов умеренной или большой тяжести исходно было невелико. На протяжении первых шести месяцев после рандомизации значения наихудшего балла и площадей под кривыми не отличались для двух групп лечения по всем пяти функциональным шкалам, восьми из девяти шкалам симптоматики и по глобальному статусу здоровья. Единственным исключением была тошнота и рвота, которая была более тяжелой для больных, получавших обычную химиотерапию (р=0,0014 для наихудшего балла, р=0,005 для площади под кривой). На Рис. 6 приведены значения балла во времени для трех симптомов, наиболее типичных для рака яичников – чувства усталости, тошноты и рвоты, а также для боли и глобального статуса здоровья. Для глобального статуса здоровья отмечалось незначительное снижение доли больных, определяемых как имеющие нехорошее самочувствие или очень низкий статус здоровья на протяжении первых шести месяцев. Аналогичная тенденция отмечалась для чувства усталости. Напротив, болевая симптоматика в обеих группах возвращается к значениям, характерным для периода до лечения.
Хотя имеются определенные указания на различия по тошноте и рвоте в пользу группы, получавшей паклитаксел/платина, такие различия носят временный характер, относясь лишь к первым 15 неделям.
Обсуждение
С учетом данных по выживаемости без прогрессии заболевания и общей выживаемости, в нашем испытании достаточно число больных выжило и находилось в группе риска на 4-летний срок, чтобы сделать вывод о том, что общие результаты на этот срок являются надежными. Девяносто процентов больных было рандомизировано после первого рецидива, а 75% более чем через 12 месяцев после завершения химиотерапии препаратом платины. Считается, что такие больные имеют разумный прогноз. То обстоятельство, что наше испытание является крупномасштабным, позволило нам проанализировать подгруппы для оценки того, насколько однотипным является эффект комбинации паклитаксел/ платина. Тем не менее, многие из подгрупп невелики по численности и поэтому возможность выявления реальных различий невелика. Но, как бы то ни было, хорошие данные в пользу большего эффекта или меньшего эффекта комбинации паклитаксел/платины по сравнению с обычным лечением в любой из подгрупп отсутствуют. Величина эффекта комбинации паклитаксел/платина близка для разных групп рандомизации, несмотря на различия в критериях, использованных для включения больных в испытание, и факторы стратификации. Далее, нет указаний на то, что эффект комбинации паклитаксел/платина отличался для больных, которые получали таксаны в качестве составной части лечения первой линии (около 40% общего числа рандомизированных больных) и тех больных, которые таксаны не получали.
Паклитаксел в качестве индивидуального препарата сравнивался с циклофосфамидом, доксорубицином и цисплатином (схема САР) среди больных, давших ответ на химиотерапию первой линии препаратом платины, однако заболевание у которых рецидивировало после более чем 12-месячного периода отсутствия лечения.13 В испытании, о котором идет речь, у 97 больных с оцениваемым заболеванием монотерапия паклитакселом давала медианный срок без прогрессии заболевания, составлявший 9 месяцев, по сравнению с 15,7 месяцами для схемы САР (отношение риска 0,69 [95%-ный ДИ 0,37-0,97]). Средняя общая выживаемость составляла 25,8 месяца для монотерапии паклитакселом и 34,7 месяца для схемы САР (0,58 [0,34-0,98]). Хотя число больных недостаточно велико, чтобы сделать окончательные выводы, эти результаты позволяют полагать, что химиотерапия на основе препарата платины является важным компонентом химиотерапии при рецидиве, если заболевание остается чувствительным к платине.
Наши результаты указывают на аддитивный эффект платины и паклитаксела.
Сходные данные были отмечены в ряде испытаний первой линии ( комбинация циклофосфамид 750 мг/м2 в сочетании с цисплатином 75 мг/м2 использовалась в испытании группы GOG-11114 и в испытании OV1015), но не в других испытаниях (монотерапия цисплатином в дозе 100 мг/м2; испытание GOG-13216 и карбоплатин с минимальным значением до AUC 5 или комбинация циклофосфамида 500 мг/м2, доксорубицина 20 мг/м2 и цисплатина 50 мг/м2, использовавшаяся в испытании ICON36)17. Результаты испытаний ICON3 и GOG-132 отличаются от положительного результата, отмеченного в нашем испытании, в котором 85% больных в группе паклитаксел/платина получали комбинацию карбоплатина и паклитаксела. Однако исследованные контингенты больных группы довольно различны. Женщины в нашем исследовании могут считаться имеющими чувствительное к платине заболевание и имеющими высокую вероятность ответа на дальнейшее назначение препарата платины, однако их заболевание, вероятно, менее чувствительно к платине, чем у больных, которым химиотерапия не проводилась вообще. В пользу этой теории говорит ответ на обычную химиотерапию, равный в наших условиях 54%, что слегка ниже, чем ожидается для лечения первой линии.14 Среди больных, давших рецидив заболевания, чувствительного к платине, паклитаксел может компенсировать относительное снижение чувствительности к платине. Другое возможное объяснение заключается в том, что количество платины, которое эти больные могут получить во время терапии второй линии ограничено по сравнению с количеством, которое они могут получить во время терапии первой линии. Например, лишь 40% наших больных получили более 90% общей запланированной дозы карбоплатина. Для сравнения укажем, что примерно 75% больных получили более 90% запланированной общей дозы карбоплатина в испытании ICON3 при терапии первой линии.6 Предварительные результаты испанского рандомизированного испытания по сравнению карбоплатина с комбинацией паклитаксел/карбоплатин у 81 больной с теми же самыми критериями включения в испытание, что и в протоколе MRC CTU, близки к нашим результатам в отношении процента реагирования, времени выживания без прогрессии заболевания и токсических эффектов.18 Паклитаксел в сочетании с препаратом платины обычно является более токсичной схемой, по сравнению с обычной схемой химиотерапии на основе платины, вызывая большую алопецию и неврологические токсические эффекты. Неврологические токсические эффекты отмечались у 20% больных, что близко к цифрам, наблюдающимся при лечении первой линии.6 Эта доля меньше по сравнению с ожидаемой, в частности поскольку треть больных ранее получала препарат таксана. Опыт исследований Дизона и соавт.8 является сходным, и применение доцетаксела у 3% наших больных могло внести определенный, хотя и незначительный вклад в меньший процент периферического неврита. Однако соблюдение назначенных правил лечения было хорошим, причем 72% больных завершили по крайней мере шесть курсов лечения. Другой причиной, конечно, могло быть то, что больные со склонностью к развитию нейропатий не вошли в испытание из-за опыта полученного ими во время лечения первой линии. Обычная химиотерапия препаратом платины связана с более серьезными токсическими эффектами в отношении кроветворения по сравнению со схемой паклитаксел/платина, что глвлрит в поддержку опубликованных ранее сообщений, что паклитаксел может оказывать защитное воздействие на костный мозг.19 Лечение рецидивов рака яичников содержит значительный паллиативный компонент. Поэтому оценка больной собственного качества жизни является важной, чтобы сказать, будет ли схема паклитаксел/платина иметь какие-либо недостатки по отношению к обычной химиотерапии препаратом платины (или наоборот) с точки зрения связанных с лечением токсических эффектов и бессимптомного интервала. Мы не обнаружили ясных указаний, что какая-то из использованных схем является хуже другой в отношении функциональных аспектов, симптоматики или глобального статуса здоровья.
Наши результаты говорят о положительном эффекте комбинации паклитаксел/платина на общую выживаемость и выживаемость без прогрессии заболевания в группе больных с рецидивом чувствительного к платине рака яичников. Паклитаксел чаще всего комбинировали с карбоплатином, а наиболее часто применявшаяся обычная схема химиотерапии препаратом платины включала использование карбоплатина в качестве единственного агента. Поэтому мы полагаем, что все женщины, у которых рецидив развивается позже, чем через 6 месяцев после завершения химиотерапии препаратом платины, должны рассматриваться в качестве кандидатов на комбинированную химиотерапию платиной и паклитакселом, даже если они получали паклитаксел в качестве составной части схемы лечения первой линии.
Заявление о конфликте интересов J.A.Lederman получил небольшой гонорар за специальные консультации компании Бристол-Майерс Сквибб.
Таблица 1. Группы рандомизации и исходные характеристики больных
|
Характеристика |
Обычная ХТ |
Паклитаксел+платина |
|
Численность в группе рандомизации |
||
|
ICON4 MRC CTU |
270 (66%) |
266 (68%) |
|
ICON4 Italy |
113 (28%) |
100 (26%) |
|
AGO |
27 (7%) |
26 (7%) |
|
Возраст (годы) |
||
|
<55 |
123 (30%) |
127 (32%) |
|
55-65 |
162 (40%) |
151 (39%) |
|
>65 |
125 (30%) |
114 (29%) |
|
Медиана |
59,2 |
60,0 |
|
Функциональный статус по ВОЗ |
||
|
0 |
262 (64%) |
246 (63%) |
|
1 |
122 (30%) |
121 (31%) |
|
2-3 |
26 (6%) |
25 (6%) |
|
Планируемый препарат платины |
||
|
Карбоплатин |
341 (83%) |
332 (85%) |
|
Цисплатин |
69 (17%) |
60 (15%) |
|
Последняя химиотерапия |
||
|
Паклиатаксел и карбоплатин |
141 (34%) |
133 (34%) |
|
Карбоплатин |
128 (31%) |
119 (30%) |
|
САР |
72 (18%) |
62 (16%) |
|
Паклитаксел и цисплатин |
20 (5%) |
27 (7%) |
|
Доцетаксел и карбоплатин |
14 (3%) |
7 (2%) |
|
Другие препараты на основе платины |
30 (7%) |
34 (9%) |
|
Другие препараты |
5 (1%) |
10 (3%) |
|
Число предшествующих линий химиотерапии |
||
|
1 |
380 (93%) |
354 (90%) |
|
2* |
24 (6%) |
22 (6%) |
|
>2* |
6 (1%) |
15 (4%) |
|
Неизвестно |
0 |
1 (<1%) |
|
Время после завершения последней химиотерапии (месяцы) |
||
|
≤12 |
111 (27%) |
92 (23%) |
|
>12 |
299 (73%) |
300 (77%) |
Таблица 2. Лечение по протоколу во время испытания
|
Обычная ХТ |
Паклитаксел+платина |
|
|
Лечение |
||
|
Карбоплатин (моно) |
292 (71%) |
1 (<1%) |
|
САР |
68 (17%) |
0 |
|
Карбоплатин и цисплатин* |
18 (4%) |
0 |
|
Цисплатин и доксорубицин |
12 (3%) |
0 |
|
Цисплатин (моно) |
8 (2%) |
0 |
|
Карбоплатин в комбинации (не с таксаном) |
3 (<1%) |
0 |
|
Паклитаксел и карбоплатин |
1 (<1%) |
314 (80%) |
|
Паклитаксел и цисплатин |
0 |
38 (10%) |
|
Паклитаксел, карбоплатин и цисплатин* |
0 |
19 (5%) |
|
Паклитаксел (моно) |
4 (1%) |
17 (4%) |
|
Прочее |
3 (<1%) |
1 (<1%) |
|
Лечение не проводится или неизвестно |
1 (<1%) |
2 (<1%) |
Таблица 3. Умеренные или тяжелые побочные эффекты во время лечения
|
Токсические эффекты |
Обычная ХТ |
Паклитаксел+платина |
|
Неврологические (степени 2-4) |
4 (1%) |
76 (20%) |
|
Неизвестно |
31 |
15 |
|
Гематологические* |
182 (46%) |
111 (29%) |
|
Неизвестно |
16 |
8 |
|
Инфекции* |
53 (14%) |
64 (17%) |
|
Неизвестно |
24 |
15 |
|
Почки* |
37 (9%) |
31 (8%) |
|
Неизвестно |
16 |
8 |
|
Мукозиты (степени 2/3) |
1 (6%) |
26 (7%) |
|
Неизвестно |
31 |
15 |
|
Тошнота и рвота (степени 2-4) |
153 (40%) |
131 (35%) |
|
Неизвестно |
29 |
15 |
|
Алопеция (степени 2-4) |
95 (25%) |
322 (86%) |
|
Неизвестно |
28 |
19 |
Литература
1 Parkin DM, Bray FI, Devesa SS. Cancer burden in the year 2000: the global picture.Eur J Cancer 2001; 37: S4–66.
2 The ICON collaborators. ICON2: randomised trial of single-agent carboplatin against three-drug combination of CAP (cyclophosphamide, doxorubicin, and cisplatin) in women with ovarian cancer. Lancet 1998; 352: 1571–76.
3 Advanced Ovarian Cancer Trialists’ Group. Chemotherapy in advanced ovarian cancer: four systematic meta-analyses of individual patient data from 37 randomized trials. Br J Cancer 1998; 78:1479–87.
4 Markman M, Reichman B, Hakes T, et al. Second-line platinum therapy in patients with ovarian cancer previously treated with cisplatin. J Clin Oncol 1991; 9: 389–93.
5 Trimble EL, Adams JD, Vena D, et al. Paclitaxel for platinum-refractory ovarian cancer: results from the first 1,000 patients registered to National Cancer Institute Treatment Referral Center 9103. J Clin Oncol 1993; 11: 2405–10·6
6 The International Collaborative Ovarian Neoplasm (ICON) Group. Paclitaxel plus carboplatin versus standard chemotherapy with either single-agent carboplatin or cyclophosphamide, doxorubicin, and cisplatin in women with ovarian cancer: the ICON3 randomised trial. Lancet 2002; 360: 505–15.
7 Rose PG, Fusco N, Fluellen L, et al. Second-line therapy with paclitaxel and carboplatin for recurrent disease following first-line therapy with paclitaxel and platinum in ovarian or peritoneal carcinoma. J Clin Oncol 1998; 16: 1494–97.
8 Dizon DS, Hensley ML, Poynor EA, et al. Retrospective analysis of carboplatin and paclitaxel as initial second-line therapy for recurrent epithelial ovarian carcinoma: application toward a dynamic disease state model of ovarian cancer. J Clin Oncol 2002; 20: 1238–47.
9 Calvert AH, Newell DR, Gumbrell LA, et al. Carboplatin dosage: prospective evaluation of a simple formula based on renal function. J Clin Oncol 1987; 7: 1748–56.
10 Parmar MKB, Machin D. Survival analysis: a practical approach. Chichester: John Wiley, 1995.
11 Fayers PMF, Aaronson NK, Bjordal K, Curran D, Groenvold M, on behalf of the EORTC Quality of Life Study Group. EORTC QLQ-C30 scoring manual, 3rd edn.
Brussels: European Organisation for the Research and Treatment of Cancer, 2001: 86.
12 Girling D, Parmar MKB, Stenning S, Stephens R, Stewart L. Clinical trials in cancer.
Oxford: Oxford University Press, 2003.
13 Cantu MG, Buda A, Parma G, et al. Randomized controlled trial of single-agent paclitaxel versus cyclophosphamide, doxorubicin, and cisplatin in patients with recurrent ovarian cancer who responded to first-line platinum-based regimens. J Clin Oncol 2002; 20: 1232–37.
14 McGuire WP, Hoskins W, Brady MF, et al. Cyclophosphamide and cisplatin compared with paclitaxel and cisplatin in patients with stage III and stage IV ovarian cancer. N Engl J Med 1996; 334: 1–6.
15 Piccart MJ, Bertelsen K, James K, et al. Randomized intergroup trial of cisplatinpaclitaxel versus cisplatin-cyclophosphamide in women with advanced epithelial ovarian cancer: three-year result. J Natl Cancer Inst 2000; 92: 699–708.
16 Muggia FM, Braly PS, Brady MF, et al. Phase III randomized study of cisplatin versus paclitaxel versus cisplatin and paclitaxel in patients with suboptimal stage III or IV ovarian cancer: a gynecologic oncology group study. J Clin Oncol 2000; 18: 106–15.
17 Sandercock J, Parmar MKB, Torri V, et al. First-line treatment for advanced ovarian cancer: paclitaxel, platinum and the evidence. Br J Cancer 2002; 87: 815–24.
18 Gonzalez Martin AA, Calro E, Bover I, et al. Randomised phase II study of carboplatin versus paclitaxel-carboplatin in platinum-sensitive recurrent advanced ovarian carcinoma with assessment of quality of life: a GEICO study (Spanish Group for Investigation on Ovarian Carcinoma). Proc ASCO 2003; 22: (abstr 1812).
19 van Warmerdam LJ, Huizing MT, Giaccone G, et al. Clinical pharmacology of carboplatin administered in combination with paclitaxel. Semin Oncol 1997; 24 (suppl 2): 97–104.
Рис. 1. Профиль испытания 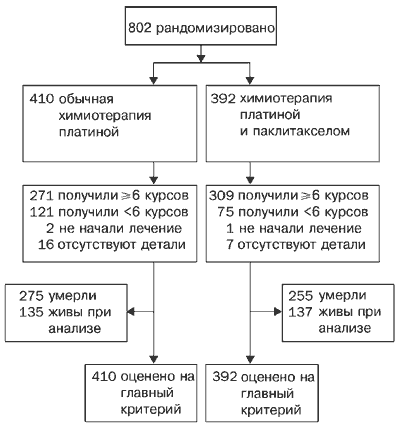
Рис. 2. Общая выживаемость 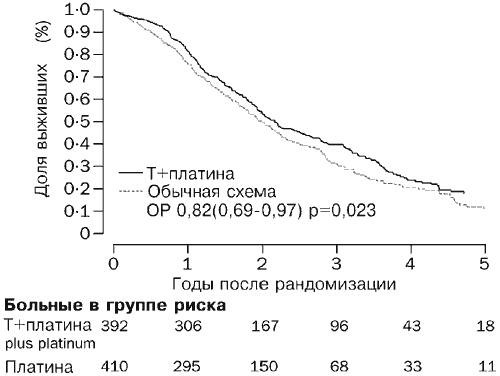
Рис. 3. Выживание без прогрессии 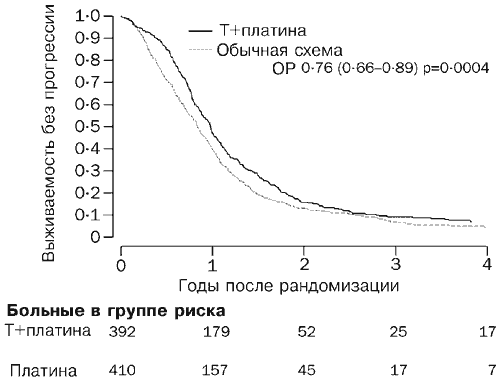
Рис. 4. Эффект XT комбинацией Т+платина на общую выживаемость в подгруппах 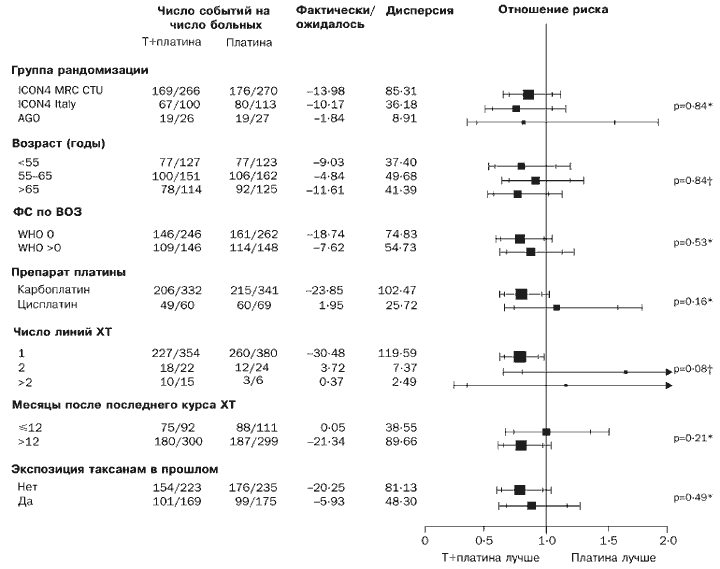
*Взаимодйствие  Тренд
Тренд
Сокращения: Т - паклитаксел; XT - химиотерапия; ФС - функциональный статус.
Комментарии
ПРАКТИКА ПЕДИАТРА
