Терапевтическая эффективность и безопасность использования фенотропила у больных с зависимостью от алкоголя
СтатьиОпубликовано в журнале:
«Вопросы наркологии», 2008, №4, с. 16-32
1 М-карбомоил-метил-4-фенил-2-пирромедон.
Иванец Н.Н., Винникова М.А., Мохначев С.О., Козырева А.В., Усманова Н.Н., Сивач Т.В.
Национальный научный центр наркологии Росздрава 119002, Москва, Мал. Могильцевский пер., 3
Проведено двойное слепое, плацебо контролируемое, рандомизированное, сравнительное клиническое исследование различных доз препарата Фенотропил® в комплексном лечении больных с зависимостью от алкоголя.
Цель исследования заключалась в изучении клинической эффективности и безопасности Фенотропила® при купировании алкогольного абстинентного синдрома (ААС), постабстинентного состояния, интеллектуально-мнестических нарушений в сравнении с плацебо.
В исследовании участвовало 120 пациентов, которые были разделены на четыре группы по 30 человек, принимавших по 100, 200, 300 мг Фенотропила® и плацебо.
Результаты исследования выявили дозозависимый эффект Фенотропила®, показали его положительное влияние на дисфорию, моторное возбуждение, идеаторные нарушения в структуре синдрома патологического влечения к алкоголю. Было отмечено его положительное терапевтическое действие на интеллектуально-мнестические нарушения у больных с зависимостью от алкоголя. Профиль безопасности препарата был оценен как высокий. Фенотропил® рекомендован для применения в комплексных программах лечения зависимости от алкоголя в стационарной и амбулаторной практике.
Хроническая алкогольная интоксикация приводит к метаболическим и дистрофическим поражениям мозга, многочисленным когнитивным нарушениям. Восстановление тканевого обмена и коррекция возникших интеллектуально-мнестических и неврологических нарушений являются важным аспектом комплексной терапии алкогольной зависимости и обеспечивают более стабильные результаты лечения [3]. Назначение ноотропов эффективно на всех этапах лечения алкогольной зависимости. Они способны уменьшать алкогольную интоксикацию, тяжесть клинических проявлений и продолжительность абстинентного алкогольного синдрома (ААС), редуцировать вялость, разбитость, апатию, тревогу. Выявлено их слабое или умеренное влияние на дисфорическую симптоматику [7, 8].
Одним из наиболее важных показаний для назначения ноотропных препаратов являются пределириозные состояния и алкогольные делирии [1, 6]. За счет редукции астенических состояний препараты ноотропного ряда обладают способностью уменьшать патологическое влечение к алкоголю. Доказана эффективность ноотропов в отношении астенического симптомокомплекса и когнитивных нарушений вследствие травматических, токсических, сосудистых и дегенеративных поражений центральной нервной системы (ЦНС) [1, 5].
Большой интерес для клинической наркологии представляет препарат фармацевтической компании ОАО «Валента» (которая раньше называлась ОАО «Отечественные лекарства») — Фенотропил®.
Фенотропил® относится к циклическим производным ГАМК и является фенильным производным пирацетамового ряда (М-карбамоил-метил-4-фенил-2-пирролидон), близким по химическому строению к эндогенным медиаторам. Так как Фенотропил® действует на большинство нейромедиаторных систем, он обладает и широким терапевтическим спектром действия [2]. Фенотропил® показан как здоровым лицам, так и людям с различными заболеваниями ЦНС: при нарушениях памяти различного генеза (старение, начальные стадии деменции, гипоксия, стресс, интоксикация, утомление, нарушения сна); в остром, подостром, раннем и позднем восстановительных периодах ишемических инсультов; при дисциркуляторной энцефалопатии и вегетососудистой дистонии; в остром периоде черепно-мозговой травмы и при ее последствиях; при астениях различного генеза, судорожных состояниях; головокружениях; неврозах и неврозоподобных состояниях; депрессии и алкогольной зависимости с целью уменьшения явлений астении, депрессии, интеллектуально-мнестических нарушений [4]. У здоровых людей Фенотропил® применяется для повышения умственной и физической активности, а также устойчивости организма к экстремальным воздействиям.
Фенотропил® быстро всасывается в желудочно-кишечном тракте и легко проходит через гематоэнцефалический барьер. Фенотропил® не метаболизируется в организме, выводится в неизмененном виде (40% с мочой и 60% с желчью и потом).
Целью исследования являлось изучение эффективности и безопасности применения различных доз Фенотропила® в комплексном лечении больных с алкогольной зависимостью.
Терапевтическая эффективность Фенотропила® изучалась в диапазоне доз 100–300 мг при ААС и в постабстинентном состоянии. Одной из наиболее важных задач являлось изучение возможности формирования лекарственной зависимости при длительном применении Фенотропила® у данного контингента больных. Особое внимание уделялось изучению профиля безопасности препарата.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследование проводилось в рамках III фазы клинических исследований: двойное слепое плацебо контролируемое, рандомизированное, сравнительное, в параллельных группах, на базе клиники ФГУ ННЦ наркологии Росздрава в отделениях клинических исследований наркоманий и клинической психофармакологии.
В исследование было включено 120 человек, проходивших курс лечения в клинике, с диагнозом по Международной классификации болезней 10-го пересмотра (МКБ-10) «психические расстройства и расстройства поведения, вызванные употреблением алкоголя» и ААС. Согласно критериям включения, в исследуемую группу набирались больные со второй (F10.2) и третьей (F10.3) стадиями заболевания.
Все больные были мужского пола, их возраст варьировал от 25 до 65 лет (средний возраст — 40,22 ± 9,2 лет). Средняя длительность заболевания у пациентов, участвующих в исследовании, составила 14,67 ± 7,8 лет. Во всех исследуемых группах преобладали больные со средним темпом прогредиентности заболевания. Псевдозапойная форма употребления алкоголя преобладала во всех группах. У пациентов всех групп выявлялся достаточно высокий уровень суточной толерантности к алкоголю. Большинство пациентов (50–60%) впервые обратились за стационарной помощью по поводу алкогольной зависимости.
Практически у всех больных в исследуемых группах имелись соматические заболевания, обусловленные длительной алкогольной интоксикацией. Согласно критериям включения, соматические заболевания были вне стадии обострения; в основном встречались токсическое поражение печени, сердца, поджелудочной железы.
Алкогольное изменение личности в виде заострения преморбидных черт характера или алкогольной деградации выявлялось у большинства (81%) больных всех групп. Социальные последствия алкогольной зависимости также выявлялись у большинства пациентов и характеризовались нарушением семейных отношений, снижением или утратой профессиональных навыков.
В исследование не включали пациентов с выраженной соматической и неврологической патологией неалкогольного генеза, в том числе с хроническими соматическими заболеваниями в стадии обострения, пределирием, установленной гиперчувствительностью к исследуемому препарату, коморбидной психической патологией, а также с зависимостью от других видов психоактивных веществ (ПАВ), кроме никотина. Из исследования исключали больных, одновременно или за 30 дней до включения в исследование принимавших ноотропные и метаболические препараты, а также препараты, влияющие на системный кровоток, или одновременно участвовавших в другом клиническом исследовании.
Основные методы исследования — клинико-психопатологический, экспериментально-психологический и статистический.
Клиническое исследование препарата Фенотропил® проводили с использованием специально разработанного Протокола, включающего сведения о социальном статусе больных, клиникодинамических характеристиках заболевания, результатах обследования физического и психического состояния, данных лабораторных анализов в динамике.
Терапевтическую эффективность Фенотропила® оценивали по следующим шкалам:
- шкала динамики психопатологической симптоматики в абстинентном синдроме, постабстинентном состоянии;
- шкала динамики соматовегетативных проявлений в абстинентном синдроме, постабстинентном состоянии;
- шкала динамики неврологических проявлений в абстинентном синдроме, постабстинентном состоянии;
- шкала общего клинического впечатления (CGI);
- шкала оценки побочных явлений (UKU).
Помимо этого проводили экспериментально-психологическое тестирование интеллектуально-мнестических функций: запоминание 10 слов (количество слов), таблицы Шульте (время), счет по Крепелину (количество ошибок).
Лабораторные исследования с определением аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ) и гамма-глутамилтранспептидазы (ГГТ) проводили в динамике всем больным.
Оценка состояния по шкалам производилась по 4-балльной системе, где 0 баллов — отсутствие симптома, 1 — слабовыраженный, 2 — средневыраженный и 3 — значительно выраженный симптом. При использовании шкалы общего клинического впечатления анализировали только разделы «терапевтическая эффективность» и «индекс эффективности». Экспериментально-психологическое тестирование интеллектуально-мнестических функций проводили два раза: на 10-й и 30-й дни терапии.
Полученные результаты обрабатывали при помощи программ SPSS 11.5, Microsoft Excel 2000 с использованием методов описательной статистики. В соответствии с поставленными задачами проводили внутри- и межгрупповое сравнение. Для анализа количественных признаков применяли t-критерий Стьюдента, U-критерий Манна–Уитни.
Для оценки корреляционных взаимосвязей использовали метод Спирмена. Считалось, что степень корреляционной связи до 0,3 — слабая, от 0,3 до 0,7 — средняя и от 0,7 до 1,0 — сильная.
Различия средних величин, а также корреляционные связи признавались достоверными при уровне статистической значимости р Схема исследования
Все включенные в двойное слепое исследование пациенты были разделены на четыре группы по 30 человек в каждой:
1-я группа получала по 300 мг Фенотропила® в сутки в течение 30 дней;
2-я группа — по 200 мг Фенотропила® в сутки в течение 30 дней;
3-я группа — по 100 мг Фенотропила® в сутки в течение 30 дней;
4-я группа — плацебо в течение 30 дней.
Пациенты основных групп, получавших препарат, и контрольной группы, получавшей плацебо, были сопоставимы по всем социально-демографическим показателям и возрасту.
Помимо Фенотропила®, пациенты получали базисную терапию ААС и постабстинентного состояния (инфузионная дезинтоксикационная терапия, транквилизаторы, витамины, гепатотропы, противосудорожные препараты, антидепрессанты). В течение 30 дней терапевтическую активность препарата Фенотропил® оценивали на 0-й, 3-й, 7-й, 10-й, 20-й и 30-й дни терапии (6 визитов).
Оценку эффективности исследуемого препарата проводили на основании динамики клинических данных, лабораторных показателей и результатов опросников и шкал.
Препарат считался эффективным на основании следующих критериев: не менее чем 50%-ная редукция симптомов по оригинальным шкалам оценки соматовегетативных и неврологических проявлений на 10-й день терапии по сравнению с 1-м днем лечения; показатели шкалы общего клинического впечатления не превышали 2 баллов на 7-й день наблюдения. Препарат считался безопасным, если редукция биохимических показателей за время лечения составляла не менее 20%.
Исследование проводили в соответствии со специально разработанным Протоколом, соответствующим правилам GCP (качественной клинической практики). Клиническое исследование было инициировано после одобрения Протокола локальным Этическим комитетом по проведению клинических исследований ННЦ наркологии. Перед началом исследования каждый пациент подписывал информированное согласие. Исследователь объяснял суть исследования, его продолжительность и цели, а также предупреждал о возможности побочных эффектов, связанных с приемом препарата.
Длительность исследования составила около 12 месяцев, длительность набора больных в исследование составила менее 6 месяцев.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Результаты оценивали у 113 пациентов, завершивших исследование согласно Протоколу. За весь период исследования выбыло 7 (5,8%) пациентов. Наиболее частыми, практически облигатными причинами выхода из исследования являлись актуализация патологического влечения к алкоголю (ПВА), отказ от лечения (в связи с актуализацией ПВА), срыв стационарного лечения на ранних сроках (табл. 1).
Таблица 1. Причины выхода из исследования пациентов
| Группа | Причина выхода из исследования, срок | Абс. |
| 3-я группа | Актуализация ПВА, 7-е сутки | 1 |
| 2-я группа | Срыв, 5-е сутки | 1 |
| Срыв, 17-е сутки | 1 | |
| Актуализация ПВА, 3-й сутки | 1 | |
| 1-я группа | — | — |
| 4-я группа | Актуализация ПВА, 5-е сутки | 1 |
| Отказ от лечения | 1 | |
| Перевод в психиатрическую больницу с диагнозом шизофрения | 1 | |
| Всего | 7 | |
Приведенные данные демонстрируют, что наиболее часто случаи актуализации ПВА и срывов наблюдались у пациентов 2-й и 4-й групп. Наиболее благоприятной в данном отношении была 1-я группа, в которой случаев досрочного выхода пациентов из исследования не было совсем.
Динамика психопатологических нарушений
При оценке динамики психопатологических нарушений у пациентов основных и контрольной групп было выявлено достоверное снижение степени их выраженности в результате проводимого комплексного лечения. Анализ динамики осознанного влечения к алкоголю показал, что снижение выраженности синдрома происходит во всех группах к концу 3-й недели стационарного лечения (5-й визит), полная редукция наблюдается к 30-му дню терапии (6-й визит). Редукция синдрома достигается быстрее у пациентов 1-й и 4-й групп, по сравнению с пациентами 2-й и 3-й групп (р Таблица 2. Динамика выраженности синдрома патологического влечения к алкоголю в процессе стационарного лечения, в баллах
| Название группы | Визит, день лечения | |||||
| 1-й, начало лечения |
2-й, 3-й день лечения | 3-й, 7-й день лечения | 4-й, 10-й день лечения |
5-й, 20-й день лечения |
6-й, 30-й день лечения |
|
| 1-я группа | 2,20 ± 0,92 | 1,50 ± 1,04 | 1,00 ± 0,61 | 0,53 ± 0,32 | 0,10 ± 0,05* | 0,00 ± 0,00 |
| 2-я группа | 2,22 ± 1,01 | 1,63 ± 1,01 | 0,93 ± 0,70 | 0,56 ± 0,25 | 0,20 ± 0,14 | 0,00 ± 0,00 |
| 3-я группа | 2,21 ± 0,74 | 1,54 ± 1,00 | 1,00 ± 0,90 | 0,64 ± 0,37 | 0,25 ± 0,19 | 0,00 ± 0,00 |
| 4-я группа | 2,29 ± 0,71 | 1,39 ± 0,83 | 0,91 ± 0,85 | 0,36 ± 0,22 | 0,11 ± 0,03* | 0,00 ± 0,00 |
Примечание: * — р
Уже к 3-му дню терапии (2-й визит) у всех пациентов отмечалось снижение степени выраженности таких симптомов, как напряженность, тревожность, подавленность, эмоциональная лабильность, расстройства сна. К 7-му дню (3-й визит) наблюдалась значительная редукция этих симптомов, степень их выраженности не превышала одного балла (слабая выраженность). Купирование вышеперечисленной симптоматики к концу лечения проходило одинаково успешно во всех группах (без статистически достоверных различий между группами). Астеническая симптоматика изначально была слабо выражена во всех группах, купировалась плавно; значительное улучшение в группах наблюдалось к концу 3-й недели терапии (табл. 3).
Таблица 3. Динамика выраженности астенической симптоматики в структуре ААС и постабстинентного состояния в процессе стационарного лечения, в баллах
| Симптомы | Визиты | 1-я группа | 2-я группа | 3-я группа | 4-я группа |
| Утомляемость | 1-й | 1,10 ± 1,06 | 1,41 ± 1,15 | 1,29 ± 1,08 | 1,43 ± 1,03 |
| 2-й | 0,87 ± 0,70 | 0,96 ± 1,09 | 1,00 ±0,94 | 1,04 ±0,88 | |
| 3-й | 0,43 ± 0,33 | 0,70 ± 0,33 | 0,61 ± 0,49 | 0,64 ± 0,53 | |
| 4-й | 0,23 ±0,15 | 0,41 ±0,14 | 0,21 ±0,15 | 0,32 ±0,17 | |
| 5-й | 0,10 ±0,05 | 0,15 ±0,16 | 0,11 ±0,09 | 0,25 ± 0,65 | |
| 6-й | 0,00 ± 0,00 | 0,00 ± 0,00 | 0,00 ± 0,00 | 0,00 ± 0,00 | |
| Неустойчивость внимания | 1-й | 1,57 ±0,94 | 1,44 ± 1,05 | 1,68 ± 0,94 | 1,50 ±0,92 |
| 2-й | 1,30 ±0,88 | 1,19 ± 1,11 | 1,14 ±0,93 | 1,18 ±0,94 | |
| 3-й | 0,90 ± 0,88 | 0 ± 0,00 | 0,75 ± 0,60 | 0,64 ± 0,53 | |
| 4-й | 0,57 ± 0,43 | 0,41 ± 0,29 | 0,29 ±0,13 | 0,39 ± 0,24 | |
| 5-й | 0,23 ± 0,25 | 0,19 ±0,18 | 0,14 ±0,09 | 0,25 ±0,17 | |
| 6-й | 0,13 ±0,10 | 0,15 ±0,09 | 0,04 ± 0,02 | 0,21 ± 0,09 | |
| Снижение настроения | 1-й | 2,13 ±0,73 | 1,93 ± 1,07 | 2,04 ± 0,84 | 1,96 ±0,74 |
| 2-й | 1,67 ±0,96 | 1,48 ±0,98 | 1,68 ± 0,86 | 1,68 ±0,55 | |
| 3-й | 1,23 ±0,94 | 1,19 ±0,92 | 1,11 ±0,79 | 1,07 ±0,54 | |
| 4-й | 0,70 ± 0,70 | 0,74 ± 0,56 | 0,57 ± 0,39 | 0,64 ± 0,42 | |
| 5-й | 0,30 ± 0,27 | 0,30 ± 0,24 | 0,11 ±0,08 | 0,21 ±0,12 | |
| 6-й | 0,10 ±0,11 | 0,15 ±0,16 | 0,11 ±0,08 | 0,00 ± 0,00 | |
| Гиперестезия | 1-й | 0,87 ± 0,70 | 1,07 ± 1,01 | 0,82 ± 0,50 | 0,75 ± 0,74 |
| 2-й | 0,70 ± 0,50 | 0,89 ± 0,67 | 0,46 ± 0,34 | 0,46 ± 0,69 | |
| 3-й | 0,40 ±0,31 | 0,59 ± 0,44* | 0,25 ± 0,22 | 0,18 ±0,16* | |
| 4-й | 0,23 ±0,14 | 0,30 ±0,21 | 0,14 ±0,06 | 0,18 ±0,09 | |
| 5-й | 0,10 ±0,10 | 0,22 ±0,19 | 0,04 ± 0,01 | 0,07 ± 0,06 | |
| 6-й | 0,00 ± 0,00 | 0,19 ±0,18 | 0,04 ± 0,01 | 0,04 ± 0,03 |
Примечание: * — р
У пациентов 2-й группы к концу 1-й недели лечения (3-й визит) достоверно чаще регистрировались гиперестезии в сравнении с пациентами 4-й группы (р Наиболее интересные данные получены при рассмотрении динамики дисфории и моторного возбуждения (табл. 4, 5).
Таблица 4. Динамика дисфории в процессе стационарного лечении, в баллах
| Название группы | Визит, день лечения | |||||
| 1-й, начало лечения |
2-й, 3-й день лечения | 3-й, 7-й день лечения | 4-й, 10-й день лечения |
5-й, 20-й день лечения |
6-й, 30-й день лечения |
|
| 1-я группа | 1,20 ± 1,19 | 0,90 ± 0,85* | 0,63 ± 0,38* | 0,23 ± 0,18 | 0,13 ± 0,05 | 0,00 ± 0,00 |
| 2-я группа | 1,17 ± 1,04 | 1,15 ± 1,03* | 0,74 ± 0,49* | 0,37 ± 0,23 | 0,26 ± 0,16 | 0,07 ± 0,02 |
| 3-я группа | 0,82 ± 1,02 | 0,71 ± 0,98 | 0,57 ± 0,32 | 0,25 ± 0,52 | 0,07 ± 0,06 | 0,04 ± 0,03 |
| 4-я группа | 0,57 ± 0,48 | 0,43 ± 0,69 | 0,18 ± 0,08 | 0,14 ± 0,08 | 0,04 ± 0,02 | 0,00 ± 0,00 |
Примечание: * — р
Таблица 5. Динамика моторного возбуждения в процессе стационарного лечения, в баллах
| Название группы | Визит, день лечения | |||||
| 1-й, начало лечения |
2-й, 3-й день лечения | 3-й, 7-й день лечения | 4-й, 10-й день лечения |
5-й, 20-й день лечения |
6-й, 30-й день лечения |
|
| 1-я группа | 1,03 ± 0,57* | 0,67 ± 0,45* | 0,47 ± 0,30* | 0,20 ± 0,13 | 0,07 ± 0,25 | 0,00 ± 0,00 |
| 2-я группа | 0,93 ± 0,37 | 0,74 ± 0,34* | 0,30 ± 0,61 | 0,19 ± 0,10 | 0,11 ± 0,32 | 0,00 ± 0,00 |
| 3-я группа | 0,93 ± 0,36 | 0,39 ± 0,14* | 0,25 ± 0,52 | 0,14 ± 0,05 | 0,04 ± 0,19 | 0,00 ± 0,00 |
| 4-я группа | 0,61 ± 0,79 | 0,25 ± 0,12 | 0,17 ± 0,06 | 0,10 ± 0,03 | 0,00 ± 0,00 | 0,00 ± 0,00 |
Примечание: * — р
У пациентов 1-й и 2-й групп исходно и на 3-й и 7-й дни лечения (2-й и 3-й визиты) дисфория регистрировалась достоверно чаще, чем у пациентов 4-й группы (р Между дозой Фенотропила® и редукцией дисфорической симптоматики существует достоверная (р = 0,039) обратная корреляционная связь средней силы: при повышении дозы Фенотропила® дисфория купируется быстрее.
Сходные данные были получены при анализе динамики моторного возбуждения (табл. 5). Пациенты рассматриваемых групп достоверно различались по частоте выявления моторного возбуждения. Так, моторное возбуждение у пациентов 1-й группы исходно регистрировалось достоверно чаще, чем у пациентов 4-й группы. К 3-му дню терапии (2-й визит) данный клинический симптом достоверно чаще регистрировался во всех группах по сравнению с группой контроля (везде — р Между дозой Фенотропила® и редукцией моторного возбуждения также выявлена достоверная (р = 0,0003) обратная корреляционная связь средней силы: при повышении дозы Фенотропила® моторное возбуждение купируется быстрее.
Динамика соматовегетативных расстройств
Наблюдавшиеся в структуре ААС соматовегетативные расстройства значительно уменьшались уже к 3-му дню лечения у всех пациентов, принимавших Фенотропил®: стабилизировались показатели гемодинамики, значительно менее выраженными были жажда, сухость во рту, потливость, гиперемия лица и склер. Практически не регистрировались такие симптомы, как нарушения ритма сердца, боли в сердце, тахикардия. При продолжении лечения состояние стабилизировалось, к 30-му дню лечения все указанные симптомы купировались полностью. Во всех трех группах получены практически идентичные результаты, статистически значимых различий между ними выявлено не было. Некоторые различия выявлялись в динамике таких симптомов, как повышение АД и белый дермографизм (табл. 6).
Таблица 6. Динамика выраженности вегетативных расстройств в процессе стационарного лечения, в баллах
| Симптомы | Визиты | 1-я группа | 2-я группа | 3-я группа | 4-я группа |
| Повышение артериального давления | 1-й | 1,33 ± 1,09 | 1,37 ± 1,04 | 1,39 ± 1,13 | 1,37 ± 1,11 |
| 2-й | 0,73 ± 1,05 | 0,81 ±0,83 | 0,54 ± 0,79 | 0,93 ± 0,98 | |
| 3-й | 0,50 ± 0,90 | 0,33 ± 0,62 | 0,14 ±0,45* | 0,57 ± 0,79 | |
| 4-й | 0,23 ± 0,50 | 0,11 ±0,32 | 0,14 ±0,45 | 0,33 ± 0,55 | |
| 5-й | 0,13 ±0,35 | 0,11 ±0,32 | 0,07 ± 0,26 | 0,26 ± 0,53 | |
| 6-й | 0,07 ± 0,25 | 0,04 ±0,19 | 0,07 ± 0,27 | 0,19 ± 0,40 | |
| Белый дермографизм | 1-й | 0,44 ± 0,89 | 0,42 ± 0,86 | 0,56 ± 1,01 | 0,37 ± 0,84 |
| 2-й | 0,26 ±0,71 | 0,31 ±0,62 | 0,25 ± 0,59 | 0,26 ± 0,66 | |
| 3-й | 0,07 ± 0,38* | 0,19 ±0,49 | 0,11 ±0,31 | 0,15 ± 0,46 | |
| 4-й | 0,07 ± 0,38 | 0,00 ± 0,00 | 0,00 ± 0,00 | 0,08 ± 0,27 | |
| 5-й | 0,00 ± 0,00 | 0,00 ± 0,00 | 0,00 ± 0,00 | 0,00 ± 0,00 |
К 7-му дню терапии (3-й визит) повышение артериального давления (АД) отмечалось достоверно реже у пациентов 3-й группы по сравнению с этими же показателями у пациентов 4-й группы (р Динамика неврологических нарушений
Наиболее ярко терапевтический эффект Фенотропила® проявился в его действии на неврологическую симптоматику. К 3-му дню комплексного лечения практически полностью купировались такие нарушения, как головная боль, головокружение, атаксия, тремор. Редукция вышеперечисленных расстройств была одинаково успешной во всех группах.
Дозозависимый эффект препарата проявлялся в отношении таких неврологических нарушений, как нистагм и нарушение координационных проб.
Исходно у пациентов 1-й и 3-й групп нистагм фиксировали чаще, чем у пациентов 4-й группы, но достоверного различия между группами не наблюдалось (табл. 7). К 30-му дню терапии (6-й визит) в этих группах была отмечена выраженная регрессия частоты встречаемости данного признака, скорость разрешения данного симптома была выше, чем при приеме плацебо.
Таблица 7. Динамика выраженности нистагма в процессе стационарного лечения, в баллах
| Название группы | Визит, день лечения | |||||
| 1-й, начало лечения |
2-й, 3-й день лечения | 3-й, 7-й день лечения | 4-й, 10-й день лечения |
5-й, 20-й день лечения |
6-й, 30-й день лечения |
|
| 1-я группа | 2,07 ± 0,74 | 1,37 ±0,89 | 0,68 ± 0,57 | 0,62 ± 0,40 | 0,38 ±0,17 | 0,07 ±0,0 3 |
| 2-я группа | 1,52 ±0,98 | 1,04 ±0,90 | 0,69 ± 0,41 | 0,51 ± 0,22 | 0,32 ±0,11 | 0,19 ±0,04 |
| 3-я группа | 2,36 ±3,73 | 1,07 ±0,81 | 0,53 ± 0,29 | 0,31 ±0,11 | 0,26 ± 0,07 | 0,00 ± 0,00 |
| 4-я группа | 1,43 ±0,74 | 0,89 ± 0,74 | 0,67 ± 0,32 | 0,59 ± 0,25 | 0,31 ±0,11 | 0,19 ±0,04 |
При этом выявлена достоверная обратная корреляционная связь между дозой Фенотропила® и выраженностью нистагма.
Исходно частота нарушения координации была примерно одинаковой во всех группах, при у пациентов 1-й и 2-й групп практически полностью этот симптом редуцировался к 7-му дню терапии (3-й визит), тогда как у пациентов 3-й и 4-й групп этот симптом исчезал не у всех пациентов даже к 20-му дню терапии (5-й визит) (табл. 8).
Таблица 8. Динамика выраженности нарушений координационных проб в процессе стационарного лечения, в баллах
| Название группы | Визит, день лечения | |||||
| 1-й, начало лечения |
2-й, 3-й день лечения | 3-й, 7-й день лечения | 4-й, 10-й день лечения |
5-й, 20-й день лечения |
6-й, 30-й день лечения |
|
| 1-я группа | 1,83 ± 0,79 | 1,03 ± 0,93 | 0,30 ± 0,25 | 0,17 ± 0,16 | 0,00 ± 0,00 | 0,00 ± 0,00 |
| 2-я группа | 1,85 ± 0,82 | 0,89 ± 0,80 | 0,41 ± 0,37 | 0,15 ± 0,08 | 0,00 ± 0,00 | 0,00 ± 0,00 |
| 3-я группа | 1,79 ± 0,74 | 0,71 ± 0,71 | 0,29 ± 0,23 | 0,04 ± 0,09 | 0,04 ± 0,19 | 0,04 ± 0,09 |
| 4-я группа | 1,75 ± 0,75 | 0,86 ± 0,65 | 0,21 ± 0,12 | 0,04 ± 0,02 | 0,04 ± 0,02 | 0,04 ± 0,02 |
При этом выявлена достоверная (р = 0,02) обратная корреляционная связь средней силы между дозой Фенотропила® и редукцией нарушений координационных проб.
Таким образом, динамика психопатологической, соматовегетативной и неврологической симптоматики ААС и постабстинентного состояния была сходной во всех группах: у пациентов всех групп наблюдалось значительное улучшение состояния уже к 3-му дню лечения.
Данный факт объясняется тем, что на всех больных на протяжении стационарного курса оказывалось комплексное терапевтическое воздействие: в первые дни всем больным проводилась инфузионная терапия с применением гепатотропов, витаминов, антиоксидантов, в дальнейшем Фенотропил® действовал в комплексе с другими психотропными препаратами (чаще антидепрессантами, транквилизаторами). Пациенты продолжали принимать витамины, гепатопротекторы, что и обусловило сходный терапевтический эффект во всех исследуемых группах.
Однако субъективные оценки (самоотчеты) пациентов, получавших Фенотропил®, свидетельствовали о том, что у них общее улучшение физического самочувствия было более выраженным: ощущения вялости, заторможенности проходили быстрее, раньше появлялись бодрость, желание заниматься повседневными делами, интерес к окружающему, повышалась работоспособность, появлялась «ясность мыслей», внимание становилось более устойчивым. Подобный эффект делает применение Фенотропила®, несомненно, полезным и эффективным как в абстинентном, так и в постабстинентном состояниях.
Экспериментально-психологическое тестирование
При изначально одинаковом выполнении пациентами теста «запоминание 10 слов» через 4 недели терапии наблюдалось улучшение выполнения задания во всех группах с небольшой тенденцией опережения результата в группах пациентов, получающих Фенотропил®, по сравнению с плацебо.
Время работы с таблицами Шульте в большинстве случаев не выходило за рамки нормативного во всех группах уже при первом обследовании (10-й день терапии, 4-й визит) (рис. 1).
Рис. 1. Среднее время работы с таблицами Шульте в группах, с
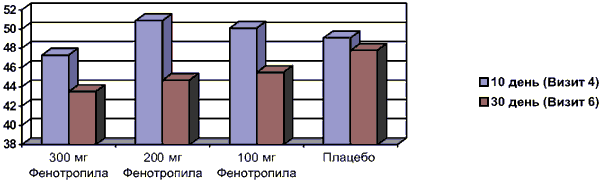
При этом в группах пациентов, принимавших Фенотропил®, к 30-му дню терапии показатели улучшались в среднем на 5 с. У пациентов 4-й группы такого улучшения не происходило. На рис. 1 представлено среднее время работы с пятью таблицами Шульте на 10-й и 30-й дни лечения.
При анализе результатов выполнения методики «Счет по Крепелину», было установлено, что достоверное уменьшение количества ошибок к концу лечения (30-й день терапии, 6-й визит) наблюдалось только у пациентов 1-й группы (300 мг Фенотропила®) (р Рис. 2. Среднее количество ошибок при выполнении методики «Счет по Крепелину» (за 3 мин).
Примечание: * — р 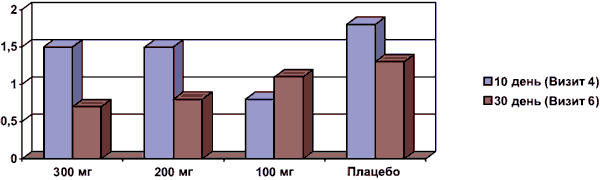
Уже на 10-й день терапии у большинства пациентов всех групп ошибки не обнаруживались (или были единичными), однако у некоторых пациентов их было достаточно много. К 30-му дню лечения в группах пациентов, принимавших Фенотропил®, значимо снижалось количество ошибок при выполнении методики (практически в 2 раза). У пациентов, получавших плацебо, не наблюдалось такого улучшения работоспособности (рис. 2).
Таким образом, результаты экспериментально-психологического исследования продемонстрировали положительное влияние Фенотропила® на мнестические функции (оперативное запоминание, отсроченное воспроизведение) и свойства внимания (концентрация, устойчивость, распределение, объем) к 30-му дню лечения (6-й визит). При этом у больных с алкогольной зависимостью собственно ноотропный (улучшающий когнитивные функции) эффект Фенотропила® проявляется не сразу, становясь клинически заметным не ранее, чем через 4 недели терапии.
Шкала общего клинического впечатления (CGI)
Терапевтическое действие Фенотропила® оценивалось на 7-й день (3-й визит) и 30-й день (6-й визит). Клинико-статистический анализ показал, что по признаку «большое улучшение»1 наиболее выраженная динамика наблюдалась в 1-й группе (300 мг Фенотропила®): он встречался у 13,3% пациентов на 7-й день терапии и у 40% пациентов на 30-й день терапии, т.е. число пациентов с показателем «большое улучшение» увеличилось в процессе лечения в 3 раза.
1 В связи с малой частотой встречаемости признака «очень большое улучшение» (всего 5 клинических случаев), он рассматривался в группе «большое улучшение» посредством суммирования результата.
Менее выраженная положительная динамика наблюдалась в 3-й и 4-й группах: 21,4 и 57,1% пациентов в 3-й группе и 17,85 и 50% пациентов в 4-й группе имели признак «большое улучшение» на 7-й и 30-й день терапии, соответственно.
Обращает на себя внимание отсутствие подобной динамики у пациентов 2-й группы: 44,44 и 40,74% пациентов имели признак «большое улучшение» на 7-й и 30-й день терапии, соответственно. Эти данные требуют клинической интерпретации.
К окончанию курса лечения (30 дней терапии) улучшение состояния наблюдалось практически у половины пациентов всех групп (от 40 до 60%), однако внутригрупповая динамика была различной. В 1-й группе пациентов к 30-му дню состояние улучшилось практически в 4 раза по сравнению с первой неделей приема препарата.
По признаку «небольшое улучшение» наблюдалась следующая динамика: после первой недели лечения (7-й день, 3-й визит) во всех группах преобладали пациенты с небольшим улучшением, но при продолжении лечения и улучшении состояния их количество уменьшалось и они переходили в группу «большое улучшение». Таким образом, в данном случае наблюдается обратная тенденция по сравнению с результатами признака «большое улучшение».
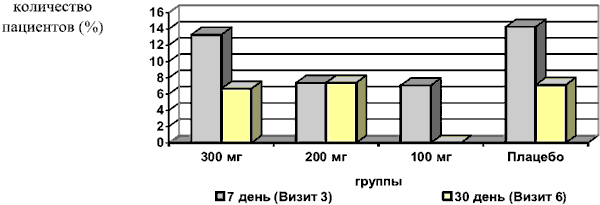
Особый клинический интерес вызывают те пациенты, у которых на фоне лечения не обнаруживалось изменений состояния: наибольшее количество пациентов с отсутствием изменений наблюдалось в 4-й группе, наименьшее количество — наблюдалось среди пациентов 3-й группы (рис. 3).
Рис. 3. Распределение пациентов с отсутствием динамики по шкале CGI
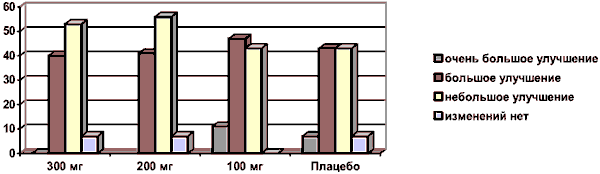
В целом, анализ шкалы CGI подтвердил эффективность Фенотропила® (рис. 4). В процессе исследования была показана зависимость терапевтического эффекта от выбранной дозы: чем выше доза препарата, тем быстрее достигался терапевтический эффект. В то же время стабильный терапевтический эффект наблюдался при любой дозе препарата после 4-х недель его применения, что является практически облигатной характеристикой любого ноотропного препарата.
Рис. 4. Распределение пациентов по виду терапевтического эффекта по шкале CGI (число человек в каждой группе к концу лечения)
Нежелательные явления, серьезные нежелательные явления
Нежелательные явления были зарегистрированы лишь у 2 (2,2%) пациентов, получавших Фенотропил® в дозах 200 и 100 мг (в начале и в середине курса терапии). Серьезных нежелательных явлений не наблюдалось.
Особое внимание в процессе исследования уделялось изучению возможности развития привыкания и синдрома зависимости от препарата. Оценка проводилась путем опроса пациентов с применением диагностических критериев синдрома зависимости по МКБ-10. Ни одного случая развития привыкания и синдрома зависимости не зарегистрировано.
Безопасность Фенотропила® оценивалась по динамике лабораторных показателей в процессе терапии. Как отмечалось ранее, в начале лечения у большинства пациентов имела место гиперферментемия. К концу стационарного курса лечения происходило значительное снижение показателей АСТ, АЛТ и ГГТ (табл. 9). Результаты пациентов всех групп сравнимы с результатами пациентов 4-й группы, достоверных различий между группами не было. Полученные данные свидетельствуют о безопасности Фенотропила®
Таблица 9. Сравнение динамики лабораторных показателей в процессе стационарного лечения
| Ферменты | Дни лечения | 1-я группа | 2-я группа | 3-я группа | 4-я группа |
| АЛТ, ед/л | 0 | 78,67 ± 54,54 | 61,09 ± 46,82 | 73,67 ± 78,06 | 81,32 ± 70,91 |
| 30 | 56,73 ± 31,70 | 43,73 ± 24,93 | 46,80 ± 31,04 | 58,11 ± 28,69 | |
| ACT, ед/л | 0 | 105,87 ± 81,71 | 84,42 ± 63,01 | 110,75 ± 148,79 | 117,71 ± 90,51 |
| 30 | 57,96 ± 24,31 | 49,38 ± 16,56 | 56,92 ± 46,65 | 64,11 ± 35,77 | |
| ГГТ, ед/л | 0 | 418,50 ± 1390,9 | 128,42 ± 112,57 | 132,96 ± 225,78 | 269,07 ± 181,24 |
| 30 | 135,84 ± 202,71 | 88,24 ± 80,75 | 92,84 ± 157,73 | 126,82 ± 120,97 |
ЗАКЛЮЧЕНИЕ
Результаты двойного слепого рандомизированного плацебо контролируемого исследования показали, что проводимое комплексное лечение оказывает положительное действие на психопатологическую, соматовегетативную и неврологическую симптоматику в рамках ААС и постабстинентного состояния — у всех пациентов происходит значительное улучшение состояния к 3– 7-му дню терапии. Использование Фенотропила® в лечебных программах позволяет добиться более выраженного и быстрого улучшения и значительно оптимизировать терапевтические подходы.
Фенотропил® оказывает влияние на осознанное влечение к алкоголю. Редукция данного компонента синдрома быстрее достигается при использовании Фенотропила® в дозе 300 мг (достоверные различия как с группой плацебо, так и с группами пациентов, получавших 100 и 200 мг Фенотропила®). Выявлено более выраженное влияние Фенотропила® в дозе 300 мг на дисфорию и моторное возбуждение (достоверные различия как с группой плацебо, так и с группами пациентов, получавших 100 и 200 мг Фенотропила®). Следует отметить, что в 1-й группе пациентов не наблюдалось случаев обострения синдрома ПВА, срывов в процессе стационарного лечения. В то же время влияние Фенотропила® на другие психопатологические расстройства (депрессивного спектра, астеническую симптоматику) было сравнимо с группой плацебо, что можно объяснить тем, что пациенты группы плацебо получали стандартную терапию: транквилизаторы, антидепрессанты, витамины, гепатотропы.
Полученные результаты позволяют сделать вывод о специфичности и узкой направленности терапевтического действия Фенотропила® в отношении психопатологической симптоматики у больных с зависимостью от алкоголя. Кроме того, следует подчеркнуть зависимость терапевтического эффекта Фенотропила® от его дозы.
Необходимо отметить, что субъективные оценки (самоотчеты) пациентов, получавших Фенотропил®, свидетельствовали о том, что в этих группах общее улучшение физического самочувствия было более выраженным. Подобный эффект делает применение Фенотропила®, несомненно, полезным и эффективным как в абстинентном, так и в постабстинентном состояниях.
Фенотропил® оказывает положительное влияние на определенные вегетативные и неврологические нарушения в рамках ААС: при использовании Фенотропила® в дозе 300 мг у пациентов быстрее купировались колебания АД, нистагм, нарушения координационных проб.
Результаты экспериментально-психологического исследования показали положительное влияние Фенотропила® на мнестические функции (оперативное запоминание, отсроченное воспроизведение) и свойства внимания (концентрация, устойчивость, распределение, объем). Собственно ноотропный (улучшающий когнитивные функции) эффект Фенотропила® у больных с зависимостью от алкоголя проявлялся не сразу, становился клинически заметным не ранее, чем через 4 недели терапии.
Анализ шкалы общего клинического впечатления подтвердил эффективность Фенотропила® и его высокую безопасность. В процессе исследования показана зависимость терапевтического эффекта от выбранной дозы: чем выше доза препарата, тем быстрее достигается терапевтический эффект. В то же время, стабильный, хороший терапевтический эффект наблюдается при использовании любой дозы препарата после 4-х недель его применения.
Серьезных нежелательных явлений и осложнений на фоне лечения Фенотропилом® зарегистрировано не было. В группах пациентов, принимавших Фенотропил®, уровень печеночных ферментов снижался не менее чем на 20%. В проведенном исследовании не было ни одного клинического случая привыкания к препарату и развития синдрома зависимости, что также является важным показателем безопасности препарата.
Таким образом, Фенотропил® является высокоэффективным препаратом с оптимальным профилем безопасности, что позволяет рекомендовать его для использования в комплексных терапевтических программах в стационарных и амбулаторных условиях при лечении больных с зависимостью от алкоголя.
ЛИТЕРАТУРА
1. Ахапкина В.И. Адаптогенное действие ноотропных препаратов / В.И. Ахапкина //Российский медицинский журнал. 2005. № 3. С. 40–43.
2. Ахапкина В.И. Спектр фармакологических эффектов Фенотропила / В.И. Ахапкина, Т.А. Воронина //Фарматека. 2005. № 13. С. 12–13.
3. Воронина Т.А. Ноотропные препараты, достижения и новые проблемы / Т.А. Воронина, С.Б. Середенин //Экспериментальная и клиническая фармакология. 1998. Т. 61. № 4. С. 3–9.
4. Иванец Н.Н. Применение Фенотропила у больных хроническим алкоголизмом / Н.Н. Иванец, В.И. Ахапкина // Тезисы докладов XI Российского национального конгресса «Человек и лекарство». — М., 2004. С. 169.
5. Ковалев Г.В. Ноотропные средства / Г.В. Ковалев. — Волгоград, 1990. — 368 с.
6. Майский А.И. Сравнительное психофармакологическое изучение препаратов, используемых для дифференцированной фармакотерапии алкоголизма / А.И. Майский //Тезисы материалов симпозиума «Нейро-психотропные препараты». — М., 1994. С. 65.
7. Malik R. Towards better brain management: nootropics / R. Malik, A. Sangwan, R. Saihgal et al. //Curr. Med. Chem. 2007. Vol. 14. № 2. P. 123–131.
8. Ng H.J. Nootropic alpha-7 nicotinic receptor allosteric modulator derived from GABA receptor modulators / H.J. Ng, E.R. Whittemore, M.B. Tran et al. //Proc. Nat. Acad. Sci. USA. 2007. Vol. 104. № 19. P. 8059–8064.
