Почему комбинация периндоприл аргинин индапамид является оптимальным средством нефропротекции при сахарном диабете типа 2?
СтатьиОпубликовано в журнале:
CONSILIUM MEDICUM, том 13, № 12
С.В.Недогода
Волгоградский государственный медицинский университет, кафедра терапии и эндокринологии ФУВ
Тесная связь между контролем артериальной гипертензии (АГ), поражением органов-мишеней и состоянием функции почек хорошо известна, равно как и зависимость между сахарным диабетом (СД), почками и риском развития сердечно-сосудистых осложнений (ССО). Фактически наличие АГ и СД обусловливает до 2/3 всех новых случаев терминальной почечной недостаточности.
Известно, что раннее выявление поражения почек при СД типа 2 и проведение целенаправленной современной фармакологической нефропротекции как минимум отдаляет момент развития необратимых изменений почечной ткани и последующей почечной недостаточности, но в последнее время стали обращать внимание на способность такой терапии улучшать прогноз за счет снижения ССО и смертности.
Важно, что препараты, используемые для нефропротекции при СД, должны быть эффективны не только на начальном этапе кардиоренального континуума, когда имеются функциональные изменения без серьезного органического поражения, но и при наличии уже выраженных органических изменений. В этом случае «идеальная» нефропротекция должна не только замедлить и приостановить патологический процесс в почках, но и хотя бы у части пациентов способствовать его обратному развитию.
Всемирная организация здравоохранения рассматривает микроальбуминурию (МАУ) как один из компонентов метаболического синдрома (1999 г.). Она является доказанным маркером развития системной эндотелиальной дисфункции и на фоне МАУ, как правило, имеется более выраженное поражение органов-мишеней (рис. 1), кроме того, МАУ часто сопутствует другим факторам риска ССО (ожирение по центральному типу, инсулинорезистентность, повышение С-реактивного протеина, гиперурикемия, курение, дислипидемия, пожилой возраст).
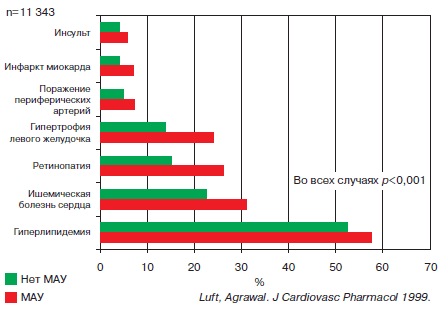
Рис. 1. Частота выявления сопутствующей патологии при АГ в зависимости от наличия МАУ.
Считается, что приблизительно у 30–40% всех больных АГ имеет место МАУ. Причем это минимальное значение частоты ее встречаемости, так как в крупном международном исследовании i-SEARCH с участием около 22 тыс. пациентов МАУ встречалась у 53–71% больных, особенно часто – при неконтролируемой и резистентной АГ [1].
По данным различных исследований, МАУ встречается у 10–40% больных СД типа 1 и у 15–40% – СД типа 2. Результаты эпидемиологических исследований [1, 2] показали, что частота МАУ при СД составляет около 33%, незначительно возрастая на фоне сопутствующей АГ (до 35%) и при наличии макро- и/или микрососудистых осложнений (до 38–39%). По данным исследования UKPDS, при СД риск возникновения МАУ прогрессивно возрастает с увеличением длительности заболевания приблизительно на 1–2% в год. При сочетании различных факторов риска, особенно на фоне АГ и/или СД, вероятность нарушения функции почек еще больше возрастает.
В последнее время дискутируется прогностическое значение МАУ. Не вдаваясь в полемику по данному вопросу, необходимо только констатировать, что результаты многочисленных клинических и эпидемиологических исследований доказывают, что МАУ является одним из важнейших независимых факторов риска сердечно-сосудистых и цереброваскулярных событий, а также смерти от них [3, 4]. Достаточно привести результаты крупных субисследований:
- LIFE – повышенный уровень соотношения альбумин/креатинин прямо коррелировал с повышением частоты развития серьезных сердечно-сосудистых событий (кардиоваскулярной смерти, нефатальных инсульта, инфаркта миокарда) и выраженностью гипертрофии левого желудочка.
- HOPE – у пациентов с АГ из группы высокого риска повышение соотношения альбумин/креатинин в моче на каждые 0,4 мг/ммоль выше нормы увеличивает риск серьезных сердечно-сосудистых событий на 5,9%.
- DIABHYCAR (the type 2 DIABetes, HYpertension, microalbuminuria or proteinuria, CArdiovascular events and Ramipril study) – при наличии МАУ повышен риск развития сердечной недостаточности.
- EPIC-Norfolk (European Prospective Investigation into Cancer in Norfolk study) – при МАУ достоверно повышен риск инсульта.
- Copenhagen City Heart-3 – риск ишемической болезни сердца и сердечно-сосудистой смерти достоверно повышался уже при уровне альбуминурии выше 4,8 мкг/мин (общепринятый нижний порог для диагностирования МАУ – 20 мкг/мин).
Для борьбы с МАУ и эффективной нефропротекции прежде всего необходимо обеспечить достижение целевых цифр АД (рис. 2).
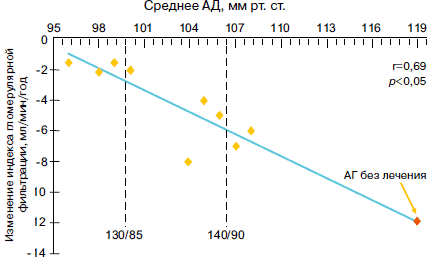
Рис. 2. Метаанализ: зависимость между средним АД и ухудшением функции почек у больных диабетической и недиабетической нефропатией.
Parving HH et al. Br Med J 1989. Moschio G et al. N Engl J Med 1996. Viberti GC et al. JAMA 1993. Bakris GL et al. Kidney Int 1996. Klhr S et al. N Engl J Med 1994. Bakris GL. Hypertension 1997. Hebert L et al. Kidney Int 1994. The GISEN Group. Lancet 1997. Lebovitz H et al. Kidney Int 1994.
Bakris GL et al. Am J Kidney Dis 2000; 36 (3): 646–61.
Reprinted by permission, Harcourt Inc.
Интересно, что при этом на фоне уменьшения МАУ может иметь место дополнительное снижение систолического АД [5]. Но при этом необходимо особо отметить, что для нефропротекции ключевое значение имеют антигипертензивные препараты, подавляющие активность ренин-ангиотензин-альдостероновой системы (ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина II). Доказано, что их нефропротективный эффект обусловлен не только снижением АД, но и другими, в том числе плейотропными эффектами этих препаратов [6–8].
В последнее время стало очевидно, что для эффективной нефропротекции, особенно у пациентов с СД типа 2 требуется использование комбинации антигипертензивных препаратов.
Во-первых, именно комбинированная антигипертензивная терапия позволяет достичь целевого АД у подавляющего числа пациентов. Во-вторых, именно комбинация антигипертензивных препаратов может обеспечить наиболее выраженное защитное действие в отношении почек и сердца. Однако доказательная база по применению комбинаций имеется в отношении единичных комбинаций [фиксированные комбинации: периндоприл + индапамид (исследования ADVANCE и PREMIER), трандалоприл + верапамил SR (исследование BENEDICT) и произвольная комбинация кандесартан лизиноприл (исследование CALM)]. При этом необходимо подчеркнуть, что комбинация периндоприл + индапамид является единственной эффективной на всех этапах ренального континуума (табл. 1). Это объясняется способностью ее компонентов практически полностью устранять дисбаланс между повышением афферентного и эфферентного давления в почке при АГ и СД.
Таблица 1. Ренальные эффекты Нолипрела (ADVANCE)
| Прогрессирование повреждения почек | Уменьшение риска на фоне лечения Нолипрелом А форте |
| Все почечные осложнения | -21% (p<0,0001) |
| Прогрессирование альбуминурии на 1 и более стадию | -22% (p<0,0001) |
| Новые случаи МАУ | -21% (p<0,0001) |
| Новые случаи макроальбуминурии | -31% (p<0,003) |
| Обратное развитие нефропатии | Улучшение прогноза на фоне лечения Нолипрелом А форте |
| Уменьшение альбуминурии на 1 и более стадию | +16% (p<0,002) |
| Восстановление почечной функции | +15% (p<0,007) |
Сегодня благодаря исследованию ADVANCE применение фиксированной комбинации периндоприла с индапамидом у больных СД типа 2 оказалось единственным вариантом лечения, который не только оказывает нефропротективное действие, но и снижает смертность при этой патологии (табл. 2). В это исследование было включено 11 140 больных СД типа 2 с высоким риском осложнений. В ходе длительного наблюдения риск главных макро- и микрососудистых событий снизился на 9%.
Таблица 2. Влияние различных вариантов лечения на нефропротекцию и смертность пациентов
| Рандомизированное клиническое исследование | Препарат | Снижение почечных осложнений | Изменение сердечно-сосудистой смертности | Снижение общей смертности |
| ADVANCE | Нолипрел/форте | -21% | -18% | -14% |
| IDNT | Ирбесартан | -23% (КТ*) | Нет | Нет |
| RENAAL | Лозартан | -16% (КТ) | ? | Нет |
| ONTARGET | Телмисартан | Нет | ? | Нет |
| TRANSCEND | Телмисартан | Нет | ? | Нет |
| ROADMAP | Олмесартан | -23% | +494% (!) | +70% |
| ACCOMPLISH | Беназеприл/амлодипин | -47% | ? | Нет |
В исследовании ADVANCE достигнутый уровень АД в группе, принимавшей периндоприл + индапамид (Нолипрел), составил 134,7/74,8 мм рт. ст. и сопровождался достоверным снижением сердечно-сосудистой и общей смертности, коронарных событий и ухудшения функции почек. При этом необходимо отметить, что исходный уровень АД в группе активной терапии составлял 145/81 мм рт. ст.
Ранее в исследовании UKPDS были получены впечатляющие результаты по снижению риска ССО, что было связано прежде всего с различиями в снижении АД (в исследовании ADVANCE оно было для систолического АД в 17 раз (!), а для диастолического АД – в 2,5 раза (!) меньшим, чем в исследовании UKPDS) и длительностью терапии, которая в исследовании ADVANCE также была в 2 раза короче по сравнению с исследованием UKPDS. При этом гипотензивная терапия Нолипрелом начиналась фактически при том уровне АД, который был достигнут через 9 лет терапии в исследовании UKPDS. Но даже при такой «невыгодной» исходной позиции для Нолипрела в исследовании ADVANCE удалось добиться более выраженного нефопротективного эффекта, чем в UKPDS, что, безусловно, связано не только со снижением АД, но прямым нефропротективным эффектом периндоприла и индапамида, входящих в его состав.
Благодаря результатам исследования Нолипрел стал первой фиксированной антигипертензивной комбинацией, продемонстрировавшей положительное влияние на конечные точки у пациентов с СД вне зависимости от исходного уровня АД у них.
Лечение Нолипрелом у больных СД типа 2 уменьшило риск смерти от всех причин на 14%, а от сердечнососудистых – на 18%. В группе активного лечения риск развития коронарных осложнений был ниже на 14%, почечных – на 21%. Итак, улучшение контроля АД с помощью Нолипрела у больных СД типа 2 приводит к реальному снижению смертности. В дальнейшем были проанализированы результаты влияния контроля уровня АД с помощью Нолипрела у больных СД типа 2 на риск развития почечных осложнений в клиническом исследовании ADVANCE. Терапия Нолипрелом обеспечивала нефропротекцию у всех больных СД типа 2, даже среди больных с исходным АД меньше 120/70 мм рт. ст. Очень важно, что Нолипрел показал высокую эффективность в снижении риска сердечнососудистых осложнений на фоне самой современной терапии с использованием других антигипертензивных препаратов, статинов и дезагрегантов.
В 2010 г. были представлены новые данные по оценке влияния комбинации периндоприл/индапамид на риск развития сердечно-сосудистых и почечных осложнений у больных СД типа 2 и хроническим почечным заболеванием. Из 10 640 больных, включенных в исследование ADVANCE, у 6125 из них не было нарушений почечной функции, у 2482 больных была I–II стадия, у 2033 – III стадия хронического почечного заболевания. Терапевтические выгоды от присоединения Нолипрела к лечению больных СД типа 2 в виде снижения риска сердечно-сосудистых, почечных осложнений и смертности были получены у всех пациентов, независимо от исходного состояния почечной функции. Наиболее последовательно преимущества комбинации периндоприл + индапамид для нефропротекции отстаивал L.Ruilope и соавт. [9]. Так, на ежегодном конгрессе Европейского общества по артериальной гипертонии (ЕОАГ) в июне 2010 г. был представлен доклад, в котором проанализированы результаты наиболее крупных клинических исследований по изучению влияния препаратов, воздействующих на активность ренин-ангиотензиновой системы на почечные исходы у больных СД типа 2. Показано (см. табл. 2), что только в исследовании ADVANCE фиксированная комбинация периндоприл/индапамид не только снизила риск прогрессирования почечной недостаточности, но и улучшила выживаемость.
Дальнейший анализ результатов выявил ряд интересных тенденций. Так, в исследовании ADVANCE практически 100% пациентов через 3 мес лечения перешли с комбинации периндоприл/индапамид 2,0/0,625 мг на комбинацию 4,0/1,25 мг, а к концу периода наблюдения к этой терапии у 74% пациентов были добавлены другие антигипертензивные препараты (45% – периндоприл, 10% – блокаторы рецепторов ангиотензина II, 31% – β-адреноблокаторы, 32% – антагонисты кальция, 27% – другие антигипертензивные средства). То есть большинство пациентов получали либо «тройную» терапию, либо доза периндоприла была «двойной». Несколько позже появились результаты анализа [10] исследований PIXEL и PREMIER (PREterax in albuMInuria rEgRession), которые показали необходимость использования комбинации периндоприл + индапамид в максимальных терапевтических дозах практически у 30% пациентов.
В этой связи новая дозировка Нолипрела А – Би-форте, фиксированная комбинация периндоприла аргинина 10 мг и индапамида 2,5 мг упрощает возможность достижения эффективной нефропротекции в условиях реальной клинической практики у пациентов с СД типа 2 при неконтролируемом АД.
Еще один важный аргумент в пользу применения Нолипрела у пациентов с СД типа 2 – весьма выигрышная позиция с точки зрения влияния на глюкозоинсулиновый обмен, так как он не только снижает уровень глюкозы натощак и после нагрузочного теста, но и уменьшает инсулинорезистентность (рис. 3, 4).
Количество больных СД постоянно растет и по расчетам специалистов в 2025 г. их будет около 300 млн. В настоящее время главной причиной высокой смертности в этой популяции пациентов являются высокая частота ССО. Поэтому стратегия снижения сосудистых осложнений, базирующаяся на терапии Нолипрелом А/ форте/ Би-форте, имеет приоритетное значение для системы здравоохранения в целом.
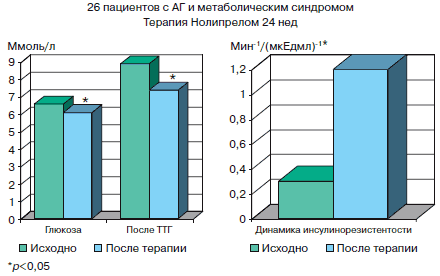
Рис. 3. Влияние Нолипрела на показатели глюкозоинсулинового обмена.
Примечание. ТТГ – пероральный 2-часовой тест толерантности к глюкозе.
Чазова И.Е., Мычка В.Б.
Кардиоваскулярная терапия и профилактика. 2006; 5 (1): 31–6.
Литература
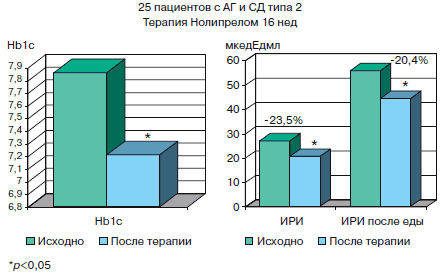
Рис. 4. Влияние Нолипрела на показатели глюкозоинсулинового обмена.
Примечание. ИРИ – иммунореактивный инсулин.
Аметов А.С. Кардиология. 2004; 11: 55–60.
