Эффективность и безопасность новой лекарственной формы амоксициллина/ клавуланата при респираторных инфекциях у детей
Статьи Опубликовано в журнале:Трудный пациент №9, том 6, 2008
О.А. Егорова1, Л.П.Жаркова1, Е.П. Карпова2, Е.П. Кунах1, С.Н. Владимиров3, Е.Ю. Балычева3, С.В. Ерофеева3, С.В. Штанько3, А.Ф. Неретина4
1Смоленская государственная медицинская академия
2Российская медицинская академия последипломного образования, Москва
3Детская городская больница, Таганрог
4Воронежская государственная медицинская академия им. Бурденко
Респираторные инфекции дыхательных путей относятся к распространённым заболеваниям детского возраста, являются частой причиной госпитализации и поводом для назначения системных антимикробных препаратов (АМП) [1]. Среди них важное место в структуре бактериальных инфекций дыхательных путей (ИДП) у госпитализированных детей занимают внебольничная пневмония (ВП), острый средний отит (ОСО) и острый бактериальный риносинусит (ОРС).
В большинстве случаев в виду сложности этиологическая диагностика ИДП не проводится и АМП назначаются эмпирически на основании предполагаемой структуры возбудителей, региональных или локальных данных об антибиотикорезистентности и доказанной эффективности в контролируемых клинических исследованиях.
В большинстве своём ИДП начинаются с симптомов ОРВИ, возбудителями которых являются вирусы. Однако очень быстро в детском возрасте к вирусам присоединяется назофарингеальная бактериальная микрофлора, среди которой можно выделить S. pneumoniae, H. influenzae, которые являются основными бактериальными возбудителями ИДП. Реже встречаются M. catarrhalis, S. pyogenes, S. аureus и атипичные возбудители -C. pneumoniae, M. pneumoniae, в раннем детском возрасте - C. trachomatis, U. urealyticum [2, 3].
Согласно современным рекомендациям Союза педиатров России, препаратом выбора для лечения ИДП является амоксициллин или ингибиторозащищённые пенициллины (амоксициллин/клавуланат) [4]. При этом выбор конкретного антибиотика основан на степени тяжести течения заболевания и предшествующей АБТ. Так, при первом эпизоде и нетяжёлом течении заболевания, отсутствии сопутствующих заболеваний (анемия, аденоидит и др.) препаратом выбора является амоксициллин. Тяжёлое течение заболевания, требующее госпитализации, предшествующая АБТ в связи с частыми заболеваниями у детей, посещающих детские учреждения, требуют назначения ингибиторозащищённых пенициллинов (амоксициллина/клавуланата) в связи с возможным распространением среди них резистентных к амоксициллину штаммов H. influenzae, M. catarrhalis [3].
В России уровень резистентности основных возбудителей респираторного тракта, как показали результаты исследования ПеГАС-1 и ПеГАС-2, достаточно низкий. Так, резистентность S. pneumoniae к амоксициллину и амоксициллину/клавуланату в 1999-2003 гг. составила 0,1 % и 0 % соответственно и оставалась на уровне 0,3 % для обоих АМП в 2004-2005 гг. Уровень устойчивости H. influenzae к амоксициллину (2004-2005 гг.) также оказался на низком уровне - 0,8 % резистентных и 4,6 % умеренно резистентных штаммов соответственно [5].
Высокая клиническая эффективность и безопасность амоксициллина/клавуланата в педиатрии при лечении ИДП подтверждена многочисленными сравнительными исследованиями [6-8]. Однако при сравнении его с другими бета-лактамными антибиотиками и макролидами, традиционные таблетированные формы амоксициллина/клавуланата отличаются худшей переносимостью что обусловлено изменениями со стороны желудочно-кишечного тракта в виде диареи, частота которой при применении обычных лекарственных форм может достигать 18-20 % и более [9, 12].
С появлением новой инновационной лекарственной формы - диспергируемых таблеток Флемоклав Солютаб® - удалось значительно улучшить переносимость амоксициллина/клавуланата. Отличительной чертой этого препарата является создание оптимальных концентраций активных компонентов в очаге инфекции за счёт более полного в сравнении с традиционными таблетками и предсказуемого всасывания амоксициллина и клавулановой кислоты в желудочно-кишечном тракте. Этот эффект достигается за счёт структуры лекарственной формы: таблетка состоит из микросфер, содержащих амоксициллин и клавулановую кислоту. Наполнитель микросфер кислотоустойчив, поэтому высвобождение активных веществ начинается в верхних отделах тонкого кишечника, где создаются оптимальные условия для максимально быстрого и полного всасывания. Минимальный по времени контакт клавулановой кислоты с кишечником позволяет снизить до 3 % частоту нежелательных реакций, в частности, развитие диареи [13]. Помимо прочего, новая форма амоксициллина/клавуланата - диспергируемые таблетки Солютаб - позволяет максимально улучшить комплаентность - таблетки можно разжевать или растворить для самых маленьких, они обладают приятным вкусом.
Всё это послужило основанием для проведения исследования по оценке клинической эффективности и безопасности препарата Флемоклав Солютаб®, назначаемого внутрь в течение 7-14 дней, при внебольничных ИДП (внебольничная пневмония, острый средний отит и острый риносинусит) у госпитализированных детей.
Пациенты и методы
Под наблюдением находились дети с установленным диагнозом ИДП (ВП, ОСО и ОРС), которые по тяжести течения заболевания могли принимать АМП внутрь, не получали системных АМП на протяжении 2 недель до включения в исследование, включая настоящий эпизод заболевания, либо предшествующая АБТ данного эпизода ИДП являлась неэффективной (неэффективность определялась как сохранение или ухудшение клинических симптомов и признаков заболевания и/или развитие осложнений ИДП через ≥ 48 ч с момента начала лечения).
Дети, имеющие в анамнезе аллергические реакции на препараты пенициллина, аллергические реакции немедленного типа на бета-лактамные антибиотики, а также с симптомами инфекционного мононуклеоза, лимфолейкоза, дисфункцией печени и/или желтухой на приём амоксициллина/клавулановой кислоты в анамнезе, нуждающиеся в одновременном назначении других системных АМП и/или более продолжительной АБТ, с тяжёлым течением заболевания и/или другими факторами, определяющими целесообразность парентерального введения АМП, при наличии госпитализаций по любому поводу в предшествующие 14 дней, не включались в исследование.
Диагноз заболевания устанавливался на основании типичных клинических симптомов и результатов дополнительных методов исследования.
Осмотр врача (педиатра и/или оториноларинголога) осуществлялся в день постановки диагноза, на 3-5-й день АБТ, через 1-2 дня (8-й или 12-й день) и 7-10 дней по окончании приёма АМП.
Всем детям проводилось физикальное обследование, исследование основных показателей жизнедеятельности, включая термометрию 2 раза в сутки, стандартные лабораторные исследования: клинические анализы крови и мочи, по показаниям - биохимический анализ крови, рентгенография органов грудной клетки (ВП) и придаточных пазух носа (ОРС), отоскопия (традиционная или пневматическая) (ОСО). Регистрация нежелательных явлений (НЯ), оценка их серьёзности, степени тяжести, связи с АМП проводилась во время всего периода лечения и последующего наблюдения.
Результаты и обсуждение
Всего под наблюдением находилось 125 детей, из них 65 (52 %) мальчиков и 60 (48 %) девочек в возрасте от 3 месяцев до 16 лет. Распределение детей по нозологическим формам, возрасту и полу представлено в таблице 1.
Таблица 1. Распределение детей по нозологическим формам, городам и полу
| Диагноз | Город | Число детей | Пол девочки/ мальчики, % | Средний возраст, лет | |
| N | % | ||||
| Внебольничная пневмония | Таганрог | 7 | 5,6 | 28,6/71,4 | 2,5 ± 1,9 |
| Острый риносинусит | Таганрог | 38 | 30,4 | 44,7/55,3 | 10,4 ± 5,2 |
| Острый средний отит | Всего | 80 | 74 | 51,3/48,8 | 3,2 ± 1,2 |
| Воронеж | 17 | 21,25 |   |   | |
| Москва | 29 | 36,25 |   |   | |
| Смоленск | 32 | 40 |   |   | |
| Таганрог | 2 | 2,5 |   |   | |
| Всего | 125 | 100 | 48/52 | 5,3 ± 4,5 | |
Продолжительность заболевания на момент установления диагноза составила в среднем 7,4 ±9,1 дней. Обращает внимание, что наименьшая длительность заболевания при госпитализации была отмечена при ОСО - 3,6 ± 5,3 дней, средняя при ВП - 5,9 ± 1,8 дней и наибольшая при ОРС - 15,4 ± 10,8 дней.
Из анамнеза пациентов выяснено, что 19 (15,2 %) детей в предшествующие 3 месяца перенесли ИДП, из них - 2 детей (28,6 %) госпитализированных с ВП, 7 детей (18,4 %) - с ОРС и 10 пациентов (12,5 %) - с ОСО, что указывает на то, что они относились к "часто болеющим" детям. Среднее количество ИДП на 1 ребёнка составило 1,4 ± 0,7 эпизода соответственно, при ОРС -1,3 ± 0,7; при ОСО - 1,4 ± 0,7 и при ВП - 1,5 ± 0,7.
До госпитализации дети не получали АМП по поводу данной ИДП. Однако 8/19 (42,1 %) пациентов в предшествующие 3 месяца получали АБТ бета-лактамными антибиотиками (цефтриаксон, амоксициллин/клавуланат, амоксициллин), большинство из которых переносили ОСО - 7 (36,8 %) и 1 (5,2 %) ребёнок - ОРС.
У 12 (9,6 %) детей ИДП протекали на фоне сопутствующей патологии, среди которых: атопический дерматит (16,6 %), дискинезия желчевыводящих путей (41,7 %), доброкачественный невус глаза (16,7 %), состояние после операции по поводу атрезии ануса (8,3 %), двусторонняя хроническая нейросенсорная тугоухость (8,3 %) и острый трахеобронхит (8,3 %).
В период лечения всем детям назначался амоксициллин/клавуланат компании Астеллас Фарма (Флемоклав Солютаб®) в форме диспергируемых таблеток, содержащих 125 мг или 250 мг амоксициллина и 31,25 мг или 62,5 мг клавулановой кислоты соответственно, в дозе 30-60 мг/кг/сут в 3 приёма непосредственно перед приёмом пищи.
Средняя суточная доза препарата при ВП составила 302,1 ± 124,4 мг; при ОРС - 1066,6 ± 492,1 мг и при ОСО - 367,5 ± 47,7 мг.
Средняя продолжительность курса терапии ВП составила 7,6 ± 1,8 дней при длительности госпитализации 11,9 ± 2,5 дней; ОРС - 8,5 ± 0,95 дней при длительности госпитализации 12,3 ± 2,2 дней и ОСО - 8,1 ± 1,9 дней при длительности госпитализации 10,3 ± 3,1 дней.
Кроме АМП все дети получали сопутствующую терапию - муколитики, бронходилататоры, антигистаминные препараты, деконгестанты и т. д.
Завершил планируемый курс лечения 121 (96,8 %) ребёнок, 4 пациента (2,4 %) досрочно прекратили приём АМП: 1 ребёнок из-за отсутствия эффекта на 3-й день терапии (ОРС), 1 - отсутствия эффекта на 7-й день лечения (ОСО), 1 - развития НЯ средней степени тяжести и 1 - по желанию родителей.
Клиническая эффективность терапии ИДП составила - 96,8 %, отсутствие эффекта отмечалось у двух пациентов (1,2 %). У 2-х пациентов оценить клинический ответ было невозможно. Клиническая эффективность Флемоклава Солютаб® при ОРС и ОСО представлена на рисунках 1-2. НЯ наблюдались у 4/125 (3,2 %) пациентов, в 4 из 5 случаев характеризовались лёгким течением и не потребовали отмены АМП. Средняя продолжительность НЯ составила 2,8 ± 0,8 дней, в 1 случае связь с приёмом Флемоклава Солютаб® рассматривалась как вероятная, по 2 из 5 случаев - возможная и сомнительная соответственно.
Рис. 1. Клиническая эффективность амоксициллина/клавуланата в форме диспергируемых таблеток при остром риносинусите у детей (n = 37)
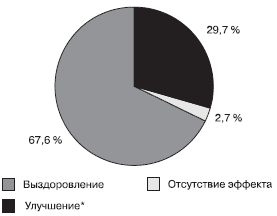
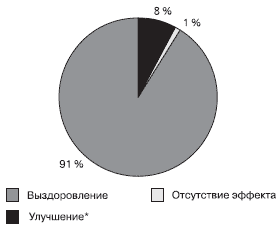
Рис. 2. Клиническая эффективность амоксициллина/клавуланата в форме диспергируемых таблеток при остром среднем отите у детей (n = 79)
Частота НЯ, зарегистрированных в ходе исследования, представлена в таблице 2.
Таблица 2. Частота НЯ у детей с ИДП на фоне приёма амоксициллина/клавуланата в форме диспергируемых таблеток (n = 125)
| Характер нежелательного явления | N | % |
| Сыпь | 2 | 1,6 |
| Тошнота и болезненость в эпигастральной области | 1 | 0,8 |
| Увеличение частоты стула до 4 раз в сутки | 1 | 0,8 |
| Эритема на коже лица | 1 | 0,8 |
Заключение
Таким образом, проведённое многоцентровое исследование клинической эффективности и безопасности препарата Флемоклав Солютаб®, назначаемого в дозе 30-60 мг/кг массы тела в сутки в 3 приёма в течение 7-14 дней у детей с бактериальными ИДП подтвердило высокую клиническую эффективность и благоприятный профиль безопасности препарата.
Клиническая эффективность Флемоклава Солютаб® при ИНД составила 96,8 % (от 97,3 % у пациентов с ОРС до 100 % - при ВП).
Нежелательные явления встречались с частотой 3,2 %, характеризовались нетяжёлым течением и только в одном случае потребовали отмены АМП.
Результаты проведённого исследования позволяют рекомендовать использование Флемоклава Солютаб® при лечении нетяжёлых острых бактериальных инфекций верхних и нижних дыхательных путей у детей как препарата выбора. Литература
1. Острые респираторные заболевания у детей: лечение и профилактика / Научно-практическая программа Союза педиатров России под ред. акад. РАМН А.А. Баранова. М.: 2002.
2. Каманин Е.И., Стецюк О.У. Инфекции верхних дыхательных путей и ЛОР-органов. Практическое руководство по антиинфекционной химиотерапии / Под ред. Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козловаю Смоленск: МАКМАХ, 2007; 248-258.
3. Вильямс Д. Резистентность к бета-лактамным препаратам // Антибиотики и химиотерапия. 1997; 42: 10: 5-9.
4. Применение антибиотиков у детей в амбулаторной практике / Под ред. А.А. Баранова, Л.С. Страчунского // Клиническая микробиология и антимикробная химиотерапия 2007; 9: 3: 200-10.
5. Решедько Г.К., Козлов Р.С. Состояние резистентности к антиинфекционным химиопрепаратам в России. Практическое руководство по антиинфекционной химиотерапии / Под ред. Л.С. Страчуского, Ю.Б. Белоусова, С.Н. Козлова Смоленск: МАКМАХ, 2007: 32-46.
6. Hoberman A., Paradise J.L., Block S., etal. Efficacy of amoxicillin/clavulanate for acute otitis media: relation to Streptococcus pneumoniae susceptibility // Pediat Infect Dis J. 1996; 15: 955-62.
7. Tomasz A. Multiple-antibiotic-resistant pathogenic bacteria: a report on the Rockfeller University Workshop, N Engl J Med 1994; 30:1247-51.Hendley JW. Otitis media // N Engl J Med. 2002; 347: 1169-74.
8. Brook I., GoberA.E. Effect of amoxicillin and co-amoxiclav on the aerobic and anaerobic nasopharangeal flora // J Antimicrob Chemother. 2002; 49: 689-92.
9. Sher L., Arguedas A., Husseman M. et al. Randomized, investigator-blinded, multicenter, comparative study of gatifloxacin versus amoxicillin/clavulanate in recurrent otitis media and acute otitis media treatment failure in children // Pediatr. Infect. Dis. J. 2005 Apr; 24: 4: 301-8.
10. Sethi S., Breton J., Wynne B. Efficacy and safety of pharmacokinetically enhanced amoxicillin-clavulanate at 2,000/125 milligrams twice daily for 5 days versus amoxicillin-clavulanate at 875/125 milligrams twice daily for 7 days in the treatment of acute exacerbations of chronic bronchitis // Antimicrob. Agents. Chemother. 2005 Jan; 49: 1: 153-60.
11. Solbiati M, Concia E, Bassetti D. The role of Augmentin in the treatment of upper and lower respiratory tract infections in children, 6th Mediterr Congress Chemother. Taormina, 1988. Absrt. 18.
12. Treadway G, PontaniD. Pediatric safety of azitromycin: worldwide experience // J Antimicrob Chemoter. 1996; 37: Suppl. C: 143-49.
13. Карпов О.И., Рязанцев С.В., Тихомирова И.А. Путь повышения эффективности и переносимости антибиотикотерапии при синусите у детей // Детские инфекции, 2006; 3: 57-60.
