Место фенспирида в фармакотерапии респираторных заболеваний
СтатьиОпубликовано в журнале:
«CONSILIUM MEDICUM» 2007, ТОМ №10, № 12, с. 64-69
Н.Г.Бердникова, Н.А.Малыдева, А.Н.Цой
ГОУ ВПО ММА им. И.М.Сеченова
Хотя по химической структуре и механизму действия фенспирид (Эреспал) нельзя отнести ни к стероидам, ни к нестероидным противовоспалительным средствам (НПВС), он является препаратом с противовоспалительным действием, ингибирующим метаболизм арахидоновой кислоты. В настоящее время существуют несколько групп лекарственных средств, оказывающих противовоспалительное действие путем воздействия на разные уровни метаболизма арахидоновой кислоты: фенспирид уменьшает поступление в клетку ионов кальция, ответственного за активацию фосфолипазы А2 глюкокортикостероиды (ГКС) блокирует фосфолипазу А2, стимулируя синтез белка-ингибитора; НПВС ингибируют циклооксигеназный путь образования простагландинов и тромбоксана; блокаторы лейкотриенов ингибируют липооксигеназный путь образования лейкотриенов (рис. 1).
Рис. 1. Метаболизм арахидоновой кислоты и группы лекарственных средств влияющие на разные уровни метаболизма.
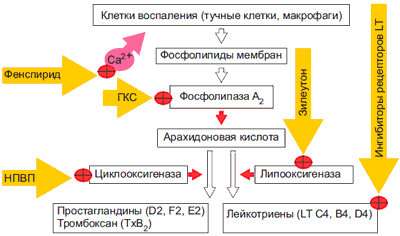
Механизм действия
Уменьшая активность фосфолипазы А2, фенспирид снижает синтез простагландинов, тромбоксанов и лейкотриенов - основных провоспалительных белков, инициирующих сосудистую фазу воспаления; предотвращает сокращение гладкой мускулатуры бронхов, вызываемое действием этих агентов. Доказано, что лейкотриены являются еще и хемоаттрактантом для эозинофилов и нейтрофилов, которые играют огромную роль в процессе воспаления. Нейтрофилы способны вырабатывать протеолитические ферменты и оксиданты, которые повреждают паренхиму легких и инактивируют ингибиторы протеиназ, что приводит к разрушению эластической ткани легких. В свою очередь, белки, образующиеся при разрушении эластина, коллагена и других компонентов интерстиция легких, привлекают новые нейтрофилы, которые поддерживают круг повреждения, способствуют хронизации процесса и приводят к формированию необратимых изменений.
Кроме того, фенспирид снижает продукцию и объем секреции муцина за счет уменьшения гиперплазии бокаловидных клеток, что положительно отражается на свойствах мокроты у больных с респираторными заболеваниями.
Экспериментальные исследования in vitro показали, что фенспирид имеет дополнительные противовоспалительные механизмы, включающие регуляцию и других медиаторов воспаления, в том числе таких, как провоспалительные цитокины и гистамин. Показано, что фенспирид способен блокировать H1-гистаминовые рецепторы, оказывая противоотечное действие, и α1-адренорецепторы, поэтому случаи передозировки препарата могут привести к снижению артериального давления.
Препарат в наибольшей степени ингибирует фактор некроза опухоли (TNF-a) и снижает миграцию клеток воспаления за счет уменьшения образования факторов хемотаксиса. Таким образом, противовоспалительный механизм действия фенспирида складывается из снижения активности метаболизма арахидоновой кислоты, блокады H1-гистаминовых и α1-адренергических рецепторов, снижения секреции бокаловидых клеток, уменьшения образования TNF-a и других медиаторов воспаления, подавления миграции эффекторных воспалительных клеток.
Следовательно, фенспирид уменьшает действие основных патогенетических факторов, которые способствуют развитию воспаления, гиперсекреции слизи, гиперреактивности и обструкции бронхов (рис. 2).
Рис. 2. Механизм действия и фармакологические эффекты фенспирида.
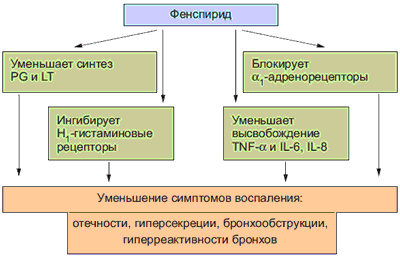
PG – простагландины, LT – лейкотриены, IL – интерлейкины.
Фенспирид не обладает болеутоляющим, антиагрегатным и жаропонижающим действием и по своему противовоспалительному эффекту уступает ГКС и НПВС. Он лишен нежелательных эффектов, свойственных этим препаратам.
В целом многофакторное воздействие фенспирида на воспалительный процесс реализуется в клинической практике уменьшением проявлений симптомов воспаления, в том числе и вирусной/бактериальной природы, и/или предупреждением развития обострений хронических заболеваниях или их осложнений.
Клинические проявления эффекта фенспирида проявляются в снижении количества и изменении качества выделяемой мокроты, что связано с уменьшением образования и выделения секрета (хотя он не обладает муколитическим и отхаркивающим действием), в улучшении мукоцилиарного транспорта, что приводит к уменьшению обтурации и обструкции дыхательных путей и, соответственно, к улучшению клинического состояния больных. Высокий профиль безопасности и хорошая переносимость препарата позволяют использовать фенспирид у детей с 3-месячного возраста. Обычно препарат можно назначать в качестве дополнительного средства при лечении больных с острыми респираторными вирусными инфекциями (ОРВИ), при обострениях хронических бронхо-обструктивных состояний, для профилактики обострений хронических обструктивных заболеваний легких (ХОБЛ). При необходимости его можно сочетать с антибактериальными и жаропонижающими лекарственными средствами, с бронхолитиками, ГКС и др.
Результаты клинических исследований
Многочисленные исследования применения фенспирида при острых респираторных заболеваниях верхних дыхательных путей у детей разного возраста показали его высокую эффективность [1—4]. В крупномасштабном сравнительном исследовании «Эльф» у 4 328 детей (5,2±3,7 года) с симптомами вирусной инфекции, получавших эреспал-сироп в течение 7-10 дней, показано, что на фоне приема фенспирида основные симптомы вирусной инфекции разрешались значительно быстрее. Они уменьшились уже к 4-му дню терапии, при этом к 7-му дню приема препарата у 71,3% пациентов было достигнуто полное выздоровление, а в контрольной группе - у 53,8% [5].
В другом сравнительном исследовании эффективности эреспала (240 мг/сут в течение 14 дней) у 141 взрослого пациента с острым трахеобронхитом на фоне ОРВИ (из них 54 пациента составляли группу контроля) статистически значимое клиническое улучшение наблюдалось уже на 3-й день лечения фенспиридома, в то время как в группе контроля положительная динамика выявлялась в более поздние сроки (только к 7-му дню терапии). В группе фенспирида быстрее наступало и выздоровление больных: 20% больных досрочно прекратили прием препарата в связи с хорошим самочувствием [6].
При применении фенспирида (240 мг/сут) у 597 пациентов с острым бронхитом, из которых 27% имели легкое течение и 72%- умеренной тяжести, через 1 нед лечения 25% пациентов отметили полное выздоровление, а через 2 нед -87%, у остальных 13% пациентов сохранялись незначительные жалобы. Из общего количества больных 87 (14,5%) пациентам потребовалось присоединение антибактериальной терапии [7].
В мультицентровом сравнительном исследование «Эра» также было показано сокращение сроков разрешения симптомов при острых респираторных заболеваниях верхних дыхательных путей (синусит, фарингит, ларингит, трахеит, бронхит). В этом исследовании пациенты принимали фенспирид 240 мг/сут в течение 10 дней, а в группе контроля использовались муколитики, антигистаминные препараты, антисептики, парацетамол. К 7-му дню лечения количество пациентов со снижением интенсивности кашля в группе фенспирида почти в 2 раза превышало число больных в группе контроля (243 и 131 пациент соответственно). В этом же исследовании пациенты с острым бронхитом, принимающие эреспал, также продемонстрировали более быстрые сроки выздоровления по сравнению с группой контроля: к 10-му дню количество выздоровевших больных в группе фенспирида составило 94% против 54,7% в контрольной группе [8].
Положительное влияние фенспирида (240 мг/сут в течение 7 дней) отмечено и у 371 пациента с острым респираторным заболеванием, причем у 57% пациентов выявлено полное исчезновение симптомов, у 39% частичное исчезновение и у 4 человек эффект отсутствовал [9]. Исследователи отмечали, что более раннее назначение фенспирида способствует более быстрому исчезновению клинических проявлений респираторной инфекции и, соответственно, уменьшению вероятности развития осложнений.
Учитывая многофакторность механизма действия и возможность воздействия непосредственно на патогенетические звенья бронхолегочной патологии, фенспирид может оказать положительное влияние на пациентов с хроническим бронхитом (ХБ) и ХОБЛ как в стабильном состоянии, так и при обострении. В связи с этим изучалось влияние фенспирида на течение обострений и/или профилактику обострений при длительном лечении в стабильном состоянии. В ряде клинических исследований был продемонстрирован положительный эффект его использования (табл. 1).
Таблица 1. Исследования влияния фенспирида у пациентов с ХБ и ХОБЛ.
| Вид исследования; источник | Число больных, диагноз, возраст, длительность лечения | Группа терапии, срок, число больных | Оценка эффективности, методы | Результаты |
| Открытое [10] | n=20, ХОБЛ; 3 нед при обострении и 3 мес после обострения | Фенспирид 160 мг/сут, 6 мес | Симптомы; индуцированная мокрота, маркеры, качество жизни | При обострении: ↓ кашля, улучшение отхождения мокроты; ↓ СРБ, цитоза, нейтрофилов в индуцированной мокроте. Через 3 мес: улучшение качества жизни |
| Рандомизированное, контролируемое плацебо [11] | n=39, ХОБЛ, (обострение); 61,1 ±9,8 года, 30 дней | 1-я группа п=19, амоксициллина клавуланат (10 дней) + фенспирид 240 мг/сут 1 мес; 2-я группа n=20, амоксициллина клавуланат (10 дней) + плацебо 1 мес | Симптомы | Через 10 дней в группе феспирида: ↓ кашля (44% против 16% на плацебо); ↓ хрипов (83% против 47% на плацебо); обострение разрешилось у 28% больных, в группе плацебо - 0 пациентов. Через 1 мес: различий между обеими группами не было |
| Рандомизированное, контролируемое плацебо [12] | n=157, ХБ; возраст 20-74 года; 6 мес | 1-я группа: фенспирид 160 мг/сут; 2-я группа: плацебо | Симптомы, число и длительность обострений. время до 1-го обострения | В группе фенспирида: ↓ мокроты и кашля (р=0,027) против плацебо (р=0,049); ↓ числа обострений (0,53 против 1,12 плацебо (р=0,038)); ↓ длительности обострений (3,3 дня против 7,3 плацебо (р=0,034)); Время до 1-го обострения статистически значимо не различалось |
| Сравнительное контролируемое плацебо [13] | n=60, ХОБЛ (1, 2 стадии) стабильное состояние; 6 мес | 1-я группа n=30; фенспирид 160 мг/сут; 2-я группа n=30, плацебо | Симптомы, маркеры число обострений | В группе фенспирида: ↓ симптомов у 26 (86,6%) больных против 16 (53,3%) в группе плацебо; ↓ IL-8, лактоферина, NOx, увеличение муцина в слюне и отсутствие динамики в группе плацебо; Изменения ОФВ1 недостоверны в обоих группах |
| Открытое, сравнительное [14] | n=79, ХОБЛ (2 стадии, стабильное состояние). 6 мес | 1-я группа n=40 ипратропия бромид 80 мкг/сут + фенспирид 160 мг/сут; 2-я группа n=39 ипратропия бромид 80 мкг/сут | Симптомы, прием салбутамола, ФВД, число и длительность обострений, мнение больного и врача | При комбинации ипратропия бромид + фенспирид: уменьшился кашель (р<0,05); ОФВ1 изменился недостоверно; врачи и пациенты отметили улучшение состояния и качества жизни (р<0,05). Не выявлено различий между группами: в количестве и продолжительности обострений легкой степени, в потребности в сальбутамоле |
| Открытое сравнительное [15] | n=20, ХОБЛ и n=60: ХБ стабильное состояние, 25-65 лет; 6 мес | 1 -я группа: фенспирид 160 мг/сут ипратропия бромид 160 мкг/сут получали 28 пациентов с ХБ и 11 с ХОБЛ; 2-я группа - только ипратропия бромид 160 мкг/сут -32 пациента с ХБ и 9 - с ХОБЛ | Симптомы, ФВД, маркеры индуцированная мокрота | При комбинированной терапии: ↓ симптомов и улучшение ФВД (р<0,05). В индуцированной мокроте при ХБ: уменьшение цитоза, снижение числа нейтрофилов, лимфоцитов и эозинофилов. Снижение TNF-a в сыворотке и IL-8 в мокроте (р<0,05) |
| Открытое [16] | n=49, ХОБЛ, стабильное состояние, 3 мес | Фенспирид 160 мг/сут в комбинации с ипратропия бромидом | Симптомы, цитология бронхиального смыва | Уменьшение кашля и мокроты (р>0,05), изменения цитограммы трахеобронхиального дерева (уменьшение нейтрофилов и увеличение макрофагов; р>0,05) |
| Открытое [17] | n =229, ХОБЛ, стабильное состояние | 1-я группа: легкая стадия - ипратропия бромид + фенспирид; 2-я группа: умеренная стадия - ипратропия бромид + фенспирид + салбугамол 2-я группа (подгруппа) - умеренная - ипратропия бромид + иГКС +фенспирид | Симптомы, ФВД. толерантность к физической нагрузке, число обострений | Наилучшие результаты были у больных в 1 группе - J, симптомов (р<0,05), | ОФВ на 14% (р<0,05) и толерантности к физической нагрузки - на 17,27% (р<0,05). Уменьшилось число обострений во всех группах, больше всего в 1 группе - в 2 раза. |
Из нежелательных реакций отмечались сухость во рту, сонливость, тахикардия, тошнота, боли в мышцах, головокружение и головная боль, однако эти симптомы носили легкий или умеренный характер, и в большинстве случаев не требовали отмены препарата. Имеются сообщения о 2 случаях орто-статической гипотонии [18]. В целом, как пациенты, так и врачи сообщают о хорошей переносимости препарата.
Мы приводим неопубликованные результаты наших собственных исследований, которые проводились на кафедре клинической фармакологии ММА им. И.М.Сеченова у больных ХОБЛ.
Цель нашего исследования выявить наличие противовоспалительно эффекта при длительном назначении фенспирида у больных ХОБЛ стабильного течения на фоне базисной терапии холинолитиками и b2-агонистами.
Материал и методы
В исследование были включены 14 пациентов с диагнозом ХОБЛ вне обострения (12 мужчин и 2 женщины); средний возраст 59,4±6,3 года; продолжительность ХОБЛ 14,3±2,5 года. Пациенты курили и продолжали курить (длительность курения -46,2±3,4 пачек/лет). Количество обострений за последний год составило 1,3±0,5. Все пациенты принимали ипратропия бромид по 160 мкг/сут и салбутамол в режиме «по потребности» за 3,5±0,7 мес до начала исследования. Учитывая присоединение фенспирида (160 мг/сут.) к приему ипратропиума бромида, то все обнаруженные изменения в ходе визитов (клинические, функциональные и морфологические) следовало относить к действию фенспирида. Общая продолжительность исследования - 6 мес. Клиническая и функциональная оценка проводилась до назначения фенспирида, а также через 3 и 6 мес и включала спирометрическое исследование, расчет количества используемого салбутамола, учет числа обострений. Анализ влияния терапии на клинические симптомы ХОБЛ проводили по дневникам, заполненным пациентами в ходе исследования. Дневник включал вопросы, касающиеся выраженности клинических симптомов ХОБЛ (кашель, количество мокроты, характеристика мокроты, затруднение дыхания/одышка, характер отхожде-ния мокроты). Выраженность симптомов пациенты оценивали в баллах от 0 до 3 (0 - отсутствие симптомов, 1 - редкие и/или слабо выраженные, 2 - умеренные и/или частые и 3 - постоянные и/или максимально выраженные симптомы).
Значения объема форсированного выдоха (OФВ1) до приема фенспирида (т.е. исходные, условно трактуемые как результат длительного лечения холинолитиками в максимальной дозе) составили 59,4±5,8%, отношение OФВ1 к форсированной жизненной емкости легких - 50,3±4,8 от должных величин.
С целью оценки степени воспаления (визуальной и морфологической) проведены бронхоскопия и исследование бронхиальных смывов до начала лечения и через 6 мес. Для эндоскопической характеристики воспалительных изменений бронхиального дерева использовали следующую классификацию:
- 1-я стадия - воспаление: слизистая бледно-розовая, смазанный сосудистый и хрящевой рисунки, секрет слизистый умеренный или обильный;
- 2-я стадия: слизистая ярко-красная, сосудистый и хрящевой рисунки не определяются, умеренная контактная кровоточивость, отделяемое слизисто-гнойное;
- 3-я стадия: слизистая багрово-синюшная, утолщена, отечна, сосудистый и хрящевой рисунки не просматриваются, выраженная контактная кровоточивость, большое количество гнойного отделяемого [19].
Склеротические изменения оценивались по степени дискинезии трахеи и главных бронхов, атрофическим изменениям слизистой оболочки и деформации трахеобронхиального дерева (1-3 степень).
- 1-я степень - одна из трех деструкции трахеобронхиального дерева: дискинезия трахеи и главных бронхов I—II степени, субатрофические изменения слизистой оболочки, либо ограниченная деформация трахеобронхиального дерева;
- 2-я степень - сочетание трахео-бронхиальной дискинезии I—II степени с признаками субатрофии слизистой оболочки и ограниченной деформацией, либо один выраженный признак: трахеобронхиальная дискинезия III степени или атрофия слизистой оболочки;
- 3-я степень - сочетание выраженных склеротических изменений: трахеобронхиальная дискинезия III степени и атрофия слизистой.
Обтурация мокротой бронхов оценивалась по количеству мокроты, обтурирующей разные уровни бронхов.
+++ - обтурация главных бронхов;
++ - обтурация мокротой в сегментарных бронхах;
+ - обтурация мокротой в субсегментарных бронхах.
Учитывая небольшую выборку пациентов, использовался парный непараметрический статистический анализ.
Результаты
При анализе данных влияния терапии на основные симптомы ХОБЛ статистически значимые изменения отмечались только при оценке выраженности кашля к 6-му месяцу наблюдения (р=0,02; рис. 3).
Рис. 3. Интенсивность кашля на фоне приема фенспирида.
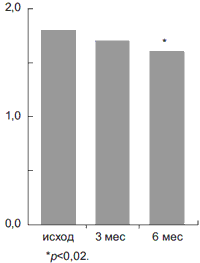
У 6 пациентов выявлено обострение ХОБЛ: у 3 больных - обострение легкой степени, у 2 - среднетяжелой, потребовавшее использования антибиотиков, и у 1 - тяжелое, когда пациент принимал и антибиотики и курс пероральных ГКС. Пациенты во время обострения продолжали прием фенспирида. Средняя продолжительность обострений - 13,6+1,5 дня. Обострения ХОБЛ у всех пациентов разрешились до проведения повторной бронхоскопии.
Имелась тенденция к уменьшению количества используемого салбутамола в режиме «по требованию»: с 4,4±0,3 до 3,7±0,2 вдохов в сутки (р>0,05). Не зарегистрировано различий в ФВД (OOBj) на фоне лечения фенспиридом: через 3 мес он составил 60,2 ±2,9%, а через 6 мес - 61,4+3,2% (р>0,05).
При визуальной оценке бронхоскопической картины у пациентов с ХОБЛ в стабильном состоянии в исходе были выявлены признаки, характерные для воспаления 0-1 степени, незначительные склеротические изменения и наличие густой трудноотделяемой мокроты. При повторной бронхоскопии через 6 мес отмечалось статистически достоверное уменьшение признаков воспаления и количества мокроты без динамики степени выраженности склеротических изменений (рис. 4).
Рис. 4. Степень выраженности воспаления и обтурации бронхов по результатам бронхоскопического исследования у пациентов с ХОБЛ.
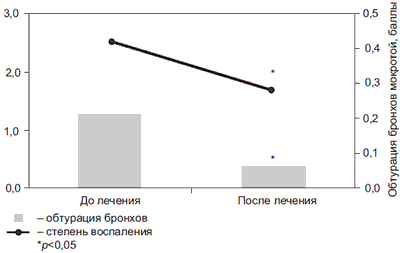
По данным цитологического исследования бронхиальных смывов выявлены признаки воспаления, увеличение количества нейтрофилов (табл. 2).
Таблица 2. Цитограмма больных с ХОБЛ до и после лечения фенспиридом (M±SD)
| Показатель | До лечения | Через 6 мес |
| Цитоз в 1 мл | 621 184±203 | 877 215±284* |
| Нейтрофилы, % | 50,3±13,1 | 29,1 ±9,1* |
| Лимфоциты, % | 6,9±1,4 | 10,6±3,2 |
| Альвеолярные макрофаги, % | 8,2±3,2 | 7,3±3,0 |
| Бронхиальный эпителий, % | 34,6±12,5 | 52,8±22,7* |
Примечание. *р
Через 6 мес лечения фенспиридом на фоне базисной терапии бронхолитиками в цитограмме больных отмечалось статистически достоверное увеличение цитоза, клеток бронхиального эпителия и уменьшение нейтрофилов. Это может свидетельствовать о проявлении противовоспалительного эффекта фенспирида.
Таким образом, у больных ХОБЛ легкой и умеренной стадии, находящихся в стабильном состоянии и принимающих длительное время базисную терапию бронхолитиками, в бронхиальном дереве сохраняются процессы воспаления. Степень воспаления несколько уменьшается при дополнительной, длительностью не менее 6 мес, терапии фенспиридом. При этом наряду с клиническими проявлениями, уменьшаются частота обострений, признаки обтурации бронхов мокротой, степень воспаления бронхиальной стенки.
Среди больных, получавших фенспирид, побочные эффекты легкой степени, не потребовавшие отмены препарата, отмечены в 2 случаях (в 1 - боль в животе и диспепсия, в 2 -сухость во рту).
Обсуждение
Инфекционные заболевания респираторного тракта широко распространены не только среди детей, но и у взрослых, а любая вирусная инфекция у пациентов, страдающих хроническими респираторными заболеваниями, как правило, приводит к их обострению. В свою очередь, обострение поддерживает и усугубляет состояние хронического воспаления в дыхательных путях.
Вирусные инфекции обычно влекут за собой воспалительную реакцию, затрагивающую слизистую оболочку тех или иных отделов дыхательных путей. В связи с этим проведены исследования, целью которых было показать эффективность фенспирида у детей и взрослых с ОРВИ.
Фенспирид обладает многофакторным действием и, учитывая его противовоспалительный эффект, применение данного препарата у больных ХОБЛ считается патогенетически обоснованным. Исследование противовоспалительной активности фенспирида, по результатам бронхоскопических исследований у пациентов со стабильным течением ХОБЛ, выявило уменьшение степени воспаления и уменьшение обтурации мокротой бронхиального дерева. Анализ цитологической картины продемонстрировал увеличение цитоза, количества клеток бронхиального эпителия и уменьшение нейтрофилов, что свидетельствует о противовоспалительном эффекте.
Таким образом, на основании анализа результатов проведенных исследований можно отметить следующее:
- дополнительная терапия фенспиридом уменьшает клинические проявления и ускоряет процесс выздоровления у пациентов с острыми респираторными инфекциями по сравнению с неспецефической противовирусной терапией;
- у пациентов с обострением хронического необструктивного бронхита и ХОБЛ I—II степени присоединение длительного приема фенспирида к базисной терапии бронхолитиками (ипратропиумом бромидом) способствует уменьшению симптомов - кашля и количества отделяемой мокроты, а также числа и продолжительности обострений;
- продемонстрирован противовоспалительный эффект фенспирида, особенно в комбинации с холинолитиками, который заключается в уменьшении степени воспаления бронхов, уровня маркеров воспаления (нейтрофилов, TNF-a, IL-8);
- для достижения противовоспалительного эффекта у пациентов со стабильным нетяжелым течением ХОБЛ желателен длительный прием фенспирида в составе базисной терапии.
В целом пациенты отмечали улучшение состояния, а нежелательные эффекты, которые были зарегистрированы в некоторых исследованиях, были легкими по интенсивности и не требовали отмены препарата.
Таким образом, по данным бронхоскопии и цитограммы бронхиальных смывов, присоединение фенспирида к холинолитикам способствует уменьшению выраженности кашля и степени хронического воспаления.
ЛИТЕРАТУРА
1. Овсянникова Е.М. Бронхообструктивный синдром инфекционного генеза у детей. Consilium Medicum. Педиатрия 2005; 2.
2. Коровина Н.А. и др. Комплексная терапия обструктивного бронхита с применением фенспирида (эреспала) у детей раннего возраста. Клин. фармакол. и тер. 2001; 5: 1–4.
3. Zielnik-Jurkiewicz B, Jurkiewicz D. Usefulness of fenspiride in the treatment of acute otitis media in children Pol Merkur Lekarski. 2005; 18 (108): 624–8.
4. Zawisza E. Effectiveness and tolerance of fenspiride treatment in chronic sinusitis. Results of the Polish multicenter study. Otolaryngol Pol. 2005; 59 (1): 141–5.
5. Пульмонология детского возраста: проблемы и решения. Под ред. Ю.Л.Мизерницкого, А.Д.Царегородцева. 2005; 5.
6. Белевский А.С. Возможности оптимизации терапии острых бронхитов на фоне ОРВИ. Леч. врач 2001; 8.
7. P_usa T, Ochwat A. Fenspiride in patients with acute bronchitis. Pol Merkur Lekarski 2005; 19 (109): 32–6.
8. Овчаренко С.И. Противовоспалительная терапия бронхита. Consilium Medicum 2004; 3 (5).
9. Плус Т., Навацка Д. Эффективность и переносимость фенспирида у взрослых больных с острыми респираторными заболеваниями. Леч. врач. 2005.
10. Fedorova TA, Ekkert NV, Chernekhovskaia NE et al. Potential of antiinflammatory therapy in patients with chronic obstructive lung disease. Klin Med (Mosk) 2005; 83 (7): 24–9.
11. Lirsac B, Benezet O, Dansin E et al. Evaluation and symptomatic treatment of surinfectious exacerbations of COPD: preliminary study of antibiotic treatment combined with fenspiride (Pneumorel 80mg) versus placeboRev Pneumol Clin 2000; 56 (1): 17–24.
12. Pirozynski M, Skucha W, S_omi_ski M et al. The effect of fenspiride on the number of exacerbations and the time of first exacerbation in patients with chronic bronchitis Pol Merkur Lekarski. 2005; 19 (110): 139–43.
13. Игнатова Г.Л., Степанищева Л.А., Печенкина Ю.О. Оценка влияния фенспирида на некоторые показатели мукозального иммунитета при хронической обструктивной болезни легких ранней стадии. www.pulmonology.ru
14. Чучалин А.Г., Шмелев Е.И., Овчаренко С.И. с соавт. Эффективность фенспирида у больных хронической обструктивной болезнью легких. Consilium Medicum 2005; 5 (10).
15. Volkova LI, Budkova AA, Filonova NN et al. Efficacy of supplemental anti-inflammatory therapy with fenspiride in chronic obstructive and nonobstructive bronchitis. Clin Drug Investig 2005; 25 (4): 257–64.
16. Безлепко А.В. Опыт длительного применения эреспала при лечении больных хроническим обструктивным бронхитом. 2002. www.pulmonology.ru
17. Шмелев Е.И. Противовоспалительная терапия фенспиридом больных хронической обструктивной болезнью легких. Consilium Medicum. Пульмонология 2008; 35–9.
18. Chodorowski Z, Sein Anand J, Korolkiewicz R. Acute intoxication with fenspiride. Przegl Lek. 2004; 61 (4): 435–6.
19. Чернеховская Н.Е, Ярема И.В. Хронические обструктивные заболевания легких. М.: Петит, 1998.


