Сравнение влияния рамиприла на среднесуточное и офисное АД. Субисследование HOPE
Статьи Опубликовано в: "Hypertension." 2001г.; №38; С.28-32 (Comparative Effects of Ramipril on Ambulatory and Office Blood Pressures. A HOPE Substudy)P. Svensson, U. Faire, P. Sleight, S. Yusuf, J. Еstergren
Резюме - В исследовании HOPE ингибитор АПФ рамиприл вызывал значительное снижение сердечно-сосудистой заболеваемости и смертности у больных группы высокого сердечно-сосудистого риска. Этот эффект можно было только частично связать с умеренным снижением офисного АД за исследуемый период (в среднем на 3/2 мм рт. ст.). Однако рамиприл в этом исследовании назначали один раз в день перед сном, а АД измеряли днем, поэтому результаты офисных измерений могли давать заниженную оценку снижению суточного АД. У 38 больных с атеросклерозом периферических артерий, включенных в исследование HOPE, перед рандомизацией и через 1 год после начала лечения проводили суточное амбулаторное мониторирование АД. Офисное АД измеряли в положении сидя непосредственно перед установкой монитора. Терапия рамиприлом через 1 год привела к недостоверному снижению офисного АД (на 8/2 мм рт. ст.) и дневного АД (на 6/2 мм рт. ст.). Суточное АД достоверно снизилось (на 10/4 мм рт. ст., P<0.03), в основном за счет более значительного гипотензивного эффекта в ночное время (на 17/8 мм рт. ст.; P<0.001). Отношение АД в ночное и дневное время также значительно снизилось в группе рамиприла. При назначении рамиприла один раз в день перед сном наблюдается более значительное снижение суточного АД, особенно в ночное время, чем офисного АД. Хотя динамика офисного АД может быть использована для сравнения полученных данных с результатами предыдущих крупных клинических и эпидемиологических исследований, тем не менее, благоприятные эффекты рамиприла на сердечно-сосудистую заболеваемость и смертность, продемонстрированные в исследовании HOPE, могут в большей степени отражать его антигипертензивное действие, чем это считалось ранее. (Hypertension. 2001;38:28-32.)
Ключевые слова: антигипертензивная терапия, амбулаторное мониторирование АД, клинические исследования, поражение периферических сосудов, ингибиторы АПФ, рамиприл
В исследовании Heart Outcomes Prevention Evaluation (HOPE) лечение ингибитором АПФ рамиприлом привело к снижению сердечно-сосудистой заболеваемости и смертности у широкого круга пациентов высокого риска [1]. В исследование включали пациентов в возрасте >55 лет с коронарной болезнью сердца, цереброваскулярными заболеваниями, поражением периферических артерий или сахарным диабетом и еще по крайней мере одним дополнительным сердечно-сосудистым фактором риска. Примерно 50% больных страдали артериальной гипертонией и получали лечение антигипертензивными средствами. Снижение офисного АД при лечении рамиприлом было небольшим (на 3/2 мм рт. ст.), а у большинства больных исходное АД было нормальным (в среднем 139/79 мм рт. ст.) [1], поэтому благоприятный эффект препарата объясняли в основном не снижением АД как таковым, а другими механизмами, связанными с ингибированием АПФ. Подобные механизмы могут включать в себя улучшение функции эндотелия или антиатеросклеротическое действие [2].
В соответствии с протоколом HOPE рамиприл назначали в дозе 10 мг один раз в день перед сном. Офисное АД измеряли при визитах к врачу в дневное время — в большинстве случаев через 10-18 часов после приема препарата; соответственно, эти результаты могли быть причиной заниженной оценки снижения суточного АД. Кроме того, важное значение может иметь снижение АД в ночное время и утренние часы, когда чаще всего развиваются сердечно-сосудистые осложнения [3,4].
Целью исследования было изучение эффекта рамиприла на суточное АД у 38 больных с поражением периферических сосудов, у которых в рамках исследования HOPE проводили суточное амбулаторное мониторирование АД перед рандомизацией и через 1 год после начала лечения.
Методы
Больные
У обследованных больных наблюдалась перемежающаяся хромота, а лодыжечно-плечевой индекс составлял ≤0,9 по данным Допплеровского исследования. Они были включены в исследование HOPE в северной части Стокгольма (больницы Каролинска и Дандерид).
Из исследования исключали больных с болью в покое, тяжелым заболеванием почек (сывороточный уровень креатинина более 200 мкмоль/л), неконтролируемой гипертонией и сердечной недостаточностью, сопровождающейся снижением фракции выброса левого желудочка менее 40%.
Информированное согласие на участие в исследовании дали 38 больных (в том числе 19 мужчин) в возрасте, в среднем, 71 год. Характеристики больных приведены в табл. 1. Двадцать пациентов были рандомизированы в группу рамиприла и 18 — в группу плацебо. Средняя доза рамиприла через 1 год составляла 8,1 мг. У 2 пациентов лечение рамиприлом было прекращено ранее, чем через 1 год, из-за кашля. Сопутствующая терапия исходно и через 1 год приведена в табл. 2. В группе плацебо в течение 1 года 2 больным были назначены новые антигипертензивные препараты или увеличены дозы старых средств, а у 2 пациентов лечение антигипертензивными средствами было прекращено. В группе рамиприла новые антигипертензивные средства были назначены 3 больным, а у 1 пациента антигипертензивная терапия была прекращена.
Таблица 1. Основные характеристики обследованных больных (n=38)
| Характеристики | Рамиприл (n=20) |
Плацебо (n=18) |
|---|---|---|
| Возраст, лет | 70±6 | 72±8 |
| Мужчины/женщины | 9/11 | 10/8 |
| Курящие/бросили курить/ никогда не курили | 4/14/2 | 4/11/3 |
| Индекс массы тела, кг/м2 | 24±3 | 25±5 |
| Лодыжечно-плечевой индекс p<0.05 | 0.62±0.13 | 0.53±0.14 |
| Сахарный диабет | 4 | 5 |
| Артериальная гипертония | 7 | 7 |
| Ишемическая болезнь сердца | 9 | 6 |
| Цереброваскулярные заболевания | 2 | 4 |
Таблица 2. Сопутствующая терапия у больных двух групп исходно и через 1 год
| Препараты | Исходно | Через 1 год | ||
|---|---|---|---|---|
| Рамиприл (n=20) |
Плацебо (n=18) |
Рамиприл (n=20) |
Плацебо (n=18) |
|
| Бета-блокаторы | 2 | 3 | 3 | 4 |
| Антагонисты кальция | 5 | 4 | 8 | 6 |
| Диуретики | 5 | 5 | 7 | 5 |
| Ингибиторы АПФ | 0 | 0 | 0 | 1 |
| Аспирин | 8 | 7 | 11 | 5 |
| Нитраты | 10 | 8 | 13 | 6 |
| Гиполипидемические средства | 2 | 2 | 5 | 3 |
Протокол исследования был одобрен этическим комитетом больницы Каролинска.
Офисное АД
Офисное АД регистрировалось дважды опытной медсестрой на обеих руках с помощью ртутного сфигмоманометра в положении сидя после 15-минутного отдыха. Расчитывали среднее значение двух измерений. Если разница систолического или диастолического АД на двух руках превышала 10 мм рт. ст., то фиксировали более высокое значение. В противном случае регистрировали АД на доминирующей руке [5]. На протяжении всего исследования для регистрации офисного АД и мониторирования АД использовали одну и ту же руку.
Амбулаторное суточное мониторирование АД
Мониторирование АД проводили с помощью неинвазивного осциллометрического метода (SpaceLabs 90207, SpaceLabs Inc). Монитор устанавливала опытная медсестра. Во время мониторирования больным рекомендовали не ограничивать свою повседневную активность. Перед началом мониторирования сверяли результаты автоматического и ручного измерения АД, чтобы обеспечить правильность его регистрации. АД и частоту сердечных сокращений регистрировали автоматически каждые 15 минут в течение 24 часов.
"Ручная" обработка данных не производилась, чтобы исключить системную ошибку. Рассчитывали среднесуточное, среднедневное (с 7.00 до 21.00) и средненочное (с 24.00 до 6.00) АД. Измерения проводили после завершения вводного плацебо периода за день до рандомизации. Больных рандомизировали на группы рамиприла (дозу его титровали до 10 мг один раз в день перед сном) или плацебо. Повторное мониторирование АД проводили через 1 год. Пациенты принимали исследуемый препарат перед сном за день до мониторирования и в день, когда проводилось мониторирование АД проводили через 1 год. Пациенты принимали исследуемый препарат перед сном за день до мониторирования и в день, когда проводилось мониторирование АД.
Статистический анализ
Результаты приведены в виде средних значений и стандартных отклонений, если не указано иное. Статистический анализ проводили с помощью программы Statistica 4.0 (Statsoft Inc, 1993). Для оценки различий между группами рамиприла и плацебо использовали критерий t Стьюдента для независимых выборок. Различия считали статистически значимыми при p<0,05. Результаты Офисное АД и суточное мониторирование АД
У всех больных удалось адекватно измерить более 80% показателей; медиана составила 94 на больного (от 78 до 98). В 5 случаях АД измеряли на доминирующей руке. Офисное АД исходно составляло 152±21/83±7 мм рт. ст. в группе рамиприла и 149±19/79±12 мм рт. ст. в группе плацебо (различие недостоверно), а среднесуточное АД - 148±19/78±9 и 153±18/80±8 ммрт. ст. соответственно (различие недостоверно). Динамика показателей АД в течение 1 года приведена в табл. 3 и на рис. 1 (см. 2 стр обложки).
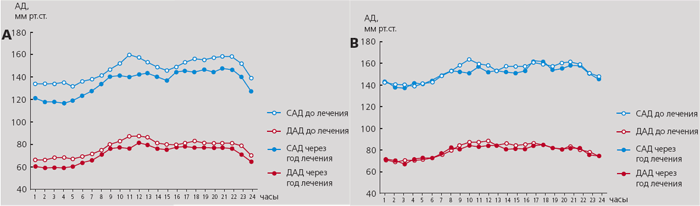
Рис. 1. Средние значения АД систолического (САД) и диастолического (ДАД) в различное время суток в группах рамиприла (А, n=20) и плацебо (В, n=18) исходно и через 1 год.
Таблица 3. Офисное АД и результаты суточного мониторирования АД у больных, рандомизированных в группы рамиприла и плацебо (исходно и их снижение через 1 год)
| АД, мм рт. ст. | Исходно | Снижение через 1 год | ||||
|---|---|---|---|---|---|---|
| Рамиприл (n=20) |
Плацебо (n=18) |
Ρ | Рамиприл (n=20) |
Плацебо (n=18) |
Ρ | |
| Систолическое офисное АД | 152±21 | 149±19 | нд | 12±24 | 4±27 | нд |
| Диастолическое офисное АД | 83±7 | 79±12 | нд | 5±10 | 3±12 | нд |
| Среднесуточное систолическое АД | 148±19 | 153±18 | нд | 12±15 | 2±10 | 0.03 |
| Среднесуточное диастолическое АД | 78±9 | 80±8 | нд | 5±7 | 1±6 | 0.03 |
| Среднедневное систолическое АД | 153±20 | 159±19 | нд | 10±15 | 4±12 | нд |
| Среднедневное диастолическое АД | 83±9 | 84±9 | нд | 4±7 | 2±7 | нд |
| Средненочное систолическое АД | 136±20 | 142±19 | нд | 16±16 | -1±11 | <0.001 |
| Средненочное диастолическое АД | 69±9 | 71±9 | нд | 7±7 | -1±6 | <0.001 |
Через 1 год снижение офисного АД (на 8/2 мм рт. ст.) и среднедневного АД (на 6/2 мм рт. ст.) достоверно не отличалось между группами рамиприла и плацебо. Среднесуточное АД в группе рамиприла достоверно снизилось по сравнению с контролем (на 10/4 мм рт. ст.; р<0.03). Значительное снижение АД при лечении рамиприлом отмечалось в ночное время (на 17/8 мм рт. ст., p<0.001). Исходно отношение среднего АД в ночное и дневное время составляло 0.86±0.06 в группе рамиприла и 0.87±0.07 в группе плацебо (различие недостоверно). Через 1 год этот показатель снизился при лечении рамиприлом (0.82±0.06) по сравнению с плацебо (0.89±0.07, p<0.01) (рис. 2 и 3).
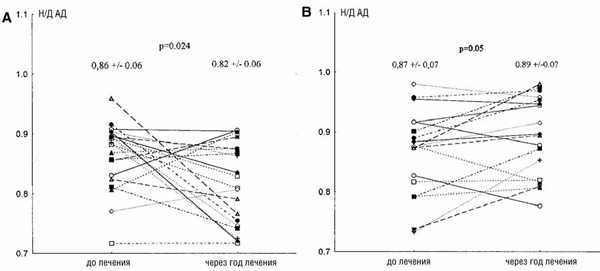
Рис. 2. Отношение ночного и дневного среднего амбулаторного АД (Н/Д АД) в группах рамиприла (А, n=20) и плацебо (В, n=18) исходно и через 1 год.
Обсуждение
В настоящем исследовании средненочное АД значительно снизилось при лечении рамиприлом в дозе 10 мг один раз в день перед сном по сравнению с плацебо. Динамика офисного и среднедневного АД была незначительной и сопоставимой с умеренным снижением АД во всей выборке исследования HOPE. Отсутствие статистически значимого снижения АД в дневное время могло быть связано с тем, что в нашем исследовании принимало участие небольшое число больных. Отношение АД в ночное и дневное время значительно снизилось в группе рамиприла по сравнению с плацебо за счет выраженного гипотензивного эффекта препарата в ночное время (p<0.01). Последний мог объясняться тем, что рамиприл назначали перед сном. Ранее было показано, что рамиприл дает достаточно плавный антигипертензивный эффект, который сохраняется в течение 24 часов, что позволяет применять его один раз в день [6]. Однако как и при использовании других антигипертензивных средств, гипотензивное действие меняется в течение суток, а эффект рамиприла достигает пика через 3-6 часов после приема [8,9]. Коэффициент Р/Т (отношение снижения АД на пике действия и в конце интервала дозирования) рамиприла составляет 0,5, т.е. через 24 ч отмечается сохранение 50% от максимального эффекта [7-9]. Офисное АД в нашем исследовании (и, вероятно, у всех больных, принимавших участие в HOPE) измеряли более чем через 12 часов после приема рамиприла.
В клинических исследованиях антигипертензивная терапия обычно вызывает более значительное снижение офисного АД, чем среднесуточного АД. Другим возможным объяснением различий между предыдущими данными и результатами нашего исследования является то, что в клинических исследованиях больных обычно отбирают на основании офисного АД, т.е. находящихся в верхней части распределения его в популяции. В процессе наблюдения регрессия к среднему приводит к снижению офисного АД, которое лучше отражает "истинное" АД (а также теснее коррелирует со среднесуточным АД). Антигипертензивная терапия при значениях офисного АД, находящихся в верхней части спектра, может привести к их более значительному снижению, чем среднесуточного АД (что является обычным результатом в клинических исследованиях). В HOPE и нашем исследовании отбор больных производился не на основании высокого офисного АД, поэтому оно могло отражать более "нормальное" распределение АД. На фоне антигипертензивной терапии в подобной выборке отмечается более тесная связь снижения офисного и среднесуточного АД.
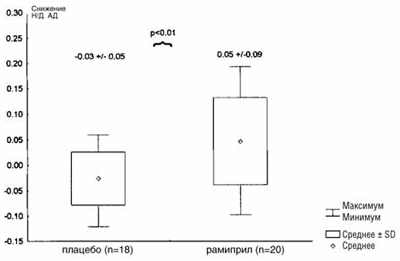
Рис. 3. Снижение отношения ночного и дневного среднего амбулаторного АД (Н/Д АД) в группах рамиприла (А, n=20) и плацебо (В, n=18) исходно и через 1 год.
Среднее снижение офисного АД в исследовании HOPE (3/2 мм рт. ст.) с учетом результатов предыдущих исследований [10,11] позволяет объяснить снижение частоты инсульта примерно на 13% и инфаркта миокарда примерно на 5%. Однако в исследовании HOPE относительный риск развития этих осложнений снизился на 31 и 20% соответственно. В связи с этим было высказано предположение о том, что указанные позитивные изменения объясняются не только снижением АД как таковым, но и протективными эффектами препарата на сосуды, связанными с ингибированием АПФ.
Результаты нашего исследования свидетельствуют о том, что благоприятные эффекты рамиприла в исследовании HOPE могут быть в большей степени связаны со снижением АД (особенно в ночное время), чем можно было бы предположить на основании изменений офисного АД в исследовании в целом и нашем исследовании. Однако представления об АД как сердечно-сосудистом факторе риска базируются главным образом на результатах эпидемиологических и клинических исследований, в которы регистрировали офисное АД. С другой стороны, в нескольких когортных исследованиях было показано, что среднесуточное АД является более важным фактором риска, чем офисное АД [12-14].
Учитывая тот факт, что в предыдущих исследованиях измеряли офисное АД, трудно проводить связь между снижением среднесуточного АД и сердечно-сосудистого риска. Нельзя исключить, что в этих исследованиях зафиксированные эффекты могли быть заниженными или завышенными. Следовательно, сравнивать разные исследования следует на основании офисного, а не среднесуточного АД. Как нам известно,
НОРЕ было единственным крупным исследованием, в котором антигипертензивный препарат в соответствии с протоколом [15] рекомендовали принимать перед сном. Оно может быть уникальным исследованием с точки зрения эффектов препарата на вариабельность АД в ночное - дневное время и времени измерения офисного АД после приема препарата.
В некоторых эпидемиологических исследованиях выявлена корреляция между сердечнососудистым риском и степенью снижения отношения ночного и дневного АД [13,15]. У 393 больных (1666 человеко-лет наблюдения) группы плацебо в исследовании SYST-Eur отмечена ассоциация между этим коэффициентом и частотой сердечно-сосудистых осложнений, которая не зависела от срреднесуточного АД. При увеличении отношения ночного и дневного АД на каждые 10% сердечно-сосудистый риск повышался на 41% [14]. В нашем исследовании величина этого коэффициента исходно составляла в среднем 0,86 в обеих группах, а через 1 год отличалась на 8% (0,89 и 0,82 в группах плацебо и рамиприла соответственно). Таким образом, снижение его ассоциировалось с уменьшением риска сердечно-сосудистых исходов, отмеченным в НОРЕ.
Высказывались опасения по поводу того, что снижение АД в ночное время ниже нормальных значений у больных с сердечно-сосудистыми заболеваниями может оказать негативное влияние на перфузию головного мозга и миокарда [16,17]. Если результаты нашего исследования отражают изменения ночного АД во всей выборке HOPE (у больных с сердечно-сосудистыми заболеваниями и в среднем "нормальным" АД), то снижение риска развития инсульта на 32%, продемонстрированное в этом исследовании, свидетельствует о безосновательности подобных опасений.
Важными различиями между нашим небольшим исследованием и всей выборкой HOPE являются особенности критериев включения (поражение периферических сосудов имелось у 100 и 19% больных соответственно), более высокое исходное офисное АД (151/81 и 139/79 мм рт. ст.) и старший возраст (71 и 66 лет). Эти особенности могли отразиться на некоторых результатах нашего исследования и препятствуют распространению полученных данных на выборку HOPE в целом. Однако результаты нашего исследования свидетельствуют о том, что тип измерения АД и время его регистрации после приема препарата являются важными факторами, которые следует учитывать при оценке влияния антигипертензивных средств на риск развития неблагоприятных клинических исходов.
Таким образом, среднесуточное АД при применении рамиприла один раз в день перед сном снижается в большей степени (особенно в ночное время), чем офисное АД. Однако при сравнении результатов исследования с предыдущими крупными исследованиями и большинством эпидемиологических исследований следует ориентироваться на офисное АД. Хотя наши данные были получены в небольшом исследовании, они свидетельствуют о том, что благоприятные эффекты рамиприла на сердечно-сосудистую заболеваемость и смертность, продемонстрированные в HOPE, могут в большей степени отражать его антигипертензивное действие, чем это считалось ранее.
Литература
1. Yusuf S, Sleight P, Pogue J, Bosch J, Davies R, Dagenais G. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients: the Heart Outcomes Prevention Evaluation Study Investigators. N Engl J Med. 2000;342:145-153.2. Lonn EM, Yusuf S, Jha P, Montague TJ, Teo KK, Benedict CR, Pitt B. Emerging role of angiotensin-converting enzyme inhibitors in cardiac and vascular protection. Circulation. 1994;90:2056-2069.
3. Muller JE, Toffler GH. Circadian variation and cardio-vascular disease. N Engl J Med. 1991;325:1038-1039.
4. Muller JE. Circadian variation and triggering of acute coronaryevents. Am Heart J. 1999;137:S1-S8.
5. O'Shea JC, Murphy MB. Ambulatory blood pressure monitoring: which arm? J Hum Hypertens. 2000;14:227-230.
6. Piepho RW. Overview of the angiotensin-converting-enzyme inhibitors. Am J Health Syst Pharm. 2000;57(suppl 1):S3-S7.
7. McCarron D. Twenty-four—hour blood pressure profiles in hypertensive patients administered ramipril or placebo once daily: magnitude and duration of antihypertensive effects: Ramipril Multicenter Study Group. Clin Cardiol. 1991;14:737-742.
8. Heber ME, Brigden GS, Caruana MP, Lahiri A, Raftery EB. First dose response and 24-hour antihypertensive efficacy of the new once-daily angiotensin converting enzyme inhibitor, ramipril. Am J Cardiol. 1988; 62:239-245.
9. Zannad F, Matzinger A, Larche J. Trough/peak ratios of once daily angiotensin converting enzyme inhibitors and calcium antagonists. Am J Hypertens. 1996;9:633-643.
10. MacMahon S, Peto R, Cutler J, Collins R, Sorlie P, Neaton J, Abbott R, Godwin J, Dyer A, Stamler J. Blood pressure, stroke and coronary heart disease, 1: prolonged differences in blood pressure: prospective observational studies corrected for the regression dilution bias. Lancet. 1990;335:764-774.
11. Collins R, Peto R, MacMahon S, Hebert P, Fiebach NH, Eberlein KA, Godwin J, Qizilbash N, Taylor JO, Hennekens CH. Blood pressure, stroke, and coronary heart disease, 2: short term reductions in blood pressure: overview of randomised drug trials in their epidemiological context. Lancet. 1990;335:827-838.
12. Verdecchia P. Prognostic value of ambulatory blood pressure: current evidence and clinical implications. Hypertension. 2000;35:844-851.
13. Verdecchia P, Porcellati C, Schillaci G, Borgioni C, Ciucci A, Battistelli M, Guerrieri M, Gatteschi C, Zampi I, Santucci A. Ambulatory blood pressure: an independent predictor of prognosis in essential hypertension. Hypertension. 1994;24:793-801.
14. Staessen JA, Thijs L, Fagard R, O'Brien ET, Clement D, de Leeuw PW, Mancia G, Nachev C, Palatini P, Parati G, Tuomilehto J, Webster J. Predicting cardiovascular risk using conventional vs ambulatory blood pressure in older patients with systolic hypertension. JAMA. 1999;282:539-546.
15. The design of a large, simple randomized trial of an angiotensinconverting enzyme inhibitor (ramipril) and vitamin E in patients at high risk of cardiovascular events: The HOPE study investigators. Can J Cardiol. 1996;12:127-137.
16. P Owens, E O'Brien. Hypotension in patients with coronary disease: can profound hypotensive events cause myocardial ischaemic events? Heart. 1999;82:477-481.
17. Watanabe N, Imai Y, Nagai K, Tsuji I, Satoh H, Sakuma M, Sakuma H, Kato J, Onodera-Kikuchi N, Yamada M, Abe F, Hisamichi S, Abe K. Nocturnal blood pressure and silent cerebrovascular lesions in elderly Japanese. Stroke. 1996;27:1319-1327.
