Сравнение трех двойных комбинаций на основе платины при распространенном немелкоклеточном раке легкого: рандомизированное испытание по фазе II
СтатьиОпубликовано в журнале: Journal of Clinical Oncology, 20: 4285-4291 (2002)
Г.В. Скалиотти, Ф. Де Маринис, М. Ринальди, Л. Крино, К. Гриделли, С. Риччи, Е. Матано, К. Бони, М. Марангало, Г. Файлла, Г. Альтавилла, В. Адамо, А. Кербелли, М. Клеричи, Ф. Ди Касианцо, Л. Франтини и М. Танато от имени Итальянского проекта по раку легкого
Цель исследования.
Выяснить, будут ли две обычно используемых новых схемы на основе платины давать какие-либо преимущества по сравнению с комбинацией винорелбин/цисплатин (стандартная схема) в отношении процента ответа у больных с распространенным немелкоклеточным раком легкого (НМРЛ).
Больные и методы.
Ранее не получавшие химиотерапии больные были рандомизированы на получение гемцитабина в дозе 1250 мг/м2 в дни 1-й и 8-й плюс цисплатин в дозе 75 мг/м2 в день 2-й, курс повторяли каждый 21 день (группа GC), или на получение паклитаксела в дозе 225 мг/м2 (3-часовое вливание) с последующим вливанием карбоплатина (до AUC 6), оба в день 1-й с интервалом в 21 день (группа PCb), или на введение винорелбина в дозе 25 мг/м2 /неделю на протяжении 12 недель, затем раз в две недели плюс цисплатин в дозе 100 мг/м2 в день 1, один раз в 28 дней (группа VC).
Результаты.
На лечение было рандомизировано 612 больных (205 GC, 204 PCb и 203 VC). Общий процент ответа для схемы GC 30% и PCb 32% достоверно не отличался от результата в группе VC (30%). Не наблюдалось различий в общей выживаемости, времени до прогрессии или времени до отказа лечения. Медианная выживаемость для групп GC, PCb и VC составляла 9,8 месяцев, 9,9 месяцев и 9,5 месяца, соответственно.
Нейтропения была значительно более выраженной в группе VC (GC 17%, PCb 35%, VC 43% курсов, Р<0,001); тромбоцитопения была более выраженной в группе GC (GC 16%, VC 0,1% курсов, Р<0,001). Алопеция и периферическая нейротоксичность отмечались чаще всего в группе PCb, а тошнота/рвота в группе VC (P<0,05).
Вывод.
По эффективности экспериментальные группы и референс-группа существенно не отличались, хотя были обнаружены различия в токсичности. Эти данные указывают на то, что химиотерапия при НМРЛ достигла терапевтического плато.
* * *
Комбинированная терапия на основе цисплатина считается в настоящее время наиболее активным вариантом лечения для больных с местно-распространенным или метастатическим немелкоклеточным раком легкого (НМРЛ) [1-3]. Девяностые годы возвестили появление новых активных препаратов (гемцитабин, винорелбин, таксаны и ингибиторы топоизомеразы I), которые при комбинации с соединениями платины в контексте фазы II давали ответ и процент годичного выживания, превышавший 50% [4]. Четыре рандомизированных клинических испытания определенно продемонстрировали превосходство разных двойных схем на основе цисплатина, включая некоторые из новых препаратов, по сравнению с монотерапией цисплатином с точки зрения общего процента ответа и времени до прогрессии заболевания [5-8], а в случае трех испытаний также медианного времени выживания [5-7]. Другая группа рандомизированных клинических испытаний была посвящена сравнению новых двойных комбинаций с более старыми схемами (например, со схемами цисплатин/эпиподофиллотоксины, митомицин/ифосфамид/цисплатин или цисплатин/виндезин) [9-14]. В большинстве этих исследований новые двойные комбинации дали достоверное увеличение процента объективных ответов, которые, однако, не всегда соответствовали улучшению времени до прогрессии заболевания или общей выживаемости.
Среди новых двойных комбинаций схемы гемцитабин/цисплатин (GC) и паклитаксел/карбоплатин (PCb) широко используются в настоящее время в клинической практике. Соответственно Итальянский проект по раку легкого, включающий 31 медицинское учреждение, провел рандомизированное испытание у ранее не получавших химиотерапии больных с распространенным рецидивирующим и/или метастатическим НМРЛ, в котором главный критерий общего процента ответа сравнивался для двух экспериментальных групп, GC и PCb, и стандартной группы винорелбин/цисплатин (VC).
Из-за повышенного интереса к ощущению больными симптомов заболевания, побочных эффектов лечения и их функциональной значимости, мы также оценили качество жизни с помощью инструмента, специфического в отношении рака легкого – анкеты QLQ-C30-LC13 [15] Европейской организации по исследованию и лечению рака (EORTC).
БОЛЬНЫЕ И МЕТОДЫ
Отбор больных
Больные, удовлетворяющие критериям участия в испытании, должны были иметь местно-распространенный НМРЛ (стадия IIIB или с выпотом в плевру, или с поражением надключичного узла N3), рецидивирующий и/или метастатический (стадия IV). Новообразование должно было быть пригодным для клинической оценки по данным объективной визуализации в соответствии с поставленным патологом (гистологическим или цитологическим) диагнозом НМРЛ. Наличие, по крайней мере, одного измеримого очага в одном направлении было обязательным условием, но предпочтительным было наличие опухоли, измеряемой в двух направлениях. Хотя требовалось, чтобы больные ранее не получали химиотерапии или иммунотерапии, лучевая терапия была разрешена, если ее заканчивали, по крайней мере, за 4 недели до начала испытания (при условии, что облученный очаг не был единственным очагом, где можно было измерять степень поражения), а предшествующая хирургическая операция разрешалась, если больной отвечал все прочим установленным критериям.
Больные должны были иметь функциональный статус по ECOG от 0 до 2, и ожидаемую продолжительность жизни не менее 12 недель. Дополнительные критерии включали достаточный резерв костного мозга (содержание лейкоцитов ≥3,5х109/л, тромбоциты ≥100х109/л, гемоглобин ≥10 г/л и гематокрит ≥30%), а также достаточную функцию печени и почек (креатинин <1,5 раза верхнего предела нормы).
Больных исключали из испытания в случае активной инфекции, симптоматических метастазов в ЦНС, требующих неотложной лучевой терапии и/или применения кортикостероидов, серьезного сопутствующего системного нарушения, второго первичного злокачественного заболевания (за исключением карциномы шейки матки insitu или немеланомного рака кожи) и тяжелых сердечно-сосудистых заболеваний.
Беременные или кормящие грудью в испытании участвовать не могли.
У каждого больного перед записью в испытание после информирования было получено письменное согласие на участие. Испытание проводилось по утверждению соответствующих этических комитетов и в соответствии с рекомендациями высокоэффективной клинической практики. Соблюдались рекомендации Хельсинской Декларации относительно биомедицинских исследований на людях.
Схема испытания и размер выборки
Испытание было предназначено для того, чтобы с 80%-ной уверенностью выявить различия между группами сравнения (GC и PCb) и референс-группой (VC) в отношении процента ответа. Размер требуемой для этого выборки составлял 600 больных, которые должны были быть рандомизированы равными долями в три группы лечения. Этот размер выборки определяли с использованием уровня достоверности 5% для альфа и 20% для бета для проверки гипотезы о том, что все три группы лечения являются одинаковыми, по отношению к альтернативной гипотезе, заключавшейся в том, что процент ответа в группах сравнения на 15% лучше по сравнению с эталонной группой.
Рандомизацию проводили централизованно, и больных стратифицировали по трем прогностическим переменным: стадия заболевания (местно-распространенное или метастатическое заболевание), функциональный статус (исходный функциональный статус по ECOG, равный 0-1 или 2) и учреждение, где проводилось исследование.
Больные были сбалансированы по отношению к лечению в каждой из стратифицированных групп и в отношении каждого фактора с использованием алгоритма, описанного Pocock и Simon [16].
График лечения
В группе GC больные получали гемцитабин в дозе 1250 мг/м2 внутривенно (в/в) в дни 1-й и 8-й и цисплатин в дозе 75 мг/м2 (с соответствующей гидратацией и использованием антиэметиков) на 2-й день 21-дневного курса лечения. В группе PCb больные получали паклитаксел в дозе 225 мг/м2 в форме 3-часового вливания, а затем карбоплатин внутривенно в дозе, соответствующей площади под кривой AUC 6 по формуле Кальверта (17), оба препарата в 1-й день 21-дневного курса лечения. В группе VC больные получали винорелбин в дозе 25 мг/м2 в дни 1-й, 8-й, 15-й и 22-й в форме 30-минутного внутривенного вливания и цисплатин в дозе 100 мг/м2 внутривенно (при соответствующей гидратации и использовании антиэметиков) в 1-й день 28-дневного курса лечения. После 12 недель лечения винорелбин вводили раз в две недели.
Больные, достигшие стабилизации заболевания, получали максимум шесть курсов лечения, в то время как больные, давшие объективный ответ (полный или частичный) продолжали лечение по усмотрению врача-исследователя в течение двух дополнительных курсов, всего до восьми курсов. Больные с прогрессирующим заболеванием или неприемлемой токсичностью, или больные, которые не могли получать препарат в течение 6 недель с момента предшествующего введения, были исключены из дальнейшего испытания. Корректировки доз в пределах курса проводились на основе абсолютного содержания нейтрофилов и содержания тромбоцитов в день лечения и на основании оценки негематологической токсичности.
Исходная оценка и оценки в ходе лечения
Перед началом испытания для каждого больного составляли историю болезни, проводили физическое обследование, измерение пальпируемых или визуализируемых очагов опухоли, делали рентгеновский снимок грудной клетки, определяли полное содержание форменных элементов крови, проводили биохимический анализ крови, анализ мочи, снимали ЭКГ, определяли жизненные признаки и рассчитывали креатининовый клиренс. Дополнительные оценки до испытания включали радиологические исследования (КТ-сканирование или магнитно-резонансную визуализацию), если это было необходимо для измерения опухоли или если клинические или лабораторные данные говорили о признаках заболевания в локализации, которая была недоступна с помощью других методов визуализации. Тот же метод оценки, который использовался для определения статуса заболевания на исходный момент, в последующем использовался для оценки эффективности лечения в ходе испытания.
Перед каждым курсом больные заполняли анкету QLQ-C30-LС13 и подвергались ограниченному опросу в отношении истории болезни, физического обследованию (включая измерение опухоли) и делали рентгеновский снимок грудной клетки. Во время каждого цикла больным проводили биохимический анализ крови в 1-й день и полный анализ форменных элементов крови еженедельно. Кроме того, для больных в группах GC и VC рассчитывался креатининовый клиренс в 1-й день каждого курса. В конце каждого курса проводили оценку больных в отношении токсичности в соответствии с критериями токсичности Национального института рака (версия 2.0).
Перед каждым вторым курсом лечения больным проводили радиологическую визуализацию для оценки статуса заболевания. Все больные, получившие, по крайней мере, два курса лечения, считались пригодными для оценки в отношении объективного ответа со стороны опухоли. Объективный ответ опухоли оценивался с помощью стандартных критериев ВОЗ. Для опухолей, которые можно было измерить в одном направлении, частичный ответ определялся как уменьшение от исходного значения на ≥70% в отношении максимального диаметра опухоли, а прогрессирующее заболевание определялось как увеличение по отношению к исходному моменту более, чем на 30%.
все больные, давшие полный или частичный ответ, должны были быть повторно исследованы через 4 недели после первой документации ответа. Для верификации объективных ответов КТ-сканы в дальнейшем представлялись в независимую онкологическую группу для верификации.
Продолжительность объективного (полного или частичного) ответа измерялась с момента, когда ответ был впервые документирован до даты прогрессии заболевания.
Общую выживаемостьрасчитывали, начиная с даты рандомизации до даты смерти.
Время до отказа лечения определялось как период с момента рандомизации до прогрессии заболевания или до прекращения лечения из-за смерти больного или вызванной препаратом токсичности. Все рандомизированные больные, вошедшие в испытание, оценивались в отношении безопасности.
Статистический анализ Анализ выполнялся на данных, полученных от всех больных, включенных в испытание и получивших лечение. Оценка времени до наступления события, считавшегося критерием, проводилась с помощью метода Каплана-Мейера [18], оценки сравнивали с помощью лог-рангового критерия. Сравнение ответов проводилось с помощью критерия χ2 по Пирсону. Влияние исходных факторов (функциональный статус, метастазы в мозг, плоскоклеточная гистология, число мест метастазирования и стадия заболевания) оценивалось в отношении критерия времени до наступления события с использованием модели пропорциональных рисков по Коксу, их влияние на ответ анализировалось с помощью логистической регрессии. Факторы, которые казались имеющими индивидуальное прогностическое значение в моделях с одной переменной, оценивались на совместную прогностическую ценность в модели с множественными переменными. Окончательная модель была создана на основании стратегии обратной селекции. Лечение добавлялось к окончательной модели для оценки эффекта лечения после корректировки на наличие важных прогностических факторов.
Каждая шкала анкеты QLQ-C30-LC13 анализировалась путем анализа дисперсии (однонаправленной). Оценивались различия между начальным моментом и концом второго курса для каждой из шкал, а также то, остается ли обнаруженное различие в конце четвертого курса. Если имелось общее различие, связанное с лечением (P<0,05), проводились сравнения для каждых из экспериментальных групп с контрольной группой (группа VC).
РЕЗУЛЬТАТЫ
Демографические характеристики больных и характеристики заболевания
В период с августа 1998 по май 2000 г.г. в испытание было включено 612 больных. Из этих больных трое в группе PCb и двое в группе VC прошли рандомизацию, но не получили лечения. Демографические характеристики больных и характеристики заболевания исходно для 607 больных, получивших лечение (205 GC, 201 PCb и 201 VC), были хорошо сбалансированы для групп лечения (Таблица 1). Большинство больных со стадией заболевания IIIB имели поражение N3 (30 GC, 35 PCb и 35 VC), и лишь у немногих имел место выпот в плевру.
Таблица 1. Демографические характеристики больных и характеристики заболевания
|
Переменная |
GC |
PCb |
VC |
|||
|
Число |
% |
Число |
% |
Число |
% |
|
|
Число пролеченых больных |
205 |
201 |
201 |
|||
|
Мужчины |
167 |
81 |
152 |
76 |
157 |
78 |
|
Возраст (годы) |
||||||
|
|
63 |
62 |
63 |
|||
|
|
28-81 |
30-77 |
38-78 |
|||
|
Функциональный статус по ECOG 0-1 |
194 |
95 |
184 |
92 |
185 |
92 |
|
Предшествующая хирургия |
16 |
8 |
16 |
8 |
12 |
6 |
|
Гистология |
||||||
|
|
103 |
50 |
96 |
48 |
111 |
55 |
|
|
67 |
33 |
65 |
32 |
55 |
27 |
|
|
13 |
6 |
20 |
10 |
12 |
6 |
|
|
22 |
11 |
20 |
10 |
23 |
12 |
|
Степень дифференциации |
||||||
|
|
9 |
5 |
11 |
5 |
6 |
3 |
|
|
29 |
14 |
30 |
15 |
25 |
13 |
|
|
50 |
24 |
65 |
32 |
66 |
32 |
|
|
8 |
4 |
9 |
5 |
6 |
3 |
|
|
109 |
53 |
86 |
43 |
99 |
49 |
|
|
167 |
81 |
164 |
82 |
163 |
81 |
|
Количество очагов метастатического заболевания |
||||||
|
|
124 |
74 |
118 |
72 |
109 |
67 |
|
|
35 |
21 |
35 |
21 |
46 |
28 |
|
|
8 |
5 |
11 |
7 |
8 |
5 |
|
Очаги метастатического заболевания |
||||||
|
|
81 |
49 |
66 |
40 |
68 |
42 |
|
|
31 |
19 |
27 |
16 |
24 |
15 |
|
|
21 |
13 |
26 |
16 |
30 |
18 |
|
|
40 |
24 |
45 |
27 |
45 |
28 |
|
|
30 |
18 |
30 |
18 |
37 |
23 |
Ответ и время до наступления события Данные по ответу опухоли на лечение приведены в Таблице 2. Общие значения процента ответа для групп GC 30% и PCb 32% существенно не отличались от ответа в группе VC (30%) (сравнение GC с VC, Р=0,982; сравнение PCb с VC, Р=0,747), хотя в группе VC больший процент больных (23%) не мог быть оценен в отношении ответа опухоли по сравнению с группой GC (13%) или PCb (14%) (P<0,02). Не наблюдалось достоверных отличий между экспериментальными группами и референс-группой в отношении медианной продолжительности ответа (GC 9,4 или PCb 8,7 месяцев по сравнению с VC 8,2 месяца, P>0,14).
Таблица 2. Процент ответа
|
|
GC |
PCb |
VC |
|||
|
|
Число |
% |
Число |
% |
Число |
% |
|
Рандомизированных больных |
205 |
204 |
203 |
|||
|
Пролеченых больных |
205 |
201 |
201 |
|||
|
ПО |
0 |
1 |
0,5 |
1 |
0,5 |
|
|
ЧО |
62 |
30 |
63 |
31 |
60 |
30 |
|
Стабильное заболевание |
81 |
40 |
75 |
37 |
62 |
31 |
|
Прогрессия заболевания |
36 |
18 |
3 |
18 |
34 |
17 |
|
Не оценено |
26 |
13* |
28 |
14* |
46 |
23 |
|
Общий процент ответа |
30 |
32 |
30 |
|||
|
95%-ный ДИ |
24-37 |
25-38 |
24-36 |
|||
Сокращения: ПО=полный ответ; ЧО=частичный ответ
*Достоверное отличие от группы VC (P<0,02, тест χ2).
Общий ответ опухоли в группах GC, PCb и VC по стадиям заболевания составлял 39%, 24% и 26%, соответственно, для стадии III и 28%, 34% и 31%, соответственно, для стадии IV. Соответствующие значения общего процента ответа у больных с метастазами в мозг составляли 32%, 52% и 25%.
Результаты по эффективности, выраженные в виде времени до наступления события, приведены в Таблице 3. Медианные значения времени наблюдения для этих анализов составляли 8,8 месяца (95%-ный доверительный интервал [ДИ] от 8,0 до 9,7 месяца) для GC, 9,3 месяца (95%-ный ДИ от 8,2 до 10,2 месяца) для PCb и 8,7 месяцев (95%- ный ДИ от 8,1 до 9,7 месяцев) для VC. Не наблюдалось различий между экспериментальными группами и референс-группой в отношении общей выживаемости, времени до прогрессии и времени до отказа лечения. На Рис. 1 представлены кривые для общей выживаемости по Каплану-Мейеру в зависимости от группы лечения. Медианные значения времени выживания для групп GC, PCb и VC составили 9,8 месяца, 9,9 месяца и 9,5 месяцев, соответственно. Соответствующие проценты выживания на срок в 1 год составляли 37%, 43% и 37% (сравнение GC и VC Р=0,484; сравнение PCb и VC Р=0,105). На момент проведения анализа скончалось 450 больных (150 GC, 148 PCb и 152 VC), что дает цензурированный процент по выживаемости, равный 26,8%, 26,4% и 24,4%, соответственно. Кривые по Каплану- Мейеру для времени до прогрессии заболевания и времени до отказа лечения в зависимости от группы лечения приведены на Рис. 2.
Многофакторный анализ показал, что функциональный статус (ECOG), равный 2, и наличие более чем двух очагов метастазирования являются отрицательными прогностическими факторами для общей выживаемости, времени до прогрессии заболевания и времени до отказа лечения. При введении поправки на эти факторы не наблюдалось влияния лечения на общую выживаемость (отношение риска [ОР] 0,92 для НС и 0,87 для PCb), время до прогрессии заболевания (ОР 1,01 для GC и 0,96 для PCb) или времени до отказа лечения (ОР 0,91 для GC и 0,89 для PCb) (Таблица 3).
Наличие метастазов в мозг было исключено в качестве независимого отрицательного прогностического фактора.
Токсичность
Гематологическая токсичность степени 3/4 по курсам лечения приведена в Таблице 4.
Для групп GC и PCb процент курсов с нейтропенией степени 3/4 (17% и 35%, соответственно) и анемией (6% и 2%, соответственно) были меньшим, чем в группе VC (43% и 7%, P<0,001), в то время как частота тромбоцитопении степени 3/4 была более высокой в опытных группах (16% и 3% по сравнению с 0,1%, P<0,001). Ни в одной из групп не отмечалось серьезных проблем, связанных с кровотечениями. Число больных с фебрильной нейтропенией (1 GC, 2 PCb и 6 VC) было низким и сходным для разных групп, в то время как переливание эритроцитарной массы проводились значительно реже в группе PCb (P<0,01). Процент больных, получавших переливание тромбоцитов, для каждой группы (GC 8%, PCb 2% и VC 8%) не соответствовал проценту больных с тромбоцитопенией степени 3/4.
При выражении данных в процентном отношении к больным (Таблица 4), нейтропения и тромбоцитопения также были достоверно ниже в опытных группах по сравнению с группой VC (P<0,05), в то время как для анемии выявилось достоверное различие только для группы PCb (меньше, чем в группе VC, P<0,001). Данные по негематологической токсичности степени 3/4 (максимальная тяжесть) приведены в Таблице 5. Тошнота/рвота чаще отмечалась в группе VC (13%), чем в каждой из двух других групп (GC 7%, PCb 0,5%, P<0,05). Частота алопеции (степень 1/2) и периферической нейропатии (степень 1-3), которая была максимальной в группе PCb (52% и 30%, соответственно), была достоверно более высокой, чем в группе VC (11% и 7%, соответственно; P<0,05).
На протяжении первых двух курсов лечения скончалось 32 больных (5,2%). Причем 14 скончались от причин, не связанных с применением препаратов (пять больных в группе GC, пять больных в группе PCb и четыре больных в группе VC), и 18 больных скончалось от причин, связанных с лекарственными препаратами (восемь больных в группе GC, три больных в группе PCb и семь больных в группе VC). За этот же период отмечалось восемь эпизодов почечной недостаточности степени 3 или 4 (один в группе GC и семь в группе VC); а 17 (2,8%) серьезных побочных эффектов (VCе из них сосудистые), отнесенных врачами-исследователями к категории умеренных/тяжелых, распределились следующим образом: четыре эпизода (один в группе GC, два в группе PCb и один в группе VC) тромбоза глубоких вен, один случай массивной легочной эмболии (VC), три эпизода церебральной ишемии (VCе в группе GC), три случая инфаркта миокарда (один в группе GC, один в группе PCb и один в группе VC) и шесть эпизодов остановки сердца или сердечно-сосудистой недостаточности (один в группе GC, два в группе PCb и три в группе VC).
Проведение лечения
Предписанное лечение завершило всего 115 больных (45 в группе GC, 47 в группе PCb и 23 в группе VC). Большинство больных, прекративших участие в испытании, сделали это из-за прогрессии заболевания (80 в группе GC, 76 в группе PCb и 95 в группе VC).
Общее число курсов лечения для групп GC, PCb и VC составило 825 (в среднем на больного 4,0), 851 (в среднем на больного 4,2) и 653 (в среднем на больного 3,2), соответственно. Для больных в группе VC процент снижения доз было максимальным (17%), как и процент пропуска доз (19%), главным образом, из-за гематологической токсичности. Процент снижения и пропуска доз составлял 12,6% для группы GC и 13,0% для группы PCb, соответственно. Фактические интенсивности дозы составляли 90,6% для гемцитабина, 100% для цисплатина (с гемцитабином), 74% для винорелбина, 94,8% для цисплатина (с винорелбином), 94,7% для паклитаксела и 99,2% для карбоплатина.
Таблица 5. Негематологическая токсичность степени 3/4 (% больных с токсическими эффектами)
|
Токсичность |
GC (n=197) |
PCb (n=197) |
VC (n=198) |
|
Алопеция (степень 1/2) |
9,6/0,5 |
50,8/1,5* |
11,1/0 |
|
Тошнота/рвота |
5,6/1* |
0,5/0* |
11,1/1,5 |
|
Периферическая нейропатия (степень 1/2/3) |
4/0/0 |
22,8/7/0* |
4/2,5/0,5 |
|
Запор |
0,5/0 |
0/0* |
2,5/0,5 |
|
Почечная |
0/0,5 |
0/0 |
1,5/3,5 |
|
Сердечно-сосудистая |
0,5/2,5 |
1,0/1,5 |
0,5/2,5 |
|
Кожная |
0,5/0 |
0/0 |
0,5/0 |
Качество жизни
Процент заполнения анкет QLQ-C30-LC13 на исходный момент был высоким, однако в последующие курсы процент заполнения анкет больными, продолжавшими получать лечение, снижался. Процент заполнения в ходе испытания приведен в Таблице 6.
Таблица 6. Процент заполнения анкет по качеству жизни (% больных, заполнивших анкеты)
|
Время |
VC |
GC |
PCb |
|||
|
Число |
% |
Число |
% |
Число |
% |
|
|
Исходно |
205 |
94,6 |
201 |
94,0 |
201 |
93,0 |
|
Конец курса 2 |
184 |
75,5 |
181 |
78,4 |
167 |
71,9 |
|
Конец курса 4 |
132 |
67,4 |
138 |
76,8 |
99 |
60,6 |
После двух курсов лечения только шесть функциональных шкал и шкал симптомов QLQ-C30-LC13 обнаружили различия, связанные с лечением: ролевое функционирование (способность больных работать или участвовать в досуге), чувство усталости, тошнота/рвота, анорексия, периферическая нейропатия и алопеция.
Дальнейший анализ показал, что не наблюдалось статистически достоверных различий между группами GC и VC. Однако группа PCb достоверно отличалась от группы VC по таким признакам, как ролевое функционирование, чувство усталости, тошнота/рвота и анорексия – преимущество было в группе PCb, а также для периферической нейропатии и алопеции, где преимущество было в группе VC. Когда аналогичный анализ был проведен после четырех курсов лечения, единственными шкалами, давшими связанные с лечением различия, были шкалы боли, тошноты/рвоты, периферической нейропатии и алопеции. Дальнейший анализ показал статистическое различие между группами GC и VC в отношении периферической нейропатии в пользу группы GC. Этот анализ также выявил статистические различия между группами PCb и VC в отношении боли, периферической нейропатии и алопеции, во всех случаях лучшие результаты были в группе VС. Существенные параметры, взятые после второго курса, приведены на Рис. 3. Эти же параметры показаны для четвертого курса, чтобы проиллюстрировать, являлись ли различия, связанные с лечением, устойчивыми.
Только тошнота/рвота, периферическая нейропатия и алопеция обнаружили устойчивые различия, связанные с лечением.
Лечение после испытания Всего 124 больных (20%) (43 в группе GC, 47 в группе PCb и 34 в группе VC) получали лучевую терапию, а 220 больных (36%) (76 в группе GC, 76 в группе PCb и 68 в группе VC) получали химиотерапию после завершения участия в испытании. Для группы GC большинство из тех (75%), кто получал химиотерапию после испытания, лечились схемами на основе винорелбина или таксана, а в группах PCb и VC большинство получали лечение на основе гемцитабина (72% и 74%, соответственно).
ОБСУЖДЕНИЕ
При распространенном НМРЛ химиотерапия на основе цисплатина улучшает результаты по выживаемости, смягчает симптоматику и является экономически эффективной. Несмотря на эти обнадеживающие данные, большинство врачей далеки от того, чтобы считать химиотерапию стандартным подходом для лечения своих больных.
Два других крупномасштабных, имеющих достаточные размеры кооперативных исследования, а именно ECOG 1594 (19) и SWOG 9509 (20), уже исследовали терапевтические возможности более новых схем лечения у больных с распространенным НМРЛ. В испытании SWOG с четырьмя группами по сравнению комбинации GC, доцетаксела/цисплатина и паклитаксела(3 часа)/карбоплатина с паклитакселом(24 часа)/цисплатином, выживаемость в экспериментальных группах (от 7,4 до 8,2 месяца) достоверно не отличалась от выживаемости в контрольной группе (7,8 месяцев), за исключением времени до прогрессии заболевания в группе GC, которое было достоверно выше, чем в контрольной группе (4,2 и 3,4 месяца, соответственно; Р=0,001). В испытании SWOG контрольная схема VC сравнивалась со схемой PCb, эквивалентной той, которая использовалась в испытании ECOG.
Характеристики больных по существу были близкими к характеристикам больных в испытании ECOG. В этом случае также не было отмечено различий между группами в отношении каких-либо критериев, связанных с эффективностью.
В настоящем крупномасштабном многоцентровом рандомизированном испытании, проведенном Итальянским проектом по раку легкого, сравнение двух двойных схем последнего поколения – GC и PCb – с эталонной схемой VC продемонстрировало значительную активность с точки зрения общего процента ответа, медианной выживаемости, выживаемости за 1 год, времени до прогрессии и времени до отказа лечения. Более высокие проценты ответа и лучшие приблизительно на 2 месяца медианные значения выживаемости по сравнению с тем, что наблюдалось в испытаниях ECOG и SWOG, вероятно, можно связать с меньшим процентом больных со стадией IV, включенных в наше испытание (около 80% в нашем испытании и 90% в ECOG 1594 и 89% в SWOG 9509).
Предполагалось, что возможным объяснением отсутствия каких-либо преимуществ в выживаемости между экспериментальными и эталонными группами ECOG 1594 и SWOG 9509 является терапия второй линии, однако, к сожалению, эти данные не отражены в названных испытаниях. В нашем испытании большая часть больных, получивших терапию первой линии в группах PCb и VC, получали на момент рецидива лечение, основанное на гемцитабине. Среди больных, получавших химиотерапию после испытания в группе GC, половина получала таксан, а другая половина винорелбин. Сходство между тремя группами лечения в отношении медианного времени до отказа лечения, времени до прогрессии и общей выживаемости ставит под вопрос возможность какого-либо позитивного воздействия терапии второй линии.
Общий профиль токсичности для группы VC был более выраженным, чем в экспериментальных группах: достоверно более высокое число больных не могло быть оценено на ответ на время второго курса (23% в группе VC, 13% в группе GC и 14% в группе PCb; P<0,02) из-за прекращения участия в испытании в связи с побочными эффектами или с прогрессией заболевания. Кроме того, меньший процент больных в группе VC завершил четыре курса или полный курс химиотерапии (40% и 25%, соответственно, по сравнению с 59% и 37% для группы GC и 62% и 46% для группы PCb).
Нейтропения степени 3/4 чаще отмечалась в случае использования схемы VC, и шесть из девяти эпизодов фебрильной нейтропении были описаны именно в этой группе.
Тромбоцитопения степени 3/4 чаще отмечалась в группе GC и выявлялась только при еженедельной оценке содержания форменных элементов крови, однако она не была связана с какими-либо серьезными эпизодами кровотечений. Более того, частота тромбоцитопении в группе GC была значительно меньшей по сравнению с тем, что было описано в предыдущих испытаниях, где использовался 4-недельный график введения [11, 12, 20, 21]. Несоответствие между тромбоцитопенией и данными по трансфузиям тромбоцитов для каждой группы непонятно, однако может отражать различия в критериях в отношении проведения трансфузии или различный уровень профессионализма при лечении токсических эффектов, связанных с кровью.
В группе PCb отмечалась наибольшая частота алопеции (степень 1/2 у 52% больных) и периферической нейропатии (степень 1-3 у 30% больных), а в группе VC максимальной была частота тошноты/рвоты (степень 3/4 у 13% больных). Последний токсический эффект мог быть связан с более высокой дозой цисплатина в день 1 (100 мг/м2) в отличие от дозы 75 мг/м2, применявшейся в группе GC, однако такие дозы были выбраны для обеспечения одинаковой интенсивности дозы цисплатина в обеих группах. В группе PCb периферическая нейропатия степени более 2, носила кумулятивный характер, варьируя от 17% во время второго курса до 32% во время шестого курса. Процент нейротоксичности (7%, максимальная степень) в группе PCb близок к соответствующему проценту, описанному в испытаниях SWOG (12%) и ECOG (10%), где исследователи использовали аналогичный график введения.
Результаты в отношении качества жизни указывают на небольшие различия между группами VC и GC. Хотя результаты после двух курсов лечения говорят в пользу группы PCb по сравнению с группой VC, результаты после четырех курсов указывают на преимущество группы VC. Использование анкеты в конце цикла лечения, возможно, не смогло выявить эффекты острой токсичности на качество жизни. Кроме того, пониженный процент возврата анкеты, возможно, ограничил статистическую возможность демонстрации различий, особенно в ходе более поздних курсов. Другие рандомизированные испытания не смогли продемонстрировать достоверных различий в качестве жизни между группами лечения по аналогичным причинам [10-12, 20].
Настоящее испытание не смогло продемонстрировать терапевтического преимущества ни одной из экспериментальных схем по сравнению с эталонной схемой с точки зрения выживаемости и ответа на лечение. Этот результат полностью соответствует результатам испытаний ECOG и SWOG и представляет дополнительный аргумент в пользу того, что все эти схемы представляют собой разумные варианты выбора для больных с распространенным НМРЛ. Несмотря на то, что настоящее испытание не смогло продемонстрировать каких-либо преимуществ в отношении процента ответа, выживаемости и качества жизни для двух экспериментальных схем, группа VC характеризовалась более высокой токсичностью, достоверно меньшим процентом больных, доступных для оценки, и меньшим средним числом курсов лечения, несмотря на модификацию схемы с целью ограничить токсичность, описанную в предшествующих рандомизированных испытаниях [9, 20]. Эти потенциальные ограничения могут уменьшать ценность VC в качестве референс-группы в будущих испытаниях. Альтернативные графики (например, меньшие дозы цисплатина или введение винорелбина в дни 1-й и 8-й раз в 3 недели) требуют верификации в контексте фазы III.
Весьма вероятно, что эффективность химиотерапии при НМРЛ достигла плато, что подчеркивает неопределенность того, насколько можно рассчитывать на получение лучших результатов путем добавления третьего препарата или изменения последовательности применения имеющихся активных препаратов. Новые стратегии, включающие комбинированную химиотерапию с использованием новых биологических агентов, представляются перспективным направлением. Поскольку в настоящее время для НМРЛ появляются такие агенты, все с нетерпением ожидают результатов идущих рандомизированных испытаний.
Таблица 3. Резюме результатов по сроку до события
|
Критерий |
GC |
PCb |
VC |
Эффект лечения |
Эффект лечения |
||||||
|
ОР** |
95% ДИ |
ОР** |
95% ДИ |
||||||||
|
GC |
PCb |
GC |
PCb |
GC |
PCb |
GC |
PCb |
||||
|
Общая выживаемость |
0,87 |
0,84 |
0,69-1,09 |
0,67-1,05 |
0,92 |
0,87 |
0,74-1,16 |
0,69-1,09 |
|||
|
Медиана |
9,8 мес |
10,0 мес |
9,5 мес |
||||||||
|
95% ДИ |
8,6-11,2 |
9,0-12,5 |
8,3-11,0 |
||||||||
|
Время до прогрессии заболевания |
0,95 |
0,91 |
0,77-1,17 |
0,74-1,12 |
1,01 |
0,96 |
0,82-1,25 |
0,78-1,19 |
|||
|
Медиана |
5,3 мес |
5,5 мес |
4,6 мес |
||||||||
|
95% ДИ |
4,4-6,3 |
4,6-6,4 |
3,9-5,6 |
||||||||
|
Время до отказа лечения |
0,85 |
0,85 |
0,69-1,04 |
0,69-1,04 |
0,91 |
0,89 |
0,74-1,12 |
0,73-1,10 |
|||
|
Медиана |
4,6 мес |
4,6 мес |
3,8 мес |
||||||||
|
95% ДИ |
4,0-5,4 |
2,9-5,5 |
3,0-4,4 |
||||||||
*См. в тексте детали по прогностическим факторам.
**ОР для события в группе GC или PCb по сравнению с группой VC
Таблица 4. Гематологическая токсичность степени 3/4 в процентах к числу курсов и в процентах к числу больных
|
% курсов с токсическими эффектами |
||||||||
|
GC |
PCb |
VC |
||||||
|
|
Все курсы (n=885) |
Курс 1 (n=197) |
Все курсы (n=898) |
Курс 1 (n=194) |
Все курсы (n=712) |
Курс 1 (n=198) |
||
|
Нейтропения |
13,7/2,9* |
12,7/3,1* |
22,6/11,9* |
13,4/6,2* |
22,9/20,5 |
23,7/27,8 |
||
|
Тромбоцитопения |
10,6/5,5* |
14,2/6,6* |
1,9/1,0* |
1,6/0,5** |
0/0,1 |
0/0 |
||
|
Анемия |
5,0/0,5 |
2,0/1,0 |
2,2/0,1* |
0,5/0 |
6,7/0,7 |
3,0/0 |
||
|
|
% больных с токсическими эффектами (наиболее высокой степени) |
|||||||
|
|
(GC (n=197) |
PCb (n=194) |
VC (n=198) |
|||||
|
Нейтропения |
30,0/8,1* |
24,4/25,9** |
22,7/41,9 |
|||||
|
Тромбоцитопения |
19,3/17,3* |
4,1/3,6* |
0/0,5 |
|||||
|
Анемия |
15,7/2,0 |
6,1/0* |
17,2/2,0 |
|||||
*Достоверное различие для группы VC для степени 3 и 4 совместно (P<0,001, критерий χ2) Литература
**Достоверное различие группы VC в отношении степени 3 и 4 совместно (P<0,05, критерий χ2)
1. Ihde DC: Chemotherapy of lung cancer. N Engl J Med 327:1434-1441, 1992
2. Bunn PA Jr: The treatment of non-small cell lung cancer: Current perspectives and controversies, future directions. Semin Oncol 21:49-59, 1994
3. Non-Small Cell Lung Cancer Collaborative Group: Chemotherapy in non-small cell lung cancer: A meta-analysis using updated data on individual patients from 52 randomised clinical trials. BMJ 311:899-909, 1995
4. Lilenbaum R, Green MR: Novel chemotherapeutic agents in the treatment of non-small-cell lung cancer. J Clin Oncol 11:1391-1402, 1993
5. Sandler AB, Nemunaitis J, Denham C, et al: Phase III trial of gemcitabine plus cisplatin versus cisplatin alone in patients with locally advanced or metastatic non-small-cell lung cancer. J Clin Oncol 18:122-130, 2000
6. Wozniak AJ, Crowley JJ, Balcerzak SP, et al: Randomized trial comparing cisplatin with cisplatin plus vinorelbine in the treatment of advanced non-small-cell lung cancer: A Southwest Oncology Group study.J Clin Oncol 16:2459-2465, 1998
7. von Pawel J, von Roemeling R, Gatzemeier U, et al: Tirapazamine plus cisplatin versus cisplatin in advanced non-small-cell lung cancer: A report of the international CATAPULT I study group—Cisplatin and tirapazamine in subjects with advanced previously untreated non-small-cell lung tumors.J Clin Oncol 18:1351-1359, 2000
8. Gatzemeier U, von Pawel J, Gottfried M, et al: Phase III comparative study of high-dose cisplatin versus a combination of paclitaxel and cisplatin in patients with advanced non-small cell lung cancer. J Clin Oncol 18:3390-3399, 2000
9. Le Chevalier T, Brisgand D, Douillard JY, et al: Randomized study of vinorelbine and cisplatin versus vindesine and cisplatin versus vinorel-bine alone in advanced non-small-cell lung cancer: Results of a multi-center European trial including 612 patients. J Clin Oncol 12:360-367, 1994
10. Crino` L, Scagliotti GV, Ricci S, et al: Gemcitabine and cisplatin versus mitomycin, ifosfamide, and cisplatin in advanced non-small-cell lung cancer: A randomized phase III study of the Italian Lung Cancer Project.J Clin Oncol 17:3522-3530, 1999
11. Cardenal F, Lopez-Cabrerizo MP, Anton A, et al: Randomized phase III study of gemcitabine-cisplatin versus etoposide-cisplatin in the treatment of locally advanced or metastatic non–small-cell lung cancer. J Clin Oncol 17:12-18, 1999
12. Bonomi P, Kim K, Fairclough D, et al: Comparison of survival and quality of life in advanced non-small-cell lung cancer patients treated with two dose levels of paclitaxel combined with cisplatin versus etoposide with cisplatin: Results of an Eastern Cooperative Oncology Group trial. J Clin Oncol 18:623-631, 2000
13. Giaccone G, Splinter TA, Debruyne C, et al: Randomized study of paclitaxel-cisplatin versus cisplatin-teniposide in patients with advanced non-small-cell lung cancer: The European Organization for Research and Treatment of Cancer Lung Cancer Cooperative Group. J Clin Oncol 16:2133-2141, 1998
14. Belani CP, Natale RB, Lee JS, et al: Randomized phase III trial comparing cisplatin/etoposide versus carboplatin/paclitaxel in advanced and metastatic non-small cell lung cancer (NSCLC). Proc Am Soc Clin Oncol 17:455a, 1998 (abstr 1751)
15. Bergman B, Aaronson NK, Ahmedzai S, et al: The EORTC QLQ-LC13: A modular supplement to the EORTC Core Quality of Life Ques-tionnaire (QLQ-C30) for use in lung cancer clinical trials. Eur J Cancer 30A:635-642, 1994
16. Pocock S, Simon R: Sequential treatment assignment with balancing of prognostic factors in the controlled clinical trial. Biometrics 31:103-115, 1975
17. Calvert AH, Newell DR, Gumbrell LA, et al: Carboplatin dosage: Prospective evaluation of a simple formula based on renal function. J Clin Oncol 7:1748-1756, 1989
18. Kaplan EL, Meier P: Nonparametric estimation from incomplete observations. J Am Stat Assoc 53:457-481, 1959
19. Schiller JH, Harrington D, Belani C, et al: Comparison of four chemotherapy regimens for advanced non-small cell lung cancer. N Engl J Med 346:92-98, 2002
20. Kelly K, Crowley J, Bunn PA Jr, et al: Randomized phase III trial of paclitaxel plus carboplatin versus vinorelbine plus cisplatin in the treatment of patients with advanced non-small-cell lung cancer: A Southwest Oncology Group trial. J Clin Oncol 19:3210-3218, 2001
21. Rinaldi M, Crino` L, Scagliotti GV, et al: A three-week schedule of gemcitabine-cisplatin in advanced non-small-cell lung cancer with two different cisplatin dose levels: A phase II randomized trial. Ann Oncol 11:1295-1300, 2000
Рис. 1. Общие кривые выживаемости для групп GC, PCb и VC 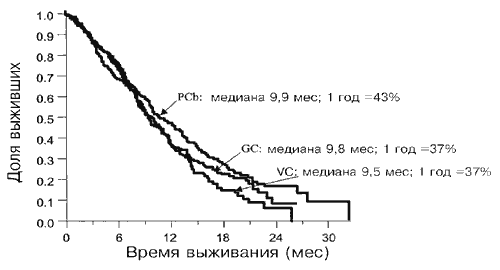
Рис. 2. (А) Кривые времени до прогрессии заболевания для групп GC, PCb и VC. (B) Кривые времени до отказа лечения для групп GC, PCb и VC 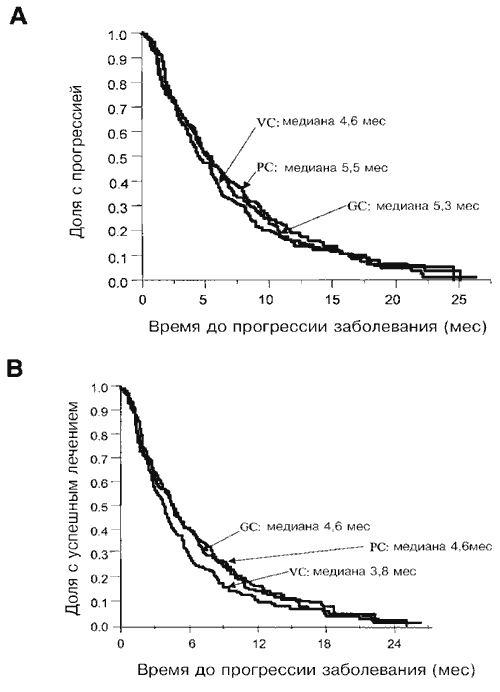
Рис. 3. Важные параметры качества жизни после двух циклов с последующей оценкой после четырех циклов. V2 и V4 для VC, G2 и G4 для GC, P2 и P4 для PCb. 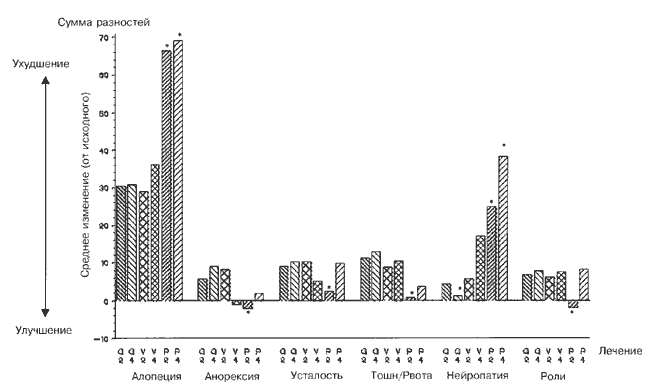
*Значения ролевого функционирования инвертированы, чтобы отразить положительные результаты как ухудшение. Достоверное отличие (P<0,05) от контрольной группы.
