Экономические аспекты профилактики лекарственных осложнений
СтатьиА.Е. Каратеев
ГУ Институт ревматологии РАМН, Москва
Любое эффективное терапевтическое вмешательство, затрагивающее те или иные функции человеческого организма, неизбежно приводит к изменениям физиологии в целом, создавая предпосылки для развития нежелательных эффектов.
Со стороны общества к проблеме безопасности лечения в последнее время приковано очень большое внимание, и все лекарственные препараты и методы терапии тщательно оцениваются с позиции баланса между прямым лечебным действием и возможным риском осложнений. Это обосновывается стремлением защитить права пациента, снизить угрозу его жизни и здоровью из-за возможных ятрогенных осложнений, а также повысить бдительность лечащих врачей в отношении этой патологии. Кроме того, нежелательные эффекты лекарственной терапии - это не только угроза здоровью больного (хотя этот аспект, несомненно, наиболее важен), но и существенные материальные затраты на диагностику и лечение подобных осложнений, которые ложатся серьёзным бременем на общество.
Принципиальным моментом, связанным с проблемой нежелательных эффектов лекарств, является то, что в подавляющем большинстве случаев эти осложнения являются предсказуемыми и потенциально предотвращаемыми, т. е. их развитие связано с ошибками назначения или использования препаратов.
В 2003 г. J. Gurwitz и сотр. в США провели исследование частоты и характера нежелательных эффектов, развившихся в группе 30 397 амбулаторных больных с различными заболеваниями за 12-месячный период (1999-2000 гг.). Всего было выявлено 1523 подобных осложнений, причём 38 % из них были оценены как серьёзные, угрожающие жизни и фатальные. Нежелательные эффекты были связаны с электролитными, почечными, геморрагическими, метаболическими нарушениями, поражением желудочно-кишечного тракта (ЖКТ) и нейропсихическими расстройствами, причинами которых наиболее часто являлись приём кардиологических препаратов, диуретиков, неопиоидных анальгетиков, гипогликемических средств и антикоагулянтов. Важно отметить, что 421 эпизод (27,6 %), был отнесён авторами к категории «предотвращаемых» [1].
Ещё более серьёзную оценку данной проблемы дают P. McDonnell и M. Jacobs, которые провели анализ 158 серьёзных побочных эффектов, потребовавших госпитализации; 96 эпизодов (62,3 %) были оценены авторами как «потенциально предотвращаемые», которые в большинстве случаев оказались связаны с неправильным назначением или превышением дозы препаратов, а также несоблюдением режима их приёма [2].
Весьма острой и хорошо известной проблемой, связанной с предотвращением нежелательных эффектов лекарственных препаратов на популяционном уровне, является вопрос адекватной профилактики серьёзных ЖКТ-осложнений, связанных с приёмом нестероидных противовоспалительных препаратов (НПВП).
Среди всех лекарств НПВП в клинической практике и повседневной жизни используются наиболее часто, занимая незыблемую на сегодняшний день позицию наиболее удобного, эффективного и доступного средства для патогенетического воздействия на боль и воспаление любого генеза. На популяционном уровне основной круг потребителей НПВП составляют больные с хронической патологией суставов и позвоночника (ревматическими заболеваниями), при которых боль и воспаление являются основными клиническими проявлениями [3].
К сожалению, клинические достоинства «традиционных» НПВП (неселективных ЦОГ-2 ингибиторов, н-НПВП), таких как диклофенак, кетопрофен, ибупрофен и другие, ограничиваются риском развития серьёзных осложнений со стороны ЖКТ. Этот риск неизбежен, поскольку связан с класс-специфическим действием н-НПВП, блокадой «физиологической» изоформы циклооксигеназы (ЦОГ-1), играющей важную роль в поддержании многих параметров гомеостаза человеческого организма, в т. ч. защитного потенциала слизистой ЖКТ.
Наиболее распространённой и опасной патологией, возникающей при приёме НПВП, является НПВП-гастропатия. Эта патология связана с системным действие НПВП, развивается независимо от способа введения (внутрь, в виде свечей или парентерально) и проявляется видимым повреждением слизистой верхних отделов ЖКТ с формированием эрозий и язв, а также угрожающих жизни осложнений - кровотечения, перфорации и нарушения проходимости ЖКТ.
Едва ли имеет смысл приводить в данной статье общеизвестные и многократно цитированные работы по статистике этих осложнений. Суммируя эти данные, мы можем сказать, что из 100 случайно выбранных больных, регулярно принимающих в течение года н-НПВП (например, диклофенак), примерно у 10-15 возникнут язвы желудка и/или двенадцатиперстной кишки, а у одного больного разовьётся кровотечение или перфорация. Пациенты, регулярно принимающие НПВП, погибают от подобных осложнений в два раза чаще, чем в популяции [4-6].
Современная концепция профилактики НПВП-гастропатии опирается на выделение чётко определённых групп больных, имеющих высокий риск ЖКТ-осложнений. Работы эпидемиологов позволили выделить факторы риска данной патологии, которые условно могут быть разделены на две большие группы. Первую составляют «модифицируемые», которые можно устранить, снизив тем самым вероятность развития ЖКТ-осложнений: приём высоких доз НПВП или нескольких препаратов из этой группы одновременно, курение, приём алкоголя, инфекция H. pylori. «Немодифицируемые» факторы риска не могут быть устранены - это пожилой возраст, наличие язвенного анамнеза (наибольшее значение имеет наличие в анамнезе осложненных язв) и сопутствующий приём низких доз аспирина, антикоагулянтов, глюкокортикоидов, т. е. препаратов, повышающих риск образования язв и развития кровотечения [4-6].
В 2004 г. в США экспертная группа, включавшая троих ревматологов, двоих интернистов, двоих гастроэнтерологов и двоих кардиологов, провела анализ 304 возможных клинических сценариев с сочетанием различных факторов риска для определения стратегии профилактики серьёзных осложнений НПВП (Dubois R., 2004). Согласно выводам комиссии, в основе стратегии безопасной терапии НПВП лежит использование у больных с основными факторами риска селективных ЦОГ-2 ингибиторов (с-НПВП) или неселективных (н-НПВП) в комбинации с мощным гастропротектором [7].
В реальной клинической практике обе стратегии профилактики НПВП-гастропатии занимают примерно равноценное положение. Например, J. Greenberg и сотр., наблюдая за группой из 3755 больных воспалительными ревматоидными заболеваниями, показали, что в 2005 г., после печально знаменитого «кризиса коксибов», с-НПВП назначаются 36,1 % больных, в то время как комбинация н-НПВП и гастропротекторов - 53,7 %. Среди больных без факторов риска эта пропорция составляла 37,2 и 57,1 %, с одним фактором риска - 37,2 и 57,1 %, а среди больных с двумя и более факторами риска НПВП-гастропатии - 41,5 и 65,4 % соответственно [8].
Эффективными гастропротекторами, которые должны использоваться для профилактики НПВП-гастропатии, по мнению большинства экспертов, являются ингибиторы протонной помпы (ИПП). Назначение этих препаратов в комбинации с н-НПВП позволяет снизить риск развития серьёзных ЖКТ-осложнений как минимум на 50 % [9]. Такой же благоприятный уровень безопасности наблюдается и при использовании с-НПВП. Оценить реальный уровень снижения частоты серьезных побочных эффектов на фоне приёма этого класса препаратов можно на примере нимесулида, который является одним из наиболее популярных НПВП в России [10]. Синтезированный доктором G. Moore в биохимической лаборатории ЗМ (подразделение Riker Laboratories) и лицензированный в 1980 г. швейцарской фирмой Helsinn Healthcare SA, нимесулид появился на фармакологическом рынке с 1985 г. и сейчас используется в 50 странах мира, в т. ч. в государствах Европейского Союза (в Италии, в частности, он остаётся наиболее популярным НПВП). С момента начала использования и по 2005 г. было проведено 450 млн терапевтических курсов этого препарата [11]. Нимесулид зарекомендовал себя как эффективное средство при ревматических заболеваниях, причём важнейшим его достоинством является мощный и быстрый обезболивающий эффект, что было продемонстрировано в нескольких двойных слепых рандомизированных контролируемых исследованиях (РКИ) [11-13].
Весьма интересен опыт применения нимесулида (Найз®) при ревматоидном артрите. Российское многоцентровое 4-недельное РКИ эффективности нимесулида в дозе 200 мг и 400 мг при раннем ревматоидном артрите (n = 268) показало, что этот препарат недостоверно более эффективен в отношении купирования боли и уменьшения числа воспаленных суставов по сравнению с диклофенаком в дозе 100 мг и 200 мг [14]. Основным достоинством нимесулида, как и других препаратов из группы с-НПВП, является значительно меньший риск развития серьёзных ЖКТ-осложнений по сравнению с традиционными НПВП [3, 11]. По данным популяционного исследования, проведённого в Северной Италии (анализ 10 608 сообщений о побочных действиях НПВП, произошедших с 1988 по 2000 гг.), стало известно, что нимесулид был причиной осложнений со стороны ЖКТ в 10,4 % случаев, в то время как диклофенак - в 21,2 %, кетопрофен - в 21,7 %, а пироксикам - в 18,6 % [15].
F. Bradbury (2004) проанализировал число сообщений о нежелательных эффектах со стороны ЖКТ на фоне приёма нимесулида и диклофенака в клинической практике Ирландии. Анализ включал группы из 3807 и 3553 больных, принимавших соответствующие препараты. Оказалось, что нимесулид вызывал подобные осложнения в 1,5 раза реже - 8,0 и 12,1 % соответственно (p < 0,05) [16].
Близкие данные показала работа О.Н. Минушкина (2003), представляющая собой когортное исследование безопасности нимесулида (Найз®) в дозе 200 мг в сутки, который в течение одного - трёх месяцев принимали более 600 российских больных. Суммарная частота ЖКТ-осложнений составила лишь 9 %, причём не было выявлено ни одного случая развития желудочно-кишечного кровотечения или перфорации язвы [17].
В 2003 г. нами было проведено РКИ безопасности нимесулида у больных, которым данный препарат назначался непосредственно после заживления НПВП-индуцированных язв и множественных эрозиё слизистой желудка и/или двенадцатиперстной кишки. Было показано, что у пациентов, принимавших нимесулид 200 мг в сутки, в течение ддвух месяцев наблюдения число рецидивов составило лишь 5,6 %, в то время как в контрольной группе, получавшей диклофенак 100 мг в свечах, -33,3 % [18].
В цитированном выше исследовании эффективности НПВП при раннем ревматоидном артрите было показано, что в двух группах, принимавших нимесулид (200 мг и 400 мг в сутки), язвы желудка или ДПК возникли лишь у двоих больных, тогда как у принимавших диклофенак 100 мг и 200 мг сутки - у семи [14].
Проблемы
К сожалению, несмотря на чётко определённые факторы риска и столь же чётко определённые методы профилактики НПВП-гастропатии, проблема серьёзных ЖКТ-осложнений, связанных с приёмом НПВП, остаётся достаточно острой. В первую очередь это связано с тем, что у существенной части больных, нуждающихся в проведении анальгетической и противовоспалительной терапии, рекомендации по предупреждению НПВП-гастропатии не выполняются. Так, используя базу данных эндоскопического кабинета ГУ Института ревматологии РАМН, мы могли оценить выполнение стандартов профилактики НПВП-гастропатии у 2897 больных ревматоидными заболеваниями, направленных для проведения эндоскопического исследования в 2003-2005 гг. Из них 745 больных (17,7 %) имели один из основных факторов риска НПВП-гастропатии (возраст от 65 лет и старше или язвенный анамнез), 232 (8,0 %) -сочетание двух основных факторов риска или одного основного и дополнительного (высокие дозы НПВП или сопутствующий приём низких доз аспирина), а 34 (1,2 %) -сочетание трёх и более факторов. Оказалось, что среди лиц с одним фактором риска с-НПВП или н-НПВП в комбинации с ИПП использовались лишь у 46,2 % больных, с двумя факторами - у 34,6 %, с тремя и более - у 35,5 % [19].
Реальное состояние дел с профилактикой НПВП-гастропатии в России также иллюстрирует опрос 3037 больных, принимавших НПВП, в Москве и 6 регионах России. Среди 239 респондентов, имевших в анамнезе язву желудка или двенадцатиперстной кишки, лишь 41 % получали с-НПВП и 12,9 % - н-НПВП в сочетании с ИПП [20].
Таким образом, лишь меньшая часть российских больных, имеющих серьёзные факторы риска НПВП-гастропатии, получают адекватные методы профилактики этой патологии. Однако ситуация в России выглядит ещё сравнительно благоприятной по сравнению с данными, приводимыми по этой проблеме западными коллегами.
В масштабном исследовании W. Smolley и сотр. был проведён анализ использования профилактики серьёзных ЖКТ-осложнений у 76 765 пациентов, принимавших НПВП, в штате Теннеси, США (1999-2000 гг.). Оказалось, что у больных, имевших два и более факторов риска (возраст 75 лет и старше, язвенный анамнез, приём антикоагулянтов или ГК), одна из эффективных стратегий профилактики ЖКТ-осложнений использовалась лишь у 30 % (!) [21].
По данным M. Sturkenboom и сотр., в Голландии ситуация с адекватной профилактикой ЖКТ-осложнений представляется ещё более серьёзной. Среди 69 648 больных, принимавших НПВП за период с 1996 по 2002 гг., лишь 6,6 % получали н-НПВП в сочетании с гастропротекторами, а 1,3 % - селективные ЦОГ-2 ингибиторы. Из имевших одиин фактор риска одну из гастропротективных стратегий получали лишь 13,4 %, два и более факторов риска - 18,8 % [22].
Канадские исследователи N. Hertnell и сотр. провели анализ факторов, влияющих на назначение гастропротективных стратегий у больных с факторами риска НПВП-гастропатии (исследуемую группу составили 14 587 больных от 65 лет и старше, регулярно получавших НПВП). Оказалось, что на использование адекватной профилактики НПВП-гастропатии влияли, помимо наличия высокого риска осложнений, такие социальные факторы, как проживание в городах и уровень годового дохода более 50 тыс. долларов [23].
Как видно из приведённых выше данных, проблемы с профилактикой НПВП-гастропатии могут иметь совершенно объективные причины. Большинству больных хроническими ревматоидными заболеваниями требуется длительный (порой пожизненный) приём НПВП, что определяет необходимость столь же длительной профилактики ЖКТ-осложнений. Длительный приём ИПП существенно увеличивает стоимость лечения НПВП, а финансовая сторона вопроса, как было отмечено выше в исследовании N. Hertnell, может играть заметную роль при выборе подходящей стратегии профилактики. Особое значение вопрос финансовых затрат имеет при назначении с-НПВП, чья номинальная стоимость заметно выше по сравнению со многими недорогими традиционными НПВП. Приобретение целекоксиба или генуинного препарата мелоксикама (Мовалис) может оказаться непосильным для многих социально незащищённых больных. Поэтому многие пациенты (даже с высоким риском НПВП-гастропатии!) вынуждены отдавать предпочтение более опасным, но значительно менее дорогим н-НПВП, таким как широко применяемые в нашей стране дженерики диклофенака.
Выбор стратегии профилактики: фармакологическая составляющая
Согласно известной фармакоэкономической концепции, дешёвое лекарство на самом деле не всегда является недорогим средством лечения. Действительно, реальную стоимость терапии определяют не только прямые затраты на покупку препарата, но и связанные с возникающими нежелательными эффектами косвенные затраты - на их лечение и профилактику, а также на временную или постоянную утрату здоровья вследствие серьёзных лекарственных осложнений. Часто приходится слышать, что использование более дорогих, но более безопасных препаратов с позиции фармакоэкономики оказывается выгоднее, чем менее дорогих лекарственных средств, чаще вызывающих нежелательные эффекты. Однако это положение может оказаться верным только в том случае, если разница в номинальной стоимости лекарств не столь велика.
Примером подобного фармакоэкономического анализа является работа K. Lee и сотр. (2003). Она основана на результатах классического исследования F. Chan, в ходе которого сравнивалась частота рецидивов желудочно-кишечного кровотечения (ЖКК) за 6-месячный период в группе из 287 больных, имевших в анамнезе осложнённые кровотечением язвы желудка или ДПК. Все больные получали НПВП - целекоксиб 400 мг в сутки и диклофенак 150 мг в сочетании с омепразолом 20 мг. Частота рецидивов ЖКК достоверно не различалась и составила 4,9 и 6,4 % соответственно. Фармакоэкономический анализ показал, что целекоксиб оказался статистически достоверно более выгодным препаратом - его использование в среднем на каждого больного с учётом прямых (номинал) и косвенных (лечение осложнений) затрат было на 11 % дешевле, чем диклофенака и омепразола: 9714 vs 10 915 долларов Гонконг ($HK). Однако следует отметить, что номинальная стоимость диклофенака (Вольтарен®) и омепразола (Лосек®), которые использовались в данной работе, была почти в два раза выше, чем целекоксиба, - 15,1 vs 8 $HK в день. При этом стоимость медицинских услуг в Гонконге (по сравнению с российскими) достаточно высока - в частности, диагностическая эзофагогастродуоденоскопия (ЭГДС) обходилась в 3500 $HK (487 долл. США по курсу на момент исследования) [24].
Ситуация совершенно меняется, когда разница в стоимости препаратов очень велика - в том случае, если сравниваются затраты при использовании генуинных лекарств и дженериков. В этом плане наиболее показательным является исследование, проведённое в США (Fendick A., 2002). Авторы, основываясь на данных серии РКИ, провели теоретический анализ стоимости двух стратегий назначения НПВП - использование достаточно дорогих, но относительно безопасных с-НПВП (средняя стоимость 60 долл. США в месяц) и дешёвого дженерика НПВП (5 долл. США в месяц) у больных без явных факторов риска НПВП-гастропатии. Согласно результатам исследования, несмотря на прогнозируемую высокую частоту осложнений, в среднем в год на одного больного использование дешёвых дженериков всё равно оказывается выгоднее, чем дорого безопасного препарата - 239 vs 831 долл. США (!), ведь исходная разница в номинале препаратов - двенадцатикратная [25].
Мы попытались смоделировать подобный подход в отношении российской медицинской практики, тем более что дженерики составляют большую часть нашего фармакологического рынка, а стоимость медицинских услуг значительно меньше, чем в большинстве стран мира.
Целью нашего исследования было оценить затраты (прямые и косвенные) при использовании различных стратегий назначения НПВП. Первая из них (стратегия 1) представляет использование дешёвого дженерика НПВП (диклофенак) без каких-либо методов профилактики НПВП-гастропатии, вторая (стратегия 2) - применение дорогого генуинного с-НПВП (Мовалис), третья (стратегия 3) - недорогого дженерика нимесулида (Найз) и 4-я (стратегия 4) - диклофенака в комбинации с недорогим дженериком омепразола (Омез).
Методы. Расчёт проводился на основании среднестатистической частоты развития ЖКТ-осложнений в группах больных, регулярно и длительно принимающих НПВП (см. выше).
Мы исходили из гипотезы, что при использовании стратегии 1 за 12 месяцев у одного больного из 100 разовьётся ЖКК, которое потребует хирургического вмешательства (резекция желудка). У 10 больных из 100 возникнут язвы желудка или ДПК, по поводу которых будет назначено курсовое противоязвенное лечение на основе ИПП (Омез 40 мг в течение 4 недель) и антихеликобактерной терапии (кларитромицин 1 г и амоксициллин 2 г в течение 10 дней). Мы также рассчитывали, что стратегии 2-4 эквивалентны по своей безопасности и обеспечивают 50 % снижение риска развития ЖКТ-осложнений по сравнению со стратегией 1. В данном анализе мы принимаем положение, что все оцениваемые препараты, методы обследования и лечения оплачиваются исходя из существующих на настоящий момент коммерческих цен в Москве. При этом мы не берём в рассмотрение косвенных расходов на утрату здоровья из-за соответствующих лекарственных осложнений ввиду сложности их учёта и явной недостаточности таких данных по России. Следует напомнить, что существенная часть больных, регулярно получающих НПВП, относятся к категории неработающих (пенсионеры и инвалиды).
Результаты
Согласно проведённому расчёту прямых и косвенных затрат, на 100 больных, получавших НПВП в соответствии со стратегией 1, при номинальной цене препарата 75 руб./мес., будет суммарно затрачено 332 940 рублей (табл. 2). Исходя из положения, что число серьёзных осложнений со стороны ЖКТ при использовании стратегий 2-4 будет в два раза меньше, прямые и косвенные затраты на 100 больных в год составят: стратегия 2 (номинал 939 руб./мес.) - 1 248 270 руб., стратегия 3 (номинал 195 руб./мес.) - 355 470 руб., стратегия 4 (номинал 210 руб./мес.) - 372 728 руб.
Таким образом, оценивая расходы на одного больного, применение дешёвых дженериков диклофенака, достаточно часто вызывающих серьёзные осложнения со стороны ЖКТ, с позиции теоретической фармакологической оценки представляется более выигрышным, чем какая-либо иная стратегия терапии НПВП (см. рисунок). Этот на первый взгляд удивительный результат на самом деле полностью оправдывается существующими в нашей стране низкими ценами на ряд дженериков НПВП и низкими расценками на медицинские услуги. Конечно, проведённый нами анализ носит упрощённый и предварительный характер. В работе было сделано серьёзное допущение, что все используемые препараты эквивалентны по своей эффективности. Кроме того, мы не учитываем здесь иные осложнения, связанные с приёмом НПВП, прежде всего такие частые, как диспепсия и ухудшение течения гастроэзофагеальной рефлюксной болезни. Вероятно, суммарный анализ затрат при использовании НПВП должен включать и данные по относительно нередким осложнениям со стороны сердечно-сосудистой системы, учитывая, что существенную часть больных, регулярно принимающих НПВП, составляют лица пожилого возраста, многие из которых страдают артериальной гипертензией. Как мы уже говорили, мы не учитываем затраты, связанные с нетрудоспособностью. И тем не менее, наш анализ ясно показывает невозможность оправдать использование дорогостоящих генуинных препаратов наличием прямой экономической выгоды.
Таблица 1.
Цены на препараты и медицинские услуги в Москве (по данным 5 сетевых источников и Медицинского информационно-аналитического центра РАМН на июнь 2007 г.)__
| Препараты и медицинские услуги | Стоимость, руб. |
| Диклофенак 100 мг № 20 | 50 |
| Мелоксикам (Мовалис®, Берингер) 15 мг № 10 | 313 |
| Омепразол (Омез®, Доктор Реддис) 20 мг № 30 | 135 |
| Нимесулид (Найз®, Доктор Реддис) 100 мг № 20 | 65 |
| Кларитромицин (Фромилид®, КРКА) 500 мг № 14 | 538 |
| Амоксициллин (Флемоксин-солютаб®, Астеллас) 500 мг № 20 | 173 |
| ЭГДС + первичная консультация эндоскописта к.м.н. + биопсия на H.pylori (уреазный тест) | 3200 |
| ЭГДС + повторная консультация эндоскописта к.м.н. | 1200 |
| Резекция желудка1 | 35916 |
| Анестезиологическое пособие | 1661 |
| Первичная консультация гастроэнтеролога к.м.н. | 900 |
| Повторная консультация гастроэнтеролога к.м.н. | 600 |
| Пребывание в палате интенсивной терапии | 3844 |
| Пребывание в палате хирургического отделения | 9727 |
| 1В зависимости от вида операции от 28 536 до 44 390 руб. | |
Таблица 2.
Прямые и косвенные затраты при использовании дешёвого дженерика диклофенака 100 мг в сутки (на 100 больных за 12 месяцев)
| Стоимость препаратов и медицинских услуг | На одного больного в год, руб. | На 100 больных в год, руб. |
| Препарат | 900 | 90 000 |
| Диагностика, лечение и профилактика желудочно-кишечного кровотечения: ЭГДС (3200 руб.) + резекция желудка и анестезиологическое пособие (37 577 руб.) + 3 дня в ОИТ (11 531 руб.) + 10 дней в хирургическом отделении - (97 270 руб.) + консультация гастроэнтеролога (900 руб.) + курсовое лечение язвы (1692 руб.), при1м Омеза 20 мг в течение 10 мес. после операции (1350 руб.) | 153520 | 153520 |
| Лечение язв: 2 ЭГДС (4400 руб.) + две консультации гастроэнтеролога (1500 руб.) + курсовое лечение язвы (1692 руб.) + Омез 20 мг 10 мес. (1350 руб.) | 8942 | 89420 |
| Итого | 332940 | |
Рисунок. Теоретический расчёт прямых и косвенных затрат при лечении НПВП с использованием стратегий 1-4 (в среднем на одного больного за 12 месяцев, руб.) 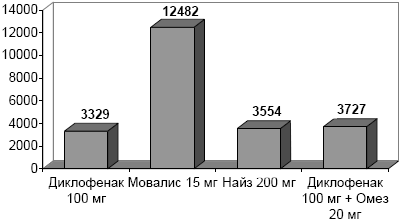
Вероятно, будущие исследователи фармакоэкономики НПВП в России должны опираться на конкретные данные, полученные в ходе обширных ретроспективных или проспективных исследований, с учётом конкретных затрат и всего спектра наиболее частых осложнений, а также таких факторов, как эффективность терапии и удовлетворённость лечением.
В заключение следует отметить, что стратегии 3 и 4 (применение недорогого дженерика нимесулида - Найз®) или комбинации н-НПВП и ИПП (недорогого дженерика омепразола - Омез®) лишь не намного превышают по затратам использование дешёвого диклофенака. Однако при этом мы существенно снижаем риск развития опасных осложнений и тем самым косвенно повышаем эффективность противовоспалительной терапии. Несомненно, что с учётом особенностей российской медицинской практики, когда большую часть пациентов с хроническими заболеваниями суставов и позвоночника составляют малообеспеченные люди, эти стратегии выбора НПВП представляются наиболее выигрышными как с медицинской, так и с социальной точек зрения. Литература
1. Gurwitz J., Field T., Harrold L., et al. Incidence and preventability of adverse drug events among older persons in the ambulatory setting // JAMA. 2003 Mar 5;289(9):1107-1116.
2. McDonnell P., Jacobs M. Hospital admissions resulting from preventable adverse drug reactions // Ann Pharmacother. 2002, 36(9), 1331-1336.
3. Насонов Е.Л., Лазебник Л.Б., Мареев В.Ю. и сотр. Применение нестероидных противовоспалительных препаратов. Клинические рекомендации. М., 2006.
4. Singh G. Recent consideration in nonsteroidal anti-inflammatory drug gastropathy // Am J Med, 1998; 105: 31-38.
5. Lain L. Proton pump inhibitor co-therapy with nonsteroidal anti-inflammatory drugs-nice or necessery? // Rew Gastroenterol Dis 2004; 4: 33-41.
6. Lanas A. Prevention and treatment of NSAID-induced gastrointestinal injury // Curr Treat Options Gastroenterol 2006; 9: 147-156.
7. Dubois R.W., Melmed G.Y., Henning J.M., Lane L. Guidelines for the appropriate use of non-steroidal anti-inflammatory drugs, cyclooxygenase-2 specific inhibitors and proton pump inhibitors in patients requiring chronic anti-inflammatory therapy // Aliment Pharmacol Ther 2004; 19: 197-208.
8. Greenberg J., Yariei Y., Kremer J. et al. Decline of NSAID gastroprotection in patients treated by rheumatologist in the post-rofecoxib era. // Arthritis Rheum., 2006, 54 (abstract suppl.), 109.
9. Singh G., Triadafilopoulos S. Appropriative choice of proton pump inhibitor therapy in the prevention and management of NSAID-related gastrointestinal damage // Int J Clin Pract 2005; 59: 1210-1215.
10. Насонов Е.Л. Эффективность и переносимость нестероидного противовоспалительного препарата. Нимесулид: новые данные // РМЖ, 2001, 15: 6-8.
11. Rainsford K. Nimesulide - a multifactorial approach to inflammation and pain: scientific and clinical consensus // Curr Med Res Opin. 2006, 22(6), 1161-1170.
12. Bianchi M., Broggini M. A randomized, double-blind, clinical trial comparing the efficacy of nimesulide, celecoxib and rofecocxib in osteoarthritis of the knee // Drag., 2003, 63, suppl. 1, 37-46.
13. Bianchi M., Broggini M., Balzarini P. et al. Effect of nimesulide on pain and synovial fluid concentrations of substance P, interleukin-6, and interleukin-8 in patients with knee osteoarthritis: comparison with celecoxib // Ann Rheum Dis., 2006, 65, 225.
14. Каратеев А.Е., Каратеев Д.Е., Лучихина Е.Л. и др. Эффективность и безопасность монотерапии высокими дозами НПВП при раннем артрите. РМЖ, 2006, 16, 24-29.
15. Conforti A., Leone R., Moretti U., Mozzo F., Velo G. Adverse drug reactions related to the use of NSAIDs with a focus on nimesulide: results of spontaneous reporting from a Northern Italian area. Drug Saf., 2001, 24, 1081-1090.
16. Bradbury F. How important is the role of the physician in the correct use of a drug? An observational cohort study in general practice. Int. J. Clin. Pract. (Suppl). 2004, 144, 27-32.
17. Минушкин ОН. Использование препарата "Найз" у больных, страдающих сочетанной патологией суставов и поражением верхних отделов желудочно-кишечного тракта. Научо-практическая ревматология 2003; 5: 72-76.
18. Каратеев АЕ, Каратеев ДЕ, Насонов ЕЛ. Гастродуоденальная переносимость нимесулида (НИМЕСИЛ, Berlin Chemie) у больных с язвенным анамнезом: первое проспективное исследование безопасности селективных ЦОГ-2 ингибиторов у больных с высоким риском развития НПВП-индуцированных гастропатий. Научно-практическая ревматология 2003; 1: 45-48.
19. Каратеев А.Е. Эффективная профилактика ЖКТ-осложнений у больных ревматическими заболеваниями: реальное состояние дел. Тезисы Всероссийской конференции «Социальные аспекты ревматических заболеваний». Науч. практ. ревм., 2006, 2, 88.
20. Каратеев А.Е., Насонов Е.Л. НПВП-ассоциированная патология ЖКТ: реальное состояние дел в России // РМЖ. 2006. № 15. С. 1073-1078.
21. Smolley W., Stein C., Arbogast P. et al. Underutilization of gastroprotective measures in patients receiving nonsteroidal antiinflammatory drugs // Arthritis Rheum., 2002, 46, 2195-2280.
22. Sturkenboom M., Burke T., Dieleman J., et al. Underutilization of preventive strategies in patients receiving NSAIDs // Rheumatology (Oxford). 2003, 42, 23-31.
23. Hartnell N., Flanagan P., MacKinnon N., Bakowsky V. Use of gastrointestinal preventive therapy among elderly persons receiving antiarthritic agents in Nova Scotia, Canada // Am J Geriatr Pharmacother. 2004, 2(3), 171-180.
24. Lee K., You H., Ho J., et al. Economic analysis of celecoxib versus diclofenac plus omeprazole for the treatment of arthritis in patients at risk of ulcer disease // Alim. Pharmacol. Ther., 2003, 18, 217-222.
25. Fendrick A., Bandekar R., Charnew M., Scheiman J. Role of initial NSAID choice and patient risk factors in the prevention of NSAID gastropathy: a decision analysis // Arthritis Rheum., 2002, 47, 36-43.
Комментарии
ПРАКТИКА ПЕДИАТРА
