Мексидол в качестве дополнительной терапии у больных непрерывной параноидной шизофренией при наличии поздней дискинезии
СтатьиОпубликовано:
Психиатрия и психофармакотерапия Том 13 №4
А.Л. Дьяконов
ГОУ ВПО Ярославская государственная медицинская академия Минздравсоцразвития РФ Резюме. При умеренной поздней дискинезии у больных с непрерывной параноидной шизофренией, получающих галоперидол и циклодол, добавление мексидола приводило к ослаблению нежелательных явлений. Наибольший положительный результат зафиксирован по шкалам AIMS, BAS. Показатели шкалы Симпсона–Ангуса на дополнительное включение мексидола реагировали в меньшей степени.
Ключевые слова: мексидол, поздняя дискинезия.
Mexidol as additional therapy for the patient with continuous paranoid type of schizophrenia in the in the presence of a late dyskinesia
A.L. Dyakonov
Summary. At a moderate late dyskinesia at patient with continuous paranoid type of schizophrenia receiving treatment with haloperidoli and cyclodoli with addition of mexidoli leads to easing of the undesirable phenomena. The most positive results is revealed on scales AIMS, BARS. Indicators of a scale of SAS on additional inclusion of mexidoli reacted to a lesser degree.
Key words: mexidol, late dyskinesia.
Молекулярный кислород является неотъемлемым составным элементом метаболизма человека. Реакция четырехэлектронного восстановления кислорода до воды – основа биоэнергетики клеток. Для большинства патологических состояний, в том числе шизофрении, присуще состояние окислительного стресса, когда неполное электронное восстановление кислорода приводит к накоплению так называемых свободных радикалов, которые повреждают макромолекулы ДНК, липидов белков. Свободнорадикальная теория высказана в 1955 г. Д. Харманом, и автор был выдвинут в качестве претендента на получение Нобелевской премии по медицине.
В этой ситуации патогенетически обоснованным является введение в схему лечения шизофрении лекарственных препаратов, которые способны предотвращать избыточный синтез активных метаболитов кислорода, повышать содержание или активность эндогенных антиоксидантов, снижать чрезмерную интенсивность реакций перекисного окисления.
Всеми указанными свойствами обладает янтарная кислота, ее соли и эфиры, в частности, производное янтарной кислоты – мексидол. Не вдаваясь в подробности механизма действия препарата, которые хорошо описаны в руководствах, аннотациях, остановимся на клиническом действии мексидола и причинах, побудивших применять его при таком серьезном заболевании, как шизофрения. Препарат обладает широким поликомпонентным спектром терапевтического действия. Препараты с широким спектром действия являются проблемными с позиций классификации [6]. В психиатрии мексидол использовался в комплексной терапии конверсионного расстройства [32], панических и других тревожных расстройств [12, 25, 34], психических расстройств у ликвидаторов катастрофы на Чернобыльской АЭС [15], при психоорганических расстройствах [14, 30], в том числе с неврозоподобной симптоматикой [11, 22, 27]. При этом мексидол апробирован не только при легких проявлениях психоорганического синдрома [8, 9, 18, 38], но и при умеренных [16, 17, 38]. В ряде случаев препарат показан при атрофическом процессе в мозге (болезнь Альцгеймера) [8].
Мексидол обладает антиоксидантным действием, противоишемическим, улучшая микроциркуляцию, реологические свойства крови [24, 33, 37].
При лечении шизофрении средством первого выбора являются нейролептики, в том числе классические, которые все указанные психоорганические изменения и вызывают, и усиливают. Таким образом, мексидол показан и с этой точки зрения. Более того, мексидол способен усиливать действие психотропных препаратов, что в ряде случаев позволяет снизить их дозу [14, 31], ослабляет экзогенную (психотропные препараты) и эндогенную (шизофренический процесс) интоксикации [10, 19, 36].
Противосудорожный эффект мексидола [1] позволяет избежать киндлинг-эффекта (возникновение тонико-клонических судорог) у больных шизофренией в результате колебаний концентрации (даже при стабильной терапевтической дозе) нейролептика в крови (особенно галоперидола). Описаны антистрессорные [2, 7], ноотропные свойства препарата, т.е. он улучшает синаптическую передачу, усиливая развитие коллатералей, взаимосвязь структур мозга [2, 3, 15]. При использовании мексидола замедляется развитие нарушений памяти, апатико-абулического синдрома, снижается интенсивность головной боли, напряжения, мигрени [23–26, 37].
Гепатопротекторные свойства позволяют замедлить патологические изменения в печени, поджелудочной железе [13, 20, 21], что также немаловажно, так как прием нейролептиков при шизофрении может сопровождаться этими нарушениями.
Наконец, мексидол обладает транквилизирующим, седативным действием [2, 28, 29, 34], в связи с чем ряд авторов [35] предлагают называть его «транквилоноотропом» или «ноотранквилизатором».
С учетом изложенного была сделана попытка определить влияние мексидола на проявления хронического нейролептического синдрома у больных шизофренией, принимавших галоперидол.
Обследовано 72 пациента в возрасте от 20 до 50 лет (38,2±2,03 года) с параноидной формой непрерывно текущей шизофрении (галлюцинаторно-бредовый этап), которые на протяжении длительного времени принимали от 5 до 15 мг/с галоперидола в сочетании с 4–6 мг циклодола и (периодически) транквилизаторы бензодиазепинового ряда (в основном феназепам, альпрозалам или клоназепам). У всех пациентов имели место поздние (тардивные) экстрапирамидные нежелательные явления. Все обследованные разделены на 2 группы: 1-я – больные принимали препараты в прежнем режиме (30 человек), 2-я группа – к препаратам прежнего режима добавлялся мексидол в дозе 250 мг/с (утро, обед). Клиническая оценка в обеих группах производилась на 10, 20 и 40-й дни. Заполнялись шкалы: патологических произвольных движений (АIМS), акатизии Барнеса (BAS), неврологическая шкала Симпсона–Ангуса. Статистическая обработка производилась по методу Стьюдента. Кроме того, использовались стандартные статистические показатели: средние значения и стандартная ошибка.
Результаты исследования
Поздняя (тардивная) дискинезия обычно ассоциируется с длительной (не менее 2 лет) нейролептической терапией. В данном исследовании терапию галоперидолом пациенты получали в среднем 4,2±1,35 года. Однако в 5 случаях поздние экстрапирамидные расстройства у больных возникли в течение первого года интенсивной терапии. Помимо наличия патологических движений на фоне галлюцинаторно-бредовой симптоматики, представленной в основном синдромом Кандинского-Клерамбо, и дефекта в эмоционально-волевой сфере, отмечалась аффективная неустойчивость со вспышками агрессии (46; 63,9%), назойливость (38; 52,8%), психофизическая истощаемость (72; 100%).
Баллы в шкалах, отражающих нежелательные явления на терапию галоперидолом, в обеих анализируемых группах распределялись примерно одинаково. У всех больных регистрировался комплекс насильственных движений в челюстно-лицевой мускулатуре, движение губами по типу чмокания, сосания, хореоатетоидные движения языком, жевательные движения челюстей, хореоподобные и атетоидные движения конечностей и частей тела, а также в ряде случаев (51; 70,8%) любая комбинация этих движений. Указанные симптомы исчезали во время сна, но усиливались при малейшем волнении.
Согласно шкале непроизвольных патологических движений (AIMS) в обеих группах нежелательные явления в среднем в баллах распределялись следующим образом (рис. 1). Достоверность определена только в 10-м пункте, отражающем осознание пациентом патологических движений. Так, в группе, где в дальнейшем назначался мексидол, патологические движения причиняли пациентам несколько больше беспокойства. Сплошной линией подчеркнуты доминирующие патологические движения.
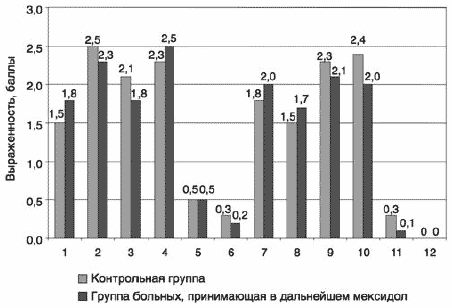
Рис. 1. Показатели шкалы AIMS в анализируемых группах до начала исследования.
Примечание. 1 – Мимические мышцы, например нахмуривание лба, бровей, гримасы верхней части лица. 2 – Губы и область вокруг рта (чмокание, сосание, надувание губ). 3 – Челюсти (покусывание, стискивание зубов, жевательные движения). 4 – Язык (увеличение движений). 5 – Верхние конечности (руки, запястья, кисти, пальцы), не включая тремор. 6 – Нижние конечности (боковые движения колен, постукивание ногами по полу, выворачивание ступней наружу или внутрь, извивающиеся движения ступнями). 7 – Движения туловища (покачивания, изгибания). 8 – Интенсивность патологических движений. 9 – Неудобства, связанные с патологическими движениями. 10 – Осознание пациентами патологических движений. 11 – Текущие проблемы с зубами или протезами. 12 – Пациент обычно носит протезы.
Распределение нежелательных явлений в соответствии со шкалой акатизии Барнеса (BAS) представлено на рис. 2. При объективной оценке акатизии, которая выражалась в основном в топтании на месте, шаркающих движениях ногами (во время беседы эти движения присутствовали в течение приблизительно 1/2 периода наблюдения), что в среднем по группам составляло соответственно 1,3 и 1,2 балла. Субъективное осознание беспокойства соответствовало 2,2 и 2,1 балла. Пациенты осознавали неспособность находиться без движения, ощущали внутреннее напряжение, беспокойство. Свое субъективное страдание, связанное с беспокойством, оценивалось ими как умеренное. Общая клиническая оценка акатизии представлена как умеренная. Достоверных различий между группами в проявлениях акатизии не выявлено.
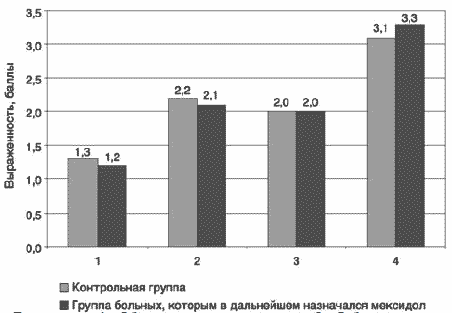
Рис. 2. Показатели шкалы BAS в анализируемых группах до начала исследования.
Примечание. 1 – Объективная оценка акатизии. 2 – Субъективная оценка акатизии – осознание беспокойства. 3 – Субъективное страдание, связанное с беспокойством. 4 – Общая клиническая оценка акатизии.
Неврологическая шкала Симпсона–Ангуса (SAS) также указывала на наличие нежелательных явлений в обеих группах исследуемых (рис. 3). Согласно этой шкале у пациентов в большей степени констатировалось значительное уменьшение движений руками во время ходьбы (пункт 1), замедленное опускание («падение») рук без отскока – руки разведены в стороны, подняты до уровня плеч, происходит их непроизвольное опускание (пункт 2), умеренная ригидность и сопротивление в локтевых, лучезапястных, плечевых суставах (пункты 3–6), умеренная ригидность затылочных мышц (пункт 7). При постукивании по переносице при широко раскрытых глазах и просьбе «не моргать» наблюдалось от 6 до 15 морганий (пункт 8). Из всех симптомов неврологической шкалы явно преобладал тремор кистей рук, периодически переключающийся на всю руку, ногу (пункт 9). Саливация была выражена не сильно и проявлялась только тогда, когда открыт рот и поднят язык, при отсутствии какое-то время сглатывания (пункт 10). Достоверных различий между показателями контрольной группы и группы пациентов, которые принимали мексидол, не выявлено.
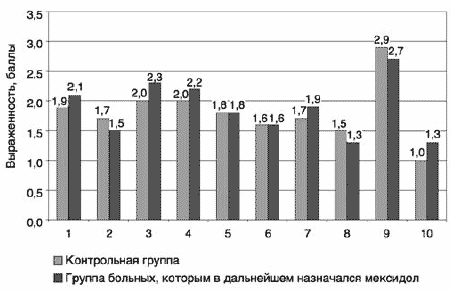
Рис. 3. Показатели неврологической шкалы Симпсона–Ангуса в анализируемых группах до начала исследования.
Спустя 10 дней от начала наблюдения и присоединения к терапии пациентов 2-й группы мексидола показатели всех шкал, отражающих анализируемые нежелательные явления, не претерпели существенных изменений (достоверность отсутствовала).
Через 20 дней в 1-й группе пациентов, которые не получали мексидола, баллы оставались приблизительно на том же уровне, в то время как при наличии дополнительного введения в схему мексидола некоторые показатели нежелательных явлений уменьшились (рис. 4).
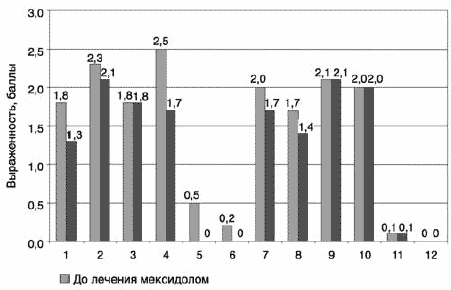
Рис. 4. Показатели шкалы AIMS у больных до лечения мексидолом и через 20 дней лечения.
Так, по шкале AIMS к 20-му дню терапии достоверно уменьшились движения мимических мышц верхней части лица и языка, движения конечностей (пункты 1, 4, 5).
Через 40 дней терапии мексидолом по шкале AIMS патологические непроизвольные движения продолжали ослабевать (рис. 5). Помимо тех нарушений, которые достоверно уменьшились к 20-му дню терапии мексидолом, дополнительно достоверно ослабли сосание, жевательные движения челюстей, атетоидные движения верхних конечностей, покачивания и в целом интенсивность патологических движений (пункты 2, 3, 5, 7, 8).
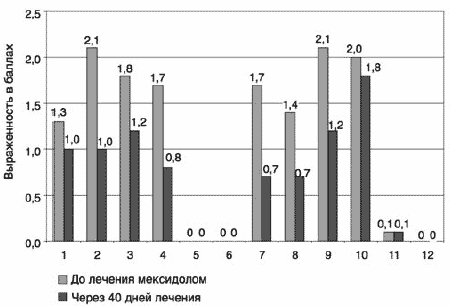
Рис. 5. Показатели шкалы AIMS у больных до лечения мексидолом и через 40 дней лечения.
Следовательно, добавление к основной терапии галоперидолом и циклодолом дополнительно мексидола, согласно шкале AIMS, способствовало достоверному ослаблению патологических непроизвольных движений в структуре поздних экстрапирамидных нарушений. В контрольной группе достоверного уменьшения патологических непроизвольных движений не отмечено.
При анализе акатизии с использованием шкалы BAS (рис. 6) на фоне лечения мексидолом значимое снижение всех показателей имело место также к 20-му дню терапии, продолжая снижаться к 40-му. Между 20 и 40-м днем разница в баллах недостоверна во всех пунктах, кроме общей клинической оценки акатизии (пункт 4), где имело место достоверное снижение. Если сравнивать результаты шкалы BAS до назначения мексидола и через 40 дней терапии, то снижение нежелательной акатизии имело место с высокой степенью результативности по всем 4 пунктам.
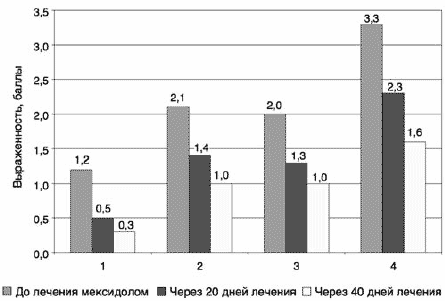
Рис. 6. Показатели шкалы BAS у больных до лечения мексидолом, на 20 и 40-й дни лечения.
В группе больных, где мексидол не был назначен, результаты наблюдения за 40 дней по шкале BAS не претерпели существенных изменений.
Результаты анализа показателей неврологической шкалы Симпсона–Ангуса подтверждали данные анализа показателей шкал AIMS и BAS в том плане, что первые 10 дней приема препарата не давали достоверного снижения баллов (рис. 7).
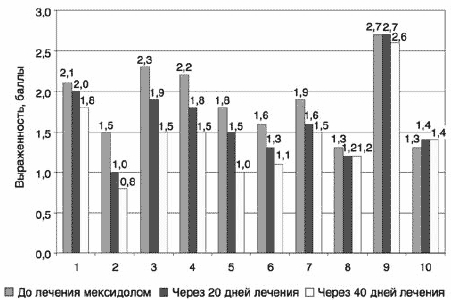
Рис. 7. Показатели неврологической шкалы Симпсона–Ангуса у больных до лечения, на 20 и 40-й дни лечения.
На 20-й день лечения мексидолом достоверно уменьшился лишь один из показателей шкалы: замедленное «падение» рук без отскока (пункт 2). К 40-му дню по сравнению с 20-м достоверного снижения неврологических проявлений нежелательных явлений согласно шкале не выявлено. Однако при сравнении с показателями до лечения дополнительно получены к 40-му дню терапии значимые результаты по пунктам: ригидность, сопротивление в лучезапястных, локтевых, плечевых суставах (пункты 3–6). По другим показателям значимых послаблений неврологической симптоматики не определено.
Таким образом, при регистрируемой умеренной тардивной экстрапирамидной симптоматике у больных непрерывной параноидной шизофренией, леченных галоперидолом, циклодолом, добавление в стандартную схему мексидола оправданно. Положительный результат появлялся к 3-й неделе дополнительной терапии, усиливался к 6-й неделе. Согласно анализируемым шкалам наибольший положительный результат имел место при наличии патологических произвольных движений (AIMS) и акатизии Барнеса (BAS) Показатели неврологической шкалы Симпсона–Ангуса на дополнительное включение в схему мексидола реагировали в меньшей степени и не в полном объеме.
Список использованной литературы
