Влияние современных противоэпилептических препаратов на качество жизни больных эпилепсией
СтатьиИ.Г. Рудакова, О.С. Морозова, А.С. Котов
Impact of the current antiepileptic drugs on quality of life of epileptic patients
I.G. Rudakova, O.S. Morozova, A.S. Kotov
Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского, Москва Целью исследования явилась сравнительная оценка влияния противоэпилептических препаратов на качество жизни получающих их больных. Были обследованы 192 пациента (средний возраст 30,6±1,05 года) с симптоматическими и предположительно симптоматическими фокальными эпилепсиями, получающих монотерапию одним из противоэпилептических препаратов: вальпроаты (52 человека), карбамазепины (36), топирамат (56), леветирацетам (24) и окскарбазепин (24). Исследование включало общеклинический и неврологический осмотр, ЭЭГ и/или видео-ЭЭГ-мониторинг, РКТ и/или МРТ головного мозга, нейропсихологическое тестирование c использованием шкал QOLIE-31 и HUDS в сроки от 3 мес от начала терапии. Наиболее часто высокие оценки качества жизни отмечены в группах, получавших леветирацетам и окскарбазепин (83,3 и 72% соответственно), наибольшая частота низких оценок среди принимавших карбамазепин и вальпроаты (16,5 и 17%). Клинически значимые психоэмоциональные расстройства чаще отмечались при применении топирамата (21,8%), вальпроатов (21,4%) и карбамазепина (16,6%), значительно реже — окскарбазепина (8,3%), отсутствовали при лечении леветирацетамом. Отмечена сильная корреляционная связь качества жизни с эффективностью и побочными эффектами терапии, психоэмоциональными нарушениями. Лучшие показатели качества жизни наблюдались при применении противоэпилептических препаратов нового поколения.
Ключевые слова: эпилепсия, противоэпилептические препараты, качество жизни.
The purpose of the study was the comparative evaluation of antiepileptic drugs (AED) impact on quality of life (QOL). One hundred and ninety-two patients with symptomatic and probably symptomatic focal epilepsies (mean age 30, 6±1,05) were investigated. All patients received the following AED as monotherapy: valproate (52), carbamazepine (36), topiramate (56), levitiracetam (24), oxcarbazepine (24). The clinical and neurological examination, EEG and/or video-EEG-monitoring, CT and/ or MRA scan, neuropsychological tests (31-item Quality of Life in Epilepsy — QOLIE-31, version 1 and HUDS) were performed after 3 months of treatment. The higher results of QOL assessment were obtained in the LEV and OXC groups (83,3 and 72%, respectively), the lowest ones — in the CBZ and VPA groups (16,5 and 17%). Clinically relevant emotional disorders occurred more frequently in patients receiving TPM (21,8%), VPA (21,4%) and CBZ (16,6%), significantly rarely in the OXC (8,3%) group and were absent in the LEV group. The strong correlations between QOL, effectiveness, adverse effects and psychoemotional disorders of AED treatment were found. The best QOL scores were observed in patients treated with newer AED.
Key words: epilepsy, antiepileptic drugs, quality of life.
Стратегия лечения эпилепсии в настоящее время претерпела значительные изменения. Современный подход к проблеме лечения эпилепсии предусматривает решение ряда вопросов, касающихся не только достижения максимального терапевтического эффекта, но и адекватного и комфортного функционирования больных в обществе (получение образования, выбор профессии, трудоустройство, создание семьи). Если еще в 50—80-е гг. прошлого столетия приоритетом терапии являлась эпилепсия как болезнь, а целью — устранение припадков и психоэмоциональных расстройств, то на современном этапе приоритетом является больной, а целью — улучшение качества его жизни (КЖ) [3]. Согласно определению Всемирной организации здравоохранения, КЖ — восприятие людьми своего положения в жизни в контексте культуральных и ценностных ориентаций в соответствии с их собственными целями, ожиданиями, стандартами и заботами (цит. по [4]). КЖ определяется как удовлетворенность человека своим физическим, психическим и социальным благополучием во всех аспектах его функционирования в обществе.
В многочисленных исследованиях было установлено значительное ухудшение КЖ у больных эпилепсией по сравнению с остальной популяцией [6]. Факторы, снижающие КЖ при эпилепсии, весьма многообразны. Часто уже сам диагноз эпилепсии оказывается драматичным для больного, вызывая социальную дизадаптацию, способствуя психологическому дистрессу и снижению КЖ. [7, 9]. Негативное влияние оказывают также эпилептические приступы, страх их повторения и настороженное отношение к ним окружающих [10]. Именно с приступами связан повышенный риск развития психических и когнитивных расстройств, нанесения ущерба физическому здоровью [8]. Одним из наиболее значимых отрицательных факторов становится необходимость длительного (иногда на протяжении всей жизни) приема противоэпилептических препаратов (ПЭП), которые сами могут снижать КЖ, вызывая физические, психические и когнитивные расстройства, обладать тератогенным воздействием [5]. В некоторых случаях сами ПЭП оказывают отрицательное влияние на течение заболевания и тяжесть приступов [2].
Таким образом, проблема КЖ больных эпилепсией связана не только с клиническими проявлениями болезни, но и с личностной реакцией на нее, с необходимостью постоянного приема лекарств, с отношением общества к больным, которое не всегда обоснованно ограничивает их стремление к социальной активности [4]. В современной эпилептологии одной из приоритетных целей является улучшение КЖ и реабилитация больных эпилепсией [1].
До недавнего времени базовыми ПЭП для применения в монотерапии при большинстве форм эпилепсии у взрослых оставались вальпроаты и карбамазепин. С появлением группы ПЭП нового поколения этот перечень расширился. В настоящее время для применения в монотерапии, в том числе в России, получили признание топирамат, окскарбазепин; зарегистрирован во многих странах мира и накапливается опыт применения в России леветирацетама. Возможности для индивидуализированного лечения эпилепсии, несомненно, расширились. Улучшился ли при этом прогноз для больных эпилепсией, и изменилось ли их КЖ в целом? Эти вопросы остаются открытыми и не всегда решаются однозначно.
Задачей данного исследования было изучение и сравнительный анализ влияния современных ПЭП, применяемых в монотерапии, на КЖ взрослых, больных эпилепсией.
Материал и методы
Обследовали 192 больных эпилепсией (90 мужчин и 102 женщины) в возрасте от 16 до 65 лет (средний возраст 30,63±1,05 года). Отбор больных осуществлялся по обращаемости в консультативный кабинет эпилептолога консультационно-диагностического отделения Московского областного научно-исследовательского клинического института им. М.В. Владимирского в 2007—2008 гг.
Критериями включения пациентов в исследование были: возраст старше 16 лет, диагноз симптоматической (криптогенной) фокальной эпилепсии, установленный в соответствии с Международной классификацией эпилепсий и эпилептических синдромов (1989), монотерапия одним из ПЭП первого выбора для данной формы эпилепсии (стартовая или последующая, в том числе после неадекватной политерапии). Из исследования исключали больных по следующим критериям: политерапия, отмена ПЭП в связи с неэффективностью или побочными эффектами в сроки менее 3 мес от начала лечения, наличие грубых интеллектуальных и психических расстройств, тяжелая соматическая патология, некомплаентность.
В зависимости от принимаемого ПЭП все больные были разделены на 5 групп: группу, принимающую вальпроаты (52 пациента), карбамазепин (36), топирамат (56), леветирацетам (24) и окскарбазепин (24). Используемые суточные дозировки ПЭП соответствовали индивидуальным клинически эффективным или максимально переносимым дозам: для вальпроатов 1000—3000 мг, для карбамазепина 800—1600 мг, для топирамата 200—400 мг, для леветирацетама 1500—3000 мг, для окскарбазепина 900— 2400 мг. Режим приема всех ПЭП был 2 раза в сутки утром и вечером.
Использовали следующие методы исследования: общее клиническое неврологическое, ЭЭГ и/ или видео-ЭЭГ-мониторинг (с целью диагностики эпилепсии и, в ряде случаев, контроля эффективности терапии), нейровизуализация (РКТ, МРТ головного мозга).
Исследование КЖ проводилось всем больным в сроки от 3 до 12 мес (в среднем 6±2,5 мес) от начала монотерапии и включало нейропсихологическое тестирование с использованием опросника QOLIE-31 (Quаlity of life in epilepsy — Качество жизни при эпилепсии, версия 1.0), позволяющего количественно (в баллах) оценить 7 основных сфер КЖ больного эпилепсией: боязнь приступов, общее КЖ, эмоциональное благополучие, энергичность/утомляемость, когнитивные функции, влияние препаратов, социальное функционирование. Для оценки влияния психоэмоционального состояния на КЖ больных была использована госпитальная шкала тревоги и депрессии (HADS).
Результаты
Во всех выделенных группах отмечалась комбинация различных видов приступов с преобладанием сложных парциальных (СПП) и вторично-генерализованных (ВГСП) над простыми парциальными (ППП). Изначальная частота приступов была для ВГСП: 1—5 в мес, для СПП и ППП: 4—14 в мес. Среди больных, получающих лечение традиционными ПЭП (вальпроаты и карбамазепин), преобладали лица, у которых терапия эпилепсии была стартовой — 58 и 72% соответственно. Среди больных, получающих новые ПЭП (топирамат, леветирацетам и окскарбазепин), большую часть составляли пациенты, у которых был осуществлен переход с ранее применяемой терапии в связи с ее неэффективностью или побочными эффектами — 52, 79 и 75% соответственно (табл. 1). Этот факт, безусловно, отражает тенденцию использования новых дорогостоящих ПЭП лишь в случае обоснованной необходимости. Более редкое (21%) назначение в качестве стартовой монотерапии леветирацетама было обусловлено отнюдь не его меньшей эффективностью, а скорее относительной новизной препарата и недостаточным опытом применения, а в отношении окскарбазепина (13%) еще и отсутствием возможности льготного обеспечения.
Таблица 1. Частота встречаемости различных видов приступов и характер монотерапии в выделенных группах больных
| Препарат | Тип приступов | Характеристика монотерапии | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ППП | СПП | ВГСП | стартовая | перевод с неэффективной терапии |
перевод из-за побочных эффектов |
|||||||
| абс. | % | абс. | % | абс. | % | абс. | % | абс. | % | абс. | % | |
| Вальпроаты (n=52) |
7 | 13 | 22 | 42 | 42 | 81 | 30 | 58 | 14 | 27 | 8 | 15 |
| Карбамазепин (n=36) |
11 | 31 | 22 | 61 | 24 | 67 | 26 | 72 | 9 | 25 | 1 | 3 |
| Топирамат (n=56) |
11 | 20 | 25 | 45 | 50 | 89 | 27 | 48 | 16 | 29 | 13 | 23 |
| Леветирацетам (n=24) |
0 | — | 12 | 50 | 20 | 83 | 5 | 21 | 15 | 62 | 4 | 17 |
| Окскарбазепин (n=24) |
11 | 46 | 10 | 42 | 20 | 83 | 3 | 13 | 14 | 58 | 7 | 29 |
Эффективность терапии при применении различных ПЭП оценивалась по показателю снижения частоты эпилептических приступов в процентах от исходной частоты: 100% — ремиссия, 75—99% — существенное улучшение, 50—74% — умеренное улучшение. Снижение частоты приступов менее чем на 50% (минимальное улучшение) расценивалось как отсутствие клинически значимого эффекта, учащение приступов — как ухудшение. Результаты оценки представлены на рис. 1.
В среднем во всех группах отмечена достаточно высокая эффективность монотерапии. Максимальная частота достижения ремиссии отмечена в группе, принимавшей топирамат (57%), несколько реже (р>0,05) в группах, принимавших леветирацетам (54%), вальпроаты (50%) и окскарбазепин (50%), существенно реже (р<0,05) — среди принимавших карбамазепин (39%). Суммарный показатель высокой эффективности лечения (снижение частоты приступов более чем на 75%) был выше в группах больных, получавших новые ПЭП (см. рис. 1). Несмотря на лучшие результаты терапии в группе больных, получавших топирамат, в этой же группе у 2 (4%) пациентов отмечено ухудшение течения эпилепсии в виде учащения СПП и ВГСП, не зарегистрированное в других группах. Отсутствие аггравации приступов у пациентов, принимавших карбамазепин, объясняется активным выявлением на этапе прескрининга при помощи ЭЭГ-мониторинга предикторов этого осложнения терапии — феномена вторичной билатеральной синхронизации. Самая высокая частота неэффективности терапии зафиксирована в группах, принимавших окскарбазепин (16%) и вальпроаты (14%), самая низкая — в группе, принимавшей леветирацетам (4%).

Рис. 1. Эффективность монотерапии различными ПЭП.
Побочные эффекты наиболее часто наблюдались при приеме вальпроатов (31%), несколько реже при лечении окскарбазепином (25%) и карбамазепином (25%). При приеме топирамата и леветирацетама этот показатель составил 16 и 12,5% соответственно. Между тем частота отмены ПЭП в связи с клинически значимыми побочными эффектами практически не различалась для вальпроатов, карбамазепина и топирамата, составив 7,6—9%. Следует отметить, что при применении топирамата у 36% больных констатировано снижение массы тела на 2—30 кг (в среднем — на 6,5±3,5 кг), но ни в одном случае это не привело к ухудшению здоровья или КЖ и отмене лечения, поэтому мы не включили это проявление в список побочных эффектов. Напротив, у 20% больных, получавших вальпроаты, отмечалось увеличение массы тела на 3—25 кг (в среднем — на 12±5,5 кг у пациентов, прошедших курс лечения 6 мес и более), и именно это явилось причиной отмены препарата у 5 (9,6%) больных, у которых показатель индекса массы тела значительно отклонился от нормы. Снижение уровня КЖ как единственная причина, потребовавшая отмены принимаемого ПЭП, зарегистрировано у 1 (2%) пациента, принимавшего вальпроаты, 2 (5%) – карбамазепин и 3 (5%) — топирамат. При лечении леветирацетамом и окскарбазепином побочные эффекты ни разу не стали причиной прекращения лечения.
При анализе результатов нейропсихологического тестирования с помощью опросника QOLIE-31 мы условно приняли балльную оценку менее 30 за соответствующую очень низкому КЖ, от 30 до 39 — низкому, от 40 до 49 — среднему, от 50 до 59 — хорошему, свыше 60 баллов — высокому КЖ.
При сравнении итогового показателя КЖ больных разных групп наибольшее количество пациентов, оценивших свое КЖ как высокое, отмечено в группах, получавших леветирацетам (83,3%) и окскарбазепин (72%). У больных, принимавших топирамат, карбамазепин и вальпроаты, этот показатель соответствовал хорошему КЖ, составив 59, 53 и 52% соответственно. Низкие оценки КЖ не были получены ни в одном случае после приема леветирацетама. При приеме окскарбазепина, топирамата, карбамазепина и вальпроатов такие оценки были у 6, 11, 16,5 и 17% больных соответственно. Таким образом, больные, получающие ПЭП нового поколения, в среднем оценивали свое КЖ более высоко, что, несомненно, является отражением высокой эффективности и хорошей переносимости этих препаратов. Результаты сравнительной оценки суммарного показателя КЖ в группах представлены на рис. 2.
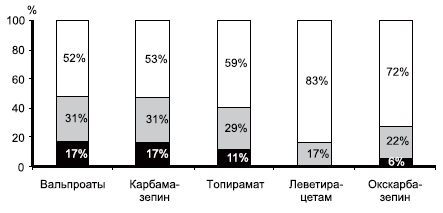
Рис. 2. Сравнительная оценка суммарного показателя КЖ в группах больных, принимавших различные ПЭП, в соответствии с тестом QOLIE-31.
Серой части столбцов соответствует низкое, черной — среднее, белой — высокое КЖ.
Данные, полученные при анализе зависимости показателей КЖ от терапевтического эффекта, свидетельствуют о значительном влиянии эффективности проводимой терапии на КЖ больных эпилепсией.
Таким образом, наличие приступов является важным фактором снижения КЖ. При анализе показателей КЖ пациентов в зависимости от типа приступов достоверно более низкие показатели КЖ получены у пациентов с СПП (р<0,01). В меньшей степени КЖ снижали ВГСП (р<0,05). Не было выявлено статистически значимых различий в группах пациентов с ППП и ремиссией заболевания. Сильная корреляционная связь КЖ от эффекта терапии в группе пациентов, получавших леветирацетам, может быть объяснена очень хорошей переносимостью этого ПЭП.
Результаты анализа показателей КЖ больных эпилепсией в зависимости от наличия или отсутствия побочных эффектов терапии показали, что у пациентов с побочными эффектами во всех группах отмечались более низкие оценки показателей КЖ по всем сферам опросника, однако уровня статистической достоверности они достигали только в группе, принимавшей вальпроаты, в разделах общее КЖ, энергичность/утомляемость, когнитивные функции. Больные этой группы, имеющие побочные эффекты от терапии, оценили свое КЖ значительно ниже (45,6±2,4), чем больные этой же группы без побочных эффектов (57,7±1,7; р<0,05). В других группах такой зависимости не наблюдалось, что, по-видимому, связано с бо льшим фрустрирующим воздействием специфических побочных эффектов вальпроатов. Так, исключительное влияние на показатели общей оценки КЖ имели прогрессирующая прибавка массы тела и алопеция, негативное психоэмоциональное воздействие которых часто не соответствовало выраженности самого побочного эффекта. Снижение массы тела, с высокой частотой встречающееся при лечении топираматом, напротив, часто оценивалось позитивно, существенно реже сопровождалось эмоциональным дистрессом и наблюдалось преимущественно у мужчин молодого возраста. Психоэмоциональные расстройства, развивающиеся по различным причинам, имели значимое влияние на показатели КЖ. Частота их встречаемости в исследуемых группах в форме тревожных и депрессивных расстройств различной модальности — клинически выраженных и субклинических представлена в табл. 2.
Таблица 2. Частота психоэмоциональных расстройств (%) по шкале HADS
| Препарат | Расстройства | Тревога | Депрессия | ||||||
|---|---|---|---|---|---|---|---|---|---|
| субклини- ческие |
клини- ческие |
отсутст- вуют |
субклини- ческие |
клиниче- ские |
отсутст- вуют |
субклини- ческие |
клини- ческие |
||
| Вальпроаты | 14,3 | 21,4 | 73,8 | 7,1 | 19,1 | 78,6 | 11,9 | 9,5 | |
| Карбамазепин | 12,5 | 16,6 | 75 | 16,7 | 8,3 | 79,2 | 12,5 | 8,3 | |
| Топирамат | 28,1 | 21,8 | 71,9 | 12,5 | 15,6 | 62,5 | 31,3 | 6,2 | |
| Леветирацетам | 16,7 | — | 83,3 | 16,7 | — | 100 | — | — | |
| Окскарбазепин | 12,5 | 8,3 | 75 | 16,7 | 8,3 | 83,3 | 12,5 | 4,2 | |
Психоэмоциональные расстройства в форме депрессии и тревоги в клинически выраженной и субклинической форме наиболее часто отмечались у больных, принимавших топирамат (49,9%), карбамазепин (29,1%) и вальпроаты (35,7%), существенно реже — среди получавших окскарбазепин (20,8%) и леветирацетам (16,7%). В группе пациентов, получавших леветирацетам, клинически выраженных форм психоэмоциональных нарушений не встречалось вообще. Тревожные расстройства преобладали над депрессивными несущественно и отмечались преимущественно в форме сочетанного тревожно-депрессивного синдрома. Были выявлены отрицательные корреляционные связи (сильные и средней силы) между аффективными расстройствами и практически всеми сферами опросника QOLIE-31: чем выше была оценка по шкале HADS, тем ниже больные оценивали свое КЖ. У больных с продолжающимися приступами аффективные расстройства встречались достоверно чаще, чем у лиц с ремиссией (р<0,005). В большей степени это касалось СПП и ВГСП, при которых больные имели достоверно более высокий уровень тревоги и депрессии (р<0,05), чаще отмечая тревожные опасения и страх ожидания новых приступов. Во всех группах отмечалась тенденция к более высоким оценкам по шкале HADS у больных с побочными эффектами терапии, однако статистической достоверности эта связь достигала только у получавших топирамат и препараты вальпроевой кислоты.
Безусловно, психотравмирующим воздействием обладают не только факторы, связанные с лечением. Парный анализ внутри групп продемонстрировал более высокую степень психоэмоциональной дизадаптации у инвалидов по сравнению с лицами, не имеющими инвалидности. Причем выраженность дизадаптации у этих больных, как правило, не коррелировала с тяжестью заболевания и частотой приступов. Достоверно ниже у них оказался и итоговый балл КЖ (р<0,05). Эмоциональный дистресс и итоговый показатель КЖ у трудоустроенных и учащихся пациентов был достоверно выше, чем у пациентов, не участвующих в трудовом или учебном процессе. Достоверно более высокие показатели КЖ были получены у лиц, не состоящих в браке (р<0,05). Такие результаты могут быть связаны с отрицательным опытом реагирования на болезнь окружающих, в том числе членов семьи (супругов).
Таким образом, результаты проведенного сравнительного исследования влияния современных ПЭП на КЖ больных эпилепсией продемонстрировали в среднем более высокие показатели у пациентов, принимавших ПЭП новых поколений, коррелирующую с более высокой эффективностью и переносимостью терапии. Наибольшую противоприступную эффективность среди всех анализируемых ПЭП продемонстрировал топирамат, частота клинически значимых побочных эффектов и отмены лечения при применении которого не отличали его от традиционных ПЭП, а частота выявления психоэмоциональных расстройств была достоверно выше, чем у больных, принимавших карбамазепин (p<0,05), леветирацетам и окскарбазепин (p<0,01). Итоговый показатель КЖ у больных, принимавших топирамат, был оценен как хороший, однако по своему абсолютному значению он был ближе к оценкам больных из групп, получавших леветирацетам и окскарбазепин (высокое КЖ), чем к оценкам пациентов, принимавших вальпроаты и карбамазепин (хорошее КЖ).
Достоверно лучшие показатели КЖ продемонстрировали пациенты, принимавшие леветирацетам, противоприступная эффективность которого несущественно уступала только топирамату. Общая частота побочных эффектов была самой низкой, сопоставимой с показателями, демонстрируемыми топираматом, однако их выраженность была незначительной и ни разу не привела к отмене препарата. Выраженность психоэмоциональных расстройств не выходила за рамки субклинических нарушений. Оценки КЖ больных, получавших окскарбазепин, приближались к показателям леветирацетама, уступая лишь по показателю психоэмоциональной фрустрированности.
Литература
- Гехт А.Б., Авакян Г.Н., Гусев Е.И. Современные стандарты диагностики и лечения эпилепсии в Европе. Журн неврол и психиат 1999;7:4— 7.
- Зенков Л.Р. Некурабельные эпилепсии. Неврол журн 2001;4:4—10.
- Карлов В.А. Стратегия и тактика терапии эпилепсии сегодня. Журн неврол и психиат 2004;8:28—34.
- Незнанов Н.Г., Громов С.А., Михайлов В.А. и др. Эпилепсия, качество жизни, лечение. Ст-Петербург: ВМА 2005;294.
- Ушкалова Е.А. Влияние антиконвульсантов на качество жизни больных эпилепсией. Фарматека 2003;16:29—40.
- Berto P. Quality of life in patients with epilepsy and impact of treatments. Pharmacoeconomics 2002;20:1039—1059.
- Kendrick A. Quality of life. The clinical psychologists handbook of epilepsy: assesment and management. Eds. C. Cull, Goldstein. London—New York 1997;171—176.
- Kirby S., Sadler R.M. Injury and death as a result of seizures. Epilepsia 1995;36:25—28.
- McLaughlin D., Pachana N., Mcfarland K. Stigma, seizure frequency and quality of life: The impact of epilepsy in late adulthood. Seizure 2007.
- Scicutella A., Ettinger A.B. Treatment of anxiety in еpilepsy. Еpilep Behav 2002;3:10—12.
