Эффективность Кеппры в составе комплексной терапии при фармакорезистентной эпилепсии у взрослых
СтатьиОпубликовано в журнале:
Журнал неврологии и психиатрии, 7, 2005
В.А. Карлов, П.Н. Власов
Efficacy of keppra in combined therapy in pharmacoresistant adult epilepsy patients
V.A. Karlov, P.N. Vlasov
Кафедра нервных болезней лечебного факультета Московского государственного медико-стоматологического университета Проведен анализ эффективности леветирацетама (кеппры) при использовании в составе комплексной терапии у 31 больного парциальной труднокурабельной эпилепсией и у 2 больных идиопатической генерализованной эпилепсией (возраст пациентов 19—51 год). В 25,8% случаев достигнута медикаментозная ремиссия эпилепсии на период более 4 мес. Снижение частоты припадков более чем на 75% произошло у 12,9%, более чем на 50% — у 48,4% больных. Отсутствие эффекта и недостаточная эффективность отмечены только в 12,9% наблюдений. Установлена хорошая переносимость препарата. Отмена кеппры по причине побочных явлений имела место только в одном случае. Полученные результаты свидетельствуют о перспективности применения кеппры в эпилептологии и в частности при фармакорезистентной эпилепсии.
Ключевые слова: фармакорезистентная эпилепсия, леветирацетам (кеппра), эффективность, побочные проявления.
There were analyzed efficacy of keppra (Levetiracetam) in combined therapy in 31 patients with pharmacoresistant partial epilepsy and in 2 cases with idiopathic generalized epilepsy. During the 4 months 48,4% experienced at least a 50% reduction in the frequency of partial-oncet seizures, 12,9% at least a 75% reduction, and 25,8% demonstrated a seizure free. The combined therapy was ineffective only in 12,9%. The authors emphasize a good tolerability of keppra. There was only one case with side-effect, that demand cancel of Levetiracetam. The results obtained reveal effectiveness of keppra using in epileptology, in particular, in pharmacoresistant epilepsy.
Key words: pharmacoresistant epilepsy, Levetiracetam (Keppra), efficacy, side-effects.
Последние годы ознаменованы внедрением в клинику новых антиэпилептических препаратов (АЭП). Их синтез стимулируется высоким процентом (20—30) резистентных эпилепсии, широкой распространенностью политерапии (30—40%) и, естественно, стремлением создать препарат, с наилучшим соотношением эффективности и переносимости, характеризующийся широким спектром действия, простотой применения, отсутствием фармакокинетических взаимодействий и быстрым титрованием. Российская эпилептология, все глубже ассоциируясь с международной, участвует во многих проектах по изучению клинической эффективности вновь разработанных АЭП. Постоянно сокращается временной период между появлением нового АЭП и внедрением его в России. Так, из разработанных за последнее десятилетие препаратов, а это фелбамат (талокса), топирамат (топамакс), габапентин (нейронтин), тиагабин (габитрил), вигабатрин (сабрил), окскарбазепин (трилептал), зонисамид (эксцегран), леветирацетам (кеппра). Два — топамакс и кеппра уже широко используются в России. Фелбамат проходил клинические испытания в нашей стране, но был отозван производителем. Вигабатрин зарегистрирован Фармакологическим комитетом, но отсутствует в широкой продаже, окскарбазепин готовится к регистрации, остальные препараты проходят клиническое испытание.
Клинический опыт применения топамакса в России превышает 3 года, леветирацетама (кеппры) составляет около года. Кеппра является одним из последних АЭП, синтезированных и внедренных в клиническую практику: он лицензирован в США в 1999 г., в России в 2003 г. Несмотря на столь малый срок, число публикаций по его применению лавинообразно растет. На последнем европейском конгрессе по эпилептологии (Вена, 2004) при рассмотрении проблемы терапии эпилепсии наибольшее количество докладов было посвящено топамаксу и кеппре.
Основу молекулы кеппры составляет пятиугольное кольцо широко применяемого ноотропного средства — пирацетама. Химическая формула: (S)-alpha-ethyl-2-oxo-1-pyrrolidine acetamide. Препарат характеризуется хорошей растворимостью в воде, а следовательно, быстрой полной абсорбцией после перорального применения, линейностью фармакокинетики, отсутствием влияния на микросомальные ферменты печени и тем самым на метаболизм других лекарств (в том числе АЭП и оральных контрацептивов), чему способствует также малое связывание с белками крови [24]. Все это позволяет рассматривать кеппру как "идеальный" АЭП.
Особый интерес представляет то, что этот препарат создан на основе пирацетама и потому, помимо ноотропного, оказывает мощное антиэпилептическое действие. С этих позиций кеппру можно назвать уникальным АЭП, особенно если принять во внимание тот факт, что классические АЭП в той или иной степени сами обладают седативными свойствами и в ряде случаев отрицательно влияют на когнитивные функции.
Отличием действия кеппры является то, что она не меняет электрофизиологических характеристик неизмененных нейронов как in vitro, так и in vivo и в то же время подавляет эпилептические реакции патологически измененных. Иными словами, являясь высокоселективным АЭП, она подавляет только эпилептические разряды [20]. Точные механизмы влияния кеппры пока неизвестны. Предполагается, что препарат оказывает противоэпилептический эффект посредством влияния на ионные каналы (Ca2+, K+ возбуждающими и тормозными нейротрансмиттерными системами, отличным от действия других АЭП механизмом [11]. Показано наличие специфических церебральных рецепторов к препарату [25]. Он выводится почками преимущественно в неизмененной форме (более 66% от принятой дозы через 24 ч) и частично путем гидролиза (в тканях и крови) ацетамидной группы до неактивного метаболита. Период полувыведения составляет около 8 ч, что обусловливает адекватность двукратного приема препарата, с учетом его более длительной задержки в ЦНС [27].
Интересным представляется тот факт, что еще в 80—90-е годы XX столетия в периодических изданиях неоднократно рассматривался вопрос о возможности применения ноотропов при эпилепсии. Мы располагаем несколькими случаями высокоэффективного применения пирацетама в терапии статуса миоклонических эпилептических припадков (В.А. Карлов — собственные наблюдения).
Материал и методы
В анализ включены 31 больной труднокурабельной парциальной эпилепсией в возрасте 19—51 год и 2 пациента с идиопатической генерализованной эпилепсией.
Резистентными считали случаи неэффективной терапии с использованием многих АЭП в прошлом и во время настоящего исследования при применении одного или нескольких АЭП в предельных суточных дозах, не вызывавших выраженных побочных эффектов, в которых эпилептические припадки не исчезали и существенно снижали качество жизни.
Среди пациентов преобладали женщины — 24 (75,8%), что, видимо, определялось специфичностью научного направления кафедры в эпилептологии. Основной эпилептический очаг локализовался в височной зоне у 19 (61,3%), в лобной у 6 (19,4%) пациентов, в теменно-затылочной у 1 (3,2%) больного. У 5 (16,1%) больных идентификация эпилептического фокуса оказалась невозможной. У одного из этих пациентов из-за неадекватного состояния не удалось провести электроэнцефалографию при первичном обращении, а данные предыдущих аппаратных обследований не были представлены, хотя заболевание началось в детстве.
Соотношение симптоматических (42%) и криптогенных (58%) форм парциальной эпилепсии приближалось к 2:3. Грубые структурные изменения вещества головного мозга включали корковую дисплазию, рубцово-атрофические изменения, единичные и множественные кисты, гиппокампальный склероз.
Преобладали случаи с длительностью заболевания более 10 лет (75,8%). Наиболее часто регистрировалось сочетание парциальных и вторично-генерализованных эпилептических припадков (70,0%). Парциальные припадки без вторичной генерализации встречались значительно реже (16,1%), при этом частота их, как правило, была высокой. Мономорфные вторично-генерализованные припадки наблюдались в 9,7% случаев. У 1 (3,2%) пациента регистрировались мономорфные гипермоторные припадки сна (табл. 1).
Таблица 1. Клиническая характеристика больных парциальной эпилепсией
| Показатель | Количество больных | |
|---|---|---|
| абс. | % | |
| Длительность заболевания, годы: 5 5—10 более 10 |
4 3 24 |
12,9 9,7 75,8 |
| Характер припадков: парциальные без вторичной генерализации вторично-генерализованные сочетание парциальных и генерализованных гипермоторные припадки сна |
5 3 22 1 |
16,1 9,7 71,0 3,2 |
| Средняя частота припадков в месяц: простые, сложные парциальные и их сочетание сочетание парциальных игенерализованных |
До десятков в месяц Не менее 4 в месяц |
|
Как видно из табл. 2, в подавляющем большинстве случаев (80,7%) терапия проводилась двумя препаратами в различном сочетании как с индукторами микросомальных ферментов печени — карбамазепином, фенитоином и фенобарбиталом/бензоналом, так и с неиндукторами — вальпроевой кислотой, ламотриджином, топираматом и бензодиазепинами. Базовая монотерапия использовалась лишь в 16,1% случаев — как правило, при плохой переносимости АЭП (выраженные побочные явления вплоть до развития интоксикации при титровании второго препарата). Два ферментиндуцирующих препарата применялись в 25,8% случаев — такое сочетание позволяло добиваться наилучшего результата у конкретного пациента. Длительность приема фоновых АЭП до назначения кеппры составила не менее 3 мес. Суточные дозы и концентрации базовых АЭП во всех наблюдениях были достаточными.
Таблица 2. Фоновая терапия с труднокурабельной парциальной эпилепсией (до назначения кеппры)
| Базовая терапия | Количество больных | |
|---|---|---|
| абс. | % | |
| Один препарат | 5 | 16,1 |
| Два энзиминидуцирующих препарата | 8 | 25,8 |
| Два: индуктор+неиндуктор | 14 | 45,2 |
| Два неиндуктора (депакин+ламотриджин) | 3 | 9,7 |
| Три препарата | 1 | 3,2 |
Из изложенного видно, что подавляющее большинство наблюдений было представлено труднокурабельной височной эпилепсией с полиморфными припадками высокой частоты при длительности заболевания более 10 лет.
Первоначальная доза кеппры составила 1000 мг/сут при двукратном приеме. В случае недостаточной эффективности ее доводили до 2000 мг, а в отдельных случаях до 3000 мг. Увеличение дозы на 500 мг осуществляли еженедельно с учетом переносимости. При этом дозы базовых АЭП не меняли.
Помимо электроэнцефалографии, до назначения кеппры и после стабилизации состояния (через 2 и 3 мес), в те же сроки проводили оценку качества жизни по 5-балльной аналоговой шкале [4]. Учитывая, что основную группу больных составляли лица женского пола, определяли влияние препарата на менструальную функцию. Результаты
Данные об эффекте терапии приведены в табл. 3 и 4.
Таблица 3. Эффект терапии при применении кеппры в качестве дополнительного АЭП
| Припадки | Ремиссия | Урежение припадков | Отсутствие/ недостаточность эффекта |
|
|---|---|---|---|---|
| более чем на 75% | более чем на 50% | |||
| Парциальные без вторичной генерализации | 1 | 1 | 3 | |
| Вторично-генерализованные мономорфные | 2 | 1 | ||
| Сочетание парциальных и вторично-генерализованных | 7 | 3 | 10 | 2 |
| Гипермоторные припадки сна | 1 | |||
| Итого | 8 (25,8%) | 4 (12,9%) | 15 (48,4%) | 4 (12,9%) |
Таблица 4. Зависимость эффекта от дозы кеппры
| Суточная доза кеппры, мг | Ремиссия | Урежение припадков | Отсутствие/ недостаточность эффекта |
|
|---|---|---|---|---|
| более чем на 75% | более чем на 50% | |||
| До 1000 | 6 | 9 | 1 | |
| 1000—2000 | 2 | 4 | 6 | 2 |
| 2000—3000 | 1 | |||
| Итого | 8 (25,8%) | 4 (12,9%) | 15 (48,4%) | 4 (12,9%) |
Полного купирования припадков на период более 4 мес удалось достичь у 25,8% больных. При этом в 3/4 случаев ремиссия была достигнута уже при суточной дозе кеппры 1000 мг! В этой подгруппе преобладали криптогенные формы эпилепсии с височной локализацией эпилептического очага. Ремиссия зафиксирована у 1 больного с гиппокампальным склерозом, клинически проявлявшимся сочетанием простых и сложных парциальных припадков, и у 7 — с наличием до назначения кеппры как парциальных, так и генерализованных приступов.
Практически во всех наблюдениях с урежением припадков более чем до 75% изначальный эффект также регистрировался при суточной дозировке кеппры 1000 мг, однако ввиду его недостаточности дозу этого препарата увеличили до 1500—2000 мг/сут. Соотношение парциальных и вторично-генерализованных припадков при этом было сходным с таковым в подгруппе больных с ремиссией.
Основную подгруппу составили 15 (48,4%) больных, у которых частота эпилептических припадков уменьшилась более чем на 50%. В ней также преобладали пациенты с сочетанием парциальных (простых/ сложных) и вторично-генерализованных эпилептических припадков (10 человек). Среди больных с парциальными приступами такая степень улучшения была достигнута у 3, при моносимптомных вторично-генерализованных припадках — у 2.
Эффект кеппры при парциальной эпилепсии оказался недостаточным лишь у 4 (12,9%) больных. У одного с лобным фокусом были частые (до трех в неделю) вторично-генерализованные судорожные припадки во время сна, назначение кеппры в максимальной дозе (3000 мг/сут) не привело к выраженному снижению их частоты, структура припадков также не изменилась, однако был зафиксирован выраженный нормотимический эффект, поэтому пациент продолжает принимать кеппру по 2000 мг/сут. У другого пациента с грубой кортикальной дисплазией практически еженедельно регистрировался статус генерализованных судорожных припадков и суточная доза была доведена до 2500 мг. Частота приступов снизилась незначительно также у больного с симптоматической парциальной эпилепсией с гипермоторными припадками сна. И только в одном случае препарат был отменен из-за побочных проявлений: тошнота, головная боль, головокружение, тремор возникли уже при дозе 500 мг/сут. У этого больного на протяжении трех предшествовавших лет наблюдалось тяжелое депрессивное состояние, из которого он только перед исследованием вышел.
У одного больного в период титрования дозы отмечались легкая сонливость и чувство внутренней тревоги, которые исчезли спустя 5 дней. И в одном наблюдении имело место снижение массы тела на 5 кг за 3 мес.
Анализ ЭЭГ после применения кеппры при парциальной эпилепсии выявил существенное снижение индекса пароксизмальной активности. В большинстве наблюдений генерализованная эпилептиформная активность замещалась фокальной. В 7 (22,6%) случаях после присоединения кеппры генерализованная эпилептиформная активность редуцировала до отдельных фокальных острых волн лобной локализации (см. рисунок).
Применение 5-балльной аналоговой шкалы практически во всех случаях (за исключением трех, когда кеппра оказалась недостаточно эффективной) выявило повышение качества жизни пациентов. Очень важен тот факт, что положительный клинический эффект в отдельных случаях достигался даже при недостаточной эффективности препарата в отношении припадков, и именно благодаря его ноотропному действию.
Обсуждение
Кеппра продемонстрировала высокую эффективность у больных медикаментозно-резистентной эпилепсией при использовании в качестве дополнительного препарата в комбинации с базовыми АЭП разного механизма действия. Медикаментозная ремиссия на период более 4 мес достигнута в 25,8% наблюдений, урежение припадков более чем на 75% — в 12,9%, более чем на 50% — в 48,4%. Недостаточный эффект либо его отсутствие зафиксированы лишь в 12,9% наблюдений. Полученные данные отражают несколько более высокую эффективность препарата по сравнению с показателями обзора, проведенного на материале исследования 1400 пациентов с разными формами резистентной эпилепсии, где полная ремиссия была достигнута у 17,2% пациентов, урежение приступов более чем на 50% — у 49% [26]. Это частично может объясняться недостаточным сроком проспективного наблюдения. На чрезвычайно высокую эффективность кеппры в качестве дополнительного средства терапии труднокурабельной парциальной эпилепсии обращают внимание и другие авторы [12, 30]. По их данным, эффективность кеппры возрастала параллельно увеличению ее суточной дозы с максимальным клиническим эффектом у взрослых при дозе 3000 мг/сут.
Препарат оказался эффективным при сочетании как с ферментиндуцирующими АЭП, так и с «неиндукторами». В литературе высказано убеждение, что существующее положение, согласно которому в случае политерапии следует подбирать АЭП с разными механизмами действия, не находит подтверждения на практике [29], а основой является эмпирический опыт врача [15]. У всех больных до настоящей схемы терапии были апробированы различные комбинации АЭП, в том числе у некоторых применялись такие препараты последней генерации, как топирамат, тиагабин и габапентин, однако их эффективность также оказалась недостаточной.
Поскольку препарат не метаболизируется в печени и большая его часть (2/3) выделяется в неизмененном виде, его можно без особых опасений назначать в качестве дополнительного АЭП. Возможность широкого применения кеппры в качестве add-on препарата также обусловлена тем, что при его назначении феномен парадоксального учащения эпилептических припадков наблюдается крайне редко — не чаще, чем при использовании плацебо [17]. В настоящем исследовании парадоксального учащения припадков не отмечено ни в одном случае. В литературе учащение припадков при приеме кеппры описано у 23,2% больных, а именно у детей и подростков [14].
Очень важным показателем эффективности терапии явилось то, что пациенты отмечали повышение качества жизни, вероятно, в связи с нормотимическим и ноотропным действием кеппры. Положительное влияние препарата на когнитивные функции зафиксировано при применении его у детей и подростков с трудностями обучения [8].
Применение кеппры в составе комплексной терапии труднокурабельной эпилепсии сопровождалось хорошей переносимостью, что согласуется с данными других исследователей [19]. Только в одном случае потребовалась отмена препарата уже в дозе 500 мг/сут из-за появления тошноты, головной боли, головокружения и тремора (см. выше). На осторожность применения кеппры у пациентов с психическими отклонениями в виде депрессивных, психотических и поведенческих нарушений в анамнезе обращают внимание многие авторы [11, 21].
Одна больная похудела на 5 кг за последние 3 мес, в дальнейшем масса тела у нее стабилизировалась. Сама пациентка объясняет данное обстоятельство ведением более активного образа жизни. Повышение работоспособности с улучшением когнитивных функций обусловлено, вероятно, ноотропным действием пирролидонов. По результатам другого исследования [10], в 2 случаях из 98 за 6 мес наблюдения отмечалось повышение массы тела.
Среди причин отмены кеппры, согласно полученным в настоящем исследовании данным, на первом месте недостаточная эффективность препарата, выявленная у 2 (6,5%) больных. Это ниже показателей, приведенных в других публикациях [28]. Еще в одном наблюдении, несмотря на недостаточность эффекта кеппры, больной продолжил ее прием ввиду улучшения качества жизни. Таким образом, после 4 мес приема препарата его продолжали принимать 90,3% больных. В литературе описаны наблюдения применения кеппры без каких-либо побочных проявлений на протяжении более 8 лет [22].
Мы располагаем несколькими наблюдениями эффективности препарата в качестве монотерапии при парциальной эпилепсии, однако материал еще накапливается. Имеются сообщения о последующем переводе больных на монотерапию кеппрой [9], о назначении препарата при впервые диагностированной парциальной [6] и первично-генерализованной [13] эпилепсии.
Учитывая, что в подавляющем большинстве наблюдений кеппра использовалась у женщин, мы проанализировали ее влияние на репродуктивную функцию. Так как препарат является «неметаболизирующимся», логично было предположить, что он не будет оказывать влияния на менструальную функцию. Ни у одной из наших больных изменения характеристик менструального цикла зарегистрировано не было, однако малочисленность наблюдений пока не позволяет сделать обоснованных выводов. Опубликованные данные [7] свидетельствуют о том, что снижения эффективности оральных контрацептивов при совместном использовании с кеппрой не происходит. Ввиду короткого периода использования препарата в клинике регистр по тератогенному профилю кеппры еще накапливается, однако экспериментальные данные свидетельствуют о низком уровне ее тератогенности [31]. Можно присоединиться к мнению S. Arroyo и P. Crawford [7] о возможности использования кеппры во время беременности, если эффективность терапии существенно превышает риск применения препарата [5]. Кроме того, пирролидоны достаточно широко используются в акушерской практике при различных осложнениях беременности. Что касается периода грудного вскармливания, то следует учитывать низкую связывающую способность кеппры протеинами плазмы крови, следовательно, он должен поступать с молоком матери к ребенку. Указанные выше характеристики кеппры могут служить основанием для дальнейшего изучения этого вопроса.
Препарат оказался эффективным при использовании у пожилых людей. Частота побочных проявлений в этой группе не отличалась от таковой у пациентов молодого и зрелого возраста, это были главным образом проявления со стороны ЦНС (сонливость, астения, головокружение). Согласно данным литературы, снижения дозы препарата в таких случаях, как правило, не требуется, если у больного не нарушена выделительная функция почек [16].
Эффективность кеппры, как говорилось выше, была изучена также у двух больных с идиопатической генерализованной эпилепсией. Обычно это курабельная форма заболевания, однако не всегда. Поэтому приводим эти наблюдения.
Больная Я., 22 лет. Приступы с 16 лет. Генерализованные тонико-клонические пробуждения и частые — почти ежедневные миоклонии пробуждения — роняет предметы. На ЭЭГ регистрируются характерные разряды генерализованных билатерально синхронных симметричных полиспайк-волн. Диагностирована ювенильная миоклоническая эпилепсия. Предшествующее лечение депакином и топамаксом способствовало учащению и усилению миоклоний, а также появлению признаков непереносимости препаратов, ввиду чего депакин пришлось отменить. Другие АЭП, в том числе суксилеп, оказались неэффективны. Миоклонии были полностью устранены и ЭЭГ нормализовалась после назначения кеппры в суточной дозе 1000 мг.
Больная К., 22 лет. Болезнь дебютировала в 17 лет миоклониями век. Однако к врачу обратилась только через 2 года после развития генерализованного тонико-клонического припадка. Моргания частые спонтанные или провоцируемые фотогенно. Они наблюдались на приеме и во время записи ЭЭГ при проведении фотостимуляции: частое мигание (трепетание век) с закатыванием глазных яблок вверх. Приступ сопровождается возникновением электрографических коррелятов типичного абсанса, при этом сознание сохранено, и лишь при длительности припадка более 5 с нарушается контакт с больной. Диагностирована идиопатическая генерализованная эпилепсия в форме миоклонии век с абсансами. Концентрация депакина в плазме крови доведена до 100 мкг/мл. Доза топамакса составила в конечном итоге 300 мг/сут при массе тела больной около 50 кг. Эффективной оказалась доза кеппры 500 мг 2 раза в сутки с последующим переводом на монотерапию кеппрой. Отмечено полное устранение приступов и резкое угнетение эпилептиформной активности на ЭЭГ.
Серьезной проблемой при устранении припадков и обсуждении тактики дальнейшего ведения больного могут быть сохраняющиеся и даже нарастающие эпилептиформные изменения на ЭЭГ. Приводим наблюдение, когда прогрессирующие изменения на ЭЭГ удалось устранить только с помощью кеппры.
Больная М., 37 лет. Перинатальный анамнез не отягощен, семейный также. В 10-летнем возрасте перенесла солнечный удар, было несколько судорожных приступов. В последующем чувствовала себя здоровой. Припадки возобновились в 18 лет, когда пациентка училась в институте, и повторялись 1 раз в два года: генерализованные судорожные припадки бодрствования. Были ремиссии — до 5 лет. Во время одного из припадков получила травму головы, предплечья. Три года назад был бессудорожный приступ: отключалась, падала. Предпоследний судорожный приступ несколько лет назад. Месяц назад ехала на лошади, «отупела», продолжала ехать, затем упала, приступ амнезировала.
Соматически здорова. Психика нормальна. В неврологическом статусе отклонений нет. При МРТ в режиме Т2 обнаружен небольшой очаг повышенной плотности в левой теменной доле, расцененный как последствия ушиба головного мозга.
На ЭЭГ после предъявления нагрузок зарегистрирован коррелят простого абсанса. При полиграфии ночного сна в стадии 2 фазы медленного сна зарегистрирована спайк-волновая активность лобной локализации.
Назначен депакин, начиная с дозы с 300 мг 1 раз в сутки, постепенно дозу повышали до 900 мг/сут, на фоне чего развился генерализованный судорожный приступ. Доза депакина была увеличена до 1500 мг/кг (масса тела больной более 75 кг).
На ЭЭГ резко отрицательная динамика: повторяющиеся после начала гипервертиляции корреляты типичных абсансов. Переведена на депакин в сочетании с топамаксом. В течение 1,5 лет припадков не было, однако ЭЭГ не нормализовалась, более того, отмечена явная тенденция к нарастанию изменений. Регистрировались частые пароксизмы коррелятов типичного абсанса, провоцировавшиеся как спонтанно, так и при проведении гипервентиляции и ритмической фотостимуляции. Назначена кеппра в дозе 500 мг 2 раза в сутки. В течение месяца ЭЭГ полностью нормализовалась (см. рисунок). Топамакс отменен. Депакин пока сохранен в дозе 300 мг 2 раза в сутки.
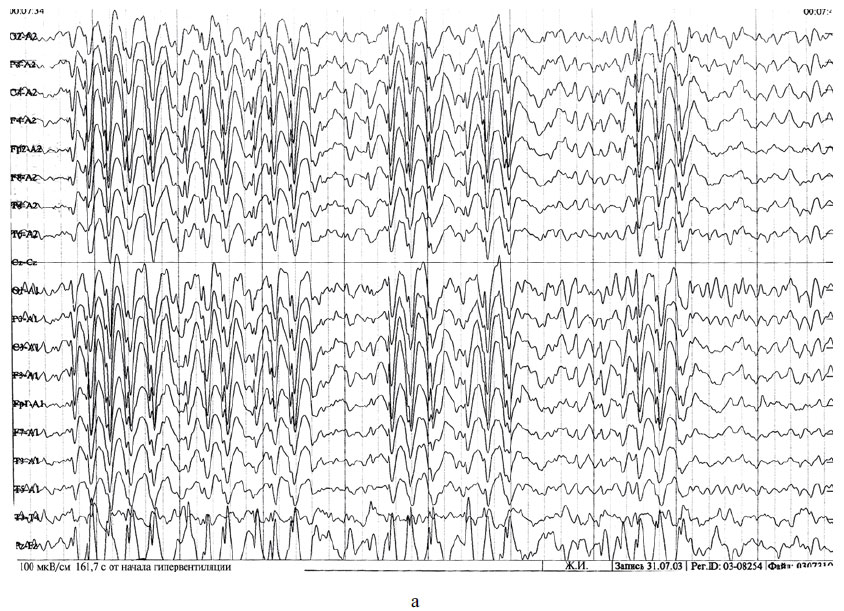
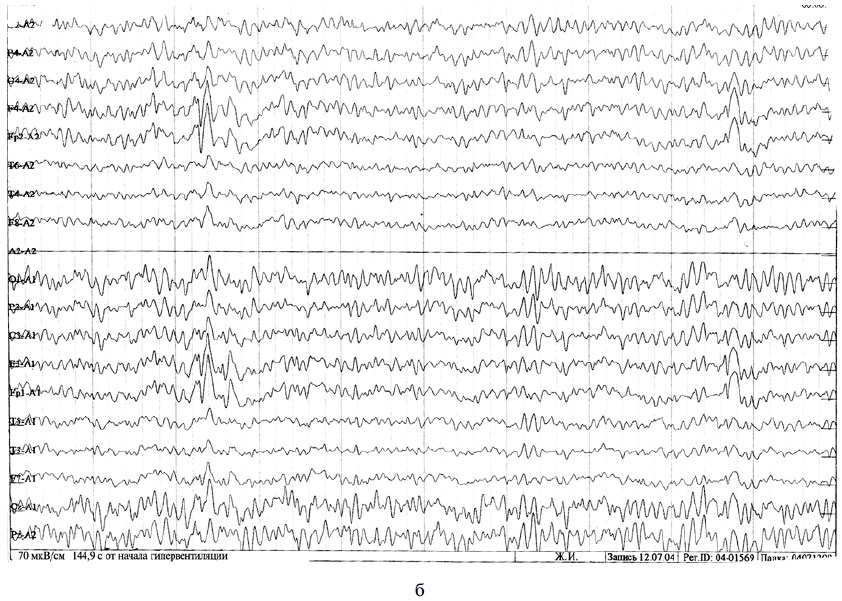
ЭЭГ больной 37 лет с коррелятами абсанса на фоне комбинированной терапии (а) и после (б) присоединения кеппры в дозе 1000 мг/сут (депакин+кеппра).
Это наблюдение интересно также лобной локализацией очага, вызывающего, в частности, абсансную активность на ЭЭГ, что уже давно является предметом нашего специального исследования [1—3]. О нормализующем влиянии кеппры на ЭЭГ у больных эпилепсией сообщалось в литературе [18].
Таким образом, резюмируя результаты проведенного исследования, можно констатировать высокую эффективность кеппры в отношении парциальных фармакорезистентных форм эпилепсии при назначении в качестве дополнительного к разным АЭП препарата у больных с парциальными и генерализованными припадками. Крайне важен тот факт, что у большинства пациентов он оказался эффективным уже в дозе 1000 мг. Это отражает высказанное в литературе убеждение в том, что если АЭП эффективен, то его действие проявляется уже при невысоких и средних терапевтических дозах [23]. Ни в одном из наблюдений не зафиксировано парадоксальной реакции на введение кеппры в виде учащения или появления другого типа приступов. Положительный клинический эффект коррелировал с улучшением характеристик ЭЭГ. Переносимость препарата была превосходной, за исключением одного наблюдения — у пациента с изначальными психическими отклонениями. Зарегистрированные побочные эффекты развились со стороны ЦНС, кроме одного случая снижения массы тела. У подавляющего большинства больных отмечено улучшение качества жизни, даже при недостаточной эффективности кеппры в отношении припадков. Препарат не влияет на здоровье женщины, и обычно не требуется снижения его дозы у больных старшего возраста. Высокая эффективность кеппры при использовании в составе комплексной терапии свидетельствует о перспективности ее применения при разных формах эпилепсии. По клиническим (эффективность, переносимость), фармакокинетическим и фармакодинамическим характеристикам кеппра приближается к «идеальному» АЭП.
Литература
- Гнездицкий В.В., Карлов В.А. Носкоеа Т.А., Тупикоеа Е.В. Соотношение дипольной локализации компонента спайк-волнового комплекса при разных формах эпилепсий. Восточно-европейская конференция, 3-я: Труды. Гурзуф 2001;19—20.
- Карлов В.А., Петренко СЕ. Значение функционального состояния орбитофронтальной коры и хвостатого ядра в эпилептоге-незе. Нейрофизиологические механизмы эпилепсии. Тбилиси: Мецниереба 1980;221—228.
- Карлов В.А., Овнатанов Б.С. Медиобазальная кора и эпилепто-генез. Журн невропатол и психиат 1987;87:6:805—811.
- Карлов В.А., Власов П.Н., Хабибова А.О. Возможности формализованных методов в обьективизации динамики тяжести течения эпилепсии. Неврол вестн 1997;29:1—2:30—33.
- Карлов В.А., Власов П.Н., Краснопольский В.И., Петрухин В.А. Особенности терапевтической тактики при эпилепсии во время беременности. Рос вестн акуш гин 2002;2:63—68.
- Alsaadi T.M., Thieman C. Levetiracetam monotherapy for newly diagnosed epilepsy patients. Seizure 2003;12:154—156. 7. Arroyo S., Crawford P. Safety profile of levetiracetam. Epileptic Dis 2003;5:Suppl 1:57—63.
- Aylett S.E., Parmeggiani L., Berry D. Levetiracetam in children and teenagers with epilepsy and learning disability. Epilepsia 2002;43:604.
- Ben-Menachem E., Falter U. Efficacy and tolerabilityof levetiracetam 3000 mg/d in patients with refractory partial seizures: a multicenter, double-blind, responder-selected study evaluating monotherapy. Epilepsia 2000;41:1276—1283.
- Betts T., Yarrow H., Greenhill L., Barrett M. Clinical experience of marketed Levetiracetam in an epilepsy clinic — a one year follow up study. Seizure 2003;12:136—140
- Brodie M.J., French J.A. Role of levetiracetam in the treatment of epilepsy. Epileptic Dis 2003;5:Suppl 1:65—72.
- Cereghino J.J., Biton V., Abou-Khali B. et al. Levetiracetam for partial seizures: results of a double-blind, randomized clinical trial. Neurology 2000;55:236—242.
- Cohen J. Levetiracetam monotherapy for primary generalised epilepsy Seizure 2003;12:150—153.
- Coppola G., Mangano S., Tortorella G. et al. Levetiracetam during 1-year follow-up in children, adolescents, and young adults with refractory epilepsy. Epilepsy Res 2004;59:35—42.
- Deckers C.L.P., Genton P., Sills G.J., Schmidt D. Current limitations of antiepileptic drug therapy: a conference review. Epilepsy Res 2003;53:1—17.
- French J. Use of levetiracetam in special population. Epilepsia 2001;42:Suppl 4:40—43.
- French J., Edrich P., Cramer J.A. A systematic review of the safety profile of levetiracetam: a new antiepileptic drug. Epilepsy Res 2001;47:77—90.
- Gallagher M.J., Eisenman L.N., Brown K.M. et al. Levetiracetam reduces spike-wave density and duration during continuous EEG monitoring in patients with idiopathic generalized epilepsy. Epilepsia 2004;45:90—91.
- Harden C. Safety profile of levetiracetam. Epilepsia 2001;42:Suppl 4:36—39.
- Klitgaard H., Matagne A., Gobert J., Wulfert E. Evidence for unique profile of levetiracetam in rodent models of seizures and epilepsy. Eur J Pharmacol 1998;353:191—206.
- Kossoff E.H., Bergey G.K., Freeman J.M. et al. Levetiracetam psychosis in children with epilepsy. Epilepsia 2001;42:1611—1613.
- Krakow K., Walker M., Otoul C. et al. Long-term continuation of levetiracetam in patients with refractory epilepsy. Neurology 2001;56:1772—1774.
- Kwan P., Brodie M. Early identification of refractory epilepsy. N Engl J Med 2000;342:314—319.
- Leppik I.E. The place of levetiracetam in the treatment of epilepsy. Epilepsia 2001;42:Suppl 4:44—45.
- Noyer M., Gillard M., Matagne A. et al. The novel antiepileptic drug levetiracetam appears to act via a specific binding site in CNS membranes. Eur J Pharmacol 1995;36:Suppl 2:137—146.
- Olwen G.O. The SKATE study: interim analysis. Int J Clin Pract 2003;57:544—545.
- Perucca E., Johannessen S.I. The ideal pharmacokinetic properties of an antiepileptic drug: how close does levetiracetam come? Epileptic Dis 2003;5:Suppl 1:17—26.
- Privitera M. Efficacy of levetiracetam: a review of three pivotal clinical trials. Epilepsia 2001;42:Suppl 4:31—35.
- Schmidt D. Strategies to prevent overtreatment with antiepileptic drugs in patients with epilepsy. Epilepsy Res 2002;52:61—69.
- Shorvon S.D., Lowenthal A., Janz D. et al. Multicenter double-blind, randomized, placebo-controlled trial of levetiracetam as add-on therapy in patient with refractory partial seizures. Epilepsia 2000;41:1179—1186.
- Spiegelstein O., Isoherranen N., Finnell R.H. et al. Teratogenicity of levetiracetam and its enantiomer (R) alpha-ethyl-2-oxopyrrolidine acetamide in mice. Epilepsia 2001;42:Suppl 7:252—253.
