Ноотроп Ноопепт: Введение
СтатьиОглавление | Следующий раздел
ВВЕДЕНИЕ
Спектр состояний, при котором имеются нарушения основных когнитивных функций (внимание, память, способность к анализу ситуации и принятию решений, пространственная ориентация), весьма широк. Он включает когнитивный дефицит при инсультах и хронической церебро-васкулярной недостаточности, травме мозга, различных хронических поражениях мозга нейро-дегенеративного характера, нейроинфекциях, постгипоксических энцефалопатиях, хроническом алкоголизме, задержке умственного развития у детей. Распространенность когнитивной патологии так же как и разнообразие ее индивидуальных проявлений у различных людей диктуют необходимость расширения арсенала веществ, нормализующих нарушенные когнитивные функции.
Ноотропные вещества, применяемые в настоящее время для лечения когнитивного дефицита, имеют ряд ограничений и недостатков. Родоначальник класса ноотропов, пирацетам, в значительном числе случаев недостаточно эффективен. Отсутствуют убедительные данные о специфических механизмах его действия. Препараты, наиболее часто применяемые для лечения когнитивного дефицита при болезни Альцгеймера, имеют ряд недостатков. Так, ингибиторы ацетилхолинэстеразы характеризуются высокой общей токсичностью, блокаторы NMDA-каналов вызывают побочные нейро-психотические симптомы. Недостаточность мнестических функций, возникающая на фоне нейротравмы, инсультов, сенильных нарушений сосудистого и нейродегенеративного характера протекает на фоне выраженных структурных изменений мозговой ткани. Для лечения этих состояний целесообразно применение препаратов, сочетающих ноотропную активность с нейропротективной. Однако, большинство нейропротективных веществ, применяемых в настоящее время в практической медицине (антиоксиданты, антагонисты кальциевых каналов), лишено прямого положительного влияния на мнестические функции. Церебральные вазодилататоры, вызывающие «обкрадывание» мозговой ткани за счет выраженных изменений общей гемодинамики, могут вести даже к ухудшению когнитивной активности, особенно у пожилых людей.
Положительное влияние ряда известных нейропептидов на когнитивные процессы обусловило поиск средств коррекции их нарушений среди этих эндогенных регуляторов. Попытки практического применения самих мнемотропных пептидов (вазопрессина, АКТГ и др.) оказались непродуктивными в связи с низкой биологической устойчивостью и плохой проницаемостью для них ГЭБ. В качестве рациональных подходов к преодолению этих затруднений описаны такие приемы как использование активных фрагментов сложных пептидов, модификации их структуры, например введением D-изомеров аминокислот, стабилизирующих группировок. Оригинальный подход, развиваемый в НИИ Фармакологии РАМН в течение почти двух десятилетий, может быть охарактеризован как дизайн коротких пептидов на основании имитации структуры непептидного нейротропного средства.
Этот подход был использован и при создании ноотропного дипептида Ноопепт (ГВС-111).
Пирацетам (N-карбамидометилпирроллидон-2), первый представитель класса ноотропов -веществ, избирательно усиливающих процессы обучения и памяти, был открыт бельгийской фармацевтической фирмой UCB в 1972 году случайно среди соединений, запатентованных в 1966 году в качестве средств для борьбы с укачиванием. Поскольку эти соединения были синтезированы как производные гамма-аминомасляной кислоты, за пирацетамом надолго закрепилось мнение о его ГАМК-ергическом механизме действия. Пирацетам является экзогенным соединением и практически полностью выводится из организма в неизменном виде, так как для его превращения нет подходящих ферментов. Ноотропные эффекты пирацетама довольно слабые как по глубине, так и по дозам. Для достижения заметного эффекта пациенты должны принимать пирацетам месяцами до 8 грамм в день. Тем не менее, в течение двух десятилетий пирацетам был единственным ноотропом. Затем были синтезированы и вошли в практику аналоги пирацетама - анирацетам, прамирацетам, этирацетам, оксирацетам и другие так называемые рацетамы. Действующие дозы были снижены, но при этом увеличилась токсичность и появились нежелательные побочные эффекты. В 80-е годы класс ноотропов стал «модным», и для его расширения к нему были добавлены вещества, по сути не являющиеся ноотропами, поскольку не имеют селективного действия на когнитивные процессы.
К середине 80-х годов ГАМК-ергический механизм действия пирацетама был отвергнут, но другой механизм не был выявлен.
В 1985 году мы выдвинули концепцию о том, что пирацетам является экзогенным аналогом некоторого эндогенного пептида, участвующего в регуляции процессов обучения и памяти. Он мог быть как миметиком короткого пептида, так и миметиком активного фрагмента более длинного нейропептида. Основой для этой концепции явилось структурное сходство пирацетама с довольно яркими по биологической роли пирролидин-содержащими аминокислотами пролином и пироглутаминовой кислотой (рис.1). В молекуле пирацетама имеется пирролидиновый цикл, который есть как у пролина, так и у пироглутаминовой кислоты, и карбонил при втором атоме углерода, имеющийся у пироглутаминовой кислоты. Кроме этих фрагментов аминокислот, при атоме азота есть ацетамидная группа, которая может имитировать амид глицина.
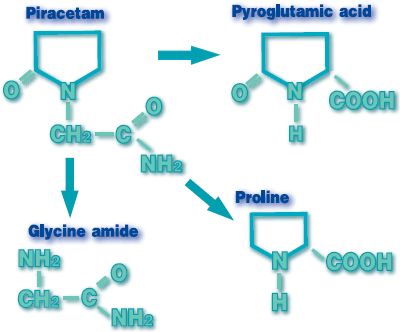
Помимо этого, пирацетам имеет определенное сходство по характеру фармакологических эффектов с регуляторными пептидами.
Это сходство выражается, во-первых, в нормализующем характере действия. Пирацетам действует тем лучше, чем больше исходное повреждение когнитивных функций. Во-вторых, сходство проявляется в модуляторном отношении с классическими нейромедиаторами. Под его действием, как и под действием некоторых нейропептидов, активируется глютаматергическая и холинергическая системы. Дозовая зависимость пирацетама является куполообразной, что также характерно для регуляторных пептидов, хотя и не является исключительно их чертой. Самое главное сходство состоит в том, что пирацетам регулирует целостную функцию ЦНС, подобно тому, как нейропептиды регулируют такие целостные функции, как память, тревога, пищевое, половое, агрессивное и другие виды поведения животных и человека.
Низкий молекулярный вес пирацетама предполагает, что и его пептидный аналог должен быть низкомолекулярным коротким пептидом, скорее всего дипептидом.
Регуляторные пептиды действуют в чрезвычайно низких дозах и не обладают токсическими эффектами. В связи с этим создание короткого пептида с ноотропной активностью могло положить начало новому классу суперактивных и нетоксичных ноотропов. Отсутствие токсичности явилось бы простым следствием того, что такие соединения целиком построены из природных аминокислот и полностью до них метаболизируются в крови под действием природных ферментов. Нагрузка на печень в этом случае отсутствует. Более того, дипептиды, в отличие от более длинных пептидов, способны проникать через гастроинтестинальный барьер за счет системы активного транспорта. В организме дипептиды более стабильны, чем олигопептиды ввиду того, что на них не действуют многие протеазы, например, пепсин и другие карбоксильные протеазы. Особенно стабильны пролил- и пироглутамилсодержащие пептиды. Другими словами, дипептиды потенциально могут быть перорально активны.
Опираясь на эту концепцию, мы сконструировали группу дипептидных аналогов пирацетама на основе пироглутаминовой кислоты. Простейшим пептидным аналогом пирацетама явился амид пироглутамилглицина. Компьютерный информационный анализ пирацетама и амида пироглутамилглицина с использованием программы PCModel с применением методов молекулярной механики в рамках силового поля ММХ показал возможность наложения обеих молекул в энергетически выгодных конформациях с высокой степенью перекрывания потенциально фармакофорных фрагментов (рис.2).
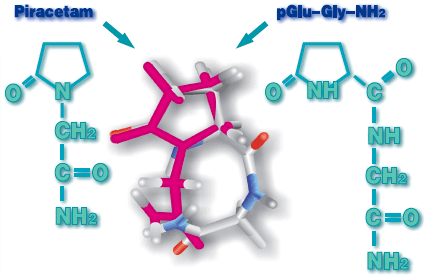
Группа состояла из нескольких дипептидов, причем все они проявляли ноотропную активность в эксперименте, по дозам в сотни и тысячи раз превосходящую активность пирацетама. Наиболее активным пироглутамилсодержащим ноотропным дипептидом явился амид пироглутамиласпарагина pGlu-Asn-NH2 , активные дозы которого были от 0,01 до 10 мг/кг внутрибрюшинно(для сравнения, в эксперименте пирацетам активен в дозах 250-1000 мг/кг). Эффект pGlu-Asn-NH2 был строго стереоспецифичен. Положительным ноотропным эффектом обладал только L-L-диастереомер, то есть, пептид, построенный из природных аминокислот. Другие диастереомеры были либо неактивны, либо ухудшали процессы обучения и памяти. Низкие действующие дозы и высокая стереоселективность свидетельствовали о близости этого дипептида к эндогенному прототипу. И действительно, почти в это же время нидерландский ученый De Wied с коллегами открыл активный метаболит известного пептида памяти вазопрессина гексапептид pGlu-Asn-Сyt-Pro-Arg-Gly-NH2, который обладал высокой ноотропной активностью и был свободен от гормональных эффектов самого вазопрессина. N-концевой дипептидный фрагмент этого гексапептида совпадал с нашим суперактивным пептидным аналогом пирацетама. Таким образом, можно было считать, что пирацетам является пептидергическим соединением и действует через специфические рецепторы, которые позже были открыты для группы фрагментов вазопрессина с ноотропной активностью.

Параллельно с группой пироглутамилсодержащих дипептидных аналогов пирацетама нами разрабатывалась и другая группа, пролинсодержащие аналоги пирацетама.
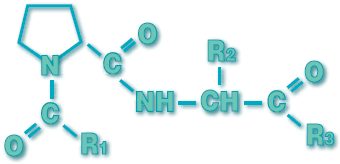
В молекулах пирацетама и пироглутамилдипептидов в пятичленном цикле присутствовал карбонильный кислород рядом с азотом (рис.3). В то же время пролин лишен такого карбонила. Мы предположили, что недостающий карбонил можно ввести рядом с азотом в виде N-ацильной группы. Так были синтезированы ноотропные дипептиды на основе пролина.
Надо отметить, что молекулярное моделирование показало высокое топологическое сходство пирацетама и его дипептидных аналогов как на основе пироглутаминовой кислоты, так и на основе пролина. Особенно близким аналогом пирацетама в топологическом отношении был цикло-пролилглицин. Количественные расчеты были сделаны в США Никифоровичем по заказу фирмы Neuropeptide Dynamics [неопубл.данные]. Позднее цикло-пролилглицин был открыт нами в качестве эндогенного пептида в мозге крыс. Таким образом был открыт новый нейропептид, обладающий ноотропной активностью. Спектр фармакологической активности цикло-пролилглицина и пирацетама практически совпадали. Дипептидные аналоги пирацетама на основе пролина включали ряд соединений, причем все сконструированные на основе нашей концепции аналоги вместе с топологическим подобием получали и ноотропную активность. Химическая структура многих из этих простых соединений например, того же цикло-пролилглицина, была ранее описана, поэтому запатентовать их не представлялось возможным. В связи с этим были синтезированы патентно чистые соединения, которые, по нашей мысли, должны были в организме под действием ферментов превращаться в цикло-пролилглицин. Группа пролинсодержащих дипептидов включала десятки соединений (рис.4), из которых был отобран для развития в качестве ноотропного препарата этиловый эфир фенилацетил-L-пролилглицина, имевший шифр ГВС-111.
Это соединение получило в России зарегистрированное название Ноопепт, а в США под шифром SGS-111 развивается компанией Saegis.
Комментарии
ПРАКТИКА ПЕДИАТРА
