Возможность терапевтической коррекции нарушений клеточного энергообмена и дефицита L-карнитина у новорожденных детей различного гестационного возраста
Статьи

ЖУРНАЛ "ПРАКТИКА ПЕДИАТРА"
Опубликовано в журнале:
«Практика педиатра», 2015, сентябрь-октябрь, с. 14-19 О.Л. Чугунова, профессор, д. м. н., С.В. Думова, доцент, к. м. н., кафедра госпитальной педиатрии № 1 педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава РФ
Ключевые слова: новорожденные, недоношенные дети, карнитиновый обмен.
Key words: newborns, premature newborns, carnitine homeostasis.
В период новорожденности наблюдается большое количество патологических состояний, связанных с нарушением тканевого дыхания и внутриклеточного энергообмена: задержка внутриутробного развития, постнатальная белково-энергетическая недостаточность, тяжелые энцефалопатии, нарушения сердечного ритма, кардиомиопатии, панцитопения. Основной причиной развития этих состояний является дыхательная и тканевая гипоксия, обуславливающая уменьшение поступления энергетических субстратов, что приводит к нарушению всех видов обмена и функционального состояния жизненно важных органов и систем [1,2]. Снижается интенсивность синтеза АТФ, активность АТФ-зависимых реакций, доставка жирных кислот через внутреннюю мембрану митохондрий [3,4]. Нарушается работа как цикла Кребса, так и процессов окислительного фосфорилирования жирных кислот. Уровень синтеза АТФ зависит от поступления жирных кислот внутрь митохондрий. Ключевым участником этого процесса является L-карнитин, который транспортирует длинноцепочечные жирные кислоты в митохондрии, в которых происходит их бета-окисление до ацетил-КоА [5,6,7,8,9].
Карнитин - производное аминомасляной кислоты, присутствующее в тканях в виде L-стереоизомера. Основным источником его поступления в организм являются продукты питания животного происхождения. Эндогенное образование карнитина осуществляется клетками печени, почек и головного мозга путем трансформации аминокислот лизина и метионина. Кофакторами синтеза служат витамины С, В6, В3 и ионы железа. Карнитин принимает непосредственное участие в катаболизме липидов, обеспечивая его начальные этапы - активацию и перенос длинноцепочечных жирных кислот в виде сложных эфиров (ацилкарнитинов) из цитоплазмы в матрикс митохондрий с образованием ацетил-КоА, который служит субстратом для цикла Кребса и последующего синтеза АТФ [9,10]. При дефиците карнитина свободные жирные кислоты не могут быть использованы в качестве источника энергии. Карнитин оказывает также защитное действие, купируя негативный эффект ряда токсических агентов, что предотвращает дегенеративное поражение нервной ткани [11].
Интенсивность внутриклеточного энергообмена оценивается по изменению активности митохондриальных ферментов и уровню свободного и связанного L-карнитина. В России разработан скрининг-метод выявления митохондриальных дисфункций по активности митохондриальных ферментов в лимфоцитах крови. Проводится оценка активности такого фермента, как сукцинатдегидрогеназа (СДГ), является наиболее информативным показателем. [12]. Изменения карнитинового обмена определяются по уровню общего, свободного карнитина (СК) и связанного карнитина - ацилкарнитины (АК) и их соотношения АК/СК, определяемых методом хроматомасс-спектрометрии [13].
По данным многих авторов, экзогенное введение карнитина, кофакторов цикла Кребса, препаратов из групп антиоксидантов и мембран-стабилизаторов приводит к восстановлению процессов окислительного фосфорилирования, цикла трикарбоновых кислот и нормализации внутриклеточных энергопроцессов [13,14].
На базе филиала № 2 ГКБ №24 мы наблюдали 207 детей первых двух месяцев жизни различного срока гестации с задержкой внутриутробного развития, острым почечным повреждением, гидронефрозом, недоношенностью. Для установления интенсивности внутриклеточного энергообмена детям проводилось определение активности митохондриальных ферментов, в частности СДГ, выявление уровня СК и АК методом хромато-масс-спектрометрии, а также для дополнительной характеристики возможной недостаточности карнитина вычислялся коэффициент соотношения ацилкарнитины/ свободный карнитин (АК/СК), повышение которого выше 0,6 [13] свидетельствует о развитии карнитиновой недостаточности.
Нами была выявлена корреляция между активностью СДГ и прибавкой массы тела у новорожденных детей с задержкой внутриутробного развития 2-3 степени. Было обследовано 52 новорожденных с диагностированной задержкой внутриутробного развития (ЗВУР) и 38 детей без ЗВУР. Всем детям проводилось определение активности СДГ на 7, 14, 21, 28 и 51 дни жизни и антропометрические измерения. В группе пациентов без ЗВУР, независимо от гестационного возраста, к 28 дню жизни наблюдалась положительная динамика как весовой кривой, так и нарастания активности СДГ. У детей этой группы показатели активности клеточных ферментов достигали значений 9,4-11,72 у.е. (при норме 12,08±1,2), а весовая кривая превышала долженствующую массу на 3-6%. У пациентов со ЗВУР 2-3 степени не отмечалось восстановления активности СДГ к 28 дню жизни, которая составляла в среднем 7,5-9,5 у.е., а фактическая масса детей отставала от долженствующей на 9-13%.
В связи с этим, для коррекции нарушений энергетического обмена 32 наблюдаемым детям со ЗВУР к стандартной терапии были добавлены энерготропные препараты: L-карнитин (Элькар®) в дозе 100 мг/кг/сут- ки, витамины группы «В», кокарбоксилаза, а остальные 20 обследуемых этой группы получали только стандартную терапию. При оценке результатов лечения на 51 день жизни детей было показано, что вне зависимости от степени ЗВУР в группе пациентов, получавших дополнительно энерготропную терапию, выявляется интенсивная прибавка массы тела, не наблюдаемая в группе детей, находящихся только на стандартной терапии (рис.1). Активность СДГ в группе детей, получавших дополнительное лечение, так же была на 15-40% выше, чем у детей, не получавших энерготропные препараты, что свидетельствовало о постепенном восстановлении внутриклеточных энергетических процессов.
Рис. 1. Сравнительная динамика прибавки массы у новорожденных детей со ЗВУР.
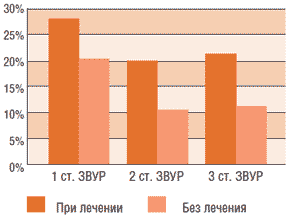
Таким образом, применение энерготропных препаратов, в том числе L-карнитина, у детей со ЗВУР приводит к более быстрому достижению долженствующих прибавок массы тела и нормализации клеточного энергоообмена.
Под наблюдением находились и 29 недоношенных детей 24-34 недель гестации, у которых определялся уровень активности СДГ, свободного L-карнитина и коэффициент соотношения АК/СК. Уровень свободного карнитина у всех наблюдаемых детей на первой неделе жизни не отличался от такового у доношенных новорожденных и соответствовал возрастным нормам (7-30 мкмоль/л), а соотношение АК/СК не превышало 0,6, что также соответствовало возрастным нормам. Однако, к 28 дням жизни коэффициент АК/СК у недоношенных детей с экстремально низкой массой тела повышался до 0,9-1,2, чего не наблюдалось у новорожденных других групп. На 14 и 21 день показатели активности СДГ у 12 детей с экстремально низкой массой тела не достигали первоначальных значений.
Непроисходило и восстановления первоначальной массы тела к концу первого месяца жизни. В связи с этим, недоношенным детям с экстремально низкой массой тела проводилась коррекция митохондриальной недостаточности с назначением L-карнитина (использовался Элькар® 30% раствор per os) и витаминов группы «В», что приводило к лучшей прибавке массы тела по сравнению с 4 детьми второй группы, не получавших данную терапию.
Таким образом, уноворожденных детей с патологическими процессами, сопровождающимися развитием гипоксии, наблюдается нарушение внутриклеточного энергообмена с нарастанием дефицита карнитина. Что свидетельствует о целесообразности применения препаратов L-карнитина в сочетании с кофакторами цикла Кребса.
Гипоксия, а также связанные с ней энергодефицит и недостаток карнитина оказывают неблагоприятное влияние на функцию почек. Под нашим наблюдением находились 76 новорожденных с развившимся острым почечным повреждением (ОПП) по критериям nRIFLE (выделяют 5 стадий - риска (risk-R), повреждения (injury-I), недостаточности (failure-F), полная потеря функции почек (loss-L) и терминальная почечная недостаточность (end stage-kidney disease-E) [15]. В подавляющем большинстве случаев причиной ОПП являлась перенесенная тяжелая гипоксия, что способствовало нарушению эергообмена. У всех новорожденных определялись маркеры острого почечного повреждения - липокалин в сыворотке (s-NGAL), в моче (u-NGAL) и цистатин C в моче (u-Cys) - методом иммуноферментного анализа (ИФА). Показатели карнитинового обмена исследовались на первой и четвертой неделе жизни. У новорожденных с ОПП наблюдалось повышение уровня соотношения АК/СК более 0,6, что свидетельствовало о карнитиновой недостаточности. Такая же тенденция наблюдалась к концу первого месяца жизни этих детей (табл.1).
Таблица 1. Показатели карнитинового обмена у недоношенных детей с развившимся острым почечным повреждением
| Возраст | Свободный карнитин (СК), мкмоль/л | Ацилкарнитины /свободный карнитин (АК/СК) | ||
| контроль | ОПП | контроль | ОПП | |
| N=44 | N=76 | N=44 | N=76 | |
| 1сут | 17,6±12 | 19,2±13,1 | 0,69±0,14 | 0,86±0,11 |
| 28сут | 32±18 | 32±18 | 0,58±0,12 | 0,95±0,15 |
На основании этих результатов в терапевтические схемы лечения был введен препарат L-карнитина (Элькар® 30% раствор) в дозировке 100 мг/кг в сутки. На фоне лечения в течение 3 недель показатель АК/СК достигал нормы к 56 с.ж. и достоверно отличался от уровня соотношений АК/СК у новорожденных без лечения (0,52±0,11 против 1,03±0,29, р=0,019). На этом фоне уровни u-NGAL и u-Cys у детей, получавших Элькар®, достоверно отличались от показателей в группе детей, не получавших L-карнитин (р=0,031 и р=0,01) (рис 2, 3). Повышение NGAL в сыворотке крови и моче связано с повреждением почечных канальцев. Уровни NGAL являются диагностическими и прогностическими при ОПП: нарастают быстро, на 1-2 дня раньше, чем креатинин, и отражают остроту и тяжесть поражения почек. Уровень цистатина С в крови и моче практически не зависит от мышечной массы, пола и возраста ребенка. Чем тяжелее ренальная патология, тем хуже цистатин С фильтруется почками и тем выше его уровень в сыворотке крови [16]. Следовательно, нормализация уровней липокалина и цистатина С в крови и моче у детей, получающих метаболическую терапию, свидетельствует о положительном влиянии L-карнитина на скорость процессов репарации почечной ткани.
Рис. 2. Различие уровней липокалина в моче в группах детей в возрасте 1 мес, получавших и неполучавших препарат L-карнитина
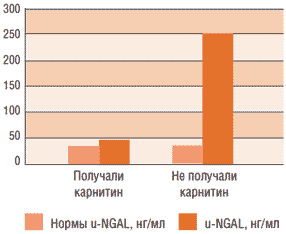
Нормы u-NGAL у детей первых двух месяцев жизни составляли 37 ± 2,3 нг/мл.
Рис. 3. Различие уровней цистатина С в моче в группах детей в возрасте 1 мес, получавших и неполучавших препарат L-карнитина
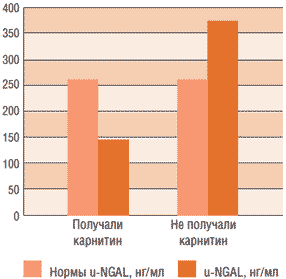
Нормы u-NGAL у детей первых двух месяцев жизни составляли 257 ± 8,2 нг/мл.
При определении активности митохондриальной СДГ у 12 новорожденных детей с гидронефрозом наблюдалось ее снижение на 26%. В связи с выявленными изменениями уровня активности СДГ в терапию 8 детям был включен препарат L-карнитина (Элькар®) и витамины группы «В». Оставшиеся 4 новорожденных не получали метаболическую терапию. По окончании курса лечения у всех 8 детей наблюдалось повышение активности митохондриальных ферментов, а рост паренхимы почек по данным динамического ультразвукового исследования (УЗИ) соответствовал возрастным нормам, в то время как у детей из контрольной группы наблюдалось отставание увеличения паренхимы почек по результатам УЗИ.
На основании результатов проведенных исследований нами была предложена следующая схема с использованием энерготропных препаратов: лекарственный препарат L-карнитина - Элькар® - раствор для приема внутрь 300 мг/мл в дозировке 100 мг/кг в сутки 2 раза в день в течение 3-4 месяцев; корилип нео 1 свеча в сутки в течение 15 дней; витамин В6 в дозе 2 мг/кг/сут - 4 недели.
Использование вышеизложенной схемы приводит к достоверному нарастанию активности митохондриальных ферментов, снижению коэффициента соотношения связанного и свободного карнитина, что свидетельствует о постепенной нормализации интенсивности внутриклеточных энергетических процессов. Клинически наблюдается нарастание темпов прибавки массы тела детей со ЗВУР и недоношенных новорожденных с экстремально низкой массой тела, восстановление функции почек и увеличение паренхимы почек по данным УЗИ.
Данные препараты целесообразно использовать для нормализации внутриклеточного энергообмена у детей с задержкой внутриутробного развития, глубоко недоношенных новорожденных с экстремально низкой массой тела, детей с острым почечным повреждением, гидронефрозом, а также при ряде других заболеваний, сопровождающихся развитием гипоксии.
Список литературы:
1. Лопухин Ю.М., Коган Э. М. Критерии жизнеспособности органов и тканей перед трансплантацией. - М.: Медицина, 1975. - 282 с.
2. Alberti K.G. Biochemical consequenses of hypoxia // J. Clin. Path. - 1977. - Vol.3., Suppl. 11. - P. 14.
3. Hochachka P.W. Living without oxygen: Closed and open systems in hypoxia tolerace.- Massachusetts, London, 1980. - 178 p.
4. Дудченко А.М. Пути и возможности стабилизации энергетических функций клеток при гипоксии //Гипоксия. Механизмы, адаптация, коррекция/Мат. Всерос. конф. - М.,1997. - С. 36-37.
5. Хватова Е.М., Сидоркина А.Н. и др. Ма- кроэргические фосфаты как показатель оценки степени тяжести гипоксии мозга // Моделирование, патогенез и терапия гипоксических состояний. - Горький, 1989. - С. 4-10.
6. Лукьянова Л.Д., Германова Э.Л., Копалад- зе Р.А. Закономерности формирования резистентности организма при разных режимах гипоксического прекондиционирования: роль гипоксического периода и реоксигенации // Бюллетень экспериментальной биологии име- дицины. - 2009. - Т.147, № 4. - С. 380-384
7. Лукьянова Л.Д. Гипоксия при патологиях. Молекулярные механизмы и принципы коррек-ции/ Л.Д. Лукьянова // Перфторорганические соединения в биологии и медицине: Сб. науч. тр. - Пущино: ОНТИ ПНЦ РАН, 2001. - С. 56-69
8. Лукьянова Л.Д., Дудченко A.M. и др. Действие интервальной нормобарической гипоксии на кинетические свойства митохондриальных ферментов // Бюллетень экспериментальной биологии и медицины. - 2007. - Т. 144, № 12. - С. 644-652.
9.Sharma S., Black S.M. Carnitine homeostasis, mitochondrial function, and cardiovascular disease. Drug Discov Today Dis Mech. 2009; 6: 1-4: e31-e39.
10.Das A.M.., Steuerwald U., Illsinger S. Inborn Errors of Energy Metabolism Associated with Myopathies. J Biomed Biotechnol. 2010; 2010: 340849.
11 .Wang C., Sadovova N., Ali H.K. et al. L-carnitine protects neurons from 1-methyl-4- phenylpyridinium-induced neuronal apoptosis in rat forebrain culture. Neuroscience.2007; 144: 1: 46-55.
12.Сухоруков В.С. Гетерогенность и клинико-морфологическая неоднородность митохондриальной патологии у детей. Автореф. дисс. ... докт. мед.наук. М., 1998;35.
13 Е.А. Николаева, М.Н. Харабадзе, И.В. Золкина, В.С. Сухоруков, П.В. Новиков. Недостаточность карнитина у детей с наследственными болезнями обмена веществ и митохондриальными заболеваниями: особенности патогенеза и эффективность лечения // Педиатрия - 2013 - Том 92 - № 3 - С 42-49.
14. Николаева Е.А., Семячкина С.В., Васильев С.Ц. Основные способы медикаментозного лечения детей с митохондриальными заболеваниями. Руководство по фармакотерапии в педиатрии и детской хирургии. Т. 2. «Клиническая генетика» под общей редакцией Царегородцева А.Д., Табо- лина В.А. М.: Медпрактика-М; 2002;32-44.
15. Akcan-Arikan A. , Zappitelli M, Loftis LL, Washburn KK, Jefferson LS and Goldstein SL. Modified RIFLE criteria in critically ill children with acute kidney injury / Kidney International, 2007 May; 71 (10): 1028-35.
16. Waikar S.S., Liu K.D., Chertow G.M. Diagnosis, epidemiology and outcomes of acute kidney injury//Clin. J Am Soc Nephrol. - 2008. - Vol.3. - P. 844-61.
