Роль магния в формировании метаболического синдрома, коррекции избыточного веса и ожирения у детей и подростков
Статьи Опубликовано в журнале:
«Педиатрия» 2014, Том 93, №2
О.А. Громова1,2, Л.Э. Федотова1,2, Т.Р. Гришина1,2, И.Ю. Торшин1, А.Г. Калачева1, О.А. Лиманова1
1Российский сателлитный центр Института микроэлементов ЮНЕСКО, Москва;
2кафедра фармакологии и клинической фармакологии ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава РФ, г. Иваново, РФ
Нарушения микронутриентного баланса у детей вследствие несоответствующего возрасту рациону питания, гиподинамии и давления психологического стресса приводят к старту несоответствующей возрасту хронической патологии. С дефицитом каждого из микронутриентов ассоциирован определенный спектр патологий. Хорошо известно, что, например, дефицит железа ассоциирован с анемией, а дефицит йода – с патологией щитовидной железы. В то же время весьма часто забывают о том, что развитие инсулинорезистентности и проблема избыточного веса в любом возрасте ассоциированы прежде всего с дефицитом магния (ДМ). По данным клинических и фундаментальных исследований, магний проявляет гепатопротекторные свойства. Важно отметить, что магний является эссенциальным кофактором более 40 ферментов, принципиально необходимых для физиологического обмена углеводов (гексокиназа, глюкокиназа, фосфофруктомутаза, енолаза и др.), и более 30 ферментов липидного метаболизма (ацил-КоА синтетазы среднецепочечных жирных кислот, лецитин-холестерин ацилтрансфераза, лигазы длинноцепочечных жирных кислот и др.).
Поэтому на фоне ДМ активность этих ферментов резко падает, что создает условия для быстрого накопления избыточной жировой ткани у детей и подростков. И, наоборот, коррекция ДМ является фундаментальным условием для развития сообразных возрасту массо-ростовых характеристик.
Ключевые слова: дети, ожирение, Mg-зависимые ферменты обмена углеводов, Mg-зависимые ферменты липидного метаболизма, коррекция дефицита магния.
Micronutrient balance disorders in children, caused by age-inappropriate diet, hypodynamia and mental pressure stress, lead to onset of age-inappropriate chronic disease. The deficiency of each micronutrient is associated with specific variety of diseases. It is a well-known fact that iron deficiency is associated with anaemia, iodine deficiency is associated with thyroid pathology. Often overlooked is the correlation of insulin resistance and obesity with magnesium deficiency (MD) in any age. Basic and clinical research suggests that magnesium exerts hepatoprotectiveproperties. It is important to note, that magnesium is an essential cofactor for more than 40 enzymes necessary for carbohydrate metabolism (hexokinase, glucokinase, phosphofructomutase, enolase etc.) and more than 30 enzymes of lipid metabolism (acetyl-CoA synthetase of MCFA, lecithin-cholesterol acyl-transferase, LCFA ligases etc.).
Therefore, magnesium deficiency reduces the activity of enzymes creating conditions for fast adipose tissue accumulation in children and adolescents. And on the contrary, magnesium deficiency correction is a basic condition of age-appropriate height and weight dynamics.
Key words: children, obesity, Mg-dependent enzymes of carbohydrate metabolism, Mg-dependent enzymes of lipid metabolism, magnesium deficiency correction.
Малоподвижный образ жизни у детей и отнюдь «не детское» жирное и высококалорийное питание в последние годы привели к резкому взлету встречаемости ожирения и других компонентов метаболического синдрома (МС) у детей и подростков. При переходе в подростковый возраст избыточная масса тела (МТ), сформировавшаяся в детском возрасте, нормализуется лишь у части подростков (так называемое «израстание»). У многих подростков детское ожирение трансформируется в ожирение взрослых, отягчающееся инсулинорезистентностью (ИР), гиперлипидемией и артериальной гипертонией (АГ), т.е. МС.
Во всем мире численность детей с ожирением удваивается каждые 30 лет [1]. В России от избыточной МТ страдают 8,5% детей, проживающих в городах, и 5,5% — в сельской местности [2]. Динамика роста встречаемости ожирения у детей также настораживает. Например, в г. Томске и в области за период с 2000 по 2008 гг. детское ожирение выросло в 1,8 раз. Была выявлена негативная динамика роста распространенности данной патологии среди мальчиков (3,7 на 100 тыс детского населения в 2000 г. и 6,4 в 2008 г.) и менее – у девочек (в 2000 г. – 6,3, а в 2008 г. – 6,6 на 100 тыс детского населения) [3].
Во многих странах проблема ожирения у детей не только медицинская, но и социальная. Так, например, в Англии 17% детей и подростков в возрасте до 19 лет страдают от избыточного веса, а доля полных людей среди взрослых достигает 33%. Два года назад британский парламент принял закон, который в крайних случаях, когда все способы воздействия на родителей, которые постоянно перекармливают детей, уже исчерпаны, разрешать «изымать детей из семей» так называемыми органами социальной защиты. Лишь за минувший год пятеро британских детей были изъяты из своих семей по причине их постоянного переедания [4].
Проблема избыточного веса у детей ассоциирована с нарушениями микронутриентного баланса в «современной диете» и прежде всего с практически полным отсутствием в детском рационе пищевых продуктов, богатых магнием. Магний является неотъемлемых компонентом хлорофилла и поэтому в значительных количествах содержится в водорослях, проростках и зеленолистных растениях. Значительное количество магния содержится в особых видах минеральных вод. При дефиците магния (ДМ) в организме ребенка развиваются «быстрые» проявления дефицита (судороги ног, нервный тик, срыгивания, беспокойный сон, аритмия, апное и др.), а также медленные метаболические (ожирение, ИР, МС, дисплазия соединительной ткани) [5–9] (рис. 1).
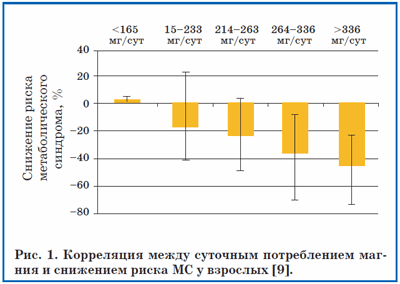
Магний, являясь одним из важнейших биоэлементов, имеет особое значение для поддержания метаболических функций организма и профилактики ожирения. Ионы Mg2+ – эссенциальный кофактор многочисленных ферментов, участвующих в обмене углеводов и жиров. Данные экспериментальных, клинических и эпидемиологических исследований указывают на то, что достаточное потребление магния из пищи и препаратов магния способствует нормализации чувствительности тканей и клеток к инсулину [10], уменьшению выраженности проявления компонентов МС [11] и снижает риск МС. В эксперименте кормление животных фруктозой провоцирует развитие различных компонентов МС, включая ИР и глюкозотолерантность. Обогащение диеты магнием, наоборот, приводит к улучшению чувствительности к инсулину, снижению гипергликемии, гиперлипидемии и перекисного окисления липидов [12].
Хронический ДМ у детей встречается достаточно часто и ассоциирован с широким спектром детских патологий. Например, при изучении распространенности выраженной гипомагниемии (магний сыворотки ДМ усугубляется к подростковому возрасту. Например, при обследовании в Мексике 5060 детей 1–11 лет низкий уровень магния в сыворотке крови был обнаружен всего у 12% детей в возрастном диапазоне от 1 года до 4 лет. У более старших детей (от 5 до 11 лет) низкая концентрация магния в сыворотке крови определялась уже у 28% детей [14]. При анализе питания у подростков в Ивановской и Владимирской областях, страдающих ранними формами АГ, было отмечено низкое потребление магния (менее 170 мг/сут), пересаливание пищи, сопровождавшиеся набором избыточной МТ [15].
В другом крупном исследовании (Мексика) в когорте 2447 подростков 12–19 лет при измерении уровней микронутриентов в сыворотке крови было показало, что ДМ был уже лидирующим. Дефицит железа у подростков отмечался у 6,9%; меди – у 14% девочек и у 12% мальчиков; цинка – у 28% девочек и у 25% мальчиков, а магния – у 40% девочек и 35% мальчиков. Дефицитные по магнию дети и подростки отличались более высоким индексом МТ (ИМТ), уровнем стресса, у девочек чаще имелись расстройства менструальной функции [16].
Установлена взаимосвязь между низкой обеспеченностью магнием в питании, низким уровнем магния в волосах и ранним стартом атерогенной программы и ожирения. Так, в группе 218 девочек 5–10 лет в Бельгии установлена обратная корреляция между кальцием и магнием в волосах и отдельными метаболическими параметрами (диастолическое артериальное давление – АД, модели оценки гомеостаза для резистентности к инсулину, снижение липопротеидов высокой плотности – ЛПВП, повышение холестерина и ИМТ). У девочек с каждым из параметров выше возрастной 75-й процентили установлено значительное снижение уровней и кальция, и магния [17].
Важным выводом из многочисленных клинико-эпидемиологических исследований является то, что проблему ДМ у детей очень сложно компенсировать за счет потребления тех или иных пищевых продуктов. Даже современная растительная пища может содержать весьма различные количества магния, в зависимости от количества магния в почве и от методик выращивания растений (гидропоника и др.). Результаты клинико-эпидемиологических исследований показывают, что даже более высокое потребление обогащенных магнием продуктов питания далеко не всегда эффективно компенсирует ДМ. Кросс-секционное сравнительное исследование 55 детей и подростков 4–14 лет с избыточной МТ и 53 детей с нормальным весом показало, что уровни магния были значительно ниже у детей с избыточным весом (2,12±0,33 мг/дл) по сравнению с детьми с нормальным весом (2,56±0,24 мг/дл, pТаким образом, возникает необходимость компенсации ДМ у детей с использованием специальных препаратов на основе органических солей магния. В настоящей статье последовательно рассмотрены роль магния как неотъемлемого кофактора метаболизма углеводов, жиров и белков, участие магния в гепатопротекции и подходы к компенсации ДМ для профилактики избыточного веса у детей.
Магний – неотъемлемый кофактор ферментов метаболизма углеводов
С физиологической точки зрения, магний требуется для осуществления энергетического метаболизма – процессов расщепления белков, жиров и углеводов и превращения их в основной «энергоноситель» клетки – молекулы АТФ. Среди 720 известных в настоящее время магний-зависимых белков протеома человека более 310 участвуют в синтезе АТФ [19]. В частности, магний необходим для передачи сигнала от рецепторов инсулина и для эффективного расщепления глюкозы [20].
Негативные тенденции в питании детей и обедненный по магнию рацион формируют ИР с детского возраста. Низкие сывороточные уровни магния связаны с ожирением и ИР у детей. Обследование группы 203 детей и подростков (117 страдающих ожирением, 86 контроль) показало, что сывороточные уровни магния были значительно ниже у тех, кто страдают ожирением, чем в контрольной группе (р=0,014). В то же время у детей без ожирения наблюдалась положительная корреляция между уровнем магния в сыворотке крови и ИМТ (р=0,03). Иначе говоря, при отсутствии ожирения более высокие уровни магния соответствуют большей МТ и пропорционально большему росту, а при ожирении эта зависимость нарушается. Избыточная МТ при нормальном росте и, особенно, при пониженном росте четко ассоциирована с ДМ [21].
Каковы же фундаментальные механизмы воздействия ДМ на патофизиологию, приводящие к ожирению и ИР? Систематический анализ молекулярных механизмов воздействия ДМ на патофизиологические процессы, связанные с нарушениями метаболизма сахаров, позволил выделить около 40 белков, снижение активности которых на фоне ДМ способствует развитию патофизиологии и сахарного диабета (СД), и МС. Эти белки относятся к метаболизму сахаров (глюконеогенез и гликолиз), сигнальному пути рецептора инсулина и метаболизму жиров (рассмотрены более подробно в следующем разделе) [19].
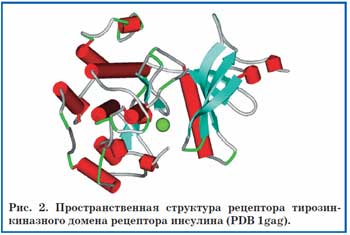
В частности, сама молекула рецептора инсулина является важнейшим магний-зависимым белком во внутриклеточном каскаде передачи сигнала от рецептора инсулина. Сигнальная активность этого каскада приводит к увеличению экспрессии транспортера глюкозы (что увеличивает поступление глюкозы в клетки), стимулирует метаболизм жиров и углеводов. При связывании инсулина рецептор претерпевает изменение конформации и начинает фосфорилировать определенные аминокислотные остатки тирозина в белках одноименного сигнального каскада. Эти первичные процессы осуществления биологических функций инсулина невозможны без участия иона магния, расположенного в активном центре молекулы рецептора (рис. 2).
Магний (сфера) стабилизирует активный центр тирозинкиназы, и при ДМ внутри клетки тирозинкиназная активность рецептора инсулина неизбежно снижается.
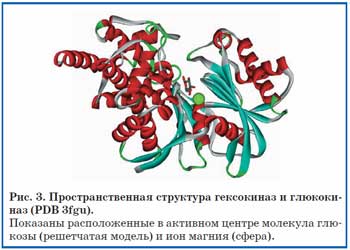
Гликолиз – один из наиболее фундаментальных биохимических путей углеводного метаболизма. Процесс гликолиза происходит в каждой клетке. Данная последовательность из 10 реакций служит входной точкой в цикл Кребса – основной цикл энергетического метаболизма митохондрий и всей клетки, синтезирующий клеточный АТФ. ДМ неизбежно приведет к значительному снижению активности по крайней мере 6 из 10 гликолитических ферментов, способствуя развитию глюкозотолерантности тканей. Например, магний-зависимая гексоки-наза 1 трансформирует D-гексозу в D-гексозу 6-фосфат, а магнийзависимая АДФ-глюкокиназа (ген ADPGK) катализирует фосфорилирование D-глюкозы в D-глюкозо-6-фосфат. Эти два фермента осуществляют первый шаг в процессе гликолиза. Инсулин, адреналин, тиреоидные гормоны повышают гексокиназную активность в клетках, в то время как глюкокортикоиды и соматотропин ее снижают. Магний – составная часть активного центра гексокиназы и схожего с ней фермента глюкокиназы (рис. 3).
Рассмотренные выше фундаментальные механизмы участия магния в процессах метаболизма углеводов на молекулярном уровне в полной мере объясняют наблюдаемые в клинической практике корреляции между ДМ и избыточной МТ/ожирением у детей.
Например, наблюдения за детьми 8–16 лет с ожирением и СД 2-го типа (СД2) показали, что уровни магния в сыворотке крови были ниже у детей с ожирением и с СД2 по сравнению с контрольной группой (рис. 4) [22].
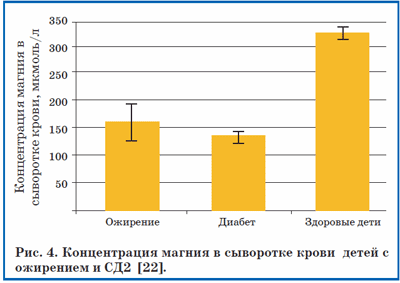
В другом исследовании сывороточные уровни магния натощак у детей 4–14 лет были значительно ниже в группе с избыточной МТ (2,12±0,33 мг/дл) по сравнению с контрольной группой (2,56±0,24 мг/дл, рПри сравнении 24 детей 8–17 лет с ожирением и 24 детей без ожирения было найдено, что уровни магния в плазме крови были значительно ниже у страдающих ожирением (0,75±0,02 ммоль/л, контроль 0,80±0,01 ммоль/л, р=0,009). Более низким уровням магния соответствовали более высокие уровни инсулина натощак (r=–0,36, р= 0,01) [23].
Прием препаратов органического магния способствует снижению гипергликемии – одного из основных патофизиологических компонентов накопления избыточного веса. Например, мета-анализ рандомизированных исследований органических препаратов магния суммарно включил 370 пациентов с СД2. Средняя продолжительность приема препаратов органического магния составила 12 недель, средняя дозировка – 360 мг/сут в расчете на элементный магний. Прием препаратов способствовал достоверному снижению уровня глюкозы натощак на –0,56 ммоль/л (95% ДИ –1,10–0,01, р=0,02) по сравнению с плацебо [24].
Пероральный прием препаратов органического магния улучшает чувствительность к инсулину у пациентов с избыточным весом, даже если у них наблюдаются нормальные уровни магния в плазме. В исследовании группы из 52 человек участники прошли пероральный тест на толерантность к глюкозе и затем были рандомизированы на получение либо Mg-аспартат-гидрохлорид (n=27), либо плацебо (n=25) в течение 6 месяцев. Прием препарата магния приводил к значительному улучшению повышенных уровней глюкозы натощак и улучшал балльные оценки чувствительности к инсулину по индексу HOMA и другим шкалам [25].
Дефицит магния и липидный метаболизм
Магний-дефицитная диета приводит к разносторонним нарушениям липидного метаболизма – увеличение уровней общего холестерина и триглицеридов плазмы, снижение уровня «хорошего» ЛПВП-холестерина и др. [26]. Современный метод биоинформационного анализа (анализ функциональных взаимосвязей [27]) позволил установить более 30 магний-зависимых ферментов, нарушение активности которых будет приводить к аномалиям липидного метаболизма и способствовать развитию ожирения. Эти белки относятся собственно к метаболизму липидов (12 ферментов, включая ацил-КоА синтетазы среднецепочечных жирных кислот, лецитин-холестерин ацилтрансферазу, лигазы длинноцепочечных жирных кислот), регуляции метаболизма липидов (8 ферментов) и передаче катехоламинового сигнала (12 ферментов).
ДМ приводит к неизбежному падению активности этих белков, что приведет к снижению скорости биотрансформаций субстратов в каждом из этих метаболических маршрутов. Спад активности липидного метаболизма, нарушения регуляции липидного метаболизма и передачи сигнала от адренергических рецепторов приведут к снижению интенсивности энергетического метаболизма и нарушению липидного баланса в плазме крови.
В частности, на фоне гипомагнеземии произойдут увеличение уровней триглицеридов плазмы (вследствие сниженной активности ACSM1, 2, 3, 4, 5, 6; ACSL1, 2, 3, 4, 5; LPIN2, 3) и снижение уровней ЛПВП (снижение активности LCAT; PPARА, В, С, D; PRKAA1, 2), что действительно наблюдается при ожирении и МС.
Магний необходим для активности ферментов, известных как «КоА-лигазы длинноцепочечных жирных кислот» (длинноцепочечные ацил-КоА синтетазы, англ. ACSL), которые играют ключевую роль в синтезе и деградации клеточных липидов с помощью Р-окисления. Ферменты типа ACSL локализованы в микросомах, внешних мембранах митохондрий, пероксисомальной мембране и катализируют первую реакцию в метаболизме жирных кислот – присоединение жирной кислоты к коферменту А. Магний является составной частью активного центра жирная кислота–КоА лигаз (рис. 5).
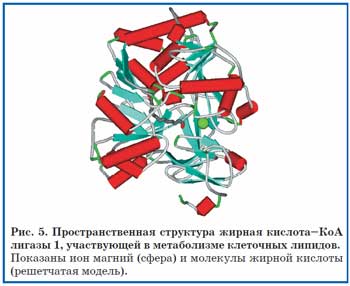
Активность этой группы ферментов зависит от концентрации ионов Mg2+; при внутриклеточном ДМ ACSL-активность падает более чем в 3 раза [28].
Ионы магния необходимы для поддержания активности фермента лецитин-холестерин ацилтрансферазы (ЛХАТ). Достаточный уровень активности Mg-зависимой ЛХАТ необходим для поддержания нормальных уровней триглицеридов и ЛПВП [28]. Магний необходим для активности фермента. В эксперименте острый ДМ был вызван применением безмагниевой диеты в течение 8 суток. Острый ДМ сопровождался увеличением уровней триглицеридов плазмы, повышением свободного холестерина и снижением уровня эстерифицированного холестерина. Активность ЛХАТ в плазме крови заметно уменьшилась – в среднем на 54% [29]. В клиническом исследовании группы 47 детей уровни ионизованного магния плазмы достоверно коррелировали с уровнями ЛПВП (r=0,31, р=0,035), аполипопротеина А-1 (r=0,39, р=0,012) и активностью ЛХАТ (r=–0,52, р=0,018) [30].
Прием препаратов на основе органических солей магния способствует нормализации метаболизма жиров. В группе из 48 человек с АГ I пациенты были рандомизированы на прием 600 мг/сут пидолата магния в течение 12 недель или в группу контроля. Помимо значимого снижения АД, в группе принимавших препарат органического магния наблюдалось значимое снижение общего холестерина, липопротеина низкой плотности (ЛПНП), триглицеридов, сопровождавшиеся увеличением уровней ЛПВП [31]. Известно, что проатерогенный профиль плазмы крови – обязательный компонент развития абдоминальной формы ожирения.
Следует отметить, что фармакокинетический синергист магния – пиридоксин – не только способствует всасыванию магния в желудочно-кишечном тракте (ЖКТ) и транспорту магния внутрь клеток, но и важен для активации белков углеводного и липидного метаболизма. В ряде экспериментальных и клинических исследований была показана взаимосвязь между обеспеченностью витамином В6, СД и МС.
Пиридоксин играет важную роль в регуляции синтеза и секреции инсулина [32]. На моделях индуцированного стрептозотоцином диабета показано, что пиридоксальфосфат, поддерживая секрецию инсулина и снижая оксидативный стресс, способствовал защите клеток островков Лангерганса [33]. В клинических исследованиях подтвердилась взаимосвязь между риском СД2 и снижением уровней пиридоксина [34]. В частности, наблюдения за группами женщин с гестационным диабетом в поздней беременности показали, что прием пиридоксина (100 мг/сут) даже в течение относительно короткого срока (2 недели) способствовал статистически значимому улучшению кривой толерантности к глюкозе [35, 36].
Кроме того, обеспеченность пиридоксином необходима для снижения уровней гомоцистеина (и связанного с гипергомоцистеинемией хронического системного воспаления) и, наряду с магнием, участвует в метаболизме углеводов, жиров и белков. Повышенный гомоцистеин является результатов дефицита других витаминов группы В (прежде всего, фолатов, В6 и В12) и также возникает вследствие ДМ. Избыток гомоцистеина является независимым фактором риска атеросклероза, АГ и МС.
Ряд пиридоксин-зависимых ферментов вовлечены в процессы метаболизма аминокислот. К ним относятся аспартатаминотрансферазы (гены GOT1, GOT2), взаимно конвертирующие аспартат в глутамат и оксалоацетат; аланина-минотрансфераза (GPT), катализирующая взаимопревращения аланина, пирувата и глутамата и участвующая в глюконеогенезе; метаболизи-рующая аланин аланин-глиоксилат аминотрансфераза (AGXT) и L-серин дегидратаза (SDS), катализирующая взаимопревращения серина и пирувата. Пиридоксин-зависимые гликоген-фосфорилазы (гены PYGB, PYGM) участвуют в глюконеогенезе. Дефекты генов гликогенфосфорилаз являются причиной гликогенозов (коды 232700, 232600 и др. по ОMIM) [19].
Таким образом, на риск развития ИР и ожирения у детей влияет не только необычно высокое для детского возраста избыточное потребление сахаров и насыщенных жиров, но и снижение способности растущего организма перерабатывать эти макронутриенты. Магний регулирует микронутриентный баланс и сам участвует в метаболизме сахаров и жиров как кофактор ферментов. Как было отмечено выше, достаточные уровни магния необходимы для поддержки более 70 белков и ферментов, которые вовлечены в метаболизм углеводов и жиров. Магний и его синергист пиридоксин также способствуют снижению системного воспаления, что оказывает дополнительное положительное влияние на состояние клеток поджелудочной железы и эндотелия сосудов (рис. 6).
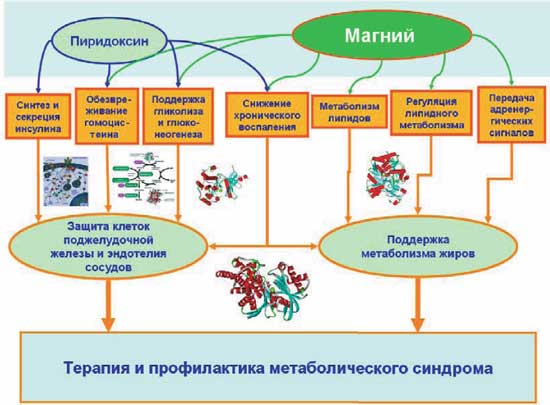
Рис. 6. Молекулярно-физиологические механизмы магния и пиридоксина в терапии и профилактике МС.
Магний как природный гепатопротектор
Здоровая печень обеспечивает эффективную детоксикацию организма ребенка от экзо- и эндотоксинов, поэтому любая патология печени рано или поздно негативно сказывается на состоянии всех органов и систем организма. Печень играет важную роль в белковом, липидном и углеводном обмене. Практически все белки крови (которых в настоящее время известно более 5000) синтезируются в печени. Печень прежде всего синтезирует важнейшие белки крови (альбумин, фибриноген, протромбин, церулоплазмин, трансферрин, ангиотензин и др.), посредством которых происходит регуляция онкотического давления, АД, гемостаза, метаболизма железа и др. [37]. Все эти процессы невозможны без определенных эссенциальных микронутриентов, которые, поддерживая активность и жизнедеятельность гепатоцитов, являются в некотором роде «эссенциальными» гепатопротекторами.
Такие эссенциальные микронутриенты, как магний и пиридоксин, характеризуются отчетливым гепатопротекторным действием, не имея при этом побочных эффектов, свойственных традиционным гепатопротекторным препаратам. Рассмотренные выше механизмы воздействия магния и пиридоксина на метаболизм жиров и углеводов на уровне молекул ферментов однозначно показывают, что характерный для так называемого «цивилизованного» питания ДМ наряду с недостаточным потреблением пиридоксина и других витаминов группы В приводит к снижению биологической активности этих ферментов. Последнее способствует развитию глюкозотолерантности, ИР, нарушениям липидного профиля, развитию компонентов МС. Все эти патофизиологические процессы, вызываемые ДМ, не могут не оказывать отрицательного влияния на состояние печени.
В экспериментальных и клинических исследованиях было установлено, что более низкие уровни магния в плазме крови ассоциированы с патологией печени. Например, в настоящее время нами на кафедре фармакологии ИвГМА проводится экспериментальное исследование эффектов безмагниевой диеты. Одним из характерных наблюдений наряду с многочисленными отклонениями в выполнении неврологических тестовых заданий является быстрое развитие ожирения и стеатогепатоза.
Изучение уровней ионизованного магния в группе 54 пациентов с заболеваниями печени и75 – в контрольной группе показало более низкие уровни магния в сыворотке у пациентов с патологией печени [38]. ДМ ускоряет накопление свободного железа в печени. Свободное, несвязанное трехвалетное железо (Fe3+) гепатотоксично и является ярко выраженным прооксидантом. В эксперименте ДМ приводил к увеличению всасывания свободно- го железа в кишечнике и снижению уровней эритроцитов (возможно, в результате снижения стабильности клеточной мембраны). Интересно отметить, что при Mg-дефицитной диете гемолитическая анемия развивалась более интенсивно [39].
Таким образом, магний проявляет антиоксидантный эффект, в частности, через нормализацию гомеостаза железа.
Терапия пероральными формами органического магния приводит к нормализации уровней АСТ и АЛТ и способствует выведению свинца из печени. И наоборот, более низкая обеспеченность магнием способствует накоплению в печени токсического свинца [40]. Следует отметить, что микроэлемент литий повышает усвояемость магния – пероральное введение лития увеличивает содержание магния в тканях (прежде всего в почках) [41].
Таким образом, гепатопротекторный эффект магния проявляется отчасти в противодействии накоплению токсичных металлов. Помимо этого существует по меньшей мере еще три аспекта гепатопротекторного воздействия магния, которые следует рассмотреть особо:
1) взаимосвязь между ДМ и желчекаменной болезнью (ЖКБ);
2) патологическая основа этой взаимосвязи – молекулярные механизмы воздействия магния на углеводный и липидный метаболизм;
3) воздействие магния на процессы воспаления.
Поскольку последние два вопроса были рассмотрены в предыдущих разделах, здесь рассмотрим взаимосвязи между ДМ, эссенциальными фосфолипидами и ЖКБ.
ЖКБ – конечно же расстройство среднего и пожилого возрасте. Однако к факторам риска заболевания относят дискинезию желчевыводящих путей, гиподинамию, избыточный вес, аномалии развития желчного пузыря и нарушения диеты – факторы, которые в полной мере относятся к детям с избыточной МТ.
Например, обследование 8 детей в возрасте 3–16 лет с холестазом при помощи теста на удержание магния показало высокую степень истощения магниевого депо у всех участников.
Потребление магния в дозах от 6 до 34 мг/кг/сут (в среднем 11 мг/кг/сут) позволило достигнуть насыщения депо у 7 из 8 участников в весьма различные сроки – от 4 до 31 мес (14 мес в среднем) [42]. ЖКБ также характеризуется более низкой концентрацией магния в желчи [43]. И наоборот, физиологически достаточное потребление магния способствует снижению риска образования камней в желчном пузыре [44].
При сравнении групп 54 пациентов с ЖКБ и 46 здоровых добровольцев молодого возраста оценка диеты проводилась посредством дневника диеты. Пациенты с ЖКБ потребляли меньше рыбы и фруктов, больше – зерновых, масла, сахара и мяса, потребляли больше калорий и жиров и меньше клетчатки, фолиевой кислоты и магния. Для всех витаминов и минералов у пациентов наблюдалось субоптимальное потребление микронутриентов, в т.ч. магния [45].
Долгосрочное потребление физиологически достаточных доз магния снижает риск возникновения ЖКБ. ДМ, наоборот, способствует возникновению дислипидемии, являющейся одной из патофизиологических причин сгущения желчи, выпадения хлопьев и образования желчных камней. Взаимосвязь между потреблением магния и риском ЖКБ была изучена в когорте 42 705 мужчин, первоначально не имевших заболевания. Потребление магния оценивали с помощью верифицированного опросника диеты. В течение 16 лет наблюдений, начиная с подросткового и молодого возраста до зрелого, были зарегистрированы 2195 случаев ЖКБ. При сравнении подгрупп с самым низким и самым высоким потреблением магния относительный риск заболевания снижался на 33% при более высоком потреблении магния (ОШ 0,67, 95% ДИ 0,59– 0,77, рВ целом, магний (1) необходим для углеводного и липидного метаболизма, (2) способствует повышению чувствительности тканей к инсулину, (3) способствует торможению избыточного воспаления (в частности, через синтез глутатиона), (4) предотвращает формирование желчных камней и (5) оказывает противодействие накоплению токсических металлов. Пиридоксин необходим для (1) метаболизма углеводов, (2) синтеза и секреции инсулина, (3) снижения гипергомоцистеинемии и воспаления, (4) повышения биодоступности магния и (5) синтеза катехоламиновых нейротрансмиттеров. Эссенциальные фосфолипиды способствуют (1) снижению воспаления, (2) нормализации липидного профиля, (3) вовлечены в секрецию инсулина и (4) необходимы для снижения гипергомоцистеинемии (рис. 7).
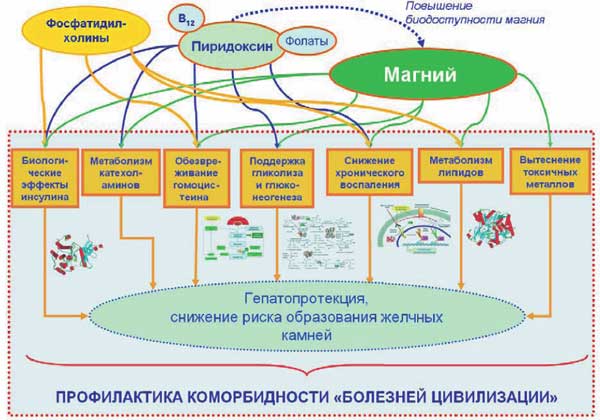
Рис. 7. Механизмы синергидного гепатопротекторного воздействия магния, пиридоксина и фосфатидил-холинов («эссенциальных фосфолипидов»).
О диагностике и компенсации дефицита магния у детей
Приведенные выше результаты фундаментальных и клинических исследований убедительно указывают на взаимосвязь между ДМ и развитием патофизиологических процессов, приводящих к накоплению избыточной МТ и ожирению. Поэтому диагностика и компенсация ДМ являются одним из важных инструментов в профилактике и терапии детского ожирения. Эффективности и безопасности мер по компенсации ДМ у детей следует уделить особое внимание.
На усиливающийся «магний-дефицитный тренд» в современном питании детей указывают результаты крупномасштабных исследований серии NHANES. Исследовались когорты детей 1–5 лет в разные годы. Исследования NHANES в периоды 1976–1980 гг., 1988–1994 гг. и 2001– 2006 гг. показали, что в 1976–1980 гг. примерно 85% детей потребляли молоко, в то время как в 2001–2006 гг. только 77% детей в возрасте 1–5 лет потребляли молоко. Если в 1976–1980 гг. потребление цветного и ароматизированного молока (содержащего искусственные розовые красители и ароматизаторы клубники, вишни, желтые красители ананаса и др.) было относительно низким (менее 3%), то к 2006 г. оно увеличилось до 14% (рГоворя о диагностике ДМ, следует отметить, что ионизированный магний в сыворотке составляет менее 1% от общего содержания магния в организме. Поэтому зачастую простое определение уровней магния в сыворотке не всегда достаточно для постановки диагноза «гипомагнеземия». Это делает необходимым использование других показателей содержания магния в организме (уровни магния в эритроцитах, лимфоцитах, содержание магния в волосах, в суточной моче и др.).
Наиболее надежным методом для оценки магниевого статуса пациента является тест нагрузки магнием. При нормальном насыщении депо магния у пациента нагрузка магнием приводит к поглощению около 6% поступившего магния; в случае недостаточности магния поглощение магния возрастает до 20–50%. Отметим, что нагрузочный тест магнием указывает на глубокое истощение депо магния у пациентов с патологией печени, в то время уровни магния в сыворотке были недостаточно информативны и не позволяли различать гипомагнеземию у пациентов [48].
Говоря о компенсации ДМ прежде всего следует отметить результаты крупных эпидемиологических исследований. Эти исследования показали, что, с одной стороны, диетарная обеспеченность магнием значительно влияет на проявления ожирения и других компонентов МС. В исследовании 535 взрослых диетарное потребление магния оценивали по 3-дневному дневнику диеты. Наличие МС определялось на основе критериев NCEP-III т.н. «Национальной образовательной программы США по холестерину». Потребление магния было обратно пропорционально наличию у пациента МС: пациенты с самым высоким потреблением магния (верхняя квартиль) имели значительно более низкий риск МС по сравнению с нижней квартилью потребления (ОШ 0,36, 95% ДИ 0,19–0,69, р=0,002). Значительная обратная связь наблюдалась между более высоким потреблением магния и более низким ИМТ (ОШ 0,47, 95% ДИ: 0,22–1,00, р=0,03), более низким уровнем глюкозы натощак (ОШ 0,41, 95% ДИ 0,22–0,77, р=0,005) [49].
С другой стороны, использование для компенсации ДМ у детей только богатых магнием продуктов питания не всегда может являться эффективной и безопасной процедурой компенсации ДМ. Например, в крупномасштабном исследовании NHANES (National Health and Nutrition Examination Survey, 1999–2004) было показано, что, несмотря на частичную компенсацию ДМ, регулярный прием орехов (не менее 10 г/сут) по-разному влиял на показатели МТ. Когорта участников (n=24 385) была разделена на подгруппы детей 2–11 лет, детей и подростков 12–18 лет и взрослых (19 лет и старше). Во всех возрастных группах регулярное потребление орехов было ассоциировано с более высоким потреблением энергии, мононенасыщенных и полиненасыщенных жирных кислот, пищевых волокон, меди и магния и более низким потреблением углеводов, холестерина и натрия. Однако в подгруппе детей в возрасте от 2 до 11 лет более высокое потребление орехов было ассоциировано с более высокой распространенностью избыточной МТ и ожирения. В то же время в возрастной группе от 12 до 18 лет потребление орехов было ассоциировано с меньшим риском избыточной МТ и ожирения [50]. Таким образом, не каждый магний-содержащий продукт питания подходит для компенсации ДМ у детей с 2 до 11 лет.
Из приведенных выше результатов крупномасштабных исследований становятся очевидны различия в эффектах повышенного потребления богатых магнием продуктов питания у детей различных возрастных групп. Действительно, такие продукты питания, как орехи, привносят в организм не только магний, но в то же время являются и высококалорийными продуктами питания. Поэтому необходимы способы таргетной компенсации ДМ. К таковым относятся использование препаратов на основе органических солей магния (цитрата, лактата, пидолата) в сочетании с синеpгистами (пиридоксином и другими витамерами). Данные по доказательной медицине препаратов на основе органических солей магния были приведены в связи с рассмотрением влияния обеспеченности магния и пиридоксина на метаболизм жиров, белков и углеводов, процессы воспаления и гепатопротекцию.
Заключение
Детское и подростковое ожирение – следствие издержек современного образа жизни: гиподинамии, переедания, избыток искусственных продуктов питания, обедненных микронутриентами и др. Для того, чтобы не допустить развитие ожирения в зрелом возрасте, следует, как минимум, восстановить в семье культуру питания и исключить такие стимулирующие ожирение продукты, как «безалкогольные напитки», лимонады, напитки типа «кола», содержащие большое количество красителей и не являющиеся источниками каких-либо микронутриентов. Дети, страдающие избыточным весом и ожирением, испытывают комплекс дополнительных психологических проблем в общении со сверстниками, трудоустройстве, построении семьи. Даже если эти дети и подростки выстраивают семью в последующем, то они неосознанно переносят неправильные привычки питания на своих детей (рис. 8).
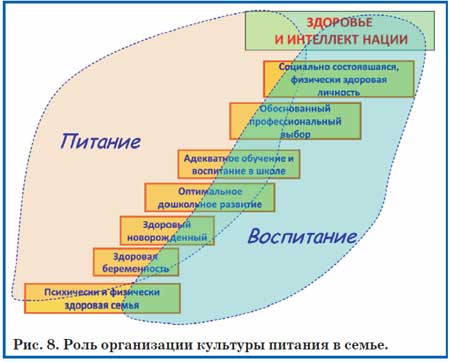
В изменившейся за последние 50–100 лет системе питания обедненный по магнию рацион питания стал обычным явлением и у взрослых, и у детей разного возраста. ДМ у детей проявляется в нарастании риска таких необычных для педиатрии проблем, как детское и подростковое ожирение, ИР, МС, АГ с подросткового и молодого возраста и др. Все эти патологические состояния ассоциированы с хроническим ДМ. Конечно, ожирению в значительной мере способствуют гиподинамия, избыточная калорийность и микронутриентная неполноценность потребляемой детьми пищи. В то же время не следует забывать и о том, что высококалорийная по углеводам и жирам пища практически лишена биоусвояемого магния, так что ДМ в такой диете провоцирует накопление избыточного висцерального жира.
По данным клинико-эпидемиологических исследований, адекватная обеспеченность населения магнием значительно снижает риск развития ожирения и других компонентов МС. Клинические испытания в рамках доказательной медицины показывают перспективность использования пероральных препаратов органического магния и его синергиста пиридоксина (органические соли магния лактат, пидолат, цитрат в составе препаратов Магне B6, Магне B6 Форте,Магне B6 в растворе для питья) для восполнения ДМ в комплексной терапии и профилактике избыточной МТ и МС как у взрослых, так и у детей. При этом компенсация дефицита и наполнение депо магния лучше всего достигаются при длительном назначении препаратов органического магния – от 6 мес до 2 лет [42]. Использование пидолата магния с пиридоксином в растворе (ампульная форма Магне B6 в растворе для питья) разрешено с 1 года; лактата и цитрата магния – с 6 лет. Восполнение ДМ цитратом магния (Магне B6 Форте) рекомендуется детям с ацидозом (или со сдвигом в сторону ацидоза) и оксалатурией для профилактики мочекаменной болезни.
Среди солей органического магния для восполнения ДМ при лечении ожирения в составе комплексной терапии у подростков наиболее подходит цитрат магния (соль магния и лимонной кислоты). Известно, что лимонная кислота помогает расщеплять жиры, ускоряет обмен веществ и устраняет чувство голода. Цитрат является исключительной по своей эффективности и безопасности формой магния, так как цитрат анион принимает участие в центральном энергетическом цикле каждой клетки – цикле Кребса. Кроме того, соли лимонной кислоты хорошо растворяются в воде и цитрат анион способствует снижению риска образования камней в почках [51]. Рекомендуется запивать препарат цитрата магния достаточным количеством чистой питьевой воды (150–300 мл). Напомним, что недостаточное потребление воды детьми и подростками приводит к задержке эндотоксинов в организме и способствует нарушениям жирового обмена.
Использование пидолата магния приводит к наибольшему увеличению уровней магния в плазме крови в течение 2–3 ч, что важно для - быстрой ликвидации ДМ [52]. Возможность применять пидолат магния с года, а также хороший профиль комплаентности (удобная форма питьевого раствора с приятным вкусом, прием 2–3 раза в день) дают возможность рекомендовать комбинацию пидолата магния и пиридоксина в качестве препарата выбора при восполнении ДМ у детей младшего возраста с избыточным весом и ожирением.
Контактная информация:
Громова Ольга Алексеевна – д.м.н., проф. каф. фармакологии с клинической фармакологией Литература 1.Livingstone B. Epidemiology of childhood obesity in Europe, Eur. J. Pediatr. 2000; 159 (Suppl. 1): 14–34.
ГБОУ ВПО «Ивановская государственная медицинская академия» Минздрава России, научный консультант Российского центра Института микроэлементов ЮНЕСКО
Адрес: 153000 г. Иваново, Шереметевский пр-кт, 8
2.Петеркова В.А., Ремизов О.В. Ожирение в детском возрасте. Ожирение и метаболизм. 2004; 1: 17–23.
3.Кравец Е.Б., Самойлова Ю.Г. Клинические лекции по детской эндокринологии. Томск: Поиск, 2010: 360 с.
4.Evans SJ. Social workers are weighing in and taking away children from parents who give in to their cravings and feed them too much. Dayly Mail, 2014.
5.Громова О.А., Калачева А.Г., Торшин И.Ю. и др. Недостаточность магния – достоверный фактор риска комор-бидных состояний: результаты крупномасштабного скрининга магниевого статуса в регионах России. Фарматека. 2013; 259 (6): 116–129.
6.Керимкулова Н.В., Никифорова Н.В., Владимирова И.С. и др. Влияние недифференцированной дисплазии соединительной ткани на исходы беременности и родов. комплексное обследование беременных с дисплазией соединительной ткани с использованием методов интеллектуального анализа данных. Земский врач. 2013; 19 (2): 34–38.
7.Громова О.А., Торшин И.Ю., Гришина Т.Р., Федотова Л.Э. Дефицит магния как проблема стресса и дезадаптации у детей. Русский медицинский журнал. 2012; 20 (16): 813–821.
8.Торшин И.Ю., Громова О.А. Дисплазия соединительной ткани, клеточная биология и молекулярные механизмы воздействия магния. Русский медицинский журнал. 2008; 16 (4): 228.
9.Ford ES, Li C, McGuire LC, et al. Intake of dietary magnesium and the prevalence of the metabolic syndrome among U.S. adults. Obesity (Silver Spring). 2007; 15 (5): 1139–1146.
10.Soltani N, Keshavarz M, Minaii B, et al. Effects of administration of oral magnesium on plasma glucose and pathological changes in the aorta and pancreas of diabetic rats. Clin. Exp. Pharmacol. Physiol. 2005; 32 (8): 604–610.
11.Belin RJ, He K. Magnesium physiology and pathogenic mechanisms that contribute to the development of the metabolic syndrome. Magnes Res. 2007; 20 (2): 107–129.
12.Olatunji LA, Soladoye AO. Increased magnesium intake prevents hyperlipidemia and insulin resistance and reduces lipid peroxidation in fructose-fed rats. Pathophysiology. 2007; 14 (1): 11–15.
13. Ahsan SK, al-Swoyan S, Hanif M, Ahmad M. Hypomagnesemia and clinical implications in children and neo- nates. Indian J. Med. Sci. 1998; 52 (12): 541–547.
14.Morales-Ruаn Mdel C, Villalpando S, Garcia-Guerra A, et al. Iron, zinc, copper and magnesium nutritional status in Mexican children aged 1 to 11 years. Salud. Publica Mex. 2012; 54 (2): 125–134.
15.Гришина Т.Р., Сатарина Т.Е., Калачева А.Г. и др. Элементный статус подростков и молодых людей, проживающих на территории Ивановской области. Вестник Ивановской медицинской академии. 2012; 17 (1): 15.
16.De la Cruz-Gоngora V, Gaona B, Villalpando S, et al. Anemia and iron, zinc, copper and magnesium deficiency in Mexican adolescents: National Health and Nutrition Survey 2006. Salud. Publica Mex. 2012; 54 (2): 135–145.
17.Vanaelst B, Huybrechts I, Michels N, et al. Hair minerals and metabolic health in Belgian elementary school girls. Biol. Trace Elem. Res. 2013; 151 (3): 335–343.
18.Jose B, Jain V, Vikram NK, et al. Serum magnesium in overweight children. Indian Pediatr. 2012; 49 (2): 109–112.
19.Torshin IYu, Gromova OA. Magnesium and pyridoxine: fundamental studies and clinical practice. Nova Science, 2011: 250. ISBN-10:1-60741-704-9.
20.Takaya J, Higashino H, Kobayashi Y. Intracellular magnesium and insulin resistance. Magnes Res. 2004; 17 (2): 126–136.
21Celik N, Andiran N, Yilmaz AE. The relationship between serum magnesium levels with childhood obesity and insulin resistance: a review of the literature. J. Pediatr. Endocrinol. Metab. 2011; 24 (9–10): 675–678.
22.Takaya J, Yamato F, Kuroyanagi Y, et al. Intracellular magnesium of obese and type 2 diabetes mellitus children. Diabetes Ther. 2010; 1 (1): 25–31.
23.Huerta MG, Roemmich JN, Kington ML, et al. Magnesium deficiency is associated with insulin resistance in obese children. Diabetes Care. 2005; 28 (5): 1175–1181.
24. Song Y, He K, Levitan EB, et al. Effects of oral magnesium supplementation on glycaemic control in Type 2 diabetes: a meta-analysis of randomized double-blind controlled trials. Diabet Med. 2006; 23 (10): 1050–1056.
25. Mooren FC, Kruger K, Volker K, et al. Oral magnesium supplementation reduces insulin resistance in non-diabetic subjects – a double-blind, placebo-controlled, randomized trial. Diabetes Obes Metab. 2011; 13 (3): 281–284.
26.Nielsen FH. Dietary fatty acid composition alters magnesium metabolism, distribution, and marginal deficiency response in rats. Magnes Res. 2009; 22 (4): 280–288.
27.Torshin IYu. Sensing the change from molecular genetics to personalized medicine. Nova Biomedical Books, NY, USA, 2009, In: «Bioinformatics in the Post-Genomic Era» series, ISBN 1-60692-217-0.
28. Weis MT, Bercute A. Comparison of long-chain fatty acyl-CoA synthetases from rabbit heart and liver: substrate preferences and effects of Mg2+. Biochem. J. 1997; 322 (Pt. 2): 649–654.
29. Gueux E, Rayssiguier Y, Piot MC, Alcindor L. Reduction of plasma lecithin-cholesterol acyltransferase activity by acute magnesium deficiency in the rat. J. Nutr. 1984; 114 (8): 1479–1483.
30. Nozue T, Ide N, Okabe H, Narui K. Correlation of serum HDL-cholesterol and LCAT levels with the fraction of ionized magnesium in children. Magnes Res. 1999; 12 (4): 297–301.
31. Hadjistavri LS, Sarafidis PA, Georgianos PI, et al. Beneficial effects of oral magnesium supplementation on insulin sensitivity and serum lipid profile. Med. Sci. Monit. 2010; 16 (6): R307–R312.
32. Abraham PM, Kuruvilla KP, Mathew J, et al. Alterations in hippocampal serotonergic and INSR function in streptozotocin induced diabetic rats exposed to stress: neuro-protective role of pyridoxine and Aegle marmelose. J. Biomed. Sci. 2010; 17: 78.
33. Kiran SG, Dorisetty RK, Umrani MR, et al. Pyridoxal 5' phosphate protects islets against streptozotocin-induced beta-cell dysfunction--in vitro and in vivo. Exp. Biol. Med. (Maywood). 2011; 236 (4): 456–465.
34. Sharafetdinov KhKh, Plotnikova OA, Meshcheriako-va VA, et al. Vitamin supply in patients with non-insulin-dependent diabetes mellitus. Сlin. Med. (Mosk). 1999; 77 (4): 26–28.
35. Spellacy WN, Buhi WC, Birk SA. Vitamin B6 treatment of gestational diabetes mellitus: studies of blood glucose and plasma insulin. Am. J. Obstet. Gynecol. 1977; 127 (6): 599–602.
36. Bennink HJ, Schreurs WH. Improvement of oral glucose tolerance in gestational diabetes by pyridoxine. Br. Med. J. 1975; 3 (5974): 13–15.
37. Северин Е.С. Биохимия. М.: ГэотарМед, 2008: 967 с.
38. Saha H, Harmoinen A, Karvonen AL, et al. Serum ionized versus total magnesium in patients with intestinal or liver disease. Clin. Chem. Lab. Med. 1998; 36 (9): 715–718.
39. Sanchez-Morito N, Planells E, Aranda P, Llopis J. Influence of magnesium deficiency on the bioavailability and tissue distribution of iron in the rat. J. Nutr. Biochem. 2000; 11 (2): 103–108.
40. Todorovic T, Vujanovic D. The influence of magnesium on the activity of some enzymes (AST, ALT, ALP) and lead content in some tissues. Magnes Res. 2002; 15 (3–4): 173–177.
41. Kielczykowska M, Musik I, Hordyjewska A, et al. Oral administration of lithium increases tissue magnesium contents but not plasma magnesium level in rats. Pharmacol. Rep. 2007; 59 (3): 291–295.
42. Heubi JE, Higgins JV, Argao EA, et al. The role of magnesium in the pathogenesis of bone disease in childhood cholestatic liver disease: a preliminary report. J. Pediatr. Gastroenterol. Nutr. 1997; 25 (3): 301–306.
43. Calderon AT, Martinez-Sarmiento J, Montes ME, et al. Quantitative study of metals in bile from patients with cholelithiasis. Rev. Esp. Enferm. Dig. 2000; 92 (7): 439–447.
44. Ko CW. Magnesium: does a mineral prevent gallstones? Am. J. Gastroenterol. 2008; 103 (2): 383–385.
45. Ortega RM, Fernandez-Azuela M, Encinas-Sotillos A, et al. Differences in diet and food habits between patients with gallstones and controls. J. Am. Coll. Nutr. 1997; 16 (1): 88–95.
46. Tsai CJ, Leitzmann MF, Willett WC, Giovannuc-ci EL. Long-term effect of magnesium consumption on the risk of symptomatic gallstone disease among men. Am. J. Gastroenterol. 2008; 103 (2): 375–382.
47. Fulgoni VL, Quann EE. National trends in beverage consumption in children from birth to 5 years: analysis of NHANES across three decades. Nutr. J. 2012; 31 (11): 92.
48. Koivisto M, Valta P, Hockerstedt K, Lindgren L. Magnesium depletion in chronic terminal liver cirrhosis. Clin. Transplant. 2002; 16 (5): 325–328.
49. McKeown NM, Jacques PF, Zhang XL, et al. Dietary magnesium intake is related to metabolic syndrome in older Americans. Eur. J. Nutr. 2008; 47 (4): 210–216.
50. O'Neil CE, Keast DR, Nicklas TA. Out-of-hand nut consumption is associated with improved nutrient intake and health risk markers in US children and adults: National Health and Nutrition Examination Survey 1999–2004. Nutr. Res. 2012; 32 (3): 185–194.
51. Торшин И.Ю., Громова О.А. Двадцать пять мгновений молекулярной фармакологии. М.: А-Гриф, 2013: 674 с.
52. Громова О.А., Торшин И.Ю., Калачева А.Г. и др. Динамика концентрации магния в крови после приема различных магнесодержащих препаратов. Фарматека. 2009; 10: 63–68.
RU.MGP.14.05.03
