Младенческие кишечные колики: современный взгляд на проблему
СтатьиОпубликовано в журнале:Публикация размещена с разрешения Администрации сайта www.con-med.ru
Все права на публикацию принадлежат ООО «ММА «МедиаМедика».
Не допускается тиражирование, воспроизведение текста или его фрагментов с целью коммерческого использования.
«Consilium Medicum. Педиатрия» №4, 2014
И.Н.Захарова1 , Г.В.Яцык2 , Т.Э.Боровик2 , В.А.Скворцова2 , Н.Г.Звонкова2 , Ю.А.Дмитриева1 , Н.Г.Сугян1, Е.Н.Касаткина3, Е.Б.Мачнева1
1ГБОУ ДПО РМАПО Минздрава России, Москва;
2ФГБНУНаучный центр здоровья детей РАН;
3ГБУЗ Тушинская детская городская больница Департамента здравоохранения г. Москвы
Функциональные нарушения органов пищеварения представляют собой обширную группу состояний, широко распространенных в раннем детском возрасте. Согласно общепринятому определению к функциональным расстройствам желудочно-кишечного тракта (ЖКТ) относят разные комбинации постоянных или повторяющихся симптомов, которые не могут быть объяснены структурными или биохимическими нарушениями [1]. При функциональных нарушениях ЖКТ могут изменяться моторная функция, переваривание и всасывание пищевых веществ, а также состав кишечной микрофлоры и активность иммунной системы. Причины функциональных расстройств часто лежат вне пораженного органа и обусловлены нарушением нервной и гуморальной регуляции деятельности пищеварительного тракта [1].
В соответствии с III Римскими критериями 2006 г. [2] к функциональным нарушениям ЖКТ у младенцев и детей второго года жизни относятся:
- G1. Срыгивание у младенцев.
- G2. Синдром руминации у младенцев.
- G3. Синдром циклической рвоты.
- G4. Младенческие кишечные колики.
- G5. Функциональная диарея.
- G6. Болезненность и затруднения дефекации (дисхезия) у младенцев.
- G7. Функциональные запоры.
У детей грудного возраста, особенно первых 6 мес жизни, часто встречаются такие состояния, как срыгивания, кишечные колики и функциональные запоры. Более чем у 1/2 детей они наблюдаются в разных комбинациях, реже - как один изолированный симптом. Поскольку причины, приводящие к функциональным нарушениям, оказывают влияние на разные процессы в ЖКТ, сочетание симптомов у одного ребенка представляется вполне закономерным. Так, после перенесенной гипоксии могут возникнуть вегетовисцеральные нарушения с изменением моторики по гипер- или гипотоническому типу и нарушения активности регуляторных пептидов, приводящие одновременно к срыгиваниям (в результате спазма или зияния сфинктеров), коликам (нарушения моторики ЖКТ при повышенном газообразовании) и запорам (гипотоническим или вследствие спазма кишки).
Термин «колика» произошел от греч. «colicos», что означает «боль в кишке». Они являются одной из наиболее частых причин обращения к педиатру родителей, имеющих детей первых месяцев.
Под синдромом кишечных колик подразумеваются эпизоды болезненного плача и беспокойства ребенка, которые занимают не менее 3 ч в день и возникают не реже 3 раз в неделю [2]. Наиболее типичное время для кишечных колик - вечерние часы. Приступы плача возникают и заканчиваются внезапно, без каких-либо внешних провоцирующих причин. По современным данным, распространенность младенческих кишечных колик среди детей первых месяцев жизни колеблется от 5 до 19% [3], хотя некоторые исследователи указывают, что кишечные колики встречаются значительно чаще. Значительные различия эпидемиологических данных, по-видимому, связаны с отсутствием единых подходов и критериев оценки данного состояния.
Принято считать, что кишечные колики впервые появляются на 2-3-й неделе жизни ребенка, усиливаются на 2-м месяце и уменьшаются после 3 мес [4]. По данным J.Paradise (1996 г.), кишечные колики развиваются у младенцев в возрасте 2,6±1,8 нед. В 1,5-месячном возрасте частота развития кишечных колик составляет 62%, в 3-месячном возрасте - 34%. Автором показано, что выраженность и частота кишечных колик уменьшаются с возрастом (в возрасте 1-3 мес они встречаются у 29% детей, в 4-6 мес -у 7-11%) [5].
A.Douwes [6] указывает на то, что кишечные колики встречаются у 25% доношенных новорожденных в возрасте до 1 мес, находящихся на грудном вскармливании и у 31% - на искусственном. Уже в 1960 г. T.Brazelton отметил, что длительность колик максимальна в возрасте 6 нед, они сохраняются до 12 нед с постепенным уменьшением продолжительности беспокойства ребенка [7]. Позже в 1962 г. тот же исследователь опубликовал данные по длительности плача здорового ребенка в зависимости от возраста.
Так, в возрасте 2 нед ребенок в среднем плачет 1 ч 45 мин, в возрасте 6 нед - 2 ч 45 мин, а в возрасте 12 нед - менее чем 1 ч. Пиковое время суток, когда ребенок интенсивно плачет,
- от 15 до 23 ч. Автор считает, что младенцы, плач которых значительно превышает эти средние значения, могут характеризоваться как имеющие колики [8].
Механизмы развития кишечных колик остаются до конца не выясненными, но многочисленные исследования позволили продвинуться в понимании данной проблемы и сделать определенные выводы:
- - младенческие колики наиболее распространены среди первенцев в семье [9];
- - колики чаще возникают у детей, рожденных у матерей старше 30 лет и имеющих высшее образование [10];
- - матери детей с коликами отличаются повышенной тревожностью и склонностью к депрессии [11];
- - в рационах питания матерей, чьи дети имеют колики, чаще содержатся коровье молоко, брокколи, цветная и белокочанная капуста, лук и шоколад [12];
- - кишечные колики чаще встречаются среди детей на грудном вскармливании [10];
- - у детей с коликами содержание в крови мотилина и серотонина, стимулирующих активность ЖКТ, повышено [13, 14], а холецистокинина (ХЦК), регулирующего восприятие боли, - снижено [15];
- - младенцы с коликами имеют повышенную кишечную проницаемость [16];
- - уровень кальпротектина, отражающего воспалительный процесс в кишечнике, при наличии колик у детей повышен [17];
- - для детей с коликами характерны дисбиотические изменения в кишечнике, сопровождающиеся увеличением содержания кишечной палочки, клебсиеллы и снижением количества лактобактерий [18].
Таким образом, возникновению кишечных колик способствуют разные факторы как со стороны матери, так и ребенка, включая неадекватное его питание (табл. 1) [19].
|
Таблица 1. Факторы, предрасполагающие к развитию кишечных колик |
||
|
Со стороны матери |
Со стороны ребенка |
Вскармливание |
|
Неблагоприятный акушерско-гинекологический анамнез матери - гестоз, гиподинамия во время беременности |
Морфофункциональная незрелость органов пищеварения |
Грудное вскармливание |
|
Нарушение питания кормящей матери (употребление коровьего молока или продуктов на его основе, очень жирной пищи, продуктов, усиливающих метеоризм) |
Недоношенность |
Неправильное разведение смесей |
|
Вредные привычки кормящей женщины (курение, употребление алкоголя, наркотиков) |
Постгипоксическое поражение ЦНС |
Неправильная техника кормления |
|
Эмоциональные стрессы в семье |
Особенности темперамента младенца |
Насильственное кормление |
|
Возраст (старше 30 лет) и образование матери |
Дисбиотические нарушения в кишечнике |
|
|
Первый ребенок в семье |
• Гастроинтестинальная форма пищевой аллергии • Лактазная недостаточность |
|
На основании имеющихся в настоящее время данных можно выделить важные причины возникновения колик, что является необходимым для выработки тактики их купирования.
В норме небольшое количество воздуха попадает в желудок во время глотания. Физиологическая его роль заключается в стимуляции моторики желудка (часть воздуха переходит транзитом через привратник в кишечник). Газы продуцируются бактериями кишечника, но при несовершенстве моторики нарушается их выведение. Имеется еще один механизм, играющий существенную роль при патологических состояниях. Он связан с уменьшением поглощения газов кишечной стенкой в результате ускоренного пассажа пищи или распространенного воспалительного процесса в слизистой кишки. Механизмы, перемещающие газ по пищеварительной трубке, изучены недостаточно. Известно, что в толстой кишке каловые массы транспортируются в 30-100 раз медленнее, чем жидкость или газ. Необходимо отметить, что растяжение или спазм любого участка пищеварительного тракта в связи с повышенным газообразованием может вызвать спектр ощущений от легкого дискомфорта до боли.
Нарушение техники кормления способствует избыточному заглатыванию большого количества воздуха (аэрофагии). У грудных детей аэрофагия возникает, например, во время сосания пустой соски или груди с малым количеством молока и может являться причиной беспокойства ребенка. К симптомам, свидетельствующим об аэрофагии у грудных детей, относятся крик во время кормления, вздутие живота, отказ от еды, а после кормления - срыгивание или реже рвота «фонтаном». Умеренная аэрофагия нередко отмечается у детей первых месяцев жизни в связи с незрелостью нервной регуляции процесса глотания. В большей степени аэрофагия характерна для недоношенных, а также детей, незрелых к моменту рождения.
Морфофункциональная незрелость пищеварительного тракта, сопровождающаяся незрелостью ферментативной системы, нарушениями микробиоценоза кишечника, приводит к неполному расщеплению жиров и углеводов, что способствует избыточному газообразованию. Возрастные особенности анатомо-физиологического строения ЖКТ у детей раннего возраста представлены в табл. 2.
|
Таблица 2. Анатомо-физиологические особенности пищеварительного тракта у детей раннего возраста [20] |
|
|
Отделы ЖКТ |
Особенности у детей раннего возраста |
|
Полость рта |
Недостаточная секреция слюны до 3-месячного возраста |
|
Пищевод |
Воронкообразная форма пищевода у детей до 3 лет, отсутствие анатомических сужений |
|
Желудок |
Малые размеры, разнообразие форм, слабо развитое кольцо кардиального жома, относительно высокий тонус привратника, гипохлоргидрия |
|
ДПК |
Низко расположенные круговые складки поперечного направления, разные варианты открытия вирсунгова и санториниева протоков |
|
Желчный пузырь |
Грушевидная, реже - веретенообразная или S-образная форма |
|
Поджелудочная железа |
Окончательно не сформирована. После введения прикорма повышается экскреторная функция |
|
Кишечник |
Повышенная проницаемость слизистой оболочки. До 3 лет отмечается относительная слабость илеоцекального клапана |
С первых дней жизни ребенок начинает получать грудное молоко (или детскую молочную смесь). Количество еды постепенно возрастает, увеличивается объем желудка, активизируются ферментативная и моторная функции ЖКТ, происходит становление микробиоценоза кишечника и т.д. На эти процессы оказывает влияние большое количество факторов, поэтому новорожденных следует рассматривать как группу повышенного риска по развитию функциональных нарушений, особенно при наличии недоношенности, морфофункциональной незрелости, перенесенной внутриутробной гипоксии или асфиксии в родах, длительного периода полного парентерального питания, раннего искусственного вскармливания.
Функционирование пищеварительной системы, взаимодействие моторики, секреции и всасывания в кишечнике регулируются сложной системой нервных и гуморальных механизмов. Выделяют три основных механизма регуляции пищеварительного аппарата: центральный рефлекторный, гуморальный и локальный. Центральное рефлекторное влияние в большей мере выражено в верхней части пищеварительного тракта. По мере удаления от ротовой полости его участие снижается, вместе с тем возрастает роль гуморальных механизмов. Наиболее выражены их влияние на деятельность желудка, двенадцатиперстной кишки (ДПК), поджелудочной железы, желчеобразование и желчевыведение. В тонкой и особенно толстой кишке проявляются преимущественно локальные механизмы регуляции (за счет механических и химических раздражений).
В ряде случаев развитию младенческих кишечных колик способствует незрелость нервной и эндокринной систем, участвующих в регуляции ЖКТ (расстройства саморегуляции кишечника). Основную роль в нервной регуляции функций ЖКТ играет энтеральная нервная система, которая является частью центральной нервной системы (ЦНС) и состоит из множества (около 100 млн) нейронов. Нейроны энтеральной нервной системы сгруппированы в ганглиях, соединены переплетениями нервных отростков в два главных сплетения - мезентериальное (мейсснеровское) и подслизистое (ауэрбахово). При растяжении гладких мышц кишечника происходит стимуляция афферентных нейронов, которые воспринимают сигнал и передают возбуждение к промежуточным нейронам вегетативной нервной системы, участвующим в регуляции моторики и секреции. Связь нервной системы кишечника с ЦНС осуществляется через моторные и сенсорные симпатические и парасимпатические пути. Вегетовисцеральные нарушения разной степени встречаются более чем у 1/2 детей первого года жизни, но чаще всего они наблюдаются у недоношенных детей. Известно, что при сроке гестации менее 32 нед наблюдается неравномерное распределение нейронов вдоль окружности кишки. Вместе с тем признаки морфофункциональной незрелости регуляторных систем кишечника встречаются и у доношенных детей. Созревание нервной системы кишечника продолжается до 12-18-месячного возраста ребенка. Нередко вегето-висцеральным нарушениям центрального генеза сопутствуют синдромы гипервозбудимости и внутричерепной гипертензии, а по мере устранения симптомов перинатального поражения ЦНС отмечается регресс висцеральных расстройств.
Следует отметить, что большую роль в возникновении кишечных колик у младенцев играют индивидуальные особенности - повышение или снижение порога болевой чувствительности, а также чувствительности к растяжению кишечной стенки.
Большое значение для гуморальной регуляции пищеварительных функций имеют гастроинтестинальные гормоны - группа биологически активных пептидов, вырабатываемых эндокринными клетками и нейронами ЖКТ и поджелудочной железы. Эти гормоны обладают регуляторным влиянием на секреторные функции, всасывание, моторику, кровоснабжение ЖКТ и трофические процессы в нем, оказывают также ряд общих воздействий на обмен веществ.
От гормонов в их классическом понимании гастроинтестинальные гормоны отличаются рядом признаков в первую очередь тем, что секретирующие их клетки не объединены в четко выраженные железистые структуры, а расположены диффузно в разных отделах ЖКТ. По сходству аминокислотного состава и последовательности аминокислот гастроинтестинальные гормоны объединяют в 3 семейства:
- - гастрина (гастрин, ХЦК);
- - секретина (глюкагон, энтероглюкагон, вазоактивный интестинальный полипептид, желудочно-ингибирующий пептид и др.);
- - панкреатического полипептида (панкреатический пептид и нейропептид Y).
Часть гастроинтестинальных гормонов, таких как гастрин-рилизинг-гормон, соматостатин, мотилин, нейротензин и др., не относится ни к одному из перечисленных семейств. «Период полужизни» для всех гастроинтестинальных гормонов измеряется минутами.
Гастрин синтезируется G-клетками, расположенными в слизистой оболочке антральной части желудка и криптах, ворсинках бруннеровых желез ДПК. Выделение гастрина стимулируется приемом пищи, растяжением желудка. Торможение секреции этого гормона происходит при закислении желудочного содержимого. Основные физиологические эффекты гастрина - стимуляция секреции соляной кислоты и пепсина, а также регуляция трофики желудка, ДПК и поджелудочной железы. Гастрин и пентагастрин повышают тонус нижнепищеводного сфинктера, усиливая барьерную функцию этой преграды для желудочно-пищеводного заброса.
Секретин - пептидный гормон, вырабатываемый S-клетками в слизистой оболочке тонкой кишки и участвующий в регуляции секреторной деятельности поджелудочной железы. Основной физиологический эффект секретина - увеличение объема жидкой части панкреатического секрета, концентрации и количества бикарбонатов в нем.
ХЦК - нейропептидный гормон, вырабатываемый I-клетками слизистой оболочки ДПК и проксимальным отделом тощей кишки. Ведущими эффектами ХЦК являются активное усиление моторики желчного пузыря и значительная стимуляция панкреатической секреции. Синхронное с сокращением желчного пузыря расслабление сфинктера Одди способствует поступлению желчи в ДПК. Сюда же выделяются стимулированные эндогенным или экзогенным ХЦК панкреатические ферменты, создавая оптимальные условия для расщепления разных компонентов пищи. В настоящее время доказана роль в генезе кишечных колик у детей ХЦК, который обладает седативным действием. Полагают, что сниженная концентрация ХЦК, регулирующего чувство насыщения и восприятие боли, может обусловливать более высокую возбудимость детей с кишечными коликами.
Панкреатический полипептид - секретируется РР-клетками островков Лангерганса поджелудочной железы. Подавляющее большинство клеток, синтезирующих панкреатический полипептид, расположено в области головки поджелудочной железы. Панкреатический полипептид по своему действию является антагонистом ХЦК. В физиологических концентрациях подавляет секрецию панкреатического сока и расслабляет гладкие мышцы желчного пузыря.
Мотилин - полипептидный гормон, секретируется энтерохромаффинными клетками слизистой оболочки ДПК и тощей кишки. Он стимулирует перистальтические сокращения гладких мышц стенки желудка, кишечника. Мотилин является важнейшим нейротрансмиттером, регулирующим желудочно-кишечную моторику путем непосредственного воздействия полипептида на стимулирующие рецепторы на мышечных клетках. Мотилин увеличивает тонус нижнепищеводного сфинктера, ускоряет опорожнение желудка и усиливает сократительную активность толстой кишки. У человека выделение мотилина стимулируется жирами, а глюкоза тормозит выделение гормона. L.Lot и соавт. (1987 г.) показали, что уровень вазоактивного кишечного пептида и гастрина повышен у детей с разными желудочно-кишечными расстройствами (но не при кишечных коликах) [21]. Авторы сообщили о повышении базального уровня мотилина у детей с коликами и выдвинули гипотезу о его роли в их возникновении.
В последнее время также есть данные о повышении уровня грелина (пептидного гормона, секретируемого P/D-клетками слизистой оболочки фундального отдела желудка) в сыворотке крови у детей с кишечными коликами в сравнении со здоровыми детьми. Предполагается, что данный гормон причастен к нарушению перистальтики кишечника и повышает аппетит. Его можно считать посредником между кишечником и головным мозгом [22].
Большинство авторов считают, что младенческие кишечные колики обусловлены незрелостью нервной и эндокринной регуляции деятельности кишечника, а также анатомическими особенностями строения ЖКТ у детей раннего возраста (длинная брыжейка, маятникообразные движения кишечника), приводящими к нарушению моторики. Для детей с кишечными коликами характерно замедление опорожнения желудка, в то время как транзит по кишке в большинстве случаев не нарушен [23].
Один из вариантов развития кишечных колик обусловлен дискинетическими явлениями в толстой кишке. Этот вариант колик чаще наблюдается во время или после приема пищи. Возникновение кишечных колик может быть связано с гастроилеальным и гастроцекальным рефлексами, которые были описаны еще в 1909 г. G.Holzknecht и S.Jonas. Сущность рефлексов состоит в том, что в течение первых 10 мин после приема пищи наблюдается периодическое повышение моторной активности толстой кишки. Перистальтические волны достигают прямой кишки, обусловливая позыв к дефекации. Общие механизмы регуляции моторики и секреции, особенно тонкой кишки, дают основания предполагать, что нарушения моторики могут сопровождаться вторичными нарушениями кишечной секреции.
На возникновение кишечных колик может влиять изменение состава кишечной микробиоты. Дисбаланс микрофлоры кишечника является фактором риска повышенного газообразования. Газ является одним из главных продуктов бактериальной ферментации углеводов и белков, поступающих в толстую кишку в результате их избыточного потребления или недостаточного переваривания [24, 25]. При лактазной недостаточности повышенное газообразование связано с образованием водорода в процессе бактериального брожения нерасщепленной лактозы. При этом в патогенезе колик играют роль не только повышенное газообразование и нарушение его пассажа, но и качественный состав газа. У детей на грудном вскармливании - это водород, который выделяется при брожении лактозы грудного молока. У детей на искусственном вскармливании или получающих прикорм - газ метан. Метан также образуется строгими анаэробами при переваривании белка и углеводов [26]. Потенциальной цитотоксичностью обладают аммиак и сероводород, продуцируемые протеолитической анаэробной микрофлорой.
Проведенные F.Savino и соавт. (2004 г.) исследования выявили различия в содержании лактобацилл у детей с коликами и без них. Так, у детей с кишечными коликами были обнаружены Lactobacillus brevis и Lactococcus lactis, а у здоровых детей в составе микробиоты преобладали Lactobacillus acidophilus. Предполагается, что L. brevis и L. lactis участвуют в патогенезе кишечных колик, увеличивая метеоризм [18]. Также установлено достоверное увеличение содержания кишечной палочки в микрофлоре кишечника у детей с кишечными коликами по сравнению со здоровыми младенцами [27].
На кафедре педиатрии ГБОУ ДПО РМАПО Минздрава России проведен анализ состояния микробиоценоза кишечника у детей грудного возраста с кишечными коликами. Нормоценоз обнаружен только у 5% детей. У большинства детей (86,7%) отмечался дисбактериоз кишечника 2- и 3-й степени. Причем дисбиотические нарушения кишечника 3-й степени (52,8%) были более характерными для детей, находящихся на грудном вскармливании [28]. При анализе состава кишечной микрофлоры у детей с кишечными коликами установлено значительное снижение содержания представителей облигатной микрофлоры. Эти изменения были более выражены при грудном вскармливании. У 55,5% детей, вскармливаемых грудью, и у 29,2% детей, находящихся на искусственном вскармливании, выявлялось низкое содержание бифидобактерий (<107). Обращает на себя внимание большой процент детей, у которых обнаружились кишечная палочка с гемолизирующими свойствами (40%) и гемолизирующие формы стафилококка (35-37%).
Регуляция моторики ЖКТ имеет многоуровневый характер и помимо ЦНС и периферической нервной системы осуществляется на местном уровне непосредственно в кишечнике. Значительный вклад в местную регуляцию моторики вносит микрофлора ЖКТ как за счет формирования каловых масс, так и путем выработки разных метаболитов, в том числе короткоцепочечных жирных кислот (КЖК).
В результате многочисленных исследований установлено, что при ферментации углеводов (нерасщепляемый крахмал, олигосахариды, пищевые волокна) анаэробными бактериями и условно-патогенной флорой (пропионобактерии, бактероиды, фузобактерии, клостридии, пептострептококки, копрококки, лактобациллы, эубактерии и др.) образуются КЖК. При расщеплении углеводов - уксусная (ацетат), пропионовая (пропионат) и масляная (бутират) кислоты. Изобутират, изовалериат и 2-метилбутират формируются из аминокислот (валина, лейцина и изолейцина соответственно), которые также являются значимым источником КЖК для человека. Около 30% белков в кишечнике превращаются в КЖК, которые образуются также при расщеплении липидов и нуклеиновых кислот. Существенным источником исходных субстратов брожения является сам организм, а именно: гликопротеиды слизи, специфическая оболочка эпителия - гликокаликс, отмершие и отделившиеся от основного пласта клетки эпителия и «остаточные» белки. Установлено, что КЖК влияют на моторику ЖКТ. В низкой концентрации они оказывают стимулирующий эффект на гладкомышечные клетки кишечника через холинэргический рефлекс, а в высокой - ингибируют моторику толстой кишки. Они влияют на моторику сегментов кишечника как местно, так и через кровеносную и нервную системы кишечника, модулируя такие физиологические функции, как илеотолстокишечное торможение, защиту от илеоцекального рефлюкса [29].
При функциональных нарушениях ЖКТ, проявляющихся кишечными коликами и диарейным синдромом, происходят резкое снижение доли уксусной кислоты и повышение количества пропионовой и масляной кислот, причем данные изменения нарастают с утяжелением степени выраженности нарушения кишечной микрофлоры. Изменения профилей кислот можно объяснить как нарушением моторной функции кишечника, так и с позиций изменения видового состава кишечной микрофлоры, продуцирующей разные короткоцепочечные кислоты. Известно, что микрофлора создает для колоноцитов как энергетическую, так и сырьевую базу синтетической деятельности [30, 31]. Анаэробы следует рассматривать как основные виды, непосредственно обеспечивающие нормальное функционирование эпителия. Имеющиеся изменения при функциональных нарушениях ЖКТ возможно объяснить стрессовым (внутриутробная гипоксия, морфофункциональная незрелость, мышечная дистония, нервно-рефлекторная возбудимость) воздействием на эпителий кишечника. При стрессе происходят переключение метаболизма колоноцитов с цикла Кребса на анаэробный вариант гликолиза, активация гексозомонофосфатного шунтирования. Такое изменение стратегии метаболизма приводит к тому, что меняется трофическая база колоноцитов, которые перестают всасывать и утилизировать КЖК в первую очередь пропионовую и масляную кислоты. Кроме того, известно, что пропионовая кислота оказывает влияние на абсорбцию воды в кишечнике через циклические аденозинмонофосфатзависимые системы, что также может стать одним из механизмов развития диареи.
На кафедре педиатрии ГБОУ ДПО РМАПО Минздрава России проанализирован спектр КЖК у детей с кишечными коликами в зависимости от характера вскармливания и степени нарушения микробиоценоза [28]. Абсолютное содержание КЖК продемонстрировало повышение их концентрации по мере усиления степени нарушений микробиоценоза кишечника, что было связано с количественным и качественным изменением состава микроорганизмов, среды их обитания и нарушениями моторики. Анализ профилей КЖК указывал на резкое снижение доли уксусной кислоты, повышение долей пропионовой и масляной кислот, отклонение значений анаэробных индексов, отражающих окислительно-восстановительный потенциал внутрипросветной среды в область резко отрицательных значений по сравнению с нормой по мере усугубления нарушений микробиоценоза.
Известно, что уксусная кислота является метаболитом облигатной, сахаролитической микрофлоры, и снижение ее доли свидетельствует об уменьшении активности и численности молочнокислых микроорганизмов (бифидо- и лактобактерий). Увеличение доли пропионовой и масляной кислот указывает на активизацию условно-патогенная микрофлора и строгих анаэробов (бактероидов, эубактерий, фузобактерий, копрококков и др.). При изучении корреляции между степенью нарушения микробиоценоза кишечника и уровнем уксусная кислота в кале у детей установлено, что коэффициент корреляции при грудном вскармливании составил r=0,922 и r=0,707 при искусственном вскармливании. Соответственно, изменение параметров КЖК отражает характер и выраженность изменения качественного состава микрофлоры и может быть использовано для скрининговой оценки ее состояния [30].
Таким образом, формируется порочный круг: изменения моторики кишечника приводят к формированию и усугублению изменений качественного состава микроорганизмов, а это в свою очередь посредством изменения продукции КЖК и других метаболитов усугубляет и поддерживает нарушения моторно-эвакуаторной функции кишечника.
У детей грудного возраста с функциональными нарушениями ЖКТ имеют место незрелость пищеварительной системы, относительная внешнесекреторная недостаточность поджелудочной железы, нарушения желчеобразования и желчеотделения. При этом нарушается переваривание белков и жиров. Недостаточное эмульгирование жиров в случае дефицита желчных кислот в дуоденальном просвете дополнительно ухудшает их расщепление. Измененная функция поджелудочной железы, сопровождающаяся дефицитом или снижением активности панкреатических ферментов, а также недостаточная активность лактазы в тонкой кишке приводят к накоплению неутилизируемых пищеварительных субстратов, что способствует развитию гниения и брожения и стимулирует пролиферацию в ней бактериальной флоры, за счет которой происходит расщепление нутриентов. Результатом этого является нарушение микробиоценоза толстой кишки, скопление в ней газов (сероводорода, углекислого газа, водорода и др.), продуктов расщепления недостаточно гидролизированных нутриентов. С другой стороны, продукты бактериального расщепления недостаточно гидролизированных нутриентов (КЖК, индол, скатол, фенол, газы и т.д.) и эндотоксины бактерий усиливают перистальтику тонкой и толстой кишки, что приводит к ускорению пассажа химуса, уменьшению времени контакта панкреатических ферментов с нутриентами в сфере полостного и мембранного пищеварения.
У многих детей грудного возраста кишечные колики сопровождаются диареей, обусловленной непереносимостью пищевых продуктов или компонентов (чаще лактозы). Расщепление дисахаридов происходит под воздействием ферментов дисахаридаз, которые вырабатываются в щеточной каемке тонкой кишки. Дисахаридазы синтезируются в полисомах кишечных ворсинок, являются мембранными гликопротеинами, расположенными поверхностно, в микроворсинках. Каждая дисахаридаза имеет гидрофобный участок, служащий мембранной основой, и интралюминальный гидрофильный участок, являющийся активной частью. Дисахаридазы делятся на два класса: b-гликозидаза (лактаза) и a-гликозидаза (сахараза-изомальтаза, мальтодекстрин-коамилаза, трегалаза). Микроворсинки энтероцитов содержат ферменты, расщепляющие олиго- и дисахариды до моносахаридов, которые абсорбируются. В норме до толстой кишки доходит лишь небольшое количество непереваренных углеводов. Избыточное поступление лактозы в толстую кишку вызывает скопление газов при ферментации, метеоризм, вздутие живота и болевой синдром. Необходимо отметить, что субъективные ощущения абдоминальной боли зависят от индивидуальной чувствительности к растяжению кишки газами.
Лактазная недостаточность может быть первичной, когда снижение активности фермента происходит при «сохранном» энтероците, и вторичной, обусловленной его повреждением. Существует целый ряд факторов, оказывающих влияние на активность лактазы: генетические, срок гестации, возраст ребенка, состояние вегетативной нервной системы, гормональные, белковые факторы роста, ускоряющие деление и созревание энтероцитов, полостные факторы, оказывающие трофическое действие на энтероцит (биогенные амины, КЖК, нуклеотиды, отдельные аминокислоты). К причинам, приводящим к повреждению энтероцита, относятся гипоксия, инфекционные, токсические, аллергические и некоторые другие.
У детей первых месяцев жизни частичная лактазная недостаточность нередко вызвана одновременно сниженной активностью фермента в силу незрелости ребенка и поражением энтероцита на фоне перенесенной гипоксии. На кафедре педиатрии ГБОУ ДПО РМАПО Минздрава России [28] изучен уровень экскреции углеводов в зависимости от интенсивности кишечных колик при грудном и искусственном вскармливании. С этой целью выраженность синдрома кишечных колик была оценена по 3-балльной системе (табл. 3).
|
Таблица 3. Оценка интенсивности кишечных колик в баллах |
|
|
Балл |
Особенности кишечных колик |
|
1 |
Только в вечернее время |
|
2 |
Возникают после каждого кормления и в ночное время |
|
3 |
Беспокоят в течение всех суток |
У детей на грудном вскармливании интенсивность кишечных колик оказалась прямо пропорциональной уровню общей экскреции углеводов с калом (1 балл - 0,54±0,09г/%; 2 балла - 0,58±0,08 г/%, 3 балла - 0,606±0,25 г/%); р<0,001. Однако экскреция лактозы была достоверно повышена лишь при интенсивности кишечных колик, оцененной в 1 балл (0,233±0,04 г/%); р=0,002. При интенсивности кишечных колик, равной 2 и 3 баллам, увеличение уровня лактозы не имело статистической значимости. Эти данные еще раз подтверждают отсутствие четкого параллелизма между степенью выраженности клинических симптомов и уровнем экскреции лактозы. Наиболее значительная экскреция глюкозы и галактозы зарегистрирована при 2-й степени интенсивности кишечных колик, а выделение ксилозы увеличивалась от 1 к 3 баллам (табл. 4).
|
Таблица 4. Экскреция углеводов с калом в зависимости от выраженности кишечных колик у детей, находящихся на грудном вскармливании |
|||||
|
Интенсивность колик |
Общие углеводы |
Лактоза |
Глюкоза |
Галактоза |
Ксилоза |
|
Норма, баллы |
0,15±0,02 |
0,07±0,02 |
0,05±0,02 |
0 |
0 |
|
1 (n=19) |
0,54±0,09* |
0,233±0,04* |
0,043±0,02 |
0,037±0,01* |
0,15±0,05* |
|
2 (n=13) |
0,586±0,08* |
0,093±0,04* |
0,118±0,03** |
0,092±0,03* |
0,217±0,10* |
|
3 (n=8) |
0,606±0,25** |
0,17±0,05* ** |
0,06±0,04* ** |
0,04±0,03** |
0,28±0,21* |
|
*р<0,05 - показатель, достоверный по сравнению с нормой; **р<0,05 - показатель, достоверный между степенью выраженности колик. |
|||||
На фоне искусственного вскармливания общая экскреция углеводов с калом также повышалась по мере увеличения степени интенсивности кишечных колик, достигая при их выраженности 3 балла - 0,473±0,25г/% (табл. 5).
Таблица 5. Экскреция углеводов в зависимости от выраженности кишечных колик при искусственном вскармливании | |||||
Интенсивность колик | Общие углеводы | Лактоза | Глюкоза | Галактоза | Ксилоза |
Норма, баллы | 0,15±0,02 | 0,07±0,02 | 0,05±0,02 | 0 | 0 |
1 (n=12) | 0,25±0,07* | 0,11±0,04 | 0,025±0,007 | 0,016±0,01* | 0,064±0,04 |
2 (n=13) | 0,470±0,05** | 0,076±0,05 | 0,192±0,10 | 0,134±0,05** | 0,042±0,03 |
3 (n=4) | 0,473±0,25 | 0,383±0,26 | 0,01±0,01 | 0* | 0,125±0,12 |
*р<0,05 - показатель достоверности между исследуемыми группами;**р<0,05 - показатель достоверности по сравнению с нормой. | |||||
При этом отмечено и существенное повышение выделения лактозы (0,383±0,26 г/%). В то же время при кишечных коликах, оцененных в 2 балла, экскреция лактозы была нормальной, а выделение глюкозы не имело отклонений при 1 - и 3-й степени выраженности кишечных колик.
В настоящее время обсуждается роль аллергии к белкам коровьего молока в возникновении кишечных колик, которые могут одинаково часто возникать у детей как на грудном, так и искусственном вскармливании. Их развитие чаще всего связывают с аллергенами коровьего молока - бычьим сывороточным иммуноглобулином (Ig) G и b-лактоглобулином, присутствующими в грудном молоке [32]. Непереносимость белков коровьего молока может реализовываться по иммунному и неиммунному пути. В первом случае возникновение кишечных колик связано с повреждением слизистой кишечника путем развития иммунологических реакций (см. рисунок).
Патогенез пищевой аллергии.
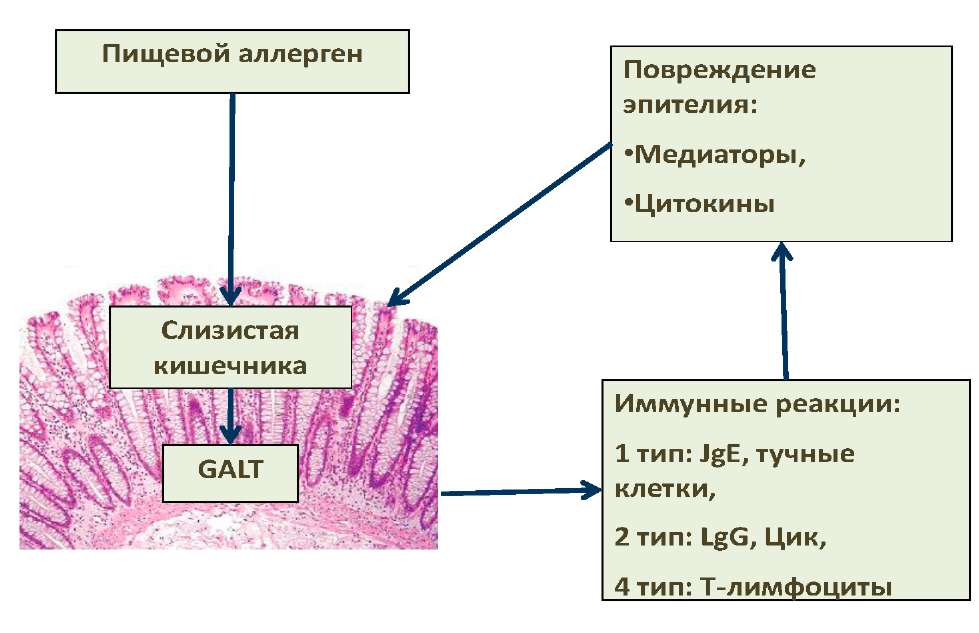
Возникает аллергическое воспаление, нарушается процесс переваривания и всасывания веществ, что приводит к увеличению газообразования, появлению слизи в стуле.
Развитию сенсибилизации может способствовать повышенная проницаемость кишечной стенки, выявляемая у детей с кишечными коликами [16].
Клинический случай
Девочка 1,5 мес, родилась от молодой женщины, страдающей бронхиальной астмой и хроническим гастритом. Беременность протекала на фоне незначительного токсикоза в I триместре. Роды в срок, самостоятельные. Масса тела 3750, рост 51 см. Приложена к груди после родов, на грудном вскармливании до 2 нед жизни, далее на смешанном вскармливании (грудное молоко и кисломолочная смесь в соотношении 1:1).
Жалобы на отсутствие самостоятельного стула с 2-недельного возраста (стул после газоотводной трубки), водянистый со слизью, выраженные кишечные колики в течение дня вне зависимости от кормления. За 1 -й месяц прибавила 1,2 кг. При осмотре: мелкоточечные единичные высыпания на лице, сухость кожи наружной поверхности предплечий и голеней. Живот вздут, урчит.
В копрограмме - умеренная стеаторея 1 -, 2-го типов, много слизи, лейкоциты 8-10 в поле зрения. Углеводы кала 1,8 мг%. Микробиологическое исследование кала: кишечная палочка со слабовыраженными ферментативными свойствами 65%, лактобактерии 105.
Педиатром поликлиники назначена коррекция питания: грудное молоко и безлактозная смесь, панкреатические ферменты. На фоне терапии состояние ребенка улучшилось незначительно, колики продолжали беспокоить в течение дня. Стул самостоятельный 3-4 раза в день, жидкий со слизью. Ребенка посмотрел другой специалист и обратил внимание на наличие обилия слизи в фекалиях, проявления атопического дерматита. Матери рекомендованы соблюдение строгой безмолочной диеты с полным исключением всех молочных продуктов и докорм смесью на основе гидролиза казеина. Через 2 нед кишечные колики полностью купированы. Стул стал кашицеобразный 3-4 раза в день, желтого цвета, слизь в незначительном количестве.
Колики часто зависят от особенностей темперамента ребенка. Однако особенности темперамента не всегда могут объяснить большинство стойких беспокойств ребенка. Существует мнение, что колики являются результатом неблагоприятного климата в семье, созданного неопытными и тревожными родителями. Нарушается взаимодействие в системе родитель-ребенок, которое имеет растущий интерес в возникновении выраженного беспокойства ребенка. На депрессивный и раздражительный настрой родителей малыш реагирует беспокойством, что в свою очередь усиливает стрессовую ситуацию для родителей. Таким образом, возникает порочный круг.
Особенное влияние оказывает негативный эмоциональный настрой матери ребенка, особенно в послеродовый период. Так, при обследовании 1015 матерей и их детей T.Vik и соавт. (2009 г.) показали, что младенческие кишечные колики и длительность беспокойства ребенка связаны с уровнем материнской депрессии. Так, наличие колик у ребенка в 2-месячном возрасте способствует к 4-месячному возрасту развитию высокого уровня депрессии у матери [33].
Курение матери во время беременности, а также после родов увеличивает риск возникновения колик у ребенка. Проведенные исследования показали, что ассоциация курения с кишечными коликами связана с повышением концентрации мотилина в плазме крови курильщика. Высокая концентрация мотилина обусловливает нарушение регуляции ЖКТ, приводящее к развитию колик [34].
Имеются данные о том, что социальный статус, образование, работа матери также оказывают влияние на частоту младенческих кишечных колик. Показано, что риск развития кишечных колик у младенцев повышается, если мать во время беременности испытывала гиподинамию и занималась умственным трудом, что связано с развитием гипоксии плода с последующей незрелостью систем ребенка [35, 36].
Имеют значение особенности нервной системы и темперамент ребенка. Проведенное 4-летнее наблюдение за детьми, имевшими в раннем возрасте кишечные колики, показало большую эмоциональную лабильность наблюдаемой группы детей по сравнению с ровесниками. У детей старшего возраста кишечные колики могут трансформироваться в функциональную абдоминальную боль, синдром раздраженного кишечника [37].
Знание патогенеза младенческих кишечных колик является важным для их дальнейшего лечения. В настоящее время лечение колик связано в большей степени с воздействием на предрасполагающие факторы и причины их возникновения. Перечень лекарственных препаратов, применяемых при младенческих кишечных коликах, минимален, к ним относится Саб Симплекс, содержащий действующее вещество симетикон. Растяжение или спазм любого участка пищеварительного тракта в связи с повышенным газообразованием у младенца приводит к болезненным ощущениям и дискомфорту. Симетикон снижает поверхностное натяжение на границе раздела фаз, затрудняет образование и способствует разрушению газовых пузырьков в кишечном содержимом. Высвобождаемые при этом газы могут поглощаться стенками кишечника или выводиться благодаря перистальтике.
Вследствие физической и химической инертности Саб Симплекс не всасывается и выводится в неизмененном виде после прохождения через желудочно-кишечный тракт. Препарат удаляет пену физическим путем, не вступая в химические реакции. Именно поэтому препарат безопасен и разрешен к применению с первых дней жизни младенца. В табл. 6 представлена сравнительная характеристика препаратов, применяемых для снижения газообразования в кишечнике у младенцев.
|
Таблица 6. Сравнительная характеристика препаратов, применяемых при кишечных коликах у младенцев [38] |
||||
|
Препарат |
Действующее вещество |
Дозировка |
Применение с первых дней жизни |
Побочные эффекты, недостатки |
|
Саб Симплекс суспензия |
Симетикон |
1 флакон на 10 дней. Во флаконе - 50 доз. По 15 капель на прием. Коррекция объема кормления не требуется |
Применяется с рождения |
Аллергические реакции при индивидуальной непереносимости |
|
Эспумизан эмульсия 100 мл |
Симетикон |
1 флакон на 4 дня. Во флаконе -20 доз. Дозируется чайными ложками. Объем разовой дозы - 5 мл. Требуется коррекция объема кормления |
Применяется с рождения |
Аллергические реакции при индивидуальной непереносимости |
|
Эспумизан L 40 мг/мл, 30 мл во флаконе |
Симетикон |
1 флакон на 6 дней. Во флаконе - 30 доз. Доза 25 капель (1 мл) |
Применяется с рождения |
Аллергические реакции при индивидуальной непереносимости |
|
Боботик |
Симетикон |
Во флаконе - 30 мл, от 28-го дня жизни до 2 лет, назначают по 8 капель 4 раза в сутки |
Нельзя применять новорожденным и детям в возрасте до 1 мес |
Аллергические реакции при индивидуальной непереносимости |
|
Плантекс |
Фенхеля плодов экстракт водный сухой, эфирное масло фенхеля, акации камедь |
Гранулы для приготовления раствора для приема внутрь. Дневная доза - 100 мл, разовая -30 мл. Требуется коррекция объема кормления |
Рекомендуется использовать у детей с 2 нед жизни |
Аллергические реакции на входящие в состав препарата эфирные масла. В состав препарата входят углеводы, которые вызывают брожение и усиливают газообразование. Для детей, находящихся на грудном вскармливании, можно использовать только свежеприготовленный раствор |
|
Бейби Калм (биологически активная добавка) |
Смесь эфирных масел на глицерине - укропное, мятное, анисовое |
Перед применением следует разбавить кипяченой водой до указанной на флаконе отметки, т.е. приготовить эмульсию. Детям до года по 10 капель перед каждым приемом пищи |
Отсутствуют данные о клинических исследованиях |
Аллергические реакции. В состав препарата входит глицерин, который может вызвать диарею |
20-летний мировой опыт применения показал эффективность и безопасность Саб Симплекса. Кроме того, препарат удобен в применении (флакон с дозатором - капельницей), экономичен (флакона хватает на 10 дней применения). Саб Симплекс имеет приятный малиновый вкус, который нравится детям и обеспечивает легкость приема препарата даже самыми маленькими пациентами. Благодаря своим свойствам, безопасности и удобству в применении симетикон может назначаться детям с первых дней жизни для купирования колик, что значительно облегчит задачу их успешной коррекции. Препарат не содержит углеводов, поэтому может применяться в том числе у больных сахарным диабетом. Одним из показателей безопасности Саб Симплекса может служить то, что его прием разрешен женщинам во время беременности и кормления грудью.
Таким образом, анализ существующих научных данных убедительно демонстрирует, что патогенез младенческих кишечных колик продолжает оставаться предметом дискуссий и исследований. В то же время понимание комплекса механизмов развития функциональных нарушений является залогом для их эффективного лечения.
Литература
1. Хавкин А.И., Эйберман А.С. Проект рабочего протокола диагностики и лечения функциональных заболеваний органов пищеварения. М., 2004.
2. Hyman PE, Milla PJ, Bennig MA et al. Childhood functional gastrointestinal disorders: neonate/toddler. Am J Gastroenterol 2006; 130 (5): 1519-26.
3. Savino F et al. A prospective 10-year study on children who had severe infantile colic. Acta Paediatr Suppl 2005; 94 (449): 129-32.
4. Самсыгина Г.А. Алгоритм лечения детских кишечных колик. Cons. Med. Педиатрия. 2009; 3: 55-67.
5. Paradise JL. Maternal and other factors in the etiology of infantile colic. JAMA 1996; 197:123-31.
6. Douwes AC, Oosterkamp RF, Fernandes J et al. Sugar malabsorption in healthy neonates estimated by breath hydrogen. Arch Dis Child 1980; 55: 512-5.
7. Brazelton TB. Crying in infancy. Pediatrics 1960; 26: 579-88.
8. Brazelton T.B. Crying in infancy. Pediatrics 1962; 29: 579-88.
9. Stahlberg M-R Infantile colic: occurrence and risk factors. Eur J Pediatr 1984; 143: 108-11.
10. Crocroft NS, Strachan DP. The social origins of infantile colic: questionnaire study covering76747 infants. BMJ 1997; 314: 1325-8.
11. Rautava P, Helenius H, Lehtonen L. Psychological predisposing factors for infantile colic.BMJ 1993; 307: 600-4.
12. Lust KD, Brown JE, Thomas W. Maternal intake of cruciferous vegetables and other foods and colic symptoms in exclusively breast-fed infants. J Am Diet Assoc 1996;96: 46-9.
13. Kurtoglu S, Uzam K, Hallac JK, Coscum A. 5 hydroxy-3-indole acetic acid levels in infantile colic: is serotoninergic tonus responsible for this problem? Acta Pediatr 1997; 86: 764-5.
14. Lothe L, Ivarsson S-A, Ekman R, Lindberg T. Motilin and infantile colic. Acta PaediatrScand 1990; 79: 410-6.
15. Matheson L. Infantile colic-what will help? Tidsskr Nor Laegeforen 1995; 115 (19): 2386-9.
16. Lothe L, Lindberg, T, Jacobsson I. Macromolecular adsorption in infants with infantile colic.Acta Paediatr 1990; 79: 417-21.
17. Rhoads JM, Fatheree NJ, Norori J. Alteredfecal microflora and increased fecal calprotectin in infant colic. J Pediatr 2009; 155 (6): 823-8.
18. Savino F, Bailo
E, Oggero R et al. Bacterial counts of intestinal Lactobacillus species in infants with colic. Pediatr Allergy Immunol 2005; 16 (1): 72-5.
19. Захарова И.Н., Сугян Н.Г., Андрюхина Е.Н., Дмитриева. Ю.А. Тактика педиатра примладенческих кишечных коликах. Рус. мед. журн. 2010; 18 (1): 11-5.
20. Захарова И.Н., Сугян Н.Г. Кишечные младенческие колики и их коррекция. Cons. Med. Украина. 2008; 2 (7): 38-41.
21. Lot L, Ivarsson, Lindberg T. Motilin, vasoactive intestinal peptide and gastrin in infantile colic. Acta Paediatr Scand 1987; 76: 316-20.
22. Savino F, Grassino EC, Guidi C et al. Ghrelin and motilin concentration in colicky infants.Acta Paediatr 2006; 95: 738-41.
23. Захарова И.Н., Еремеева А.В. Кишечные младенческие колики их коррекция. Cons. Med.Педиатрия. 2009; 1: 43-4.
24. Lust KD, Brown JE, Thomas W. Maternal intake of cruciferous vegetables and other foods and colic symptoms in exclusively breast-fed infants. J Am Diet Assoc 1996; 96: 46-9.
25. Запруднов А.М., Мазанкова Л.Н. Микробная флора кишечника и пробиотики. Педиатрия (Прил.). 1999.
26. Scheiwiller J, Arrigoni E, Brouns F. Human fecal microbiota develops the ability to degrade type 3 resistant starch during weaning. JPed Gastroenterol Nutr 2006; 43: 584-91.
27. Savino F, Cordisco L, Tarasco V et al. Molecular identification of coliform bacteria from colicky breastfed infants. Acta Paediatr 2009; 98 (10): 1582-8.
28. Сугян Н.Г. Клиническое значение короткоцепочечных жирных кислот при функциональных нарушениях желудочно-кишечного тракта у детей раннего возраста. Автореф. дис. ... канд. мед. наук. М., 2010.
29. Cherbut C, Aube AC, Blottiere HM, Galmiche JP. Effects of short-chain fatty acids on gastrointestinal motility. Scand J Gastroenterol 1997; 32 (Suppl. 222): 58-61.
30. Ардатская М.Д. Исследование содержания и профиля низкомолекулярных метаболитов сахаролитической толстокишечной микрофлоры в норме и патологии. Автореферат дис. ... канд. мед. наук. М., 1996.
31. Дубинин А.В., Бабин В.Н., Раевский П.М. Трофические, регуляторные связи кишечной микрофлоры и макроорганизма. Клин. медицина. 1991; 7: 24-8.
32. Clyne PS, Kulczycki A. Human breast milk contains bovine IgG. Relationship to infant colic?Pediatrics 1991; 87: 439-44.
33. Vik T, Grote V, Escribano J et al. European Childhood Obesity Trial Study Group. Infantile colic, prolonged crying and maternal postnatal depression. Acta Paediatr 2009; 98 (8): 1344-8.
34. Shenassa ED, Brown M-J. Maternal Smoking and Infantile Gastrointestinal Dysregulation:The Case of Colic. Pediatrics 2004; 114 (4): e497-e505.
35. Хавкин А.И. Младенческие кишечные колики. Педиатрия. 2007; 2: 105-7.
36. Canivet C, Ostergren PO, Jakobsson I, Hagander B. Higher risk of colic in infants of nonmanual employee mothers with a demanding work situation in pregnancy. Int J Behav Med2004; 11 (1): 37-47.
37. Canivet C. Infantile colic. Follow-up at four years of age: still more «emotional». ActaPaediatr 2000; 89: 13-7.
38. Регистр Лекарственных Средств России. РЛС - 2013.21 (Электронная Энциклопедия Лекарств). РЛС-Патент.
