Рак печени и желчных путей: Обсуждение
СтатьиNCCN® Практические рекомендации в онкологии
Предыдущий раздел | Содержание | Список литературы
Обсуждение
Категории доказательности и согласия NCCN
Категория 1: рекомендация основана на доказательствах высокого уровня (например, результатах рандомизированных контролируемых исследований) и единодушном согласии NCCN.
Категория 2А: рекомендация основана на доказательствах невысокого уровня и единодушном согласии NCCN.
Категория 2В: рекомендация основана на доказательствах невысокого уровня и неединодушном согласии NCCN (без значительных разногласий).
Категория 3: рекомендация основана на доказательствах любого уровня, но принята со значительными разногласиями NCCN.
Все рекомендации основаны на категории доказательности 2А, за исключением особо оговоренных.
Обзор
Рак гепатобилиарной системы отличается высокой летальностью. По прогнозам специалистов, в США в течение 2010 г. предполагалось выявить рак печени либо внутрипеченочных желчных протоков у 24 120 человек, рак желчного пузыря либо внепеченочных желчных протоков - у 9760 человек. Также ожидалось, что за этот год от рака печени или внутрипеченочных желчных протоков умрет 18 910 больных, от рака желчного пузыря либо внепеченочных желчных протоков - 3320 больных.1
Представленные здесь клинические рекомендации по диагностике и лечению рака печени и желчных путей разработаны специальной рабочей группой NCCN. В данные рекомендации включены следующие виды рака гепатобилиарной системы: гепатоцеллюлярный рак (ГЦР), рак желчного пузыря, внутрипеченочная холангиокарцинома, внепеченочная холангиокарцинома. По существу, рекомендации NCCN не могут включить в себя все возможные клинические варианты и не заменяют необходимости критического клинического анализа или индивидуализации лечения.
Наиболее предпочтительный вариант лечения рака гепатобилиарной системы - участие в проспективных клинических исследованиях, хотя это четко не обозначено на каждом этапе принятия решений предлагаемых рекомендаций.
Гепатоцеллюлярный рак
Факторы риска и эпидемиология
К факторам риска ГЦР - наиболее частой злокачественной опухоли гепатобилиарной системы - относятся вирусный гепатит В и / или С, некоторые хронические заболевания или состояния и определенные внешние факторы.2 Например, хронический гепатит В - основная причина ГЦР в Азии и Африке, а гепатит С - в Европе, Японии и Северной Америке.3,4 Ретроспективный анализ данных в центрах трансплантации печени в США показал, что вирусом гепатита С было инфицировано 50 % больных, вирусом гепатита В - 15 %, при этом примерно у 5 % больных выявлены маркеры обоих вирусных гепатитов.5 С повышенным риском ГЦР связаны также относительно редко встречающиеся врожденные нарушения метаболизма (наследственный гемохроматоз, хроническая гематопорфирия, дефицит α1-антитрипсина и болезнь Вильсона-Коновалова), аутоиммунный гепатит и первичный билиарный цирроз.2,6 В настоящее время растет число доказательств связи ГЦР с последствиями неалкогольной жировой дистрофии печени, например неалкогольного стеатогепатита (т. е. спектра состояний, гистологически характеризующихся воспалением и стеатозом печени у лиц, не злоупотребляющих алкоголем), на фоне метаболического синдрома или сахарного диабета.7,8 Известно, что факторами риска ГЦР служат чрезмерное потребление алкоголя и воздействие афлатоксина (естественного продукта жизнедеятельности грибов рода Aspergillus, обнаруживаемых в различных зерновых).2,4,9,10
В большинстве случаев факторы риска ГЦР совпадают с факторами риска цирроза печени. Установлено, что цирроз печени наблюдается у 60–80% больных ГЦР,9 причем в США этот показатель, возможно, приближается к 90%.11
В большинстве исследований, посвященных оценке риска развития ГЦР у лиц, инфицированных вирусом гепатита С, основное внимание уделяется больным с циррозом. Следует отметить, что отдельные немногочисленные данные свидетельствуют о том, что ГЦР может развиваться у некоторых пациентов, инфицированных вирусом гепатита С, с мостовидным фиброзом печени при отсутствии явного цирроза.11 При этом в некоторых популяциях больных хроническим гепатитом В (т. е. у носителей вируса) установлен повышенный риск ГЦР при отсутствии цирроза, особенно при наличии других факторов риска.4 По ориентировочным данным, у 30–50% больных хроническим гепатитом В, у которых развился ГЦР, цирроза не было.10 Среди прочих, к факторам риска развития ГЦР у носителей вируса гепатита В без проявлений цирроза печени относятся активная репликация вируса, высокий уровень ДНК вируса гепатита В, семейный анамнез ГЦР, мужчины азиатского происхождения >40 лет, женщины азиатского происхождения >50 лет, лица африканского происхождения >20 лет.4,13
Считается, что цирроз печени является предпосылкой для развития ГЦР у лиц с наследственными метаболическими заболеваниями печени или аутоиммунным поражением печени.14,15 Несмотря на то что механизмы развития ГЦР различаются в зависимости от сопутствующего заболевания,9 ГЦР обычно наблюдается у лиц с гистологическими изменениями в печени. Следовательно, любое хроническое заболевание печени представляет собой потенциальный риск развития ГЦР.2
В США отмечается рост заболеваемости ГЦР, особенно среди лиц, инфицированных вирусом гепатита С. Хронический гепатит С наблюдается примерно у 4 млн американцев,16 ежегодная заболеваемость ГЦР среди больных с циррозом печени, связанным с гепатитом С, составляет 2–8 %.4 Рост заболеваемости ГЦР, связанным с гепатитом С, несмотря на снижение в США числа случаев инфицирования вирусом гепатита С в год, можно объяснить продолжительным промежутком между инфицированием и развитием рака.16-20
В США примерно 1,5 млн человек больны хроническим гепатитом В.16-20 Результаты проспективного контролируемого исследования показали, что ежегодная заболеваемость ГЦР у носителей вируса без цирроза печени составляет 0,5 %, с циррозом печени - 2,5 %.21 При этом отмечена широкая вариабельность заболеваемости ГЦР среди больных хроническим гепатитом В.4
По оценкам специалистов, распространенность неалкогольного стеатогепатита в США составляет около 3–5%, а это немалая субпопуляция с риском цирроза и ГЦР.22 В одном исследовании с медианой наблюдения 3,2 г. ГЦР развился у 12,8% из 195 больных с циррозом, связанным с неалкогольным стеатогепатитом; ежегодная заболеваемость ГЦР составила 2,6%.23 Следует сказать, что результаты нескольких исследований показали, что вероятность развития ГЦР у больных циррозом, связанным с неалкогольным стеатогепатитом, несколько ниже, чем у больных с циррозом, обусловленным гепатитом С.24,25
Ежегодная заболеваемость ГЦР, связанным с определенными состояниями (например, наследственным гемохроматозом) или воздействием алкоголя, точно неизвестна. В первом случае это обусловлено редкостью заболевания. Во втором - на анализ заболеваемости ГЦР среди лиц с алкогольным циррозом печени влияют другие факторы риска (например, вирусный гепатит), также способствующие развитию ГЦР.26,27
Скрининг ГЦР
Задача скринингового метода диагностики рака - выявить опухоль при отсутствии у больного каких-либо клинических проявлений, когда ее своевременное обнаружение служит залогом успешного лечения. Рабочая группа поддерживает рекомендацию Американской ассоциации по изучению болезней печени (AASLD), согласно которой скрининг должен «проводиться в рамках программы или процесса, при котором исследования и повторные процедуры стандартизованы и работают процедуры контроля качества».4
Рекомендация включения лиц с высоким риском ГЦР в программу скрининга основана на результатах крупного рандомизированного контролируемого исследования, проведенного в Китае с участием 18816 больных гепатитом В или с хроническим гепатитом в анамнезе. В данном исследовании скрининг был основан на определении уровня α-фетопротеина (АФП) сыворотки и ультразвуковом исследовании (УЗИ) каждые 6 мес. В результате установлено снижение смертности от ГЦР на 37%, несмотря на то что программу исследования выполнило менее 60% участников из группы скрининга.27 Недавно в Сингапуре было завершено проспективное исследование, проходившее в течение 9 лет. В нем участвовало 638 больных ГЦР. Установлено, что вероятность носительства вируса гепатита В и выявления болезни на более поздней стадии была выше у больных в возрасте до 40 лет включительно.29 Несмотря на то что в обеих группах выживаемость не различалась, показано статистически значимое увеличение выживаемости в подгруппе больных с ранней стадией рака. Эти результаты свидетельствуют о нецелесообразности отказа от скрининга ГЦР у лиц молодого возраста.
Измерение уровня АФП и УЗИ печени - наиболее широко применяемые методы обследования с целью раннего выявления ГЦР.30 В Китае выполнено исследование с применением скрининговых методов диагностики, в котором участвовала большая популяция лиц, инфицированных вирусом гепатита В, либо больных хроническим гепатитом. Процент выявления рака, доля ложноположительных результатов и прогностичность положительного результата для УЗИ составили соответственно 84, 2,9 и 6,6%; для определения АФП - 69, 5 и 3,3%; для комбинации АФП и УЗИ - 92, 7,5 и 3%.31 Полученные данные свидетельствуют о том, что в качестве метода скрининга УЗИ лучше, чем АФП. Тем не менее, учитывая высокую субъективность УЗИ, добавление к нему анализа на АФП позволяет повысить вероятность выявления ГЦР в условиях скрининга. Следует сказать, что эффективность использования АФП в качестве скринингового биомаркера низкая (например, на ранней стадии заболевания часто отмечается нормальный уровень АФП).32-34
В разделе ГЦР-1 настоящих рекомендаций определены популяции с повышенным риском заболевания ГЦР, которым участие в программе скрининга ГЦР, скорее всего, будет полезным (см. раздел «Факторы риска и эпидемиология»).
Лицам с повышенным риском ГЦР рабочая группа рекомендует проходить периодический скрининг с применением УЗИ и определением АФП каждые 6–12 мес. (см. ГЦР-1). В случае повышенного уровня АФП сыворотки либо для дальнейшей диагностики при выявлении во время УЗИ объемного образования рекомендуется применить дополнительные методы визуализации (например, КТ с использованием контрастного средства; ПЭТ/КТ не подходит) (см. разд. «Диагностика и первичное обследование»).
Диагностика и первичное обследование
Естественное развитие ГЦР характеризуется длительным отсутствием какой-либо клинической симптоматики. К неспецифическим симптомам относятся желтуха, анорексия, снижение массы тела, недомогание, боль в верхней части живота; к физикальным симптомам - гепатомегалия и асцит.8 Также могут развиваться паранеопластические синдромы: гиперхолестеринемия, полицитемия, гиперкальциемия и гипогликемия.9
Диагностика
Методы визуализации
Рекомендации по применению дополнительных методов визуализации в случае высокой степени клинического подозрения на ГЦР (например, когда при УЗИ в печени выявляют узел либо повышен уровень АФП в сыворотке) приведены из руководства, разработанного AASLD (см. ГЦР-2).4 Очаги ГЦР характеризуются гиперваскуляризацией, что обеспечивает поступление в опухоль крови преимущественно из печеночной артерии, в отличие от окружающей ткани печени, которая кровоснабжается в основном из воротной вены.35 С целью диагностики ГЦР применяют один или несколько методов визуализации: трехфазную спиральную компьютерную томографию (КТ), трехфазную динамическую магнитно-резонансную томографию (МРТ) с использованием контрастного средства либо УЗИ с использованием контрастного средства. Последний вариант в США не получил широкого распространения.4,36,37 Термин «трехфазный» отражает три фазы сканирования: артериальную, фазу воротной вены и отсроченную венозную фазу.11 Классическая картина ГЦР характеризуется интенсивным артериальным поглощением либо усилением с последующим вымыванием контрастного средства или снижением интенсивности в отсроченную венозную фазу.4,37,38
Если при УЗИ в печени выявлен узел, больного следует обследовать с применением одного или нескольких методов визуализации. Число и характер обследования зависят от размера опухолевого узла (см. ГЦР-2). Больных с узлами размером 1-2 см рекомендуется обследовать с помощью двух различных методов из перечисленных выше. Диагностическим для ГЦР считается совпадение результатов двух методов исследования с выявлением классического артериального усиления. Если классическая картина усиления не наблюдается либо определяется только одним из методов исследования, рекомендуется провести биопсию. Результаты недавно завершенного проспективного исследования с применением УЗИ с использованием контрастного средства и МРТ с биопсийной верификацией подтвердили надежность этой диагностической тактики. В исследовании участвовали больные, у которых при УЗИ во время скрининга был обнаружен хорошо заметный одиночный солидный узел диаметром 0,5-2,0 см.39 Если размер опухоли превышает 2 см, для установления диагноза ГЦР достаточно выявить классическое артериальное усиление одним методом исследования. Наконец, при обнаружении образований менее 1 см рекомендуется повторное обследование с применением трехфазной КТ или МРТ либо УЗИ с использованием контрастного средства каждые 3-4 мес. По мере увеличения очагов выбирают методы исследования в соответствии с рекомендациями, указанными в разделе ГЦР-2. Если в течение 18 мес. узел в печени не увеличится, пациента обследуют каждые 6-12 мес.
Биопсия
Диагностика ГЦР может быть неинвазивной, поскольку не всегда для подтверждения диагноза требуется биопсия. Например, при наличии в печени узлов диаметром 1-2 см для постановки диагноза ГЦР достаточно выявить классическое артериальное усиление при использовании двух типов рекомендованных методов визуализации; если размер узла превышает 2 см, достаточно соответствующего определения одним методом (см. ГЦР-2). Тем не менее в некоторых случаях, когда диагноз ГЦР сомнителен, необходима биопсия - пункционная (методом тонкоигольной аспирации) либо трепанобиопсия. Например, она рекомендуется, если классическое артериальное усиление не подтверждается ни одним из методов визуализации либо (при наличии в печени узла диаметром 1-2 см) определяется только одним из выполненных методов. Следует отметить, что согласно результатам одного из недавно выполненных исследований с участием 64-х больных с циррозом печени, у которых появились новые узлы, в большинстве случаев диаметром 1-2 см, выявление классического артериального усиления с помощью одного метода визуализации оказалось достаточным для подтверждения диагноза ГЦР40 В этих условиях и трепанобиопсия, и пункционная биопсия обладают своими преимуществами и недостатками. Например, пункционная биопсия характеризуется меньшим числом осложнений при исследовании глубоких узлов либо узлов, расположенных рядом с крупными кровеносными сосудами. Кроме того, возможность быстро покрасить и исследовать цитологический материал позволяет сразу оценить его полноценность и поставить предварительный диагноз.41 В то же время эффективность пункционной биопсии очень сильно зависит от квалификации цитопатолога.42 В некоторых публикациях отмечается высокий уровень ложно-отрицательных,39,43 а также возможность ложно-положительных результатов.44 Трепанобиопсия - более инвазивная процедура, однако преимущество ее в том, что она позволяет исследовать не только цитологический материал, но и тканевое строение. Кроме того, образцы тканей, залитые в парафиновые блоки, можно дополнительно исследовать гистологически или иммуногистохимически.33,41,43 Следует отметить, что последние данные свидетельствуют о том, что трепанобиопсия не позволяет точно оценить степень злокачественности опухоли.45
Следует отметить, что возможности пункционной биопсии с целью диагностики ГЦР ограничивает ряд факторов, включая ошибку забора материала, особенно если размер узла равен 1-2 см.4,11 Если результат биопсии не имеет диагностической ценности, больного следует тщательно наблюдать. В случае изменения размера узла рекомендуются дополнительные методы визуализации и/или биопсия.
Сывороточные биомаркеры
Определение уровня АФП в сыворотке не относится к чувствительным или специфичным методам диагностики ГЦР.4,11 В связи с этим исследованы другие биомаркеры: дезгаммакарбоксипротромбин (ДКП), также известный как белок, индуцируемый отсутствием витамина К-II (PIVKA-II), и агглютинин-реактивный АФП чечевицы (АФП-ЬЭ) (изоформа АФП).11,46,47 Несмотря на большую чувствительность АФП по сравнению с ДКП или АФП-ЬЭ относительно выявления ранней и очень ранней стадии ГЦР, что было установлено в одном из недавно выполненных ретроспективных исследований по принципу «случай-контроль», ни один из данных биомаркеров в этом отношении не считается оптимальным. Результаты недавно выполненного исследования «случай-контроль» с участием больных с гепатитом C, включенных в крупное рандомизированное исследование HALT-C, у которых развился ГЦР показали, что комбинация АФП с ДКП как дополнительный метод скрининга превосходит любой из биомаркеров по отдельности.32
Результаты определения АФП в комплексе с другими методами исследования могут оказаться полезными для определения тактики ведения больного с подозрением на ГЦР. Например, больных с повышенным уровнем АФП сыворотки при отсутствии объемного образования в печени рекомендуется дополнительно обследовать с использованием методов визуализации (например, КТ/МРТ) (см. ГЦР-1). Если у больного с повышенным уровнем АФП опухоль в печени не выявлена, рекомендуется организовать наблюдение с более частым, например, каждые 3 мес., определением АФП и визуализацией печени. Согласно результатам 2 ретроспективных анализов небольшого числа больных,49,50 повышенный уровень АФП в сочетании с выявлением крупного образования в печени характеризуется высокой прогностичностью положительного результата относительно диагноза ГЦР хотя точность диагностики и абсолютный критический уровень АФП при этих условиях точно не определены, поэтому в различных учреждениях они могут отличаться. В соответствии с рекомендациями AASLD, уровень АФП выше 200 нг/мл либо классическое артериальное усиление при трехфазной КТ или МРТ считается подтверждением диагноза ГЦР, если размеры узлов в печени превышают 2 см (см. ГЦР-2). Следует отметить, что рабочая группа в этих условиях считает выявление классического усиления более доказательным, поскольку уровень АФП в сыворотке может повышаться у больных с некоторыми незлокачественными процессами, а также может сохраняться в нормальных пределах у значительной доли больных с ГЦР.51
Первичное обследование
Основа первичного обследования больного с диагнозом ГЦР - это комплексная оценка этиологии заболевания печени, включая определение маркеров гепатита В и/или С (см. ГЦР-3) и выявление сопутствующих заболеваний; применение методов визуализации с целью выявления метастазов; оценка функции печени, включая наличие портальной гипертензии.
Чаще всего метастазы ГЦР обнаруживают в легких, лимфоузлах брюшной полости и костях.52,53 Следовательно, при первичном обследовании рекомендуется выполнять визуализирующее исследование грудной клетки и сканирование костей (при наличии жалоб на боль в костях либо если больному предполагается пересадка печени). Трехфазная КТ или МРТ позволяют оценить опухолевую массу ГЦР, выявить метастазы, в т. ч. в лимфоузлах; установить прорастание опухоли в сосуды; оценить наличие портальной гипертензии; определить размер и локализацию ГЦР и степень поражения печени. Если предполагается выполнить резекцию, эти методы позволяют оценить отношение оставляемой части печени ко всему ее объему (см. разд. «Частичная гепатэктомия»).37
Оценку функции печени начинают с определения уровня билирубина сыворотки, активности аспартатаминотрансферазы, аланинаминотрансферазы, щелочной фосфатазы (ЩФ), протромбинового времени (ПВ)/международного нормализованного отношения (МНО), уровня альбумина и общего белка. Также рекомендуется исследовать функцию почек (т. е. азот мочевины крови и креатинин). Эти показатели применяют в качестве прогностических маркеров, если у больного имеется хроническое заболевание печени.54 Также определяют активность лактатдегидрогеназы (ЛДГ) и выполняют полный общий анализ крови (ОАК) (ГЦР-3).
Дальнейшую оценку функции печени или ее резерва у пациентов с хроническим заболеванием печени традиционно проводят с помощью шкалы Чайлда-Пью. В соответствии с этой шкалой выделяют три класса больных (А-С) в зависимости от вероятности выживаемости (см. ГЦР-А).55,56 Классификация Чайлда-Пью дает условную оценку функции печени, выделяя больных с компенсированным (класс А) или декомпенсированным (В и С) циррозом. Оценка по шкале Чайлда-Пью носит эмпирический характер и включает в себя лабораторные показатели (например, альбумин сыворотки, билирубин и ПВ), а также более субъективные клинические данные, касающиеся энцефалопатии и асцита. Недавно предложена версия шкалы Чайлда-Пью с использованием МНО (ГЦР-А). Преимущество шкалы Чайлда-Пью состоит в легкости ее применения (у постели больного) и использовании клинических показателей. Данная шкала не учитывает важные дополнительные показатели функции печени - проявления клинически значимой портальной гипертензии (варикозное расширение вен пищевода и желудка, спленомегалия, расширение подкожных вен живота, тромбоцитопения). Портальную гипертензию можно также установить с помощью КТ/МРТ.37 В настоящее время начинают применяться методики измерения градиента венозного давления печени с целью оценить степень портальной гипертензии.57-60
Другая система оценки функционального резерва печени - модель конечной стадии заболевания печени (MELD). Эта шкала предусматривает показатели от 6 (легкая форма болезни) до 40 (тяжелая форма) для лиц в возрасте 12 лет и старше. Баллы вычисляются по формуле, включающей три лабораторных показателя (билирубин сыворотки, креатинин и МНО). Изначально эта система была предназначена для оценки смертности больных, подвергающихся трансъюгулярному внутрипеченочному портосистемному шунтированию.61 Впоследствии шкалу MELD начала применять Служба обеспечения донорскими органами (UNOS) для стратификации пациентов, находящихся в списке ожидающих трансплантации, в соответствии с риском смерти в течение 3 мес.62 (см. разд. «Трансплантация печени»). В последнее время MELD иногда используют вместо шкалы Чайлда-Пью для оценки прогноза у больных с циррозом. К преимуществам шкалы MELD относятся учет показателей функции почек и получение объективной оценки, основанной на широко применяемых лабораторных показателях. При этом клиническая оценка асцита и энцефалопатии не учитывается. В настоящее время неизвестно, превосходит ли MELD шкалу Чайлда-Пью в качестве средства прогнозирования продолжительности жизни больных с циррозом печени. Шкала MELD не была утверждена в качестве средства прогнозирования продолжительности жизни больных с циррозом, не состоящих в списке ожидающих пересадки печени.56
Патоморфология и классификация по стадиям
Патоморфология
Макроскопически выделяют три морфологических типа ГЦР: узловой, массивный и диффузный.63-65 Узловой ГЦР, как правило, связан с циррозом и имеет вид узлов с четкими контурами. Массивный тип ГЦР, обычно развивающийся на фоне поражения печени без цирроза, занимает большой участок с или без сателлитных узлов. Диффузный тип встречается редко и характеризуется поражением в виде многочисленных мелких, слабо различимых опухолевых узелков, рассредоточенных по всей печени.
Классификация по стадиям
Клинические классификации рака по стадиям позволяют точнее давать прогноз до и после определенного лечения, ими можно пользоваться при выборе тактики лечения. Следовательно, от стадии рака зависит исход лечения. Таким образом, определение стадии облегчает отбор пациентов для определенного варианта терапии. Классификация по стадиям также позволяет выделить группы риска при последующем лечении.
На прогноз для больного ГЦР влияет четыре основных показателя: 1) стадия, агрессивность и активность роста опухоли; 2) общее состояние больного; 3) состояние функции печени; 4) назначенное лечение.36 Предложено несколько классификаций по стадиям ГЦР.66,67 В каждой из них учитываются показатели, основанные на оценке одного или нескольких из первых трех перечисленных выше факторов. Например, шкалы Чайлда-Пью55 и MELD68 можно рассматривать как классификации по стадиям, учитывающие только состояние функции печени. Классификация по системе TNM Американского объединенного комитета по онкологическим заболеваниям (AJCC) (см. табл. 1) учитывает только характеристики опухоли.69 Система Okuda учитывает функцию печени и характеристики опухоли.70 Французская классификация (GRETCH) использует шкалу Карновского для оценки общего состояния, а также показатели функции печени и АФП сыворотки.71 Несколько классификаций по стадиям учитывают все параметры из других систем и некоторые дополнительные. Например, прогностический индекс Китайского университета (CUPI)72 и Японская интегрированная шкала стадирования (JIS)73 используют систему TNM и классификацию Итальянской программы по борьбе с раком печени (CLIP).74 Системы Клиники Барселоны (BCLC),75 SLiDe76 и JIS включают в себя шкалу Чайлда-Пью (с измененными версиями CLIP и JIS, заменяя MELD на шкалу Чайлда-Пью).77-79 Кроме того, BCLC также использует систему Okuda, другие характеристики опухоли, показатели функции печени и общее состояние больного.4
Несмотря на то что некоторые классификации применимы для всех стадий ГЦР (например, BCLC), 4,11,68 у некоторых их них есть недостатки. Например, практическая значимость TNM-классификации AJCC невысока, поскольку большинство больных ГЦР не оперируются. Ряд исследований показал, что определенные классификации по стадиям хорошо подходят для особых групп пациентов. Более того, системы стадирования можно применять для выбора лечения и/или прогнозирования продолжительности жизни после выполненного лечения. Например, недавно было установлено, что TNM-классификация AJCC точно прогнозирует продолжительность жизни больных, подвергшихся ортотопической трансплантации печени.81 Классификации CLIP и GRETCH позволяют точно прогнозировать заболеваемость и смертность больных с поздней стадией рака.82 Отдельно установлено, что классификация CLIP служит ценным средством определения стадии заболевания у пациентов, которым выполнена трансартериальная химиоэмболизация,83 а также которые получали паллиативное лечение.84 Результаты метаанализа больных с ГЦР, не получавших лечение, включенных в рандомизированные клинические исследования, свидетельствуют о возможности применения классификации BCLC для разделения групп риска согласно естественному развитию заболевания. Преимущество системы BCLC также состоит в том, что с ее помощью можно разделить больных на группы лечения, хотя тип лечения не используется как фактор определения стадии.67 Более того, установлено, что система стадирования BCLC позволяет с высокой точностью прогнозировать исход заболевания после высокочастотной абляции.86 Недавно была разработана новая классификация по стадиям, основанная на номограмме особой клинико-патологической переменной, включавшей возраст больного, размер опухоли, состояние хирургических краев, степень послеоперационной кровопотери, наличие сателлитных очагов, инвазию сосудов, уровень АФП сыворотки. Эта классификация позволяет прогнозировать послеоперационный исход после резекции печени по поводу ГЦР87 Согласно результатам другого исследования, размер опухоли >2 см, многоочаговые опухоли, сосудистая инвазия служат независимым неблагоприятными прогностическими показателями продолжительности жизни больных с ранней стадией ГЦР после резекции или трансплантации печени.88 Данная система была ретроспективно подтверждена в популяции больных с ранним ГЦР.89
В настоящих рекомендациях нет указания на использование какой-либо одной классификации (за исключением шкалы Чайлда-Пью и TNM), однако после первичного обследования (ГЦР-3) пациента следует определить в одну из четырех категорий: 1) потенциально резектабельный рак или возможна трансплантация печени, операбельные больные по общему состоянию и сопутствующим заболеваниям; 2) нерезектабельный рак; 3) неоперабельные больные по общему состоянию или сопутствующим заболеваниям, без метастазов; 4) больные с метастазами. Выбор категории более подробно описан в ГЦР-4-ГЦР-6, ГЦР-В, ГЦР-С и в разд. «Лечение».
Лечение
Тактика лечения больного ГЦР должна быть тщательно взвешена. Напомним, что лечение ГЦР осложняется патологией печени, предшествовавшей раку. Не исключено, что на эффективность терапии влияет воздействие на печень реципиента различных этиологических факторов ГЦР90 В лечении больных ГЦР участвуют гепатологи, специалисты лучевой диагностики и терапии, трансплантологи, патоморфологи, онкологи (терапевты и хирурги), что обусловливает необходимость высокоэффективной координации медицинской помощи.101
Хирургическое лечение
Частичная гепатэктомия
Частичная гепатэктомия (т. е. резекция печени) - потенциально радикальный метод лечения больных с ранней стадией ГЦР, подходящих для этой процедуры.91,92 При правильном отборе пациентов частичная гепатэктомия по поводу ГЦР в настоящее время позволяет обеспечить низкий уровень послеоперационных осложнений и смертности (<5 %).93,94 Результаты крупных ретроспективных исследований показывают, что 5-летняя выживаемость после резекции печени по поводу ГЦР превышает 50%.94-96 Данные некоторых исследований говорят о том, что у больных, отобранных по определенным критериям, с сохранной функцией печени и ранней стадией ГЦР этот показатель достигает 70%.96-98 В то же время сообщается, что частота рецидивов ГЦР в течение 5 лет после резекции печени превышает 70%.4,95
Риски резекции печени у больных ГЦР обусловлены удалением функционально активной паренхимы органа на фоне основного заболевания печени. Поэтому крайне важно тщательно отбирать пациентов, исходя из состояния больного, печени и характеристик опухоли. Оценивают общее состояние пациента. Установлено, что наличие сопутствующих заболеваний служит независимым прогностическим фактором периоперационной смертности.99 Более того, перед тем как принять решение о резектабельности опухоли, необходимо оценить общее состояние функции печени; размер и функцию части, которую предполагается оставить; технические вопросы операции (см. ГЦР-4).
Резекция рекомендуется только при условии сохранения функции печени. Оценку функции печени можно получить с помощью шкалы Чайлда-Пью, хотя недавно высказано мнение о том, что эта шкала более эффективна как средство исключения пациентов из числа подходящих для резекции печени (т. е. служит средством выявления больных с существенно декомпенсированным поражением печени).100 Оценка наличия у больного значимой портальной гипертензии - также важная часть предоперационного обследования (см. разд. «Первичное обследование»). В целом возможность резекции допускается, если функция печени соответствует классу А по шкале Чайлда-Пью при отсутствии признаков портальной гипертензии (см. ГЦР-4). Вместе с тем тщательно отобранным пациентам, соответствующим классу В по Чайлду-Пью, особенно при нормальных показателях функции печени и отсутствии клинических признаков портальной гипертензии, можно выполнить ограниченную резекцию печени.
Для оценки характеристик опухоли и части печени, которую предполагается оставить в ходе резекции, незаменимы методы визуализации.37 КТ/МРТ позволяют установить количество и размер опухолевых очагов ГЦР выявить внепеченочные метастазы, установить прорастание опухоли в воротную, нижнюю полую вену, локализацию опухолей относительно сосудов и желчных протоков.
Резекцию печени лучше всего выполнять больным с одиночной опухолью, не прорастающей в крупный сосуд. Ограничений для резекции печени по размеру опухоли нет, однако чем больше опухоль, тем выше риск прорастания в сосуд и метастазирования.93,101 Согласно результатам одного исследования, инвазия сосудов не наблюдалась примерно у 1/3 больных с одиночным ГЦР размером более 10 см.93 Тем не менее наличие макро- или микроскопических проявлений сосудистой инвазии считается мощным прогностическим фактором рецидива ГЦР93,102,103 Целесообразность резекции печени у больных с многоочаговыми опухолями и/или признаками прорастания в крупные сосуды спорна. Вместе с тем результаты недавно выполненного ретроспективного анализа показали, что 5-летняя общая выживаемость отобранных по определенным критериям пациентов с одной опухолью размером не более 5 см или тремя опухолями и менее размером не более 3 см после резекции печени составила 81%.105 По взаимному согласию членов рабочей группы резекция печени показана тщательно отобранным пациентам с названными выше характеристиками опухоли. Наличие внепеченочных метастазов считается противопоказанием к резекции.
Другой важный фактор предоперационного обследования - оценка части печени, которую предполагается оставить после резекции, что позволяет прогнозировать функцию печени после операции. Для измерения оставляемой части печени применяют КТ, с помощью которой можно рассчитать и общий объем печени. На основе данных КТ вычисляют отношение оставляемого объема к общему объему печени (вычитаемый объем печени).106 Рабочая группа рекомендует, чтобы это отношение было не менее 20% у больных без цирроза и не менее 30-40% у больных, соответствующих классу А по шкале Чайлда-Пью.107 Если это соотношение меньше рекомендованного, но по остальным параметрам пациенту резекция печени не противопоказана, рекомендуется, если это возможно, предоперационная эмболизация воротной вены. Это безопасная и эффективная процедура, позволяющая перенаправить кровоток в часть печени, оставляемую во время операции. В этих сегментах печени стимулируется гипертрофия, тогда как эмболизированная часть печени подвергается атрофии.108
Трансплантация печени
Трансплантация печени - привлекательный, потенциально радикальный метод лечения больных с ранней стадией ГЦР.91 Во время процедуры удаляют как выявленные, так и невыявленные опухолевые очаги, можно излечить от цирроза печени и избежать осложнений, связанных с уменьшением функционально активной части печени вследствие резекции. В 1996 г. опубликованы результаты эпохального исследования Mazzaferro et al., согласно которым в подгруппе больных с нерезектабельным ГЦР, соответствующих определенным критериям отбора (а именно Миланским критериям), 4-летная общая и безрецидивная выживаемость составили 85 и 92% соответственно.109 Эти результаты подтверждаются данными последующих исследований, в которых эти критерии применяли для отбора пациентов для трансплантации.110 Данные критерии отбора были приняты UNOS (включают в себя рентгенологическое доказательство одиночной опухоли диаметром до 5 см либо 2-3 опухоли диаметром до 3 см и отсутствие признаков инвазии крупного сосуда либо отдаленных метастазов),111 поскольку они позволяют выделить подгруппу больных ГЦР, у которых результаты трансплантации печени аналогичны таковым у больных с конечной стадией цирроза без ГЦР
Критерии UNOS также устанавливают, что больные, подходящие для трансплантации печени, не должны быть кандидатами на резекцию печени.111 Следовательно, трансплантация печени рассматривается как стартовая терапия больных с начальной стадией ГЦР и умеренным либо тяжелым циррозом (т. е. классы В и С по шкале Чайлда-Пью). Частичная гепатэктомия обычно рассматривается как наилучший вариант первой линии лечения пациентов с начальной стадией ГЦР! относящихся к классу А по Чайлду-Пью, и при условии, что локализация опухоли позволяет выполнить резекцию. Однако исследований, сравнивающих эффективность резекции и пересадки печени в последней группе пациентов, не проводилось. Таким образом, вопрос, с чего следует начинать лечение данной группы больных, остается открытым.112-115 По взаимному согласию членов рабочей группы NCCN основным вариантом лечения больных, функциональное состояние печени которых соответствует классу А по Чайлду-Пью и которые удовлетворяют критериям UNOS, может быть как частичная гепатэктомия, так и трансплантация. Кроме того, эти пациенты должны быть операбельны исходя из общего состояния и сопутствующих заболеваний (см. ГЦР-В).116
Шкала MELD, оценивающая функцию печени (см. разд. «Первичное обследование»), также применяется в качестве предиктора смертности до трансплантации. С 2002 г. UNOS начала использовать эту шкалу с целью оценить риск смерти в течение 3 мес. нахождения в списке ожидающих пересадку трупной печени. В соответствии с современной политикой UNOS больные с ГЦР стадии Т2 (по критериям UNOS это 1 узел диаметром 2-5 см либо 2-3 узла, каждый из которых диаметром менее 3 см) получают дополнительное преимущество в 22 балла по MELD (так называемое MELD-исключение).62,111 Результаты ретроспективного анализа данных, предоставленных UNOS, свидетельствуют о том, что из 15906 пациентов, которым впервые была выполнена трансплантация печени в 1997-2002 гг., у 4,6% имелся ГЦР При этом из 19404 пациентов, которым впервые была выполнена трансплантация печени в 2002-2007 г., ГЦР был у 26%. Следует отметить, что в последней группе большинство больных получили «ГЦР MELD-исключение».117 В 2002-2007 гг. у больных с «ГЦР MELD-исключением» выживаемость была аналогична таковым без ГЦР Важными прогностическими показателями низкой выживаемости после трансплантации у больных ГЦР были оценка по MELD >20 и уровень АФП >455 нг/мл.117 Следует отметить, что надежность шкалы MELD как предиктора смертности после трансплантации пока не доказана. Также значительно ниже была выживаемость в подгруппе пациентов с опухолью размером 3-5 см.
В настоящее время активно обсуждается распространение Миланских критериев и критериев UNOS на больных, размер опухолей у которых незначительно превышает крайние показатели пригодности для трансплантации.110,118,119 Группой ученых Университета Калифорнии в Сан-Франциско (UCSF) предложен перечень расширенных критериев, которые позволяют считать возможной пересадку печени больным с одиночной опухолью до 6,5 см, максимум 3 опухолями, размер каждой из которых не превышает 4,5 см, а совокупный размер всех опухолей - менее 8 см.120 Результаты исследований выживаемости после трансплантации в случае превышения Миланских критериев, но соответствия критериям UCSF отличаются сильным различием показателей 5-летней выживаемости (от 38 до 93 %).118,119,121-113 В пользу расширения Миланских критериев и критериев UNOS свидетельствует общепризнанный факт, показывающий, что многих больных, у которых характеристики опухоли превышают Миланские критерии, можно излечить путем трансплантации печени.119 Противники расширения Миланских критериев и критериев UNOS указывают на дефицит донорских органов, а также повышенный риск сосудистой инвазии и рецидива у пациентов с более крупными опухолями и более тяжелой стадией ГЦР.110118121 В некоторой степени второе возражение подтверждается результатами крупного ретроспективного анализа базы данных UNOS, свидетельствующими о значительно меньшей продолжительности жизни больных из подгруппы с размером опухоли 3-5 см по сравнению с больными с меньшим размером опухоли.117
Переходная терапия
В ряде исследований изучалась роль локорегионарной терапии ГЦР в качестве перехода к трансплантации печени у больных, находящихся в листе ожидания трансплантации.4124 В этих исследованиях в качестве средств переходной терапии применяли радиочастотную абляцию (РЧА),125,126 химиоэмболизацию127 и сорафениб.128 Однако небольшой объем этих исследований, гетерогенность исследованных популяций наряду с отсутствием данных рандомизированных клинических исследований, посвященных оценке роли переходной терапии в снижении процента исключения из очереди на трансплантацию печени, ограничивает выводы, которые можно было бы сделать.129,130 Тем не менее, применение переходной терапии в этих условиях растет, ее назначают в некоторых центрах NCCN.
Локорегионарная терапия
Методы местного лечения больных ГЦР направлены на достижение селективного некроза опухоли. Их можно разделить на две категории: абляция и эмболизация. Не доказано, что эффективность локорегионарной терапии ГЦР сопоставима с эффективностью резекции печени или трансплантации.83,112 Рабочая группа считает, что эти методы не следует применять вместо резекции или трансплантации печени у больных, которые удовлетворяют критериям выбора для проведения операции (см. ГЦР-5; ГЦР-6; ГЦР-С).
Абляция
Некроз опухоли можно вызвать прямым воздействием на нее определенным химическим веществом (например, этанолом, уксусной кислотой) либо термическим воздействием (высокочастотная, микроволновая абляция, криоабляция).30,91 Любую абляционную терапию можно выполнить лапароскопически, чрескожно или путем лапаротомии. Чаще всего применяют РЧА и чрескожные инъекции этанола (ЧИЭ). Абляционная терапия показана больным, у которых размер и локализация первичной опухоли полностью подходят для этого лечения. Частота осложнений, связанных с абляционной терапией ГЦР, относительно мала. Например, в ходе рандомизированного контролируемого исследования, в котором сравнивалось лечение больных ГЦР путем РЧА либо ЧИЭ, частота серьезных осложнений и смертность составили 4,8 и 0 % соответственно.132
Степень некроза опухоли, вызванного абляционной терапией, определяют с помощью КТ/МРТ в определенное время после процедуры (в отличие от гистологического исследования).11,133 Отсутствие поглощения контрастного средства опухолью по сравнению с контрольными данными визуализации до лечения расценивается как отсутствие остаточной васкуляризации и полный некроз опухоли. Тем не менее, для определения эффективности локорегионарной терапии используют ряд факторов, разрабатываются критерии для оценки степени регрессии опухоли в ответ на лечение.124,134-138
Результаты исследований свидетельствуют, что абляционная терапия наиболее эффективна при ГЦР малых размеров.125,126,139,140 По взаимному согласию членов рабочей группы абляционную терапию ГЦР лучше всего выполнять при размере опухоли не более 3 см. Если размер опухоли составляет 3-5 см, абляционную терапию рекомендуется комбинировать с эмболизацией (см. разд. «Катетерная эмболизация и химиоэмболизация» и «Комбинация местных методов лечения»). По мнению рабочей группы, чрескожная абляция очень хорошо подходит для лечения больных, соответствующих всем необходимым критериям, у которых имеются небольшие нерезектабельные опухоли.
В одном ретроспективном анализе оценивались результаты РЧА, ЧИЭ либо комбинации этих процедур, выполненных в период ожидания трансплантации 40 пациентам с ГЦР, соответствующим классу А или В по шкале Чайлда-Пью. Установлено, что после РЧА частота полных некрозов составила 46,7%, частичных - 53,3%, после ЧИЭ - 23,1 и 46,1% соответственно. В то же время после ЧИЭ в 30,8 % опухолей признаков некроза не выявлено. Общая частота полных некрозов составила 53,1% для опухолей менее 3 см и 14,3% для опухолей 3 см и более (p=0,033). Однако после РЧА опухолей диаметром менее 3 см этот показатель повысился до 61,9%. Результаты исследования Mazzaferro et al. подтверждают вывод о том, что размер опухоли служит основным фактором, определяющим эффективность абляционной терапии ГЦР126 В этом проспективном исследовании участвовало 50 отобранных произвольным путем больных циррозом печени, которым в период ожидания трансплантации была выполнена РЧА. Частота полного некроза опухоли составила 55% для всех опухолей и 63% для опухолей размером не более 3 см.
Эффективность РЧА и ЧИЭ при лечении больных ГЦР, относящихся к классу А по шкале Чайлда-Пью, сравнивали в нескольких рандомизированных контролируемых исследованиях.141-143 Установлено, что РЧА превосходит ЧИЭ по частоте полного ответа (65,7 us 36,2%; p=0,0005)142 и по частоте местных рецидивов.141,143 Кроме того, в результате одного исследования оказалось, что больным в группе РЧА требовалось меньшее количество процедур.143 Следует отметить, что преимущество РЧА перед ЧИЭ в плане общей выживаемости установлено лишь в двух из названных исследований.141,143 Результаты третьего исследования не выявили статистически значимых различий в общей продолжительности жизни больных в обеих группах лечения.142 РЧА также сравнивали с резекцией печени в ходе проспективного рандомизированного контролируемого исследования.133 Между группами лечения не установлено различий по продолжительности жизни без рецидивов и общей продолжительности жизни, хотя исследование характеризуется такими недостатками, как небольшое число участников и отсутствие анализа на неменьшую эффективность.
Судя по данным литературы, частота местных рецидивов после абляционной терапии ГЦР варьирует в широких пределах. Возможно, это обусловлено применением различных критериев отбора пациентов и протоколов лечения. Например, по данным Shiina et al., 4-летняя частота рецидивов у больных с тремя и менее опухолями до 3 см составила 70% в группе РЧА и 85 % в группе ЧИЭ.143 Результаты другого исследования показали, что среди больных с одиночной опухолью менее 2 см рецидивы в течение 31 мес. после курса РЧА наблюдались менее чем в 3 % случаев.140
Результаты некоторых долгосрочных исследований свидетельствуют о том, что после абляционной терапии рецидивы не наблюдались в течение 5 лет более чем у 50% больных.144,145 Тем не менее следует отметить значительную вариабельность показателей общей выживаемости, установленных в результате исследований с участием больных ГЦР, получавших абляционное лечение.133,141-146 Вполне возможно, это обусловлено различиями исследуемых популяций по определенным характеристикам заболевания (например, по размеру и количеству опухолей) и, что представляется более важным, по состоянию функции печени.145,146
Если говорить о локализации опухоли, то поражение определенных участков печени (например, вблизи диафрагмальной поверхности) препятствует чрескожному доступу. Абляционное лечение опухолей, связанных с капсулой печени, может привести к разрыву органа; крупные сосуды, проходящие в непосредственной близости от опухоли, способствуют поглощению больших количеств тепла при использовании РЧА.11 Рабочая группа обращает особое внимание на необходимость соблюдения осторожности при выполнении абляции вблизи крупных сосудов, крупных желчных протоков и других органов брюшной полости (см. ГЦР-С).
Эмболизация
Лечение ГЦР путем трансартериальной эмболизации (химиоэмболизация, простая катетерная эмболизация, радиоэмболизация) основано на селективном чрескатетерном введении частиц в ветвь печеночной артерии, питающей часть печени с растущей опухолью.147 Эмболизационная терапия осуществима благодаря двойному кровоснабжению печени. Если нормальная ткань печени в основном кровоснабжается через воротную вену, то опухоли - через печеночную артерию.35 Более того, ГЦР характеризуются гиперваскуляризацией и более интенсивным кровотоком по сравнению с нормальной тканью печени.
В каждом случае до проведения эмболизации необходимо оценить анатомическую картину артериального кровоснабжения печени. Поскольку неприцельная эмболизация печени может причинить существенный вред больному, трансартериальную эмболизацию ограничивают сегментом, субсегментом либо долей печени. Все ГЦР независимо от локализации можно рассматривать как пригодные для эмболизации, если можно изолировать артериальное кровоснабжение опухоли.148-151 Некроз опухоли, обусловленный эмболизацией, обычно оценивают по степени уменьшения поглощения контрастного средства на КТ/МРТ в динамике в определенное время после процедуры по сравнению с исходными данными визуализации. Тем не менее для определения эффективности локорегионарной терапии используют ряд факторов, разрабатываются критерии для оценки степени регрессии опухоли в ответ на лечение.124,134-138
Эмболизация показана неоперабельным больным, пациентам с нерезектабельной опухолью, с опухолями, которые невозможно лечить только путем абляционной терапии, и при отсутствии отдаленных метастазов (см. ГЦР-5; ГЦР-6; ГЦР-С). Также следует учитывать общее состояние больного и функцию печени (шкала Чайлда-Пью). Кроме того, при отборе пациентов рекомендуется учитывать вид эмболизации. Это позволит избежать значительной интоксикации (см. разд. «Катетерная эмболизация и химиоэмболизация» и «Радиоэмболизация»).
По мнению рабочей группы, неоперабельным больным, пациентам с нерезектабельной опухолью показана трансартериальная эмболизация, если диаметр опухоли более 5 см. Больным с опухолями диаметром 3-5 см рекомендуется комбинированное лечение с абляцией и трансартериальной эмболизацией (см. ГЦР-С; разд. «Комбинация местных методов лечения»).
Катетерная эмболизация и химиоэмболизация
Принцип катетерной эмболизации, называемой также трансартериальной эмболизацией (ТАЭ), и трансартериальной химиоэмболизации (ТАХЭ) основан на уменьшении кровоснабжения опухоли, что приводит к ее ишемии и некрозу. С целью блокады артериального кровотока применяют частицы желатиновой губки, поливинилового спирта и полиакриламидные микросферы.149,152,153 Во время ТАХЭ в отличие от ТАЭ до введения эмболизирующих частиц через катетер подается концентрированная доза химиопрепарата (например, доксорубицин или цисплатин) в сочетании с эмульгирующим агентом.152 Результаты двух рандомизированных клинических исследований свидетельствуют о более высокой продолжительности жизни больных, получавших ТАХЭ, по сравнению с теми, кто получал симптоматическое лечение по поводу нерезектабельного ГЦР.151,154 В одном из исследований пациентов рандомизировали на группы лечения с помощью ТАЭ, ТАХЭ и симптоматической терапии.151 В этих группах 1- и 2-летняя выживаемость составили 82 и 63%, 75 и 50%, 63 и 27% соответственно. У большинства больных в этом исследовании функция печени соответствовала классу А по шкале Чайлда-Пью, общее состояние - 0, размер основного опухолевого узла - около 5 см. В группе больных, получавших ТАХЭ либо ТАЭ, частота частичных или полных регрессий, продолжавшихся минимум 6 мес., составила примерно 30 и 1% соответственно. Недостатками данного исследования было его досрочное прекращение, а также неспособность выявить различия между группами ТАХЭ и ТАЭ из-за слабой статистической мощности.149
На результаты многих клинических исследований, посвященных оценке эффективности ТАЭ и ТАХЭ при лечении больных ГЦР! влияет применение сильно различающихся стратегий терапии, включая тип эмболизирующих частиц, тип химиотерапии, тип эмульгирующего агента (для исследований с применением ТАХЭ) и количество выполненных процедур.149,153 Согласно данным одного из недавно выполненных ретроспективных анализов, после проведения ТАЭ по стандартизованной методике 1-, 2- и 3-летняя общая выживаемость больных ГЦР были 66, 46 и 33% соответственно. В подгруппе пациентов без внепеченочного распространения опухоли и без поражения воротной вены эти показатели возросли до 84, 66 и 51 % соответственно.149
Согласно данным многофакторного анализа, выполненного Maluccio et al. по результатам ТАЭ, к неблагоприятным прогностическим факторам относятся размер опухоли 5 см и более, наличие 5 опухолевых узлов или более и внепеченочное распространение опухоли. Окклюзия воротной вены не была независимым прогностическим фактором выживаемости.149 Однако имеются доказательства того, что окклюзия воротной вены,155,156 состояние функции печени, соответствующее классу С по Чайлду-Пью,156 уровень общего билирубина сыворотки более 3 мг/ мл157 служили статистически значимыми показателями неблагоприятного прогноза у больных, которым была выполнена ТАХЭ. Таким образом, рабочая группа полагает, что тромбоз основного ствола воротной вены должен рассматриваться как противопоказание к ТАХЭ, и не рекомендует ее пациентам, состояние функции печени которых соответствует классу С по шкале Чайлда-Пью. Поскольку ТАЭ повышает риск некроза печени и абсцесса печени у больных с нарушением проходимости желчных протоков,127 рабочая группа предлагает считать относительным противопоказанием к ТАХЭ или ТАЭ уровень общего билирубина более 3 мг/мл, за исключением случаев, когда возможна сегментная эмболизация (см. ГЦР-С). Более того, у больных, которым ранее накладывали билиодигестивный анастомоз, повышен риск образования внутрипеченочного абсцесса после ТАХЭ.152
К осложнениям ТАЭ и ТАХЭ относятся острый тромбоз воротной вены, холецистит, угнетение кроветворения и другие побочные эффекты.30,158 Следует отметить, что в ходе разных исследований установлена различная частота серьезных побочных эффектов. Как сообщается, относительно часто у больных после ТАЭ и ТАХЭ развивается постэмболизационный синдром, включающий повышение температуры тела, боль в животе и кишечную непроходимость.30,158 По данным разных авторов, летальность, связанная с ТАЭ и ТАХЭ, обычно не превышает 5% 30,149,151,158
Согласно результатам многоцентрового рандомизированного исследования со сравнением доксорубицин-высвобождающих эмболизирующих микрошариков с традиционной ТАХЭ доксорубицином у 212 больных с циррозом А/В по шкале Чайлда-Пью и локализованным нерезектабельным ГЦР без поражения регионарных лимфатических узлов оба метода характеризовались сопоставимой эффективностью, хотя в первом случае число побочных эффектов было значительно меньше.159
Радиоэмболизация
Радиоэмболизация - новый метод эмболизации, предусматривающий местное воздействие высокой дозы радиоактивного излучения на капиллярное ложе опухоли.147,160 Достигается это за счет транскатетерного введения микросфер с внедренным в них источником Р-излучения иттрием-90. Данный метод обеспечивает ограниченное проникновение радиации во избежание воздействия на нормальную ткань печени. Подобные микросферы выпускают двух видов: TheraSpheres (стеклянные) и SIR-Spheres (на основе смолы). Хотя радиоэмболизация, так же как ТАЭ и ТАХЭ, подразумевает определенную окклюзию сосудов, считается, что она в большей степени блокирует микро-, а не макрососуды, при этом некроз опухоли, скорее всего, развивается за счет воздействия ионизирующей радиации, нежели ишемии.150
В исследовании II фазы с участием 108 больных с нерезектабельным ГЦР с или без тромбоза воротной вены после радиоэмболизации частота частичных регрессий за 6 мес. наблюдения составила 42,2%.150 Побочные явления III-IV степени чаще всего наблюдались у больных с тромбозом основного ствола воротной вены. Следует отметить, что у больных с тромбозом ветвей воротной вены частота нежелательных явлений в виде повышения уровня билирубина была такой же, как у больных без тромбоза воротной вены. Результаты одного из последних одноцентровых проспективных продольных когортных исследований, в котором участвовал 291 больной с НСС, получавший радиоэмболизационную терапию, свидетельствуют о статистически значимом различии продолжительности жизни больных с разной степенью нарушения функции печени (класс А по шкале Чайлда-Пью 17,2 мес. и класс В - 7,7 мес.; р=0,002).161 Медиана продолжительности жизни больных, соответствующих классу В по шкале Чайлда-Пью, с тромбозом воротной вены, составляла 5,6 мес. После радиоэмболизации возможны такие осложнения, как холецистит и формирование абсцесса.150,161,162 Необходимы рандомизированные контролируемые исследования радиоэмболизации с участием больных ГЦР.
Комбинация местных методов лечения
Недавно проведен ряд исследований, направленных на оценку эффективности использования комбинации местных видов лечения у неоперабельных больных или пациентов с нерезектабельным ГЦР Например, в основе комбинации РЧА и ТАЭ лежит усиление теплового воздействия РЧА за счет окклюзии сосудов при ТАЭ, поскольку циркуляция крови внутри опухоли увеличивает передачу тепла опухолевой ткани.
Результаты ретроспективного анализа у отдельных больных с одиночной опухолью размером до 7 см, которых лечили путем комбинации ТАЭ с абляцией либо путем резекции печени, свидетельствуют о том, что 1-, 3- и 5-летняя вероятная выживаемость после комбинированного лечения составили 97, 77 и 56%, после хирургического лечения - 81, 70 и 58% соответственно.148 В другом исследовании со сходной программой 1-, 3- и 5-летняя выживаемость больных с опухолями, соответствующими критериям UNOS по количеству и размеру, в группе комбинированного лечения составили соответственно 98, 94 и 75%, в группе хирургического лечения - 97, 93 и 81%.105
По взаимному согласию членов рабочей группы больных с ГЦР размером 3-5 см, не подходящих для резекции или трансплантации печени, можно лечить путем комбинации РЧА и эмболизации.
Конформная или стереотаксическая лучевая терапия
Дистанционная лучевая терапия (3-D конформная или стереотаксическая) обеспечивает воздействие высокой дозы радиации на очаг ГЦР без облучения окружающих тканей печени, тем самым ограничивая риск лучевого поражения печени у больных с нерезектабельным/неоперабельным раком.136
Эффективность конформной или стереотаксической лучевой терапии у больных с нерезектабельной опухолью, характеризующейся обширным поражением, или не подходящим для трансплантации печени по другим параметрам, а также с локальным поражением, но не операбельных из-за общего состояния или сопутствующих заболеваний164 (см. ГЦР-5; ГЦР-6), изучена слабо. В связи с этим этот метод лечения отнесен к категории 2В. Данный метод не включен в настоящие рекомендации в качестве варианта лечения больных с метастазами (см. ГЦР-6).
Системная терапия
В большинстве случаев ГЦР выявляют на поздних стадиях, и у многих больных радикальное лечение невозможно. Учитывая, что у пациентов с нерезектабельным ГЦР ограниченным пределами печени, возможно лечение путем различных вариантов эмболизации и абляции, системную терапию назначают лишь больным с последней стадией заболевания.
Результаты практически всех клинических исследований с применением химиотерапии (например, доксорубицина) для лечения больных с поздней стадией ГЦР свидетельствуют о низкой частоте ответа на лечение. Доказательств благоприятного влияния химиотерапии на общий коэффициент выживания среди больных ГЦР нет.165-167 Рабочая группа рекомендует применять системную моно- или комбинированную химиотерапию, интраартериальную химиотерапию, а также комбинацию химиотерапии с лучевой для лечения больных с нерезектабельным ГЦР только в условиях клинического исследования (см. ГЦР-5).
Сорафениб, пероральный мультикиназный ингибитор, подавляющий пролиферацию опухолевых клеток и ангиогенез, изучали в одном исследовании II фазы и двух рандомизированных плацебо-контролируемых исследованиях III фазы с участием больных с поздней стадией или с метастазами ГЦР90,124 153,168-170,177
В исследовании III фазы Sorafenib in Advanced Hepatocellular Carcinoma (SHARP) участвовало 602 больных, которых рандомизировали на группы лечения сорафенибом и симптоматической терапии. В данном исследовании под поздней стадией ГЦР понимали невозможность хирургического или локорегионарного лечения либо прогрессирование заболевания после этих видов лечения.168 Примерно у 70% больных в данном исследовании отмечались макроскопически заметная сосудистая инвазия и/или распространение опухоли за пределы печени. Тем не менее у большинства пациентов функция печени была сохранена (т. е. 95% пациентов и более отнесены к классу А по Чайлду-Пью) и отмечались высокие показатели общего состояния (т. е. более 90% больных соответствовало уровню 0 или 1 по шкале ECOG). Это позволило исключить другие возможные причины смерти. Этиология ГЦР у участников исследования была различной. У 29 % больных причиной ГЦР был гепатит С, у 26% - алкоголь, у 19% - гепатит В. Медиана общей выживаемости в группе лечения сорафенибом была статистически значимо выше (10,7 мес. в группе сорафениба vs 7,9 мес. в группе плацебо; отношение рисков 0,69; 95%-й доверительный интервал [ДИ] 0,55-0,87; p<0,001).
В азиатско-тихоокеанском исследовании III фазы со сходной программой участвовало 226 пациентов, которых рандомизировали на группы лечения сорафенибом или плацебо (150 и 76 человек соответственно).169 Это исследование и SHARP существенно различались по характеристикам больных и заболевания, хотя критерии включения/исключения и процент пациентов, относящихся к классу А по Чайлду-Пью (97%), были одинаковыми. В азиатско-тихоокеанском исследовании участвовали только больные азиатского происхождения. По сравнению с участниками исследования SHARP в этой популяции больных была выше вероятность следующих факторов: более молодой возраст, обусловленность рака гепатитом В (>70 %), наличие клинических проявлений, большее количество опухолевых очагов. Отношение рисков в группе лечения сорафенибом по сравнению с группой плацебо (0,68; ДИ 0,50-0,93; p=0,014) было почти таким же, как и в исследовании SHARP. Медиана общей выживаемости в азиатско-тихоокеанском исследовании была ниже как в группе лечения, так и в группе плацебо (6,5 vs 4,2 мес.).
На основе данных исследования SHARP выполнен ряд анализов, направленных на оценку эффективности сорафениба в отдельных подгруппах пациентов. Результаты этих анализов свидетельствуют о благоприятном влиянии сорафениба на продолжительность жизни больных с общим состоянием 1-2 балла по шкале ECOG171 и у которых ГЦР был связан со злоупотреблением алкоголем172 либо гепатитом С.173 Лечение сорафенибом характеризовалось хорошей переносимостью в обоих рандомизированных клинических исследованиях. К побочным эффектам сорафениба в исследовании SHARP относили диарею, снижение массы тела, ладонно-подошвенную эритродизестезию.168
Оценить эффективность сорафениба при лечении больных с функцией печени, соответствующей классу В по шкале Чайлда-Пью, невозможно ввиду малого объема наблюдений; почти у всех больных в описанных рандомизированных исследованиях функция печени была сохранена (класс А по Чайлду-Пью).177 В исследовании II фазы с изучением эффективности сорафениба в лечении ГЦР у 28% из 137 участников состояние функции печени соответствовало классу В по Чайлду-Пью.170 Результаты подгруппового анализа данных этого исследования свидетельствуют о меньшей общей выживаемости больных, соответствующих классу В по Чайлду-Пью, по сравнению с теми, кто относится к классу А (14 vs 41 нед.).174 Кроме того, нарушение функции печени, возможно, влияет на дозировку сорафениба и выраженность побочных явлений. По данным Abou-Alfa et al., в группе больных, соответствующих классу В по Чайлду-Пью, отмечались более выраженные гипербилирубинемия, энцефалопатия и асцит, однако дифференцировать степень влияния исследуемого препарата и имеющегося заболевания на эти проявления трудно.90,174 Изучение фармакокинетики сорафениба и исследование I фазы с участием больных с нарушением функции печени и почек позволили установить связь между повышением уровня билирубина и возможным токсическим влиянием препарата на печень.175 Кроме того, по данным исследования сорафениба, частота побочных эффектов III-IV степени у пациентов с низким риском составила 34%. В исследуемую популяцию входило 26 % больных, относящихся к классу В или C по Чайлду-Пью, и 50 % больных с тромбозом воротной вены.176 Наконец, важно отметить необходимость разработки достоверных критериев оценки реакции опухоли на сорафениб, поскольку объективно подтвержденная регрессия наблюдается редко.177
На основании результатов этих исследований сорафениб рекомендуется в качестве выбора категории 1 (для некоторых пациентов с функцией печени класса А по Чайлду-Пью) и категории 2А (для некоторых пациентов с функцией печени класса В по Чайлду-Пью) при следующих характеристиках заболевания: нерезектабельный рак и обширное поражение/противопоказание к трансплантации печени, местное поражение только у неоперабельных больных в связи с общим состоянием или сопутствующими заболеваниями, наличие метастазов. Тем не менее рабочая группа полагает, что имеющихся данных по безопасности и дозировке сорафениба при лечении больных, состояние функции печени которых соответствует классу В по шкале Чайлда-Пью, недостаточно, и рекомендует соблюдать крайнюю осторожность при назначении сорафениба пациентам с повышенным уровнем билирубина (см. ГЦР-5; ГЦР-6).
Симптоматическое лечение
Рабочая группа рекомендует назначать симптоматическое лечение больным с нерезектабельным раком, неоперабельным, которым противопоказаны другие виды лечения (см. ГЦР-5; ГЦР-6).
Наблюдение
Данные о роли диспансерного наблюдения после резекции ГЦР весьма малочисленны. Рекомендации основываются на взаимном согласии членов рабочей группы о том, что раннее выявление заболевания способствует участию больного в исследованиях или повышает возможность применения других форм лечения. Рабочая группа рекомендует проводить визуализационные исследования с поперечными срезами высокого качества каждые 3-6 мес. в течение 2 лет, затем - ежегодно. Если изначально уровень АФП был повышен, контрольные анализы выполняют каждые 3 мес. в течение 2 лет, затем - каждые 6 мес. В случае прогрессирования заболевания рекомендуется повторное обследование по программе первичного (см. ГЦР-4; ГЦР-5).
Рак желчного пузыря
Факторы риска
Факторы риска рака желчного пузыря, среди которых преобладает желчнокаменная болезнь, обусловлены хроническим воспалением.
Кальциноз желчного пузыря («фарфоровый» желчный пузырь) вследствие хронического воспаления также создает угрозу развития рака.178,179
Диагностика и первичное обследование
Рак желчного пузыря часто выявляют на поздней стадии, что обусловлено агрессивностью опухоли, которая быстро распространяется. Причиной поздней диагностики служит также неспецифическая клиническая картина, сходная с печеночной коликой или хроническим холециститом.178 Таким образом, рак желчного пузыря нередко устанавливают случайно в ходе операции или при патоморфологическом исследовании после холецистэктомии по поводу желчнокаменной болезни. Рекомендации по хирургическому и послеоперационному обследованию больных, у которых рак желчного пузыря выявлен во время или после операции, см. в разд. «Лечение рака желчного пузыря».
Другие возможные проявления рака желчного пузыря - бессимптомное объемное образование, выявляемое при УЗИ, либо желтуха. Первичное обследование таких больных обязательно включает оценку показателей функции и функционального резерва печени. При необходимости определяют уровень раково-эмбрионального антигена (РЭА) и СА 199, хотя эти маркеры неспецифичны для рака желчного пузыря.149 Для оценки прорастания опухоли в стенки желчного пузыря, выявления прямой инвазии соседних органов/желчных путей, инвазии крупных сосудов и определения отдаленных метастазов и поражения регионарных лимфоузлов рекомендуется использовать методы визуализации высокого качества.37 Кроме того, необходимо рентгенологическое исследование грудной клетки. Если отдаленные метастазы не обнаружены, выполняют диагностическую лапароскопию, поскольку при этом заболевании высок риск диссеминации опухоли по брюшине.179,180 Если пациент поступает с желтухой, выполняют холангиографию с целью оценить прорастание опухоли в печень и желчные протоки.37 Неинвазивная магнитно-резонансная холангиография (МРХГ) предпочтительнее эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) или чрескожной чреспеченочной холангиографии (ЧЧХ), за исключением случаев, когда планируется лечебное вмешательство. Роль позитронно-эмиссионной томографии (ПЭТ) в обследовании пациентов с раком желчного пузыря не установлена, растет число наблюдений, свидетельствующих о ценности этого метода как средства выявления отдаленных метастазов у больных с потенциально резектабельной опухолью по остальным параметрам.181182
Патоморфология и классификация по стадиям
Примерно 80% злокачественных опухолей желчного пузыря относятся к аденокарциномам.178,183 Рак желчного пузыря часто характеризуется ранним распространением в лимфоидную ткань и системный кровоток.178,184
Критерии TNM-классификации рака желчного пузыря, разработанные AJCC, представлены в табл. 2. Обзор данных примерно 2500 пациентов с раком желчного пузыря, полученных из больничных онкологических регистров США, показал, что стадия опухоли тесно связана с продолжительностью жизни больного. 5-летняя выживаемость больных с 0-IV стадией рака составила соответственно 60, 39, 15, 5 и 1 %.185 Недавно был выполнен ретроспективный одноцентровый анализ, в котором медиана общей выживаемости в общей популяции больных раком желчного пузыря составила 10,3 мес. от момента диагностики.183 Медиана продолжительности жизни для пациентов со стадиями Ia-III и IV равнялась 12 и 5,8 мес. соответственно.183
Лечение рака желчного пузыря
Единственным радикальным методом лечения служит операция. Согласно результатам ретроспективного анализа, охватывающего период с 1995 по 2005 г., клинически радикальная резекция по поводу рака желчного пузыря в одном центре была выполнена 123 из 435 пациентов, при этом у 47% больных рак желчного пузыря выявлен как случайная находка во время лапароскопической холецистэктомии.183
Хотя лечение больных, у которых рак желчного пузыря выявлен во время холецистэктомии либо при патоморфологическом исследовании после нее, отличается от лечения больных, у которых это заболевание установлено до операции (см. далее), хирургическая тактика в случае резектабельного рака одинакова, если желчный пузырь не был удален и рак был случайно выявлен при патоморфологическом исследовании. Во всех случаях операцию должен выполнять хирург, имеющий соответствующую подготовку. Факторами, определяющими резектабельность рака желчного пузыря, служат стадия опухоли по ТNM-классификации AJCC (см. табл. 2) и ее локализация.178 Всем больным перед операцией выполняют КТ/МРТ и рентгенографию грудной клетки для выявления отдаленных метастазов. Учитывая высокую ценность диагностической лапароскопии, ее рекомендуется выполнять перед лапаротомией с целью радикальной резекции рака желчного пузыря.
Анализ проспективных данных 104 больных, которым была выполнена операция по поводу рака желчного пузыря в 1990-2002 гг., показал, что большая резекция печени с удалением общего желчного протока значительно повышала частоту хирургических осложнений и не влияла на продолжительность жизни. Авторы анализа пришли к выводу, что в таком объеме операцию следует проводить только при невозможности радикально удалить опухоль другим путем.186 Согласно результатам другого исследования с ретроспективной оценкой 115 больных, установлена связь отрицательного хирургического края (R0) при повторной резекции по поводу случайно выявленного рака желчного пузыря с долгосрочной выживаемостью.187 Рабочая группа рекомендует пациентам с резектабельным раком желчного пузыря выполнять холецистэктомию с резекцией печени единым блоком и лимфаденэктомию с или без удаления желчного протока.178,188 При лимфаденэктомии удаляют лимфоузлы в области ворот печени, желудочно-печеночной связки и в ретродуоденальной области. В случае поражения лимфоузлов за пределами данного региона (чаще всего чревных, ретропанкреатических или в борозде между аортой и нижней полой веной) опухоль считается нерезектабельной.
При ретроспективном анализе больных раком желчного пузыря, получавших лечение в одном учреждении, установлено, что в 74% случаев после повторного хирургического исследования, выполненного в связи со случайным обнаружением рака желчного пузыря после лапароскопической холецистэктомии, имелись остатки опухоли.183 Если рак желчного пузыря выявляют в ходе операции, рабочая группа рекомендует определять стадию заболевания интраоперационно с исследованием замороженных срезов желчного пузыря. В зависимости от заключения хирурга и резектабельности опухоли возможна расширенная холецистэктомия, как описано выше. Если при случайном выявлении рака желчного пузыря патоморфологическое исследование свидетельствует об отрицательном хирургическом крае, у больных со стадией T1a можно ограничиться наблюдением, поскольку эти опухоли не прорастают мышечный слой.179 Больным с резектабельными опухолями стадии Т1Ь и выше оперативное лечение рекомендуется после проведения КТ/МРТ, исследования грудной клетки и лапароскопического исключения метастазов. В пользу данной рекомендации свидетельствует то, что у значительной доли больных обнаруживают остаточную опухоль в печени; также установлена связь между повышенным риском метастазов в локорегионарные лимфатические узлы и повышением Т-стадии.187 Если опухоль резектабельна, рекомендуется резекция печени и лимфаденэктомия с или без удаления желчного протока.189 По взаимному согласию членов рабочей группы не следует выполнять операцию, если резектабельность опухоли не установлена либо если хирург не имеет опыта проведения подобных операций (см. РЖП-1). Имеются доказательства того, что отложенная открытая лапаротомия после случайного выявления рака желчного пузыря не связана со снижением продолжительности жизни по сравнению с неотложной резекцией.190,191 Тем не менее, рабочая группа считает предпочтительным не откладывать хирургическую резекцию по поводу рака желчного пузыря, если хирург имеет опыт проведения подобных операций. Несмотря на отсутствие оптимальной стратегии адъювантной терапии больных после резекции рака желчного пузыря, можно предложить такие варианты, как химиолучевая терапия с фторпиримидином (за исключением Т1Ь, N0) и химиотерапия с фторпиримидином или гемцитабином (см. РЖП-3 и разд. «Химиолучевая терапия и химиотерапия в лечении рака желчного пузыря и холангиокарциномы»).
Если до операции установлена нерезектабельная опухоль, берут биопсию с целью верификации диагноза. Если у больного с нерезектабельным раком желчного пузыря или его метастазами наблюдается желтуха, до начала химиотерапии целесообразно наладить дренирование желчных протоков, если это технически возможно (см. РЖП-2). Дренирование желчных протоков с последующей химиотерапией улучшает качество жизни больного.192 Другие варианты лечения этих больных - химиолучевая терапия (для больных с локализованной опухолью) и химиотерапия (см. разд. «Химиолучевая терапия и химиотерапия в лечении рака желчного пузыря и холангиокарциномы»), участие в клиническом исследовании либо симптоматическое лечение.
Наблюдение
Данных в пользу активного наблюдения после резекции рака желчного пузыря нет. Режим наблюдения/обследования с применением методов визуализации определяет врач, обсудив этот вопрос с пациентом. Больных, перенесших расширенную холецистэктомию по поводу рака желчного пузыря, рекомендуется обследовать с применением методов визуализации каждые 6 мес. в течение 2 лет. В случае прогрессирования заболевания следует повторно обследовать больного по программе первичного обследования (см. РЖП-3).
Холангиокарцинома
Понятие «холангиокарцинома» объединяет все опухоли, происходящие из эпителия желчного протока.193,194 Холангиокарциномы могут возникать в любых желчных протоках. Их различают по анатомической локализации и, как правило, делят на внутри- и внепеченочные. Внутрипеченочные холангиокарциномы также называют периферическими, они растут в паренхиме печени (рис. 1). В настоящих рекомендациях к внепеченочным холангиокарциномам относят опухоли Клацкина, развивающиеся в области слияния правого и левого печеночных протоков. Следовательно, холангиокарциномы, растущие в любом месте общего печеночного протока, в области слияния правого и левого печеночных протоков либо в общем желчном протоке (включая внутрипанкреатическую часть), относятся к внепеченочным (см. рис. 1). Внепеченочные холангиокарциномы встречаются чаще внутрипеченочных, причем в большей части случаев наблюдается холангиокарцинома в области слияния правого и левого печеночных протоков.195
Факторы риска
У большинства больных с холангиокарциномой не отмечается никаких предрасполагающих факторов.196 Тем не менее известны факты, свидетельствующие о возможной связи с данным заболеванием некоторых факторов риска. Эти предрасполагающие факторы, как и при раке желчного пузыря, обусловлены хроническим воспалением и включают в себя хронический холелитиаз, кисты общего желчного протока и фасциолез.194,197 В отличие от рака желчного пузыря, считается, что желчнокаменная болезнь не повышает риска развития холангиокарциномы.178 Недавно была продемонстрирована связь внутрипеченочной холангиокарциномы с инфицированностью вирусом гепатита С,198 что позволяет объяснить повышенную частоту образования этой опухоли, наблюдавшуюся в некоторых центрах.199 Для того чтобы подтвердить эту предполагаемую связь, требуется проведение дополнительных исследований.200
Диагностика и первичное обследование
На ранней стадии клинические проявления, как правило, отсутствуют. Больной с внутрипеченочной холангиокарциномой обычно обращается с неспецифическими симптомами, такими как повышение температуры тела, снижение массы тела и/или боль в животе. Нередко наблюдаются симптомы обструкции желчных путей. С другой стороны, внутрипеченочную холангиокарциному можно выявить случайно при обследовании с применением метода визуализации в виде изолированного внутрипеченочного образования.37 И наоборот, больной с внепеченочной холангиокарциномой, скорее всего, поступит с желтухой, признаками непроходимости желчных протоков или патологическими изменениями при последующем обследовании с применением метода визуализации.178
При первичном обследовании этих больных следует определять показатели функции печени. При необходимости определяют РЭА и СА 19-9, хотя эти маркеры неспецифичны для холангиокарциномы и связаны с другими злокачественными и доброкачественными заболеваниями.178,201 В рамках первичного обследования рекомендуется как можно быстрее провести хирургический консилиум, чтобы оценить резектабельность обоих типов холангиокарциномы (см. разд. «Лечение холангиокарциномы»).
При обследовании больных с внутрипеченочной холангиокарциномой рекомендуется выполнить КТ/МРТ с отсроченным использованием контрастного средства. У внутрипеченочной холангиокарциномы нет патогномоничных особенностей на КТ/МРТ, однако эти методы позволяют охарактеризовать первичную опухоль, ее взаимоотношение с расположенными вблизи крупными сосудами и желчными путями, установить наличие сателлитных очагов и отдаленных метастазов в печени, поражение лимфоузлов и таким образом установить резектабельность опухоли.37 Кроме того, следует исследовать грудную клетку, используя методы визуализации, и выполнить диагностическую лапароскопию (если не обнаружено метастазов - выполнить лапароскопическую операцию). Рабочая группа обращает внимание на необходимость изучения результатов КТ/МРТ врачами различных специальностей, в т. ч. опытными рентгенологами и хирургами. Это позволяет установить стадию заболевания и определить возможные варианты лечения (например, резекцию или другой метод).
При подозрении на внепеченочную холангиокарциному во время первичного обследования выполняют КТ/МРТ с отсроченным использованием контрастного средства, что позволяет оценить объем поражения печени, визуализировать крупные сосуды, близлежащие лимфоузлы и отдаленные участки.37 Поскольку многие больные поступают с желтухой, дополнительно выполняют холангиографию с целью оценить прорастание опухоли в печень и желчные пути.37 Магнитно-резонансная холангиография (МРХГ) представляет собой неинвазивный метод исследования и считается более безопасной альтернативой прямой холангиографии. Иными словами, этот метод исследования предпочтительнее ЭРХПГ или ЧЧХ, за исключением случаев, когда планируется лечебное вмешательство. Роль ПЭТ в обследовании больных с холангиокарциномой не установлена, однако растет число наблюдений, свидетельствующих о ценности этого метода как средства выявления вовлеченности лимфоузлов и отдаленных метастазов у больных с потенциально резектабельной опухолью по остальным параметрам.181,182,202,203
Патоморфология и классификация по стадиям
Более 90% холангиокарцином относятся к аденокарциномам.204 В зависимости от макроскопической картины холангиокарциномы можно разделить на три типа: массивная, околопротоковая и внутрипротоковая.193,205
AJCC разработал классификации холангиокарцином по стадиям (табл. 1 и 3). Классификация внутрипеченочных холангиокарцином аналогична классификации ГЦР (табл. 1). Она не предусматривает прогностических клинико-патологических показателей, специфичных для внутрипеченочной холангиокарциномы.37 Используются также другие, более практичные классификации внутрипеченочной холангиокариномы.206,207 Классификация по стадиям внепеченочной холангиокарциномы, разработанная AJCC (см. табл. 3), основана на патоморфологических критериях, однако непригодна для определения резектабельности опухоли или прогнозирования исхода.33 Jarnagin et al. разработали практически приемлемую систему определения стадии до операции для холангиокарциномы в области слияния правого и левого печеночных протоков. Эта классификация позволяет прогнозировать резектабельность опухоли, вероятность появления метастазов и продолжительность жизни.208
Лечение холангиокарциномы
Внутрипеченочная холангиокарцинома
Единственный потенциально радикальный метод лечения больных с внутрипеченочной холангиокарциномой - полная резекция, однако большинство больных неоперабельны, поскольку этот рак обычно выявляют на поздней стадии. В ходе операции удаляют пораженную долю печени или сегмент вдоль желчного протока, в котором растет опухоль.209 Резектабельность опухоли и наличие метастазов устанавливают, исходя из стадии заболевания. Для этого можно использовать диагностическую лапароскопию. Имеются доказательства того, что резекция R0 связана со значительно более высокой выживаемостью больных, оперированных по поводу внутрипеченочной холангиокарциномы.210 5-летняя выживаемость, по данным публикаций, составляет от 20 до 43%.210-214
Оптимальная стратегия лечения больных с удаленной внутрипеченочной холангиокарциномой не установлена. Пациентов, которым выполнена полная резекция (отрицательный хирургический край) с или без абляции, можно только наблюдать. В условиях клинического исследования можно использовать адъювантную химиотерапию.
В случае положительного края резекции (R1) либо остаточной опухоли (R2) дальнейшую тактику лечения определяют индивидуально после обследования различными специалистами. Оптимальная стратегия лечения не определена, однако возможны следующие варианты:
1) дополнительная резекция; 2) абляционная терапия; 3) химиолучевая терапия с фторпиримидином; 4) химиотерапия на основе фторпиримидина либо гемцитабина (см. ВнуХК-2 и разд. «Химиолучевая и химиотерапия рака желчного пузыря и холангиокарциномы»).
Возможные варианты лечения больных с нерезектабельной опухолью:
1) клиническое исследование; 2) химиотерапия на основе фторпиримидина или гемцитабина; 3) химиолучевая терапия с фторпиримидином; 4) симптоматическое лечение (см. ВнуХК-1). Варианты основного лечения больных с метастазами аналогичны вышеописанным, за исключением химиолучевой терапии (см. разд. «Химиолучевая и химиотерапия рака желчного пузыря и холангиокарциномы»).
Внепеченочная холангиокарцинома
Основной метод радикального лечения больных с внепеченочной холангиокарциномой - полная резекция. Хирургическое лечение пациентов с резектабельной опухолью направлено на удаление части внепеченочных желчных протоков, в которых находится опухоль. Больным с опухолями, расположенными в проксимальной трети внепеченочного билиарного дерева, выполняют резекцию ворот печени с лимфаденэктомией и резекцией печени единым блоком.
При этом настоятельно рекомендуется резекция хвостатой доли печени. Рекомендация по поводу резекции печени подтверждается результатами ретроспективных анализов, согласно которым между частичной гепатэктомией и улучшением исходов имеется взаимосвязь.208,215 Поскольку данная связь сохранялась только при включении в анализ больных, у которых достигнута резекция R0, ее нельзя приписывать исключительно повышенной вероятности резекции R0 при выполнении сопутствующей частичной гепатэктомии. Для больных с опухолью в дистальной трети внепеченочного билиарного дерева рекомендуется панкреатикодуоденэктомия с лимфаденэктомией.178 В очень редких случаях, когда у пациента имеется небольшая опухоль в средней трети билиарного дерева, можно выполнить изолированную резекцию желчного протока с лимфаденэктомией. 5-летняя выживаемость больных после лечения по поводу холангиокарциномы в области слияния правого и левого печеночных протоков составляет от 20 до 40 %,208,216,217 после лечения по поводу рака дистальной трети внепеченочного билиарного дерева - 37 %.193
Резектабельность опухоли определяют на основе стадии заболевания. Для этого проводят диагностическую лапаротомию или лапароскопию. Члены рабочей группы пришли к взаимному соглашению о том, что при высокой степени уверенности в диагнозе рака операцию можно выполнять без биопсии. При необходимости перед операцией рекомендуется наладить дренирование желчных протоков, хотя такая тактика вызывает много споров относительно соотношения ее риска и пользы.218,219 Предоперационное дренирование желчных протоков осуществляется путем ЭРХПГ либо ЧЧХ.
В случае отрицательного хирургического края резекции (R0) и отсутствия метастазов в регионарных лимфоузлах больного можно просто наблюдать либо назначить химиолучевую терапию с фторпиримидином или химиотерапию с фторпиримидином или гемцитабином. Алгоритмы химиолучевой и химиотерапии в настоящее время не разработаны из-за отсутствия достаточного объема данных клинических исследований. Больному рекомендуется участие в клиническом исследовании. Если после резекции установлен положительный край резекции (R1) либо выявлена остаточная опухоль (R2), рак in situ, метастазы в регионарных лимфоузлах, дальнейшую тактику выбирают после комплексного обследования больного различными специалистами. Оптимальная стратегия лечения пока не разработана. Возможные варианты:
1) химиолучевая терапия с фторпиримидином (брахитерапия или дистанционное облучение) с последующей дополнительной химиотерапией с фторпиримидином или гемцитабином; 2) для больных с метастазами в регионарных лимфоузлах - химиотерапия на основе фторпиримидина или гемцитабина (см. ВнеХК-2). В настоящее время недостаточно данных, позволяющих говорить о преимуществе конкретных режимов химиолучевой или химиотерапии (см. разд. «Химиолучевая и химиотерапия рака желчного пузыря и холангиокарциномы»).
Второй потенциально радикальный вариант лечения больных с внепеченочной холангиокарциномой - трансплантация печени.220,221 Она рекомендуется тщательно отобранным пациентам либо с нерезектабельной опухолью и сохранной функцией печени и желчевыведения, либо с хроническим заболеванием печени, препятствующим проведению операции. Результаты одного ретроспективного исследования свидетельствуют о значительно большей общей выживаемости больных с холангиокарциномой, которым выполнена трансплантация печени с предоперационной химиолучевой терапией, по сравнению с больными, которым выполняли резекцию.222 В то же время следует отметить, что характеристики пациентов в этих двух группах лечения существенно отличались. Рабочая группа рекомендует продолжать клинические исследования в этой области.
При необходимости исследовать отдаленные образования либо если больному показано паллиативное лечение, выполняют ЭРХПГ, которая позволяет осмотреть проток и наладить шунтирование в случае непроходимости. Кроме того, с внутренней поверхности протока можно взять щеточный биоптат. Образования в области ворот печени можно визуализировать путем ЧЧХ. Эндоскопическое УЗИ позволяет исследовать дистальный отрезок общего желчного протока, выявить в нем опухоль в виде объемного образования либо патологического утолщения. Этот метод можно применять для прицельной биопсии. Прямая визуализация протока с прицельной биопсией - идеальный метод диагностики холангиокарциномы.
Больным с нерезектабельным раком налаживают дренирование желчных протоков либо путем обходного анастомоза, либо эндоскопически (ЭРХПГ) или чрескожно (ЧЧХ), чаще всего с установкой стента.178,223-225 Перед тем как приступать к лечению, рекомендуется выполнить биопсию. К дополнительным вариантам лечения относятся:
1) клиническое исследование; 2) химиолучевая терапия с фторпиримидином; 3) химиотерапия на основе фторпиримидина либо гемцитабина; 4) симптоматическое лечение (см. ВнеХК-1). Данных, позволяющих предложить определенный режим химиолучевой либо химиотерапии, недостаточно (см. разд. «Химиолучевая и химиотерапия рака желчного пузыря и холангиокарциномы»).
Больным с метастазами рекомендуется наладить дренирование желчных протоков путем установки стента эндоскопически либо чрескожным доступом. Перед тем как приступить к лечению, для подтверждения диагноза рекомендуется провести биопсию. К дополнительным методам лечения относят клиническое исследование, симптоматическое лечение, химиотерапию на основе фторпиримидина или гемцитабина (см. ВнеХК-1). Данных, позволяющих предложить определенный режим химиолучевой либо химиотерапии, недостаточно (см. разд. «Химиолучевая и химиотерапия рака желчного пузыря и холангиокарциномы»).
Фотодинамическая терапия - относительно новый метод местного лечения холангиокарциномы. Принцип этого абляционного метода состоит во внутривенном введении фотосенсибилизатора с последующим избирательным облучением светом с определенной длиной волны, активирующего этот препарат. Метод применяют с паллиативной целью.226,227 В ходе двух небольших рандомизированных клинических исследований установлено, что комбинация фотодинамической терапии со стентированием желчного протока увеличивает общую выживаемость больных с нерезектабельной холангиокарциномой.228,229
Наблюдение
Данных, свидетельствующих о необходимости активного наблюдения за больными, которым выполнена резекция по поводу холангиокарциномы, нет. Планирование обследования пациента, в т. ч. с применением методов визуализации, определяется врачом после обсуждения с пациентом. Больных рекомендуется обследовать с применением методов визуализации каждые 6 мес. на протяжении 2 лет. В случае прогрессирования заболевания проводят повторное обследование по программе первичного (см. ВнуХК-2; ВнуХК-2).
Химиолучевая и химиотерапия при лечении рака желчного пузыря и холангиокарциномы
Учитывая низкую заболеваемость раком билиарной системы (т. е. раком желчного пузыря и холангиокарциномой), большинство работ, посвященных оценке эффективности и безопасности химиотерапии или ее сочетания с лучевой терапией, за небольшим исключением, представляют собой одноцентровые исследования II фазы. Большинство этих исследований нерандомизированные, часто с участием больных с раком желчного пузыря, внутри- и внепеченочной холангиокарциномой; количество участников небольшое, что в совокупности не позволяет сделать определенные выводы. Некоторые рекомендации, включенные в настоящее руководство, особенно касающиеся химиолучевой терапии, основаны главным образом на практическом опыте организаций, входящих в NCCN, и ретроспективных анализах одноцентровых наблюдений. Несмотря на то что для участия в рандомизированных исследованиях III фазы набрать большое число пациентов с раком билиарной системы очень трудно, подобные исследования следует проводить, причем с отдельной оценкой опухолей различных локализаций.230 В связи с отсутствием достаточного объема данных и разнородности популяций больных, участвовавших во многих из опубликованных исследований, большинство рекомендаций по применению химиотерапии либо химиолучевой терапии дано без учета специфики определенного типа рака билиарной системы.
Химиотерапия и химиолучевая терапия как варианты адъювантной терапии
Место адъювантной химиотерапии/химиолучевой терапии у больных после резекции рака билиарной системы практически не выяснено. Согласно данным недавно проведенного ретроспективного анализа лечения больных раком желчных путей в одном учреждении с 1995 по 2005 г., установлено, что адъювантную химиотерапию получало 6,5% пациентов, такое же количество больных получали адъювантную химиолучевую терапию и адъювантную химиолучевую в сочетании с химиотерапией.183 В ходе другого ретроспективного анализа базы данных SEER (течение, распространение и исходы злокачественных новообразований) установлено, что за период с 1992 по 2002 г. среди больных раком желчного пузыря 17% из 2325 пациентов из группы хирургического лечения получали адъювантную химиолучевую терапию.231
Исследования адъювантной химиотерапии у больных с раком билиарной системы единичны, поэтому накоплено недостаточно данных клинических исследований, чтобы определить стандартную схему адъювантной химиотерапии или утверждать о ее эффективности. Результаты двух больших ретроспективных анализов пациентов с раком билиарной системы не выявили пользы от применения одной только адъювантной химиотерапии.183,232 Следует отметить, что такое лечение получало очень мало больных,183 а в последнем исследовании, охватившем период с 1988 по 1997 г., новые химиопрепараты не применялись.194 В ходе одного исследования III фазы оценивали эффективность адъювантной химиотерапии у больных после резекции рака панкреатобилиарной зоны.233 Примерно у 50% больных, включенных в это исследование, были рак желчного пузыря либо холангиокарцинома. Пациентов рандомизировали в группы адъювантной химиотерапии с 5-фторурацилом (5-ФУ)/митомицином С и в контрольную группу. Результаты подгруппового анализа свидетельствовали о статистически значимо большей 5-летней выживаемости больных раком желчного пузыря из группы химиотерапии. Следует отметить, что при сравнении подгрупп больных раком билиарной системы статистически значимых различий между двумя группами не установлено. Ретроспективный анализ данных 177 пациентов, перенесших резекцию по поводу рака билиарной системы, показал, что первичный рецидив в виде отдаленных метастазов наблюдался у 85% больных раком желчного пузыря и у 41% - с холангиокарциномой в области ворот печени. Это подтверждает необходимость активной адъювантной системной терапии больных раком желчного пузыря.184 Учитывая недостаточный объем данных, касающихся использования адъювантной химиотерапии, приведенные здесь рекомендации по поводу химиотерапии на основе фторпиримидина или гемцитабина представляют главным образом экстраполяцию результатов исследований больных с поздней стадией рака (см. РЖП-3; ВнуХК-2; ВнеХК-2).
Основная сложность радикального лечения больных раком билиарной системы после операции - местные рецидивы, что также подтверждает необходимость адъювантной лучевой терапии. Опубликованы ценные обзоры результатов применения лучевой терапии у больных раком билиарной системы со ссылками на ряд исследований, относящихся к данному вопросу.234-236 Согласно результатам ретроспективного анализа 2325 пациентов из базы данных SEER, перенесших операцию по поводу рака желчного пузыря в период с 1992 по 2002 г., медиана продолжительности жизни в группе адъювантной химиотерапии составила 14 мес., в группе без адъювантной химиолучевой терапии - 8 мес. (p<0,0001). Еще большее различие в продолжительности жизни больных, получавших адъювантную химиолучевую терапию (16 vs 5 мес., p<0,0001), установлено при сравнении группы больных с метастазами в регионарных лимфоузлах.231 Ретроспективный анализ одноцентровых наблюдений, касающихся пациентов, перенесших резекцию по поводу внепеченочной холангиокарциномы и получавших химиолучевую терапию с фторпиримидином, также свидетельствует о том, что применение химиолучевой терапии более эффективно предотвращает местные рецидивы. В то же время следует отметить высокую частоту рецидивов в виде отдаленных метастазов.237,238 Результаты одного из последних популяционных анализов больных с локорегионарной внепеченочной холангиокарциномой, включенных в базу данных SEER, охватывающую период с 1973 по 2005 гг., свидетельствуют о том, что если адъювантная лучевая терапия сопровождалась начальным повышением продолжительности жизни в течение 1-2 лет после операции, то при долгосрочном наблюдении (т. е. >5 лет) этот эффект отсутствовал.239
Многофакторная модель пропорциональных рисков Кокса, разработанная с целью индивидуального прогнозирования продолжительности жизни в зависимости от применения лучевой терапии после резекции по поводу рака желчного пузыря, показала, что максимальная польза лучевой терапии наблюдалась у больных с опухолью на стадии Т2 или выше и метастазами в регионарных лимфоузлах.240 Результаты этих исследований свидетельствуют о нецелесообразности адъювантной химиолучевой терапии в послеоперационном лечении больных с раком желчного пузыря стадии Т1Ь, N0 (см. РЖП-3).
Определенные свидетельства в пользу адъювантной химиотерапии у больных с внутрипеченочной холангиокарциномой получены в результате ретроспективного анализа базы данных SEER.241 В этом исследовании установлено статистически значимое увеличение общей продолжительности жизни, если хирургическое лечение дополняли химиолучевой терапией (p=0,014). Результаты одного ретроспективного анализа пациентов с внепеченочной холангиокарциномой свидетельствуют об отсутствии статистически значимых различий в продолжительности жизни больных с отрицательным хирургическим краем после операции, которые не получали адъювантную терапию, по сравнению с больными с положительным хирургическим краем, которые получали химиолучевую терапию. Эти результаты свидетельствуют о том, что применение химиолучевой терапии во второй группе позволяет повысить продолжительность жизни.242 Результаты другого ретроспективного анализа больных с внепеченочной холангиокарциномой показали, что добавление поддерживающей химиотерапии вслед за адъювантной химиолучевой терапией повышает продолжительность жизни (3-летняя общая выживаемость в группе с поддерживающей химиотерапией составила 75,6 vs 34,8 % в группе без нее; p = 0,001).243 Эти результаты свидетельствуют в пользу рекомендации дополнять химиолучевую терапию с фторпиримидином химиотерапией с фторпиримидином или гемцитабином у больных с внепеченочной холангиокарциномой как с положительным хирургическим краем, так и с метастазами в регионарных лимфоузлах (см. ВНеХК-2).
Накопленный опыт химиолучевой терапии рака билиарной системы в основном касается одновременного применения химиолучевой терапии и 5-ФУ.234,235 Относительно недавно исследовали эффективность одновременной химиолучевой терапии с капецитабином.242,244 Применять одновременную химиолучевую терапию с гемцитабином не рекомендуется, поскольку отсутствует опыт такого лечения и неизвестны его побочные эффекты.245
Химиотерапия и химиолучевая терапия у больных с поздней стадией рака
Прогноз для больных с поздней стадией рака билиарной системы неблагоприятный. Медиана продолжительности жизни больных, получающих только симптоматическое лечение, небольшая.246 После публикации результатов одного из последних исследований III фазы с участием больных с поздней стадией рака билиарной системы или его метастазами комбинация гемцитабин/цисплатин в этой популяции больных рассматривается как стандарт лечения и химотерапия первой линии.247 В ходе исследования установлено, что продолжительность жизни больных, получавших комбинацию гемцитабин/цисплатин была значительно выше по сравнению с больными, получавшими только гемцитабин. (Подробности этого исследования описаны далее.) В последнем опубликованном обзоре проанализированы результаты многих исследований, касающихся данного вопроса.230
Сравнение режима комбинированной химиотерапии с 5-ФУ/лейковорином/этопозидом с симптоматической терапией свидетельствует в пользу химиотерапии больных с поздней стадией рака билиарной системы.248 В последующем выполнено исследование III фазы с участием больных с поздней стадией рака билиарной системы. Участников рандомизировали в группы лечения 5-ФУ/лейковорин/ этопозид либо 5-ФУ/цисплатин/эпирубицин. Результаты исследования не выявили преимуществ одного режима перед другим в плане общей выживаемости (12,03 vs 9,02 мес. соответственно). Следует отметить, что статистическая мощность исследования не позволяла выявить подобное различие.249
Больные с поздней стадией рака билиарной системы участвовали в клинических исследованиях с изучением ряда других химиотерапевтических комбинаций, а также монотерапии.230 (См. Hezel and Zhu230 и ссылки в этой публикации.) В исследованиях II фазы установлена эффективность следующих комбинаций в лечении больных с поздней стадией рака билиарной системы: гемцитабин/цисплатин,250-254 гемцитабин/капецитабин,255,256 гемцитабин /оксалиплатин,257,258 капецитабин/оксалиплатин,259 капецитабин/цисплатин,250 5-ФУ/цисплатин260 и др. Результаты недавно выполненного объединенного анализа данных 104 исследований с участием больных с поздней стадией рака билиарной системы свидетельствуют о том, что наибольшая эффективность химиотерапии наблюдалась в подгруппе пациентов, получавших комбинацию гемцитабина и платиносодержащего препарата.261 В пользу гемцитабина как основного препарата для лечения поздней стадии рака билиарной системы свидетельствуют результаты ретроспективного анализа данных 304 больных, получавших химиотерапию на основе гемцитабина, цисплатина либо фторпиримидина.262 В этом исследовании установлено, что у пациентов, получавших химиотерапию на основе гемцитабина, риск смерти был меньше. Наиболее важно, что недавно опубликованное рандомизированное контролируемое исследование АВС-02 III фазы, в котором участвовало 410 пациентов с местнораспространенной или метастазирующей формой холангиокарциномы, рака желчного пузыря или ампулярного рака, показало, что комбинация гемцитабина и цисплатина повышает общую выживаемость и выживаемость без прогрессирования на 30% по сравнению с монотерапией гемцитабином.247 Медиана общей выживаемсоти составила 11,7 и 8,1 мес. (отношение рисков 0,64; 95% ДИ 0,52-0,80; p<0,001), медиана выживаемости без прогрессирования - 8,0 и 5,0 мес. (отношение рисков 0,63; 95% ДИ 0,51-0,77; p<0,001), в обоих случаях соотношение в пользу комбинированной терапии. Хотя частота нейтропении была выше в группе гемцитабина/цисплатина, статистически значимой разницы в частоте связанных с нейтропенией инфекций между группами не было.218
Учитывая результаты исследований II фазы и рандомизированного исследования III фазы АВС-02, для лечения больных с поздней стадией рака билиарной системы рекомендуются следующие варианты химиотерапии на основе гемцитабина и фторпиримидина: комбинации гемцитабин/цисплатин; гемцитабин/ оксалиплатин; гемцитабин/ капецитабин; капецитабин/цисплатин; капецитабин/ оксалиплатин; 5-ФУ/цисплатин и 5-ФУ/оксалиплатин, а также монотерапия 5-ФУ, капецитабином и гемцитабином. Комбинация гемцитабин/5-ФУ не включена в этот перечень вследствие повышенной частоты побочных эффектов и низкой эффективности, о чем свидетельствуют результаты сравнения режимов на основе гемцитабина /капецитабина при лечении больных с поздней стадией рака билиарной системы.230
Химиолучевая терапия больных с поздней стадией рака билиарной системы предотвращает прогрессирование симптомов заболевания вследствие стабилизации роста опухоли и способствует увеличению общей выживаемости, хотя имеющихся данных клинических исследований недостаточно, чтобы предложить алгоритм химиолучевой терапии либо считать доказанной эффективность этого варианта. Опубликованы ценные обзоры результатов применения лучевой терапии у больных раком билиарной системы со ссылками на ряд исследований, относящихся к данному вопросу.234,235 Согласно результатам одного ретроспективного анализа, у 37 пациентов с неоперабельной внепеченочной холангиокарциномой, получавших химиолучевую терапию, вероятностная общая выживаемость через 1 и 2 года составила соответственно 59 и 22%. В этот период времени у большинства больных отмечалось отсутствие роста опухоли (вероятностная частота отсутствия прогрессирования через 1 и 2 года составила соответственно 90 и 61%).264 Наиболее интенсивно в качестве средства сопутствующей химиолучевой терапии у больных раком билиарной системы исследовали 5-ФУ.234,235 Следует отметить, что в некоторых исследованиях 5-ФУ меняли на капецитабин.244 Рабочая группа рекомендует в качестве средства химиотерапии, назначаемого одновременно с лучевой терапией, использовать 5-ФУ либо капецитабин. Это лечение следует назначать только больным без метастазов. Применять одновременную химиолучевую терапию с гемцитабином не рекомендуется, поскольку отсутствует опыт такого лечения и неизвестны его побочные эффекты.
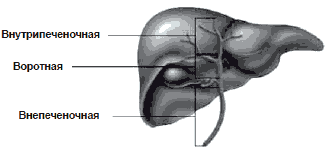
Публикуется с разрешения из: Patel T. Cholangiocarcinoma. Nat Clin Pract Gastroenterol Hepatol. 2006;3:33-42.
Заключение
Несмотря на то что у многих больных рак гепатобилиарной системы выявляют на поздней стадии, во всех случаях необходимо оценить возможность радикального лечения. Важную роль играет тщательный выбор метода лечения и активное взаимодействие специалистов различного профиля. С участием больных раком гепатобилиарной системы проведено очень мало высококачественных рандомизированных клинических исследований, поэтому наиболее предпочтительный вариант лечения пациентов с любой стадией заболевания - участие в проспективном клиническом исследовании.
Предыдущий раздел | Содержание | Список литературы
Комментарии
ПРАКТИКА ПЕДИАТРА
