Эффективность комбинации различных лекарственных форм кетопрофена лизиновой соли (Артрозилен) у пациентов с выраженной мышечно-скелетной болью в реальной клинической практике. Результаты исследования КУЛОН
СтатьиОпубликовано в журнале "Клиническая фармакология и терапия", 2013.-N 4.-С.23-30
Каратеев А.Е., Журавлева М.В., Алексеев В.В., Денисов Л.Н., Цапина Т.Н.
Острая боль, возникающая на фоне патологии опорно-двигательного аппарата – одна из наиболее частых причин потери трудоспособности и обращения за медицинской помощью. Поэтому эффективное обезболивание традиционно считается одной из первоочередных задач, стоящих перед лечащим врачом. Значение анальгетической терапии определяется не только очевидной необходимостью наиболее полно и быстро устранить симптом, вызывающий основные страдания больного. В последние годы врачи пришли к четкому пониманию того факта, что купирование острой боли играет ключевую роль в предупреждении развития хронической боли. Это принципиально важно, ведь хроническая мышечно-скелетная боль рассматривается сегодня как самостоятельный клинический синдром, который не только выступает в числе главных причин инвалидизации, но и является фактором, существенно влияющим на продолжительность жизни пациентов [1-3].
Одним из главных инструментов контроля мышечно-скелетной боли являются нестероидные противовоспалительные препараты (НПВП). Эти лекарства сочетают в себе обезболивающий, противовоспалительный и жаропонижающий потенциал, что обеспечивает их преимущество в сравнении с другими анальгетиками – парацетамолом и опиоидами, в частности, трамадолом [4,5].
Хотя НПВП достаточно эффективны, тем не менее, существенное улучшение при их использовании отмечается далеко не у всех пациентов. Нюансы фармакокинетики конкретных препаратов, индивидуальные особенности клинической ситуации и пациента (включая такие «тонкие материи» как генетические особенности метаболизма ксенобиотиков и психологический настой в момент назначения терапии) могут существенно повлиять на достижение терапевтического успеха. Поэтому перед практикующим врачом часто оказывается проблема выбора препарата для дебюта анальгетической терапии, а также подбора альтернативного средства в том случае, если после первого назначения не удалось достичь существенного улучшения состояния.
Одним из представителей группы НПВП, который отлично подходит в качестве средства «первой линии» для купирования острой боли, а также для замены оказавшегося малоэффективным препарата, может считаться кетопрофен. Этот препарат используется в мире с 1971 г. и завоевал доверие врачей как эффективный и удобный анальгетик, обладающий хорошей переносимостью. Он прошел серьезную проверку в ходе большого числа клинических испытаний при самых разных заболеваниях, сопровождающихся выраженной болью – начиная от анестезиологической практики и заканчивая системными ревматическими заболеваниями [6,7].
Особый интерес представляет «улучшенный» кетопрофен – кетопрофен лизиновая соль (КЛС), которая обладает высокой биодоступностью и устойчивой фармакодинамикой. Эффективная концентрация препарата к плазме крови достигается уже через 15-20 мин. после перорального приема и 10-15 минут – после в/м введения. Малый размер и липофильность молекулы КЛС определяет хорошую абсорбцию при накожном нанесении – поэтому он является весьма удачной субстанцией для производства локальных форм НПВП.
КЛС представлен на российском рынке препаратом Артрозилен®, причем в распоряжении врачей имеется вся «линейка» его лекарственных форм: раствор для в/м и в/в введения, капсулы 320 мг контролируемого высвобождения (для приема1 раз в сутки), ректальные свечи, а также высокодозный гель и спрей для накожного несения. Такое разнообразие позволяет практикующему врачу подбирать индивидуальную схему применения КЛС в зависимости от особенностей пациента и клинической ситуации.
Для оценки терапевтических возможностей Артрозилена® было проведено исследование КУЛОН.
Цель исследования: оценить результаты комбинированного и/или последовательного применения различных лекарственных форм КЛС у больных с выраженной мышечно-скелетной болью в реальной клинической практике.
План исследования: Участниками исследования были врачи различных специальностей, проводящие поликлинический прием и занимающиеся в своей повседневной практике лечением пациентов, испытывающих мышечно-скелетные боли: терапевты, неврологи, травматологи, ревматологи. Всего приняло участие 115 врачей из городов: Москвы, Санкт-Петербурга, Воронежа, Липецка, Саратова, Тольятти, Белгорода, Курска, Новосибирска, Красноярска, Волгограда, Ростова, Краснодара, Н.Новгород.
Им предлагалось в течение календарного месяца проводить ретроспективный анализ результатов 2-х недельного применения КЛС у больных, обратившихся с жалобами на выраженные боли (не менее 40 мм по 100 мм визуальной аналоговой шкале – ВАШ), связанные с острой или хронической патологией опорно-двигательного аппарата. Необходимость назначения КЛС, а также лекарственная форма препарата (или их комбинация) определялись лечащим врачом по собственному усмотрению, в зависимости от клинической ситуации. Все данные вносились в специально разработанные анонимные исследовательские карты, которые затем были собраны организаторами исследования для проведения соответствующего анализа.
Исследуемая группа: Исследуемую группу составили 3349 больных, 2157 (64.4%) женщин и 1192 (35.6%) мужчин, средний возраст 50.2 + 12.9, обратившихся к поликлиническим врачам с жалобами на выраженные боли, связанные с патологией органов опорно-двигательного аппарата. Выраженность боль исходно составила в среднем 66.2 + 16.6, ухудшения самочувствия - 58.1 + 21.1.
Патология, ставшая причиной обращения к врачам, представлена в таблице 1. Как видно, подавляющее большинство пациентов страдали от боли в различных отдела спины («дорсопатия») – всего 1601 пациент (47.8%). Учитывая неоправданное разнообразие диагнозов, используемых в нашей стране для обозначения этой патологии (основным из которых оставался архаичный «остеохондроз»), в таблице приведена лишь основная локализация боли – соответственно, в шейном, грудном или поясничном отделе. Детальное же рассмотрение формулировок, используемых российскими врачами для обозначения «дорсопатий» представляет большой интерес и будет представлено нами в отдельной работе.
Таблица 1.
Заболевания и патологические состояния, ставшие причиной обращения к врачу в поликлинике
| Группы | Число больных | Основные заболевания | Число больных |
|---|---|---|---|
| Воспалительные ревматологические заболевания | 203 | Ревматоидный артрит | 125 |
| Подагра | 46 | ||
| Серонегативные спондилоартриты, включая АС и ПсА | 22 | ||
| Реактивный артрит | 10 | ||
| Остеоартроз | 1008 | Полиартроз | 348 |
| Коксартроз | 140 | ||
| Гонартроз | 401 | ||
| Плечевые суставы | 18 | ||
| Кисти | 24 | ||
| Локти | 8 | ||
| Стопы | 24 | ||
| Не уточнен | 45 | ||
| Дорсопатия | 1601 | Боль в шейном отделе позвоночника | 381 |
| Боль в грудном отделе позвоночника | 66 | ||
| Боль в поясничном отделе позвоночника | 1254 | ||
| Не уточнен | 214 | ||
| Острые травмы | Переломы костей, ушибы, растяжения связок и мышц | 101 | |
| Воспаление околосуставных мягких тканей ревматической природы | 156 | Плечелопаточный периартрит | 73 |
| Тендиниты | 22 | ||
| Бурсит локтя | 5 | ||
| Субакромиальный бурсит | 5 | ||
| Эпикондилит | 23 | ||
| «Периартрит» | 22 | ||
| Пяточная шпора | 3 | ||
| Трохантерит | 3 | ||
| Неуточненный моно- олигоартрит | 53 | ||
| Редкие диагнозы | 13 | Метастазы рака (1), ОРЛ (1),СКВ (1), узловатая эритема (3), трофические язвы (4), карбункул шеи (1), «хроническая головная боль» (1), фибромиалгия (1) | |
На втором месте по частоте обращения находится остеоартроз – 1008 пациентов (30.1%), причем наибольшее число из них составили лица, страдающие поражением крупных суставов нижних конечностей – гонартрозом и коксартрозом, а также поражением суставов нескольких групп («полиартроз»).
Третью по численности группу пациентов представляли лица, страдающие воспалительными ревматическими заболеваниями (n=203), преимущественно ревматоидным артритом и подагрой.
Меньшее число составили пациенты с острым воспалением околосуставных мягких тканей ревматической природы (тендиниты, тендовагиниты, бурситы и др.), n=156, острыми травмами (переломы, ушибы мягких тканей, повреждение связок и др.), n=101 и моно/ олигоартритом неясной этиологии (n=53).
Более трети пациентов (n=1380, 41.2%) на момент назначения артрозилена уже получали другие НПВП, в основном нимесулид (n=412, 35.3%), диклофенак (n=304, 22.0%) и мелоксикам (n=248, 17.9%). Однако это практически не влияло на выраженность боли и ухудшения самочувствия. Так, при первом визите, у больных, принимавших НПВП, оценка этих параметров составила 67.5 + 17.6 и 59.1 + 21.8 мм ВАШ соответственно, у не принимавших – 65.6 + 16.2 и 57.4 + 20.9 мм ВАШ соответственно.
Кроме НПВП, 555 (16,6%) больных на момент начала исследования принимали различные миорелаксанты: 274 (49.4%) толперизон, 208 (37.5%) тизанидин и 73 (13.8%) баклофен. Другие лекарства, применяемые включенными в исследования больными, представлены в таблице 2.
Таблица 2.
Сопутствующая терапия, получаемая больными
| Группы | Препараты | Число больных |
|---|---|---|
| Базисные противовоспалительные препараты | метотрексат | 41 |
| сульфасалазин | 12 | |
| лефлюнамид | 7 | |
| Генно-инженерные биологические препараты | Инфликсимаб - 2, адалимумаб - 1, абатасепт - 1, ритуксимаб - 1 | |
| Глюкокортикоиды | Преднизолон, метипред – 5 | |
| Медленно действующие симптоматические средства | Пиаскледин | 42 |
| Дона | 33 | |
| Артра | 38 | |
| Структум | 24 | |
| Терафлекс | 37 | |
| Иные препараты, применяемые при ОА | Альфлутоп | 46 |
| Хондроксид | 45 | |
| Артрофоон | 8 | |
| Иные препараты, применяемые при лечении дорсопатии | Мильгамма | 347 |
| Флупиртин | 49 | |
| Пентоксифиллин | 77 | |
| Антигипертензивные препараты | 155 | |
| Гастропротекторы | Омепразол – 36 , ранитидин – 8 | |
Все больные, включенные в исследование, получали КЛС в виде различных лекарственных форм и их комбинации (рисунок 1).
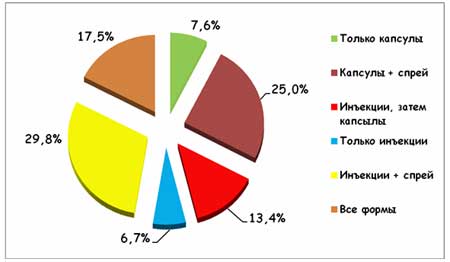
Рисунок 1. Различные лекарственные формы и их сочетания,
использованные в исследовании КУЛОН
В работе были использованы Артрозилен® 320 мг (капсулы с контролируемым высвобождением КЛС), р-р для парентерального введения 80 мг/мл и 15% спрей КЛС. Как видно, большинство предпочитали назначать инъекционные препараты в сочетании с другими лекарственными формами или использовать последовательное назначение – в первые 3 дня в/м инъекции, а затем переходить на капсулы. Кроме этого, у небольшой части больных (в основном при острых травмах и остром воспалении мягких тканей ревматической природы) врачи посчитали возможным ограничиться лишь кратковременным курсом парентерального введения артрозилена.
Критериями оценки эффективности терапии была динамика выраженности боли и самочувствия, выраженных в мм по ВАШ. Также оценивалась субъективная удовлетворенность результатами лечения по 6-ти бальной шкале, в которой цифра «5» соответствовала отличному действию препарата, а «0» - ухудшению состояния. Кроме этого, изучалась переносимость препарата – число и характер побочных эффектов, прежде всего со стороны желудочно-кишечного тракта (ЖКТ).
Электронная база данных была создана с помощью программы Microsoft Office Excel 2007, статистический анализ проводился с помощью программы SPSS 10.0. Средние значения даны в формате M + m. Для оценки статистической значимости отличия количественных параметров был использован t-тест Стъюдента, качественные параметры сравнивались с помощью показателя χ2 или точного теста Фишера.
Результаты:
Большинство больных после проведенного курса лечения отметило существенное улучшение состояния. Так, средняя оценка боли в конце исследования составили 15.3 + 13.6 мм, а нарушения самочувствия 12.2 + 12.4, т.е. их значение уменьшилось на 76.9% и 79.0% по сравнению с исходным уровнем (р 40 мм). Как видно, почти у половины больных было достигнуто практически полное купирование боли. Лишь у 27.7% больных после использования артрозилена сохранялись выраженные болевые ощущения.
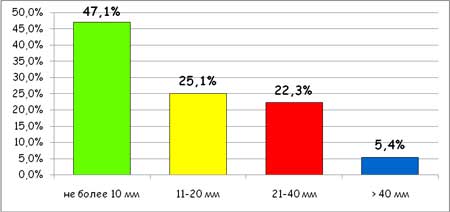
Рисунок 2. Выраженность боли в конце периода наблюдения
Эффективность КЛС подтверждается субъективной оценкой удовлетворенности проведенным лечением (рис.3). Подавляющее большинство больных (суммарно 87%) оценили результат применения артрозилена как «отличный» или «хороший».
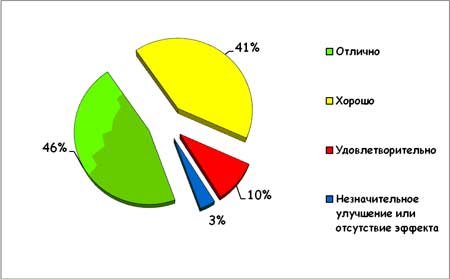
Рисунок 3. Субъективная оценка эффективности лечения
Проведенный анализ показал, что эффективность артрозилена различалась при использовании разных форм препарата и их комбинаций (таблица 3). Так, наилучшим образом «работала» схема, при которой дебютом лечения было в/м введение препарата, а затем, после получения быстрого облегчения боли, прием препарата продолжался перорально. В этой подгруппе большинство больных оценили эффективность артрозилена как «отличную».
Таблица 3. Зависимость эффективности от формы препарата
| Форма препарата | Оценка эффекта терапии (% от общего числа больных) | |||
|---|---|---|---|---|
| «Отличный» | «Хороший» | «Умеренный» | «Низкий или отсутствует» | |
| Только капсулы | 39.2 | 40.5 | 16.8 | 3.5 |
| Капсулы и спрей | 39.1 | 47.5 | 11.0 | 2.4 |
| Инъекции и капсулы | 60.4* | 26.4 | 10.1 | 3.1 |
| Только инъекции | 45.1 | 40.4 | 11.2 | 3.3 |
| Инъекции и спрей | 48.1 | 41.7 | 4.1 | 6.1 |
| Все формы | 44.1 | 43.5 | 11.3 | 1.1 |
Следует отметить, что при парентеральном введении лекарства – как в качестве монотерапии, так и в комбинации с другими формами, достигалось большее облегчение боли, чем при его пероральном применении.
Отдельно был рассмотрен вопрос эффективности артрозилена при различных нозологических формах (таб. 4). Наилучшее действие препарата было отмечено у пациентов с острым подагрическим артритом: 67.4% посчитали его «отличным», и – что особенно важно, никто из этих больных не сообщил об отсутствии значимого облегчения боли.
Таблица 4.
Зависимость эффективности от нозологической формы
| Диагноз | Оценка эффекта терапии (% от общего числа больных) | |||
|---|---|---|---|---|
| «Отличный» | «Хороший» | «Умеренный» | «Низкий или отсутствует» | |
| Гонартроз | 27.3* | 51.3 | 16.0 | 5.4 |
| Коксартроз | 27.1* | 42.1 | 26.4 | 4.4 |
| Дорсалгия (поясничный отдел) | 51.0 | 38.7 | 5.7 | 4.6 |
| Дорсалгия (шейный отдел) | 51.8 | 37.9 | 6.1 | 4.2 |
| Дорсалгия (грудной отдел) | 56.3 | 32.8 | 7.8 | 3.1 |
| Ревматическая патология мягких тканей | 54.1 | 35.4 | 7.4 | 3.1 |
| Острая травма | 37.1* | 45.2 | 12.3 | 5.4 |
| Ревматоидный артрит | 44.4 | 52.4 | 2.4 | 0.8 |
| Подагрический артрит | 67.4 | 28.3 | 4.3 | 0 |
| * - Достоверно меньше (р=0.001) в сравнении с дорсалгиями и подагрическим артритом | ||||
Артрозилен оказался весьма эффективным и у пациентов с дорсопатиями и воспалительным поражением мягких тканей воспалительной природы: отличный эффект был отмечен более чем у половины участников исследования (от 51.0% до 56.0%, в зависимости от локализации патологии). Существенно хуже результат терапии оказался у пациентов, страдающих ОА крупных суставов. Хотя при гонартрозе и коксартрозе большинство больных отметили значительное улучшение (суммарно 76.3% и 69.2%), тем не менее «отличную» оценку новому препарату дали лишь чуть более четверти больных, т.е. в 2 раза меньше, чем при дорсопатиях (р Безопасность:
Артрозилен хорошо переносился и достаточно редко вызывал серьезные побочные эффекты. В основном проблемы касались ЖКТ. Так, у 1 больной развилась язва желудка, а у двух пациентов, у которых появились гастралгии, при проведении эндоскопического исследования были выявлены множественные эрозии слизистой желудка. У 15 пациентов возникла выраженная диспепсия (гастралгии, тошнота, тяжесть в эпигастральной области), что потребовало прерывания лечения и назначения противоязвенных средств.
Кардиоваскулярные осложнения практикующие врачи не зафиксировали – лишь у одного пациента на фоне приема артрозилена отмечена стойкая артериальная гипертензия, потребовавшая коррекции антигипертензивной терапии, которую тот ранее получал.
У двух больных были отмечены постинъекционные осложнения (выраженная боль в месте введения препарата), а еще у двух возникла кожная аллергическая реакция.
Такими образом, серьезные побочные эффекты, которые привели к прерыванию лечения, могли представлять угрозу здоровью больных или потребовали назначения специальных средств для их коррекции, были зафиксированы у 23 больных (0.75%).
Слабые или умеренно выраженные гастралгии, изжога, тошнота, чувство тяжести были отмечены у 396 (11.7%) пациентов; у 172 участников исследования развилась диарея (5.1%), у 57 (1.7%) - запоры.
Анализ показал, что появление осложнений существенно влияло на субъективную оценку эффективности лечения. Так, при возникновении диспепсии существенно меньше больных определяли результат использования артрозилена как «отличный», в сравнении с теми, кто не испытывал каких-либо осложнений: 25.8% и 49.1% соответственно (р Обсуждение результатов
Полученные данные показывают, что Артрозилен® - весьма действенный анальгетик, обеспечивающий надежное и быстрое купирование острой боли при различных заболеваниях опорно-двигательной системы. Очень важно, что этот препарат «работал» и в тех случаях, когда другие НПВП (в т.ч. в комбинации с миорелаксантами) оказались недостаточно эффективны.
Подавляющее большинство больных – 87%, отметили значительное улучшение, дав препарату отличную или хорошую оценку. Важно отметить, что субъективный критерий оценки эффективности точно совпадал с более объективным критерием снижения боли (по ВАШ). Так, значительное уменьшение ее выраженности (Артрозилен оказался особенно эффективен у лиц, испытывающих острую боль – при подагрическом артрите, воспалительном поражении мягких тканей и дорсалгии. Хороший, однако не столь яркий результат был получен и у пациентов, испытывающих болевые ощущения в течение длительного времени: в частности, у больных ОА крупных суставов.
Следует отметить, что практика парентерального назначения НПВП в качестве дебюта анальгетической терапии при использовании артрозилена себя полностью оправдала: оценка эффективности была достоверно выше у пациентов, которым этот препарат вначале назначался в/м, а затем осуществлялся переход на пероральный прием и/или использование локальных форм.
Конечно, результаты открытых неконтролируемых исследований, к которым относится КУЛОН, всегда следует трактовать с определенной осторожностью. Очевидно, что надежды, связываемые с появлением нового препарата, в значительной степени влияют на оценку результатов его применения, как со стороны пациентов, так и лечащих врачей – особенно в том случае, когда предыдущие методы терапии не обеспечили существенного улучшения состояния. Именно поэтому эффективность лекарств, оцениваемых в ходе открытых клинических испытаний, всегда существенно выше, чем при проведении «правильных», с точки зрения доказательной медицины исследований – рандомизированных, слепых, плацебо-контролируемых (РКИ).
Следует отметить, что чрезмерно оптимистичные результаты, когда превосходное действие нового препарата отмечается у подавляющего большинства включенных в исследование пациентов, характерны не только для российской научной практики. В качестве примера можно привести работу немецких ученых Zeidler H. и сотр. (2002 г.), которые изучали эффективность и безопасность мелоксикама. Они представили данные открытого исследования, в ходе которого этот препарат был назначен 13307 пациентам с РЗ (в основном - ОА, РА и АС) на срок от 1 до 3 месяцев. Как и в нашей работе, результаты лечения оценивались путем анализа анкет, заполненных практикующими врачами и отосланных по почте организаторам исследования. Согласно полученным данным, «хороший» или «очень хороший» эффект от лечения был отмечен у 85% пациентов. При этом, хотя большинство участников исследования были старше 60 лет, а 12% имели язвенный анамнез, нежелательные эффекты со стороны ЖКТ были отмечены у минимального числа больных - 0.8% (?!), а серьезные ЖКТ - осложнения возникли лишь у 5 (4 неосложненных язвы желудка и 1 перфорация) [8].
Аналогично было спланировано открытое неконтролируемое исследование Lammel E. и сотр (2002 г.). В ходе этой работы 23.407 пациентам (основные диагнозы - РА, ОА, АС, дорсопатии и травмы) из Австрии, Бельгии, Голландии и Греции был назначен относительно новый НПВП ацеклофенак. Важно отметить, что более половины этих больных уже получали различные НПВП (как это было и в нашей работе), но остались недовольны их эффектом.
Продолжительность лечения определялась лечащими врачами, исходя из особенностей клинической ситуации, и в среднем составила 2 недели. В конце периода наблюдения, 85% пациентов определили терапевтическое действие ацеклофенака как «очень хорошее», а 32% сообщили о полном прекращении боли. При этом число пациентов, которые на момент включения в исследование оценивали боль как «тяжелую» сократилось с 41% до 2% [9].
Подобное испытание было проведено и для кетопрофена. В 1989 г. Le Loet X. и сотр. опубликовали результаты европейского открытого исследования, охватившего около 20 тыс. больных с различной мышечно-суставной патологией, в основном ОА (т.е. с хронической болью). Через 1 месяц более 70% пациентов, принимавших кетопрофен в дозе 200 мг/сутки, отметили хороший или превосходный результат лечения. При этом переносимость лечения оказалось очень хорошей: общее число осложнений со стороны ЖКТ (в основном, слабая или умеренная диспепсия) составило 13.5%, а серьезные осложнения - язвы и кровотечения, возникли всего у 0.03% [10].
Однако мы можем предположить, что высокая эффективность КЛС, показанная в нашем исследовании, определяется в большей степени не субъективными, а объективными факторами. Кетопрофен заслуженно считается одним из наиболее удачных по своим терапевтическим свойствам представителей группы НПВП [7,11]. Именно поэтому он так долго и успешно используется в мировой клинической практике; более того, в последние годы отмечается отчетливый рост его популярности в европейских странах. Например, по данным Venegoni M. и сотр., на фоне небольшого, но явного снижения общих продаж основных «рецептурных» НПВП в Италии, продажа кетопрофена за период с 2006 по 2009 гг. выросла на 93%, т.е. почти в 2 раза [12].
По мнению ряда экспертов, высокий анальгетический потенциал кетопрофена может быть связан с липофильностью и относительно небольшими размерами его молекулы [7,13]. Благодаря этим параметрам он может легко проникать в воспаленную ткань, что обеспечивает высокую концентрацию действующего вещества непосредственно в зоне поражения [7,13].
Большое значение придается также способности кетопрофена к диффузии через гематоэнцефалический барьер и воздействию на центральные структуры ноцицептивной системы [14,15]. Экспериментальные данные четко подтверждают равновесие между концентрацией несвязанной фракции кетопрофена в плазме крови, и его концентрацией в цереброспинальной жидкости [16].
Необходимо заметить, что центральное действие этого препарата может определяться не только характерным для всех НПВП механизмом (блокада ЦОГ-2). В частности, обсуждается стимулирующее воздействие S-стереоизомера кетопрофена на серотонинэргическую антиноцицептивную систему [17].
Важным подтверждением преимуществ кетопрофена стала работа итальянских ученых Atzeni F. и сотр., представленная на ежегодном конгрессе американской коллегии ревматологов (ACR), прошедшем в ноябре 2012 в г. Чикаго. Исследователи провели мета-анализ РКИ, в которых сравнивалось обезболивающее действие кетопрофена 50-200 мг/сутки с ибупрофеном 600-1800 мг/сутки или диклофенаком 75-100 мг/сутки. В мировой литературе им удалось найти 13 исследований такого рода: 8 сравнений с ибупрофеном и 5 с диклофенаком, суммарно 898 участников. Препараты назначались больным РА, ОА, АС, БНЧС и страдающим болью в плече.
Кетопрофен, согласно полученным результатам, в 9 из 13 РКИ оказался достоверно более эффективным, чем препараты сравнения. При этом вероятность достижения значительного улучшения при назначении кетопрофена в среднем была почти в 2 раза выше (p=0.000) [18].
В качестве примера эффективности кетопрофена можно привести работу Jokhio I. и сотр. Они сравнили лечебное действие этого препарата и диклофенака у 180 пациентов, испытывающих выраженные боли (среднее значение по ВАШ ~ 70 мм) вследствие травмы или острой патологии мягких тканей ревматической природы. При этом – как и в нашем исследовании, была использована т.н. «ступенчатая» терапия: в первый день НПВП применяли в виде в/м инъекций, а затем они назначались перорально. Соответственно, половина пациентов получили две инъекции кетопрофена по 100 мг, а затем принимали этот препарат по 100 мг 2 раза в день. Другая половина получила две инъекции диклофенака по 75 м, а в дальнейшем 3 раза в день принимали его по 50 мг 3 раза в день внутрь. Курс лечения составил 2 недели. К концу периода наблюдения, в группе кетопрофена у 75% пациентов интенсивность боли уменьшилась до умеренной или слабой, а у 25% она полностью купировалась. В группе диклофенака результаты лечения был скромнее: сильная боль сохранялась у 3%, умеренная или слабая у 87%, а отсутствие боли было зафиксировано лишь у 10% пациентов. При этом 72% больных, получавших кетопрофен, оценили его переносимость как «хорошую или отличную»; такую оценку диклофенаку дали лишь 50% пациентов [19].
Необходимо отметить, что кетопрофен, помимо выраженного обезболивающего действия, обладает хорошим противовоспалительным потенциалом. Этот факт подтверждается успешным опытом применения кетопрофена при анкилозирующем спондилоартрит и подагре – заболеваниях, когда эффективное подавление воспаления имеет принципиальное значение для достижения клинического успеха [20,21].
Так, Altman R. и сотр. сравнили действие кетопрофена (по 100 мг 3 раза в день) и индометацина (по 50 мг 3 раза в день) у 59 больных с острым приступом подагрического артрита. На фоне приема кетопрофена значимое облегчение боли в первый же день лечения отметили 92% больных, столько же, сколько в контрольной группе - 91%. Через неделю лечения приступ был полностью купирован у 24% и 22% пациентов. При этом кетопрофен, не уступая индометацину в эффективности, четко превосходил его по переносимости: в группе кетопрофена какие-либо побочные эффекты были отмечены у 11% больных, в группе индометацина – у 20% [21].
Результаты Altman R. подтверждают наши данные, показавшие наилучшее действие Артрозилена у больных с подагрическим артритом: более высокую частоту достижения субъективно отличного эффекта, в сравнении с пациентами, страдающими другими нозологическими формами.
Следует учесть, что артрозилен представляет собой кетопрофен в виде лизиновой соли, т.е. препарат, обладающий, по мнению европейских экспертов, более высоким терапевтическим потенциалом, чем «обычный» кетопрофен [7]. При этом лекарственные формы артрозилена содержат максимальное количество активной субстанции. Так, в капсуле артрозилена находится 320 мг КЛС – высшая суточная доза этого препарата, которую обеспечивает однократный прием. Аналогично, в/м введение артрозилена (2 мл содержат 160 мг КЛС) 2 раза в день также обеспечивает поступление в организм пациента максимальной суточной дозы действующего вещества. Учитывая хорошую фармакодинамику КЛС, применение артрозилена с первого же дня формируют устойчиво высокую концентрацию активного вещества в плазме крови, что должно обеспечить наилучший клинический эффект.
Максимально высокую концентрацию субстанции имеют и локальные формы артрозилена, в особенности спрей (15%). Как было отмечено выше, кетопрофен очень удобно использовать в качестве действующей субстанции для препаратов, которые наносятся на кожу. Его липофильная, небольшая молекула достаточно легко проникает через кожные покровы, обеспечивая терапевтическую концентрацию действующего вещества в пораженных областях человеческого тела. По мнению экспертов, фармакологические особенности кетопрофена, используемого в качестве действующего начала местных обезболивающих препаратов, определяет его преимущество в сравнении с другими НПВП [7, 22-24].
Четким доказательством эффективности локальной формы кетопрофена стало масштабное британское рандомизированное исследование Patel R. и сотр. В ходе этой работы 1575 больных с острой травмой мягких тканей (вывихи, ушибы, перенапряжение мышц и др.) три раза в день на протяжении 5 дней получали гелевые формы кетопрофена (2.5%), диклофенака (1%) или пироксикама (0.5%). Согласно полученным результатам, кетопрофен достоверно превосходил препараты контроля: так, «значительное улучшение» отметили 38%, 30% и 26% больных соответственно. Аналогично, большая часть больных, получавших кетопрофен, отметила «охлаждающий» эффект геля, в сравнении с контрольными средствами: 71%, 60% и 49% соответственно.
Переносимость геля кетопрофена, по мнению авторов исследования, оказалась «превосходной» [25].
Другим примером успешного использования локальной формы кетопрофена является работа Esparza F. и отр. В ходе этого исследования 223 пациента, перенесших острую спортивную травму, в течение 7-ми дней локально (в области повреждения мягких тканей) наносили ТДС с кетопрофеном или гель диклофенака. Через неделю число пациентов, у которых боль отсутствовала, у получавших кетопрофен составило 64%, в то время как в контрольной группе – только 46% (р=0.001) [26]. Учитывая благоприятный опыт использования локальных форм «обычного» кетопрофена, следует думать, что включение в схему терапии острой мышечно-скелетной боли высокодозных локальных форм КЛС должно существенно повышать суммарную эффективность анальгезии.
Отдельного рассмотрения требует вопрос безопасности артрозилена. Необходимо признать, что ряд эпидемиологических исследований и их мета-анализ демонстрирует существенный риск ЖКТ – осложнений на фоне приема кетопрофена. Данный факт, в частности, был отмечен в работе Castellsague J. и сотр. – мета - анализе 28 эпидемиологических исследований, выполненных с января 1980 по май 2011 гг. и оценивающих развитие ЖКТ - осложнений при использовании различных НПВП. Согласно полученным результатам, наименьший относительный риск (RR) был отмечен для целекоксиба (1.45) и ацеклофенака (1.4); умеренный при использовании ибупрофена (1.84). Существенно выше опасность была при использовании диклофенака (3.34), мелоксикама (3.47) и нимесулида (3.83). Кетопрофен вошел в число препаратов, демонстрирующих наибольший риск - 3.92, напроксен - 4.1 и индометацин - 4.14 [27].
Иные результаты показало одно из наиболее крупных европейских популяционных исследований, проведенных в последние годы - работа финских ученых Helin-Salmivaara A. и сотр. Они оценили причины развития 9191 случаев кровотечения, язв и перфорации, отмеченных в Финляндии за период с 2000 по 2004 гг. Контроль составили 41.780 лиц, соответствующих по полу и возрасту. Согласно полученным результатам, опасность развития ЖКТ - осложнений при использовании кетопрофена была ниже, в сравнении с диклофенаком: OR 3.7 и 4.2 соответственно. Следует отметить, что кетопрофен демонстрировал аналогичный или даже меньший риск ЖКТ - осложнений, чем «селективные» НПВП (за исключением целекоксиба). Так, OR для мелоксикама, нимесулида и эторикоксиба составил соответственно 3.4, 4.0 и 4.4 [28].
Полученные нами данные показывали хорошую переносимость артрозилена. Хотя нежелательные явления отмечались более чем у 10% участников исследования, в подавляющем большинстве случаев это была слабая или умеренно выраженная диспепсия, не потребовавшая отмены терапии или назначения дополнительных лекарств. Серьезные осложнения возникали очень редко – менее чем у 1% больных.
Надо сказать, что европейские исследования также демонстрируют благоприятную переносимость кетопрофена. Так, Schattenkirchner M. и сотр. оценили безопасность этого лекарства у 823 больных ОА и РА, которые получали его в течение года. На фоне лечения осложнения со стороны ЖКТ возникли у 28% пациентов (лишь у 1.7% серьезные), а со стороны сердечно-сосудистой системы - у 3.2%, что относительно немного, учитывая преимущественно пожилой возраст пациентов и тяжелый коморбидный фон [29].
В приведенном выше исследовании Le Loet X. и сотр. число нежелательных явлений примерно соответствовало нашим данным – 13.5%, а серьезные ЖКТ - осложнения были зафиксированы лишь у 6 из 20 тыс. больных [10].
В России также был проведен ряд клинических исследований кетопрофена, которые подтвердили хорошую репутацию этого препарата: он демонстрировал хороший терапевтический потенциал и низкую частоту нежелательных явлений [30-34].
Среди этих работ необходимо отметить исследование Л.Б. Лазебника и сотр., которые провели 3-х месячное сравнение безопасности 4-х НПВП: лорноксикама, нимесулида, целекоксиба и кетопрофена у 132 больных ОА. Интересным моментом этой работы стало сопоставление и ЖКТ (по данным эндоскопического контроля), и кардиоваскулярной безопасности (по данным суточного мониторирования АД). Кетопрофен, согласно полученным данным, показал очень хорошую переносимость. Так, число эрозивно-язвенных изменений при использовании лорноксикама составило 66% (!), нимесулида – 13.5%, кетопрофена – 13.0%, целекоксиба – 8.3%. Дестабилизация АГ - повышение свыше 130/90 мм рт.ст., была отмечена лишь у 2% больных, получавших кетопрофен. В отношении лорноксикама и нимесулида ситуация оказалась совсем иной – у пациентов, принимавших эти препараты дестабилизация АГ была отмечена у 11% и 13% соответственно [34].
Это исследование показало одно из наиболее ценных преимуществ кетопрофена, которому в последнее время придается столь больше значение – низкий риск осложнений со стороны сердечно-сосудистой системы (ССС).
Влияние кетопрофена на развитие кардиоваскулярных катастроф изучалось в нескольких масштабных эпидемиологических исследованиях, проведенных в разных странах мира. Так, низкий риск развития инфаркта миокарда при использовании кетопрофена был показан американскими учеными Singh G. и сотр., использовавших для своего анализа одну из крупнейших компьютерных систем США - California Medical Database. Проанализировав причины 15.343 эпизодов инфаркта миокарда (61.372 лиц составили соответствующий контроль), авторы сопоставили частоту развития этого опасного осложнения у лиц, принимавших наиболее популярные НПВП. Согласно полученным результатам, кетопрофен ассоциировался с наименьшим риском инфаркта миокарда (OR 0.88) – даже в сравнении с напроксеном (OR 1.08), который традиционно считается наиболее безопасным в отношении ССС препаратом из группы НПВП [35].
Похожие данные были получены Solomon M. и сотр., которые сравнили использование различных НПВП у 4425 больных, у которых развился инфаркт миокарда, и 17700 лиц без данного осложнения, основываясь на данных медицинской системы штата Нью-Джерси, США. Согласно полученным данным, разницы по приему кетопрофена в этих группах не было: его получали 53 больных, развивших кардиоваскулярное осложнение (1.2%) и 190 лиц, составлявших контроль (1.1%). Таким образом, использование кетопрофена, по данным этого исследования не повышало риск
развития кардиоваскулярных катастроф [36]. Относительно низкий риск осложнений со стороны ССС был показан в исследовании финских ученых Helin-Salmivaara A. и сотр. Их работа была основана на сопоставлении данных о приеме НПВП у 33.309 лиц, перенесших острый инфаркт миокарда, и 138.949 здоровых людей. Согласно полученным данным, прием кетопрофена фактически не увеличивал опасность развития кардиоваскулярных катастроф (OR 1.11). Соответствующий уровень риска для многих других популярных НПВП был значительно выше – так, для диклофенака он составил 1.35, для мелоксикама - 1.25, для нимесулида - 1.69 [37].
Результаты исследования КУЛОН подтверждают низкий риск сердечно-сосудистых осложнений при использовании кетопрофена.
Среди полученных нами анкет лишь в одной содержалась информация о кардиоваскулярных проблемах - ухудшении артериальной гипертензии. Правда, лечащие врачи, в большей степени занятые купированием острой мышечно-скелетной боли, могли не обращать должного внимания (с учетом минимального времени, которое выделяется на осмотр посетителя в российской поликлинике) на состояние ССС своих пациентов. На это указывает тот факт, что лишь немногие специалисты нашли необходимым отметить в исследовательских картах использование «кардиологических» препаратов. Так, антигипертензивная терапия была указана у 155 больных (4.6%). Столь низкая цифра не может соответствовать действительности, поскольку существенную часть участников исследования составляли люди пожилого возраста, многие из которых, несомненно, страдают артериальной гипертензией. С другой стороны, отсутствие упоминаний о кардиологических проблемах может объясняться и тем, что больные не предъявляли соответствующие жалобы. Ведь жалобы со стороны ЖКТ и высказывались, и фиксировались.
Разумеется, хорошая переносимость КЛС не отменяет необходимости учета факторов риска осложнений со стороны ЖКТ и сердечно-сосудистой системы перед его назначением, и проведения в случае необходимости всего комплекса соответствующих профилактических мероприятий.
Таким образом, мы можем заключить, что артрозилен является эффективным средством для купирования острой и контроля хронической боли. Разнообразные лекарственные формы этого препарата позволяют выбирать индивидуальную схему анальгетической терапии для конкретного пациента и конкретной клинической ситуации. Он показал хорошую переносимость, редко вызывая серьезные осложнения со стороны ЖКТ и сердечно-сосудистой системы. Такое сочетание клинических достоинств может позволить считать артрозилен препаратом выбора для существенной части больных, страдающих патологией опорно-двигательного аппарата.
Литература:
1. Боль (практическое руководство для врачей). Под ред. Яхно Н.Н., Кукушкина М.Л., Москва, Издательство РАМН, 2012, 512 c.
2. Lee Y. Effect and treatment of chronic pain in inflammatory arthritis. Curr Rheumatol Rep. 2013; 15(1): 300.
3. Яхно Н.Н., Кукушкин М.Л. Хроническая боль: медико-биологические и социально-экономические аспекты. Вестник Российской Академии медицинских наук, 2012, N 9, 54-58
4. van de Laar M. Pergolizzi J., Mellinghoff H., et al. Pain Treatment in Arthritis-Related Pain: Beyond NSAIDs. The Open Rheumatology Journal, 2012, 6, 320-330
5. Каратеев А.Е., Яхно Н.Н., Лазебник Л.Б. и сотр. Применение нестероидных противовоспалительных препаратов. Клинические рекомендации. Москва, «ИМА-ПРЕСС», 2009, 167 с.
6. Veys E. 20 years' experience with ketoprofen. Scand J Rheumatol Suppl. 1991; 90: Suppl 1-44.
7. Sarzi-Puttini P., Atzeni F., Lanata L., et al. Pain and ketoprofen: what is its role in clinical practice? Reumatismo. 2010, 62(3): 172-188.
8. Zeidler H., Kaltwasser J., Leonard J., et al. Prescription and tolerability of meloxicam in day-to-day practice. Postmarketing observational cohort study of 13.307 patients in Germany. J. Clin. Rheumatol., 2002, 8, 305-315
9. Lemmel E., Leeb B., De Bast J., Aslanidis S. Patient and physician satisfaction with aceclofenac: results of the European Observational Cohort Study (experience with aceclofenac for inflammatory pain in daily practice). Curr Med Res Opin. 2002, 18(3), 146-153.
10. Le Loet X. Safety of ketoprofen in the elderly: a prospective study on 20,000 patients. Scand J Rheumatol Suppl. 1989; 83: 21-27.
11. Barden J., Derry S., McQuay H., Moore R. Single dose oral ketoprofen and dexketoprofen for acute postoperative pain in adults. Cochrane Database Syst Rev. 2009 Oct 7;(4):CD007355.
12. Venegoni M., Da Cas R., Menniti-Ippolito F., Traversa G. Effects of the European restrictive actions concerning nimesulide prescription: a simulation study on hepatopathies and gastrointestinal bleedings in Italy. Ann Ist Super Sanita. 2010;46(2):153-157.
13. Kokki H. Ketoprofen pharmacokinetics, efficacy, and tolerability in pediatric patients. Paediatr Drugs. 2010; 12(5):313-329.
14. Netter P., Lapicque F., Bannwarth B., et al. Diffusion of intramuscular ketoprofen into the cerebrospinal fluid. Eur J Clin Pharmacol. 1985; 29(3): 319-321.
15. Mannila A., Kokki H., Heikkinen M., et al. Cerebrospinal fluid distribution of ketoprofen after intravenous administration in young children. Clin Pharmacokinet. 2006; 45(7): 737-743.
16. Mannila A., Kokki H., Heikkinen M., et al. Cerebrospinal fluid distribution of ketoprofen after intravenous administration in young children. Clin Pharmacokinet. 2006; 45(7): 737-743.
17. Díaz-Reval M., Ventura-Martínez R., Déciga-Campos M., et al. Evidence for a central mechanism of action of S-(+)-ketoprofen. Eur J Pharmacol. 2004; 483(2-3): 241-248.
18. Atzeni F., Sarzi-Puttini P., Lanata L., Bagnasco M. Efficacy of Ketoprofen Vs Ibuprofen and Diclofenac: A Systematic Review of the Literature and Meta-Analysis. Arthritis Rheum., 2012, 64 (10), 114-115
19. Jokhio I., Siddiqui K., Waraich T., et al. Study of efficacy and tolerance of ketoprofen and diclofenac sodium in the treatment of acute rheumatic and traumatic conditions. J Pak Med Assoc 1998; 48: 373-376.
20. Dougados M., Béhier J., Jolchine I., et al. Efficacy of celecoxib, a cyclooxygenase 2-specific inhibitor, in the treatment of ankylosing spondylitis: a six-week controlled study with comparison against placebo and against a conventional nonsteroidal antiinflammatory drug. Arthritis Rheum. 2001, 44(1):180-185.
21. Altman R., Honig S., Levin J., Lightfoot R. Ketoprofen versus indomethacin in patients with acute gouty arthritis: a multicenter, double blind comparative study. J Rheumatol. 1988, 15(9):1422-1426.
22. Kawai S., Uchida E., Kondo M., et al. Efficacy and safety of ketoprofen patch in patients with rheumatoid arthritis: a randomized, double-blind, placebo-controlled study. J Clin Pharmacol. 2010, 50(10):1171-1179.
23. Coaccioli S. Ketoprofen 2.5% gel: a clinical overview. Eur Rev Med Pharmacol Sci. 2011; 15(8): 943-949.
24. Komatsu T., Sakurada T. Comparison of the efficacy and skin permeability of topical NSAID preparations used in Europe. Eur J Pharm Sci. 2012; 47(5): 890-895.
25. Patel R., Leswell P. Comparison of ketoprofen, piroxicam, and diclofenac gels in the treatment of acute soft-tissue injury in general practice. General Practice Study Group. Clin Ther. 1996; 18(3): 497-507.
26. Esparza F., Cobián C., Jiménez J., et al. Topical ketoprofen TDS patch versus diclofenac gel: efficacy and tolerability in benign sport related soft-tissue injuries. Br J Sports Med. 2007, 41(3): 134-139.
27. Castellsague J., Riera-Guardia N., Calingaert B., et al. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta-analysis of observational studies (the SOS project).Drug Saf. 2012; 35(12): 1127-1146.
28. Helin-Salmivaara A., Saarelainen S., Gronroos J., et al. Risk of upper gastrointestinal events with the use of various NSAIDs: A case-control study in a general population. Scan J Gastroenterol, 2007; 42: 923-932
29. Schattenkirchner M. Long-term safety of ketoprofen in an elderly population of arthritic patients. Scand J Rheumatol Suppl. 1991; 91: 27-36.
30. Чичасова Н.В., Иммаметдинова Г.Р., Каратеев А.Е., и соавт. Эффективность и безопасность кетопрофена (кетонал) при ревматоидном артрите (клинико-эндоскопическое исследование). Научно-практическая ревматология 2001; 1; 47-52
31. Осипова Н.А., Петрова В.В., Ермолаев П.М., Береснев В.А. Нестероидные противовоспалительные препараты в лечении послеоперационной боли у онкологических больных. Фарматека, 2006, №6 (121)
32. Шмидт Е.И., Коган К.М., Белозерова И.В. Оценка эффективности кетонала ретард у больных остеоартрозом. Научно-практическая ревматология 2000; 2:77-79.
33. Новиков Г.А., Вайсман М.А., Прохоров Б.М. и др. Кетонал в лечении болевого синдрома у пациентов с распространенными формами злокачественных новообразований. Паллиативная медицина и реабилитация, №3, 2002, 48–51.
34. Лазебник Л.Б., Дроздов В.Н., Коломиец Е.В. Сравнительная эффективность и безопасность применения кетопрофена, лорноксикама, нимесулида и целекоксиба у больных остеоартрозом. РМЖ, 2004, 12 (14), 844-847.
35. Singh G., Mithal A., Triadafilopoulos G. Both selective COX-2 inhibitors and non-selective NSAIDs increase the risk of acute myocardial infarction in patients with arthritis; selectivity is with patients, not the drug. Ann Rheum Dis 2005, 64 (suppl 3), 85
36. Solomon D., Glynn R., Levin R., Avorn J. Nonsteroidal Anti-inflammatory Drug Use and Acute Myocardial Infarction. Arch Intern Med. 2002; 162: 1099-1104
37. Helin-Salmivaara A., Virtanen A., Vesalainen R., et al. NSAID use and the risk of hospatalisation for first myocardial infarction in the general population: a national case-control study from Finland. Eur Heart J 2006; 27: 1657-1663


