Проблемы нефропротекции у пациентов с артериальной гипертонией. Значение показателя микроальбуминурии для врача общей практики
Статьи
Г.П. Арутюнов, доктор медицинских наук, профессор Т.К. Чернявская
Российский государственный медицинский университет, Москва
В последние годы стало очевидно, что прогноз относительно жизни больного артериальной гипертонией (АГ) регламентируется в первую очередь вовлеченностью в патологический процесс органов-мишеней и выраженностью их морфофункциональных изменений [1, 23, 25]. В свете этого роль почек в патогенезе и развитии АГ вновь стала предметом оживленной дискуссии, остроту которой придает наличие длительного периода латентно протекающей почечной дисфункции [2, 4, 5, 13, 15]. Это доклинические этапы поражения почек, когда привычные и широко применяемые в терапевтической практике тесты оценки их состояния (уровень креатинина сыворотки крови, скорость клубочковой фильтрации, уровень протеинурии и т.д.) практически не изменены, а потому не позволяют врачу судить о выраженности процессов деструкции почек [22, 30]. Данное состояние может длиться десятилетиями, постепенно усугубляясь и перерастая в явную патологию, проявляющуюся клиническими маркерами хронической почечной недостаточности (ХПН) и декомпенсацией функции почек. Финал болезни - стадия явных клинических маркеров почечной недостаточности - как правило, протекает стремительно, приводя в конечном счете к развитию необратимой терминальной стадии ХПН [4, 13]. Поэтому клиницистам особенно важно выявить начальный период почечной дисфункции, когда агрессивная тактика назначения лекарственных средств позволяет замедлить процесс деструкции почечного клубочка и принципиально изменить судьбу пациента [6, 7].
Сегодня стало возможным выявлять начало почечной дисфункции. Среди маркеров начального периода ведущее место занимает микроальбуминурия (МАУ). Этап МАУ не дискретен, а является составной частью развития нефропатии [4, 5]. На этот этап приходятся I-II стадии развития ХПН, когда традиционные маркеры почечной недостаточности не дают врачу никакой информации о степени истинной дисфункции почек [7, 9, 21].
К сожалению, раннее определение уровня теряемого альбумина у больных АГ сегодня далеко от практического применения [3, 4]. Несмотря на относительную дешевизну, этот метод не входит в перечень обязательных медицинских манипуляций, а его истинное клиническое значение не очевидно для врача.
Определение МАУ
Термин МАУ применяется для обозначения экскреции альбумина ниже уровня, определяемого качественным тестом, но выше уровня, встречающегося в общей популяции. МАУ принято считать скорость экскреции альбумина (СЭА) с мочой в пределах от 20-30 до 300 мкг/мин, что составляет от 20-30 до 300 мг/сут. Прирост СЭА при условии исходно ее повышенного уровня и отсутствия терапии составляет примерно 25 мкг/мин в год.
Причины возникновения МАУ
Молекулы альбумина имеют диаметр 3,6 нм (меньше размера пор), однако в физиологических условиях они, как и большинство других макромолекул, практически не достигают щелевидной диафрагмы базальной мембраны клубочка и задерживаются на уровне фенестр. Здесь создается функциональный барьер, целостность которого обеспечивается отрицательным зарядом и проявляется избирательной проницаемостью базальной мембраны клубочка по отношению к заряду молекулы. Экскреция альбумина связана в первую очередь с потерей отрицательного заряда клубочковым фильтром, а экскреция более крупных молекул происходит в большей мере при повреждении базальной мембраны. Альбумин одним из первых появляется в конечной моче при различных повреждениях почечных структур, и его концентрация прямо пропорциональна тяжести поражения почечного фильтра. Существуют нормальные суточные колебания выделения белка, при этом максимальное его выведение приходится при обычной деятельности на дневное время. Это обусловлено тем, что ходьба и вертикальное положение тела повышают действие гемодинамических сил на клубочковую фильтрацию. Кроме того, на выделение белка с мочой влияют такие, факторы как АГ, тяжелые физические нагрузки, значительное употребление соли, беременность, гиперволемия. Однако протеинурия может быть связана и с внепочечными причинами, например с распадом форменных элементов крови, присутствующих в моче (лейкоциты, эритроциты), при длительном стоянии мочи.
Способы определения МАУ
Возможность выявлять незначительные количества альбумина в моче зависит от чувствительности методов его определения. Впервые в 1964 г. Н. Кен сообщил о доступном иммунологическом методе обнаружения низкого уровня альбумина в моче. Однако широко применять такой метод определения МАУ стали в 80-е годы в эндокринологической практике для верификации начальных этапов диабетической нефропатии, и значительно позже он был введен в практику интернистов. Методы скрининга МАУ и процедуры, позволяющие получить подтверждение наличия МАУ, различны. Считают, что возможно использование следующих критериев для скрининговой методики оценки МАУ:
- СЭА с мочой (мг/сут);
- отношение альбумина к креатинину (в норме 2,5/25 мг/ммоль);
- содержание альбумина в первой порции утренней мочи (мг/л).
Экскреция альбумина может варьировать в пределах 40%, что обусловлено естественными колебаниями, поэтому необходимо выполнять несколько повторных определений.
Клиническое значение МАУ
Если устанавливать клиническое значение МАУ, то необходимо учесть, что около 30% людей в мире имеют повышенный уровень АД (этот показатель значительно возрос в настоящее время после опубликования результатов исследования HOT (Hypertension Optimal Treatment), сместившего границы нормального уровня АД до 138/83 мм рт.ст.) [18], а распространенность МАУ составляет 30-35% среди больных АГ и 40-45% среди пациентов с АГ и присоединившимся сахарным диабетом (СД) типа 2 [12, 13].
Нетрудно вычислить, что определение МАУ показано многим десяткам миллионов пациентов. Так, в исследовании MONICA (MONItoring of CArdiovascular events) [31] принимали участие 15 млн пациентов в возрасте от 25 до 64 лет, которых наблюдали в течение 10 лет. В ходе наблюдения учитывали частоту острого инфаркта миокарда, смертность от ишемической болезни сердца в зависимости от распространенности известных факторов риска. Было установлено, что наличие МАУ в 2,4 раза повышает риск развития ишемической болезни сердца по сравнению с пациентами, имеющими нормальный уровень экскреции альбумина с мочой.
Таким образом, скрининг МАУ в популяции людей, считающих себя здоровыми, оправдан и необходим, поскольку позволяет выявить латентно текущий патологический процесс и предотвратить развитие тяжелых сердечно-сосудистых заболеваний.
У больных АГ МАУ встречается в 16 раз чаще, чем у практически здоровых людей. По данным авторов статьи, повышение АД в течение пяти лет увеличивает вероятность развития МАУ в два раза, а более пяти лет - в пять раз по сравнению с впервые выявленной АГ.
Установлено, что МАУ имеет прямую корреляционную связь с уровнем диастолического АД (ДАД) и индексом массы тела. Кроме того, имеется прямая связь между уровнем МАУ и тяжестью прогноза (заболеваемость и летальность от ишемической болезни сердца) [17, 25].
Особое внимание следует обратить на группу пациентов с СД и АГ, поскольку это сочетание заболеваний повышает частоту МАУ до 89% [21, 27]. Полученные авторами статьи данные показывают, что сочетание АГ и СД уже через три года в 1,4 раза повышает вероятность обнаружения МАУ, а через пять лет и более МАУ может быть обнаружена у 9 из 10 пациентов.
У больных АГ в сочетании с СД МАУ встречается в 21 раз чаще, чем у здоровых, и в 1,25 раз чаще, чем у пациентов с АГ без СД. Кроме того, более 80% этих пациентов имеют МАУ средней и высокой степени выраженности. Поэтому данная группа пациентов является прогностически наименее благоприятной по тяжести течения заболевания и риска развития ХПН, а, следовательно, абсолютное большинство пациентов, страдающих СД типа 2 в сочетании с АГ, требует динамического мониторинга уровня МАУ.
Таким образом, МАУ - это распространенное явление, встречаемость которого зависит от конкретных условий, а именно: продолжительности болезни, ее тяжести, наличия факторов риска и ассоциированных заболеваний и осложнений [13].
Очевидно, что раннее выявление пациентов с МАУ позволяет не только выявить в общей популяции пациентов с уже сформировавшейся патологией органов-мишеней и определить прогноз заболевания, но и обосновать дифференцированный подход к лечению [14].
Влияние лекарственных средств на уровень МАУ
Еще в 1988 г. M. Marre, а затем M. Early (1993) и S. Bianchi (1994) попытались провести сравнительный анализ эффективности различных антигипертензивных препаратов в отношении МАУ [19]. Они показали, что ингибитор ангиотензинпревращающего фермента (АПФ) эналаприл значительно эффективнее снижает уровень МАУ, чем антагонист кальция никардипин, бета-адреноблокатор атенолол или просто диуретики в качестве средств монотерапии АГ.
В масштабных клинических исследованиях установлено, что ингибиторы АПФ обладают преимуществом перед другими антигипертензивными препаратами в плане воздействия на скорость развития нефропатии [22, 24, 30]. По данным двойных слепых сравнительных исследований, ингибиторы АПФ в большей степени влияли на экскрецию белка с мочой, чем другие антигипертензивные средства, хотя их антигипертензивный эффект был одинаковым [6], а следовательно, ингибиторы АПФ оказывают ренопротективное действие у всех пациентов, независимо от антигипертензивного эффекта.
Известно, что механизм ренопротективного действия ингибиторов АПФ отличен от простого антигипертензивного эффекта. Наиболее важным в действии ингибиторов АПФ на сегодняшний день принято считать ослабление эффекта циркулирующего ангиотензина II на эфферентные артериолы. Как только тонус эфферентных артериол ослабевает, внутриклубочковое давление понижается, ослабевает или исчезает гиперфильтрационный режим работы клубочка и, как следствие, уменьшаются МАУ и протеинурия. Важно отметить, что применение ингибиторов АПФ приводит к уменьшению синтеза в интерстиции факторов роста, эндотелина, что замедляет развитие нефросклероза. M. Rаvid (1993) и N.B. Shulman (1989) показали, что регулярный прием ингибиторов АПФ приводит к достоверному уменьшению диаметра пор почечного фильтра у больных с нефропатией любого генеза. Таким образом, антигипертензивными препаратами выбора для лечения пациентов с признаками почечной дисфункции и в том числе с СД и АГ являются ингибиторы АПФ.
Ренопротективное действие ингибиторов АПФ состоит не только в нормализации кровотока через почку, уменьшении сосудистого сопротивления, снижении МАУ и протеинурии, но и в метаболических эффектах: повышении чувствительности к инсулину, улучшении метаболизма глюкозы при нейтральном отношении к липидам.
Перечисленные свойства ставят ингибиторы АПФ на первое место в лечении АГ у больных СД, поскольку они влияют не только на течение самого заболевания, но и на развитие его основных сердечно-сосудистых осложнений.
Так, результаты исследования САРРР (Captopril Prevention Project) [18] показали, что пациенты, лечившиеся ингибиторами АПФ, имели значительно меньший риск развития сердечно-сосудистых осложнений и смерти, чем пациенты, получавшие комбинированную терапию диуретиком и бета-адреноблокатором. Это же исследование продемонстрировало, что СД развивался значительно чаще у пациентов, получавших тиазидный диуретик и (или) бета-адреноблокатор, по сравнению с больными, леченными ингибитором АПФ (в среднем на 21% за 6 лет наблюдения) [8].
Однако на ранних этапах развития нефропатии (как диабетической, так и недиабетической) при нормоальбуминурии преимущество ингибиторов АПФ у больных с АГ не доказано. Их эффект близок таковому других антигипертензивных препаратов. Во всех остальных случаях ингибиторы АПФ являются лекарственными средствами первого ряда при планировании и проведении ренопротективной терапии.
Результаты многочисленных исследований доказали явное преимущество спираприла (Квадроприл®) перед другими антигипертензивными средствами в плане органопротективного воздействия и достоверного улучшения течения болезни у пациентов с почечной дисфунцией. В одном из исследований [11] у больных мягкой и умеренной АГ в сочетании с сахарным диабетом и нарушенной функцией почек была показана высокая антигипертензивная эффективность спираприла в дозе 6 мг/сут и существенное улучшение функции почек: достигнуто достоверное уменьшение уровня креатинина крови (с 1,3±0,05 до 1,2±0,08 мг/дл, р<0,05) и увеличение клиренса креатинина (с 65,0±2,9 до 73,4±5,2 мл/мин, р<0,01) при отсутствии сдвигов уровней глюкозы и калия в крови; САД в среднем снизилось на 24,2±2,7 мм рт.ст., ДАД - на 12,2±1,3 мм рт.ст. Это исследование подтвердило результаты других испытаний применения Квадроприла у больных АГ и диабетической нефропатией, проведенных ранее [20, 26, 28], в одном из которых [20] через 6 мес постоянного лечения спираприлом (однократно 6 мг/сут) у больных АГ и сопутствующей диабетической нефропатией с ХПН произошло достоверное снижение фракционного клиренса альбумина (в среднем на 25,5%) и уменьшение 24-часовой экскреции альбумина (почти на 29,6%, p<0,05) (рис. 1).
Рис. 1. Эффективность спираприла при диабетической нефропатии [20].
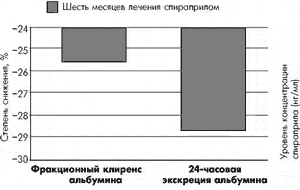
В завершение этого исследования авторы пришли к выводу, что двойной путь элиминации Квадроприла у больных АГ и диабетической нефропатией обеспечивает безопасность длительного применения препарата у больных с нарушенной функцией почек.
Нефропротективное действие спираприла (Квадроприл) проявляется также в улучшении выделительной функции почек и снижении альбуминурии [26].
Шотландское исследование [10, 20, 26], включавшее 34 больных АГ, диабетической нефропатией и ХПН, продемонстрировало высокую эффективность и безопасность спираприла у больных с далеко зашедшей почечной недостаточностью (скорость клубочковой фильтрации <20 мл/мин). Опубликованные данные [16] показали, что спираприл не кумулируется у этой категории больных не только при его однократном приеме, но и при постоянной терапии (рис. 2, 3).
Рис. 2. Применение ингибиторов АПФ при нарушенной функции почек [16].

Рис. 3. Применение спираприла у пациентов в терминальной стадии почечной недостаточности [16].
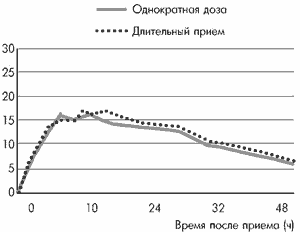
Важнейший вопрос практической медицины - это определение того уровня АД, ниже которого рост протеинурии прекращается и начинается снижение уровня МАУ. По данным, приведенным в исследовании Microalbuminuria Captoprili Study Group [29], такой уровень соответствует 125/75 мм рт.ст. В то же время, по данным D. Barnas (1998), это достигается при ДАД меньше 90 мм рт.ст. В 1998 г. были опубликованы результаты исследования HOT [18], в котором безопасный уровень АД расчетно определен как 138/83 мм рт.ст. Таким образом, ДАД меньше 90 мм рт.ст. следует считать целью при лечении больных СД и АГ.
Эффективный контроль АД становится одной из главных задач лечения пациентов с АГ и особенно при наличии СД типа 2. Эффективное снижение и поддержание нормального АД предотвращает (замедляет) как прогрессирование нефропатии, так и проявление сердечно-сосудистых осложнений.
Однако по мере возрастания тяжести исходного состояния пациентов наблюдается "ускользание" простого эффекта снижения АД и нормализации почечной гемодинамики. Установлено, что при низком уровне МАУ эффективны все препараты, нормализующие АД и почечную гемодинамику. По-видимому, на данном этапе степень деструкции почечного фильтра такова, что простой нормализации внутриклубочкового давления достаточно для нивелирования потери белка. Однако при более высоком уровне потери белка успех достигается только при применении ингибиторов АПФ и блокаторов рецепторов ангиотензина II. Нарастающий нефропротективный эффект данных препаратов прослеживается и после нормализации АД.
Таким образом, нормализация АД не всегда является гарантией нормализации экскреции белка с мочой. В более сложных ситуациях только ингибиторы АПФ и блокаторы рецепторов ангиотензина II сохраняют свои нефропротективные эффекты, что доказывает наличие у них дополнительных возможностей воздействия на патологический процесс, а следовательно, именно эти препараты становятся препаратами выбора для пациентов с нарушенной функцией почек.
Исходя из вышесказанного, ошибочно говорить о МАУ в качественном аспекте этой патологии - "обнаружена" или "не обнаружена", так как очевидно различие пациентов по тяжести почечной дисфункции, потеря альбумина у которых составляет от 30 мг/сут до 300 мг/сут. Уровень МАУ имеет большое значение - чем он выше, тем тяжелее исходное состояние больного. Следовательно, оправдана градация МАУ по уровню выраженности, поскольку очевидна различная тактика выбора медикаментозного лечения для пациентов с различными исходными уровнями МАУ.
Пациентам с низкими значениями МАУ может быть назначен любой антигипертензивный препарат, который обеспечит стойкие нормальные гемодинамические показатели, поскольку длительное поддержание нормального уровня АД приводит к восстановлению почечной гемодинамики и уменьшению МАУ. У пациентов со средними и высокими значениями МАУ предпочтение следует отдавать новым ингибиторам АПФ с улучшенной фармакокинетикой (Квадроприл®) и блокаторам рецепторов ангиотензина II, которые дают более выраженный и быстрый эффект.
Таким образом, очевидна ценность МАУ как параметра для прогноза длительности и качества жизни пациентов. Его истинная клиническая значимость состоит в том, что он не только отражает функцию почек, но и является универсальным маркером системного преморбидного состояния. МАУ начинает регистрироваться практически одномоментно с выявлением диастолической дисфункции миокарда и эндотелиальной дисфункции. В настоящее время МАУ расценивается как независимый фактор риска сердечно-сосудистой смертности и прогрессирования почечной недостаточности. Мониторинг уровня МАУ должен быть неотъемлемым компонентом комплексной оценки текущего состояния и прогноза у больных АГ.
Квадроприл® - Досье препарата
Список литературы
1. Алмазов В.А., Шляхто Е.В. Гипертоническая болезнь.- Москва, 2000.- 118 с.
2. Аннаниязова С.А., Юренев А.П. Динамика структурных гемодинамических показателей у больных гипертонической болезнью в процессе наблюдения в различные сезоны года в условиях жаркого климата // 3дравоохр. Туркменистана.- 1990.- №5.- С. 9-12.
3. Арутюнов Г.П., Чернявская Т.К., Лукичева Т.И. и др. Микроальбуминурия и пути ее медикаментозной коррекции // Клин. фармакол. и тер.- 1999.-№3.-С. 23-28.
4. Ермоленко В.М. Хроническая почечная недостаточность. В кн.: Нефрология. Руководство для врачей / Под ред. И.Е. Тареева.- М.: Медицина, 1995.-Т. 1.-С. 322-390.
5. Лифштиц Н.Л., Кутырина И.М. Особенности лечения гипертонии при хронических диффузных заболеваниях почек // Materia Medico.- 1995.- №2.-С. 39-50.
6. Моисеев В. С. Ингибиторы АПФ и нефропатия // Клин. фармакол. и тер.- 1997.- №6 (4).- С. 67-69.
7. Мухин Н.А., Сура В.В. Диабетическая нефропатия. В кн.: Нефрология. Руководство для врачей / Под ред. И.Е. Тареева.- М.: Медицина, 1995.- Т.2.- С. 312-321.
8. Сидоренко Б.А., Преображенский Д.В. Пересыпко М.К. Новые подходы к классификации и лечению артериальной гипертензии // Consilium Medicum.- 2000.- Т 2.- №3.- С. 95-127.
9. Тареев И.Е., Николаев А.Ю., ЛифшицН.Л. Диагностика и консервативное лечение хронической почечной недостаточности. Методические рекомендации для врачей.- М., 1993.
10. Элиот Г.Л. Применение ингибитора ангиотензинпревращающего фермента спираприла при хронической почечной недостаточности, гипертонии и диабетической нефропатии // Тер. архив.- 2000.-№10.-С. 2-6.
11. Якусевич В.В., МожейкоМ.У., ПалютинШ.Х. и др. Спираприл - новый ингибитор ангиотензинпревращающего фермента длительного действия: эффективность и безопасность у больных артериальной гипертонией в сочетании с сахарным диабетом и нарушением функции почек // Тер. архив.- 2000.-№ 10.-С. 6-10.
12. Anderson S. Role of local and systemic angiotensin in diabetic renal disease // Kidney. Int.- 1997.- №.52 (suppl.63).-S107-S110.
13. Bennett P.H., Haffner S., Kasiske B.L. et al. Screening and management of microalbuminuria in patients with diabetes mellitus: recommendations to the scientific advisory board of the National Kidney Foundation from an ad hoc committee of the council on diabetes mellitus of the National Kidney Foundation // Am. J. Kidney Dis.- 1995.- №. 25.-P. 107-112.
14. Bilous R.W. Early diagnosis of diabetic nephropathy // Diab. Metab. Rev.- 1996.- V. 2.- P. 243-253.
15. Borch-Johnsen K., Wenzel H., Viberti G.C., Mogensen C.E. Is screening and intervention for microalbuminuria worthwhile in patients with insulin dependent diabetes? // BMJ.- 1993.- №306.- P. 1722-1725.
16. Elliot H.L. Clinical use of angiotensin-converting enzyme inhibitors in patients with renal impairment // Blood Press.- 1994.- №3 (Suppl. 2).- P. 31-34.
17. Hansson L., Lindholm L.H., Niskanen L. et al. Effect of angiotensin-converting enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPPP) randomized trial // Lancet.- 1999.- №. 353.- P. 611-616.
18. Hansson L., Zanchetti A., Carruthers S.G. et al. Benefits of intensive blood pressure lowering and acetylsalicylic acid in hypertensive patients. Principal results of the Hypertension Optimal Treatment (HOT) Study // Lancet.- 1998.- V. II.- P. 1654-1658.
19. Maschio G., Alberti D., Janin G. et al. Effect of the angiotensin-convertingenzyme inhibitor benazepril on the progression of chronic renal insufficiency // N. Engl. J. Med.- 1996.- №334.- P. 939-945.
20. Meredith P.A., Grass P., Guitard С et al. Pharmacokinetics of spirapril in renal impairment // Blood Press.- 1993.- №3 (suppl. 2).- P. 14-19.
21. Mogensen C.E. Management of early nephropathy in diabetic patients: with emphasis on microalbuminuria // Ann. Rev. Med.- 1995.- №46.-P. 79-94.
22. Mogensen C.E. Renoprotective role of ACE inhibitors in diabetic nephropathy // Br. Heart J.-1994.- №72 (suppl.).- P. 38-45.
23. Mogensen C.E. Systemic blood pressure and glomerular leakage with particular reference to diabetes and hypertension // J. intern. Med.- 1994.-№235.-P. 297-316.
24. Mogensen C.E., Hansen K.W., Nielsen S. et al. Monitoring diabetic nephropathy: glomerular filtration rate and abnormal albuminuria in diabetic renal disease: reproducibility, progression studies and efficacy of antihypertensive intervention // Am. J. Kidney Dis.- 1993.- №22.- P. 174-187.
25. Ohkubo T., Imai Y., Tsuji I. et al. Reference values for 24-hour ambulatory blood pressure monitoring based on a prognostic criterion. The Ohasama Study // Hypertens.- 1998.- №32.- P. 255-259.
26. Opie L.H. Angiotensin-converting enzyme inhibitors. The advance continues. 3 ed. New-York: Author`s apublishing House, 1999.- 275 p.
27. Roman G.V. Renal failure in diabetes: In: Diabetic Complications / Ed. K.M.Shawn.- John Willey & Sons Ш, 1996.- Р. 53-66.
28. Sweetnam P.M. et al. // Europ. Heart J.- 1996.-V. 17.-P. 1814-1820.
29. The Microalbuminuria Captopril Study Group. Captopril reduces the risk of nephropathy in IDDM patients with microalbuminuria // Diabetologia.-1996.- №39.- P. 587-593.
30. Viberti GC., Mogensen CE., Passa P. et al. St. Vincent declaration, 1994: guidelines for prevention of diabetic renal failure. In: The kidney and hypertension in diabetes mellitus / Ed. By C.E. Mogensen, 1994.
31. WHO MONICA Project: Risk Factors // Intern. J. Epidemiol.-1989.-№18 (suppl. 1).-S46-S55.
