Ритуксимаб в лечении ревматических болезней
СтатьиОпубликовано в журнале:
«Научно-практическая ревматология» 2008, приложение к № 1, С. 3-10
Оглавление
- Ритуксимаб в лечении ревматических болезней
- Первый опыт применения моноклональных антител к В-лимфоцитам (ритуксимаб) при ревматоидном артрите в России
- Качество жизни больных ревматоидным артритом, получающих ритуксимаб
- Лабораторное обеспечение регистра пациентов, получающих препарат ритуксимаб (Мабтеру)
- Ритуксимаб: новые перспективы лечения больных СКВ
- Анти-В клеточная терапия синдрома и болезни Шёгрена
- Применение ритуксимаба у больных ревматоидным артритом: опыт работы центра антицитокиновой терапии
- Первый опыт применения Мабтеры (ритуксимаба) при ревматоидном артрите в Рязанском регионе
- Опыт применения ритуксимаба для лечения ревматоидного артрита в республике Тыва
- Первый опыт применения Мабтеры у больных с тяжелым течением ревматоидного артрита
- Опыт применения препарата ритуксимаб ("Мабтера") у больных ревматоидным артритом
- Опыт применения препарата Мабтера у больной ревматоидным артритом
Ритуксимаб в лечении ревматических болезней
Е.Л. Насонов
ГУ Институт ревматологии РАМН
Аутоиммунные заболевания включают более 80 нозологических форм, относятся к числу наиболее распространенных и тяжелых болезней человека. Частота аутоиммунных заболеваний в популяции достигает 8%. Аутоиммуннитет составляет основу широкого спектра ревматических болезней, включая ревматоидный артрит (РА), системную красную волчанку (СКВ), системную склеродермию, системные васкулиты и др. Для лечения аутоиммунных заболеваний в целом, и ревматических болезней в частности используется широкий спектр препаратов, обладающих противовоспалительной (глюкокортикоиды - ГК), цитотоксической или иммуносупрессивной (в низких дозах) активностью, большая часть из которых создавались для лечения злокачественных новообразований или подавления отторжения трансплантата. Рациональное применение этих препаратов в сочетании с экстракорпоральными методами очищения крови в период обострения, позволило существенно улучшить непосредственный и отдаленный прогноз, однако во многих случаях не позволяет контролировать прогрессирование заболевания, развития угрожающих для жизни осложнений или ассоциируется с тяжелыми побочными эффектами.
Ревматоидный артрит (РА) - наиболее частое аутоиммунное ревматическое заболевание, распространенность которого в популяции достигает 1,0%, а экономические потери для общества сопоставимы с ишемической болезнью сердца. Хотя в конце 20 века в лечении РА достигнут существенный прогресс, фармакотерапия этого заболевания, по-прежнему, остается одной из наиболее сложных проблем клинической медицины [1].
В настоящее время "золотым" стандартом фармакотерапии РА является метотрексат (МТ) и лефлуномид, эффективность и безопасность которых соответствует современным критериям "медицины, основанной на доказательствах". Однако, терапия "стандартными" БПВП (в первую очередь МТ) в максимально эффективных и переносимых дозах, начиная с самого раннего периода болезни, действительно позволила улучшить непосредственный (подавление боли и воспаления суставов) и даже отдаленный (снижение риска инвалидности) прогноз у многих пациентов, тем не менее в целом результаты лечения РА до недавнего времени не внушали оптимизма. Примерно у половины больных БПВП недостаточно эффективно контролируют клинические проявления РА и прогрессирование деструктивного процесса в суставах, часто вызывают побочные реакции, ограничивающие возможность применения этих препаратов в дозах, необходимых для достижения стойкого клинического эффекта.
Бурный прогресс биологии и медицины в конце 20 века нашел свое яркое практическое отражение в расширении возможностей фармакотерапии РА и других воспалительных ревматических заболеваний. С помощью методов биотехнологии были созданы принципиально новые противовоспалительные препараты, объединяющиеся общим термином "генно-инженерные биологические агенты" ("bio-logics"), применение которых, благодаря расшифровке ключевых механизмов иммунопатогенеза этого заболевания, теоретически хорошо обосновано и позволило существенно повысить эффективность фармакотерапии РА [1]. Среди широкого спектра "провоспалительных" медиаторов, принимающих участие в развитии РА, особое внимание привлечено к фактору некроза опухоли (ФНО)-а, который рассматривается как основной цитокин, определяющий развитие синовиального воспаления и остеокласт-опосредованной костной деструкции при артритах. Не удивительно, что именно ФНО-а в настоящее время является важнейшей "мишенью" для так называемой "антицитокиновой" терапии РА и других воспалительных заболеваний суставов, таких как анкилозирующий спондилит и псориатический артрит. Это послужило основанием для разработки группы препаратов - так называемых ингибиторов ФНО-а, блокирующих биологическую активность этого цитокина в циркуляции и на клеточном уровне [2-4].
Самый значительный клинический опыт накоплен в отношении препарата Инфликсимаб (Ремикейд) - химерных моноклональных антител к ФНО-а. Другим представителем класса ингибиторов ФНО-а является адалимумаб (Хумира) -первый и пока единственный препарат, представляющий собой полностью человеческие рекомбинантные моноклональные антитела к ФНО-а. Результаты проведенного анализа, соответствующие критериям "медицины, основанной на доказательствах", свидетельствуют о том, что инфликсимаб и адалимумаб являются эффективным препаратами для лечения РА, резистентного к терапии "стандартными" БПВП, включая МТ (рис. 1). Учитывая современную концепцию фармакотерапии РА, основанную на необходимости ранней агрессивной терапии, анализ результатов применения инфликсимаба и адалимумаба в качестве "первых" БПВП (в сочетании с МТ) при "раннем" РА, представляют особый интерес. Установлено, что у больных с "ранним" РА на фоне комбинированной терапии инфликсимабом и МТ или адалимумабом и МТ у большего числа пациентов удается достичь состоянии "ремиссии", и добиться существенного замедления прогрессирования деструкции суставов, чем на фоне монотерапии МТ.
Рис. 1.
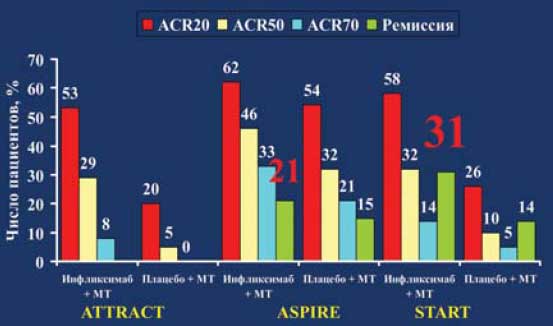
Однако, несмотря на то, что ингибиторы ФНО продемонстрировали чрезвычайно высокую эффективность при РА в процессе контролируемых исследований, в реальной клинической практике около 30-40% пациентов "рефрактерны" к терапии этими препаратами, менее, чем у половины - удается достичь полной или частичной ремиссии, а около трети вынуждены прекращать лечение из-за развития вторичной неэффективности или побочных эффектов через 2-3 года терапии (рис. 2). Необходимо принимать во внимание, что лечение ингибиторами ФНО может сопровождаться развитием инфекционных осложнений, в первую очередь туберкулезной инфекции [5] (рис. 3).
|
Рис. 2. Длительность применения инфликсимаба при РА
|
Рис. 3.
|
Ингибиторы ФНО:
|
Среди разнообразных иммунных нарушений, лежащих в основе развития аутоиммунных заболеваний, изучение дефектов В - клеточной регуляции вызывает особый интерес, в том числе и с точки зрения разработки новых патогенетически обоснованных подходов к лечению (рис. 4). Напомним, что В лимфоциты - клетки иммунной системы, участвующие в развитии и поддержании адаптивного иммунитета, образуются из гемопоэтических предшественников в костном мозге в течение всей жизни человека, участвуют в поддержании иммунологической толерантности к собственным антигенам (аутоантигенам). Дефект В клеточной толерантности, приводит к синтезу аутоантител, которые, активируя эффекторные звенья иммунного ответа, индуцируют развитие воспаления и деструкции тканей организма человека. Однако значение В клеток в развитии аутоиммунных заболеваний не исчерпывается только синтезом "патогенных" аутоантител. Установлено, что нарушения В клеточной ко-стимуляции Т лимфоцитов играют фундаментальную роль в развитии аутоиммунных патологических реакций и могут развиваться на самых ранних стадиях патологического процесса до клинической манифестации заболевания (рис. 5). Данные экспериментальных исследований свидетельствуют о фундаментальной роли В-лимфоцитов в иммунопатогенезе РА (рис 6 и 7). При изучении экспериментального артрита у мышей с тяжелым комбинированным иммунодефицитом (NOD-SCID), развивающимся при переносе синовиальной ткани от пациентов с активным РА, было показано, что В - лимфоциты участвуют в активации CD4+ Т - клеток по Th1 типу в воспаленной синовиальной ткани, выполняя функцию специфических антиген-презентирующих клеток. В - клетки, синтезирующие РФ, обладают уникальной способностью взаимодействовать с иммунными комплексами и "презентировать" широкий спектр аутоантигенов, а активированные В - клетки экспрессируют костимуляторные молекулы (B7 и CD40), необходимые для полноценной активации Т-клеток. Обсуждается и эффекторная роль В - клеток в развитии суставной деструкции при РА, которая реализуется за счет синтеза "провоспалительные" цитокинов (ФНО , ИЛ-1 и лимфотоксин), а также ИЛ-6 и ИЛ-10, которые оказывают дополнительное стимулирующее действие на В-лимфоциты. Кроме того, по данным клинических и эпидемиологических исследований у пациентов с аутоиммунными ревматическими заболеваниями наблюдается увеличение риска развития В клеточных не-Ходжскинских лимфом. Все это вместе взятое делает В клетки перспективными терапевтическими "мишенями" при аутоиммунных заболеваниях [5-11].
Рис. 4. В лимфоцит

Рис. 5. Роль В клеток в развитии аутоиммунитета
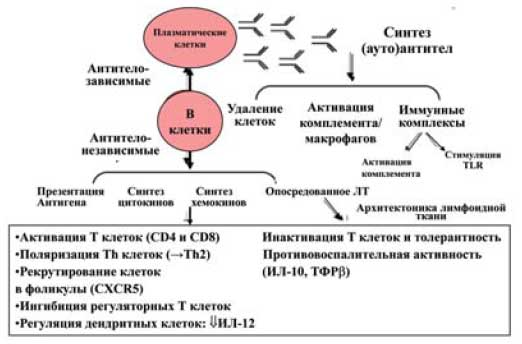
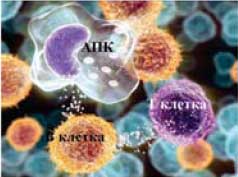
Рис. 6.
| T Cell Activation in Rheumatoid Synovium Is B Cell Dependent
Seisuke Takemura, Piotr A. Klimiuk, Andrea Braun, Jörg J. Goronzy, and Cornelia M. Weyand J Immunol 2001 167: 4710-4718. |
 |
| Antigen-Specific B Cells Are Required as APCs and Autoantibody-Producing Cells for Induction of Severe Autoimmune Arthritis Shannon K. O’Neill, Mark J. Shlomchik, Tibor T. Glant, Yanxia Cao, Paul D. Doodes, and Alison Finnegan J Immunol 2005 174: 3781-3788. |
Рис. 7. Активация Т-клеток в ревматоидной синовиальной ткани зависит от В-клеток
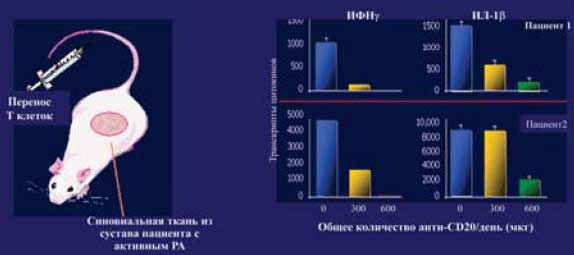
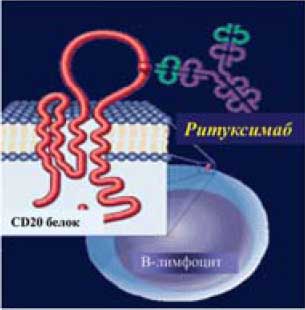
Первым и пока единственным анти-В клеточным препаратом, разрешенным к применению в клинической практике, является ритуксимаб (Rituximab, МабТера "Ф. Хоффманн-Ля Рош Лтд.") - химерные моноклональные антитела к CD20 антигену В клеток (рис 8). Препарат применяется в медицине с 1997 года для лечения В клеточных не-Ходжскинских лимфом, а в последние годы и широкого круга аутоиммунных заболеваний.
Рис. 8. РИТУКСИМАБ (Rituximab, MabThera, Roche)
| • Генно-инженерные химерные (мышь-человек) анти-СD20 моноклинальные антитела - Вариабильные участки тяжелых 451 аминокислота) и легких (213 аминокислот) цепей иммуноглобулина мышиного происхождения - Константный участок каппа цепи IgG1 человека - Афинность к CD20 антигену - 8.0 нмоль • Длительный Т 1/2 - После 2-х инфузнй по 1000 мг t1/2 19-22 сут |
 |
| Разрабатывался для лечения для лечения CD20+ не-Ходжскинских В клеточных лимфом (низкой градации или фоликулярной) (FDA, 1997) | |
Выбор CD20 молекулы в качестве мишени для моноклональных антител связан с особенностями дифференцировки В клеток, которые в процессе созревания от стволовых клеток в плазматические клетки проходят несколько последовательных стадий, для каждой из которых характерна экспрессия определенных мембранных молекул (рис. 9). Экспрессия CD20 наблюдается на мембране "ранних" и зрелых В-лимфоцитов, но не стволовых, "ранних" пре-В, дендритных и плазматических клеток. поэтому их истощение не отменяет регенерацию пула В-лимфоцитов и не влияет на синтез "нормальных" антител плазматическими клетками. Кроме того, CD20 не высвобождается с мембраны В-лимфоцитов и отсутствует в циркулирующей (растворимой) форме, которая потенциально могла бы мешать взаимодействию анти-CD20 антител с В клетками. Полагают, что способность ритуксимаба элиминировать В клетки реализуется за счет нескольких механизмов, в том числе комплемент-зависимой и антитело-зависимой клеточной цитотоксичности, а также индукции апоптоза. Механизмы, определяющие высокую эффективность ритуксимаба при РА и других аутоиммунных заболеваниях, суммированы на рис. 10.
Рис. 9. CD20: идеальная мишень для фармакологической интервенции.
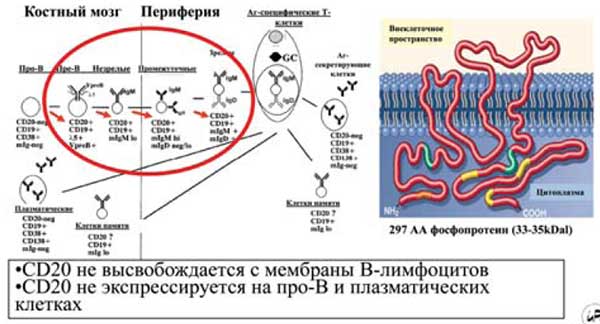
Рис. 10. Предполагаемые механизм действия ритуксимаба при аутоиммунных заболеваниях.
- Ослабление антиген-презентирующей функции В клеток в отношении индукции пролиферации и синтеза цитокинов CD4+ Т клетками
- Деструкция аберрантных ростковых центров: снижение образования аутоантиген-специфичных В клеток памяти, плазматических клеток и синтеза антител
- Истощение предшественников плазматических клеток: подавление синтеза антител и образования иммунных комплексов
- Модуляция активности других аутореактивных клеток за счет нарушения функции Т клеток
- Активация Т регуляторных клеток (CD4+ CD25+)
В настоящее время возможность эффективного контроля аутоиммунных патологических состояний путем истощения (и/или модуляции функции) В клеток, доказана в клинических исследованиях. Об этом свидетельствует высокая эффективность ритуксимаба при РА, что послужило основанием для регистрации препарата для лечения этого заболевания. В настоящее время проведены и продолжаются исследования, подтвердившие высокую эффективность ритуксимаба при РА как у больных резистентных к терапии "стандартными" БПВП, так и ингибиторами ФНО-а (рис 11-13), что позволяет рассматривать ритуксимаб как высоко эффективный базисный противовоспалительный генно-инженерный биологический препарат (рис. 14) При этом повторные курсы терапии ритуксимабом столь же эффективны как и первый (рис. 16-20), а терапевтический эффект первого курса сохраняется в среднем 40-50 недель (рис. 21). Эти данные свидетельствуют о том, что применение ритуксимаба позволяет максимально индивидуализировать лечение РА и тем самым повысить эффективность и безопасность фармакотерапии в целом. На фоне повторных курсов ритуксимаба не отмечено нарастания частоты побочных эффектов (рис. 22), включая инфекционные осложнения (рис. 23 и 24), а частота (и интенсивность) инфузионных реакций достоверно снижается (рис. 25).
Рис. 11. Программа исследований ритуксимаба при РА
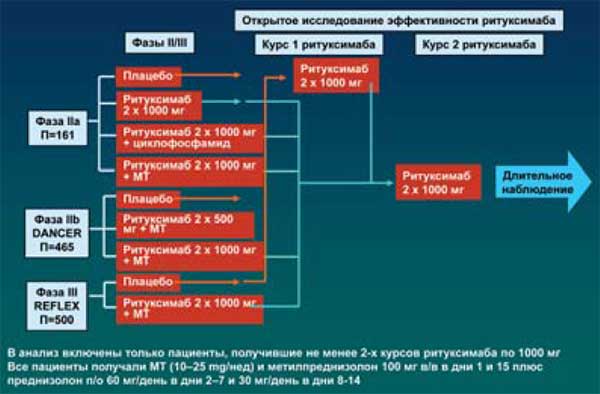
Рис. 12.
| N Engl J Med Volume 350:2572-2581 June 17, 2004 Number 25 Efficacy of B-Cell–Targeted Therapy with Rituximab in Patients with Rheumatoid Arthritis Jonathan C.W. Edwards, M.D., Leszek Szczepanski, M.D., Ph.D., Jacek Szechinski, M.D., Ph.D., Anna Filipowicz-Sosnowska, M.D., Ph.D., Paul Emery, M.D., David R. Close, Ph.D., Randall M. Stevens, M.D., and Tim Shaw, B.Sc. |
| Arthritis & Rheumatism Volume 54 Issue 5 , Pages 1390-1400 (May 2006) The efficacy and safety of rituximab in patients with active rheumatoid arthritis despite methotrexate treatment: Results of a phase IIB randomized, double-blind, placebo-controlled, dose-ranging trial
|
| Arthritis & Rheumatism Volume 54 Issue 5 , Pages 2793-2806 (May 2006) Rituximab for rheumatoid arthritis refractory to anti-tumor necrosis factor therapy: Results of a multicenter, randomized, double-blind, placebo-controlled, phase III trial evaluating primary efficacy and safety at twenty-four weeks Stanley B. Cohen, Paul Emery, Maria W. Greenwald, Maxime Dougados, Richard A. Furie, Mark C. Genovese, Edward C. Keystone, James E. Loveless, Gerd-Rüdiger Burmester, Matthew W. Cravets, Eva W. Hessey, Timothy Shaw, Mark C. Totoritis, REFLEX Trial Group |
Рис. 13. Эффективность ритуксимаба при РА по данным рандомизированных контролируемых исследований
| Авторы | Лечение (число больных) | ACR20 | ACR50 | ACR70 | |||
| 6м | 12м | 6м | 12м | 6м | 12м | ||
|
Длительно текущий (8-12 лет) активный РА, не смотря на лечение MТ (10-30 мг/нед) |
|||||||
| Edwards et al. | PT 1000 мг (40) | 65* | 33 | 33 | 15 | 15 | 10 |
| PT 1000 мг + ЦФ(41) | 76*** | 49* | 41** | 27* | 15 | 10 | |
| PT 1000 мг + МТ(40) | 73** | 65*** | 43** | 35** | 23* | 15* | |
| MТ (40) | 38 | 20 | 13 | 5 | 5 | 0 | |
| Emery et al. (DANCER) |
РТ 500 мг+МТ (105) | 55*** | 67 | 33*** | 42 | 13 | 20 |
| РТ 1000 мг + МТ(122) | 54*** | 59 | 34*** | 36 | 20*** | 17 | |
| ПЛ + МТ(122) | 28 | 45 | 13 | 20 | 5 | 8 | |
|
Длительно текущий (9 лет) активный РА, с неадекватным ответом на ингибиторы ФНО |
|||||||
| Cohen et al. (REFLEX) |
РТ 1000 мг + МТ (298) | 51**** | 51 | 27**** | 34 | 12**** | 14 |
| ПЛ+ МТ(214) | 16 | 33 | 5 | 5 | 1 | 4 | |
Рис. 14. Ритуксимаб соответствует критериям генно-инженерного биологического БПВП
| Суррогатные конечные точки | Характеристика | Эффект ритуксимаба |
| Подавление симптомов | •ACR20% (минимум) •Длительность лечения: 6 мес (НПВП 3 мес) |
•IIА •DANCER •REFLEX |
| Выраженный клинический ответ | •ACR70% •Длительность лечения: 6 мес |
|
| Полный клинический ответ | •Ремиссия или отсутствие деструкции суставов (более 6 мес) •Длительность лечения: 1 год |
|
| Ремиссия | • Утренняя скованность < 15 мин, нет болей, СОЭ< 20-30 мм/час •Длительность лечения: 1 год |
|
| Предотвращение инвалидности | •Стабилизация HAQ, SF-36 •Длительность лечения: 2-5 лет |
•REFLEX |
| Предотвращение деструкции суставов | •Отсутствие динамики индексов Шарпа или Ларсена (Rx) •Длительность лечения: > 1 года |
•REFLEX •Расширение |
Рис. 15. Повторные курсы ритуксимаба (сентябрь 2006)
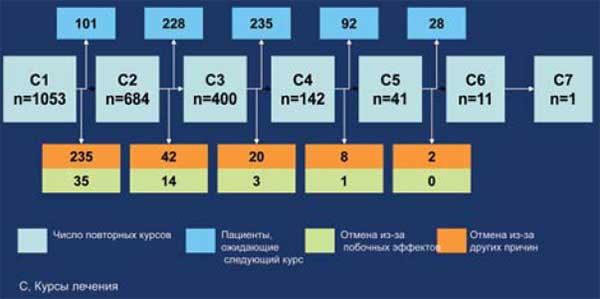
Рис. 16. Длительность применения ритуксимаба
| Длительность наблюдения | Октябрь 2005 (n) | Сентябрь 2006 (n) |
| Всего (любое) | 1039 | 1053 |
| > 6 месяцев | 987 | 1014 |
| > 1 года | 839 | 957 |
| > 2 лет | 139 | 701 |
| > 3 лет | 89 | 120 |
| Общее применение (пациенты-год) | 1669 пациентов-год | 2438 пациентов-год |
Рис. 17. Динамика активности заболевания у пациентов с неэффективностью ингибиторов ФНО
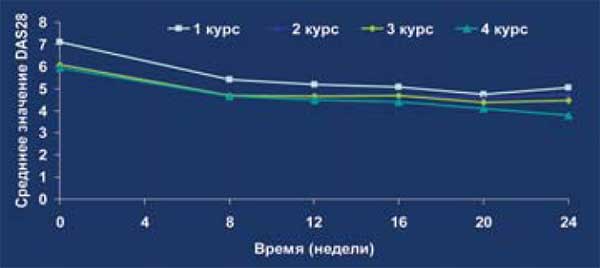
Рис. 18. Пациенты (n=96) с не эффективностью ингибиторов ФНО: АСR (24 недели)
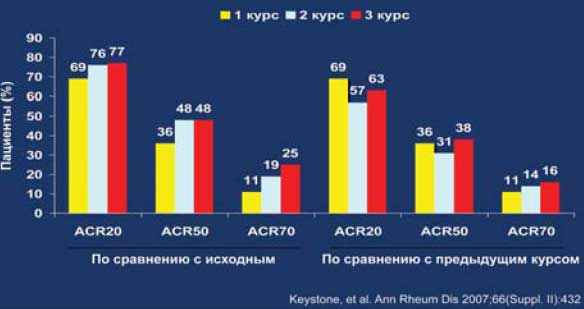
Рис. 19. Пациенты (n=97) с не эффективностью ингибиторов ФНО: EULAR (24 недели)
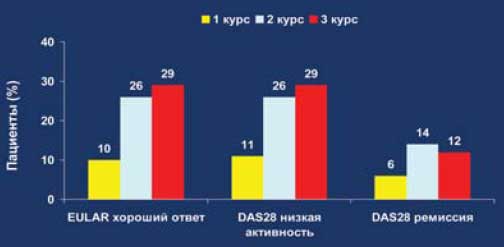
Рис. 20. Пациенты (n=57) с не эффективностью БПВП: EULAR (24 недели)
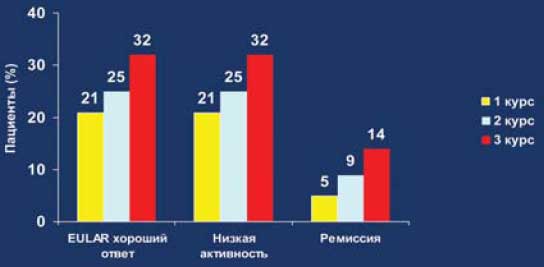
Рис. 21. Средний промежуток времени между курсами
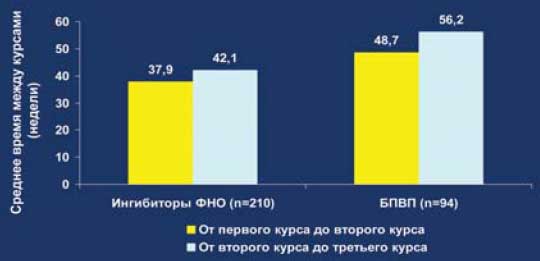
Рис. 22. Побочные эффекты
| 1 курс (n=1053) | 2 курс (n=684) | 3 курс (n=400) | 4 курс (n=142) | |
| Применение (пт-годы) | 1362.89 | 717.3 | 268.11 | 73.97 |
| ПЭ (%) | 88% | 81% | 72% | 65% |
| Частота/100 пт-годы | 328.9 | 296.8 | 344.3 | 342.0 |
| Тяжёлые ПЭ (%) | 18% | 15% | 10% | 3% |
| Частота/100 пт-годы | 19.15 | 20.21 | 20.89 | 6.76 |
| ПЭ, приведшие к отмене | 3% | 2% | <1% | <1% |
Рис. 23. Инфекционные осложнения
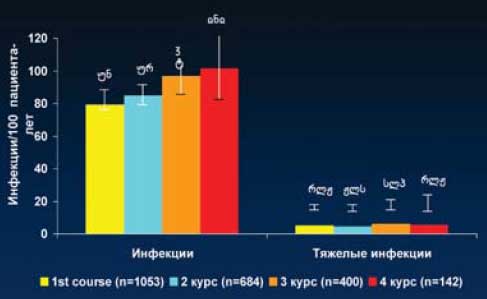
Рис. 24. Частота инфекционных осложнений
- 702 пациента (67%) имели эпизоды >1 инфекции
- Наиболее часто ВДП, включая фарингит (32%), и мочевая инфекция (11%)
- Нет опортунистических инфекций, реактивации вирусной инфекции или туберкулеза
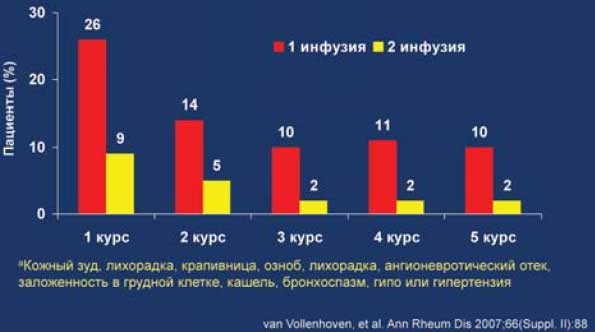
Рис. 25. Частота острых инфузионных реакций
Недавно группа авторитетных Европейских и Американских ревматологов разработали рекомендации по применению ритуксимаба при РА (рис. 26), в которых подчеркивается, что основным показанием для назначения в настоящее время является неэффективность ингибиторов ФНО-а [8]. Кроме того, ритуксимаб может назначаться пациентам, имеющим противопоказания для лечения ингибиторами ФНО-а, особенно при наличии в анамнезе лимфопролиферативных опухолей, а также при ревматоидном васкулите (рис. 27). У пациентов с неэффективностью ингибиторов ФНО-а, назначение ритуксимаба в большей степени подавляет активность воспаления суставов (уменьшение DAS28), чем замена одного ингибитора ФНО на другой [10] (рис. 28 и 29). Предварительный анализ результатов применения ритуксимаба у пациентов с не эффективностью одного ингибитора ФНО-а, свидетельствует не только о клинических, но и существенных фармакоэкономических преимуществах лечения ритуксимабом по сравнению с назначением другого ингибитора ФНО-а.
Рис. 26.
| REVIEWS: Consensus statement on the use of rituximab in patients with rheumatoid arthritis J S Smolen, E C Keystone, P Emery, F C Breedveld, N Betteridge, G R Burmester, M Dougados, G Ferraccioli, U Jaeger, L Klareskog, T K Kvien, E Martin-Mola, K Pavelka The Working Group on the Rituximab Consensus Statement Ann Rheum Dis, Feb 2007; 66: 143 - 150. |
Рис. 27. Место ритуксимаба в лечении ревматоидного артрита
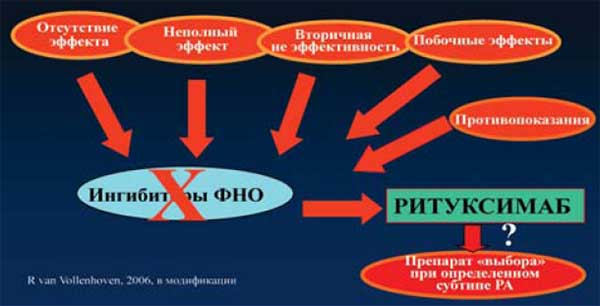
Рис. 28.
| Arthritis & Rheumatism Volume 56 Issue 5 , Pages 1417-1423 (May 2007) B cell depletion may be more effective than switching to an alternative anti-tumor necrosis factor agent in rheumatoid arthritis patients with inadequate response to anti-tumor necrosis factor agents Axel Finckh, Adrian Ciurea, Laure Brulhart, Diego Kyburz, Burkhard Möller, Silvia Dehler, Sylvie Revaz, Jean Dudler, Cem Gabay, Physicians of the Swiss Clinical Quality Management Program for Rheumatoid Arthritis |
Рис. 29. Динамика активности заболевания на фоне лечения ритуксимабом по сравнению с ингибиторами ФНО
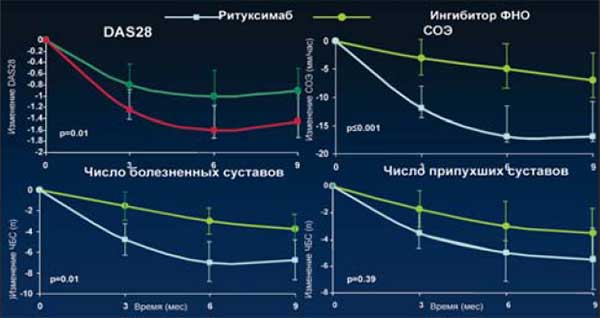
На рис. 30 суммированы основные данные, касающиеся эффективности препарата при этом заболевании, с позиции медицины, основанной на доказательствах.
Рис. 30. Эффективность ритуксимаба при РА
Основные положения
- Монотерапня (Уровень доказательности lb)
- Комбинированная терапия (Уровень доказательности 1а)
- Эффективность и длительность эффекта комбинированной терапии выше, чем монотерапии (Уровень доказательности lb)
- У «ответчиков» длительность эффекта после одного курса ритуксимаба длится более 6 мес (Уровень доказательности III)
- У пациентов с недостаточным эффектом БПВП и ингибиторов ФНО, лечение ритуксимабом замедляет прогрессированне деструкции суставов (Уровень доказательности lb)
В последние годы очень быстро накапливается клинический опыт применения ритуксимаба для лечения других аутоиммунных заболеваний человека, включая СКВ, болезнь Шегрена, системные васкулиты, идиопатические воспалительные миопатии, катастрофический анти-фосфолипидный синдром и др. (рис. 31). Следует особо подчеркнуть, что в большинстве случаев ритуксимаб с успехом применяли у пациентов с очень тяжелым течением болезней, которые были резистентны к стандартной глюкокортикоидной и цитотоксической терапии, внутривенному иммуноглобулину, экстракорпоральным методам очищения крови, нередко по жизненным показаниям [11].
Рис. 31. Заболевании, при которых продемонстрирована эффективность Ритуксимаба
| Аутоиммунные Ревматоидный артрит (суставы) Системная красная волчанка (системность) Синдром Шегрена (железы внешней секреции) АНЦА-ассоциированные васкулиты (сосуды) Антифосфолипидный синдром (сосуды) Идиопатическая тромбоцитопения (тромбоциты) Аутоиммунная гемолитическая анемия (эритроциты) Синдром Гийена Барре (периферическая нервная система) Хроническая иммунная полинейропатия (периферическая нервная система) Аутоиммунный тиреоидит (щитовидная железа) Сахарный диабет типа I (поджелудочная железа) Болезнь Адисона (надпочечники) Мембранозная нефропатия (почки) Болезнь Гудпасчера (почки, лёгкие) Аутоиммунный гастрит (желудок) Пернициозная анемия (желудок) Пузырчатка (кожа, слизистые) Первичный билиарный цирроз (печень) Дерматомиозит, полимиозит (скелетная мускулатура) Миастения (скелетная мускулатура) Целиакия (тонкий кишечник) |
Воспалительные IgA нефропатия (почки) Другие
|
Не вызывает сомнения, что ритуксимаб является чрезвычайно эффективным и относительно безопасным препаратом для лечения РА и других тяжелых аутоиммунных заболеваний. Его внедрение в клиническую практику по праву можно считать крупным достижением медицины начала 21 века, которое имеет не только важное клиническое, но и теоретическое значение, поскольку способствует расшифровке фундаментальных звеньев патогенеза аутоиммунных заболеваний человека. Фактически ритуксимаб является родоначальником нового направления в лечении аутоиммунных заболеваний человека, в основе которого лежит модуляция В клеточного звена иммунитета.
Таким образом, начало 21 века ознаменовалось бурным прогрессом в лечении аутоиммунных ревматических заболеваний, в первую очередь РА. Внедрение генно-инженерных биологических агентов позволяет надеяться, что в недалеком будущем излечение или, по крайней мере, достижение длительной ремиссии у пациентов, страдающих этими заболеваниями, станет реальностью.
ЛИТЕРАТУРА
1. Насонов Е.Л. Фармакотерапия ревматоидного артрита - взгляд в 21 век. Клин. медицина 2005; 6: 8-12
2. Насонов Е.Л. Применение инфликсимаба (моноклональные антитела к фактору некроза опухоли) в ревматологии: новые данные. РМЖ 2004; 20: 1123-1127
3. Насонов Е.Л. Применение инфликсимаба (моноклональные антитела к фактору некроза опухоли) в ревматологии: новые данные. РМЖ 2004; 20: 1123-1127
4. Насонов Е.Л. Перспективы применения полностью человеческих моноклональных антител к фактору некроза опухоли (Adalimumab -Humira) при ревматоидном артрите. Клин Фармакол. Фармакотерапия 2007; 1: 71-74
5. Furst DE, Breedveld FC, Kalden JR, et al. Updated consensus statement ob biological agents for the treatment of rheumatic diseases, 2007; Ann Rheum Dis 2007; 66:2-22
6. Насонов ЕЛ. Перспективы применения моноклональных антител к В-лимфоцитам (ритуксимаб) при ревматоидном артрите. Клин. Фармакол. терапия 2006; 1-5:55-58
7. Насонов Е.Л. Новые направления терапии ревматоидного артрита: перспективы применения моноклональных антител к В-лимфоцитам (ритуксимаб). РМЖ 2006; 25: 1778-1782
8. Smolen JS, Betteridge N, Breedveld FC, et al. Consensus statement on the use of rituximab in patients with rheumatoid arthritis. Ann Rheum Dis 2007; 66: 143-150.
9. Finckh A, Ciurea A, Brulhart L, et al. B cell depletion may be more effective than switching to an alternative anti-tumor necrosis factor agent in rheumatoid arthritis patients with inadequate response to anti-tumor necrosis factor agents. Arthritis Rheum 2007; 56: 1417-1423
10. Соловьев С.К., Котовская М.А., Насонов Е.Л. Ритуксимаб в лечении системной красной волчанки. РМЖ 2005; 13: 1731-1735
11. Насонов Е.Л. Перспективы применения ритуксимаба при аутоиммунных заболеваниях человека. РМЖ, 2007; 15(26):1958-1963
Комментарии
ПРАКТИКА ПЕДИАТРА
